文档内容
第 01 讲 有机化合物的结构特点与研究方法
目 录
01 考情透视·目标导航.........................................................................................................................2
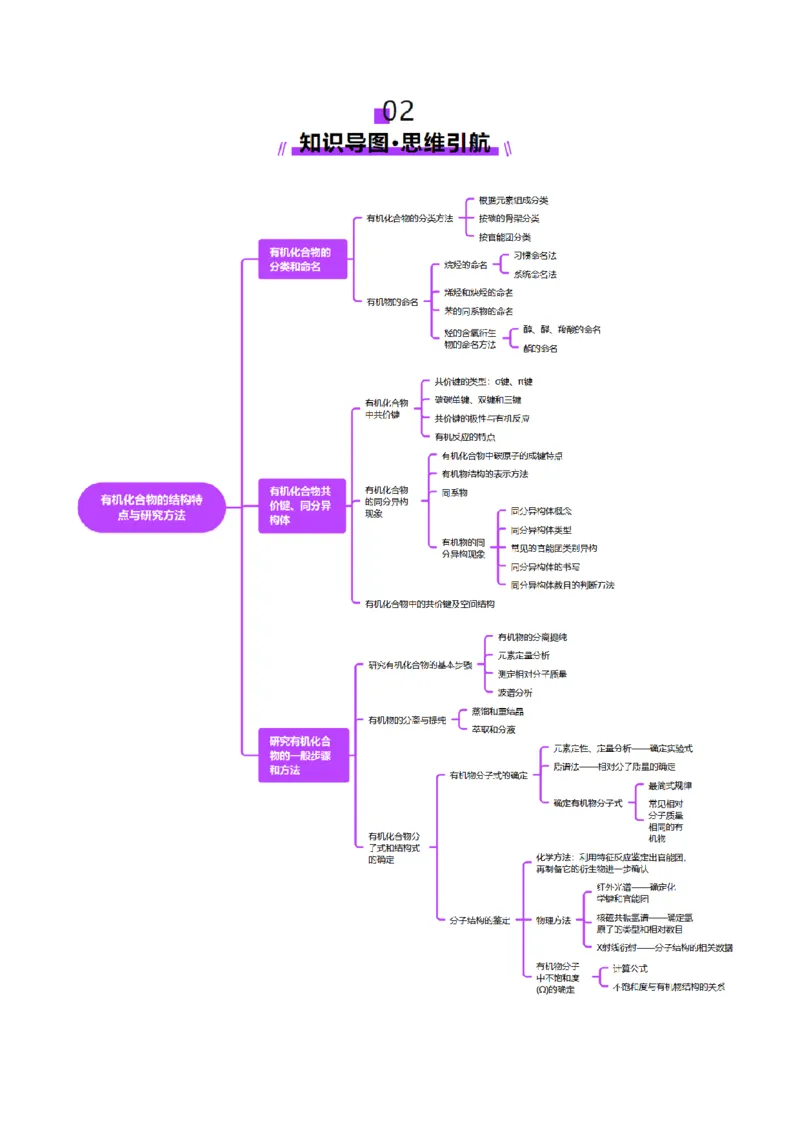
02 知识导图·思维引航.........................................................................................................................4
03 考点突破·考法探究.........................................................................................................................5
考点一 有机化合物的分类和命名.............................................................................................5
知识点1 有机化合物的分类方法...........................................................................................5
知识点2 有机物的命名...........................................................................................................6
考向1 考查有机化合物的分类...............................................................................................8
考向2 考查有机化合物的命名...............................................................................................10
考点二 有机化合物共价键、同分异构体...............................................................................11
知识点1 有机化合物中共价键.............................................................................................11
知识点2 有机化合物的同分异构现象.................................................................................12
考向1 有机化合物的结构与表示方法...................................................................................17
考向2 考查有机物的空间结构与共价键...............................................................................18
考向3 考查同分异构体的判断与书写...................................................................................21
考点三 研究有机化合物的一般步骤和方法...........................................................................22
知识点1 有机物的分离与提纯.............................................................................................22
知识点2 有机化合物分子式和结构式的确定.....................................................................23
考向1 考查有机物的分离与提纯...........................................................................................25
考向2 考查有机化合物分子式和结构式的确定...................................................................27
04 真题练习·命题洞见.......................................................................................................................30
考点要求 考题统计 考情分析
分析近三年高考试题,高考命题在本讲有以下规律:
2023辽宁卷2题,3分
有机化合物的分 1.从考查题型和内容上看,高考命题以选择题和非选择类和命名 2023浙江6月卷2题,2分 题呈现,考查内容主要有以下四个方面:
2023新课标卷卷30题,2分 (1)有机物的分类和命名。
2023全国乙卷36题,2分 (2)有机物分子的结构、碳原子的成键特征、原子共
2023全国甲卷36题,2分 线、共面问题及同分异构体数目的判断。
2023山东卷19题,2分 (3)共价键中的σ键和π键、有机反应。
2023广东卷20题,2分 (4)有机化合物的组成和分子的结构。
2023海南卷18题,2分 2.从命题思路上看,侧重有机综合题中同分异构体和有
机化合物分子结构的考查考查。对同分异构体的考查,
2022全国乙卷36题,2分
题目类型多变。常见题型有:
2022全国甲卷36题,2分
①限定范围书写或补写同分异构体。解题时要看清所限
2022山东卷19题,2分
范围,分析已知的几个同分异构体的结构特点,对比联
2022湖南卷19题,2分
想找出规律后再补写,同时注意碳的四价原则和对官能
2024·江苏卷9题,3分
团存在位置的要求。
2024·湖南卷4题,3分
②判断是否是同分异构体。做此类题时要先看分子式是
2023全国乙卷8题,6分
否相同,再看结构是否不同。对结构不同的要从两个方
2023全国甲卷8题,6分
面来考虑:一是原子或原子团的连接顺序;二是原子或
2023北京卷9题,3分
原子团的空间位置。
有机化合物共价
2023辽宁卷6题,分 ③判断取代产物同分异构体的数目。
键、同分异构体
2023年6月浙江卷10题,分 其分析方法是分析有机物的结构特点,确定不同位置的
2023年1月浙江卷9题,分 氢原子种数,再确定取代产物同分异构体数目;或者依
2022全国乙卷8题,分 据烃基的同分异构体数目进行判断。
2022全国甲卷8题,分 3.根据高考命题特点和规律,复习时要注意以下几个方
2022重庆卷6题,3分 面:
(1)掌握有机物的分类方法,弄清基本概念,如芳香
族化合物、脂肪烃等;
(2)建立有机物的结构与性质的联系,掌握常见重要
官能团及其特征反应等;
2024·浙江卷9题,3分
(3)熟悉有机物的结构特点,能看懂键线式和结构简
2024·山东卷7题,3分
研究有机化合 式;
2024·湖北卷6题,3分
物的一般步骤和 (4)能以甲烷、乙烯、乙炔、苯等分子结构为母体分
2023山东卷12题,4分
方法 析陌生有机分子中原子共线、共面问题;
2023全国乙卷26题,2分
(5)会利用“定一移一”的方法在碳骨架的基础上分
2022湖北卷2题,3分
析同分异构现象。
(6)掌握蒸馏、重结晶、萃取等分离和提纯方法的适
用范围、仪器选用、操作步骤及注意事项等。
(7)掌握由有机化合物元素含量及相对分子质量确定
分子式的一般方法和步骤。(8)了解红外光谱、核磁共振氢谱的原理,掌握有机
复习目标: 化合物分子结构鉴定的方法。
1.了解常见有机化合物的结构和常见官能团结构性质。
2.知道有机化合物是有空间结构的,认识其中碳原子的成键特点;认识有机化合物的分子结构决定于原子
间的连接顺序、成键方式。
3.认识有机化合物存在构造异构和立体异构等同分异构现象;知道简单有机化合物的命名。
4.知道红外光谱、核磁共振氢谱等现代仪器分析方法在有机化合物分子结构测定中的应用。考点一 有机化合物的分类和命名
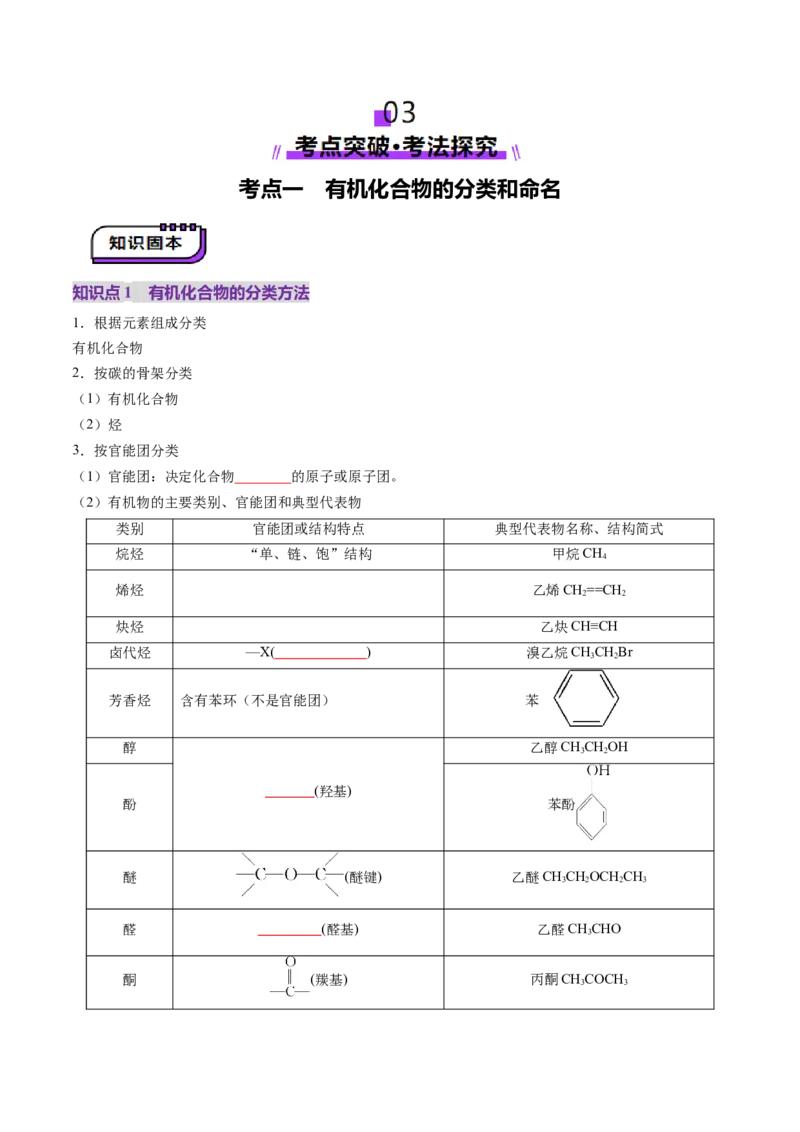
知识点1 有机化合物的分类方法
1.根据元素组成分类
有机化合物
2.按碳的骨架分类
(1)有机化合物
(2)烃
3.按官能团分类
(1)官能团:决定化合物 的原子或原子团。
(2)有机物的主要类别、官能团和典型代表物
类别 官能团或结构特点 典型代表物名称、结构简式
烷烃 “单、链、饱”结构 甲烷CH
4
烯烃 乙烯CH==CH
2 2
炔烃 乙炔CH≡CH
卤代烃 —X( ) 溴乙烷CHCHBr
3 2
芳香烃 含有苯环(不是官能团) 苯
醇 乙醇CHCHOH
3 2
(羟基)
酚 苯酚
醚 (醚键) 乙醚CHCHOCH CH
3 2 2 3
醛 (醛基) 乙醛CHCHO
3
酮 (羰基) 丙酮CHCOCH
3 3羧酸 (羧基) 乙酸CHCOOH
3
酯 (酯基) 乙酸乙酯CHCOOCH CH
3 2 3
胺 —NH ( ) 苯胺
2
酰胺 (酰胺基) 乙酰胺CHCONH
3 2
氨基酸 —NH (氨基)、—COOH(羧基) 甘氨酸
2
【特别提醒】1.官能团的书写必须注意规范性,常出现的错误有把“ ”错写成“C===C”,“—CHO”
错写成“CHO—”或“—COH”。
2.苯环不属于官能团,但是芳香化合物与链状有机物或脂环有机物相比,有明显不同的化学特征,这是
由苯环的特殊结构所决定的。
3.相同官能团有机物不一定属于同类物质。例如醇和酚官能团都是—OH。
4.含有醛基的有机物不一定属于醛类,如甲酸、甲酸盐、甲酸某酯等,虽然有醛基,但不与烃基相连,
不属于醛类。
知识点2 有机物的命名
1.烷烃的命名
(1)习惯命名法
(2)系统命名法
2.烯烃和炔烃的命名
3.苯的同系物的命名
(1)习惯命名法如 称为 , 称为 ,二甲苯有三种同分异构体,其名称分别为:
、
、 。
(2)系统命名法
①以 作为母体,其他基团作为取代基。
②将某个最简侧链所在的碳原子的位置编为 1 号,选取最小位次给其他基团编号即侧链编号之和
。
如
4.烃的含氧衍生物的命名方法
(1)醇、醛、羧酸的命名
将含有官能团(—OH、—CHO、—COOH)的最长碳链作为主链,称为
选主链
“某醇”“某醛”或“某酸”
编序号 从距离官能团最近的一端对主链上的碳原子进行编号
将支链作为取代基,写在“某醇”“某醛”或“某酸”的前面,用阿
写名称
拉伯数字标明官能团的位置
(2)酯的命名
合成酯时需要羧酸和醇发生酯化反应,命名酯时“先读酸的名称,再读醇的名称,后将‘醇’改‘酯’即
可”。如甲酸与乙醇形成酯的名称为甲酸乙酯。
【易错提醒】1.有机物命名时常用到的四种字及含义。
(1)烯、炔、醇、醛、酮、酸、酯……指官能团;
(2)1、2、3……指官能团或取代基的位置;
(3)二、三、四……指官能团或取代基的个数;
(4)甲、乙、丙、丁、戊……指碳原子数。
2.带官能团有机物系统命名时,选主链、编号位要围绕官能团进行,且要注明官能团的位置及数目。
3.书写有机物名称时不要遗漏阿拉伯数字之间的逗号及与汉字之间的短线。
4.1甲基,2乙基,3丙基是常见的命名错误,若1号碳原子上有甲基或2号碳原子上有乙基,则主链碳原
子数都将增加1,使主链发生变化。
5.卤代烃中卤素原子作为取代基看待。酯是由对应的羧酸与醇(或酚)的名称组合,即某酸某酯。聚合物:在
单体名称前面加“聚”。
6.有机化合物系统命名中常见的错误
(1)主链选取不当(不包含官能团,不是主链最长、支链最多)。
(2)编号错(官能团的位次不是最小,取代基位号之和不是最小)。(3)支链主次不分(不是先简后繁)。
(4)“-”“,”忘记或用错。
考向1 考查有机化合物的分类
例1(2024·广东·三模)抗生素克拉维酸具有抗菌消炎的功效,其结构简式如下
。下列关于克拉维酸的说法不正确的是
A.分子内的含氧官能团有羟基、羧基、醚键和酰胺基
B.最多能与1mol NaOH溶液反应
C.克拉维酸存在顺反异构体
D.一定条件下克拉维酸能被氧化生成醛类化合物
【题后反思】官能团的识别和规范书写
(1)—OH连到苯环上属于酚,连到链烃基或脂环烃基上为醇。
(2)醛类物质是醛基与烃基直接相连的有机物,甲酸、甲酸盐、甲酸某酯等不属于醛类物质。
(3)官能团书写常出现的错误:“ ”错写成“C===C”,“—CHO”错写成“CHO—”或“—
COH”。
【变式训练1】(2024·河南·模拟预测)醋丁洛尔(M)可治疗高血压、心绞痛和心律失常,其结构简式如
图所示。下列有关M的叙述正确的是
A.属于芳香烃
B.与 溶液能发生显色反应
C. 最多能与 加成
D.不能发生消去反应
【变式训练2】(2024·湖北·三模)阿斯巴甜是一种常见的合成甜味剂,其结构如图所示,下列有关说法
不正确的是A.阿斯巴甜属于糖类物质
B.分子中含有4种官能团
C.不存在含有两个苯环的同分异构体
D.1mol该分子最多与3molNaOH反应
考向2 考查有机化合物的命名
例2(2024·辽宁鞍山·一模)下列关于有机物及相应官能团的说法正确的是( )
A.乙烯与聚乙烯具有相同的官能团,都属于烯烃
B. 分子中含有醚键(虚线部分),所以该物质属于醚
C. 及 因都含有羟基,故都属于醇
D.不是所有的有机物都具有一种或几种官能团
【易错提醒】1.有机物系统命名中常见的错误
(1)主链选取不当,如所选主链不包含官能团,不是主链最长、支链最多。
(2)编号错,如所编官能团的位次不是最小。
(3)支链主次不分,不是先简后繁。
(4)连接线“-”“,”忘记或用错。
2.弄清系统命名法中四种字的含义
(1)烯、炔、醛、酮、酸、酯……指官能团。
(2)二、三、四……指相同取代基或官能团的个数。
(3)1、2、3……指官能团或取代基的位置。
(4)甲、乙、丙、丁……指主链碳原子个数分别是1、2、3、4……
【变式训练1】(2024·河南鹤壁·模拟)下列有关物质命名正确的是( )
A.CHCH(OH)CH(CH ):3-甲基-2-丁醇
3 3 2
B. :3-甲基-2-丁烯
C. 加氢后得到2-乙基丁烷
D. :1,4,5,6-四甲基苯
【变式训练2】(2024·安徽蚌埠·模拟)下列有机物命名正确的是( )
A. :间二甲苯B. :2-甲基-2-丙烯
C. :2,2,3-三甲基戊烷
D. :6-羟基苯甲醛
考点二 有机化合物共价键、同分异构体
知识点1 有机化合物中共价键
1.共价键的类型——共价键中一定存在σ键,不饱和键中才存在π键
物质 甲烷 乙烯 乙炔
球棍
模型
共价键 5个σ键、 3个σ键、
4个σ键
类型 1个π键 2个π键
碳原子
sp3 sp2 sp
杂化类型
2.碳碳单键、双键和三键
碳碳单键 碳碳双键 碳碳三键
结构 —C≡C—
C原子的杂化方式 sp3 Sp2 sp
键的类型 σ键 1个σ键、1个π键 1个σ键、2个π键
键角 CH:109°28′ C H:120° C H:180°
4 2 4 2 2
空间结构 碳原子与其他4个原 双键碳原子及与之相连的原 碳原子及与之相连的原子处
子形成正四面体结构 子处于同一平面上 于同一直线上
3.共价键的极性与有机反应
①由于不同的成键原子间电负性的差异,共用电子对偏向电负性较大的原子。偏移的程度越大,共价键极
性越强,在反应中越容易发生断裂。
a.乙醇中氧原子的电负性较大,导致碳氧键和氢氧键极性较强,容易发生取代反应。
乙醇与钠反应的化学方程式:2CHCHOH+2Na―→2CHCHONa+H↑;
3 2 3 2 2
乙醇与氢溴酸反应的化学方程式:CHCHOH+HBr――→CHCHBr+HO。
3 2 3 2 2b.乙烯(CH===CH )分子中 π 键不稳定,容易断裂发生加成反应,乙烯与 Br 反应的化学方程式:
2 2 2
CH===CH +Br ―→CHBrCHBr。
2 2 2 2 2
②键的极性对对羧酸酸性的影响
a.键的极性对羧酸酸性大小的影响实质是通过改变羧基中羟基的极性而实现的,羧基中羟基的极性越大,
越容易电离出H+,则羧酸的酸性越大。
b.与羧基相邻的共价键的极性越大,过传导作用使羧基中羟基的极性越大,则羧酸的酸性越大。
c.烃基是推电子基团,即将电子推向羟基,从而减小羟基的极性,导致羧酸的酸性减小。一般地,烃基越
长,推电子效应越大,羧酸的酸性越小。
4.有机反应的特点
①反应速率较小,有机反应往往发生在共价键上,而共价键的断裂需要吸收大量的能量
②副反应较多,产物比较复杂,有机化合物分子中存在多个极性键,发生反应时共价键断裂的位置存在多
种可能。
知识点2 有机化合物的同分异构现象
1.有机化合物中碳原子的成键特点
(1) 最外层4个电子,可形成 个共价键;
(2) 碳原子间以较稳定的共价键结合,不仅可以形成 键,还可以形成稳定的 键或叁键;
(3) 多个碳原子可以互相结合成 状,也可以结合成环状,还可以带有支链,碳链和碳环也可以结合;
2.有机物结构的表示方法
种类 表示方法 实例
分子式 用元素符号表示物质的分子组成 CH、C H
4 2 6
最 简 式 ( 实 验 用元素符号表示化合物中各元素原子个数的最简整数比 乙烷的最简式
式)
电子式 在元素符号周围用“.”或“×”表示原子的最外层电子的成 甲烷的电子式
键情况的式子
结构式 用短线“-”来表示1个共价键,用“-”(单键)、“=” 乙烯的结构式
(双键)或“≡”(三键)将所有的原子连接起来的式
子
结构简式 (1)表示单键的“-”可以省略,将与碳原子相连的其他 乙烯的结构简式
原子写在其旁边,在右下角注明其个数;
(2)表示双键、三键的“=”“≡”不能省略;(3)醛基( )、羧基( )可简化成-CHO、-COOH
键线式 (1)进一步省去碳、氢元素的元素符号,只要求表示出 苯的键线式:
分子中碳碳键以及与碳原子相连的基团;
(2)键线式中的每个拐点或终点均表示一个碳原子,每
个碳原子都形成四个共价键,不足的用氢原子补足
球棍模型 小球表示原子,短棍表示化学键 乙烯的球棍模型
空间填充模型 用不同体积的小球表示不同大小的原子 乙烯的空间填充模型:
【易错提醒】①把简单有机物的分子式与结构简式等同起来,如C HOH是乙醇的结构简式而非分子式,
2 5
乙醇的分子式是C HO。
2 6
②把不饱和烃结构中的碳碳双键或三键省略,如将乙烯的结构简式误写为CHCH,乙炔的结构简式误写为
2 2
CHCH等。
③空间填充模型与球棍模型辨别不清,从而产生错误,原因是未能理解它特点及二者的区别。
3.同系物
相似,分子组成上相差一个或若干个 原子团的化合物互称为同系物。
(1)下列物质中属于丙烯的同系物的是 (填序号)。
① ②CHCH===CHCH
3 3
③ ④CH ===CH—CH===CH
2 2
(2)下列物质属于乙醇的同系物的是 (填序号)。
①丙醇 ②乙二醇( )
③CH ===CHCHOH
2 2
注意:同系物判定两要点:① 种类、 均相同;②具有相同的 。
4.有机物的同分异构现象
(1)同分异构体:化合物分子式 、结构 的现象称为同分异构现象。具有同分异构现象的
化合物互为同分异构体。
【注意】相对分子质量相等的物质,不一定是同分异构体。
(2)同分异构体类型
构 碳链异构 碳链骨架不同,如CH—CH—CH—CH 和
3 2 2 3
造 位置异构 官能团位置不同,如:CH===CH—CH—CH 和
2 2 3
异 官能团异 官能团种类不同,如:CHCHOH和 ,常见的官能团异构有醇、酚、醚;醛
3 2
构 构 与酮;羧酸与酯等
立 顺反异构 在有双键或小环结构(如环丙烷)的分子中,由于分子中双键或环的原子间的键的自由旋转受阻碍,存在不同的空间排列方式而产生的立体异构现象,又称几何异构,如
CHCH===CHCH 存在顺反异构顺-2-丁烯,
3 3
又称为手性异构,任何一个不能和它的镜像完全重叠的分子就叫做手性分子,它的一
体
对映异构 个物理性质就是能使偏振光的方向发生偏转,具有旋光活性,如CHFClBr存在对映异
异
构。
构
构造式相同的化合物由于单键的旋转,使连接在碳上的原子或原子团在空间的排布位
构象异构 置随之发生变化产生的立体异构现象,如环己烷存在椅式( )和船式( )
两种较稳定的构象
(3)常见的官能团类别异构
组成通式 不饱和度(Ω) 可能的物质类别
C H 1 烯烃和
n 2n
C H 2 炔烃、二烯烃和 烃
n 2n-2
C H O 0 饱和一元醇和
n 2n+2
饱和一元醛和 、
C H O 1
n 2n
等
饱和一元羧酸和 、
C H O 1
n 2n 2
等
(4)同分异构体的书写
1)书写步骤
①官能团异构:首先判断该有机物是否有官能团异构。
②位置异构:就每一类物质,先写出碳链异构,再写官能团的位置异构体。
③书写:碳链异构体按“主链由长到短,支链由整到散,位置由心到边”的规律书写。
④检查:看是否有书写重复或书写遗漏,根据“碳四价”原则检查是否有书写错误。
2)烷烃同分异构体的书写
烷烃只存在碳链异构,书写时要注意全面而不重复,具体规则如下:3)芳香族化合物的同分异构体的书写及判断
①苯的一氯代物只有 种。
②苯的二氯代物有邻、间、对 种。
③甲苯(C H) 芳香烃的同分异构体。
7 8
④分子式为C H 的芳香烃的同分异构体有 种。
8 10
⑤甲苯的一氯代物的同分异构体有 种。
⑥苯的三元取代物,三个取代基相同时有 种,三个取代基中有两个相同时有 种,三个取代基中
都不同时有 种。
【易错警示】同分异构体的分子式相同,相对分子质量相同。但相对分子质量相同的化合物不一定是同分异
构体,如C H 与HCHO,C HOH与HCOOH不是同分异构体。
2 6 2 5
(5)同分异构体数目的判断方法
1)记忆法:记住一些常见有机物的同分异构体数目,如
①凡只含一个碳原子的分子 同分异构体(除 );
②乙烷、丙烷、乙烯、乙炔 同分异构体;
③4个碳原子的烷烃有 种同分异构体,5个碳原子的烷烃有 种同分异构体,6个碳原子的烷烃有
种同分异构体。
2)基元法:如丁基有4种同分异构体,则丁醇、戊醛、戊酸都有 种同分异构体。
3)替代法:如二氯苯(C HCl)有3种同分异构体,四氯苯也有 种同分异构体(将H和Cl互换);又如CH
6 4 2 4
的一氯代物只有 种,新戊烷C(CH) 的一氯代物也只有 种。
3 4
4)等效氢法:是判断同分异构体数目的重要方法,其规律有:
①同一碳原子上的氢原子等效。
②同一碳原子上的甲基上的氢原子等效。
③位于对称位置上的碳原子上的氢原子等效。
5.有机化合物中的共价键及空间结构
碳为sp3杂化,形成σ键,四面体形结
甲烷型
构
碳为 杂化,含π键,以双键为中
乙烯型
心 原子共平面
碳为 杂化,含大π键Π,以苯环
苯型
为中心 原子共平面
碳为 杂化,含π键,以三键为
乙炔型
中心 原子共直线
碳为 杂化,以碳原子为中心
甲醛型
原子共平面
注意:①在分子中,形成单键的原子可以绕键轴旋转,而形成双键、三键等其他键的原子不能绕键轴旋
转。②若平面间靠单键相连,所连平面可以绕键轴旋转,可能旋转到同一平面上,也可能旋转后不在同一平面上。
③若平面间被多个点固定,则不能旋转,一定共面。如 分子中所有环一定共面。
考向1 有机化合物的结构与表示方法
例1(2024·浙江杭州·模拟预测)下列有关化学用语表示正确的是
A.CaC 的电子式:
2
B.异戊二烯的键线式为:
C.能体现环己烷(C H )稳定空间构型的键线式:
6 12
D.甲醛中π键的电子云轮廓图:
【归纳拓展】(1)书写有机化合物的结构简式时一定要表示出其官能团,特别是烯烃和炔烃,不能省略
碳碳双键或碳碳三键;对于含氧官能团,书写结构简式时官能团一定要写准确,如丙醛应写成
CHCHCHO,不要写成CHCHCOH。
3 2 3 2
(2)键线式中的端点、拐点或折点为碳原子,碳连接的氢原子省略。
【变式训练1】(2024·天津北辰·三模)下列有关化学用语表示正确的是
A.乙炔分子的空间填充模型:
B.水的VSEPR模型:
C.基态Cr原子电子排布式
D.1-丁醇的键线式:
【变式训练2】(2024·天津河西·二模)下列化学用语或表述正确的是
A.丙炔的键线式:
B.顺-2-丁烯的分子结构模型:
C. 的空间结构:V形D.基态碳原子的轨道表示式:
考向2 考查有机物的空间结构与共价键
例2(2024·陕西延安·一模)下列有关说法正确的是( )
A.CHCH===CHCH 分子中的4个碳原子可能在同一直线上
3 3
B.苯乙烯( )分子的所有原子可能在同一平面上
C. 分子中的所有原子都在同一平面上
D. 的名称为3-甲基-4-异丙基己烷
【思维建模】有机化合物的空间结构
1.四种基本模型
(1)甲烷分子中所有原子一定不共平面,最多有3个原子处在一个平面上,即分子中碳原子若以四个单键
与其他原子相连,则所有原子一定不能共平面(如图1)。
(2)乙烯分子中所有原子一定共平面,若用其他原子代替其中的任何H原子,所得有机物中的所有原子
仍然共平面(如图2)。
(3)苯分子中所有原子一定共平面,若用其他原子代替其中的任何H原子,所得有机物中的所有原子也
仍然共平面(如图3)。
(4)乙炔分子中所有原子共直线,若用其他原子代替H原子,所得有机物中的所有原子仍然共直线(如图
4)。
2.注意碳碳单键的旋转
碳碳单键两端碳原子所连原子或原子团能以“C-C”为轴旋转,例如 ,因①键可以旋转,故
的平面和 确定的平面可能重合,也可能不重合。因而 分子中的所
有原子可能共面,也可能不共面。
3.结构不同的基团连接后原子共面分析
(1)直线与平面连接,则直线在这个平面上。如苯乙炔,所有原子共平面。
(2)平面与平面连接:如果两个平面结构通过单键相连,由于单键的旋转性,两个平面可以重合,但不一定重合。
(3)平面与立体连接:如果甲基与平面结构通过单键相连,则由于单键的旋转性,甲基的一个氢原子可
能暂时处于这个平面上。
4.审准题目要求
题目要求中常有“可能”“一定”“最多”“最少”“所有原子”“碳原子”等限制条件。如
分子中所有原子可能共平面, 分子中所有碳原子一定共平面而所有原子一定不
能共平面。
【变式训练1】(2024·浙江丽水·模拟)下列说法正确的是( )
A.CHCH==CHCH 分子中的四个碳原子在同一直线上
3 3
B.a( )和c( )分子中所有碳原子均处于同一平面上
C. 中所有碳原子可能都处于同一平面
D.化合物 (b)、 (d)、 (p)中只有b的所有原子处于同一平面
【变式训练2】(2024·四川成都·模拟预测)4-溴甲基肉桂酸甲酯是合成抗肿瘤药物帕比司他的重要中间
体,其结构简式如图。关于该有机物的说法错误的是
A.能发生加成反应、氧化反应、聚合反应
B.含有3种官能团
C.其苯环上的二氯代物有四种(不考虑立体异构)
D.最多有18个原子共平面
考向3 考查同分异构体的判断与书写
例3(2024·福建三明·模拟)能使溴水褪色,含有3个甲基,其分子式为C H Br的有机物(不考虑立体异
6 11
构)共有( )
A.10种 B.11种
C.12种 D.13种
【思维建模】限定条件下同分异构体书写步骤【变式训练1】(2024·湖南郴州·模拟)分子式为C HBrCl的有机物共有(不含立体异构)( )
4 8
A.8种 B.10种
C.12种 D.14种
【变式训练2】(23-24高三上·黑龙江·开学考试)下列有机物的同分异构体数目判断正确的是
A.分子式为C H 的链状烃共有(考虑顺反异构体)7种
5 10
B.正丁烷的一氯代物同分异构体有2种,二氯代物的同分异构体有5种
C. 的一溴代物和 的一溴代物都有4种(不考虑立体异构)
D.三联苯( )的一氯代物有4种
考点三 研究有机化合物的一般步骤和方法
知识点1 有机物的分离与提纯
1.研究有机化合物的基本步骤
(1)分离提纯:得到 有机物;
(2)元素定量分析:确定有机物的 ;
(3)测定相对分子质量:确定有机物的 ;
(4)波谱分析:确定有机物的 ;
2.分离提纯有机物常用的方法
(1)蒸馏和重结晶
适用对象 要求
常用于分离、提纯液态有机 ①该有机物热稳定性较强
蒸馏
物 ②该有机物与杂质的 相差较大①杂质在所选溶剂中溶解度很小或很大
常用于分离、提纯固态有机
重结晶 ②被提纯的有机物在此溶剂中溶解度受 影
物
响较大
(2)萃取和分液
液—液萃取 利用待分离组分在两种互不相溶的溶剂中的 不同,将其从一种溶剂转
移到另一种溶剂的过程
固—液萃取 用溶剂从固体物质中溶解出待分离组分的过程
注意:①液—液萃取所使用分液漏斗分液时先将下层液体从下口放出,再将上层液体从上口倒出。②常用
的萃取剂:苯、CCl 、乙醚、石油醚、二氯甲烷等。
4
知识点2 有机化合物分子式和结构式的确定
1.有机物分子式的确定
(1)元素定性、定量分析——确定实验式
①元素定性、定量分析:用化学方法测定有机化合物的元素组成,以及各元素的质量分数,如燃烧后
C→CO,H→H O。
2 2
②李比希氧化产物吸收法定量分析原理:一定量 有
机物中所含各元素质量分数→各元素原子的最简整数比→实验式。
如:C、H、O元素的有机物 分子中碳、氢元素的质
量分数→剩余的为氧元素的质量分数。
(2)质谱法——相对分子质量的确定
①相对分子质量的测定——质谱法:在质谱图中,有机分子的相对分子质量=最大质荷比。。
②计算气体相对分子质量的常用方法
a.M=
b.M=22.4ρ(标准状况)
c.阿伏加德罗定律,同温同压下==D,则M=M=DM
1 2 2
③根据有机分子的 和 确定分子式。
(3)确定有机物分子式
①最简式规律
最简式 对应物质
CH 乙炔和苯
CH 烯烃和环烷烃
2
CHO 甲醛、乙酸、甲酸甲酯、葡萄糖、果糖
2
②常见相对分子质量相同的有机物
a.同分异构体相对分子质量相同。
b.含有n个碳原子的醇与含(n-1)个碳原子的同类型羧酸和酯相对分子质量相同。c.含有n个碳原子的烷烃与含(n-1)个碳原子的饱和一元醛(或酮)相对分子质量相同,均为14n+2。
说明: 的余数为0或碳原子数大于或等于氢原子数时,将碳原子数依次减少一个,每减少一个碳原子即增加
12个氢原子,直到饱和为止。确定烃的最大饱和氢原子数的分子式,在此基础上,每减少一个碳原子和四
个 氢 原 子 就 增 加 一 个 氧 原 子 , 直 到 不 能 减 为 止 , 从 而 得 到 一 系 列 可 能 的 分 子 式 , 如
C H →C H O→C H O→C HO→C HO。
9 20 8 16 7 12 2 6 8 3 5 4 4
2.分子结构的鉴定
(1)化学方法:利用特征反应鉴定出官能团,再制备它的衍生物进一步确认,常见官能团特征反应如
下:
官能团种类 试剂 判断依据
碳碳双键或 溴的CCl 4 溶液 橙红色褪去
碳碳三键
酸性KMnO 溶液 紫色褪去
4
卤素原子 NaOH溶液,AgNO 和稀硝酸的混合液 有沉淀产生
3
醇羟基 钠 有氢气放出
FeCl 溶液 显紫色
3
酚羟基
浓溴水 有白色沉淀产生
银氨溶液 有银镜生成
醛基
新制Cu(OH) 悬浊液 有红色沉淀产生
2
羧基 NaHCO 溶液 有CO 气体放出
3 2
(2)物理方法
①红外光谱——确定 和 :
分子中化学键或官能团可对红外线发生振动吸收,不同化学键或官能团吸收频率不同,在红外光谱图上将
处于不同的位置,从而可以获得分子中含有何种化学键或官能团的信息。
②核磁共振氢谱——确定 的类型和相对数目:
不同化学环境的氢原子
③X射线衍射——分子结构的相关数据:
根据X射线衍射图,经过计算可获得分子结构的有关数据,如 、 等,将X射线衍射技术用
于有机化合物 的测定。
(3)有机物分子中不饱和度(Ω)的确定
①计算公式:Ω=n(C)+1-
其中,n(C)为分子中碳原子数目,n(H)为分子中氢原子数目,若分子中含有Cl、F等,则用n(H)加上其数
目,若分子中含有N等,则用n(H)减去其数目,若分子中含有O、S等,其数目不计入计算公式。
②不饱和度与有机物结构的关系
不饱和度与有机物结构的关系考向1 考查有机物的分离与提纯
例1(2024·黑龙江哈尔滨·模拟)下列有关有机化合物分离、提纯的方法错误的是( )
选项 混合物 试剂 分离提纯方法
A 乙烯(SO ) NaOH溶液 洗气
2
B 乙醇(乙酸) NaOH溶液 分液
C 苯(苯甲酸) NaOH溶液 分液
D 乙烷(乙烯) 溴水 洗气
【归纳总结】常见有机化合物的分离、提纯(括号内为杂质)
混合物 试剂 分离方法 主要仪器
甲烷(乙烯) 溴水 洗气 洗气瓶
酸性高锰酸钾溶
苯(乙苯) 分液 分液漏斗
液、NaOH溶液
乙醇(水) CaO 蒸馏 蒸馏烧瓶
溴乙烷(乙醇) 水 分液 分液漏斗
醇(酸) NaOH溶液 蒸馏 蒸馏烧瓶
硝基苯(HNO、
3
NaOH溶液 分液 分液漏斗
HSO )
2 4
苯(苯酚) NaOH溶液 分液 分液漏斗
酯(酸或醇) 饱和NaCO 溶液 分液 分液漏斗
2 3
NaOH溶液 分液 分液漏斗
【变式训练1】(2024·河北邢台·一模)常温下,乙酰苯胺是一种具有解热镇痛作用的白色晶体,20 ℃
时在乙醇中的溶解度为36.9 g,在水中的溶解度如下表(注:氯化钠可分散在醇中形成胶体)。
温度/℃ 25 50 80 100
溶解度/g 0.56 0.84 3.5 5.5
某种乙酰苯胺样品中混入了少量氯化钠杂质,下列提纯乙酰苯胺的方法正确的是( )
A.用水溶解后分液
B.用乙醇溶解后过滤
C.用水作溶剂进行重结晶
D.用乙醇作溶剂进行重结晶
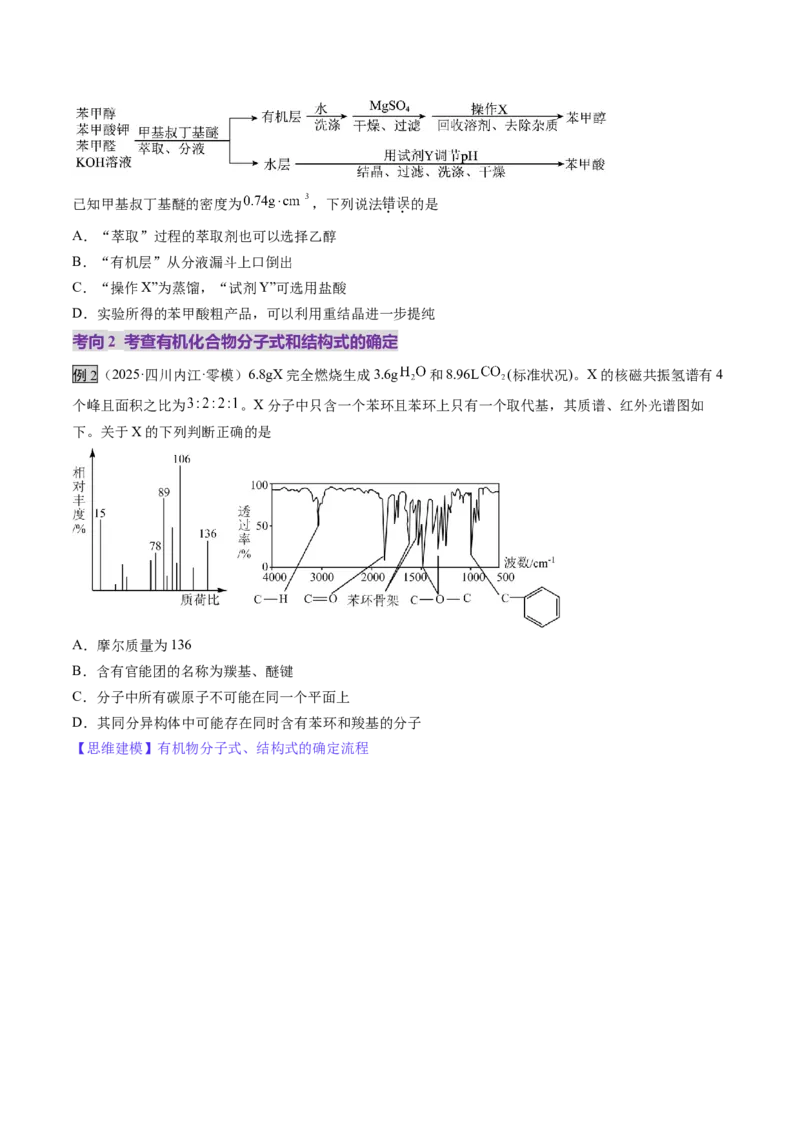
【变式训练2】(2024·浙江绍兴·三模)从苯甲醛和KOH溶液反应后的混合液中分离出苯甲醇和苯甲酸
的过程如下:已知甲基叔丁基醚的密度为 ,下列说法错误的是
A.“萃取”过程的萃取剂也可以选择乙醇
B.“有机层”从分液漏斗上口倒出
C.“操作X”为蒸馏,“试剂Y”可选用盐酸
D.实验所得的苯甲酸粗产品,可以利用重结晶进一步提纯
考向2 考查有机化合物分子式和结构式的确定
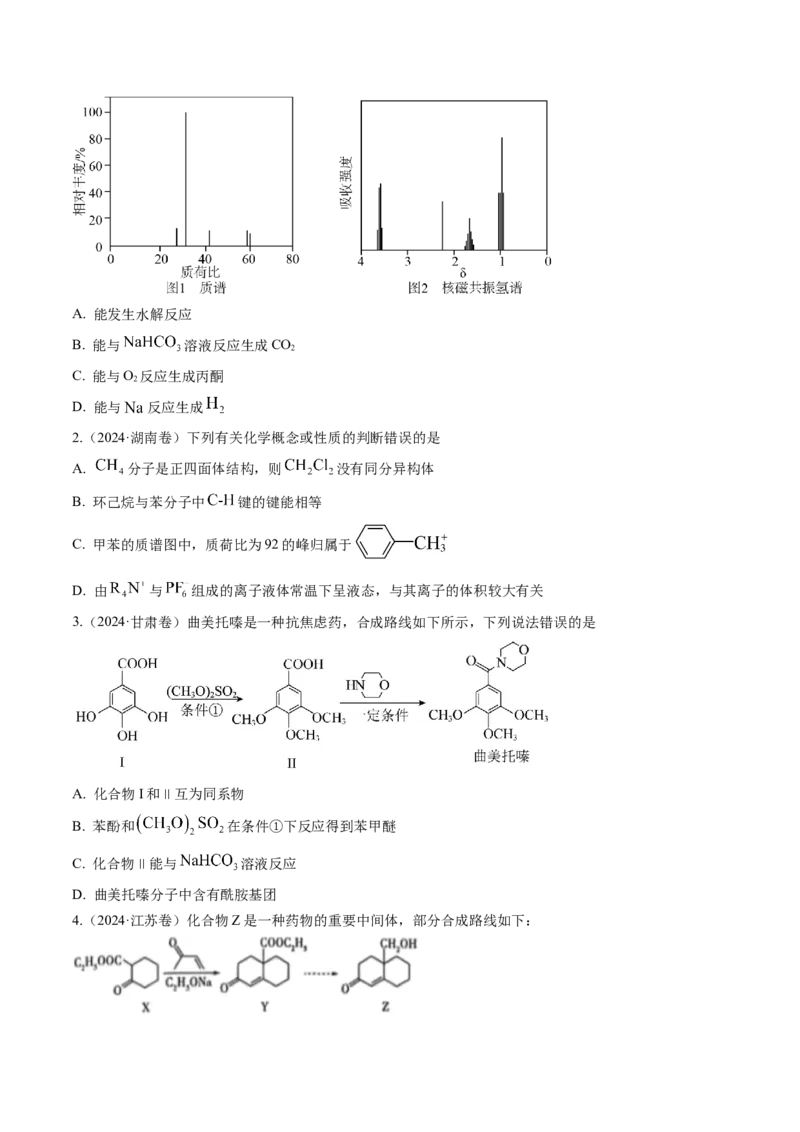
例2(2025·四川内江·零模)6.8gX完全燃烧生成3.6g 和8.96L (标准状况)。X的核磁共振氢谱有4
个峰且面积之比为 。X分子中只含一个苯环且苯环上只有一个取代基,其质谱、红外光谱图如
下。关于X的下列判断正确的是
A.摩尔质量为136
B.含有官能团的名称为羰基、醚键
C.分子中所有碳原子不可能在同一个平面上
D.其同分异构体中可能存在同时含有苯环和羧基的分子
【思维建模】有机物分子式、结构式的确定流程【变式训练1】(2024·四川成都·模拟预测)取有机物M 6.2g 在纯氧中充分燃烧,将产物先后通过浓硫
酸和碱石灰,两者分别增重5.4g 和8.8 g,核磁共振氢谱显示有2组峰,峰面积之比为1:2,下列对反应
的描述正确的是
A.①最终的生成物为HOOC-COOH
B.②可能生成一种六元环状化合物
C.③可发生缩聚生成有机高分子Y
D.④的反应条件为溴水
【变式训练2】(2024·山东济宁·三模)下列方法或仪器使用错误的是
A.红外光谱可用于分析、鉴定元素
B.色谱法可用于分离、提纯有机化合物
C.X射线衍射可测定键长、键角等分子结构信息
D.核磁共振氢谱可用于测定有机物中不同类型的氢原子及其相对数目等信息
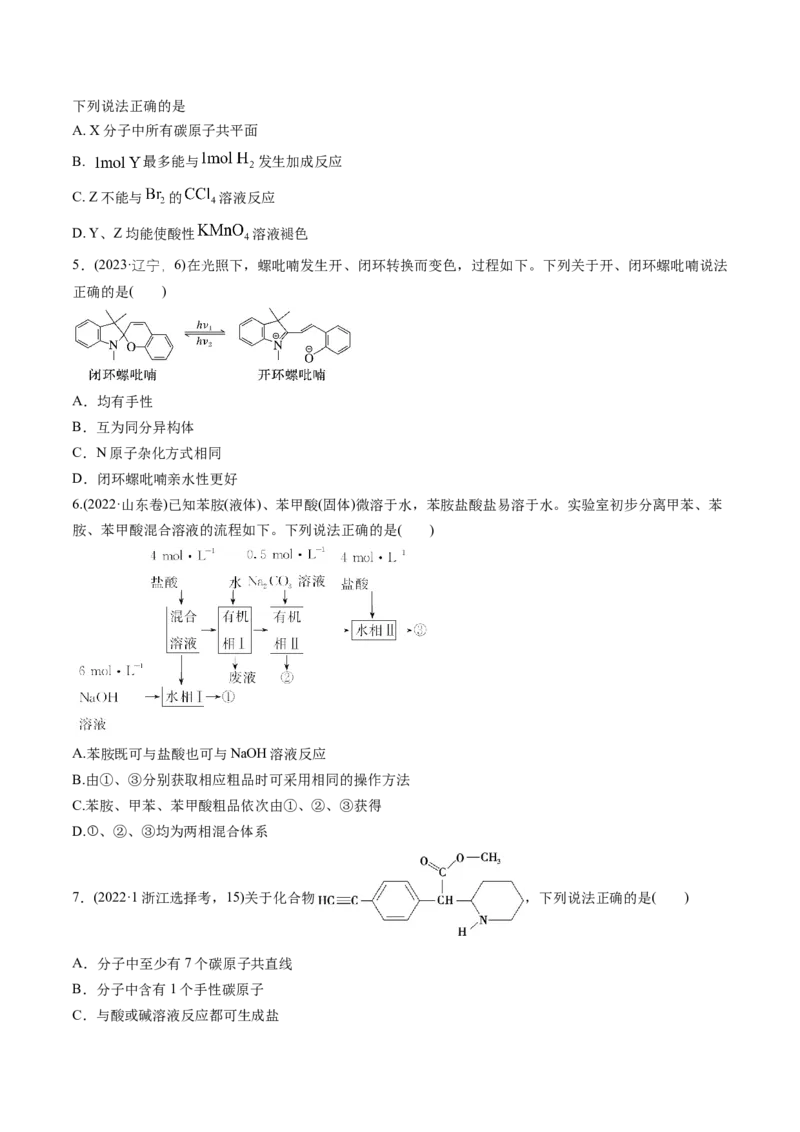
1.(2024·浙江卷)有机物A经元素分析仪测得只含碳、氢、氧3种元素,红外光谱显示A分子中没有醚
键,质谱和核磁共振氢谱示意图如下。下列关于A的说法正确的是A. 能发生水解反应
B. 能与 溶液反应生成CO
2
C. 能与O 反应生成丙酮
2
D. 能与 反应生成
2.(2024·湖南卷)下列有关化学概念或性质的判断错误的是
A. 分子是正四面体结构,则 没有同分异构体
B. 环己烷与苯分子中 键的键能相等
C. 甲苯的质谱图中,质荷比为92的峰归属于
D. 由 与 组成的离子液体常温下呈液态,与其离子的体积较大有关
3.(2024·甘肃卷)曲美托嗪是一种抗焦虑药,合成路线如下所示,下列说法错误的是
A. 化合物I和Ⅱ互为同系物
B. 苯酚和 在条件①下反应得到苯甲醚
C. 化合物Ⅱ能与 溶液反应
D. 曲美托嗪分子中含有酰胺基团
4.(2024·江苏卷)化合物Z是一种药物的重要中间体,部分合成路线如下:下列说法正确的是
A. X分子中所有碳原子共平面
B. 最多能与 发生加成反应
C. Z不能与 的 溶液反应
D. Y、Z均能使酸性 溶液褪色
5.(2023·辽宁,6)在光照下,螺吡喃发生开、闭环转换而变色,过程如下。下列关于开、闭环螺吡喃说法
正确的是( )
A.均有手性
B.互为同分异构体
C.N原子杂化方式相同
D.闭环螺吡喃亲水性更好
6.(2022·山东卷)已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步分离甲苯、苯
胺、苯甲酸混合溶液的流程如下。下列说法正确的是( )
A.苯胺既可与盐酸也可与NaOH溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
7.(2022·1浙江选择考,15)关于化合物 ,下列说法正确的是( )
A.分子中至少有7个碳原子共直线
B.分子中含有1个手性碳原子
C.与酸或碱溶液反应都可生成盐D.不能使酸性KMnO 稀溶液褪色
4