文档内容
第 04 讲 化学反应的方向、化学反应的调控
目 录
01 考情透视·目标导航.........................................................................................................................2
02 知识导图·思维引航.........................................................................................................................3
03 考点突破·考法探究.........................................................................................................................3
考点一 化学反应的方向.............................................................................................................3
知识点1 自发过程与自发反应...............................................................................................3
知识点2 化学反应的方向与能量、熵变的关系...................................................................4
知识点3 化学反应方向判断方法...........................................................................................5
考向1 考查自发过程和自发反应的概念...............................................................................6
考向2 考查化学反应方向的判据...........................................................................................7
考点二 化学反应的调控.............................................................................................................8
知识点1 控制反应条件的目的及措施...................................................................................8
知识点2 工业合成氨的条件选择...........................................................................................9
考向1 考查合成氨反应适宜条件的选择.............................................................................11
考向2 考查工业上选择适宜生产条件的原则.....................................................................11
04 ........................................................................................................................................................13考点要求 考题统计 考情分析
分析近三年高考试题,高考命题在本讲有以下规律:
1.从考查题型和内容上看,高考命题以选择题和非
2024湖北卷12题,3分
选择题呈现,主要考查化学反应的熵变及反应进行的
2023湖北卷3题,3分
化学反应的方向 方向、化工生产中条件的选择等。
2022湖北卷8题,3分
2.从命题思路上看,侧重以化工生产为背景,考查
2022浙江卷20题,2分
结合反应速率及焓变考查化工生产条件的选择。
(1)选择题:考查反应进行的方向,工业生产适宜
条件的选择。
(2)非选择题:常常与基本理论、工业生产相联
系,通过图像或表格提供信息,从反应时间、投料比
2023辽宁卷3题,3分
化学反应的调控 值、催化剂的选择、转化率等角度考查生产条件的选
2021江苏卷14题,3分
择;
3.根据高考命题特点和规律,复习时要注意以下方
面:平衡原理在化工生产中的综合应用。
复习目标:
1.结合学过的化学反应实例,了解自发过程和化学反应的自发性。
2.通过“有序”和“无序”的对比,了解熵和熵变的意义。
3.初 初 初 初 初 变和熵变初 化学反应方向的初 初 初 能初 初 变和熵变初 初 化学反应的方向初 初 初 初 据初 初 与初 初 初 知能初 初
4.认识化学反应速率和化学平衡的综合调控在生产、生活和科学研究中的重要作用。
5.知初 初 化初 初 初 初 变反应初 程初 初 调控化学反应初 初 初 初 初 初 初 初 初考点一 化学反应的方向
知识点1 自发过程与自发反应
1.自发过程
(1)概念:在一定条件下,不需要借助外力作用就能自动进行的过程。
(2)特点:
①体系趋向于从高能状态转变为低能状态(体系对外部做功或释放热量)。
②在密闭条件下,体系有从有序转变为无序的倾向性(无序体系更加稳定)。
2.自发反应
(1)概念:在一定条件下无需外界帮助就能自发进行的反应称为自发反应。
(2)特点:①自发反应具有方向性,即反应的某个方向在一定条件下自发进行,而该反应的逆方向在该条件下肯定不
能自发进行。
②能够自发进行的反应在常温下不一定能够发生,自发性只能用于判断反应的方向,不能确定反应是否一定
会发生和发生的速率。
知识点2 化学反应的方向与能量、熵变的关系
1.熵与熵变
(1)熵的含义:熵是衡量一个体系混乱度的物理量,即表示体系的不规则或无序状态程度的物理量。混
乱度越大,体系越无序,体系的熵就越大。用符号S表示。同一条件下,不同物质有不同的熵值,同一物质在
不同状态下熵值也不同,一般规律是S(g)>S(l)>S(s)。
(2)熵变的含义:熵变是反应前后体系熵的变化,用 Δ S 表示,化学反应的 Δ S 越大,越有利于反应自发
进行。
2.化学反应的方向与能量的关系
能量变化是一个与反应能否自发进行有关的因素,但不是决定反应能否自发进行的惟一因素。
(1)多数能自发进行的化学反应是放热反应。
例如:在常温、常压下,氢氧化亚铁被氧化为氢氧化铁的反应是自发的,反应放热:
4Fe(OH) (s)+2HO(1)+O(g)===4Fe(OH) (s) ΔH(298 K)=-444.3 kJ/mol
2 2 2 3
(2)有不少吸热反应也能自发进行。
例如:NH HCO (s)+CHCOOH(aq)===CO (g)+CHCOONH(aq)+HO(1) ΔH(298 K)=+37.30 kJ/mol
4 3 3 2 3 4 2
(3)有一些吸热反应在室温条件下不能自发进行,但在较高温度下则能自发进行。
例如:在室温下和较高温度下均为吸热过程的CaCO 的分解反应。
3
CaCO (s)===CaO(s)+CO(g) ΔH(298 K)=+178.2 kJ/mol ΔH(1 200 K)=+176.5 kJ/mol
3 2
结论:研究表明,对于化学反应而言,绝大多数放热反应都能自发进行,且反应放出的热量越多,体系能
量降低得也越多,反应越完全。可见,反应的焓变是制约化学反应能否自发进行的因素之一。
注意:①反应能量判据不是决定反应能否自发进行的惟一因素。②有些吸热反应也能自发进行。
3.化学反应的方向与熵变的关系
化学反应中要发生物质的变化或物质状态的变化,因此存在着熵变。反应的熵变ΔS为反应产物总熵与反
应物总熵之差。对于确定的化学反应,在一定条件下具有确定的熵变。
(1)许多熵增加的反应在常温、常压下可以自发进行。产生气体的反应,气体物质的物质的量增大的反
应,熵变通常都是正值,为熵增反应。
例如:2HO(aq)===2H O(l)+O(g);NH HCO (s)+CHCOOH(aq)===CO (g)+CHCOONH(aq)+HO(l);
2 2 2 2 4 3 3 2 3 4 2
(2)有些熵增的反应在常温、常压下不能自发进行,但在较高温度下可以自发进行。
例如:CaCO (s)===CaO(s)+CO(g);C(石墨,s)+HO(g)===CO(g)+H(g);
3 2 2 2
(3)铝热反应是熵减的反应,它在一定条件下也可以自发进行。
例如:2Al(s)+Fe O(s)===AlO(s)+2Fe(s);
2 3 2 3
结论:研究表明,除了热效应外,决定化学反应能否自发进行的另一个因素是体系的混乱度,大多数自发
反应有趋向于体系混乱度增大的倾向。
注意:①少数熵减少的反应在一定条件下也可以自发进行,如NH (g)+HCl(g)=NH4Cl(s)。②孤立体系或绝热
3体系的自发过程才向着熵增的方向进行。
知识点3 化学反应方向判断方法
1.传统的判断方法
(1)由不稳定物质向稳定物质转变
2NaHCO NaCO+CO↑+HO,稳定性:NaCO >NaHCO 。
3 2 3 2 2 3 3
(2)离子反应中,对于复分解反应,一般是由易电离的物质向难电离的物质转变,或向离子浓度减小的
方向转变。
①由溶解度大的物质向溶解度小的物质转变。
如NaSO +CaCl ===CaSO ↓(微溶)+2NaCl,CaSO +NaCO===CaCO ↓+NaSO ,所以溶解性:CaCl >
2 4 2 4 4 2 3 3 2 4 2
CaSO>CaCO 。
4 3
②由相对强酸(碱)向相对弱酸(碱)转变。
如2CHCOOH+NaCO===2CH COONa+CO↑+HO,NaSiO +CO +HO===H SiO↓+NaCO ,所以酸
3 2 3 3 2 2 3 2 2 2 3 2 3
性强弱:CHCOOH>HCO>HSiO。
3 2 3 2 3
(3)由难挥发(高沸点)性物质向易挥发(低沸点)性物质转变。
①由难挥发性酸向易挥发性酸转变。
如NaCl+HSO (浓) NaHSO+HCl↑,所以沸点:HSO (浓)>HCl。
2 4 4 2 4
②由难挥发性酸酐向易挥发性酸酐转变。
如CaCO +SiO=====CaSiO +CO↑,所以沸点:SiO>CO。
3 2 3 2 2 2
③由难挥发性金属向易挥发性金属转变。
如2RbCl+Mg=====MgCl +2Rb,所以沸点:Mg>Rb。
2
(4)由氧化性(还原性)强的物质向氧化性(还原性)弱的物质的转变。
如2FeCl +2KI===2FeCl +2KCl+I 2FeCl +Cl===2FeCl ,所以氧化性Cl>FeCl >I。
3 2 2, 2 2 3 2 3 2
2.用焓变和熵变判断反应的方向
体系的自由能变化(符号为 Δ G ,单位为 kJ/mol)综合考虑了焓变和熵变对体系的影响,可用于化学反应自
发进行的方向的判断,ΔG= Δ H - T Δ S 。
(1)当ΔH<0,ΔS>0时,ΔG<0,反应自发进行。
(2)当ΔH>0,ΔS<0时,ΔG>0,反应不能自发进行。
(3)当ΔH>0,ΔS>0或ΔH<0,ΔS<0时,反应是否自发进行与温度有关,在一定温度下可使ΔG=0,
即反应达平衡状态。
(4)ΔH<0、ΔS<0时,则ΔH-TΔS在较低温度时可能小于零,所以低温有利于反应自发进行。图解如下:【易错提醒】①根据ΔH-TΔS<0判断的只是反应能否自发进行的可能性,具体的反应能否实际发生,还
涉及到化学反应速率的问题。
②判断一个化学反应能否自发进行,若无任何外加条件,可以认为我们所学过的化学反应(电解反应除外)
都是能够自发进行的。
考向1 考查自发过程和自发反应的概念
例1下列不属于自发进行的变化是( )
A.红墨水加到清水使整杯水变红
B.冰在室温下融化成水
C.水电解生成氢气和氧气
D.铁器在潮湿的空气中生锈
【易错提醒】关于反应自发性需要注意:(1)化学反应方向的判据指出的仅仅是在一定条件下化学反应
自发进行的趋势,并不能说明在该条件下反应一定能实际发生,还要考虑化学反应的快慢问题。(2)自
发过程的两种倾向:①体系趋向于高能状态转变为低能状态(体系对外部做功或释放热量)。②在密闭条件
下,体系有从有序转变为无序的倾向性(无序体系更加稳定)。
【变式训练1】有关化学反应的说法,正确的是
A.自发反应都是放热反应 B.自发反应都是熵增大的反应
C.自发反应一定能实现 D.非自发反应在一定条件下能实现
【变式训练2】下列关于自发过程的叙述中,正确的是
A.只有不需要任何条件就能够自动进行的过程才是自发过程
B.需要加热才能够进行的过程肯定不是自发过程
C.非自发过程,改变温度也不能变为自发过程
D.能自发进行的反应不一定能迅速发生反应
考向2 考查化学反应方向的判据
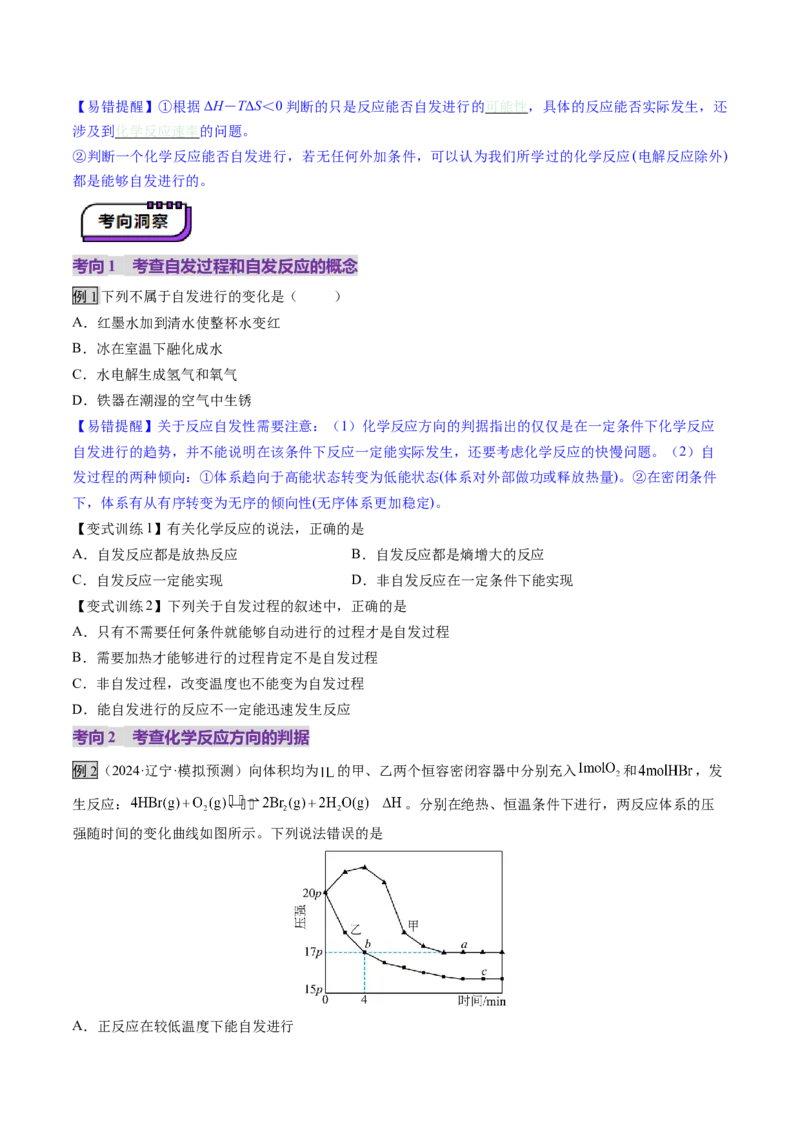
例2(2024·辽宁·模拟预测)向体积均为 的甲、乙两个恒容密闭容器中分别充入 和 ,发
生反应: 。分别在绝热、恒温条件下进行,两反应体系的压
强随时间的变化曲线如图所示。下列说法错误的是
A.正反应在较低温度下能自发进行B.乙在恒温条件下进行,
C.a点的正反应速率大于c点的正反应速率
D.甲条件下平衡常数K小于20.25
【思维建模】1.反应能否自发进行需综合考虑焓变和熵变对反应的影响,复合判据ΔH-TΔS<0的反应不
一定能够实际发生,只是指出了在该条件下化学反应自发进行的趋势,还要考虑化学反应的快慢问题。
2.焓变、熵变和温度对化学反应方向的影响
ΔH ΔS ΔH-TΔS 反应情况
- + 永远是负值 在任何温度下过程均自发进行
+ - 永远是正值 在任何温度下过程均非自发进行
+ + 低温为正高温为负 低温时非自发,高温时自发
- - 低温为负高温为正 低温时自发,高温时非自发
【变式训练1】(2024·黑龙江牡丹江·一模)工业以硫黄或黄铁矿(主要成分FeS,烧渣主要成分为Fe O)
2 2 3
为主要原料生产硫酸主要流程如下:
下列说法正确的是
A.高温焙烧1 mol FeS 时转移的电子数为15 N (N 代表阿伏加德罗数值)
2 A A
B.SO 与HS反应生成淡黄色沉淀,体现了SO 的还原性
2 2 2
C.反应2SO (g)+O(g) 2SO (g)具有自发性的原因是ΔH<0
2 2 3
D.98%浓硫酸粘度较高,与其范德华力较大有关
【变式训练2】(2024·江苏南通·二模) 可用于低温下催化氧化HCHO:
。下列关于 催化氧化甲醛的反应
说法正确的是
A.该反应 , B.HCHO、 、 均为极性分子
C.升高温度, 增大, 减小 D.使用 催化剂降低了该反应的焓变
考点二 化学反应的调控知识点1 控制反应条件的目的及措施
1.控制反应条件的目的
(1)促进有利的化学反应:通过控制反应条件,可以加快化学反应速率,提高反应物的转化率,从而促
进有利的化学反应进行。
(2)抑制有害的化学反应:通过控制反应条件,也可以减缓化学反应速率,减少甚至消除有害物质的产
生或控制副反应的发生,从而抑制有害的化学反应继续进行。
2.控制反应条件考虑因素:在实际生产中常常需要结合设备条件、安全操作、经济成本等情况,综合考虑
影响化学反应速率和化学平衡的因素,寻找适宜的生产条件。此外,还要根据环境保护及社会效益等方面
的规定和要求做出分析,权衡利弊,才能实施生产。
3.控制反应条件的基本措施
(1)控制化学反应速率的措施
通过改变反应体系的温度、溶液的浓度、气体的压强(或浓度)、固体的表面积以及使用催化剂等途径调控
反应速率。
(2)提高转化率的措施
通过改变可逆反应体系的温度、溶液的浓度、气体的压强(或浓度)等改变可逆反应的限度,从而提高转化
率。
4.工业上选择适宜生产条件的原则
外界 有利于加快速率 有利于平衡正向移动的条件
综合分析结果
条件 的条件控制 控制
增大反应物的浓 增大反应物的浓度、减小生 不断地补充反应物、及时地分离出生成
浓度
度 成物的浓度 物
催化剂 加合适的催化剂 不需要 加合适的催化剂
兼顾速率和平衡,考虑催化剂的适宜温
ΔH<0 低温
度
温度 高温
在设备条件允许的前提下,尽量采取高
ΔH>0 高温
温并考虑催化剂的活性
在设备条件允许的前提下,尽量采取高
高压(有气体参 Δν<0 高压
g
压强 压
加)
Δν>0 低压 兼顾速率和平衡,选取适宜的压强
g
知识点2 工业合成氨的条件选择
1、合成氨反应的特点
(1)反应:合成氨反应:N(g)+3H(g) 2NH (g)。已知298 K时:ΔH=-92.4 kJmol-1,ΔS=-198.2
2 2 3
Jmol-1K-1。
(2)特点:
①可逆反应
②放热反应:ΔH<0
③熵减的反应:ΔS<0④常温(298 K)下,ΔH-TΔS<0,能自发进行。
2、合成氨反应特点的分析
影响因素
对合成氨反应的影响
浓度 温度 压强 催化剂
增大合成氨的反应速率 增大 升高 增大 使用
提高平衡混合物中氨的含
增大 降低 增大 无影响
量
3、工业合成氨的适宜条件
1)工业合成氨的适宜条件
外部条件 工业合成氨的适宜条件
压强 根据反应器可使用的钢材质量及综合指标来选择压强 (1 0 ~ 30 MPa )
温度 适宜温度, 40 0 ~ 500 ℃
催化剂 使用铁触媒做催化剂( 500℃ 左右时的活性最大)
浓度 N 和 H 的物质的量之比为 1∶2. 8 的投料比,氨及时从混合气中分离出去
2 2
2)问题讨论
(1)压强:目前我国合成氨厂一般采用的压强在10~30 MPa,不采用更高压强的理由是:压强越大,对
设备的要求越高、需要的动力越大。
(2)温度:升高温度能提高化学反应速率,但工业合成氨温度不能太高的理由是:
①合成氨反应为放热反应,升高温度,转化率降低。
②400~500_℃催化剂活性最大,升高温度,催化剂活性减弱。
注意:工业生产中,必须从反应限度和反应速率两个角度选择合成氨的适宜条件,既要考虑尽量增大反应
物的转化率,充分利用原料,又要选择较快的反应速率,提高单位时间内的产量,同时还要考虑设备的要
求和技术条件。
4、合成氨的生产流程
(1)生产流程
(2)流程分析
①原料气干燥、净化:除去原料气中的水蒸气及其他气体杂质,防止与催化剂接触时,导致催化剂“中毒”而降低或丧失催化活性
②压缩机加压:增大压强
③热交换:合成氨反应为放热反应,反应体系温度逐渐升高,为原料气反应提供热量,故热交换可充分利
用能源,提高经济效益。
④冷却:生成物NH 的液化需较低温度采取迅速冷却的方法,可使气态氨变成液氨后及时从平衡混合物中
3
分离出来,以促使平衡向生成NH 的方向移动。
3
⑤循环使用原料气:因合成氨反应为可逆反应,平衡混合物中含有原料气,将 NH 分离后的原料气循环利
3
用,并及时补充N 和H,使反应物保持一定的浓度,以利于合成氨反应,提高经济效益。
2 2
考向1 考查合成氨反应适宜条件的选择
例1工业合成氨的反应为:N(g) + 3H(g) 2NH (g) △H <0,该反应应采取的适宜条件是
2 2 3
A.低温、高压、催化剂 B.适宜的温度、压强、催化剂
C.低温、常压、催化剂 D.高温、高压、催化剂
【思维建模】工业生产中,必须从反应限度和反应速率两个角度选择合成氨的适宜条件,既要考虑尽量增
大反应物的转化率,充分利用原料,又要选择较快的反应速率,提高单位时间内的产量,同时还要考虑设
备的要求和技术条件。
【变式训练1】氨是制造化肥的重要原料,如图为工业合成氨的流程图。下列有关说法错误的是
A.工业上制氮气一般用分离液态空气法
B.步骤②、③、④、⑤均有利于提高反应物的平衡转化率
C.步骤①中“净化”N、H 混合气体可以防止催化剂中毒
2 2
D.步骤③中温度选择500℃,主要是考虑催化剂的活性
【变式训练2】(23-24高三上·天津·阶段考试)某温度下发生反应:3H(g)+N(g)⇌2NH (g) ΔH=-92.4kJ/
2 2 3
mol,N 的转化率(α)与体系总压强(p)的关系如图所示,下列说法中正确的是
2
A.将1molN 、3molH 置于1L密闭容器中发生反应,放出的热量为92.4kJ
2 2
B.平衡状态由A变到B时,平衡常数K