文档内容
第 05 讲 氧化还原反应方程式的配平、书写及计算
01 模拟基础练
【题型一】氧化还原反应方程式的书写与配平
【题型二】氧化还原反应的计算方法——电子守恒法
02 重难创新练
03 真题实战练
题型一 氧化还原反应方程式的书写与配平
1.水热法制备 纳米颗粒的反应如下(反应条件忽略):
。下列说法错误的是
A.该反应中 作氧化剂 B.该反应中 和 都是还原剂
C.3个 参加反应时有1个 被氧化 D.离子方程式中
2.工业制硫酸的原理示意图如图:
下列说法不正确的是
A.燃烧的化学方程式为4FeS+11O 2Fe O+8SO
2 2 2 3 2
B.1mol SO 和足量O 充分反应转移2mol电子
2 2
C.用98.3%的浓硫酸吸收三氧化硫可避免形成酸雾
D.可用浓氨水吸收生产过程中的尾气并转化为铵盐
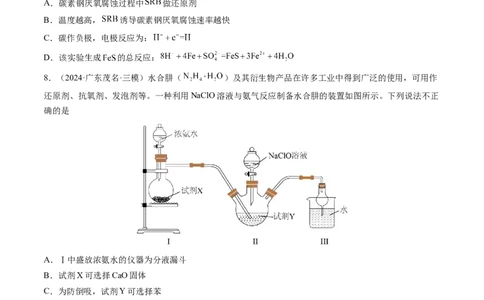
3.酸性条件下,黄铁矿催化氧化反应的产物之一为 ,实现该反应的机理如图所示。下列说法错误的
是A.酸性条件下,黄铁矿催化氧化中NO作催化剂
B.反应Ⅲ中,每消耗 转移电子
C. 在反应Ⅱ中作氧化剂
D.黄铁矿催化氧化反应为:
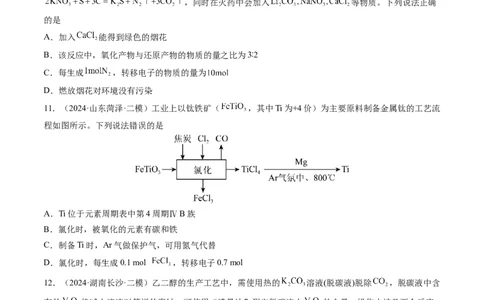
4.(2024·江苏扬州·模拟预测)CuCl为难溶于水的白色固体。室温下,以CuO为原料制备CuCl的过程如
图所示。下列说法正确的是
A.0.1 溶液中:
B.“还原”发生反应的离子方程式为:
C.“还原”后的溶液中:
D.“过滤”后得到的滤液中:
5.(2024·河北保定·二模) 是一种重要的还原剂,常用于造纸等行业。下列离子方程式错误的是
A.在溴水中滴加 溶液,溶液褪色:
B.在 和 的混合液中滴加稀硫酸:
C.在 溶液中滴加少量 溶液:
D.在石灰乳中滴加少量的饱和 溶液:
6.(2024·四川绵阳·模拟预测)下列离子方程式书写正确的是
A.KClO碱性溶液与 反应制备高铁酸钾:
B.用白醋浸泡过的淀粉—KI试纸检验加碘盐中的 :
C.向NaClO溶液中通入少量 气体:
D. 溶液与足量的NaOH溶液反应:
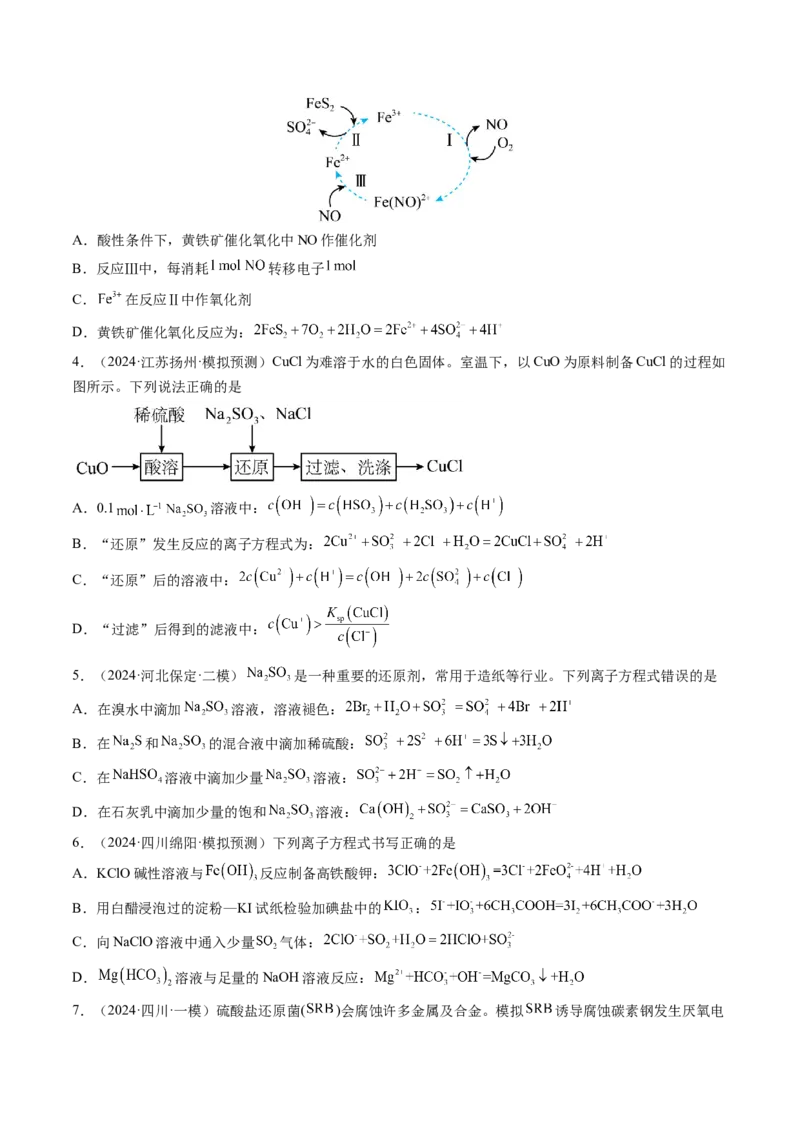
7.(2024·四川·一模)硫酸盐还原菌( )会腐蚀许多金属及合金。模拟 诱导腐蚀碳素钢发生厌氧电化学腐蚀实验,实验后发现碳素钢表面覆盖物成分是硫化物(主要含 ),腐蚀机理如图所示。下列说法
正确的是
A.碳素钢厌氧腐蚀过程中 做还原剂
B.温度越高, 诱导碳素钢厌氧腐蚀速率越快
C.碳作负极,电极反应为:
D.该实验生成 的总反应:
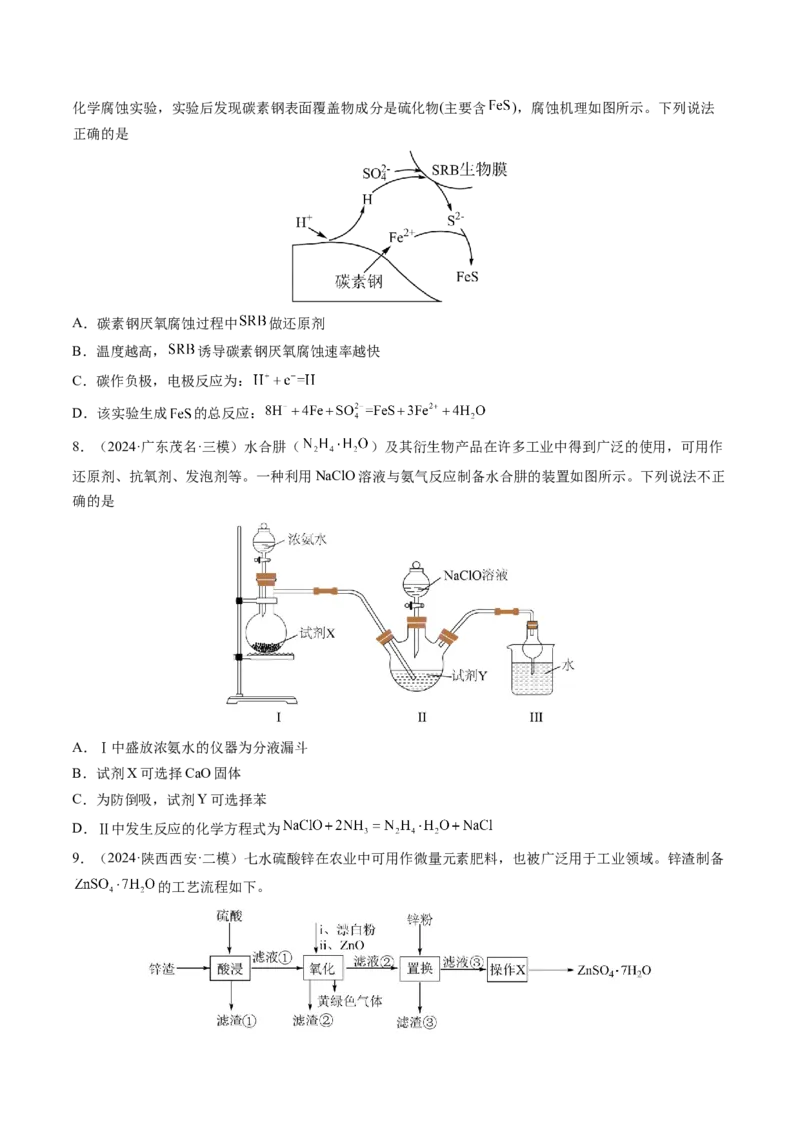
8.(2024·广东茂名·三模)水合肼( )及其衍生物产品在许多工业中得到广泛的使用,可用作
还原剂、抗氧剂、发泡剂等。一种利用NaClO溶液与氨气反应制备水合肼的装置如图所示。下列说法不正
确的是
A.Ⅰ中盛放浓氨水的仪器为分液漏斗
B.试剂X可选择CaO固体
C.为防倒吸,试剂Y可选择苯
D.Ⅱ中发生反应的化学方程式为
9.(2024·陕西西安·二模)七水硫酸锌在农业中可用作微量元素肥料,也被广泛用于工业领域。锌渣制备
的工艺流程如下。锌渣的主要成分为 ,含有少量 下列说法正确的是
A.滤渣①为 ,滤渣③为 和
B.氧化操作发生的反应为:
C.加入 的主要作用是调节溶液的
D.操作X用到的玻璃仪器有蒸发皿、玻璃棒、漏斗
题型二 氧化还原反应的计算方法——电子守恒法
10.(2024·吉林·模拟预测)元宵佳节松花江畔焰火璀璨,燃放烟花时发生:
,同时在火药中会加入 等物质。下列说法正确
的是
A.加入 能得到绿色的烟花
B.该反应中,氧化产物与还原产物的物质的量之比为3∶2
C.每生成 ,转移电子的物质的量为
D.燃放烟花对环境没有污染
11.(2024·山东菏泽·二模)工业上以钛铁矿( ,其中Ti为+4价)为主要原料制备金属钛的工艺流
程如图所示。下列说法错误的是
A.Ti位于元素周期表中第4周期ⅣB族
B.氯化时,被氧化的元素有碳和铁
C.制备Ti时,Ar气做保护气,可用氮气代替
D.氯化时,每生成0.1 mol ,转移电子0.7 mol
12.(2024·湖南长沙·二模)乙二醇的生产工艺中,需使用热的 溶液(脱碳液)脱除 ,脱碳液中含
有的 能减少溶液对管道的腐蚀。可使用“碘量法”测定脱碳液中 的含量,操作中涉及两个反应
如下:
① ;② 。
下列说法错误的是
A.反应①中氧化剂与还原剂物质的量之比为3∶2
B.反应①生成1mol 时,反应转移1mol电子
C.V的最高价为+5价,推测 有氧化性和还原性
D.溶液酸性过强时,反应②易发生其他反应13.(2024·福建漳州·三模)连二亚硫酸钠 俗称保险粉,是印染工业中常用的漂白剂。实验室制
备流程如下:
下列说法错误的是
A.将锌粉溶于水形成悬浊液可以提高反应速率
B.生成 的反应中氧化剂和还原剂物质的量之比为
C.温度超过 会导致 溶解度降低
D.加入 有利于 析出,提高产率
14.(2024·广东·二模)高铁酸钾是一种新型的消毒剂,可以做到消毒、净水两用。高铁酸钾常用反应
3ClO-+2Fe3++10OH-=2 +3Cl-+5H O制备,下列说法不正确的是
2
A.生成1mol ,转移3mol电子
B.高铁酸钾可以消毒净水两用是因其有强氧化性且生成胶体
C.高铁酸钾消毒剂不能和洁厕灵混合
D.氧化产物与还原产物物质的量之比为2:5
15.(2024·四川德阳·二模) 是有毒的污染性气体,可将其与氧气的混合气体通入
的混合溶液中进行处理,其物质转化如图所示。下列说法正确的是
A.过程①中发生的反应是复分解反应
B.过程②中每生成 转移 个电子
C.过程③中每转化 ,需
D.总反应为
16.(2024·重庆·模拟预测)科学研究发现某些酶可以促进H+和e-的转移(如下图a、b和c过程),可将海
洋中的NO 转化为N,反应过如图所示。下列说法正确的是
2 2A.过程I的离子方程式为: +2H+ NO+H O
2
B.消耗1molNO,b过程转移2mole-
C.高温有利于促进该过程中H+和e-的转移
D.过程I→III的总反应中氧化剂和还原剂的物质的量之比为1∶1
17.(2024·新疆乌鲁木齐·二模)光催化CO 还原是一种有望在固碳和绿色能源领域应用的技术。水溶液
2
中复合材料BM﹣MS(Bi MoO ﹣MoS )光催化CO 还原为醇类的机理图如图,h+是电子跃迁后留下的空
2 6 2 2
穴,具有强氧化性。下列说法不正确的是
A.HO在富集空穴的MoS 材料上发生氧化反应
2 2
B.光催化CO 还原在一定条件下也可以生成甲烷等有机物
2
C.在BiMoO 材料上,消耗标准状况下2.24 LCO 时,转移0.4 mol电子
2 6 2
D.光催化过程的总反应是2CO+3H O=C HOH+3O 和2CO+4H O=2CHOH+3O
2 2 2 5 2 2 2 3 2
18.(2024·湖南·模拟预测)钛(Ti)和钛合金被广泛应用于火箭、导弹、航天飞机等领域。工业上以钛铁矿
(FeTiO,其中Ti为+4价)为主要原料制备金属钛的工艺流程如下图所示:
3
已知:TiCl 的熔点―25℃,沸点136.4℃
4
下列说法错误的是
A.步骤①的反应过程元素的化合价没有发生变化B.步骤③的操作名称是加热或高温煅烧
C.步骤④的反应方程式TiO+2C+2Cl TiCl +2CO
2 2 4
D.由TiCl 制备Ti的过程中,可以加入氮气做保护气体
4
19.(2024·北京海淀·三模)用高分子吸附树脂提取卤水中的碘(主要以 形式存在)的工艺流程如下:
下列说法正确的是
A.经①和④所得溶液中, 后者小于前者
B.④的作用是将吸附的碘还原而脱离高分子树脂
C.若②和⑤中分别得到等量 ,则消耗的
D.由⑥能得到碘产品是因为碘分子为极性分子,与溶液中的其他微粒间的作用力较弱
20.(2024·湖南长沙·三模)一种利用含钴废料(主要成分为 ,还含有少量 等杂
质)制备 的工艺流程如下。
已知:①常温下,部分金属离子沉淀的 如下表:
金属离子
开始沉淀的 8.5 2.2 3.4 7.8
完全沉淀 (金属离子) 的的 10.0 3.0 4.5 9.4
② 的 的 。
下列说法不正确的是
A.由流程可知氧化性:
B.常温下加入的 溶液显碱性
C.气体 通入氨水至过量后所得溶液可循环利用
D.“高温焙烧”时的化学方程式:
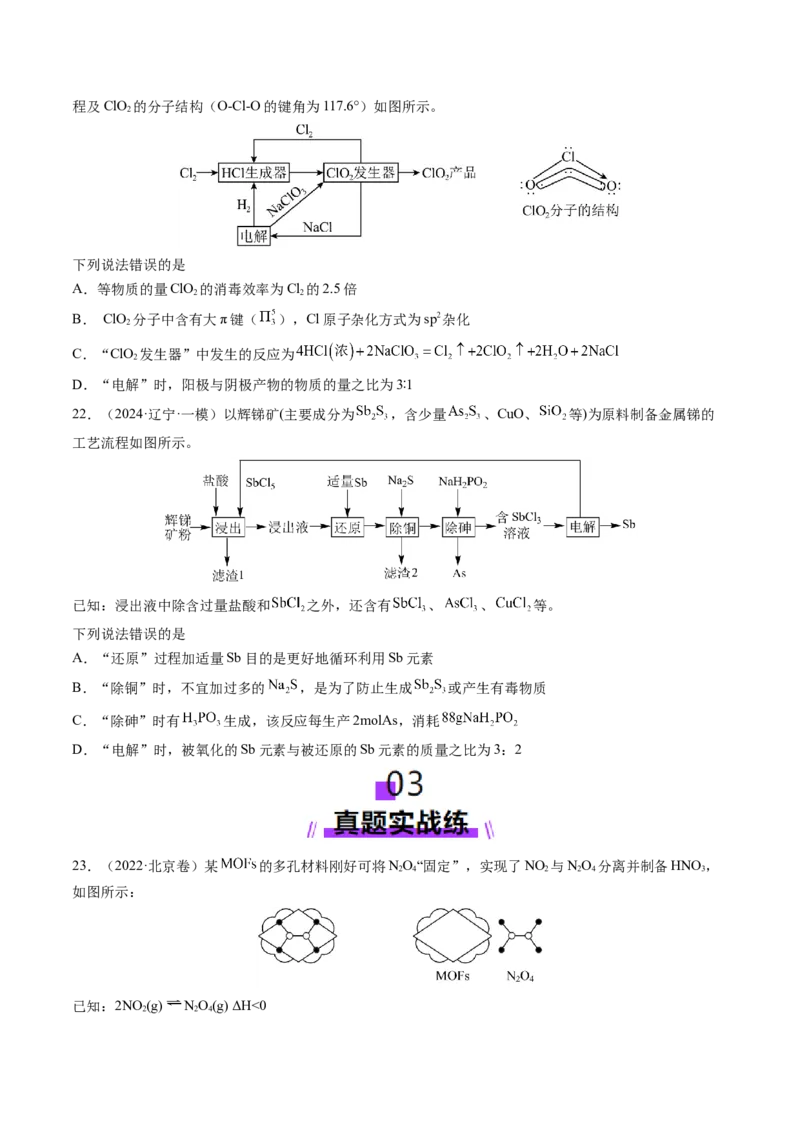
21.(2024·山东日照·三模)二氧化氯(ClO )是一种高效、安全的杀菌消毒剂。一种制备ClO 的工艺流
2 2程及ClO 的分子结构(O-Cl-O的键角为117.6°)如图所示。
2
下列说法错误的是
A.等物质的量ClO 的消毒效率为Cl 的2.5倍
2 2
B. ClO 分子中含有大π键( ),Cl原子杂化方式为sp2杂化
2
C.“ClO 发生器”中发生的反应为
2
D.“电解”时,阳极与阴极产物的物质的量之比为3∶1
22.(2024·辽宁·一模)以辉锑矿(主要成分为 ,含少量 、CuO、 等)为原料制备金属锑的
工艺流程如图所示。
已知:浸出液中除含过量盐酸和 之外,还含有 、 、 等。
下列说法错误的是
A.“还原”过程加适量Sb目的是更好地循环利用Sb元素
B.“除铜”时,不宜加过多的 ,是为了防止生成 或产生有毒物质
C.“除砷”时有 生成,该反应每生产2molAs,消耗
D.“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为3:2
23.(2022·北京卷)某 的多孔材料刚好可将NO“固定”,实现了NO 与NO 分离并制备HNO,
2 4 2 2 4 3
如图所示:
已知:2NO (g) NO(g) ΔH<0
2 2 4下列说法不正确的是
A.气体温度升高后,不利于NO 的固定
2 4
B.NO 被固定后,平衡正移,有利于NO 的去除
2 4 2
C.制备HNO 的原理为:2NO+O +2H O=4HNO
3 2 4 2 2 3
D.每制备0.4molHNO ,转移电子数约为
3
24.(2021·北京卷)用电石(主要成分为CaC ,含CaS和Ca P 等)制取乙炔时,常用CuSO 溶液除去乙
2 3 2 4
炔中的杂质。反应为:
①CuSO+H S=CuS↓+H SO
4 2 2 4
②11PH +24CuSO+12H O=3HPO +24H SO +8Cu P↓
3 4 2 3 4 2 4 3
下列分析不正确的是
A.CaS、Ca P 发生水解反应的化学方程式:CaS+2H O=Ca(OH) +H S↑、Ca P+6H O=3Ca(OH) +2PH↑
3 2 2 2 2 3 2 2 2 3
B.不能依据反应①比较硫酸与氢硫酸的酸性强弱
C.反应②中每24 mol CuSO 氧化11 mol PH
4 3
D.用酸性KMnO 溶液验证乙炔还原性时,HS、PH 有干扰
4 2 3
25.(2021·浙江卷)关于反应KHIO +9HI=2KI+4I +6H O,下列说法正确的是
2 3 6 2 2
A. KHIO 发生氧化反应 B.KI是还原产物
2 3 6
C.生成12.7g I 时,转移0.1mol电子 D.还原剂与氧化剂的物质的量之比为7:1
2
26.(2021·浙江卷)关于反应8NH +6NO=7N +12H O,下列说法正确的是
3 2 2 2
A.NH 中H元素被氧化
3
B.NO 在反应过程中失去电子
2
C.还原剂与氧化剂的物质的量之比为3:4
D.氧化产物与还原产物的质量之比为4:3
27.(2020·浙江卷) 是硅酸盐水泥的重要成分之一,其相关性质的说法不正确的是
A.可发生反应:
B.具有吸水性,需要密封保存
C.能与 ,反应生成新盐
D.与足量盐酸作用,所得固体产物主要为
28.(2022·江苏卷)用尿素水解生成的 催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,下列说法正确的是
A.上述反应
B.上述反应平衡常数
C.上述反应中消耗 ,转移电子的数目为
D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小29.(2022·浙江卷)关于反应 ,下列说法正确的是
A. 发生还原反应
B. 既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
30.(2020·浙江卷)反应 中,氧化产物与还原产物的物质的量
之比是
A.1:2 B.1:1 C.2:1 D.4:1