文档内容
第 12 讲 富集在海水中的元素——卤素
目录
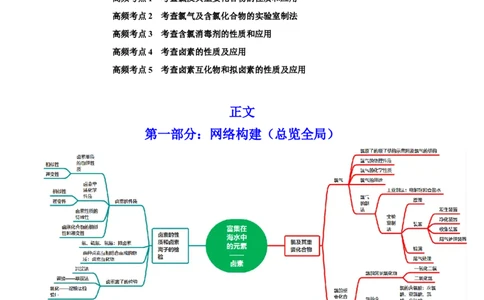
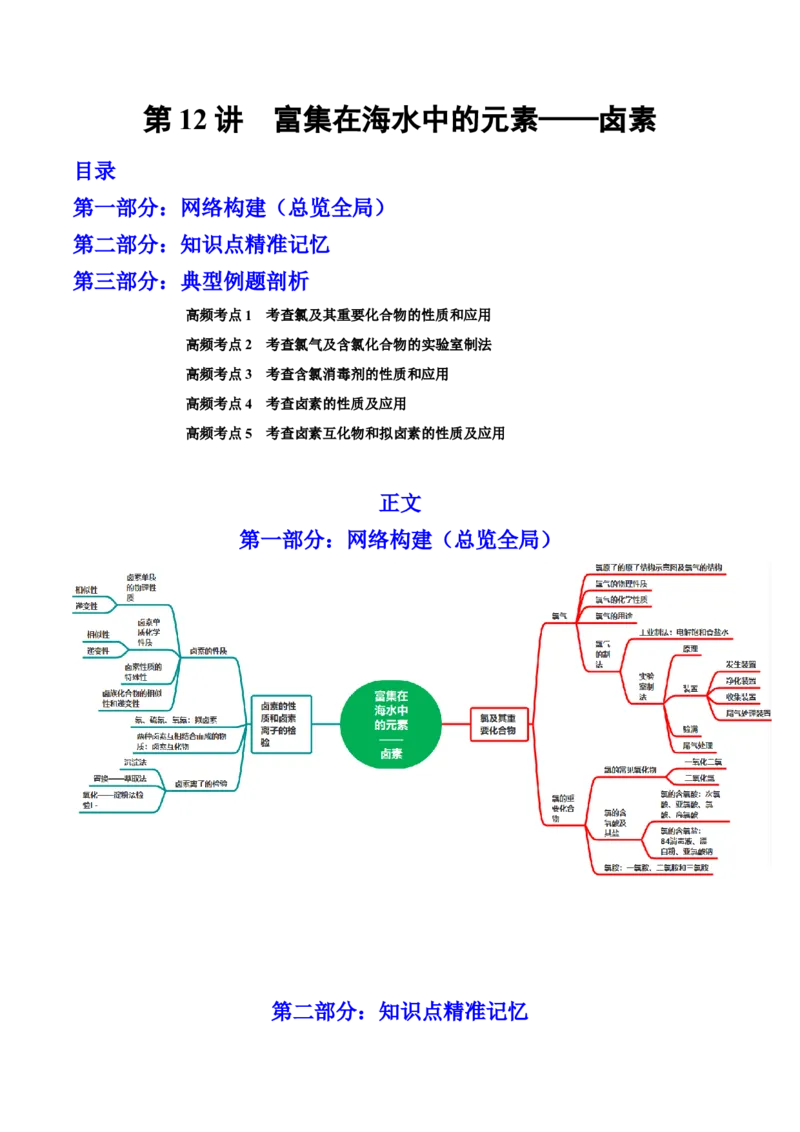
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
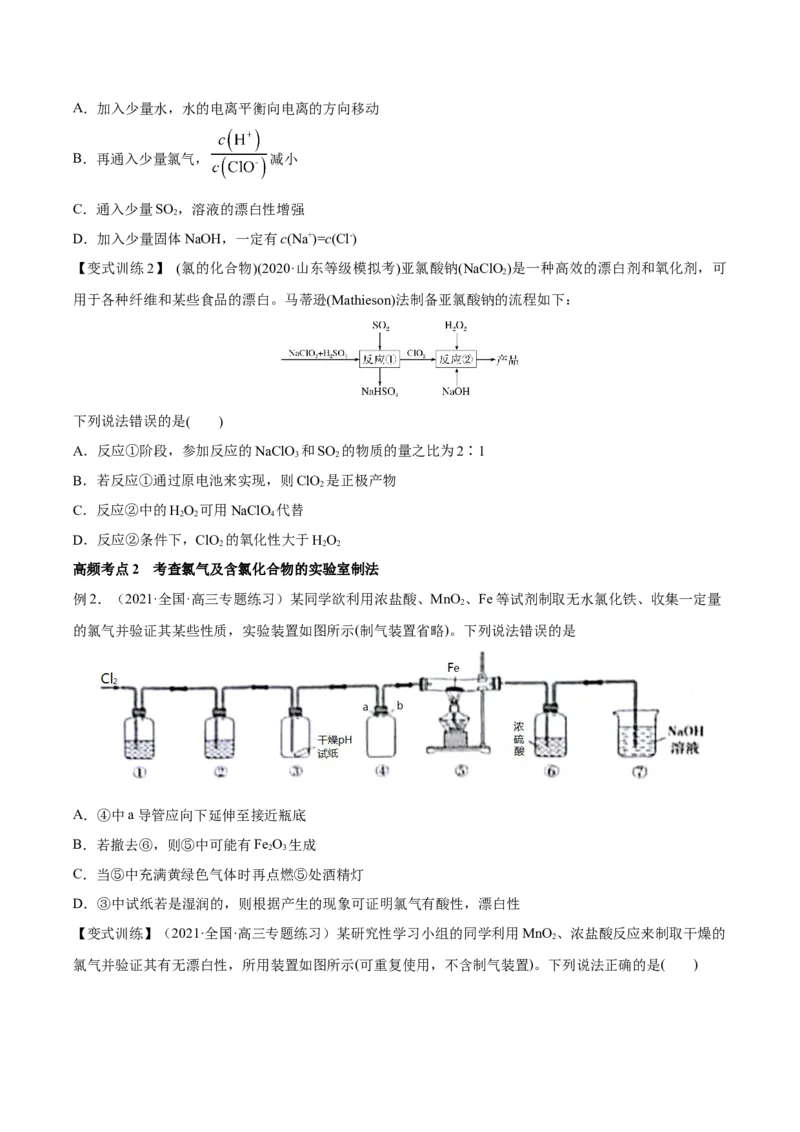
高频考点1 考查氯及其重要化合物的性质和应用
高频考点2 考查氯气及含氯化合物的实验室制法
高频考点3 考查含氯消毒剂的性质和应用
高频考点4 考查卤素的性质及应用
高频考点5 考查卤素互化物和拟卤素的性质及应用
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆知识点一 氯气及其重要化合物
(一)氯气
1.物理性质
颜色 状态 气味 密度 溶解性
1体积水溶
黄绿色 气体 刺激性 比空气大
解约2体积Cl
2
【特别提醒】实验室里闻有毒气体及未知气体气味的方法是:用手在瓶口轻轻扇动,仅使极少量气体飘进
鼻孔。
2.化学性质
1)从氯的原子结构认识氯气的氧化性:
依据氯气的氧化性完成下列方程式:
(1)与金属反应
①Fe:2Fe+3Cl=====2FeCl ,棕红色烟。
2 3
②Cu:Cu+Cl=====CuCl ,棕黄色烟。
2 2
(2)与非金属反应
H:H+Cl=====2HCl,苍白色火焰;
2 2 2
H 和Cl 的混合气体光照时会发生爆炸。
2 2
(3)与还原性无机化合物反应:
①与碘化钾溶液反应:Cl+2KI===2KCl+I。
2 2
②与SO 水溶液反应:Cl+SO +2HO===H SO +2HCl。
2 2 2 2 2 4
③与FeCl 溶液反应:Cl+2FeCl ===2FeCl 。
2 2 2 3
2)从化合价的角度认识Cl 的歧化反应
2
Cl 中氯元素化合价为0,为中间价态,可升可降,氯气与水或碱反应,氯的化合价既有升高又有降低,因
2
而氯气既表现氧化性又表现还原性。
(1)与水反应
化学方程式:Cl+HO HCl+HClO,
2 2
离子方程式:Cl+HO H++Cl-+HClO。
2 2
(2)与碱反应
①与烧碱反应:Cl+2NaOH===NaCl+NaClO+HO。
2 2②制取漂白粉:2Cl+2Ca(OH) ===CaCl +Ca(ClO) +2HO。
2 2 2 2 2
(3)从平衡的角度理解氯水的成分和性质
①氯气能溶于水(1∶2),氯气的水溶液称为氯水,溶于水的氯气只有少量与水反应,氯水中存在一个完全
电离和三个平衡:
HCl===H++Cl-
Cl+HO HCl+HClO
2 2
HClO H++ClO-
HO H++OH-
2
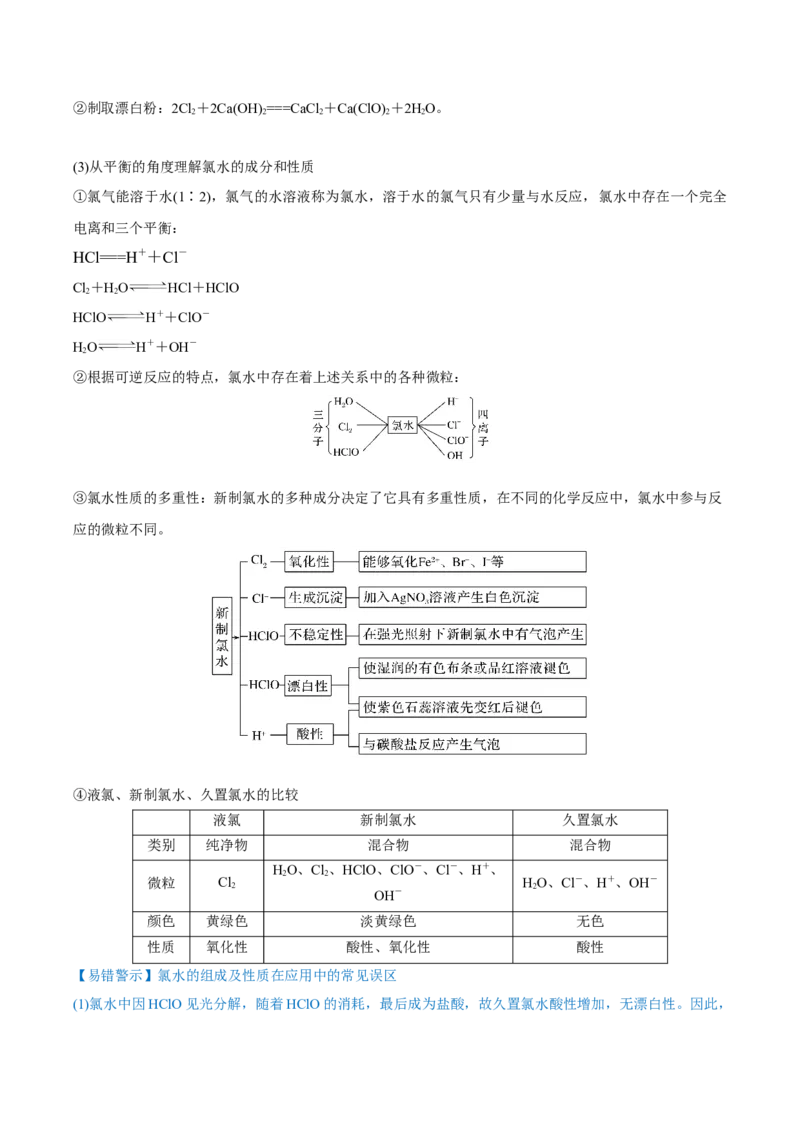
②根据可逆反应的特点,氯水中存在着上述关系中的各种微粒:
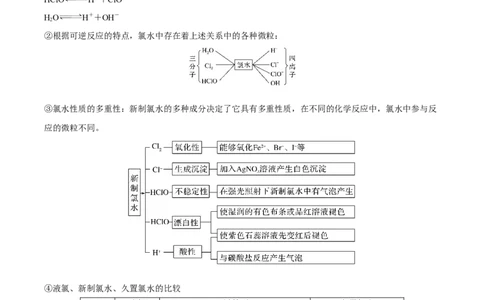
③氯水性质的多重性:新制氯水的多种成分决定了它具有多重性质,在不同的化学反应中,氯水中参与反
应的微粒不同。
④液氯、新制氯水、久置氯水的比较
液氯 新制氯水 久置氯水
类别 纯净物 混合物 混合物
HO、Cl、HClO、ClO-、Cl-、H+、
2 2
微粒 Cl HO、Cl-、H+、OH-
2 2
OH-
颜色 黄绿色 淡黄绿色 无色
性质 氧化性 酸性、氧化性 酸性
【易错警示】氯水的组成及性质在应用中的常见误区
(1)氯水中因HClO见光分解,随着HClO的消耗,最后成为盐酸,故久置氯水酸性增加,无漂白性。因此,氯水要现用现配。
(2)制取氯水的反应为Cl+HO HCl+HClO,反应中Cl 既是氧化剂,又是还原剂,且1 mol Cl 参加
2 2 2 2
反应,转移电子数为N 。
A
(3)Cl 尽管有较强的氧化性,但没有漂白性,氯水具有漂白性是因为Cl 与水反应生成了强氧化性的
2 2
HClO。
(4)ClO-与Fe2+、I-、S2-、HS-、SO等在水中因发生氧化还原反应而不能大量共存。
(二)氯的常见氧化物
1.一氧化二氯
①性质:次氯酸的酸酐,溶于水产生不稳定的次氯酸并最终变为盐酸。
②外观与性状:棕黄色气体,有刺激性气味。
③制法:用新制备的黄色氧化汞与氯气反应可制得一氧化二氯:
2HgO+2Cl===ClO+HgCl ·HgO;
2 2 2
也可以用氯气与潮湿的碳酸钠反应来制取:
2NaCO+HO+2Cl===2NaCl+2NaHCO +ClO。
2 3 2 2 3 2
2.二氧化氯
①物理性质:是一种黄绿色到橙黄色的气体,极易溶于水。
②制取:Cl+2NaClO===2ClO +2NaCl
2 2 2
或:5NaClO+4HCl===4ClO ↑+5NaCl+2HO。
2 2 2
③用途:是一种广谱、高效的灭菌剂。
(三)氯的含氧酸及其盐
1.氯的含氧酸
(1)氯的含氧酸的种类
HClO(次氯酸)、HClO(亚氯酸)、HClO(氯酸)、HClO(高氯酸)。
2 3 4
(2)氯的含氧酸的性质
酸性:HClO>HClO>HClO>HClO
4 3 2
氧化性:HClO>HClO>HClO>HClO。
2 3 4
(3)次氯酸
①不稳定性
次氯酸分解反应的化学方程式为2HClO=====2HCl+O↑,氯水要现用现配,且保存在棕色试剂瓶中,并
2
置于冷暗处。
②强氧化性
a.能将有机有色物质氧化为无色物质,作漂白剂。b.杀菌、消毒。
③弱酸性
向NaClO溶液中通入少量CO,离子方程式为ClO-+CO+HO===HCO -+HClO。
2 2 2 3
(4)亚氯酸
亚氯酸(HClO,英文名:chlorous acid)氧化性很强,比氯酸和高氯酸,氧化性HClO>HClO>HClO
2 2 3
>HClO。是目前所知唯一的亚卤酸。同时,它也是氯的含氧酸中最不稳定的。亚氯酸很不稳定,容易分
4
解,在几分钟之内便可生成Cl、ClO 和HO,8HClO=Cl+6ClO +4HO ,但生成的盐类——亚氯酸盐
2 2 2 2 2 2 2
相对稳定,亚氯酸钠是生产二氧化氯的原料之一
1)制备
①ClO 在水中分解:2ClO +HO=HClO+HClO
2 2 2 2 3
②通ClO 于NaO 或NaOH与HO 可得亚氯酸盐
2 2 2 2 2
2ClO +NaO=2NaClO +O;2ClO +HO+OH-=2ClO -+O +HO
2 2 2 2 2 2 2 2 2 2 2
③HClO 可由亚氯酸钡与稀硫酸的反应制备:Ba(ClO )+HSO =BaSO +2HClO
2 2 2 2 4 4 2
滤去硫酸钡沉淀即可得亚氯酸溶液。
2)性质与用途
①非常不稳定的化合物,但亚氯酸盐较稳定。
②具有漂白性(HClO,HClO,HClO 都有漂白性,一般用NaClO 加到水中从而生成HClO)
2 3 2 2
(5)氯酸
化学式HClO,仅存在于稀溶液中。水溶液在真空中可浓缩到质量百分浓度为40%,加热到40°C时
3
即分解爆炸:仅存在于稀溶液中。水溶液在真空中可浓缩到质量百分浓度为40%,加热到40°C时即分解
爆炸:26 HClO =10 HClO+15O+8Cl+8 H O,浓酸为浅黄色,有类似硝酸的刺激性气味;稀酸无色,在
3 4 2 2 2
常温时没有气味。有强烈氧化性,当与纸张、棉花等接触时就燃烧。氯酸是强酸,它的电离近似硝酸和盐
酸。当将稀的氯酸溶液剧烈冷却时,它将变得粘稠但不结晶。氯酸钡与硫酸作用后经过滤蒸馏而得氯酸。
其酸的重要盐类是钾盐和钠盐,氯酸钾不潮解,氯酸钠潮解。
(6)高氯酸
化学式HClO ,通常是无色 、极易吸湿的液体,在空气中强烈冒烟,熔点为-112°C,沸点为16°C
4
(2.4×103Pa)。无水高氯酸不稳定,储藏时有时会爆炸,因此应特别注意!但它的水溶液是稳定的。溅于
皮肤上会引起灼伤。高氯酸与水结合形成水合物HClO·nH O,式中n=1,2,2.5,3,3.5,皆为晶体。其
4 2
中最稳定的为1水合物,熔点为50°C,沸点为110°C,热到近沸点也不分解,它可写为[H O][ClO ]。在无
3 4
水的高氯酸中,显然有部分形成这种化合物:3HClO =[H O][ClO ]+ClO 七氧化二氯也易分解:2 Cl O
4 3 4 2 7 2 7
=4ClO +3O 这就是无水酸易爆炸的原因。高氯酸是普通含氧酸中的最强者,在水中完全电离。高氯酸的
2 2氧化力不如氯酸强,但在加热与高浓度时为强氧化剂,与有机物质发生猛烈作用。高氯酸根离子非常稳定,
它的结构是正四面体形,故较氯酸根离子(ClO ˉ)稳定的多。二氧化硫、硫化氢、亚硝酸、氢碘酸、锌、
3
铝等皆不能使它还原,氯酸却为这些还原剂还原。但低价钛、钒、钼等化合物可以使之还原,高氯酸根离
子还有一种特性,即对金属离子的配位作用很弱,所以在研究溶液的反应时,为保持溶液的离子强度不变,
常用它作稀释剂。高氯酸盐的溶解度有些异常,高氯酸的锂、钙、镁等盐在水中溶解度很高,而钾、铷、
铯的盐皆难溶于水。高氯酸镁、高氯酸钡的去水作用很强,故为优良的脱水剂。高氯酸铵分解放出大量氧
等气体,如:2NH ClO =N ↑+Cl↑+2O↑+4HO,它可作火箭推进剂,高氯酸可用于医药和电镀铅等方面。
4 4 2 2 2 2
高氯酸钾与浓硫酸在140~190°C的油浴上减压蒸馏可的高氯酸。
2.氯的含氧酸盐
1)“84”消毒液:有效成分为NaClO,它与洁厕灵(主要成分盐酸)混合立即会产生氯气,其离子方程式是
ClO-+Cl-+2H+===Cl↑+HO。
2 2
2)漂白粉
①成分:漂白粉的主要成分是CaCl 和Ca(ClO) ,其中有效成分是Ca(ClO) 。
2 2 2
②化学性质:水解呈碱性,具有强氧化性。
③漂白原理:在潮湿的空气中能吸收CO,化学方程式为Ca(ClO) +CO+HO===2HClO+CaCO ↓。
2 2 2 2 3
④久置失效原理:Ca(ClO) +CO+HO===2HClO+CaCO ↓;2HClO=====2HCl+O↑,必须密封保存。
2 2 2 3 2
3)NaClO(亚氯酸钠)
2
①性质:呈碱性,是一种强氧化剂,遇酸放出ClO 气体。
2
②用途:是一种高效氧化性漂白剂。主要用于棉纺、亚麻、纸浆漂白、食品消毒、水处理、杀菌灭藻和鱼
药制造。
(四)氯胺
1.氯胺的种类
氯胺是由氯气遇到氨气反应生成的一类化合物,主要包括一氯胺、二氯胺和三氯胺(NH Cl,NHCl
2 2
和NCl ),是常用的饮用水二级消毒剂。
3
2.氯胺的化合价:氯胺中氯为+1,N为-3,H为+1。
3.氯胺的消毒原理:氯胺在水中发生缓慢水解生成次氯酸,发挥消毒杀菌作用,水解方程式如下:
NH Cl+H O NH +HClO
2 2 3
NHCl +2H O NH +2HClO
2 2 3
NCl +3H O NH +3HClO
3 2 3
【特别提醒】①向Ca(ClO) 溶液中通入少量CO,发生的反应为Ca2++2ClO-+CO+HO===CaCO↓+
2 2 2 2 3
2HClO。②向Ca(ClO) 溶液中通入SO ,生成的是CaSO 而不是CaSO。
2 2 4 3
③次氯酸盐(ClO-)无论是在酸性、碱性还是中性条件下,均具有强氧化性,均能氧化I-、Fe2+、SO、S2-
等还原性离子。
④84消毒液(主要成分NaClO)和洁厕灵(主要成分HCl)不能混合使用,否则会产生有毒气体——氯气。
⑤氯气没有漂白性,不能使干燥的有色布条褪色,但可使湿润的有色布条褪色,起漂白作用的是HClO。
⑥常温下干燥的氯气或液氯均不与铁反应,故液氯通常储存在钢瓶中。
知识点二 氯气的制法
(一)氯气的实验室制法
1.制取原理
实验室通常用强氧化剂MnO 、KMnO 、KCr O、KClO、Ca(ClO) 等氧化浓盐酸制取氯气。
2 4 2 2 7 3 2
(1)用MnO 制取Cl 的化学方程式:MnO +4HCl(浓)=====MnCl +Cl↑+2HO。
2 2 2 2 2 2
(2)其他制备Cl 的化学反应原理(特点:不需要加热)
2
①14HCl(浓)+KCr O===2KCl+2CrCl +7HO+3Cl↑
2 2 7 3 2 2
②16HCl(浓)+2KMnO ===2KCl+2MnCl +8HO+5Cl↑
4 2 2 2
③6HCl(浓)+KClO===KCl+3HO+3Cl↑
3 2 2
④4HCl(浓)+Ca(ClO) ===CaCl +2Cl↑+2HO
2 2 2 2
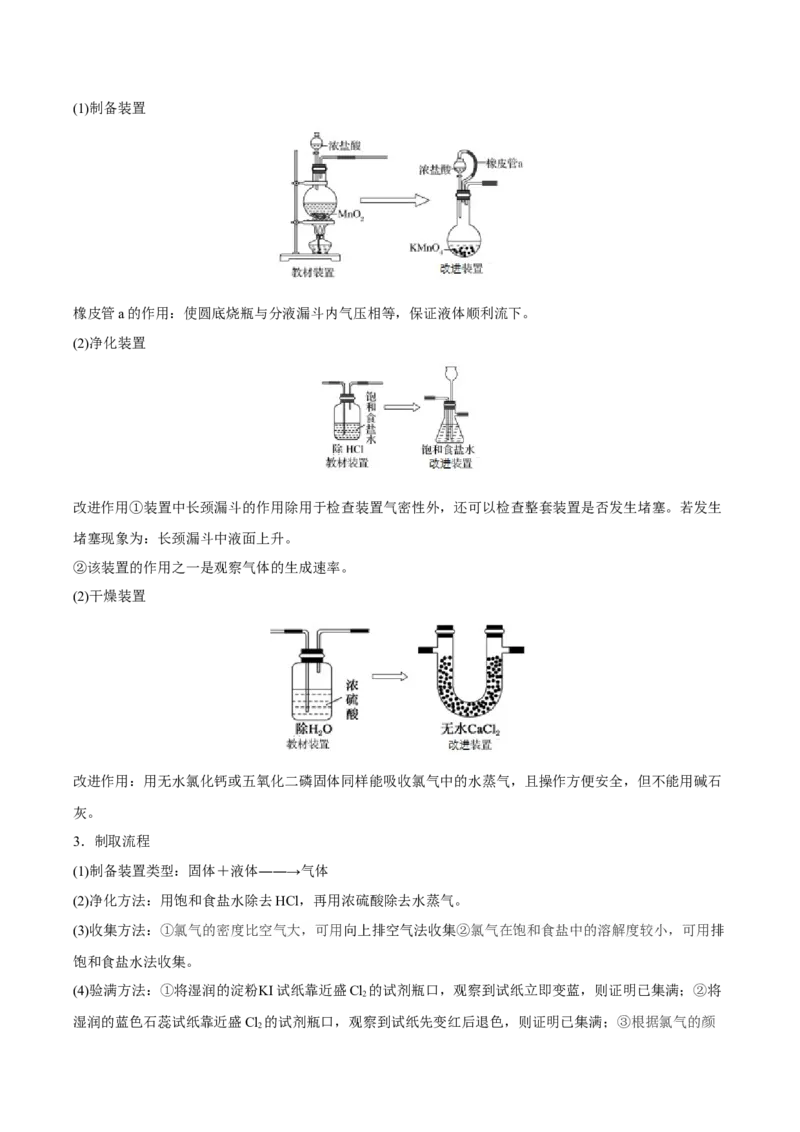
2.实验装置
注:实验装置改进(1)制备装置
橡皮管a的作用:使圆底烧瓶与分液漏斗内气压相等,保证液体顺利流下。
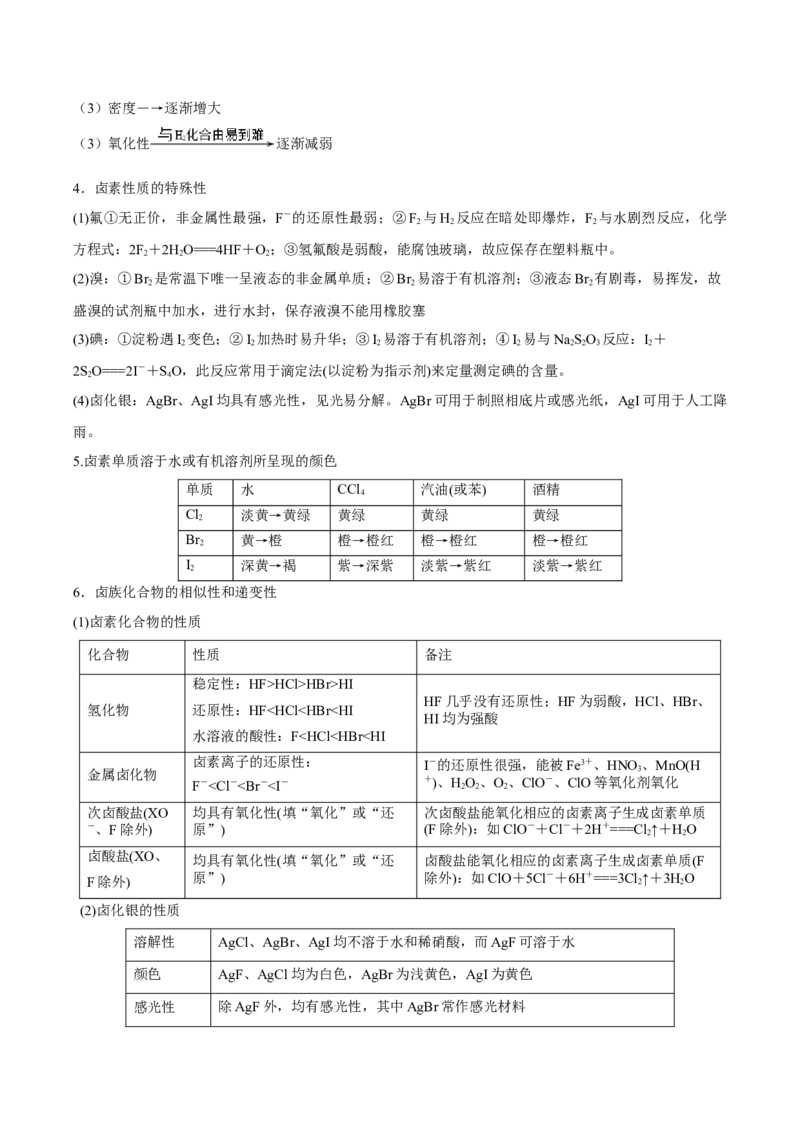
(2)净化装置
改进作用①装置中长颈漏斗的作用除用于检查装置气密性外,还可以检查整套装置是否发生堵塞。若发生
堵塞现象为:长颈漏斗中液面上升。
②该装置的作用之一是观察气体的生成速率。
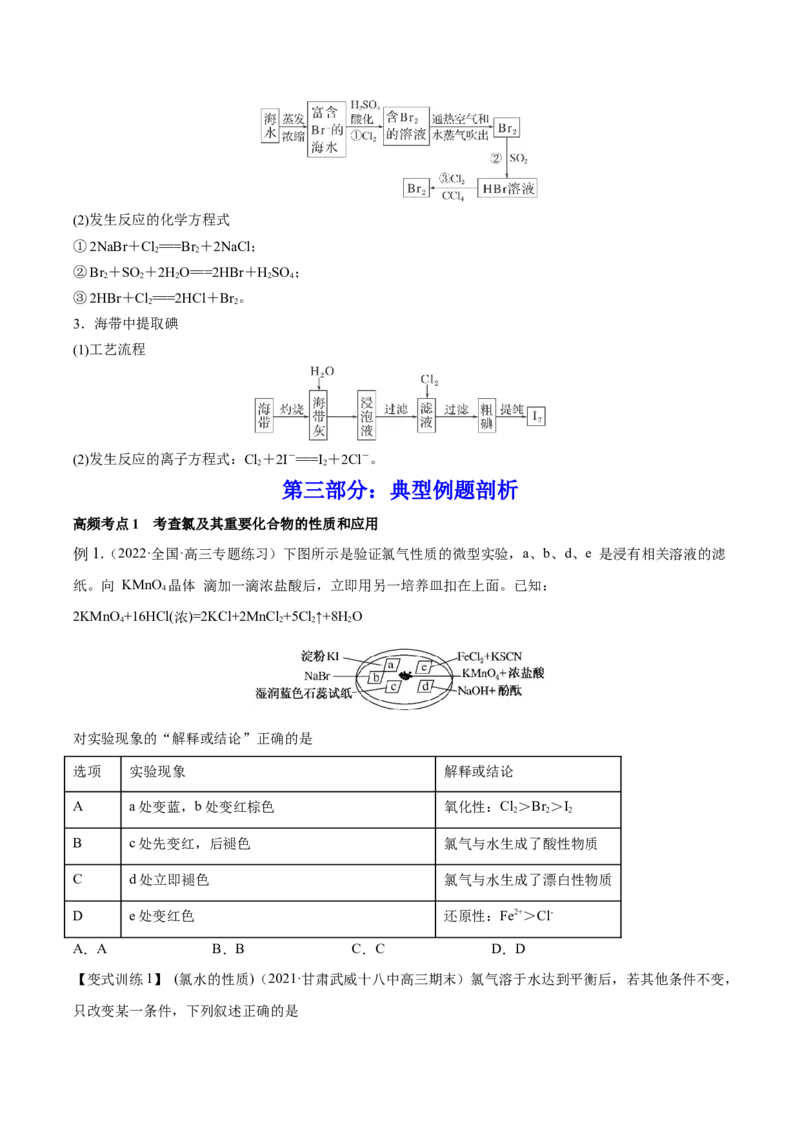
(2)干燥装置
改进作用:用无水氯化钙或五氧化二磷固体同样能吸收氯气中的水蒸气,且操作方便安全,但不能用碱石
灰。
3.制取流程
(1)制备装置类型:固体+液体――→气体
(2)净化方法:用饱和食盐水除去HCl,再用浓硫酸除去水蒸气。
(3)收集方法:①氯气的密度比空气大,可用向上排空气法收集②氯气在饱和食盐中的溶解度较小,可用排
饱和食盐水法收集。
(4)验满方法:①将湿润的淀粉KI试纸靠近盛Cl 的试剂瓶口,观察到试纸立即变蓝,则证明已集满;②将
2
湿润的蓝色石蕊试纸靠近盛Cl 的试剂瓶口,观察到试纸先变红后退色,则证明已集满;③根据氯气的颜
2色,装置充满了黄绿色气体,则证明已集满。
(5)尾气吸收:用强碱溶液(如NaOH溶液)吸收,不用Ca(OH) 溶液吸收的原因是Ca(OH) 溶解度小,溶液
2 2
浓度低,吸收不完全。
【特别提醒】实验室制取氯气的注意事项
(1)反应物的选择:必须用浓盐酸,稀盐酸与MnO 不反应,且随着反应的进行,浓盐酸变为稀盐酸时,反
2
应停止,故盐酸中的HCl不可能全部参加反应。
(2)加热温度:不宜过高,以减少HCl挥发。
(3)实验结束后,先使反应停止并排出残留的Cl 后,再拆卸装置,避免污染空气。
2
(4)尾气吸收时,用NaOH溶液吸收Cl ,不能用澄清石灰水吸收,因为澄清石灰水中含Ca(OH) 的量少,
2 2
吸收不完全。
(二)工业制法
电解饱和食盐水,反应的化学方程式为2NaCl+2HO=====2NaOH+Cl↑+H↑。
2 2 2
知识点三 卤素的性质和卤素离子的检验
(一)卤素的性质
1.溴、碘单质的物理性质
性质 Br I
2 2
颜色 深红棕色 紫黑色
状态 液体 固体
溶解性及 水中 溶解度不大,橙色 溶解度不大,黄色
溶液颜色
有机溶剂中 易溶,橙红色 易溶,紫红色
①易升华
特性 易挥发、有毒
②使淀粉溶液变蓝
2.卤素单质化学性质的相似性
(1)都能与大多数金属反应,如溴与铁反应生成FeBr ,但I 与Fe反应生成FeI。
3 2 2
(2)都能与H 反应生成HX(X代表F、Cl、Br、I)。
2
(3)都能与水反应:X+HOHX+HXO(X代表Cl、Br、I)。
2 2
(4)都能与碱溶液反应。
3.卤素单质性质的递变性
(1)颜色 逐渐加深
(2)熔、沸点 逐渐升高(3)密度―→逐渐增大
(3)氧化性 逐渐减弱
4.卤素性质的特殊性
(1)氟①无正价,非金属性最强,F-的还原性最弱;②F 与H 反应在暗处即爆炸,F 与水剧烈反应,化学
2 2 2
方程式:2F+2HO===4HF+O;③氢氟酸是弱酸,能腐蚀玻璃,故应保存在塑料瓶中。
2 2 2
(2)溴:①Br 是常温下唯一呈液态的非金属单质;②Br 易溶于有机溶剂;③液态Br 有剧毒,易挥发,故
2 2 2
盛溴的试剂瓶中加水,进行水封,保存液溴不能用橡胶塞
(3)碘:①淀粉遇I 变色;②I 加热时易升华;③I 易溶于有机溶剂;④I 易与NaSO 反应:I+
2 2 2 2 2 2 3 2
2SO===2I-+SO,此反应常用于滴定法(以淀粉为指示剂)来定量测定碘的含量。
2 4
(4)卤化银:AgBr、AgI均具有感光性,见光易分解。AgBr可用于制照相底片或感光纸,AgI可用于人工降
雨。
5.卤素单质溶于水或有机溶剂所呈现的颜色
单质 水 CCl 汽油(或苯) 酒精
4
Cl 淡黄→黄绿 黄绿 黄绿 黄绿
2
Br 黄→橙 橙→橙红 橙→橙红 橙→橙红
2
I 深黄→褐 紫→深紫 淡紫→紫红 淡紫→紫红
2
6.卤族化合物的相似性和递变性
(1)卤素化合物的性质
化合物 性质 备注
稳定性:HF>HCl>HBr>HI
HF几乎没有还原性;HF为弱酸,HCl、HBr、
氢化物 还原性:HFBr >I
2 2 2
【变式训练1】(卤素的性质及递变规律)(2021·上海宝山·一模)卤族元素大多存在于海洋中,关于
Cl、Br、I 的说法正确的是
A.原子半径 r:r(Cl)< r(Br)< r(I) B.非金属性:Cl<Br<I
C.从海洋中提取的方法:相同 D.得电子能力:Cl<Br <I
2 2 2
【变式训练2】(卤素单质氧化性的实验探究)(2021·全国·高三专题练习)证明卤族元素的非金属性强
弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检查)。实验过程:Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ. 打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。
下列说法错误的是
A.淀粉碘化钾试纸变蓝可验证氯气的氧化性强于碘。
B.B中发生反应的离子方程式是Cl+2Br-= Br+2Cl-。
2 2
C.Ⅳ中的实验现象是四氯化碳层溶液变为橙红色。
D.过程Ⅲ实验的目的是确认C的黄色溶液中无氯气,排除氯气对溴置换碘实验的干扰
高频考点5 考查卤素互化物和拟卤素的性质及应用
例5.(2021·天津天津·高三期中)“ ”表示不同卤素之间靠共用电子对形成的卤素互化物(非金属性:
),其化学性质和卤素单质相似。下列说法中正确的是
A.ICl与水反应属于氧化还原反应
B.某温度下,液态 电离: , 是一个常数,与温度无关
C. 与卤素单质一样都是非极性分子
D. 与 反应生成 和
【变式训练】(拟卤素)(2022·湖南·涟源市第一中学高三阶段练习)(SCN) 称为拟卤素,将几滴KSCN
2
溶液加入酸性的含有Fe3+的溶液中,溶液变为红色,将该红色溶液分为两份:①向其中一份溶液中加入适
量KMnO 溶液,红色褪去;②向另一份溶液中通入SO ,红色也褪去。下列说法中不正确的是
4 2
A.Fe3+与SCN-反应的离子方程式为Fe3++3SCN- Fe(SCN)
3
B.②中红色褪去的原因是SO 2 具有漂白性 ⇌
C.①中现象说明SCN-与Cl-相似,有还原性
D.SCN-在适当条件下可被氧化剂氧化为(SCN)
2