文档内容
第 14 讲 元素周期律和元素周期表
【学科核心素养】
1.宏观辨识与微观探析:能从不同层次认识物质的多样性;能从元素和原子,分子水平认识物质的组
成、结构和性质,形成“结构决定性质”的观念;能从宏观和微观相结合的视角分析元素周期律的递变性。
2.证据推理与模型认知:具有证据意识,能基于实验现象和事实对物质的组成、结构及其变化分析得
出元素周期律;能基于元素周期律理解元素周期表的编排方法,能运用元素周期表揭示元素周期律。
3.科学探究与创新意识:在探究同周期、同主族元素性质递变性的实验中,要明确探究目的,设计实
验方案,并在探究中学会合作,结合核外电子排布,元素第一电离能的特殊性等异常现象提出自己的见解。
【核心素养发展目标】
1.掌握元素周期律的实质;了解元素周期表(长式)的结构(周期、族)及其应用.
2.以第三周期为例,掌握同一周期内元素性质的递变规律与原子结构的关系.
3.以ⅠA和ⅦA族为例,掌握同一主族内元素性质递变规律与原子结构的关系.
4.了解金属、非金属元素在周期表中的位置及其性质递变规律.
【知识点解读】
知识点一 元素周期表及其应用
1.原子序数
按照元素在周期表中的顺序给元素所编的序号。
原子序数=核电荷数=核外电子数=质子数。
2.元素周期表的编排原则
(1)把电子层数相同的元素按原子序数递增顺序从左到右排成一横行,共有7个横行。
(2)把不同横行中最外层电子数相同的元素按电子层数递增的顺序从上到下排成一纵行,共有18纵行。
3.元素周期表的结构
(1)周期(7个横行,7个周期)
短周期 长周期
序号 一 二 三 四 五 六 七
元素种类 2 8 8 18 18 32 32
0族元素
2 10 18 36 54 86 118
原子序数(2)族(18个纵行,16个族)
列 1 2 13 14 15 16 17
主族
族 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
列 3 4 5 6 7 11 12
副族
族 ⅢB ⅣB ⅤB ⅥB ⅦB ⅠB ⅡB
Ⅷ族 第8、9、10,共3个纵行
0族 第18纵行
【特别提醒】
①含元素种类最多的族是第ⅢB族,共有32种元素。
②过渡元素包括7个副族和第Ⅷ族,全部是金属元素,原子最外层电子数不超过2个(1~2个)。
③最外层电子数为3~7个的原子一定属于主族元素,且最外层电子数即为主族的族序数。
(3)元素周期表中元素的分区
①分界线:如图所示,沿着元素周期表中铝、锗、锑、钋与硼、硅、砷、碲、砹的交界处画一条斜线,
即为金属元素区和非金属元素区分界线(氢元素除外)。
②各区位置:分界线左下方为金属元素区,分界线右上方为非金属元素区。
③分界线附近元素的性质:既表现金属元素的性质,又表现非金属元素的性质。
(4)元素周期表中的特殊位置
过渡 元素周期表中从第ⅢB族到第ⅡB族10个纵列共60多种元素,这些元素都是
元素 金属元素
镧系 元素周期表第六周期中,57号元素镧到71号元素镥共15种元素
锕系 元素周期表第七周期中,89号元素锕到103号元素铹共15种元素
超铀
在锕系元素中,92号元素铀(U)以后的各种元素
元素
4.元素周期表的三大应用
(1)科学预测
为新元素的发现及预测他们的原子结构和性质提供了线索。
(2)寻找新材料(3)用于工农业生产
对探矿有指导意义的是地球化学元素的分布与它们在元素周期表中的位置关系,研制农药材料等。
知识点二 元素周期律及其应用
1.元素周期律
(1)元素的性质随着原子序数的递增而呈周期性变化的规律。
(2)元素周期律的实质是元素原子核外电子排布的周期性变化的结果。
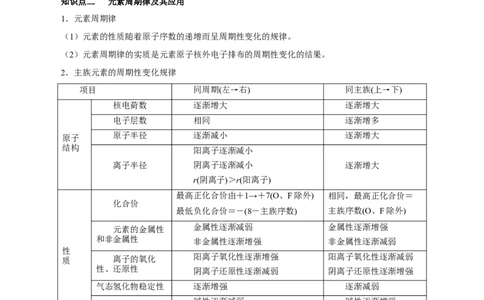
2.主族元素的周期性变化规律
项目 同周期(左→右) 同主族(上→下)
核电荷数 逐渐增大 逐渐增大
电子层数 相同 逐渐增多
原子半径 逐渐减小 逐渐增大
原子
结构
阳离子逐渐减小
离子半径 阴离子逐渐减小 逐渐增大
r(阴离子)>r(阳离子)
最高正化合价由+1→+7(O、F除外) 相同,最高正化合价=
化合价
最低负化合价=-(8-主族序数) 主族序数(O、F除外)
元素的金属性 金属性逐渐减弱 金属性逐渐增强
和非金属性 非金属性逐渐增强 非金属性逐渐减弱
性
质 离子的氧化 阳离子氧化性逐渐增强 阳离子氧化性逐渐减弱
性、还原性 阴离子还原性逐渐减弱 阴离子还原性逐渐增强
气态氢化物稳定性 逐渐增强 逐渐减弱
最高价氧化物对应 碱性逐渐减弱 碱性逐渐增强
的水化物的酸碱性 酸性逐渐增强 酸性逐渐减弱
3.元素周期律的两大应用
(1)比较不同周期、不同主族元素的性质
①比较Ca(OH) 和Al(OH) 的碱性强弱方法:
2 3
金属性:Mg>Al,Ca>Mg,则碱性:Ca(OH) >Mg(OH) >Al(OH) 。
2 2 3
②比较HO和SiH 的稳定性强弱的方法:
2 4
非金属性:C>Si,O>C,则氢化物稳定性:HO>CH>SiH 。
2 4 4(2)预测未知元素的某些性质
①已知Ca(OH) 微溶,Mg(OH) 难溶,可推知Be(OH) 难溶。
2 2 2
②已知卤族元素的性质递变规律,可推知未学元素砹(At)的化合物的性质为HAt不稳定,水溶液呈酸
性,AgAt难溶于水。
【典例剖析】
高频考点一 元素周期表的结构及应用
例1. (2020·浙江卷)X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元素的最高正价为
+4价,Y元素与Z、M元素相邻,且与M元素同主族;化合物 的电子总数为18个;Q元素的原子
最外层电子数比次外层少一个电子。下列说法不正确的是( )
A. 原子半径:
B. 最高价氧化物对应水化物的酸性:
C. 易溶于水,其水溶液呈碱性
D. X、Z和Q三种元素形成的化合物一定是共价化合物
【答案】D
【解析】X、Y、Z、M、Q为五种短周期元素,原子序数依次增大。Y元素的最高正价为+4价,则证
明该元素为第IVA族元素,又知Y元素与Z、M元素相邻,且与M同族,则在元素周期表位置应为
IVA族 VA族
Y Z
M
,故推知Y为C元素,Z为N元素,M为Si元素;化合物ZX 的电子总数为18,则推知,X为H,
2 4
该化合物为NH;Q元素的原子最外层电子总数比次外层电子数少一个电子,推出Q为Cl元素,据此结
2 4
合元素周期律与物质的结构与性质分析作答。根据上述分析可知,X为H、Y为C元素、Z为N元素、M
为Si元素、Q为Cl元素,则同周期元素从左到右原子半径依次减小,同主族元素从上到下原子半径依次
增大,则原子半径比较:Z(N) X>Y> Z B. 原子半径:Z>Y>X>W
C. 元素X的含氧酸均为强酸 D. Y的氧化物水化物为强碱
【答案】D
【解析】根据题干信息可知,W、X、Y、Z为原子序数依次增大的短周期元素,化合物XW 与WZ相
3
遇会产生白烟,则WX 为NH ,WZ为HCl,所以W为H元素,X为N元素,Z为Cl元素,又四种元素
3 3
的核外电子总数满足X+Y=W+Z,则Y的核外电子总数为11,Y为Na元素,据此分析解答。根据上述分
析可知,W为H元素,X为N元素,Y为Na元素,Z为Cl元素,则Na为金属元素,非金属性最弱,非
金属性Y<Z,A选项错误;同周期元素从左至右原子半径依次减小,同主族元素至上而下原子半径依次
增大,则原子半径:Na>Cl>N>H,B选项错误;N元素的含氧酸不一定全是强酸,如HNO 为弱酸,C
2
错误;Y的氧化物水化物为NaOH,属于强碱,D正确。
【方法技巧】金属性、非金属性强弱的判断方法
本质 原子越易失电子,金属性越强(与原子失电子数目无关)
①在金属活动性顺序表中越靠前,金属性越强
②单质与水或非氧化性酸反应越剧烈,金属性越强
金属性
判断 ③单质还原性越强或阳离子氧化性越弱,金属性越强
比较
方法 ④最高价氧化物对应水化物的碱性越强,金属性越强
⑤若Xn++Y―→X+Ym+,则Y比X的金属性强
⑥元素在周期表中的位置:左边或下方元素的金属性强
非金属 本质 原子越易得电子,非金属性越强(与原子得电子数目无关)①与H 化合越容易,气态氢化物越稳定,非金属性越强
2
判断 ②单质氧化性越强或阴离子还原性越弱,非金属性越强
性比较
方法 ③最高价氧化物对应水化物的酸性越强,非金属性越强
④元素在周期表中的位置:右边或上方元素的非金属性强
【特别提醒】
①通常根据最高价氧化物对应水化物的酸碱性的强弱判断元素金属性或非金属性的强弱,而不是根据
其他化合物酸碱性的强弱来判断。
②非金属性强弱与单质的活泼性不完全一致;通常非金属性越强,其单质越活泼,但也有例外。如非
金属性:O>Cl,但Cl 比O 活泼,原因是O 中存在O双键,比Cl—Cl单键难断裂。
2 2 2
【变式探究】 [2019新课标Ⅰ]科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同
一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是
A.WZ的水溶液呈碱性
B.元素非金属性的顺序为X>Y>Z
C.Y的最高价氧化物的水化物是中强酸
D.该新化合物中Y不满足8电子稳定结构
【答案】C
【解析】氯化钠为强酸强碱盐,水溶液呈中性,A错误;同周期元素从左到右,非金属性依
次增强,则非金属性的强弱顺序为Cl>S>P,B错误;P元素的最高价氧化物对应水化物为磷酸,
磷酸是三元中强酸,C正确;新化合物中P元素化合价为−3价,满足8电子稳定结构,故D错误。
【变式探究】下列关于元素金属性和非金属性强弱比较的说法不正确的是( )
A.将大理石加入稀盐酸中,能产生CO 气体,说明Cl的非金属性强于C
2
B.Si与H 化合所需温度远高于S与H 化合所需温度,说明S的非金属性强于Si
2 2
C.Na与冷水反应剧烈,而Mg与冷水反应缓慢,说明Na的金属性强于Mg
D.Fe投入CuSO 溶液中,能置换出Cu,说明Fe的金属性比Cu的强
4
【答案】A
【解析】盐酸中的溶质HCl不是氯元素的最高价氧化物对应的水化物,虽然HCl的酸性比碳酸的强,
但不能作为Cl、C非金属性强弱的判断依据,A错误;单质与H 越易化合,元素的非金属性越强,B正确;
2
单质与水越易反应生成碱和H ,其金属性越强,C正确;较活泼的金属单质可将较不活泼的金属从它的盐
2
溶液中置换出来,D正确。高频考点四 粒子半径的大小比较
例4. (2020·江苏,9)海水晒盐后精制得到NaCl,氯碱工业电解饱和NaCl溶液得到Cl 和NaOH,以
2
NaCl、NH 、CO 等为原料可得到 NaHCO ;向海水晒盐得到的卤水中通Cl 可制溴;从海水中还能提取镁。
3 2 3 2
下列关于Na、Mg、Cl、Br元素及其化合物的说法正确的是( )
A.NaOH的碱性比Mg(OH) 的强
2
B.Cl 得到电子的能力比Br 的弱
2 2
C.原子半径r:r(Br)>r(Cl)>r(Mg)>r(Na)
D.原子的最外层电子数n:n(Na)<n(Mg)<n(Cl)<n(Br)
【答案】A
【解析】金属性:Na>Mg,故碱性:NaOH>Mg(OH) ,A项正确;氯和溴均属于卤族元素,同一主
2
族元素从上到下,单质的氧化性逐渐减弱,得电子能力:Cl>Br ,B项错误;同一周期主族元素,从左到
2 2
右原子半径依次减小,则r(Br)>r(Na)>r(Mg)>r(Cl),C项错误;氯和溴属于同一主族,最外层电子数相等,
D项错误。
【方法技巧】粒子半径大小的比较方法
【变式探究】已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则下列叙述中
正确的是( )
A.原子序数:D>C>B>A
B.原子半径:B>A>C>DC.离子半径:C3->D->A2+>B+
D.氧化性:A2+>B+,还原性:C3-B,C、D在上一周期,为非金属元素,且原子序数D>C。由电子层数越多的原子序数越大,同周期从
左向右原子序数增大,所以原子序数为A>B>D>C,故A错误;电子层越多,半径越大,同周期原子序数
越大,半径越小,则原子半径为B>A>C>D,故B正确;具有相同电子层结构的离子,原子序数大的离子
半径小,原子序数为A>B>D>C,则离子半径为C3->D->B+>A2+,故C错误;金属性越强,其阳离子的氧
化性越弱,金属性为B>A,则氧化性:A2+>B+,非金属性:CD-,故D错误。
高频考点五 根据元素周期律预测元素的性质
例5.[2019浙江4月选考] 2019年是门捷列夫提出元素周期表150周年。根据元素周期律和元素周期表,
下列推断不合理的是
A.第35号元素的单质在常温常压下是液体
B.位于第四周期第ⅤA族的元素为非金属元素
C.第84号元素的最高化合价是+7
D.第七周期0族元素的原子序数为118
【答案】C
【解析】35号元素是溴元素,单质Br 在常温常压下是红棕色的液体,A项合理;位于第四周期第
2
ⅤA族的元素是砷元素(As),为非金属元素,B项合理;第84号元素位于第六周期ⅥA族,为钋元素
(Po),由于最高正价等于主族序数,所以该元素最高化合价是+6,C项不合理;第七周期0族元素是第
七周期最后一个元素,原子序数为118,D项合理。
【方法技巧】依据周期律预测元素性质的流程
对于同一主族的陌生元素,首先确定它在元素周期表中的位置,然后确定它是金属元素还是非金属元
素,再根据同族元素性质的相似性、递变性及同周期元素的性质变化规律(元素周期律),来推测该元素及
其化合物的性质。如已知卤族元素的性质递变规律,可推知元素砹(At)的单质应为有色固体,与H 难化合,
2
HAt不稳定,HAt水溶液呈酸性,AgAt不溶于水等。
【变式探究】(2020·湖北省武汉模拟)应用元素周期律分析下列推断,其中正确的是( )
A.铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
B.气态氢化物的稳定性HF低于HCl
C.硒(Se)位于元素周期表第ⅥA族,其最高价氧化物对应水化物的酸性比硫酸弱
D.第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性【答案】C
【解析】在元素周期表中,铊位于铝的下面,其金属性比铝的金属性强,不与碱反应,A项错误;氟
的非金属性比氯强,气态氢化物稳定性HF较强,B项错误;NH 的水溶液呈碱性,D项错误。
3
高频考点六 位、构、性关系的综合推断
例6.[2019新课标Ⅱ] 今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、
X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是
A.原子半径:W