文档内容
第 16 讲 原电池
【练基础】
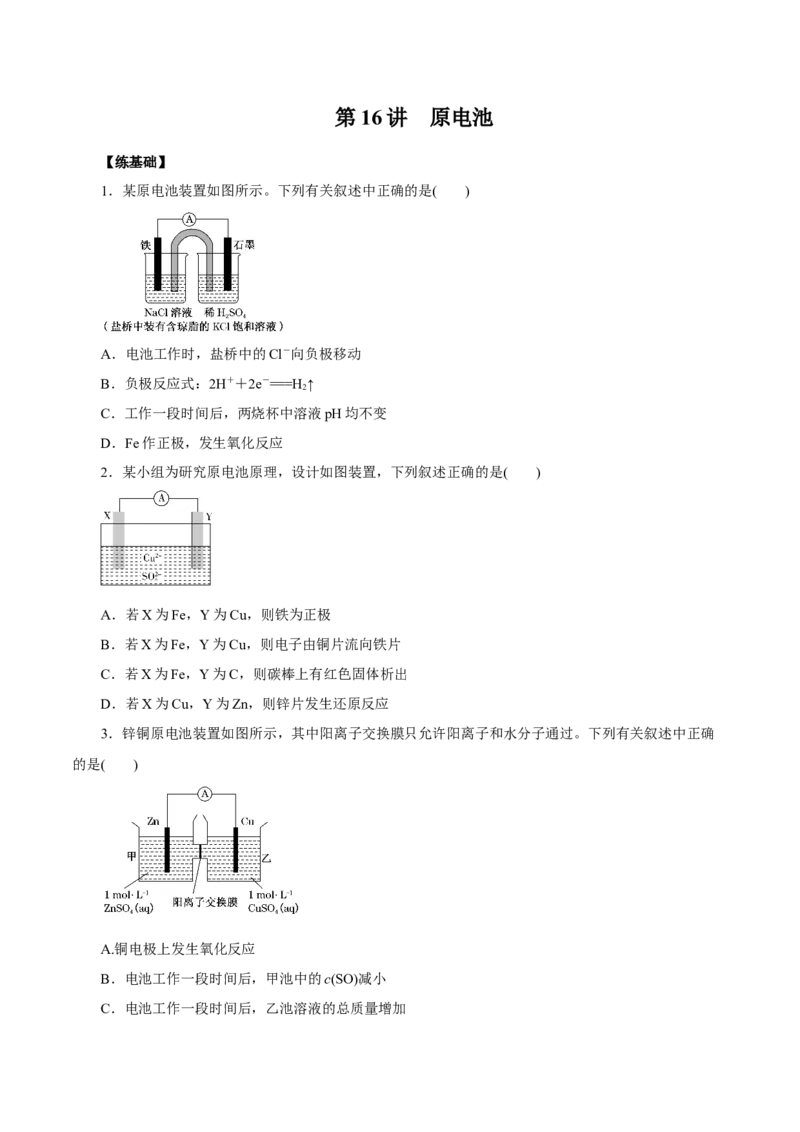
1.某原电池装置如图所示。下列有关叙述中正确的是( )
A.电池工作时,盐桥中的Cl-向负极移动
B.负极反应式:2H++2e-===H ↑
2
C.工作一段时间后,两烧杯中溶液pH均不变
D.Fe作正极,发生氧化反应
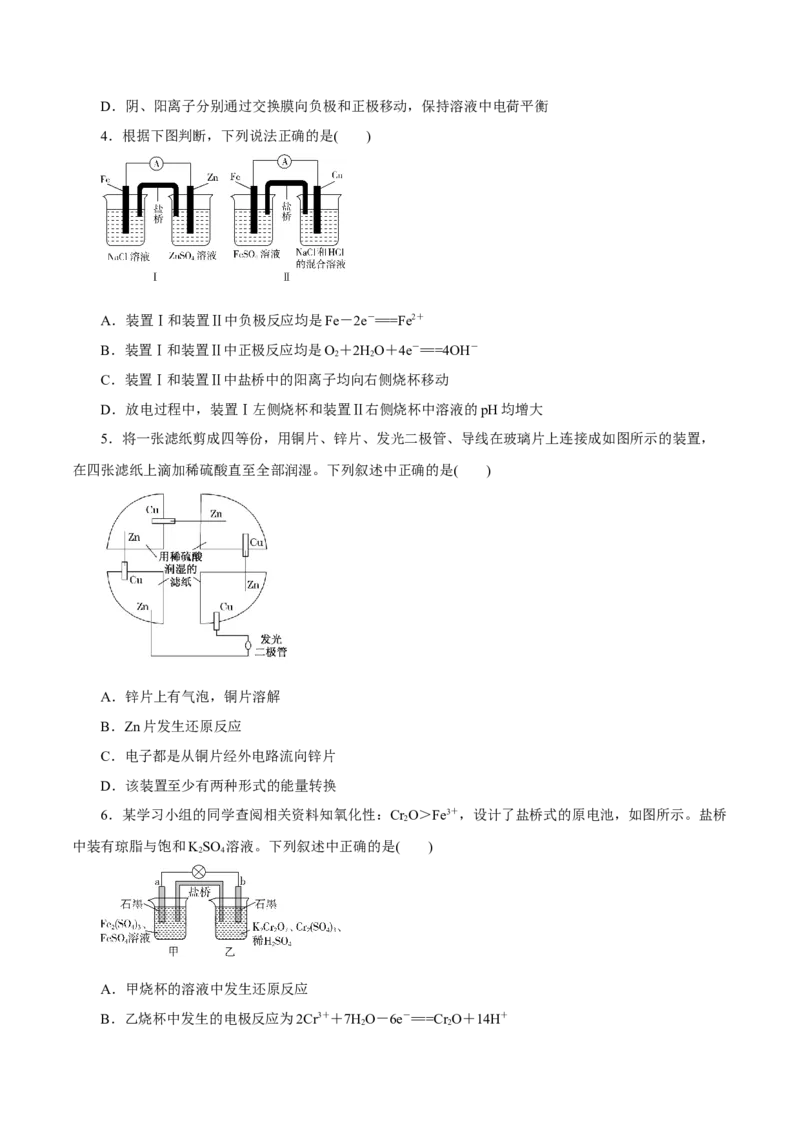
2.某小组为研究原电池原理,设计如图装置,下列叙述正确的是( )
A.若X为Fe,Y为Cu,则铁为正极
B.若X为Fe,Y为Cu,则电子由铜片流向铁片
C.若X为Fe,Y为C,则碳棒上有红色固体析出
D.若X为Cu,Y为Zn,则锌片发生还原反应
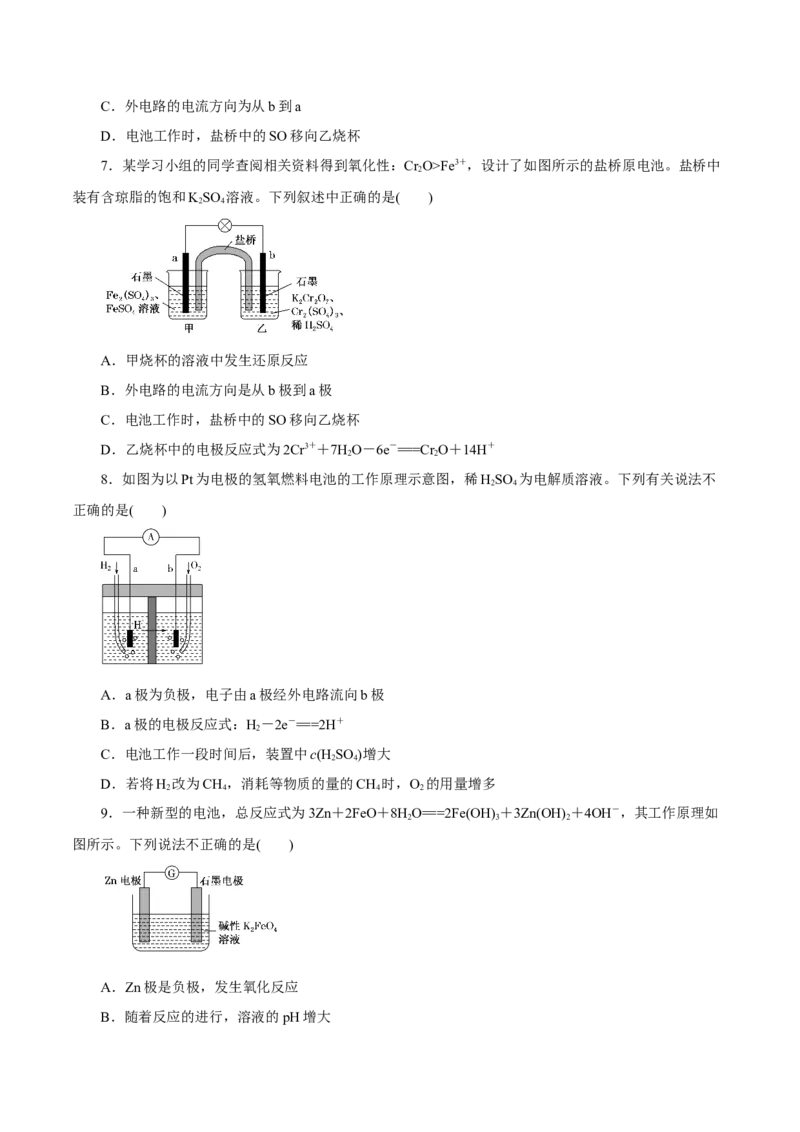
3.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过。下列有关叙述中正确
的是( )
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池中的c(SO)减小
C.电池工作一段时间后,乙池溶液的总质量增加D.阴、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
4.根据下图判断,下列说法正确的是( )
A.装置Ⅰ和装置Ⅱ中负极反应均是Fe-2e-===Fe2+
B.装置Ⅰ和装置Ⅱ中正极反应均是O+2HO+4e-===4OH-
2 2
C.装置Ⅰ和装置Ⅱ中盐桥中的阳离子均向右侧烧杯移动
D.放电过程中,装置Ⅰ左侧烧杯和装置Ⅱ右侧烧杯中溶液的pH均增大
5.将一张滤纸剪成四等份,用铜片、锌片、发光二极管、导线在玻璃片上连接成如图所示的装置,
在四张滤纸上滴加稀硫酸直至全部润湿。下列叙述中正确的是( )
A.锌片上有气泡,铜片溶解
B.Zn片发生还原反应
C.电子都是从铜片经外电路流向锌片
D.该装置至少有两种形式的能量转换
6.某学习小组的同学查阅相关资料知氧化性:Cr O>Fe3+,设计了盐桥式的原电池,如图所示。盐桥
2
中装有琼脂与饱和KSO 溶液。下列叙述中正确的是( )
2 4
A.甲烧杯的溶液中发生还原反应
B.乙烧杯中发生的电极反应为2Cr3++7HO-6e-===Cr O+14H+
2 2C.外电路的电流方向为从b到a
D.电池工作时,盐桥中的SO移向乙烧杯
7.某学习小组的同学查阅相关资料得到氧化性:Cr O>Fe3+,设计了如图所示的盐桥原电池。盐桥中
2
装有含琼脂的饱和KSO 溶液。下列叙述中正确的是( )
2 4
A.甲烧杯的溶液中发生还原反应
B.外电路的电流方向是从b极到a极
C.电池工作时,盐桥中的SO移向乙烧杯
D.乙烧杯中的电极反应式为2Cr3++7HO-6e-===Cr O+14H+
2 2
8.如图为以Pt为电极的氢氧燃料电池的工作原理示意图,稀HSO 为电解质溶液。下列有关说法不
2 4
正确的是( )
A.a极为负极,电子由a极经外电路流向b极
B.a极的电极反应式:H-2e-===2H+
2
C.电池工作一段时间后,装置中c(H SO )增大
2 4
D.若将H 改为CH,消耗等物质的量的CH 时,O 的用量增多
2 4 4 2
9.一种新型的电池,总反应式为3Zn+2FeO+8HO===2Fe(OH) +3Zn(OH) +4OH-,其工作原理如
2 3 2
图所示。下列说法不正确的是( )
A.Zn极是负极,发生氧化反应
B.随着反应的进行,溶液的pH增大C.电子由Zn极流出到石墨电极,再经过溶液回到Zn极,形成回路
D.石墨电极上发生的反应为FeO+3e-+4HO===Fe(OH) ↓+5OH-
2 3
10.可充电氟镁动力电池比锂电池具有更高的能量密度和安全性,其电池反应为Mg+
2MnF ===2MnF+MgF 。下列有关说法不正确的是( )
3 2 2
A.镁为负极材料
B.正极的电极反应式为MnF +e-===MnF+F-
3 2
C.电子从镁极流出,经电解质流向正极
D.每生成1 mol MnF 时转移1 mol电子
2
【练提升】
1.某原电池以银、铂为电极,用含Ag+的固体作电解质,Ag+可在固体电解质中自由移动。电池总反
应式为2Ag+Cl===2AgCl。利用该电池可以测定空气中Cl 的含量。下列说法中错误的是( )
2 2
A.空气中c(Cl )越大,消耗Ag的速率越快
2
B.铂极的电极反应式为Cl+2e-+2Ag+===2AgCl
2
C.电池工作时电解质中Ag+总数保持不变
D.电子移动方向:银→固体电解质→铂
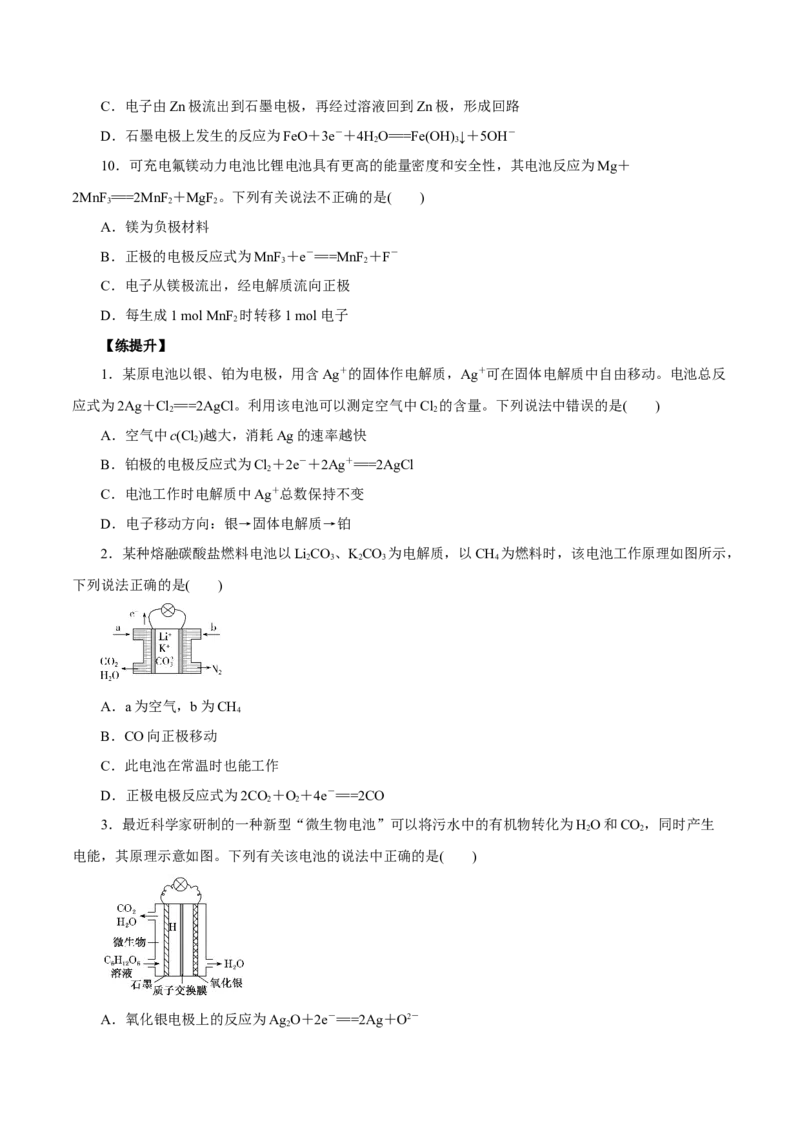
2.某种熔融碳酸盐燃料电池以LiCO、KCO 为电解质,以CH 为燃料时,该电池工作原理如图所示,
2 3 2 3 4
下列说法正确的是( )
A.a为空气,b为CH
4
B.CO向正极移动
C.此电池在常温时也能工作
D.正极电极反应式为2CO+O+4e-===2CO
2 2
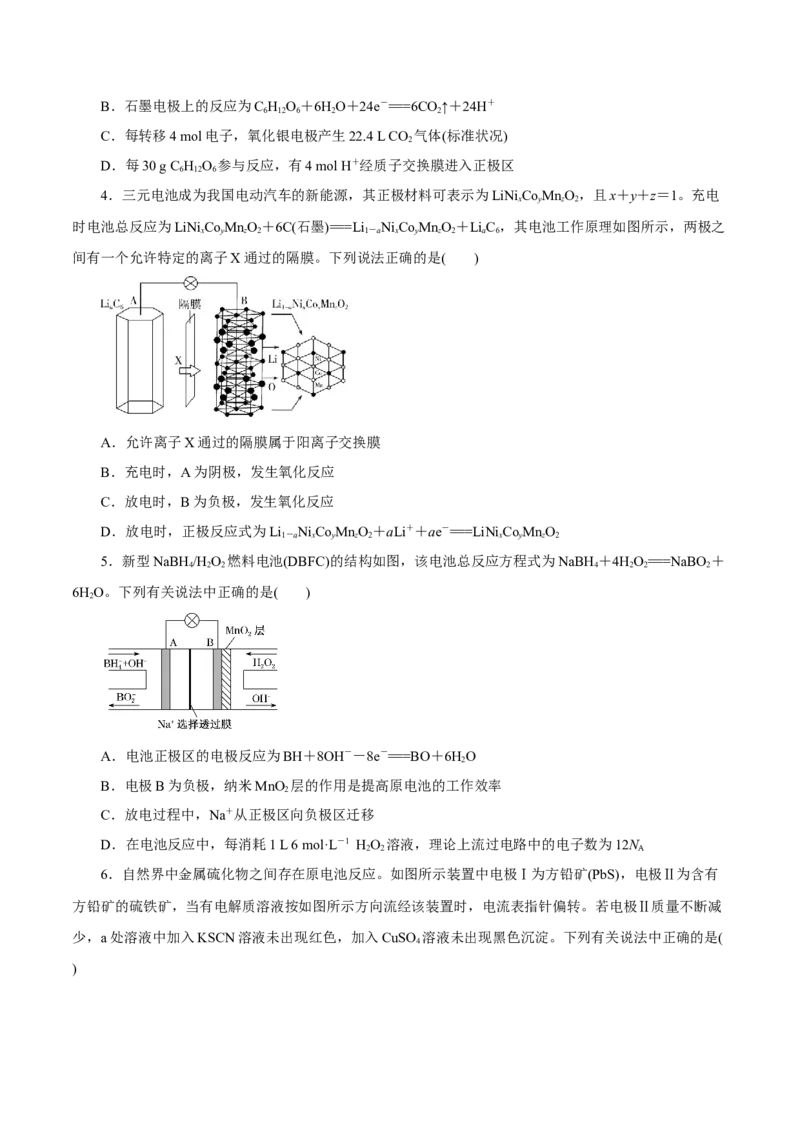
3.最近科学家研制的一种新型“微生物电池”可以将污水中的有机物转化为HO和CO,同时产生
2 2
电能,其原理示意如图。下列有关该电池的说法中正确的是( )
A.氧化银电极上的反应为Ag O+2e-===2Ag+O2-
2B.石墨电极上的反应为C H O+6HO+24e-===6CO ↑+24H+
6 12 6 2 2
C.每转移4 mol电子,氧化银电极产生22.4 L CO 气体(标准状况)
2
D.每30 g C H O 参与反应,有4 mol H+经质子交换膜进入正极区
6 12 6
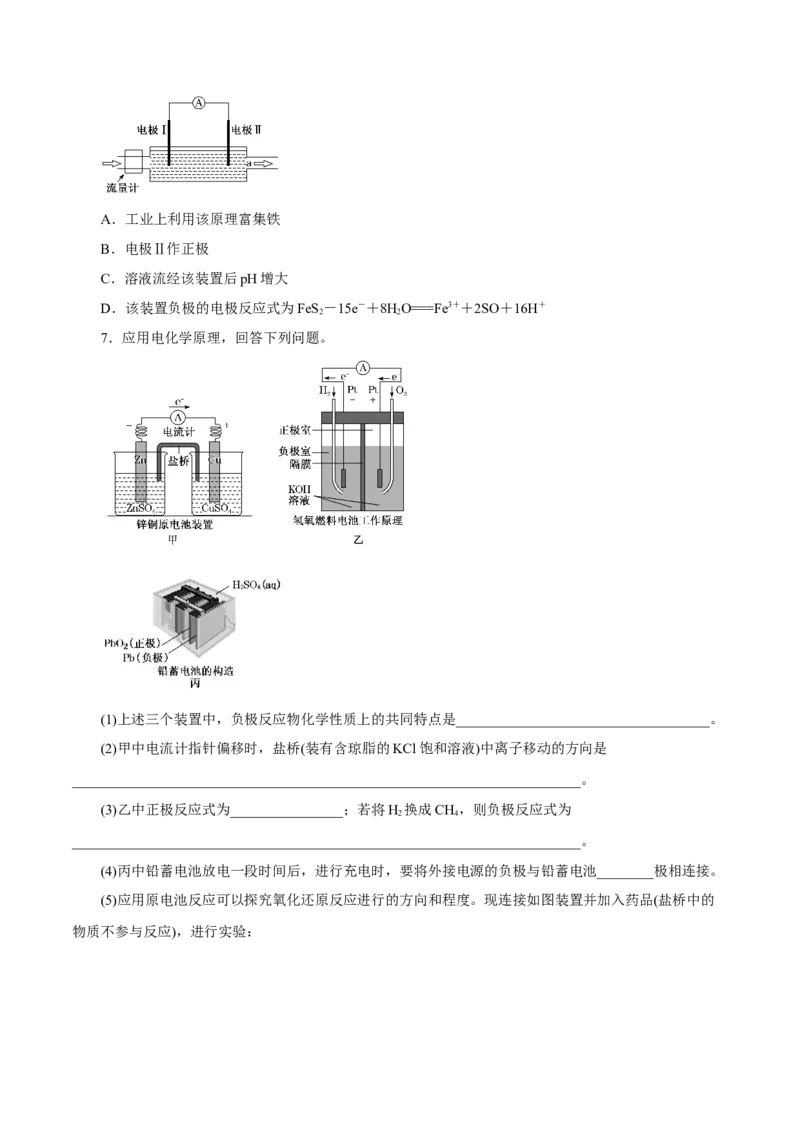
4.三元电池成为我国电动汽车的新能源,其正极材料可表示为LiNiCoMnO,且x+y+z=1。充电
x y z 2
时电池总反应为LiNiCoMnO+6C(石墨)===Li NiCoMnO+LiC ,其电池工作原理如图所示,两极之
x y z 2 1-a x y z 2 a 6
间有一个允许特定的离子X通过的隔膜。下列说法正确的是( )
A.允许离子X通过的隔膜属于阳离子交换膜
B.充电时,A为阴极,发生氧化反应
C.放电时,B为负极,发生氧化反应
D.放电时,正极反应式为Li NiCoMnO+aLi++ae-===LiNiCoMnO
1-a x y z 2 x y z 2
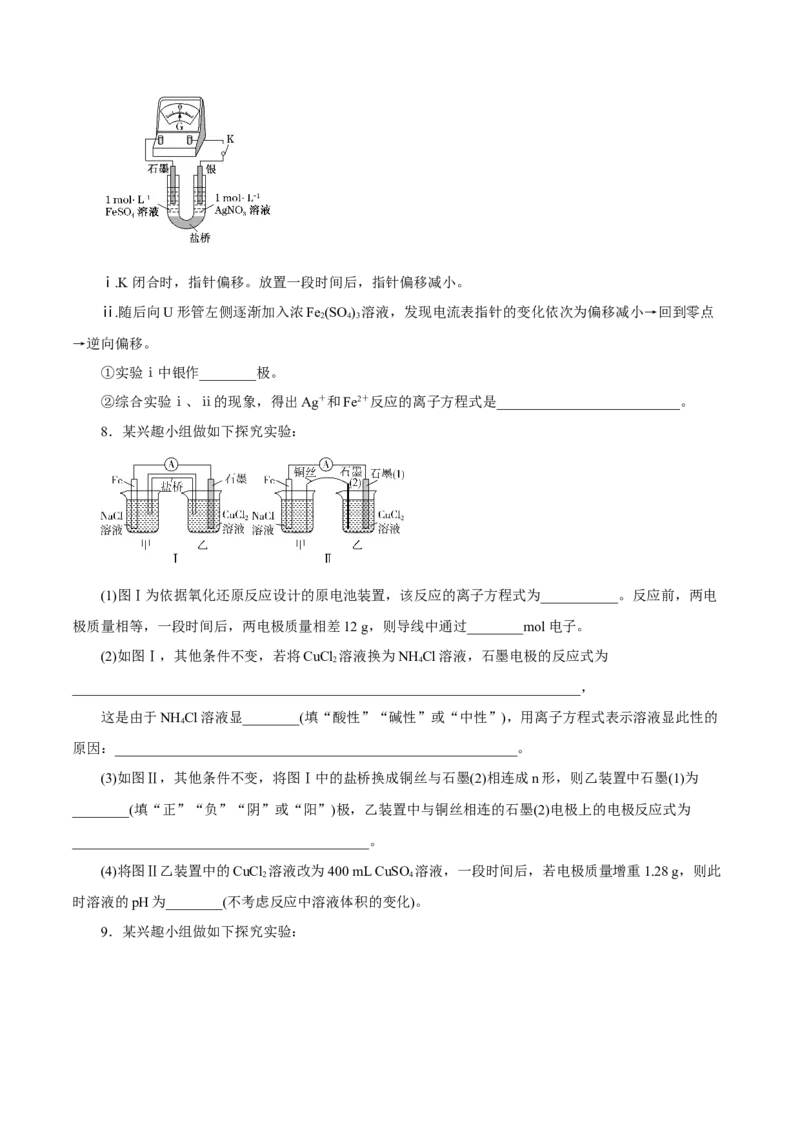
5.新型NaBH /H O 燃料电池(DBFC)的结构如图,该电池总反应方程式为NaBH +4HO===NaBO +
4 2 2 4 2 2 2
6HO。下列有关说法中正确的是( )
2
A.电池正极区的电极反应为BH+8OH--8e-===BO+6HO
2
B.电极B为负极,纳米MnO 层的作用是提高原电池的工作效率
2
C.放电过程中,Na+从正极区向负极区迁移
D.在电池反应中,每消耗1 L 6 mol·L-1 HO 溶液,理论上流过电路中的电子数为12N
2 2 A
6.自然界中金属硫化物之间存在原电池反应。如图所示装置中电极Ⅰ为方铅矿(PbS),电极Ⅱ为含有
方铅矿的硫铁矿,当有电解质溶液按如图所示方向流经该装置时,电流表指针偏转。若电极Ⅱ质量不断减
少,a处溶液中加入KSCN溶液未出现红色,加入CuSO 溶液未出现黑色沉淀。下列有关说法中正确的是(
4
)A.工业上利用该原理富集铁
B.电极Ⅱ作正极
C.溶液流经该装置后pH增大
D.该装置负极的电极反应式为FeS-15e-+8HO===Fe3++2SO+16H+
2 2
7.应用电化学原理,回答下列问题。
(1)上述三个装置中,负极反应物化学性质上的共同特点是____________________________________。
(2)甲中电流计指针偏移时,盐桥(装有含琼脂的KCl饱和溶液)中离子移动的方向是
________________________________________________________________________。
(3)乙中正极反应式为________________;若将H 换成CH,则负极反应式为
2 4
________________________________________________________________________。
(4)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池________极相连接。
(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。现连接如图装置并加入药品(盐桥中的
物质不参与反应),进行实验:ⅰ.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ⅱ.随后向U形管左侧逐渐加入浓Fe (SO ) 溶液,发现电流表指针的变化依次为偏移减小→回到零点
2 4 3
→逆向偏移。
①实验ⅰ中银作________极。
②综合实验ⅰ、ⅱ的现象,得出Ag+和Fe2+反应的离子方程式是__________________________。
8.某兴趣小组做如下探究实验:
(1)图Ⅰ为依据氧化还原反应设计的原电池装置,该反应的离子方程式为___________。反应前,两电
极质量相等,一段时间后,两电极质量相差12 g,则导线中通过________mol电子。
(2)如图Ⅰ,其他条件不变,若将CuCl 溶液换为NH Cl溶液,石墨电极的反应式为
2 4
________________________________________________________________________,
这是由于NH Cl溶液显________(填“酸性”“碱性”或“中性”),用离子方程式表示溶液显此性的
4
原因:_________________________________________________________。
(3)如图Ⅱ,其他条件不变,将图Ⅰ中的盐桥换成铜丝与石墨(2)相连成n形,则乙装置中石墨(1)为
________(填“正”“负”“阴”或“阳”)极,乙装置中与铜丝相连的石墨(2)电极上的电极反应式为
__________________________________________。
(4)将图Ⅱ乙装置中的CuCl 溶液改为400 mL CuSO 溶液,一段时间后,若电极质量增重1.28 g,则此
2 4
时溶液的pH为________(不考虑反应中溶液体积的变化)。
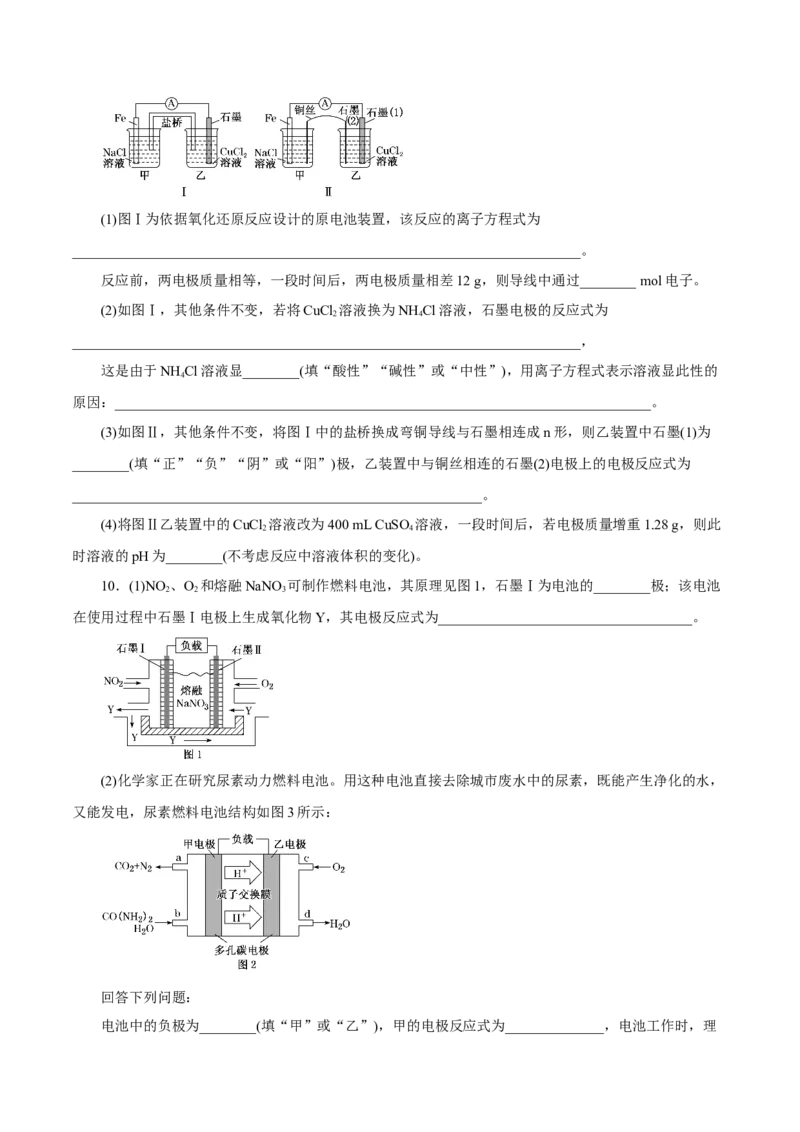
9.某兴趣小组做如下探究实验:(1)图Ⅰ为依据氧化还原反应设计的原电池装置,该反应的离子方程式为
________________________________________________________________________。
反应前,两电极质量相等,一段时间后,两电极质量相差12 g,则导线中通过________ mol电子。
(2)如图Ⅰ,其他条件不变,若将CuCl 溶液换为NH Cl溶液,石墨电极的反应式为
2 4
________________________________________________________________________,
这是由于NH Cl溶液显________(填“酸性”“碱性”或“中性”),用离子方程式表示溶液显此性的
4
原因:____________________________________________________________________________。
(3)如图Ⅱ,其他条件不变,将图Ⅰ中的盐桥换成弯铜导线与石墨相连成n形,则乙装置中石墨(1)为
________(填“正”“负”“阴”或“阳”)极,乙装置中与铜丝相连的石墨(2)电极上的电极反应式为
__________________________________________________________。
(4)将图Ⅱ乙装置中的CuCl 溶液改为400 mL CuSO 溶液,一段时间后,若电极质量增重1.28 g,则此
2 4
时溶液的pH为________(不考虑反应中溶液体积的变化)。
10.(1)NO 、O 和熔融NaNO 可制作燃料电池,其原理见图1,石墨Ⅰ为电池的________极;该电池
2 2 3
在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为____________________________________。
(2)化学家正在研究尿素动力燃料电池。用这种电池直接去除城市废水中的尿素,既能产生净化的水,
又能发电,尿素燃料电池结构如图3所示:
回答下列问题:
电池中的负极为________(填“甲”或“乙”),甲的电极反应式为______________,电池工作时,理论上每净化1 mol尿素,消耗O 的体积(标准状况下)约为________L。
2