文档内容
第 16 讲 原电池
【学科核心素养】
变化观念与平衡思想:认识原电池反应的本质是自发的氧化还原反应;能多角度、动态地分析原电池
中物质的变化及能量的转换。
证据推理与模型认知:能利用典型的原电池装置,分析原电池原理,建立解答原电池问题的思维模型,
并利用模型揭示其本质及规律。
科学态度与社会责任:具有可持续发展意识和绿色化学观念,能对与原电池有关的社会热点问题做出
正确的价值判断与分析。
【核心素养发展目标】
1.理解原电池的构成、工作原理及应用,能书写电极反应和总反应方程式。
2.了解常见化学电源的种类及其工作原理。
【知识点解读】
知识点一 原电池的工作原理及应用
1.概念和反应本质
原电池是把化学能转化为电能的装置,其反应本质是氧化还原反应。
2.构成条件
(1)一看反应:看是否有能自发进行的氧化还原反应发生(一般是活泼性强的金属与电解质溶液反应)。
(2)二看两电极:一般是活泼性不同的两电极。
(3)三看是否形成闭合回路,形成闭合回路需三个条件:
①电解质溶液;
②两电极直接或间接接触;
③两电极插入电解质溶液中。
3.工作原理
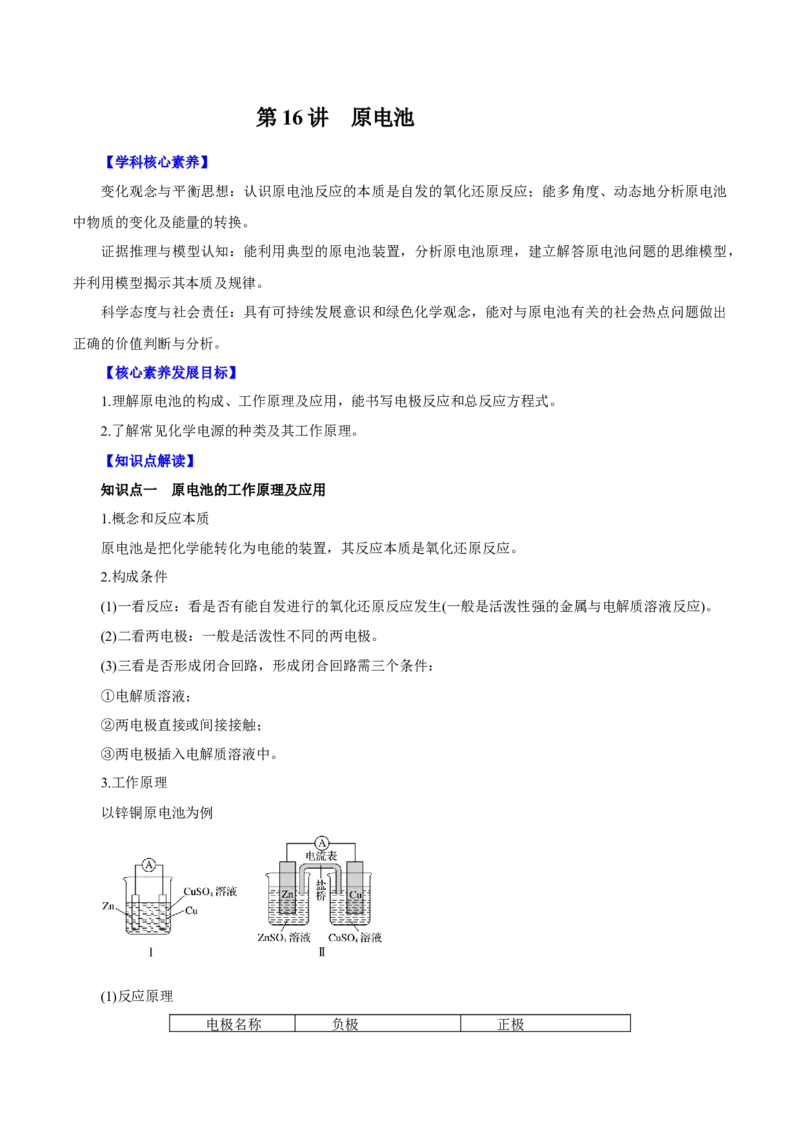
以锌铜原电池为例
(1)反应原理
电极名称 负极 正极电极材料 锌片 铜片
电极反应 Zn-2e-===Zn2+ Cu2++2e-===Cu
反应类型 氧化反应 还原反应
电子流向 由Zn片沿导线流向Cu片
盐桥中离子移向 盐桥含饱和KCl溶液,K+移向正极,Cl-移向负极
(2)盐桥的组成和作用
①盐桥中装有饱和的KCl、KNO 等溶液和琼胶制成的胶冻。
3
②盐桥的作用:a.连接内电路,形成闭合回路;b.平衡电荷,使原电池不断产生电流。
(3)单液原电池(无盐桥)和双液原电池(有盐桥)对比
名称 单液原电池 双液原电池
装置
相同点 正、负极电极反应,总反应式,电极现象
还原剂Zn与氧化剂Cu2+直接接 Zn与氧化剂Cu2+不直接接触,仅
不同点 触,既有化学能转化为电能,又有化学 有化学能转化为电能,避免了能量损
能转化为热能,造成能量损耗 耗,故电流稳定,持续时间长
4.原电池原理的应用
(1)比较金属的活动性强弱:原电池中,负极一般是活动性较强的金属,正极一般是活动性较弱的金属
(或非金属)。
(2)加快化学反应速率:氧化还原反应形成原电池时,反应速率加快。
(3)用于金属的防护:将需要保护的金属制品作原电池的正极而受到保护。
(4)设计制作化学电源
①首先将氧化还原反应分成两个半反应。
②根据原电池的工作原理,结合两个半反应,选择正、负电极材料以及电解质溶液。
知识点二 常见化学电源及工作原理
一、一次电池:只能使用一次,不能充电复原继续使用
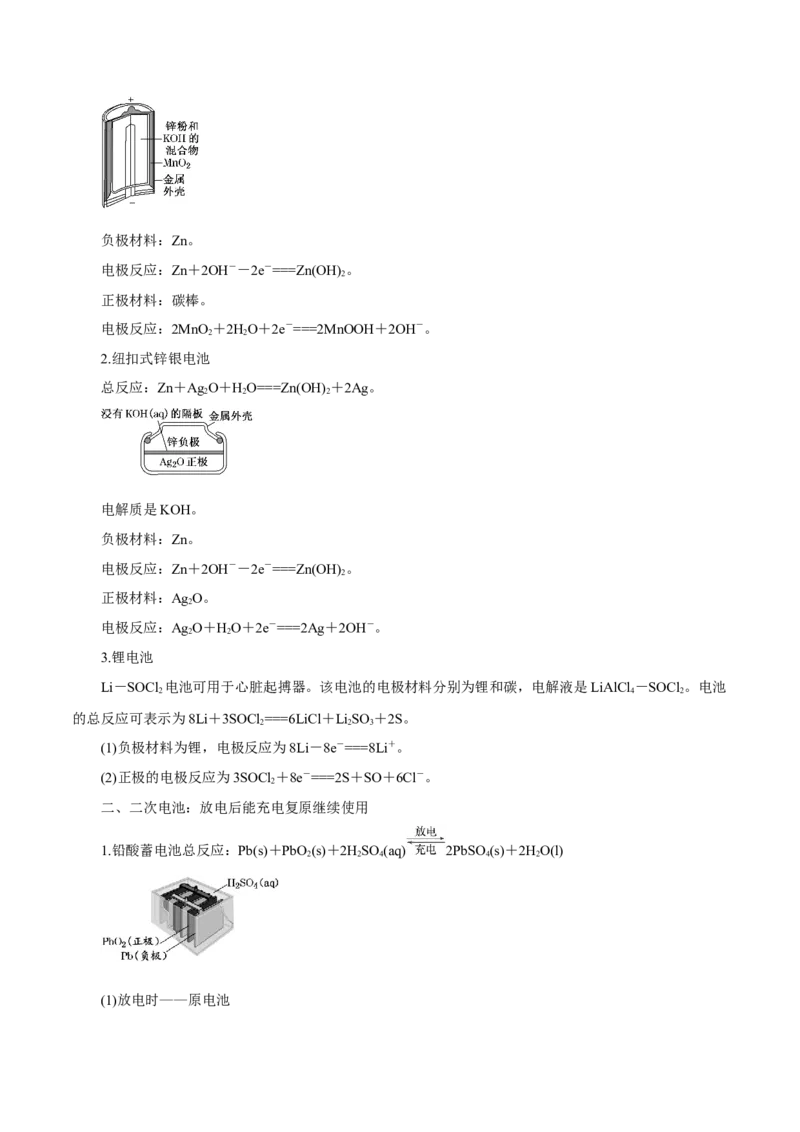
1.碱性锌锰干电池
总反应:Zn+2MnO +2HO===2MnOOH+Zn(OH) 。
2 2 2负极材料:Zn。
电极反应:Zn+2OH--2e-===Zn(OH) 。
2
正极材料:碳棒。
电极反应:2MnO +2HO+2e-===2MnOOH+2OH-。
2 2
2.纽扣式锌银电池
总反应:Zn+Ag O+HO===Zn(OH) +2Ag。
2 2 2
电解质是KOH。
负极材料:Zn。
电极反应:Zn+2OH--2e-===Zn(OH) 。
2
正极材料:Ag O。
2
电极反应:Ag O+HO+2e-===2Ag+2OH-。
2 2
3.锂电池
Li-SOCl 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl -SOCl 。电池
2 4 2
的总反应可表示为8Li+3SOCl ===6LiCl+LiSO +2S。
2 2 3
(1)负极材料为锂,电极反应为8Li-8e-===8Li+。
(2)正极的电极反应为3SOCl +8e-===2S+SO+6Cl-。
2
二、二次电池:放电后能充电复原继续使用
1.铅酸蓄电池总反应:Pb(s)+PbO (s)+2HSO (aq) 2PbSO (s)+2HO(l)
2 2 4 4 2
(1)放电时——原电池负极反应:Pb(s)+SO(aq)-2e-===PbSO (s);
4
正极反应:PbO (s)+4H+(aq)+SO(aq)+2e-===PbSO (s)+2HO(l)。
2 4 2
(2)充电时——电解池
阴极反应:PbSO (s)+2e-===Pb(s)+SO(aq);
4
阳极反应:PbSO (s)+2HO(l)-2e-===PbO(s)+4H+(aq)+SO(aq)。
4 2 2
2.图解二次电池的充放电
3.二次电池的充放电规律
(1)充电时电极的连接:充电的目的是使电池恢复其供电能力,因此负极应与电源的负极相连以获得电
子,可简记为负接负后作阴极,正接正后作阳极。
(2)工作时的电极反应式:同一电极上的电极反应式,在充电与放电时,形式上恰好是相反的;同一电
极周围的溶液,充电与放电时pH的变化趋势也恰好相反。
三、燃料电池
1.氢氧燃料电池是目前最成熟的燃料电池,可分为酸性和碱性两种。
种类 酸性 碱性
负极反应式 2H-4e-===4H+ 2H+4OH--4e-===4HO
2 2 2
正极反应式 O+4e-+4H+===2HO O+2HO+4e-===4OH-
2 2 2 2
电池总反应式 2H+O===2HO
2 2 2
备注 燃料电池的电极不参与反应,有很强的催化活性,起导电作用
2.解答燃料电池题目的思维模型
3.解答燃料电池题目的几个关键点
(1)要注意介质是什么?是电解质溶液还是熔融盐或氧化物。
(2)通入负极的物质为燃料,通入正极的物质为氧气。
(3)通过介质中离子的移动方向,可判断电池的正负极,同时考虑该离子参与靠近一极的电极反应。
【典例剖析】
高频考点一 原电池原理及其应用【例1】(2019·海南高考)微型银—锌电池可用作电子仪器的电源,其电极分别是Ag/Ag O和Zn,电解
2
质为KOH溶液,电池总反应为Ag O+Zn+HO===2Ag+Zn(OH) 。下列说法正确的是( )
2 2 2
A.电池工作过程中,KOH溶液浓度降低
B.电池工作过程中,电解液中OH-向正极迁移
C.负极发生反应:Zn+2OH--2e-===Zn(OH)
2
D.正极发生反应:Ag O+2H++2e-===Ag+HO
2 2
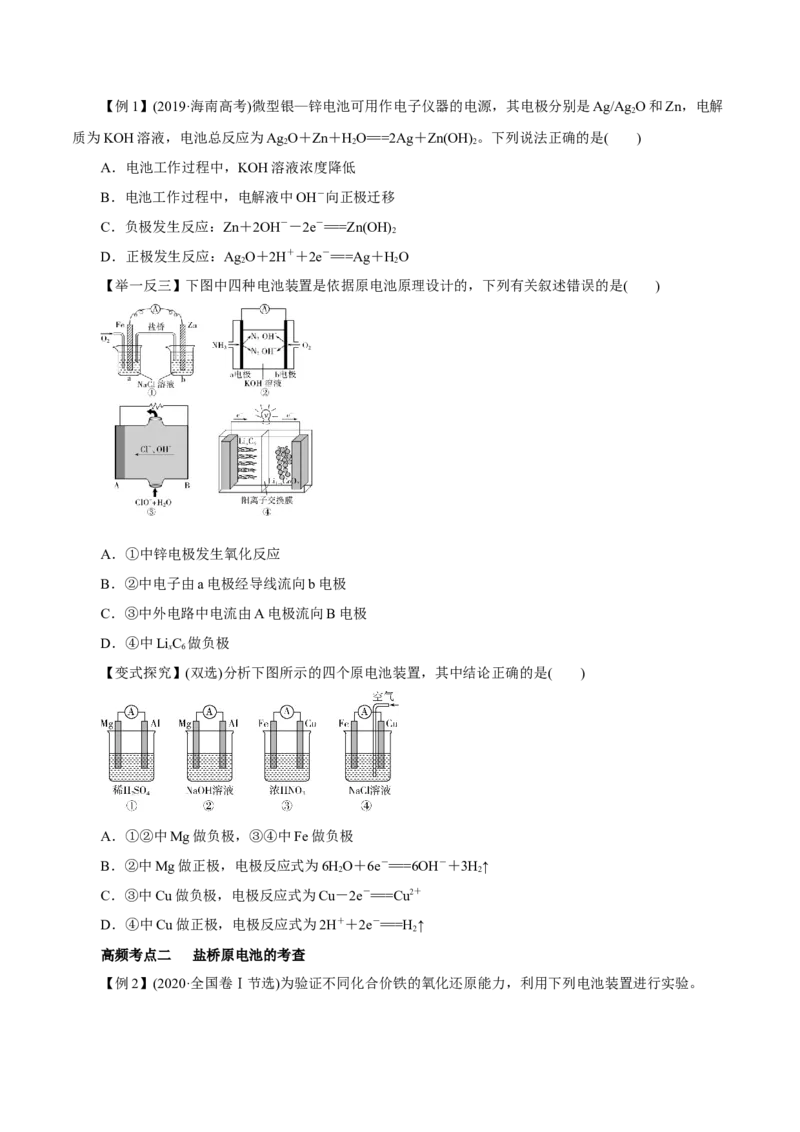
【举一反三】下图中四种电池装置是依据原电池原理设计的,下列有关叙述错误的是( )
A.①中锌电极发生氧化反应
B.②中电子由a电极经导线流向b电极
C.③中外电路中电流由A电极流向B电极
D.④中LiC 做负极
x 6
【变式探究】(双选)分析下图所示的四个原电池装置,其中结论正确的是( )
A.①②中Mg做负极,③④中Fe做负极
B.②中Mg做正极,电极反应式为6HO+6e-===6OH-+3H↑
2 2
C.③中Cu做负极,电极反应式为Cu-2e-===Cu2+
D.④中Cu做正极,电极反应式为2H++2e-===H ↑
2
高频考点二 盐桥原电池的考查
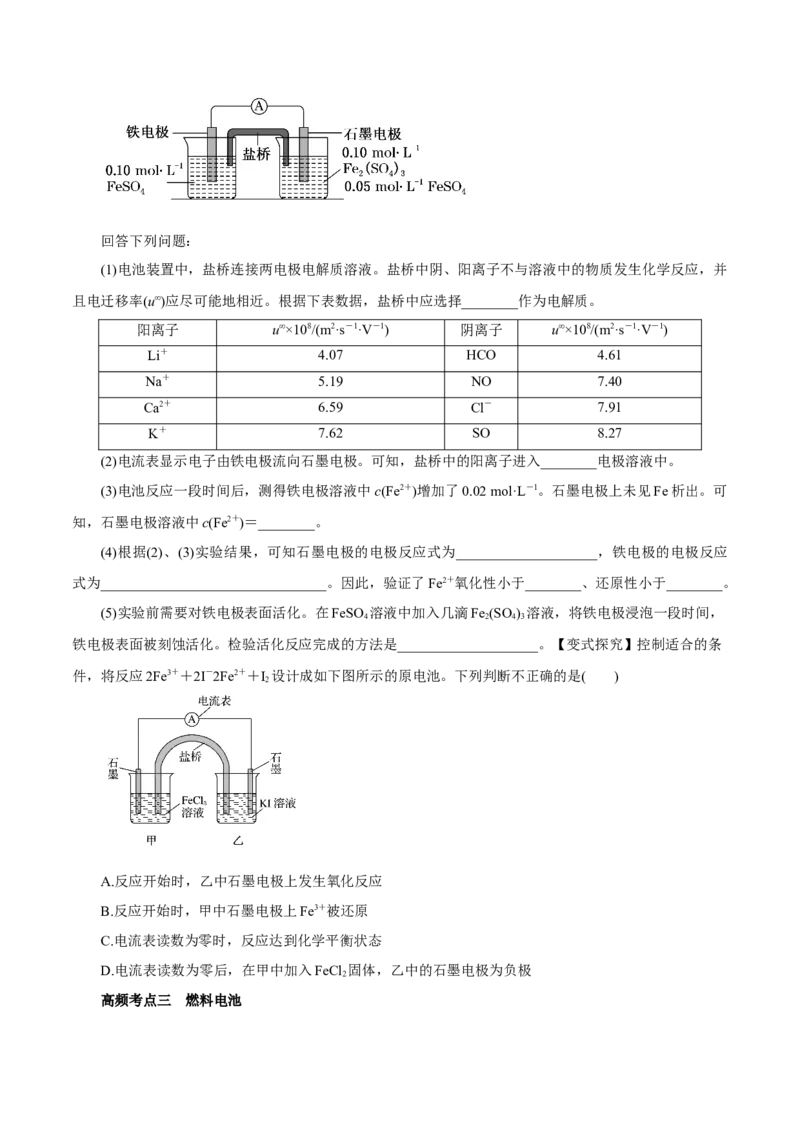
【例2】(2020·全国卷Ⅰ节选)为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。回答下列问题:
(1)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并
且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择________作为电解质。
阳离子 u∞×108/(m2·s-1·V-1) 阴离子 u∞×108/(m2·s-1·V-1)
Li+ 4.07 HCO 4.61
Na+ 5.19 NO 7.40
Ca2+ 6.59 Cl- 7.91
K+ 7.62 SO 8.27
(2)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________电极溶液中。
(3)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L-1。石墨电极上未见Fe析出。可
知,石墨电极溶液中c(Fe2+)=________。
(4)根据(2)、(3)实验结果,可知石墨电极的电极反应式为____________________,铁电极的电极反应
式为________________________________。因此,验证了Fe2+氧化性小于________、还原性小于________。
(5)实验前需要对铁电极表面活化。在FeSO 溶液中加入几滴Fe (SO ) 溶液,将铁电极浸泡一段时间,
4 2 4 3
铁电极表面被刻蚀活化。检验活化反应完成的方法是____________________。【变式探究】控制适合的条
件,将反应2Fe3++2I-2Fe2++I 设计成如下图所示的原电池。下列判断不正确的是( )
2
A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上Fe3+被还原
C.电流表读数为零时,反应达到化学平衡状态
D.电流表读数为零后,在甲中加入FeCl 固体,乙中的石墨电极为负极
2
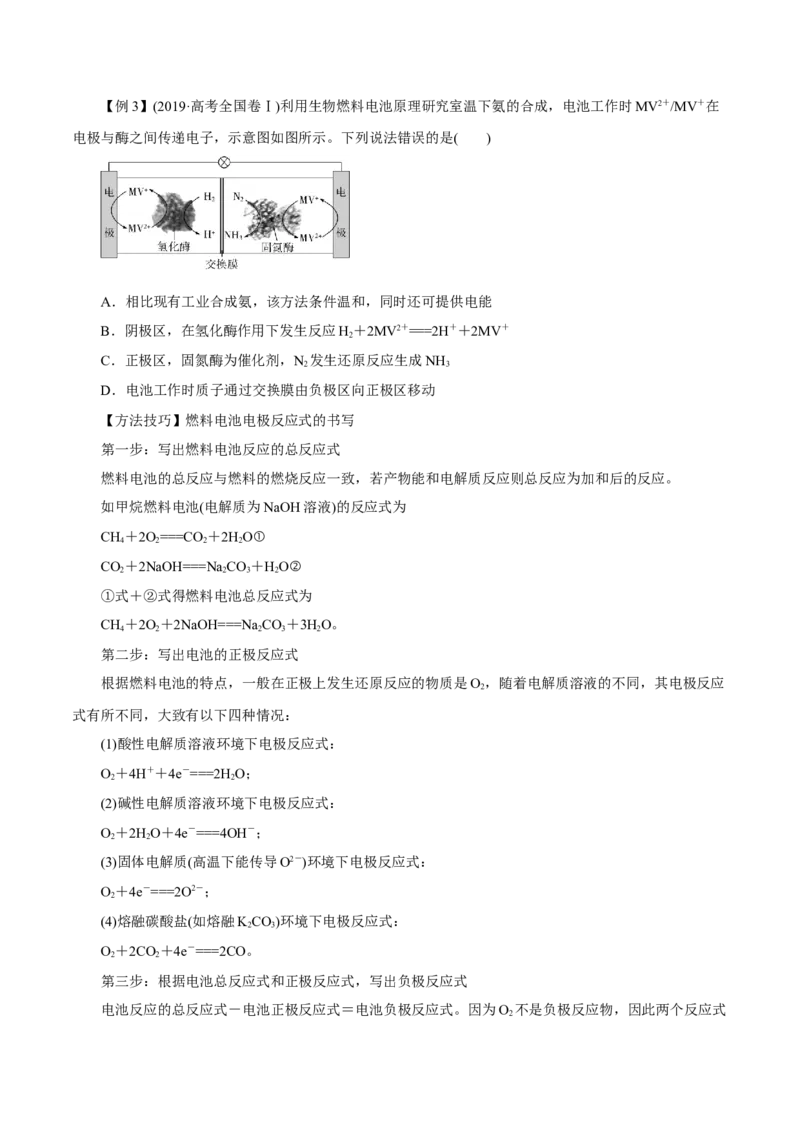
高频考点三 燃料电池【例3】(2019·高考全国卷Ⅰ)利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在
电极与酶之间传递电子,示意图如图所示。下列说法错误的是( )
A.相比现有工业合成氨,该方法条件温和,同时还可提供电能
B.阴极区,在氢化酶作用下发生反应H+2MV2+===2H++2MV+
2
C.正极区,固氮酶为催化剂,N 发生还原反应生成NH
2 3
D.电池工作时质子通过交换膜由负极区向正极区移动
【方法技巧】燃料电池电极反应式的书写
第一步:写出燃料电池反应的总反应式
燃料电池的总反应与燃料的燃烧反应一致,若产物能和电解质反应则总反应为加和后的反应。
如甲烷燃料电池(电解质为NaOH溶液)的反应式为
CH+2O===CO +2HO①
4 2 2 2
CO+2NaOH===Na CO+HO②
2 2 3 2
①式+②式得燃料电池总反应式为
CH+2O+2NaOH===Na CO+3HO。
4 2 2 3 2
第二步:写出电池的正极反应式
根据燃料电池的特点,一般在正极上发生还原反应的物质是O,随着电解质溶液的不同,其电极反应
2
式有所不同,大致有以下四种情况:
(1)酸性电解质溶液环境下电极反应式:
O+4H++4e-===2HO;
2 2
(2)碱性电解质溶液环境下电极反应式:
O+2HO+4e-===4OH-;
2 2
(3)固体电解质(高温下能传导O2-)环境下电极反应式:
O+4e-===2O2-;
2
(4)熔融碳酸盐(如熔融KCO)环境下电极反应式:
2 3
O+2CO+4e-===2CO。
2 2
第三步:根据电池总反应式和正极反应式,写出负极反应式
电池反应的总反应式-电池正极反应式=电池负极反应式。因为O 不是负极反应物,因此两个反应式
2相减时要彻底消除O。
2
【变式探究】(双选)金属锂燃料电池是一种新型电池,比锂离子电池具有更高的能量密度。它无电时
也无需充电,只需更换其中的某些材料即可,其工作示意图如下,下列说法正确的是( )
A.放电时,通入空气的一极为负极
B.放电时,电池反应为4Li+O+2HO===4LiOH
2 2
C.有机电解液可以是乙醇等无水有机物
D.在更换锂电极的同时,要更换水性电解液
高频考点四 可充电电池(二次电池)
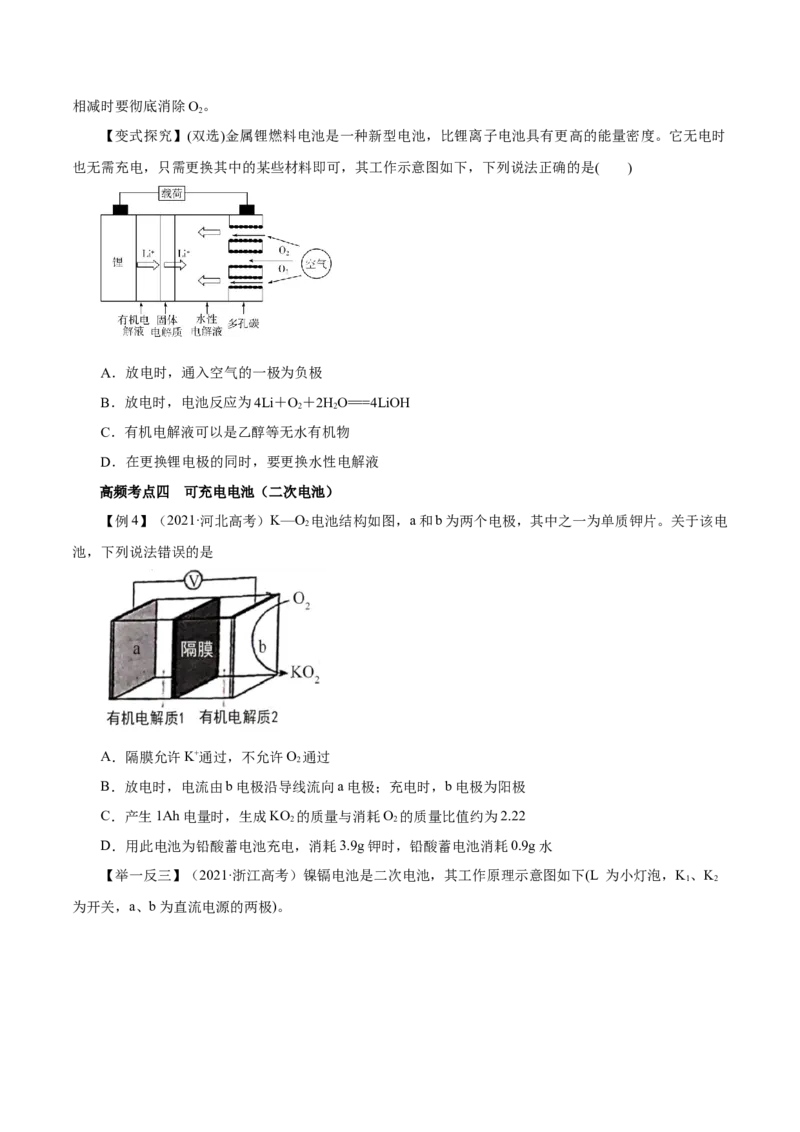
【例4】(2021·河北高考)K—O 电池结构如图,a和b为两个电极,其中之一为单质钾片。关于该电
2
池,下列说法错误的是
A.隔膜允许K+通过,不允许O 通过
2
B.放电时,电流由b电极沿导线流向a电极;充电时,b电极为阳极
C.产生1Ah电量时,生成KO 的质量与消耗O 的质量比值约为2.22
2 2
D.用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗0.9g水
【举一反三】(2021·浙江高考)镍镉电池是二次电池,其工作原理示意图如下(L 为小灯泡,K、K
1 2
为开关,a、b为直流电源的两极)。下列说法不正确的是
A.断开K、合上K,镍镉电池能量转化形式:化学能→电能
2 1
B.断开K、合上K,电极A为阴极,发生还原反应
1 2
C.电极B发生氧化反应过程中,溶液中KOH浓度不变
D.镍镉二次电池的总反应式:Cd+ 2NiOOH+2H O Cd(OH) +2Ni(OH)
2 2 2
【方法技巧】
1.可充电电池的思维模型
因此,充电时电极的连接可简记为“负接负后作阴极,正接正后作阳极”。
2.可充电电池的分析流程
(1)可充电电池有充电和放电两个过程,放电时是原电池反应,充电时是电解池反应。
(2)放电时的负极反应和充电时的阴极反应互为逆反应,放电时的正极反应和充电时的阳极反应互为逆
反应。将负(正)极反应式变换方向并将电子移项即可得出阴(阳)极反应式。
(3)充、放电时电解质溶液中离子移动方向的判断
分析电池工作过程中电解质溶液的变化时,要结合电池总反应进行分析。
①首先应分清电池是放电还是充电。
②再判断出正、负极或阴、阳极。(4)“加减法”书写新型二次电池放电的电极反应式
若已知电池放电时的总反应式,可先写出较易书写的一极的电极反应式,然后在电子守恒的基础上,
由总反应式减去较易写出的一极的电极反应式,即得到较难写出的另一极的电极反应式。
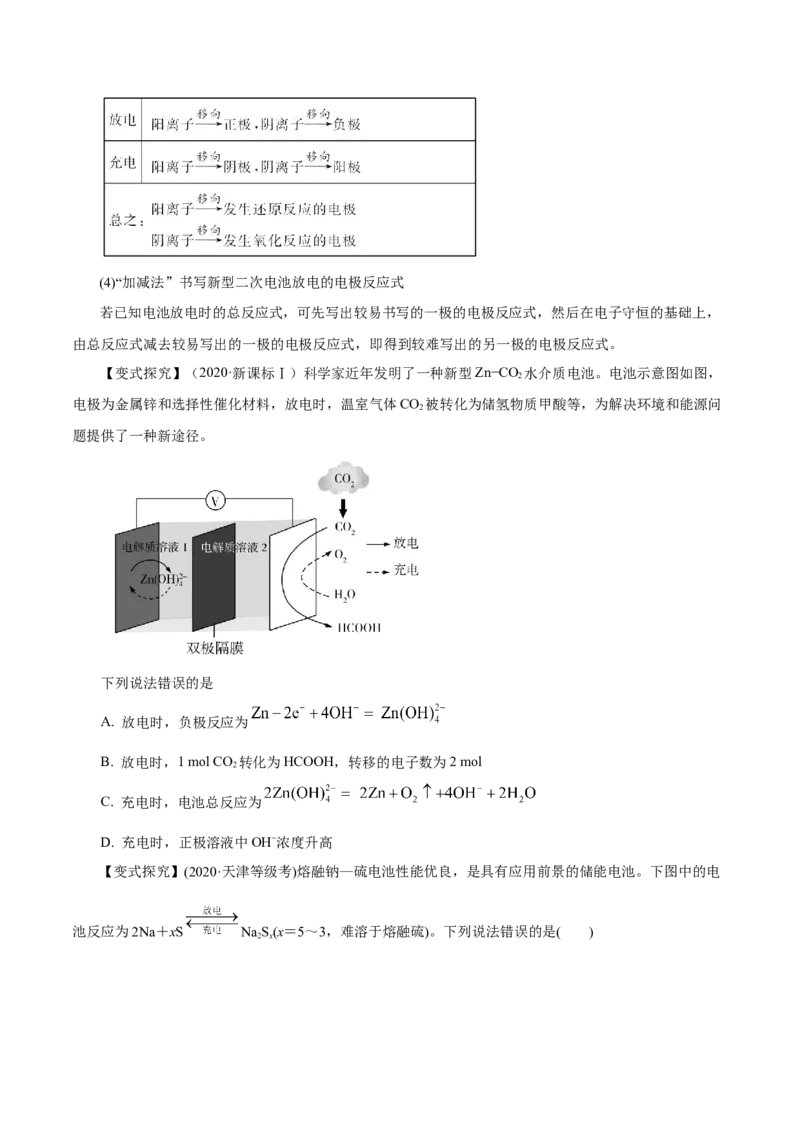
【变式探究】(2020·新课标Ⅰ)科学家近年发明了一种新型Zn−CO 水介质电池。电池示意图如图,
2
电极为金属锌和选择性催化材料,放电时,温室气体CO 被转化为储氢物质甲酸等,为解决环境和能源问
2
题提供了一种新途径。
下列说法错误的是
A. 放电时,负极反应为
B. 放电时,1 mol CO 转化为HCOOH,转移的电子数为2 mol
2
C. 充电时,电池总反应为
D. 充电时,正极溶液中OH−浓度升高
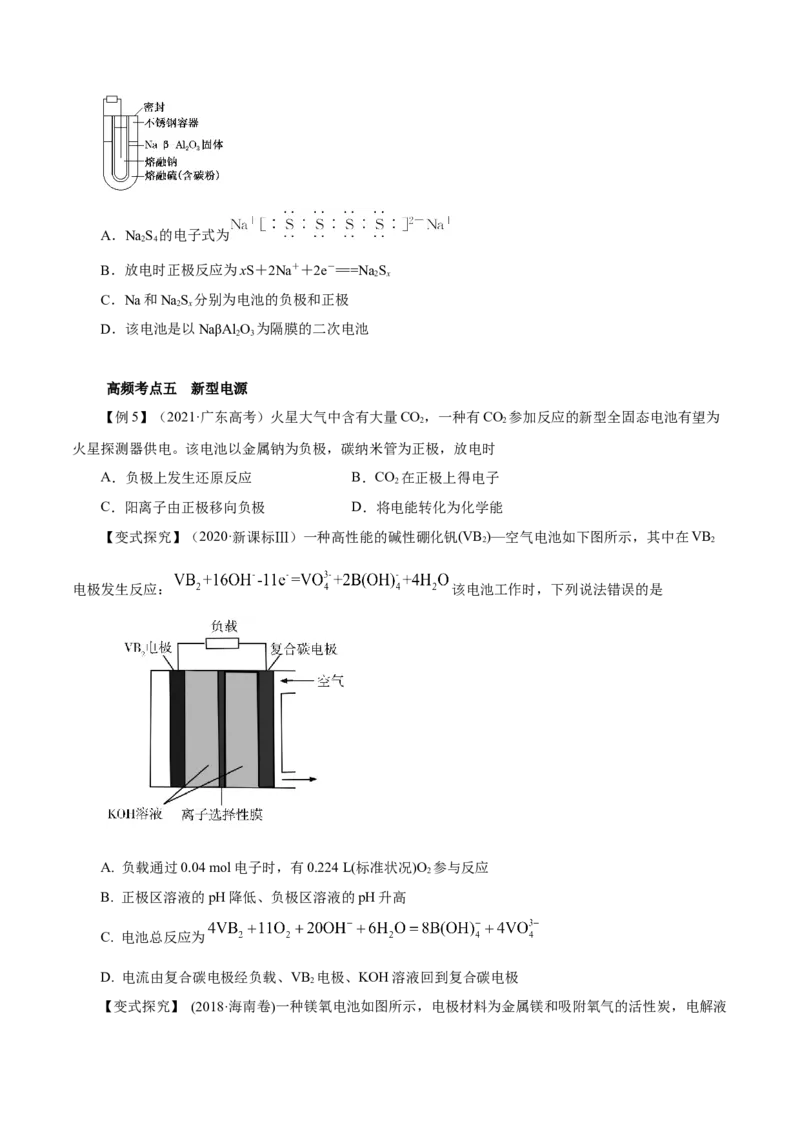
【变式探究】(2020·天津等级考)熔融钠—硫电池性能优良,是具有应用前景的储能电池。下图中的电
池反应为2Na+xS NaS(x=5~3,难溶于熔融硫)。下列说法错误的是( )
2 xA.NaS 的电子式为
2 4
B.放电时正极反应为xS+2Na++2e-===Na S
2 x
C.Na和NaS 分别为电池的负极和正极
2 x
D.该电池是以NaβAl O 为隔膜的二次电池
2 3
高频考点五 新型电源
【例5】(2021·广东高考)火星大气中含有大量CO,一种有CO 参加反应的新型全固态电池有望为
2 2
火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
A.负极上发生还原反应 B.CO 在正极上得电子
2
C.阳离子由正极移向负极 D.将电能转化为化学能
【变式探究】(2020·新课标Ⅲ)一种高性能的碱性硼化钒(VB )—空气电池如下图所示,其中在VB
2 2
电极发生反应: 该电池工作时,下列说法错误的是
A. 负载通过0.04 mol电子时,有0.224 L(标准状况)O 参与反应
2
B. 正极区溶液的pH降低、负极区溶液的pH升高
C. 电池总反应为
D. 电流由复合碳电极经负载、VB 电极、KOH溶液回到复合碳电极
2
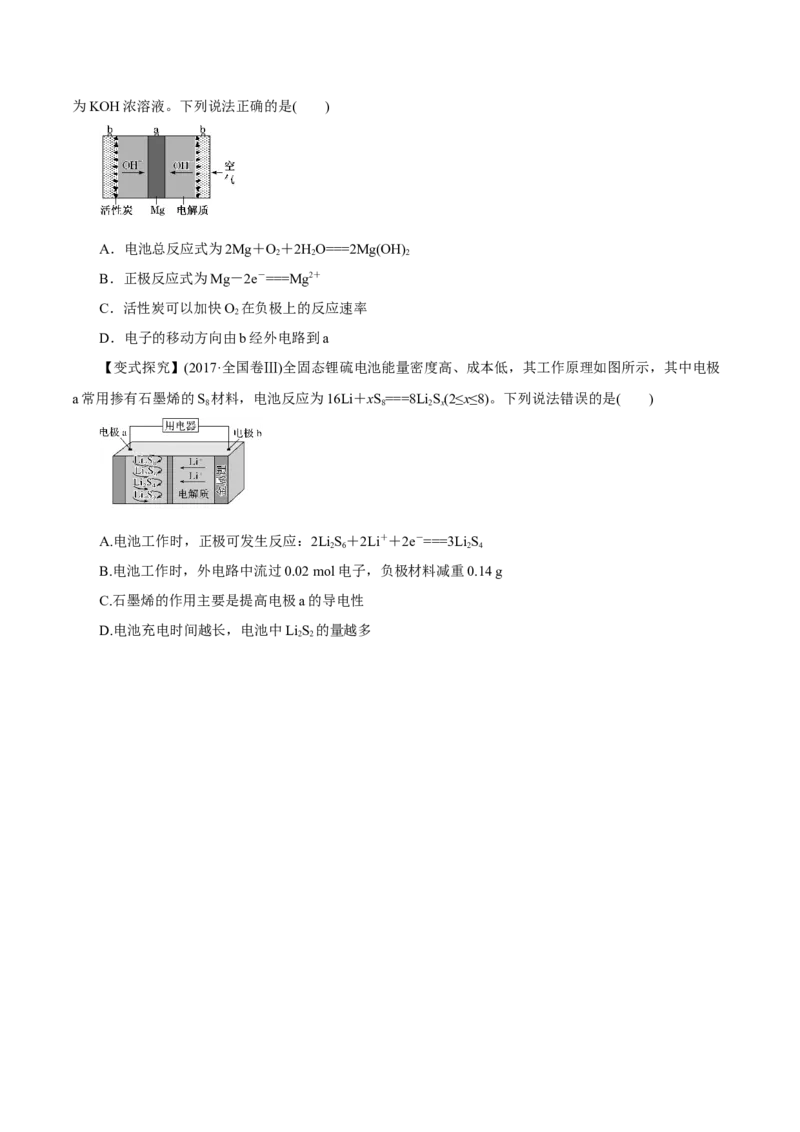
【变式探究】 (2018·海南卷)一种镁氧电池如图所示,电极材料为金属镁和吸附氧气的活性炭,电解液为KOH浓溶液。下列说法正确的是( )
A.电池总反应式为2Mg+O+2HO===2Mg(OH)
2 2 2
B.正极反应式为Mg-2e-===Mg2+
C.活性炭可以加快O 在负极上的反应速率
2
D.电子的移动方向由b经外电路到a
【变式探究】(2017·全国卷Ⅲ)全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极
a常用掺有石墨烯的S 材料,电池反应为16Li+xS===8LiS(2≤x≤8)。下列说法错误的是( )
8 8 2 x
A.电池工作时,正极可发生反应:2LiS+2Li++2e-===3LiS
2 6 2 4
B.电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g
C.石墨烯的作用主要是提高电极a的导电性
D.电池充电时间越长,电池中LiS 的量越多
2 2