文档内容
第 17 讲 电解池 金属的腐蚀与防护
1.港珠澳大桥设计寿命为120年,对桥体钢制构件采用了多种防腐措施,下列防腐措施错误的是(
)
A.用导线与石墨相连
B.用导线与电源负极相连
C.钢制构件上焊接锌块
D.表面喷涂分子涂层
【答案】A
【解析】A项,石墨、Fe和电解质溶液构成原电池,Fe作负极加速被腐蚀,错误;B项,将铁和电源
负极相连时,Fe作阴极而被保护,正确;C项,为牺牲阳极法,正确;D项,为增加防护层,正确。
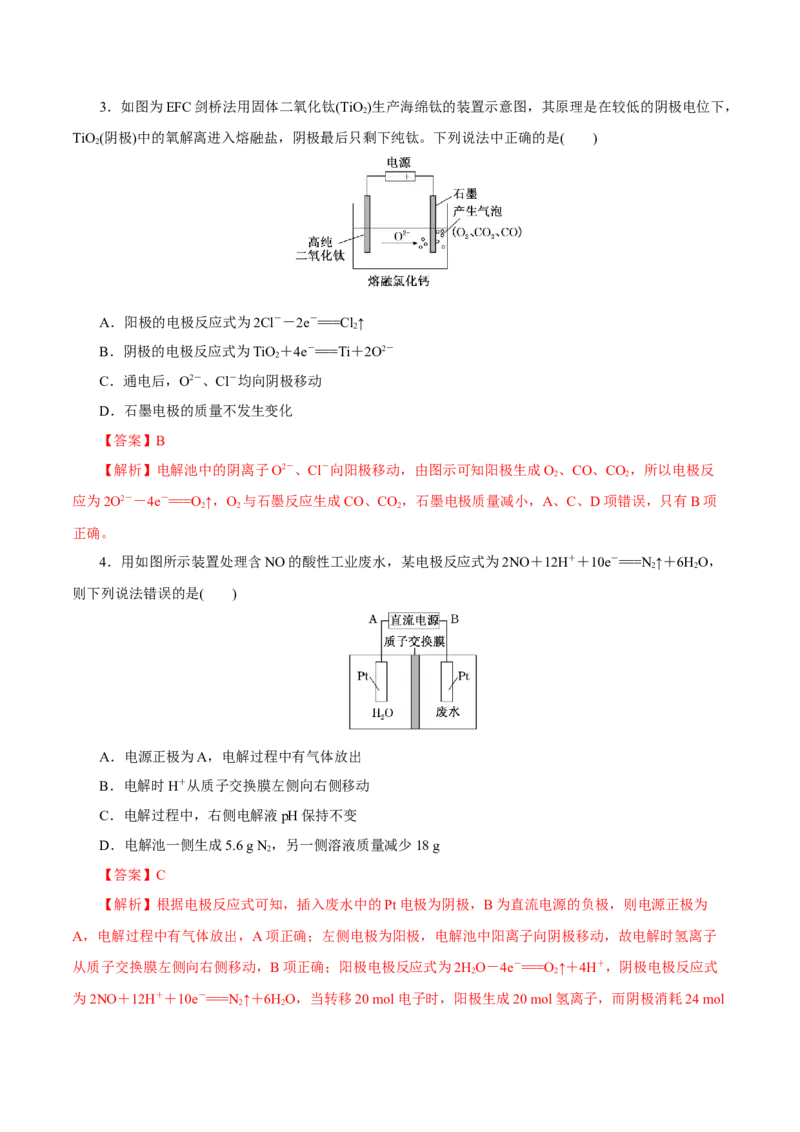
2.如图所示,各烧杯中盛有海水,铁在其中被腐蚀的速度由快到慢的顺序为( )
A.②①③④⑤⑥ B.⑤④③①②⑥
C.⑤④②①③⑥ D.⑤③②④①⑥
【答案】C
【解析】①是化学腐蚀;②③④均为原电池,③中Fe为正极,被保护;②④中Fe为负极,均被腐蚀,
但Fe和Cu的金属活动性差别大于Fe和Sn的,故FeCu原电池中Fe被腐蚀的较快;⑤是Fe接电源正极作
阳极,Cu接电源负极作阴极的电解原理腐蚀,Fe的腐蚀最快;⑥是Fe接电源负极作阴极,Cu接电源正极
作阳极的电解原理腐蚀,Fe的腐蚀最慢。根据以上分析可知铁在其中被腐蚀的速度由快到慢的顺序为⑤④②①③⑥。
3.四个电解装置都以Pt作电极,它们分别装有如下电解质溶液,电解一段时间后,测定其pH变化,
所记录的结果正确的是( )
选项 A B C D
电解质溶液 HCl AgNO KOH BaCl
3 2
pH变化 减小 增大 增大 不变
【答案】C
【解析】电解盐酸,溶质HCl的量减少,溶剂的量不变,所以酸性减弱,pH增大,A项错误;电解硝
酸银溶液生成硝酸、金属银和氧气,溶液酸性增强,pH减小,B项错误;电解氢氧化钾溶液的实质是电解
水,溶质的量不变,溶剂的量减少,溶液碱性增强,pH增大,C项正确;电解氯化钡溶液得到氢氧化钡、
氢气和氯气,溶液碱性增强,pH增大,D项错误。
4.利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产。下列说法中正
确的是( )
A.氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠
B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO
4
C.电镀工业中,X是待镀金属,Y是镀层金属
D.外加电流法中,Y是待保护金属
【答案】D
【解析】根据图像可知,X为阳极,Y为阴极,电解饱和食盐水时,阴极区得到H 和NaOH,所以Y
2
附近的得到氢氧化钠,故A错误;铜的电解精炼,应用粗铜作阳极、纯铜作阴极,所以X是粗铜,Y是纯
铜,故B错误;电镀时,应以镀层金属作阳极、待镀金属作阴极,所以X是镀层金属,Y是待镀金属,故
C错误。
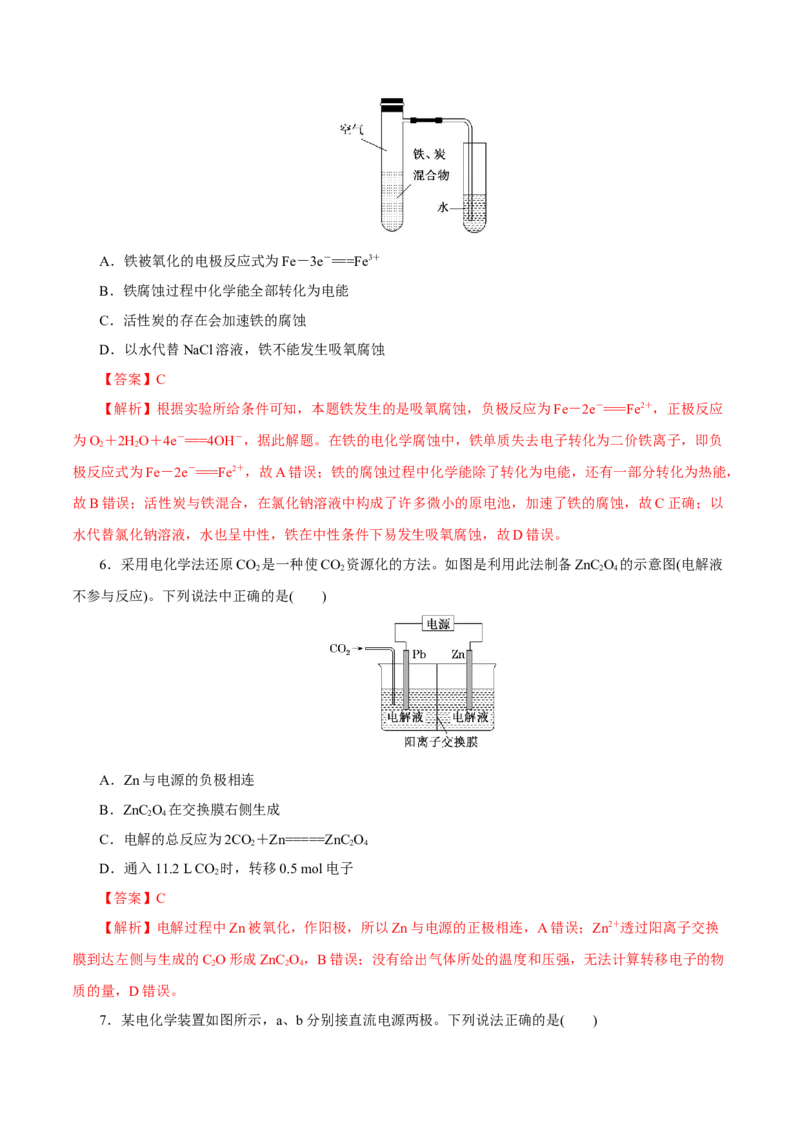
5.将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。
下列有关该实验的说法正确的是( )A.铁被氧化的电极反应式为Fe-3e-===Fe3+
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以水代替NaCl溶液,铁不能发生吸氧腐蚀
【答案】C
【解析】根据实验所给条件可知,本题铁发生的是吸氧腐蚀,负极反应为Fe-2e-===Fe2+,正极反应
为O+2HO+4e-===4OH-,据此解题。在铁的电化学腐蚀中,铁单质失去电子转化为二价铁离子,即负
2 2
极反应式为Fe-2e-===Fe2+,故A错误;铁的腐蚀过程中化学能除了转化为电能,还有一部分转化为热能,
故B错误;活性炭与铁混合,在氯化钠溶液中构成了许多微小的原电池,加速了铁的腐蚀,故C正确;以
水代替氯化钠溶液,水也呈中性,铁在中性条件下易发生吸氧腐蚀,故D错误。
6.采用电化学法还原CO 是一种使CO 资源化的方法。如图是利用此法制备ZnC O 的示意图(电解液
2 2 2 4
不参与反应)。下列说法中正确的是( )
A.Zn与电源的负极相连
B.ZnC O 在交换膜右侧生成
2 4
C.电解的总反应为2CO+Zn=====ZnC O
2 2 4
D.通入11.2 L CO 时,转移0.5 mol电子
2
【答案】C
【解析】电解过程中Zn被氧化,作阳极,所以Zn与电源的正极相连,A错误;Zn2+透过阳离子交换
膜到达左侧与生成的C O形成ZnC O,B错误;没有给出气体所处的温度和压强,无法计算转移电子的物
2 2 4
质的量,D错误。
7.某电化学装置如图所示,a、b分别接直流电源两极。下列说法正确的是( )A.溶液中电子从B极移向A极
B.若B为粗铜,A为精铜,则溶液中c(Cu2+)保持不变
C.若A、B均为石墨电极,则通电一段时间后,溶液pH增大
D.若B为粗铜,A为精铜,则A、B两极转移的电子数相等
【答案】D
【解析】电解质溶液通过离子移动导电,电解质溶液中没有电子移动,故A错误;若B为粗铜,A为
精铜,电解质溶液是硫酸铜溶液,该装置为电解精炼铜装置,溶液中c(Cu2+)略减小,故B错误;若A、B
均为石墨电极,电解总反应式为2CuSO +2HO=====2Cu+O↑+2HSO ,则通电一段时间后,溶液pH减
4 2 2 2 4
小,故C错误;根据电子守恒,阴极、阳极转移电子数一定相等,若B为粗铜,A为精铜,则A、B两极
转移的电子数相等,故D正确。
8.用惰性电极电解一定浓度的CuSO 溶液时,通电一段时间后,向所得的溶液中加入0.1 mol
4
Cu (OH) CO 后恰好恢复到电解前的浓度和pH(不考虑二氧化碳的溶解)。则电解过程中转移电子的物质的
2 2 3
量为( )
A.0.4 mol B.0.5 mol
C.0.6 mol D.0.8 mol
【答案】C
【解析】电解硫酸铜溶液时,开始发生反应:2CuSO +2HO=====2Cu+O↑+2HSO ,后来发生反应:
4 2 2 2 4
2HO=====2H↑+O↑。如果只按照第一阶段的电解,反应后只需要加入氧化铜或碳酸铜即可恢复原电解
2 2 2
质溶液,而题目中加入的是0.1 mol碱式碳酸铜,相当于加入了0.2 mol氧化铜和0.1 mol水,而0.1 mol水
是第二阶段的反应所消耗的,该阶段转移了0.2 mol电子,第一阶段转移了0.4 mol电子,即一共转移了0.6
mol电子,C项正确。
9.一种电化学制备NH 的装置如图所示,图中陶瓷在高温时可以传输H+。下列叙述错误的是( )
3A.Pd电极b为阴极
B.阴极的反应式为N+6H++6e-===2NH
2 3
C.H+由阳极向阴极迁移
D.陶瓷可以隔离N 和H
2 2
【答案】A
【解析】此装置为电解池,总反应是N+3H2NH ,Pd电极b上发生的反应是氢气失去电子,氢
2 2 3
元素的化合价升高,Pd电极b为阳极,故A说法错误;根据A选项分析,Pd电极a为阴极,反应式为N
2
+6H++6e-===2NH,故B说法正确;H+在阴极上与N 反应,则H+由阳极移向阴极,故C说法正确;根
3 2
据装置图,陶瓷可以隔离N 和H,故D说法正确。
2 2
10.载人空间站的生态系统中,要求分离人呼出的二氧化碳,同时需要提供氧气。某电化学装置利用
太阳能转化的电能可以实现上述要求,同时还有燃料一氧化碳生成,该电化学装置中得电子的电极发生的
反应是2CO+4e-+2HO===2CO+4OH-。下列判断错误的是( )
2 2
A.上述电化学装置相当于电解池
B.上述装置进行的总反应式为2CO===2CO+O
2 2
C.反应结束后该电化学装置中的电解质溶液碱性增强
D.失电子的电极发生的反应是4OH--4e-===2H O+O↑
2 2
【答案】C
【解析】该电化学装置是利用电能转化为化学能,符合电解池原理,所以上述电化学装置相当于电解
池,故A正确;该电池中,阴极电极反应式为2CO+4e-+2HO===2CO+4OH-,阳极上氢氧根离子失电
2 2
子生成氧气,得失电子相同条件下将两个电极反应式相加即得电池总反应式为2CO===2CO+O,故B正
2 2
确;阴极反应生成的OH-在阳极完全反应,电池总反应式为2CO===2CO+O,所以反应结束后该电化学
2 2
装置中的电解质溶液碱性不变,故C错误;阳极上氢氧根离子失电子生成氧气供给呼吸,电极反应式为
4OH--4e-===2H O+O↑,故D正确。
2 21.如图所示,x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无味的气体
放出,符合这一情况的是( )
选项 a极板 b极板 x电极 z溶液
A 锌 石墨 负极 CuSO
4
B 石墨 石墨 负极 NaOH
C 银 铁 正极 AgNO
3
D 铜 石墨 负极 CuCl
2
【答案】A
【解析】由题意知a极板质量增加,a应为阴极,则b为阳极,x为电源负极,y为电源正极,参考各
个选项知,A项符合,电解时,a极板有Cu附着,b极板有O 放出;B项不符合,电解时a极板无质量变
2
化;C项不符合,阳极为Fe,为活性电极,电解时Fe在阳极放电溶解,无气体生成;D项不符合,电解时,
Cl-在阳极放电生成Cl,Cl 为黄绿色有刺激气味的气体。
2 2
2.将两个铂电极插入500 mL CuSO 溶液中进行电解,通电一定时间后,某一电极增重0.064 g(设电解
4
时该电极无氢气析出,且不考虑水解和溶液体积变化),此时溶液中氢离子浓度约为( )
A.4×10-3 mol·L-1
B.2×10-3 mol·L-1
C.1×10-3 mol·L-1
D.1×10-7 mol·L-1
【答案】A
【解析】根据电解规律可知,阴极反应:Cu2++2e-===Cu,增重0.064 g,应是Cu的质量,设溶液中
H+的物质的量为x;根据总反应式:
2Cu2++2HO=====2Cu+O↑+4H+
2 2
2×64 g 4 mol
0.064 g x
解得x=0.002 mol,溶液中c(H+)==4×10-3 mol·L-1。3.如图为EFC剑桥法用固体二氧化钛(TiO )生产海绵钛的装置示意图,其原理是在较低的阴极电位下,
2
TiO (阴极)中的氧解离进入熔融盐,阴极最后只剩下纯钛。下列说法中正确的是( )
2
A.阳极的电极反应式为2Cl--2e-===Cl↑
2
B.阴极的电极反应式为TiO +4e-===Ti+2O2-
2
C.通电后,O2-、Cl-均向阴极移动
D.石墨电极的质量不发生变化
【答案】B
【解析】电解池中的阴离子O2-、Cl-向阳极移动,由图示可知阳极生成O、CO、CO,所以电极反
2 2
应为2O2--4e-===O ↑,O 与石墨反应生成CO、CO,石墨电极质量减小,A、C、D项错误,只有B项
2 2 2
正确。
4.用如图所示装置处理含NO的酸性工业废水,某电极反应式为2NO+12H++10e-===N ↑+6HO,
2 2
则下列说法错误的是( )
A.电源正极为A,电解过程中有气体放出
B.电解时H+从质子交换膜左侧向右侧移动
C.电解过程中,右侧电解液pH保持不变
D.电解池一侧生成5.6 g N ,另一侧溶液质量减少18 g
2
【答案】C
【解析】根据电极反应式可知,插入废水中的Pt电极为阴极,B为直流电源的负极,则电源正极为
A,电解过程中有气体放出,A项正确;左侧电极为阳极,电解池中阳离子向阴极移动,故电解时氢离子
从质子交换膜左侧向右侧移动,B项正确;阳极电极反应式为2HO-4e-===O ↑+4H+,阴极电极反应式
2 2
为2NO+12H++10e-===N ↑+6HO,当转移20 mol电子时,阳极生成20 mol氢离子,而阴极消耗24 mol
2 2氢离子,氢离子浓度减小,故右侧电解液pH增大,C项错误;根据电极反应式,阳极电极反应式为2HO
2
-4e-===O ↑+4H+,阴极电极反应式为2NO+12H++10e-===N ↑+6HO,电解池阴极生成5.6 g N ,转
2 2 2 2
移电子的物质的量为×10=2 mol,当转移2 mol电子时,阳极有0.5 mol O(即16 g)逸出,有2 mol H+(即2
2
g)通过质子交换膜进入右侧溶液,则左侧溶液质量减少18 g,D项正确。
5.研究电化学腐蚀及防护的装置如图所示。下列有关说法错误的是( )
A.d 为石墨,铁片腐蚀加快
B.d为石墨,石墨上电极反应为O+2HO+4e-===4OH-
2 2
C.d为锌块,铁片不易被腐蚀
D.d为锌块,铁片上电极反应为2H++2e-===H ↑
2
【答案】D
【解析】A项,由于活动性:Fe>石墨,所以铁、石墨及海水构成原电池,Fe为负极,失去电子被氧
化变为Fe2+进入溶液,溶解在海水中的氧气在正极石墨上得到电子被还原,比没有形成原电池时铁片的腐
蚀速率快,正确;B项,d为石墨,由于是中性电解质,所以发生的是吸氧腐蚀,石墨上氧气得到电子,
发生还原反应,电极反应为O+2HO+4e-===4OH-,正确;C项,若d为锌块,则由于金属活动性:
2 2
Zn>Fe,Zn为原电池的负极,Fe为正极,首先被腐蚀的是Zn,铁得到保护,铁片不易被腐蚀,正确;D项,
d为锌块,由于电解质为中性环境,发生的是吸氧腐蚀,铁片上电极反应为O+2HO+4e-===4OH-,错
2 2
误。
6.利用电解法将CO 转化为CH 的原理如图所示。下列说法正确的是( )
2 4
A.电解过程中,H+由a极区向b极区迁移
B.电极b上反应为CO+8HCO-8e-===CH +CO+2HO
2 4 2
C.电解过程中化学能转化为电能
D.电解时NaSO 溶液浓度保持不变
2 4【答案】A
【解析】通过电解法可知此装置为电解池,由a极生成O 可以判断出a极为阳极,则b极为阴极,阳
2
离子向阴极流动,电极a上反应为2HO-4e-===4H++O↑,电极b上反应为CO+8HCO+8e-===CH +
2 2 2 4
8CO+2HO。由a极生成O 可以判断出a极为阳极,b极为阴极,阳离子向阴极流动,则H+由a极区向b
2 2
极区迁移,故A正确;电极方程式配平发生错误,电极b上反应应为CO+8HCO+8e-===CH +8CO+
2 4
2HO,故B错误;通过电解法可知此装置为电解池,所以电解过程中电能转化为化学能,故C错误;电解
2
时OH-比SO更容易失去电子,所以电解NaSO 溶液的实质是电解水,溶液中的水发生消耗,所以NaSO
2 4 2 4
溶液的浓度是增大的,故D错误。
7.三室式电渗析法处理含NH NO 废水的原理如图所示,在直流电源的作用下,两膜中间的NH和
4 3
NO可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。工作一段时间后,在两极区均得到
副产品NH NO 。下列叙述正确的是( )
4 3
A.a极为电源负极,b极为电源正极
B.c膜是阴离子交换膜,d膜是阳离子交换膜
C.阴极电极反应式为2NO+12H++10e-===N ↑+6HO
2 2
D.当电路中通过2 mol电子的电量时,阳极产生标准状况下的O 5.6 L
2
【答案】A
【解析】根据题意两极均得到副产物NH NO ,可知Ⅱ室废水中的NH移向Ⅰ室、NO移向Ⅲ室,根据
4 3
电解过程中离子的移动原理,可知Ⅰ室石墨电极为阴极、Ⅲ室石墨电极为阳极。阴极所连的a极为电源负
极,b极为电源正极,A项正确;c膜通过的是NH,故c膜应为阳离子交换膜,同理可知d膜为阴离子交
换膜,B项错误;阴极上H+得电子生成氢气,C项错误;阳极上OH-失电子生成氧气,反应式为4OH--
4e-===O ↑+2HO,当电路中通过1 mol电子的电量时,阳极产生标准状态下的O 体积为5.6 L,D项错误。
2 2 2
8.HBO 可以通过电解NaB(OH) 溶液的方法制备,其工作原理如图。下列叙述错误的是( )
3 3 4A.M室发生的电极反应式为2HO-4e-===O ↑+4H+
2 2
B.N室中:a%