文档内容
[复习目标] 1.掌握速率、平衡图像的分析方法及类型。2.掌握实际工业生产中的陌生图像
的分析方法。
1.(2022·全国甲卷,28)金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前
生产钛的方法之一是将金红石(TiO)转化为TiCl ,再进一步还原得到钛。回答下列问题:
2 4
(1)TiO 转化为TiCl 有直接氯化法和碳氯化法。在1 000 ℃时反应的热化学方程式及其平衡
2 4
常数如下:
(ⅰ)直接氯化:TiO(s)+2Cl(g)===TiCl (g)+O(g) ΔH=+172 kJ·mol-1,K =1.0×10-2
2 2 4 2 1 p1
(ⅱ)碳氯化:TiO(s)+2Cl(g)+2C(s)===TiCl (g)+2CO(g) ΔH =-51 kJ·mol-1,K =
2 2 4 2 p2
1.2×1012 Pa
①反应2C(s)+O(g)===2CO(g)的ΔH为________ kJ·mol-1,K =__________Pa。
2 p
②碳氯化的反应趋势远大于直接氯化,其原因是__________________________________。
③对于碳氯化反应:增大压强,平衡________移动(填“向左”“向右”或“不”);温度升
高,平衡转化率________(填“变大”“变小”或“不变”)。
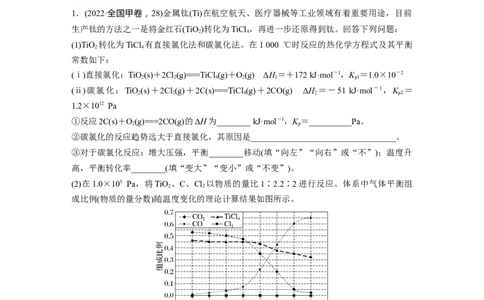
(2)在1.0×105 Pa,将TiO 、C、Cl 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组
2 2
成比例(物质的量分数)随温度变化的理论计算结果如图所示。
①反应C(s)+CO(g)===2CO(g)的平衡常数K (1 400 ℃)=__________Pa。
2 p
②图中显示,在200 ℃平衡时TiO 几乎完全转化为TiCl ,但实际生产中反应温度却远高于
2 4
此温度,其原因是___________________________________________________________
________________________________________________________________________。
(3)TiO 碳氯化是一个“气-固-固”反应,有利于 TiO-C“固-固”接触的措施是
2 2
________________________________________________________________________
________________________________________________________________________。2.[2019·北京,27(1)]氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
甲烷水蒸气催化重整是制高纯氢的方法之一。
①反应器中初始反应的生成物为H 和CO ,其物质的量之比为4∶1,甲烷和水蒸气反应的
2 2
方程式是________________________________________________________________________
________________________________________________________________________。
②已知反应器中还存在如下反应:
ⅰ.CH (g)+HO(g)===CO(g)+3H(g) ΔH
4 2 2 1
ⅱ.CO(g)+HO(g)===CO(g)+H(g) ΔH
2 2 2 2
ⅲ.CH (g)===C(s)+2H(g) ΔH
4 2 3
……
ⅲ为积炭反应,利用ΔH 和ΔH 计算ΔH 时,还需要利用____________________________反
1 2 3
应的ΔH。
③反应物投料比采用 n(H O)∶n(CH)=4∶1,大于初始反应的化学计量数之比,目的是
2 4
________(填字母)。
a.促进CH 转化
4
b.促进CO转化为CO
2
c.减少积炭生成
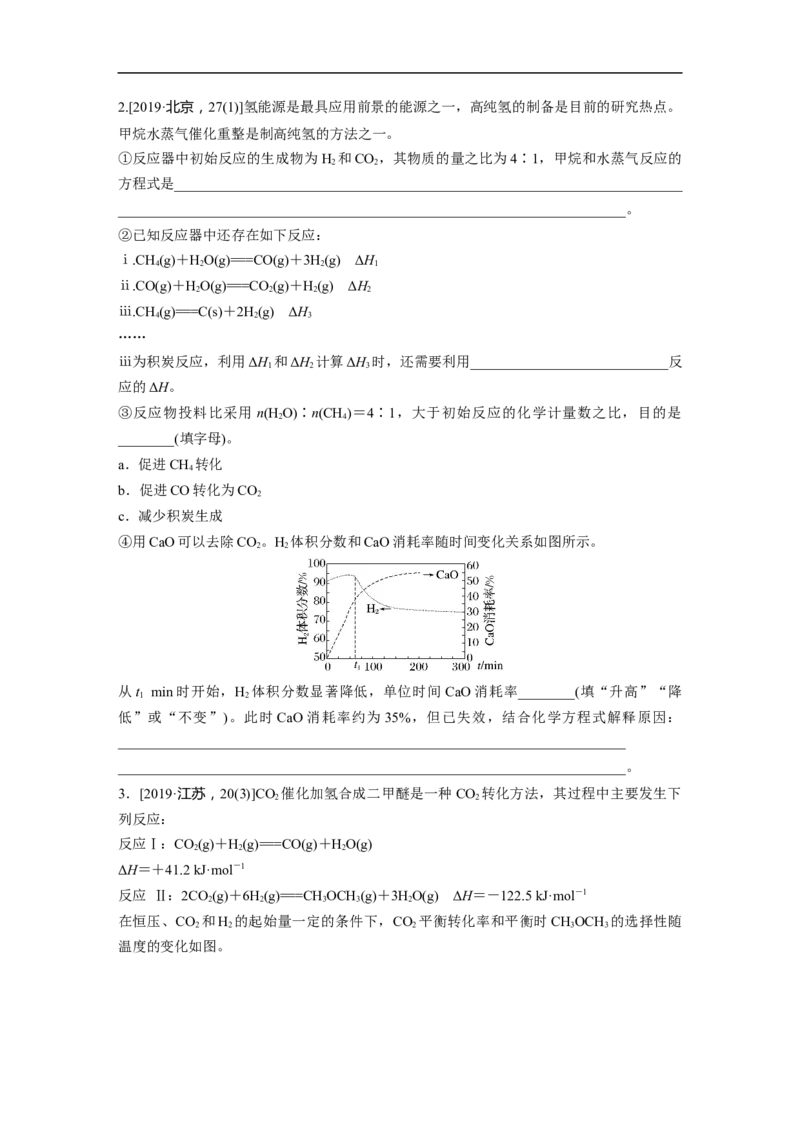
④用CaO可以去除CO。H 体积分数和CaO消耗率随时间变化关系如图所示。
2 2
从t min时开始,H 体积分数显著降低,单位时间 CaO消耗率________(填“升高”“降
1 2
低”或“不变”)。此时CaO消耗率约为35%,但已失效,结合化学方程式解释原因:
________________________________________________________________________
________________________________________________________________________。
3.[2019·江苏,20(3)]CO 催化加氢合成二甲醚是一种CO 转化方法,其过程中主要发生下
2 2
列反应:
反应Ⅰ:CO(g)+H(g)===CO(g)+HO(g)
2 2 2
ΔH=+41.2 kJ·mol-1
反应 Ⅱ:2CO(g)+6H(g)===CHOCH (g)+3HO(g) ΔH=-122.5 kJ·mol-1
2 2 3 3 2
在恒压、CO 和H 的起始量一定的条件下,CO 平衡转化率和平衡时CHOCH 的选择性随
2 2 2 3 3
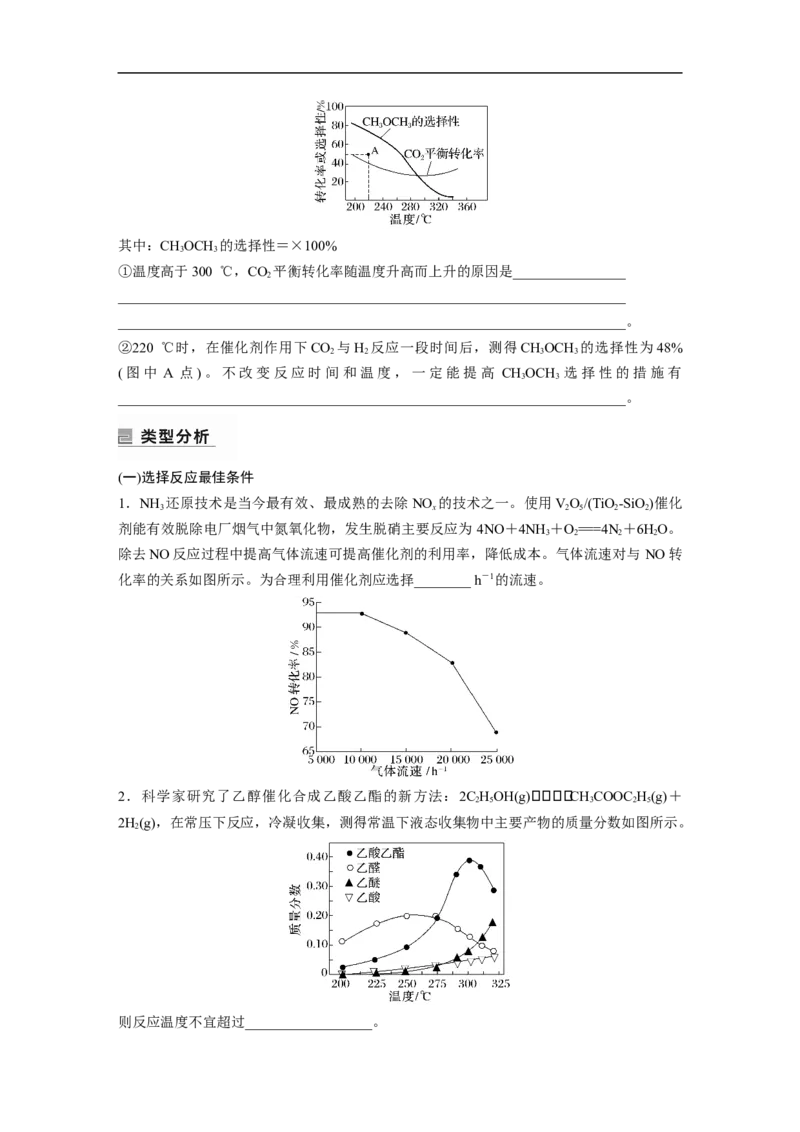
温度的变化如图。其中:CHOCH 的选择性=×100%
3 3
①温度高于300 ℃,CO 平衡转化率随温度升高而上升的原因是________________
2
________________________________________________________________________
________________________________________________________________________。
②220 ℃时,在催化剂作用下CO 与H 反应一段时间后,测得CHOCH 的选择性为48%
2 2 3 3
(图中 A 点)。不改变反应时间和温度,一定能提高 CHOCH 选择性的措施有
3 3
________________________________________________________________________。
(一)选择反应最佳条件
1.NH 还原技术是当今最有效、最成熟的去除NO 的技术之一。使用VO/(TiO -SiO)催化
3 x 2 5 2 2
剂能有效脱除电厂烟气中氮氧化物,发生脱硝主要反应为 4NO+4NH +O===4N +6HO。
3 2 2 2
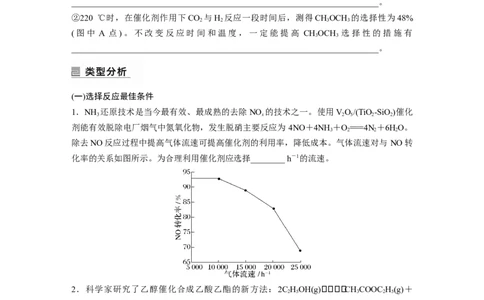
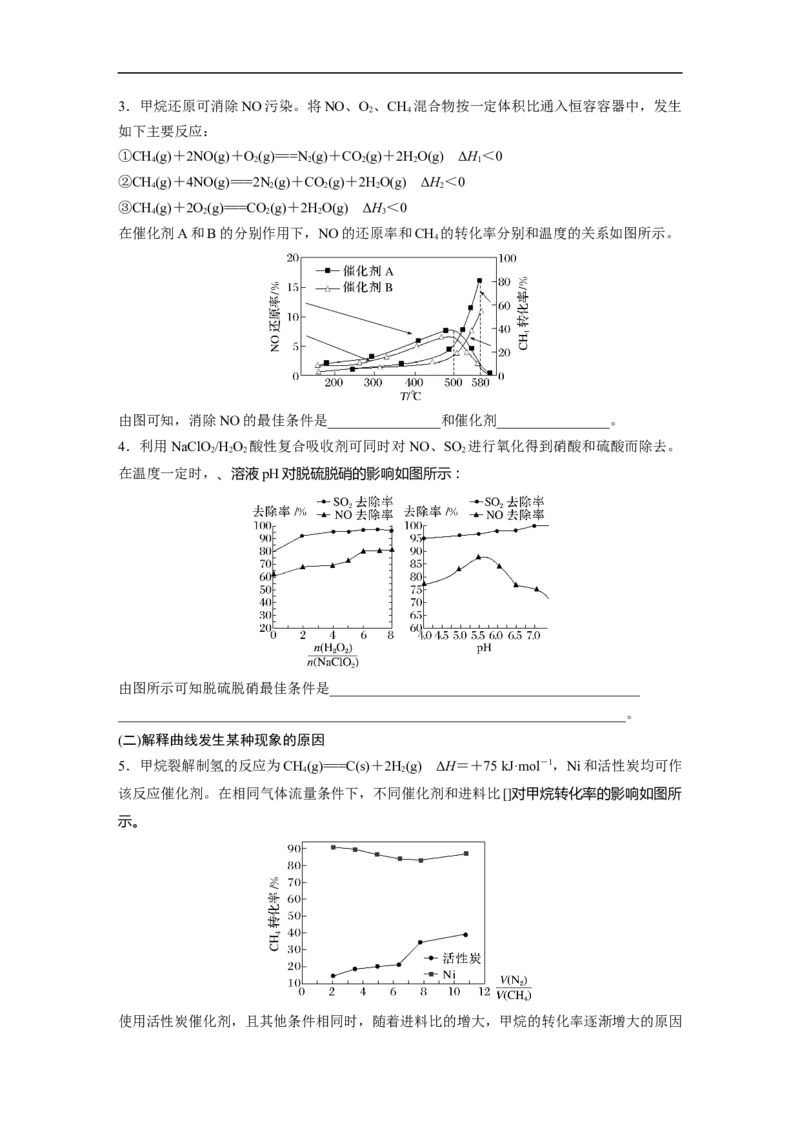
除去NO反应过程中提高气体流速可提高催化剂的利用率,降低成本。气体流速对与 NO转
化率的关系如图所示。为合理利用催化剂应选择________ h-1的流速。
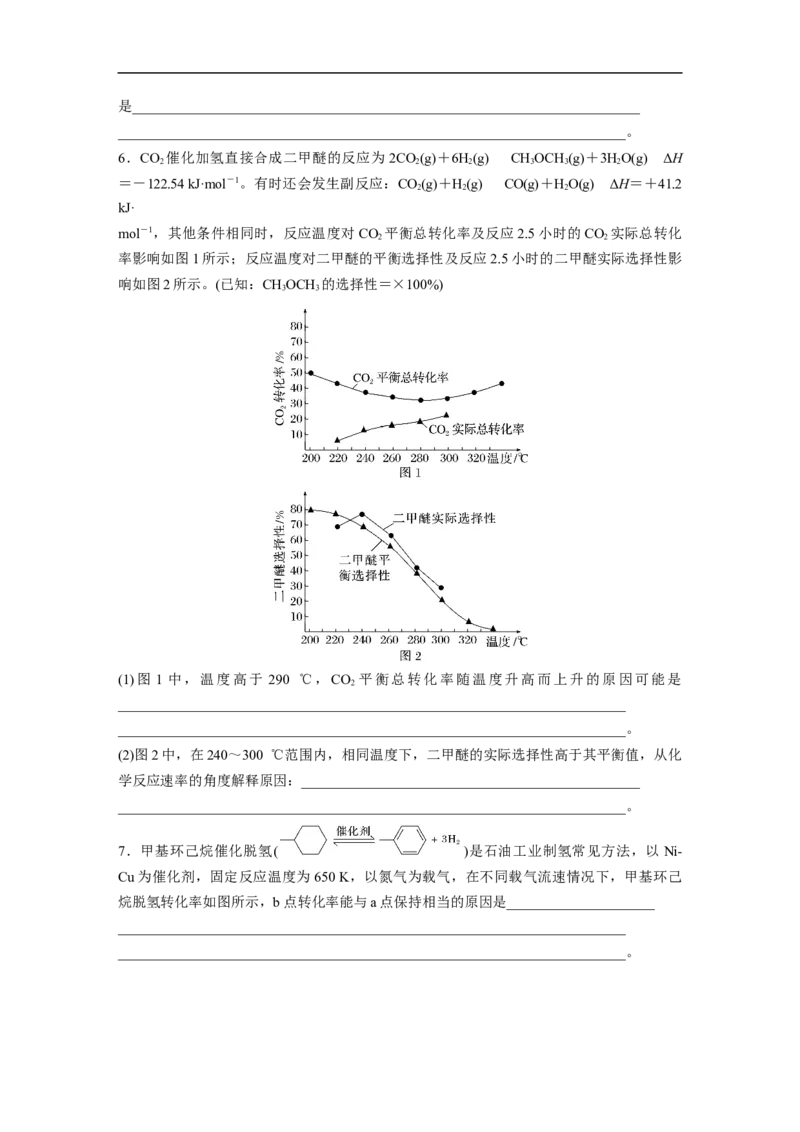
2.科学家研究了乙醇催化合成乙酸乙酯的新方法:2C HOH(g)CHCOOC H(g)+
2 5 3 2 5
2H(g),在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。
2
则反应温度不宜超过__________________。3.甲烷还原可消除NO污染。将NO、O 、CH 混合物按一定体积比通入恒容容器中,发生
2 4
如下主要反应:
①CH(g)+2NO(g)+O(g)===N(g)+CO(g)+2HO(g) ΔH<0
4 2 2 2 2 1
②CH(g)+4NO(g)===2N(g)+CO(g)+2HO(g) ΔH<0
4 2 2 2 2
③CH(g)+2O(g)===CO(g)+2HO(g) ΔH<0
4 2 2 2 3
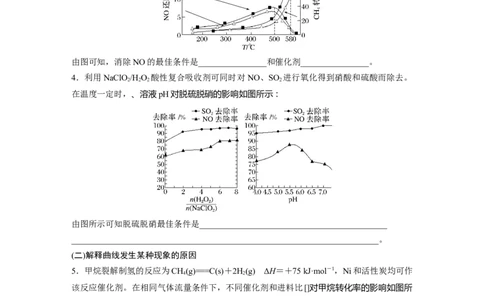
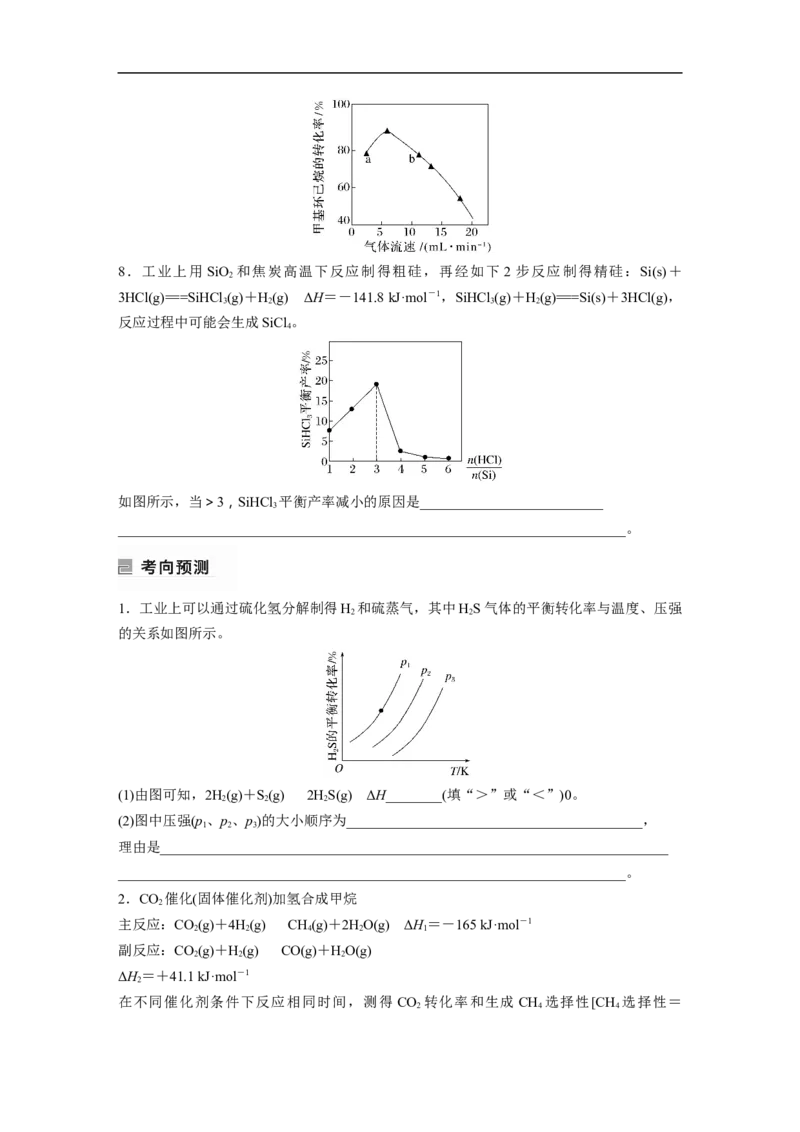
在催化剂A和B的分别作用下,NO的还原率和CH 的转化率分别和温度的关系如图所示。
4
由图可知,消除NO的最佳条件是________________和催化剂________________。
4.利用NaClO/H O 酸性复合吸收剂可同时对NO、SO 进行氧化得到硝酸和硫酸而除去。
2 2 2 2
在温度一定时,、溶液pH对脱硫脱硝的影响如图所示:
由图所示可知脱硫脱硝最佳条件是____________________________________________
________________________________________________________________________。
(二)解释曲线发生某种现象的原因
5.甲烷裂解制氢的反应为CH(g)===C(s)+2H(g) ΔH=+75 kJ·mol-1,Ni和活性炭均可作
4 2
该反应催化剂。在相同气体流量条件下,不同催化剂和进料比[]对甲烷转化率的影响如图所
示。
使用活性炭催化剂,且其他条件相同时,随着进料比的增大,甲烷的转化率逐渐增大的原因是________________________________________________________________________
________________________________________________________________________。
6.CO 催化加氢直接合成二甲醚的反应为 2CO(g)+6H(g)CHOCH (g)+3HO(g) ΔH
2 2 2 3 3 2
=-122.54 kJ·mol-1。有时还会发生副反应:CO(g)+H(g)CO(g)+HO(g) ΔH=+41.2
2 2 2
kJ·
mol-1,其他条件相同时,反应温度对CO 平衡总转化率及反应2.5小时的CO 实际总转化
2 2
率影响如图1所示;反应温度对二甲醚的平衡选择性及反应2.5小时的二甲醚实际选择性影
响如图2所示。(已知:CHOCH 的选择性=×100%)
3 3
(1)图 1 中,温度高于 290 ℃,CO 平衡总转化率随温度升高而上升的原因可能是
2
________________________________________________________________________
________________________________________________________________________。
(2)图2中,在240~300 ℃范围内,相同温度下,二甲醚的实际选择性高于其平衡值,从化
学反应速率的角度解释原因:________________________________________________
________________________________________________________________________。
7.甲基环己烷催化脱氢( )是石油工业制氢常见方法,以 Ni-
Cu为催化剂,固定反应温度为650 K,以氮气为载气,在不同载气流速情况下,甲基环己
烷脱氢转化率如图所示,b点转化率能与a点保持相当的原因是_____________________
________________________________________________________________________
________________________________________________________________________。8.工业上用 SiO 和焦炭高温下反应制得粗硅,再经如下 2 步反应制得精硅:Si(s)+
2
3HCl(g)===SiHCl (g)+H(g) ΔH=-141.8 kJ·mol-1,SiHCl (g)+H(g)===Si(s)+3HCl(g),
3 2 3 2
反应过程中可能会生成SiCl 。
4
如图所示,当>3,SiHCl 平衡产率减小的原因是__________________________
3
________________________________________________________________________。
1.工业上可以通过硫化氢分解制得H 和硫蒸气,其中HS气体的平衡转化率与温度、压强
2 2
的关系如图所示。
(1)由图可知,2H(g)+S(g)2HS(g) ΔH________(填“>”或“<”)0。
2 2 2
(2)图中压强(p、p、p)的大小顺序为__________________________________________,
1 2 3
理由是________________________________________________________________________
________________________________________________________________________。
2.CO 催化(固体催化剂)加氢合成甲烷
2
主反应:CO(g)+4H(g)CH(g)+2HO(g) ΔH=-165 kJ·mol-1
2 2 4 2 1
副反应:CO(g)+H(g)CO(g)+HO(g)
2 2 2
ΔH=+41.1 kJ·mol-1
2
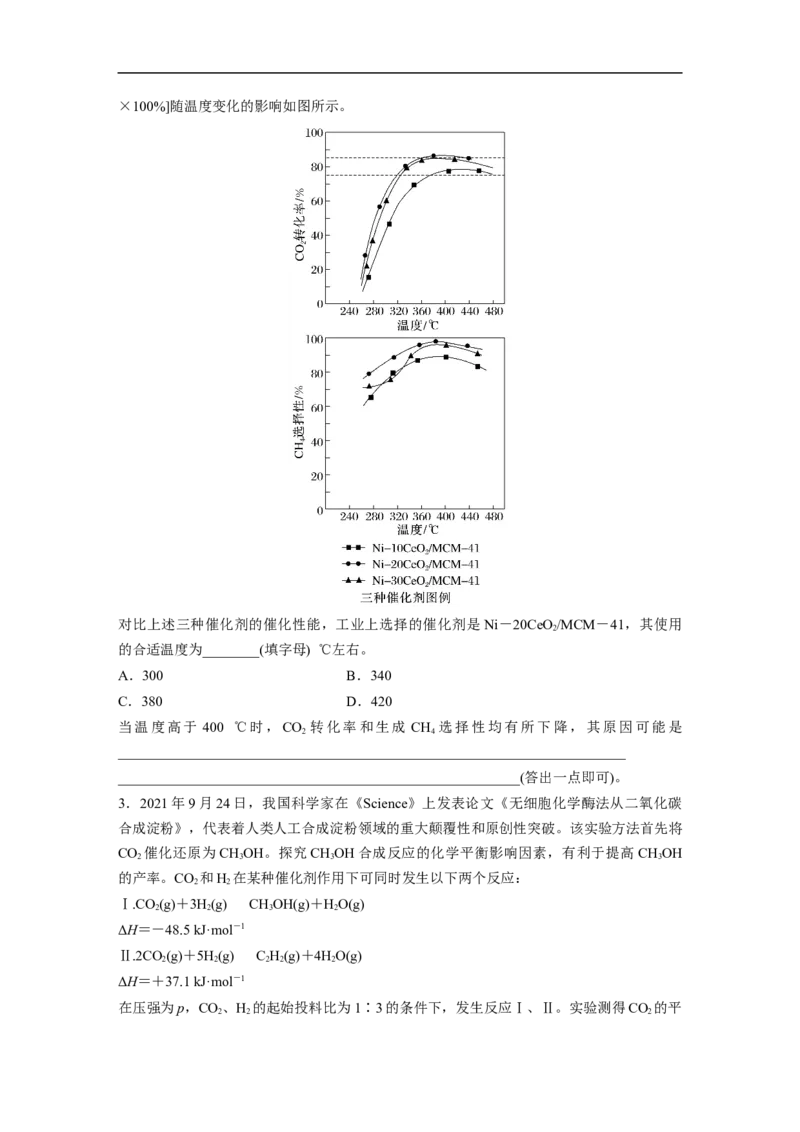
在不同催化剂条件下反应相同时间,测得 CO 转化率和生成 CH 选择性[CH 选择性=
2 4 4×100%]随温度变化的影响如图所示。
对比上述三种催化剂的催化性能,工业上选择的催化剂是Ni-20CeO/MCM-41,其使用
2
的合适温度为________(填字母) ℃左右。
A.300 B.340
C.380 D.420
当温度高于 400 ℃时,CO 转化率和生成 CH 选择性均有所下降,其原因可能是
2 4
________________________________________________________________________
_________________________________________________________(答出一点即可)。
3.2021年9月24日,我国科学家在《Science》上发表论文《无细胞化学酶法从二氧化碳
合成淀粉》,代表着人类人工合成淀粉领域的重大颠覆性和原创性突破。该实验方法首先将
CO 催化还原为CHOH。探究CHOH合成反应的化学平衡影响因素,有利于提高 CHOH
2 3 3 3
的产率。CO 和H 在某种催化剂作用下可同时发生以下两个反应:
2 2
Ⅰ.CO (g)+3H(g)CHOH(g)+HO(g)
2 2 3 2
ΔH=-48.5 kJ·mol-1
Ⅱ.2CO (g)+5H(g)C H(g)+4HO(g)
2 2 2 2 2
ΔH=+37.1 kJ·mol-1
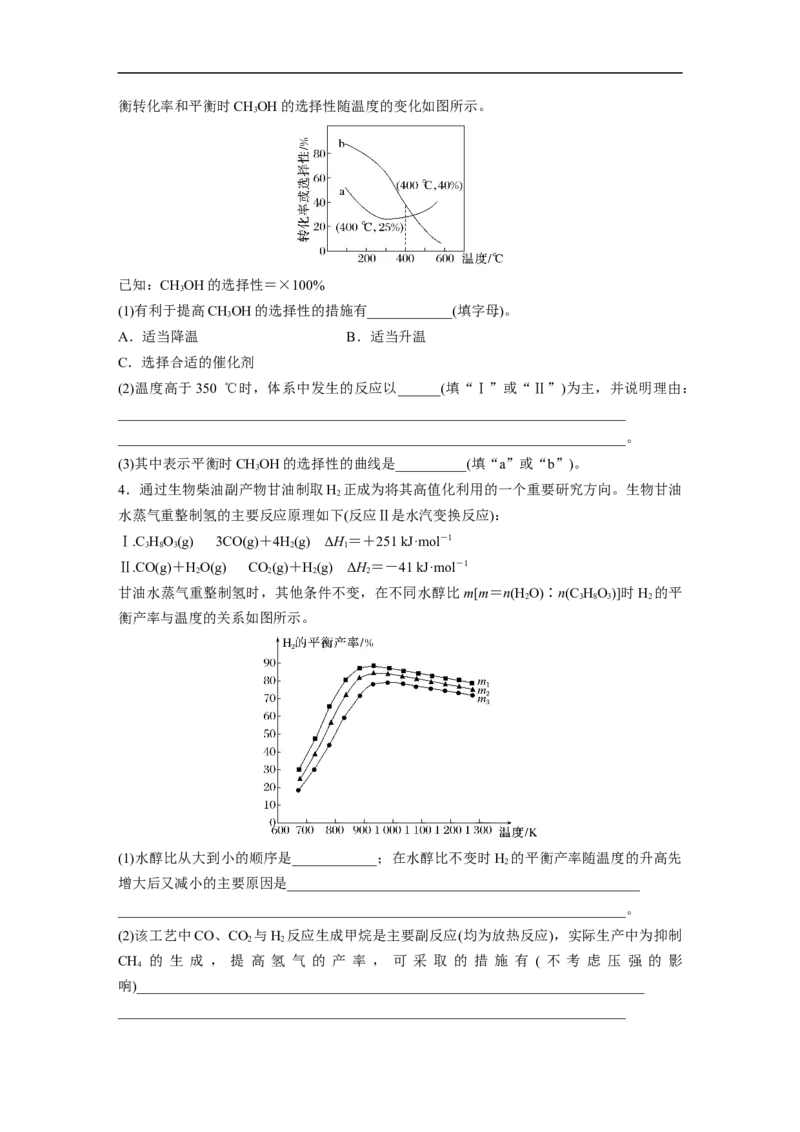
在压强为p,CO、H 的起始投料比为1∶3的条件下,发生反应Ⅰ、Ⅱ。实验测得CO 的平
2 2 2衡转化率和平衡时CHOH的选择性随温度的变化如图所示。
3
已知:CHOH的选择性=×100%
3
(1)有利于提高CHOH的选择性的措施有____________(填字母)。
3
A.适当降温 B.适当升温
C.选择合适的催化剂
(2)温度高于350 ℃时,体系中发生的反应以______(填“Ⅰ”或“Ⅱ”)为主,并说明理由:
________________________________________________________________________
________________________________________________________________________。
(3)其中表示平衡时CHOH的选择性的曲线是__________(填“a”或“b”)。
3
4.通过生物柴油副产物甘油制取H 正成为将其高值化利用的一个重要研究方向。生物甘油
2
水蒸气重整制氢的主要反应原理如下(反应Ⅱ是水汽变换反应):
Ⅰ.C HO(g)3CO(g)+4H(g) ΔH=+251 kJ·mol-1
3 8 3 2 1
Ⅱ.CO(g)+HO(g)CO(g)+H(g) ΔH=-41 kJ·mol-1
2 2 2 2
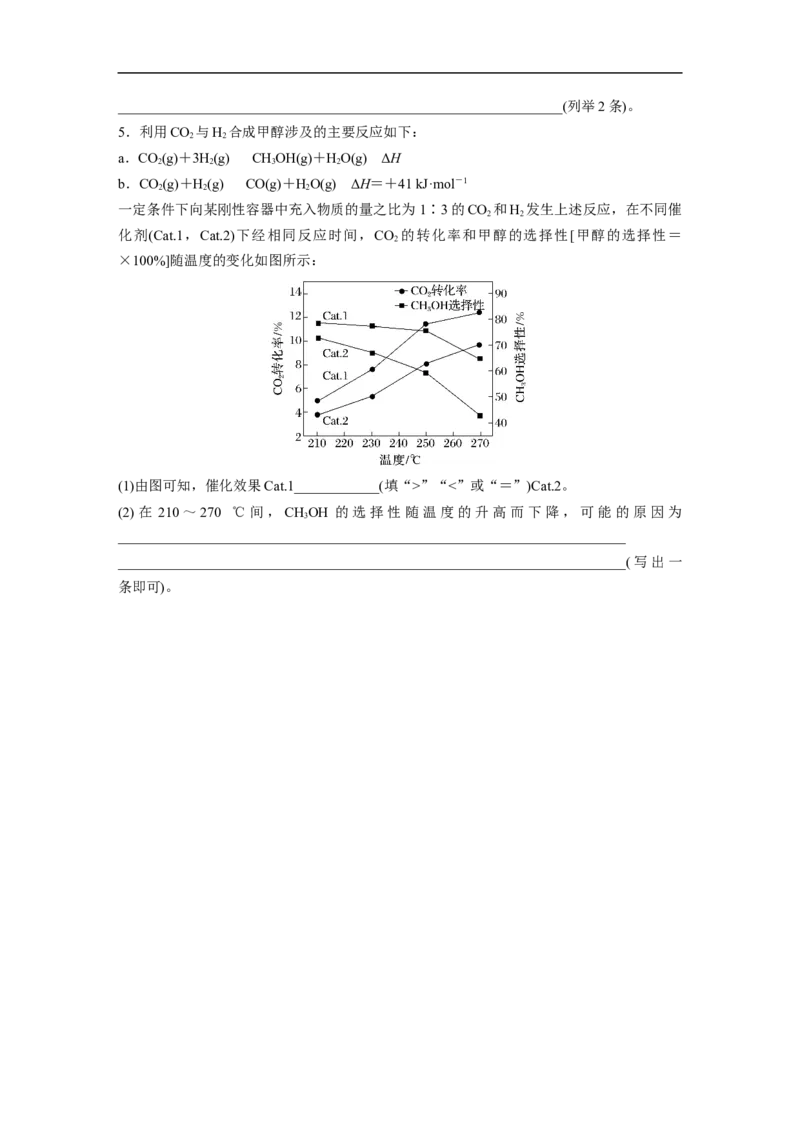
甘油水蒸气重整制氢时,其他条件不变,在不同水醇比m[m=n(H O)∶n(C HO)]时H 的平
2 3 8 3 2
衡产率与温度的关系如图所示。
(1)水醇比从大到小的顺序是____________;在水醇比不变时H 的平衡产率随温度的升高先
2
增大后又减小的主要原因是__________________________________________________
________________________________________________________________________。
(2)该工艺中CO、CO 与H 反应生成甲烷是主要副反应(均为放热反应),实际生产中为抑制
2 2
CH 的 生 成 , 提 高 氢 气 的 产 率 , 可 采 取 的 措 施 有 ( 不 考 虑 压 强 的 影
4
响)________________________________________________________________________
_______________________________________________________________________________________________________________________________________(列举2条)。
5.利用CO 与H 合成甲醇涉及的主要反应如下:
2 2
a.CO(g)+3H(g)CHOH(g)+HO(g) ΔH
2 2 3 2
b.CO(g)+H(g)CO(g)+HO(g) ΔH=+41 kJ·mol-1
2 2 2
一定条件下向某刚性容器中充入物质的量之比为1∶3的CO 和H 发生上述反应,在不同催
2 2
化剂(Cat.1,Cat.2)下经相同反应时间,CO 的转化率和甲醇的选择性[甲醇的选择性=
2
×100%]随温度的变化如图所示:
(1)由图可知,催化效果Cat.1____________(填“>”“<”或“=”)Cat.2。
(2)在 210~270 ℃间,CHOH 的选择性随温度的升高而下降,可能的原因为
3
________________________________________________________________________
________________________________________________________________________(写出一
条即可)。