文档内容
第 27 讲 化学反应速率、平衡图像
目录
考情分析 的关系图像
网络构建 【提升·必考题型归纳】
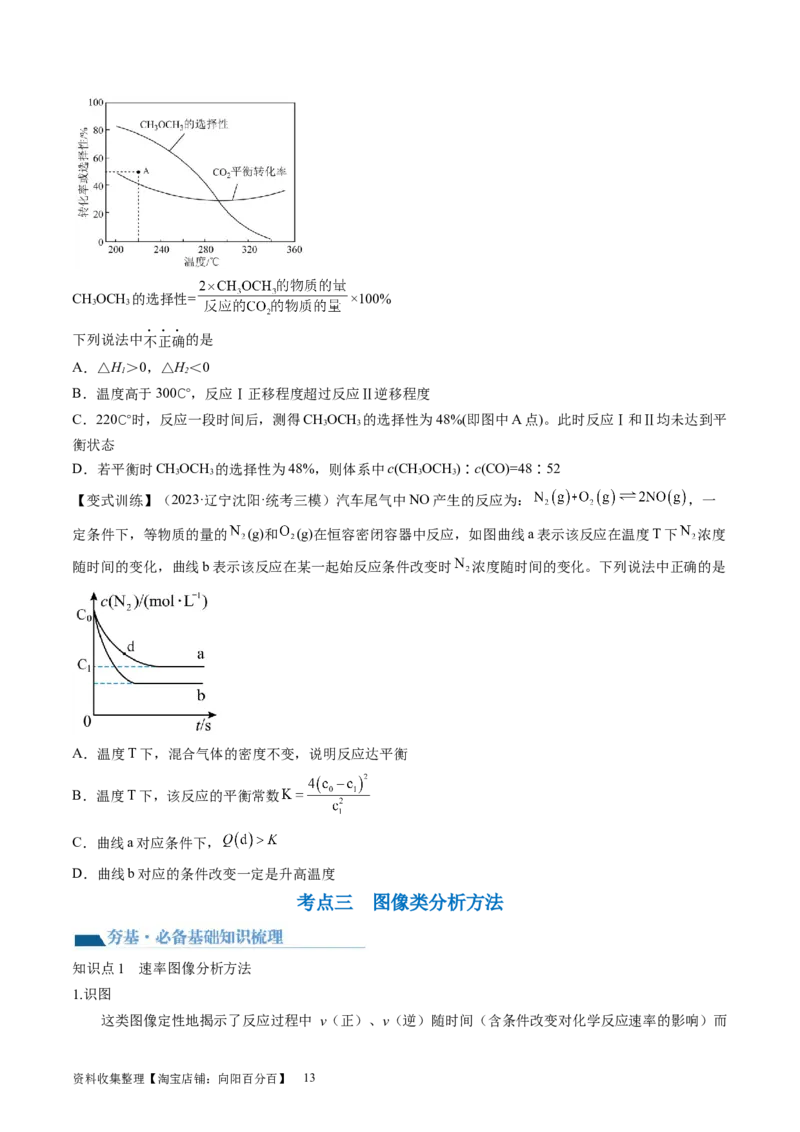
考向1 考查转化率(或百分含量)—时间—温
考点一 速率图像
度(或压强)图像的分析判断
【夯基·必备基础知识梳理】
考向2 考查恒温线或恒压线图像的分析判断
知识点1 速率—时间图像
考向3 考查组分含量或浓度与温度的关系图
知识点2 速率—压强(或温度)图像
像的分析判断
知识点3 物质的量(或浓度)—时间图像
考向4 考查化学平衡曲线外的非平衡点分析
【提升·必考题型归纳】
考向1 考查速率-时间图像
考点三 图像类分析方法
考向2 考查速率—压强(或温度)图像
【夯基·必备基础知识梳理】
考向3 考查浓度或物质的的量-时间图像
知识点1 速率图像分析
考点二 平衡图象
知识点2 平衡图像分析
【夯基·必备基础知识梳理】
【提升·必考题型归纳】
知识点1 转化率(或百分含量)—时间—温度
考向1 考查化学反应速率图像分析
(或压强)图像
考向2 考查化学平衡综合图像分析
知识点2 恒温线或恒压线图像
真题感悟
知识点3 反应过程中组分含量或浓度与温度
考点要求 考题统计 考情分析
分析近三年的高考试题,高考命题在本讲有以下规律:
2023山东卷14题,4分
速率图像 化学反应速率和化学平衡图像分析类试题经常涉及的图像类型有
2022河北卷13题,3分
含量—时间—温度(压强)图像、恒温、恒压曲线等,图像中蕴含
资料收集整理【淘宝店铺:向阳百分百】 1着丰富的信息,具有简明、直观、形象的特点,命题形式灵活,
难度不大,解题的关键是根据反应特点,明确反应条件,认真分
2021辽宁卷12题,3分
析图像,充分挖掘蕴含的信息,紧扣化学原理,找准切入点解决
问题。图像作为一种思维方法在解题过程中也有着重要作用,可
以将一些较为抽象的知识,转化为图像,然后进行解决。注意掌
2023湖南卷13题,4分
握从图像中获取有效信息,解答与化学反应速率和化学平衡有关
平衡图像 2022广东卷13题,4分
的问题,如反应速率、反应转化率、产率,提高转化率的措施
2021江苏卷14题,3分
等;从图表或图像中获取信息,计算转化率、平衡常数等。
资料收集整理【淘宝店铺:向阳百分百】 2考点一 速率图像
知识点1 速率—时间图像
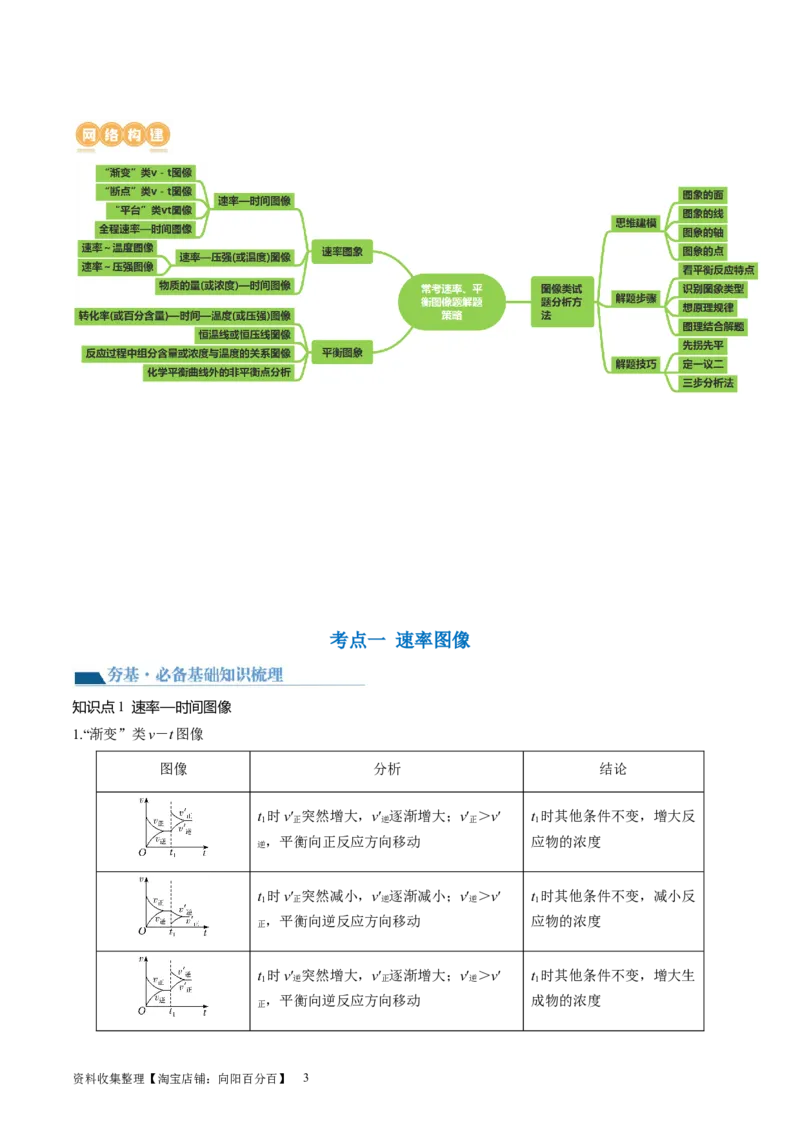
1.“渐变”类v-t图像
图像 分析 结论
t 时v′ 突然增大,v′ 逐渐增大;v′ >v′ t 时其他条件不变,增大反
1 正 逆 正 1
,平衡向正反应方向移动 应物的浓度
逆
t 时v′ 突然减小,v′ 逐渐减小;v′ >v′ t 时其他条件不变,减小反
1 正 逆 逆 1
,平衡向逆反应方向移动 应物的浓度
正
t 时v′ 突然增大,v′ 逐渐增大;v′ >v′ t 时其他条件不变,增大生
1 逆 正 逆 1
,平衡向逆反应方向移动 成物的浓度
正
资料收集整理【淘宝店铺:向阳百分百】 3t 时v′ 突然减小,v′ 逐渐减小;v′ >v′ t 时其他条件不变,减小生
1 逆 正 正 1
,平衡向正反应方向移动 成物的浓度
逆
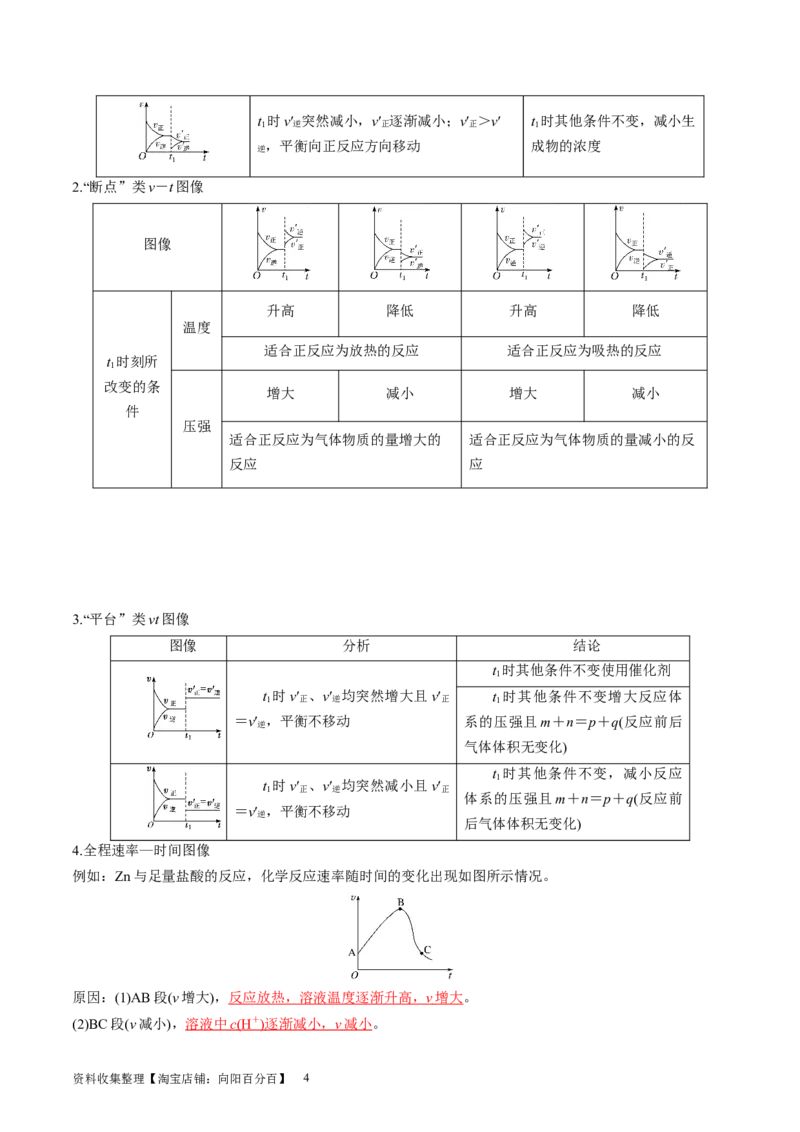
2.“断点”类v-t图像
图像
升高 降低 升高 降低
温度
适合正反应为放热的反应 适合正反应为吸热的反应
t 时刻所
1
改变的条
增大 减小 增大 减小
件
压强
适合正反应为气体物质的量增大的 适合正反应为气体物质的量减小的反
反应 应
3.“平台”类vt图像
图像 分析 结论
t 时其他条件不变使用催化剂
1
t 时v′ 、v′ 均突然增大且v′ t 时其他条件不变增大反应体
1 正 逆 正 1
=v′ ,平衡不移动 系的压强且m+n=p+q(反应前后
逆
气体体积无变化)
t 时其他条件不变,减小反应
1
t 时v′ 、v′ 均突然减小且v′
1 正 逆 正
体系的压强且m+n=p+q(反应前
=v′ ,平衡不移动
逆
后气体体积无变化)
4.全程速率—时间图像
例如:Zn与足量盐酸的反应,化学反应速率随时间的变化出现如图所示情况。
原因:(1)AB段(v增大), 反应放热,溶液温度逐渐升高, v 增大 。
(2)BC段(v减小), 溶液中 c (H + ) 逐渐减小, v 减小 。
资料收集整理【淘宝店铺:向阳百分百】 4知识点2 速率—压强(或温度)图像
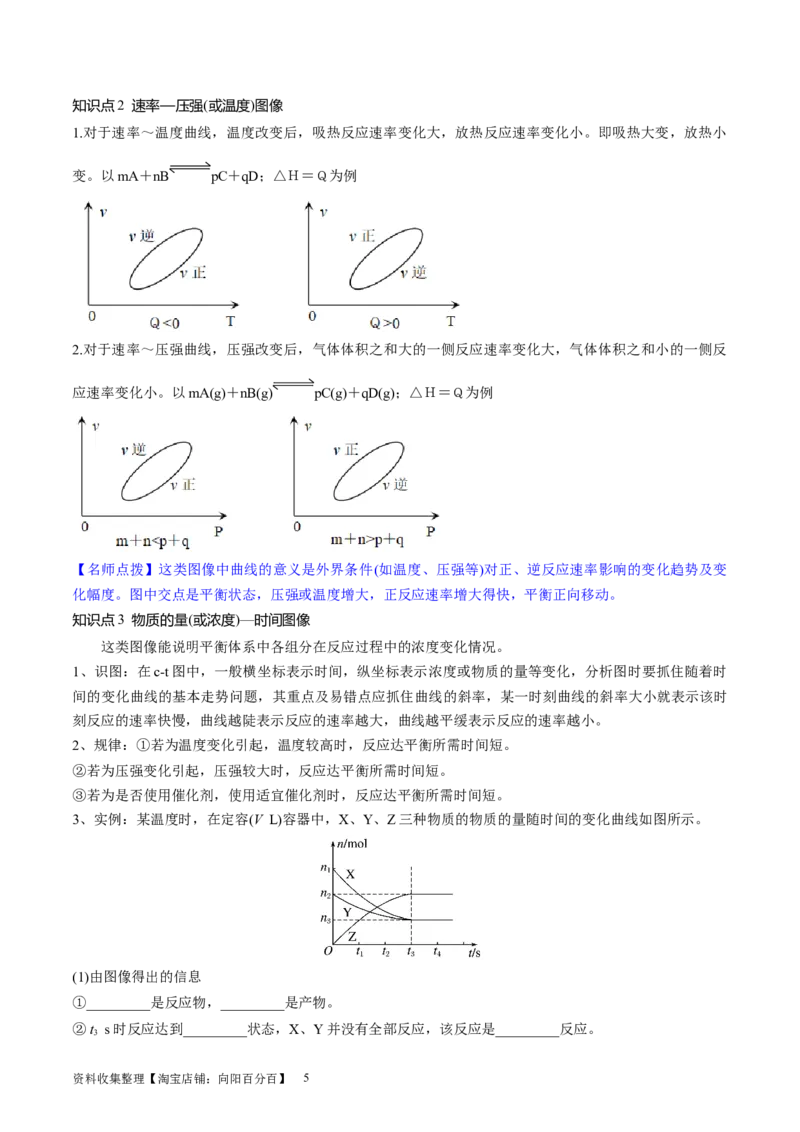
1.对于速率~温度曲线,温度改变后,吸热反应速率变化大,放热反应速率变化小。即吸热大变,放热小
变。以mA+nB pC+qD;△H=Q为例
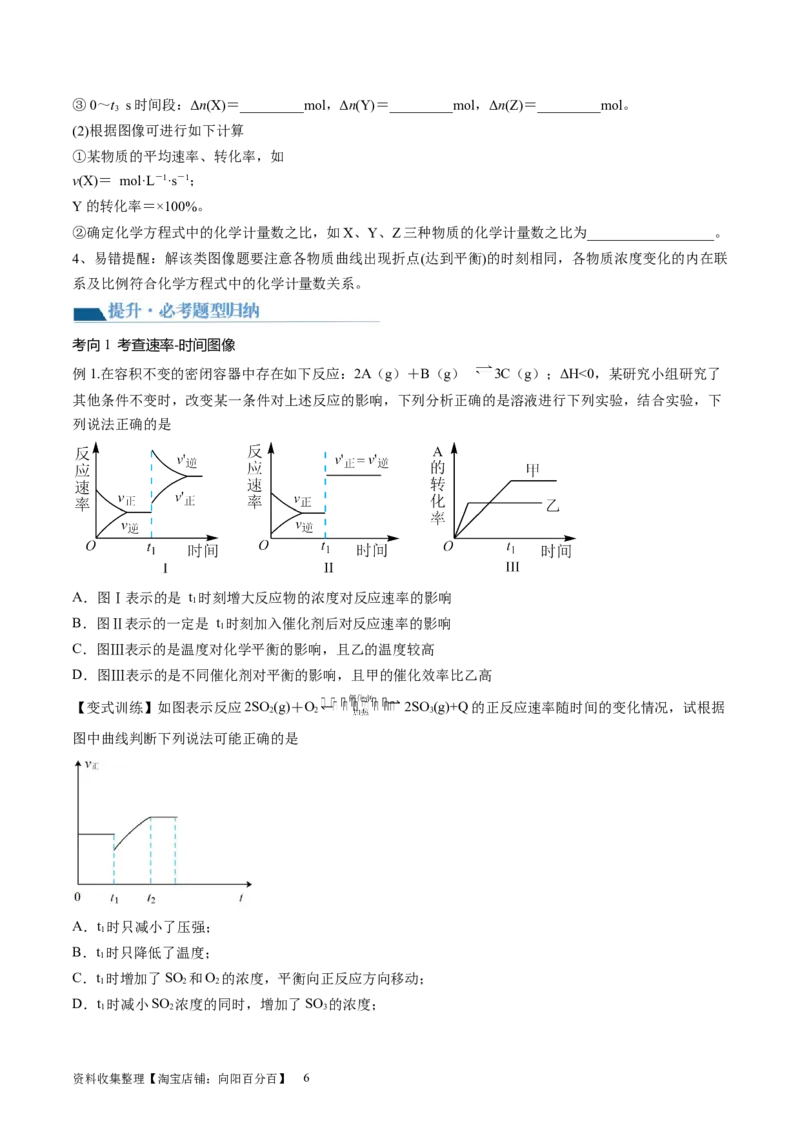
2.对于速率~压强曲线,压强改变后,气体体积之和大的一侧反应速率变化大,气体体积之和小的一侧反
应速率变化小。以mA(g)+nB(g) pC(g)+qD(g);△H=Q为例
【名师点拨】这类图像中曲线的意义是外界条件(如温度、压强等)对正、逆反应速率影响的变化趋势及变
化幅度。图中交点是平衡状态,压强或温度增大,正反应速率增大得快,平衡正向移动。
知识点3 物质的量(或浓度)—时间图像
这类图像能说明平衡体系中各组分在反应过程中的浓度变化情况。
1、识图:在c-t图中,一般横坐标表示时间,纵坐标表示浓度或物质的量等变化,分析图时要抓住随着时
间的变化曲线的基本走势问题,其重点及易错点应抓住曲线的斜率,某一时刻曲线的斜率大小就表示该时
刻反应的速率快慢,曲线越陡表示反应的速率越大,曲线越平缓表示反应的速率越小。
2、规律:①若为温度变化引起,温度较高时,反应达平衡所需时间短。
②若为压强变化引起,压强较大时,反应达平衡所需时间短。
③若为是否使用催化剂,使用适宜催化剂时,反应达平衡所需时间短。
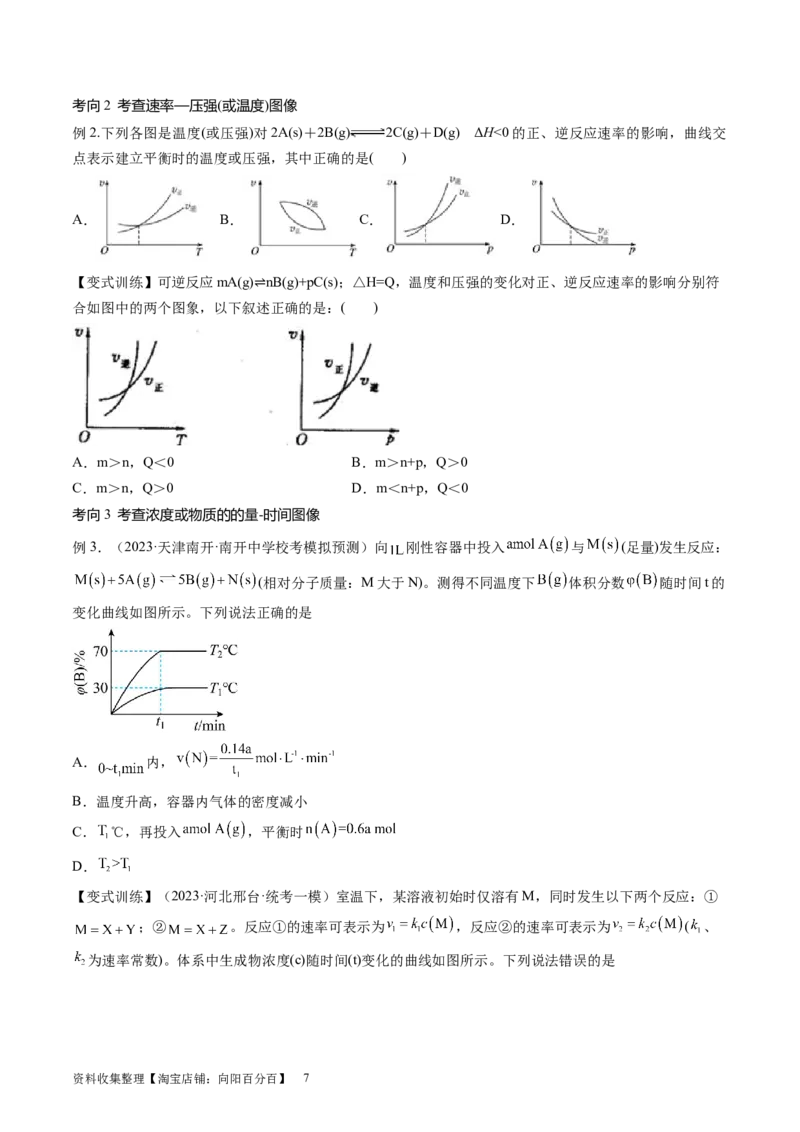
3、实例:某温度时,在定容(V L)容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。
(1)由图像得出的信息
①_________是反应物,_________是产物。
②t s时反应达到_________状态,X、Y并没有全部反应,该反应是_________反应。
3
资料收集整理【淘宝店铺:向阳百分百】 5③0~t s时间段:Δn(X)=_________mol,Δn(Y)=_________mol,Δn(Z)=_________mol。
3
(2)根据图像可进行如下计算
①某物质的平均速率、转化率,如
v(X)= mol·L-1·s-1;
Y的转化率=×100%。
②确定化学方程式中的化学计量数之比,如X、Y、Z三种物质的化学计量数之比为__________________。
4、易错提醒:解该类图像题要注意各物质曲线出现折点(达到平衡)的时刻相同,各物质浓度变化的内在联
系及比例符合化学方程式中的化学计量数关系。
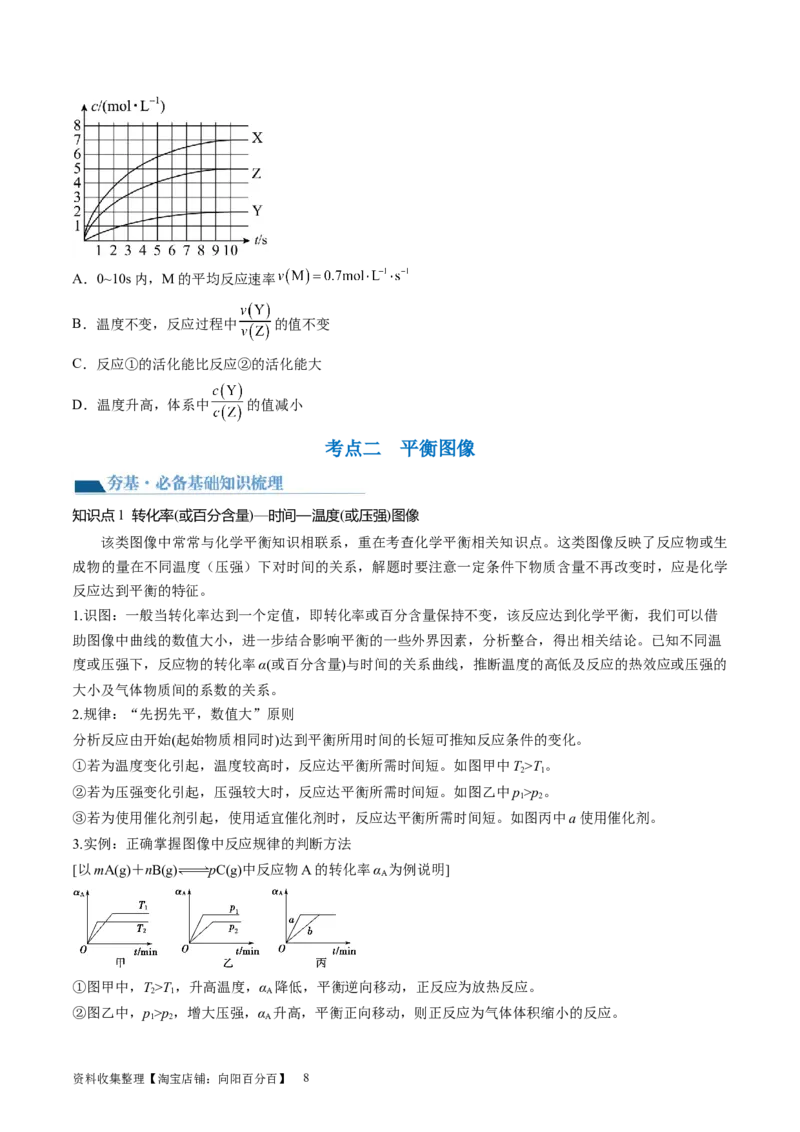
考向1 考查速率-时间图像
例1.在容积不变的密闭容器中存在如下反应:2A(g)+B(g) 3C(g);ΔH<0,某研究小组研究了
其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是溶液进行下列实验,结合实验,下
列说法正确的是
A.图Ⅰ表示的是 t 时刻增大反应物的浓度对反应速率的影响
1
B.图Ⅱ表示的一定是 t 时刻加入催化剂后对反应速率的影响
1
C.图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高
D.图Ⅲ表示的是不同催化剂对平衡的影响,且甲的催化效率比乙高
【变式训练】如图表示反应2SO (g)+O 2SO (g)+Q的正反应速率随时间的变化情况,试根据
2 2 3
图中曲线判断下列说法可能正确的是
A.t 时只减小了压强;
1
B.t 时只降低了温度;
1
C.t 时增加了SO 和O 的浓度,平衡向正反应方向移动;
1 2 2
D.t 时减小SO 浓度的同时,增加了SO 的浓度;
1 2 3
资料收集整理【淘宝店铺:向阳百分百】 6考向2 考查速率—压强(或温度)图像
例2.下列各图是温度(或压强)对2A(s)+2B(g) 2C(g)+D(g) ΔH<0的正、逆反应速率的影响,曲线交
点表示建立平衡时的温度或压强,其中正确的是( )
A. B. C. D.
【变式训练】可逆反应mA(g) nB(g)+pC(s);△H=Q,温度和压强的变化对正、逆反应速率的影响分别符
合如图中的两个图象,以下叙述正确的是:( )
⇌
A.m>n,Q<0 B.m>n+p,Q>0
C.m>n,Q>0 D.m<n+p,Q<0
考向3 考查浓度或物质的的量-时间图像
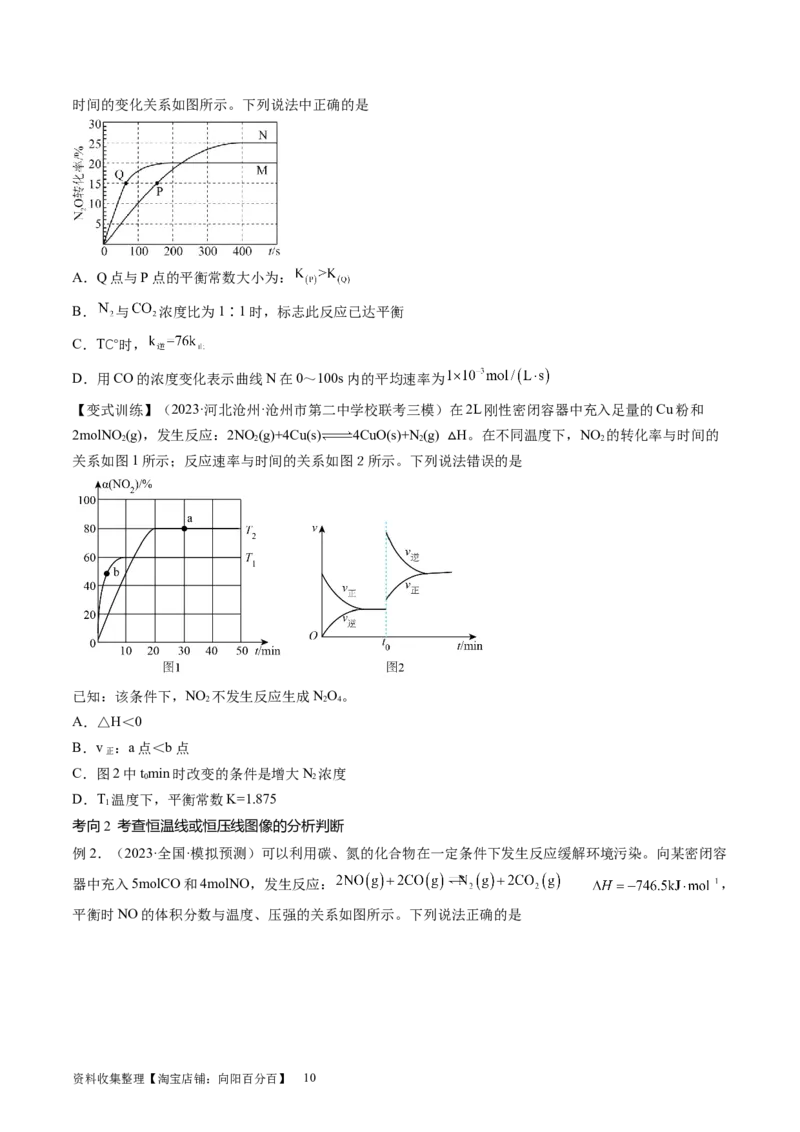
例3.(2023·天津南开·南开中学校考模拟预测)向 刚性容器中投入 与 (足量)发生反应:
(相对分子质量:M大于N)。测得不同温度下 体积分数 随时间t的
变化曲线如图所示。下列说法正确的是
A. 内,
B.温度升高,容器内气体的密度减小
C. ℃,再投入 ,平衡时
D.
【变式训练】(2023·河北邢台·统考一模)室温下,某溶液初始时仅溶有M,同时发生以下两个反应:①
;② 。反应①的速率可表示为 ,反应②的速率可表示为 ( 、
为速率常数)。体系中生成物浓度(c)随时间(t)变化的曲线如图所示。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】 7A.0~10s内,M的平均反应速率
B.温度不变,反应过程中 的值不变
C.反应①的活化能比反应②的活化能大
D.温度升高,体系中 的值减小
考点二 平衡图像
知识点1 转化率(或百分含量)—时间—温度(或压强)图像
该类图像中常常与化学平衡知识相联系,重在考查化学平衡相关知识点。这类图像反映了反应物或生
成物的量在不同温度(压强)下对时间的关系,解题时要注意一定条件下物质含量不再改变时,应是化学
反应达到平衡的特征。
1.识图:一般当转化率达到一个定值,即转化率或百分含量保持不变,该反应达到化学平衡,我们可以借
助图像中曲线的数值大小,进一步结合影响平衡的一些外界因素,分析整合,得出相关结论。已知不同温
度或压强下,反应物的转化率α(或百分含量)与时间的关系曲线,推断温度的高低及反应的热效应或压强的
大小及气体物质间的系数的关系。
2.规律:“先拐先平,数值大”原则
分析反应由开始(起始物质相同时)达到平衡所用时间的长短可推知反应条件的变化。
①若为温度变化引起,温度较高时,反应达平衡所需时间短。如图甲中T>T。
2 1
②若为压强变化引起,压强较大时,反应达平衡所需时间短。如图乙中p>p。
1 2
③若为使用催化剂引起,使用适宜催化剂时,反应达平衡所需时间短。如图丙中a使用催化剂。
3.实例:正确掌握图像中反应规律的判断方法
[以mA(g)+nB(g) pC(g)中反应物A的转化率α 为例说明]
A
①图甲中,T>T,升高温度,α 降低,平衡逆向移动,正反应为放热反应。
2 1 A
②图乙中,p>p,增大压强,α 升高,平衡正向移动,则正反应为气体体积缩小的反应。
1 2 A
资料收集整理【淘宝店铺:向阳百分百】 8③若纵坐标表示A的百分含量,则甲中正反应为吸热反应,乙中正反应为气体体积增大的反应。
知识点2 恒温线或恒压线图像
该类图像的纵坐标为物质的平衡浓度(反应物或生成物)或反应物的转化率,横坐标为温度或压强。
1.识图:(α表示反应物的转化率,c表示反应物的平衡浓度)
图①,若p>p>p ,则正反应为气体体积减小的反应,ΔH<0;图②,若T>T ,则正反应为放热反应。解
1 2 3 1 2
答此类图像问题,往往可作分析时可沿横轴作一条平行于纵轴的虚线——恒压线或恒温线,然后进行定一
议二,从而可解决问题。
2.规律:(1)“定一议二”原则:可通过分析相同温度下不同压强时反应物 A的转化率大小来判断平衡移动
的方向,从而确定反应方程式中反应物与产物气体物质间的系数的大小关系。如乙中任取两条压强曲线研
究,压强增大,α 增大,平衡正向移动,正反应为气体体积减小的反应,甲中任取一曲线,也能得出结论。
A
(2)通过分析相同压强下不同温度时反应物A的转化率的大小来判断平衡移动的方向,从而确定反应的热效
应。如利用上述分析方法,在甲中作垂直线,乙中任取一曲线,即能分析出正反应为放热反应。
知识点3 反应过程中组分含量或浓度与温度的关系及非平衡点图像
1.反应过程中组分含量或浓度与温度的关系图像
对于化学反应mA(g)+nB(g) pC(g)+qD(g),在相同时间段内,M点前,表示化学反应从反应物开
始,则v >v ,未达平衡;M点为刚达到的平衡点。M点后为平衡受温度的影响情况,即升温,A%增大
正 逆
(C%减小),平衡逆向移动,ΔH<0。
2.化学平衡曲线外的非平衡点分析
对于化学反应mA(g)+nB(g) pC(g)+qD(g),L线上所有的点都是平衡点。
左上方(E点),A%大于此压强或温度时平衡体系中的A%,E点必须向正反应方
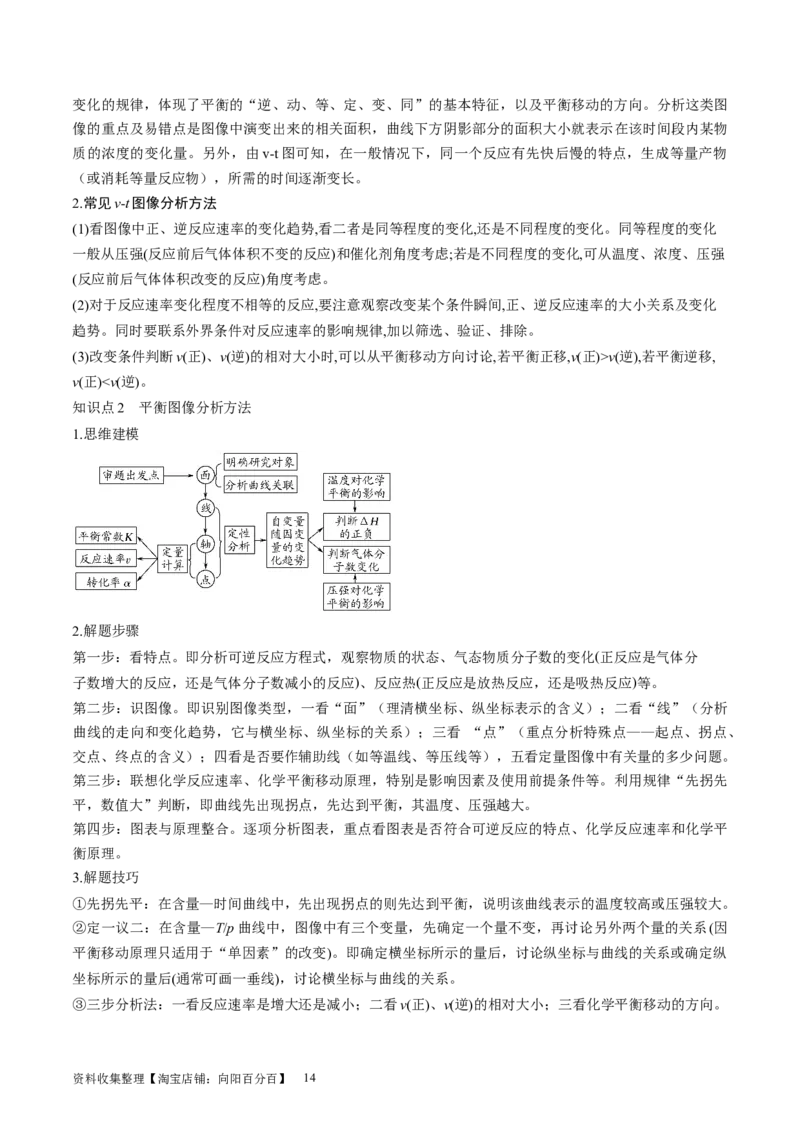
向移动才能达到平衡状态,所以,E点v >v ;则右下方(F点)v v(逆),若平衡逆移,
v(正)0
B.550℃时,充入惰性气体将使v正>v逆
C.650℃时,反应达平衡后CO 的转化率为25.0%
2
D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数K=24.0pa
p
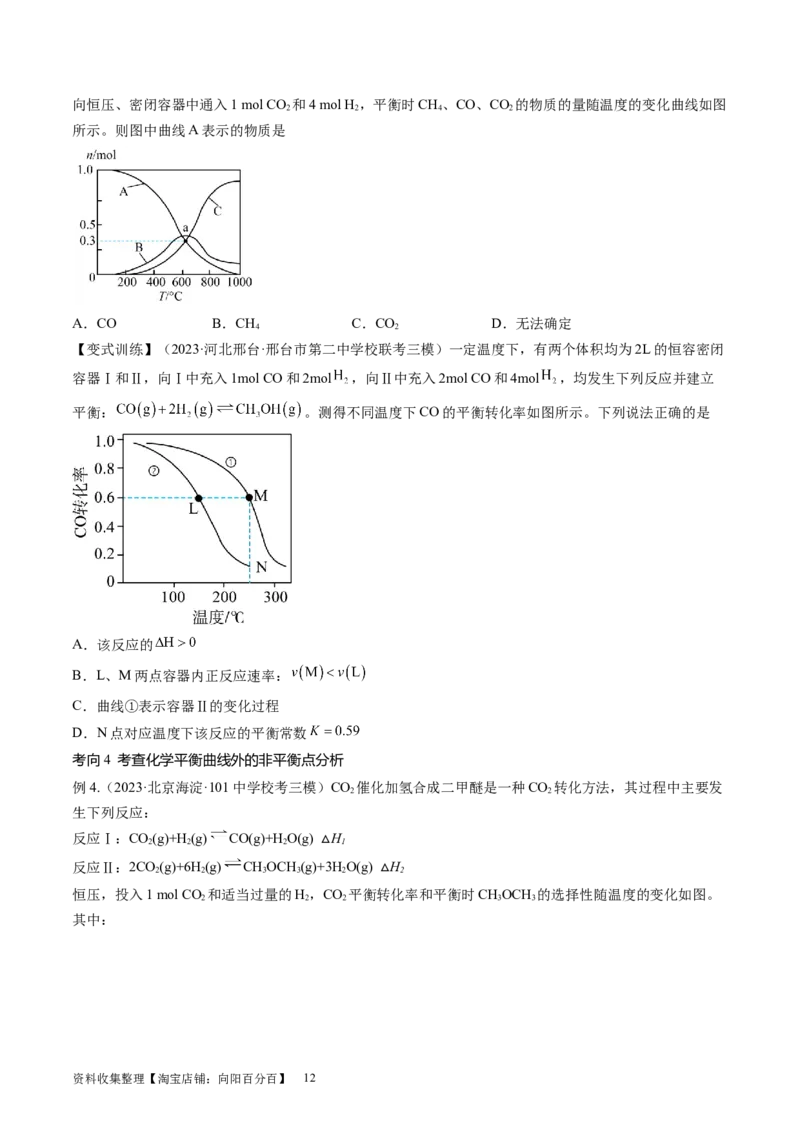
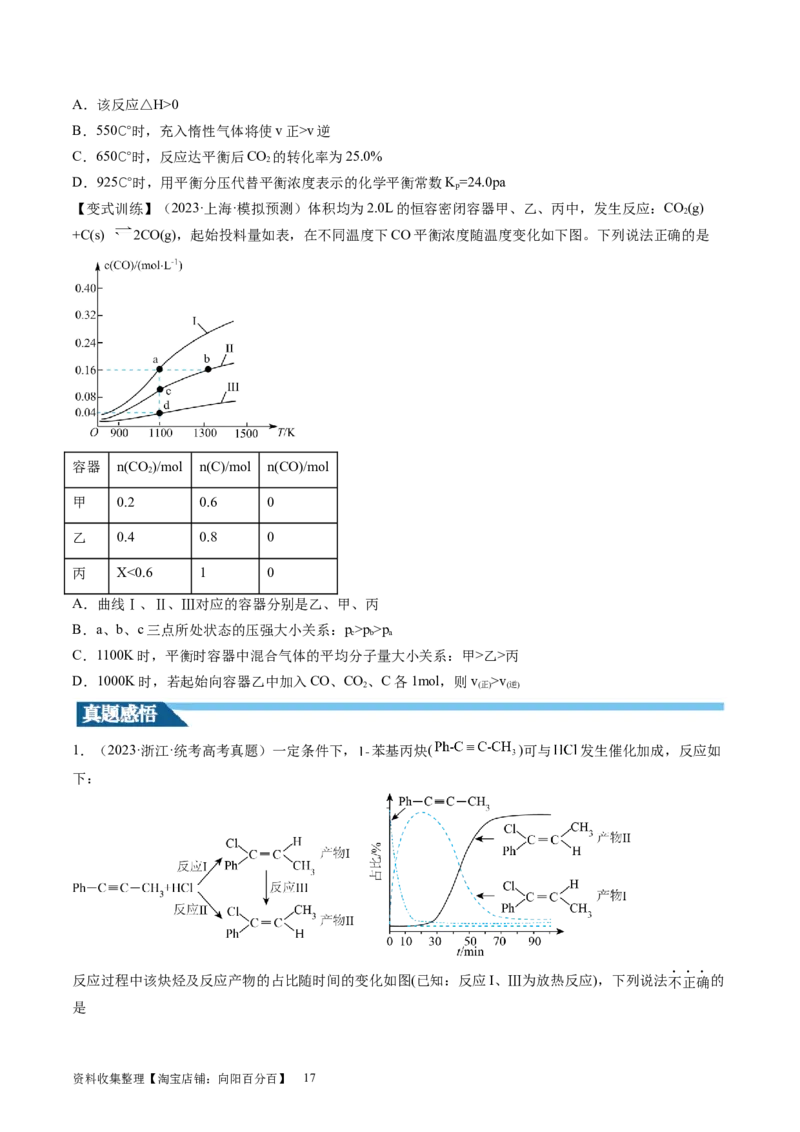
【变式训练】(2023·上海·模拟预测)体积均为2.0L的恒容密闭容器甲、乙、丙中,发生反应:CO(g)
2
+C(s) 2CO(g),起始投料量如表,在不同温度下CO平衡浓度随温度变化如下图。下列说法正确的是
容器 n(CO)/mol n(C)/mol n(CO)/mol
2
甲 0.2 0.6 0
乙 0.4 0.8 0
丙 X<0.6 1 0
A.曲线Ⅰ、Ⅱ、Ⅲ对应的容器分别是乙、甲、丙
B.a、b、c三点所处状态的压强大小关系:p>p>p
c b a
C.1100K时,平衡时容器中混合气体的平均分子量大小关系:甲>乙>丙
D.1000K时,若起始向容器乙中加入CO、CO、C各1mol,则v >v
2 (正) (逆)
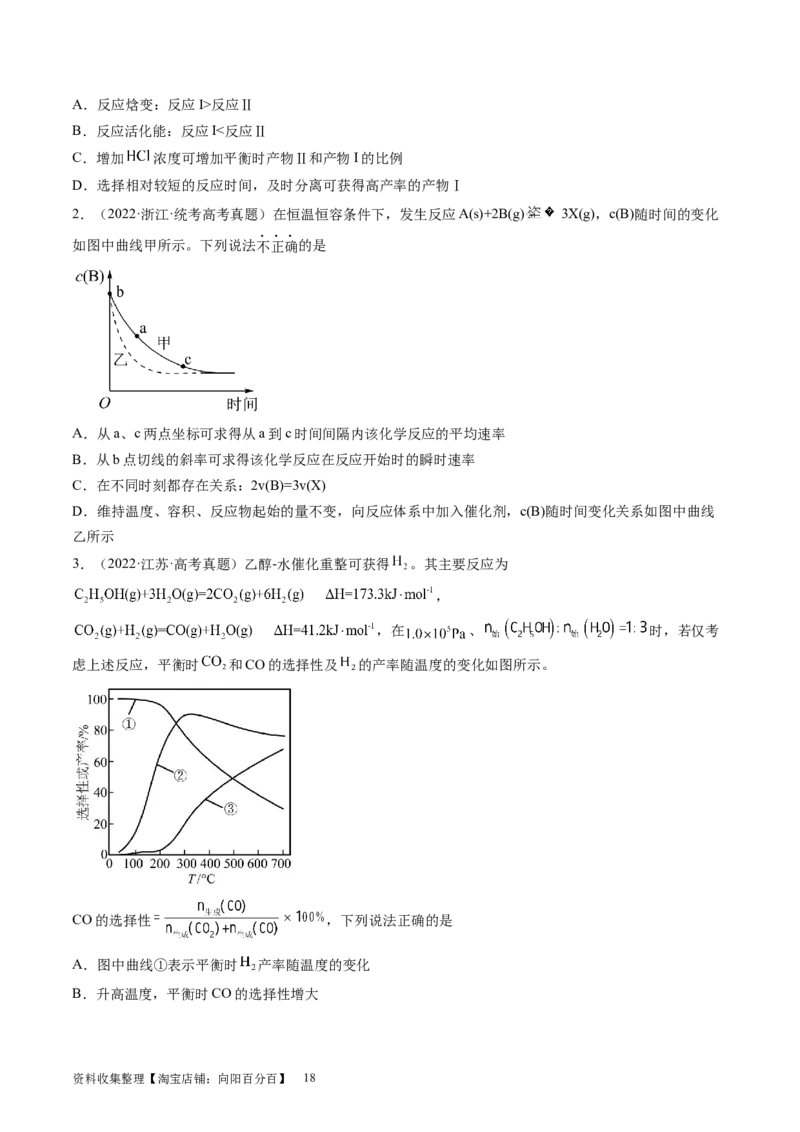
1.(2023·浙江·统考高考真题)一定条件下, 苯基丙炔( )可与 发生催化加成,反应如
下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法不正确的
是
资料收集整理【淘宝店铺:向阳百分百】 17A.反应焓变:反应I>反应Ⅱ
B.反应活化能:反应I<反应Ⅱ
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
2.(2022·浙江·统考高考真题)在恒温恒容条件下,发生反应A(s)+2B(g) 3X(g),c(B)随时间的变化
如图中曲线甲所示。下列说法不正确的是
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C.在不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线
乙所示
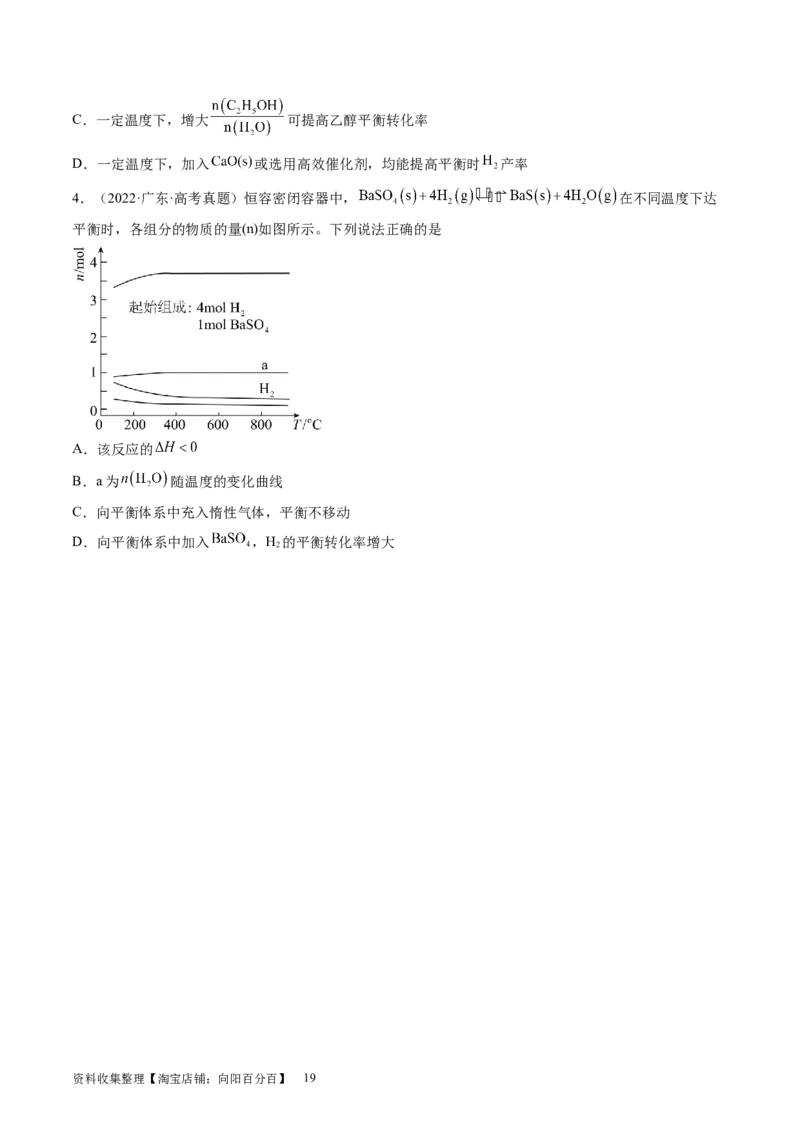
3.(2022·江苏·高考真题)乙醇-水催化重整可获得 。其主要反应为
,
,在 、 时,若仅考
虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是
A.图中曲线①表示平衡时 产率随温度的变化
B.升高温度,平衡时CO的选择性增大
资料收集整理【淘宝店铺:向阳百分百】 18C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
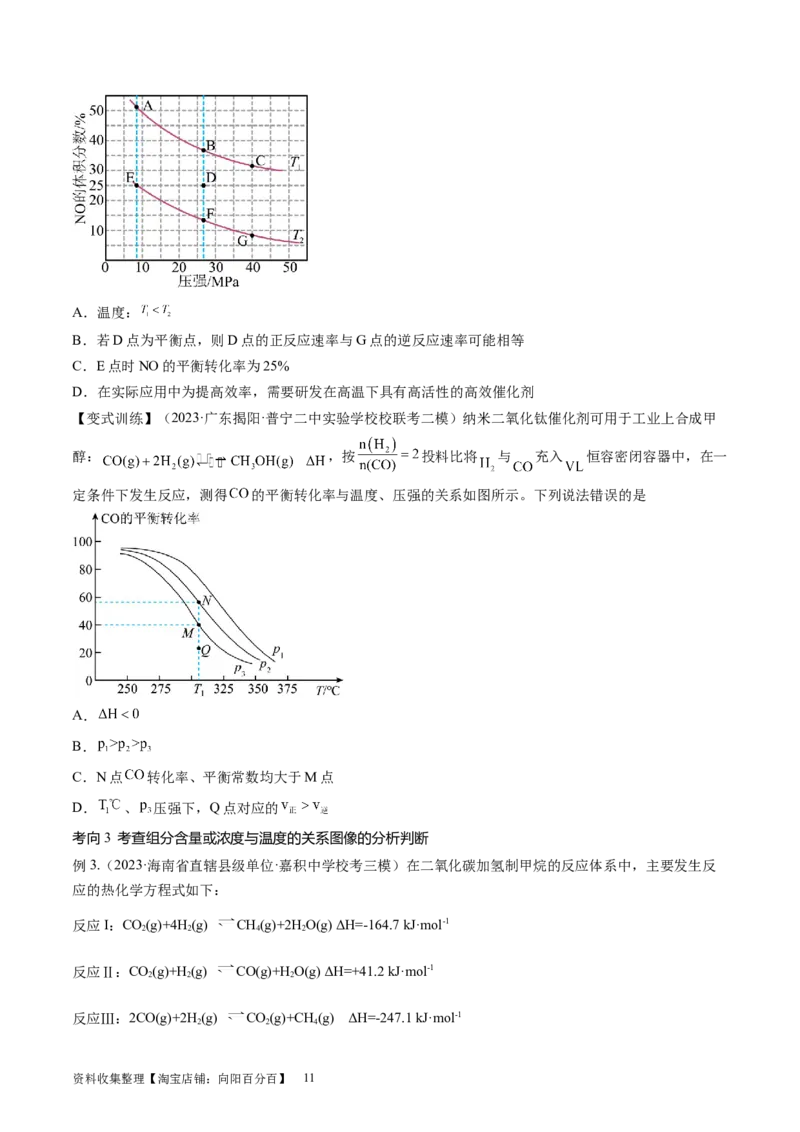
4.(2022·广东·高考真题)恒容密闭容器中, 在不同温度下达
平衡时,各组分的物质的量(n)如图所示。下列说法正确的是
A.该反应的
B.a为 随温度的变化曲线
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入 ,H 的平衡转化率增大
2
资料收集整理【淘宝店铺:向阳百分百】 19