文档内容
第 30 讲 盐类水解
目录
考情分析 知识点2 盐类水解的应用
知识点3 水解常数及应用
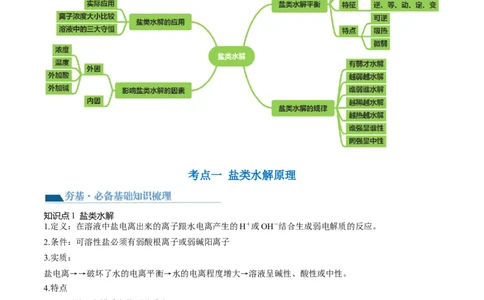
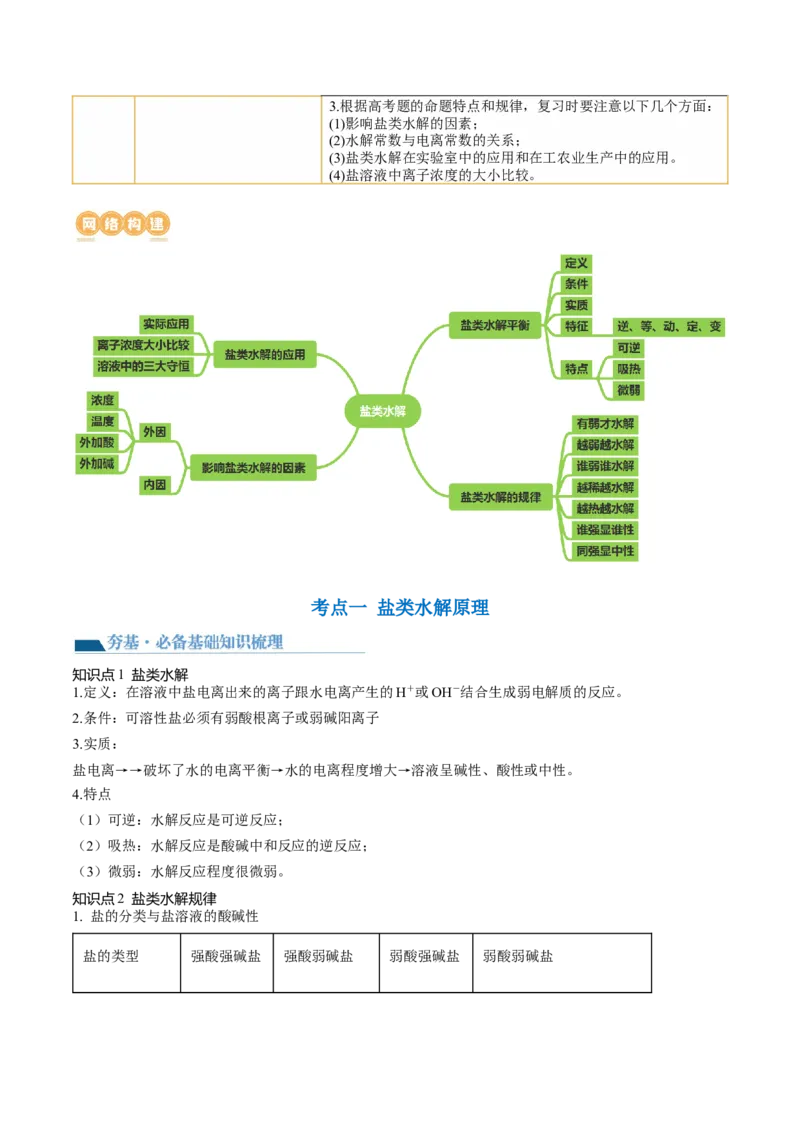
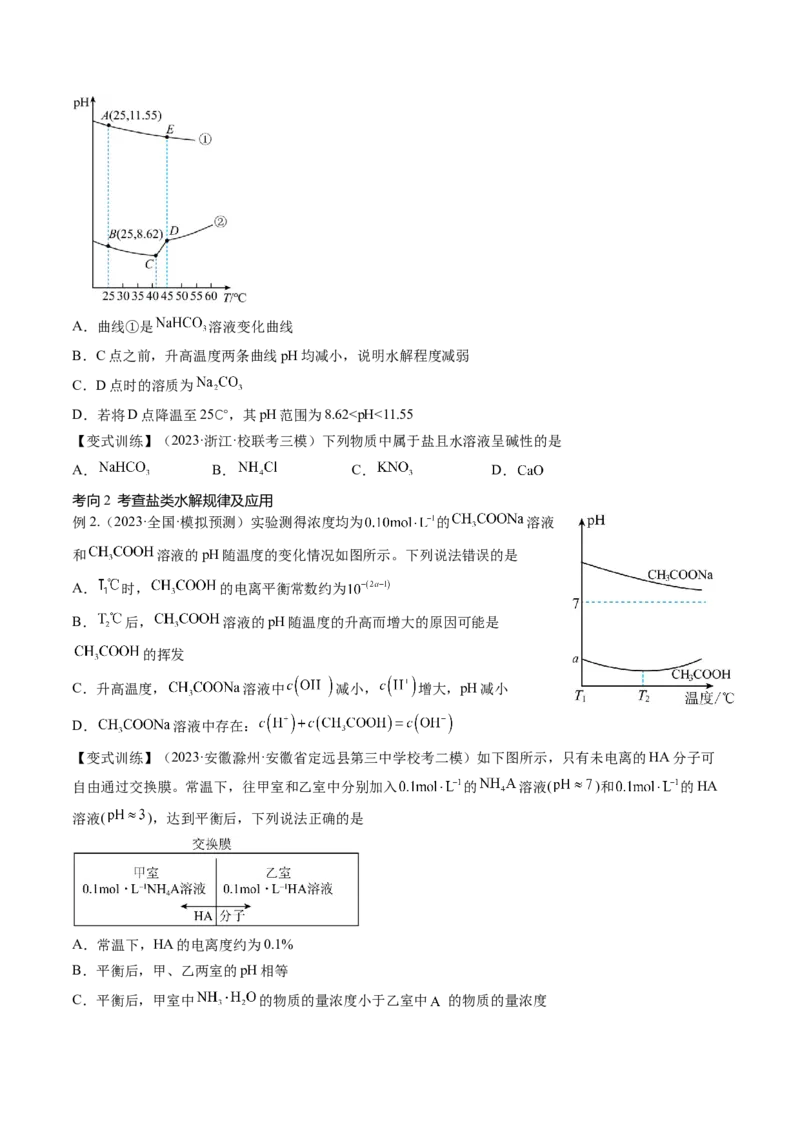
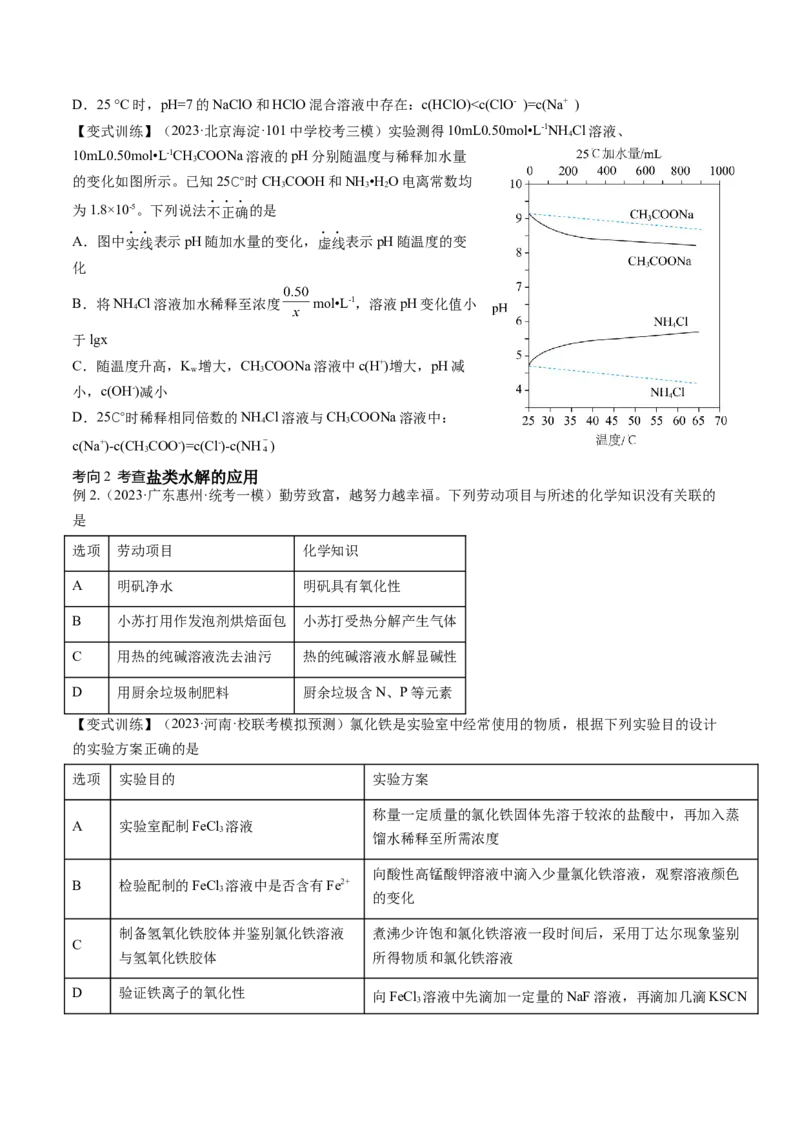
网络构建
【提升·必考题型归纳】
考向1 考查盐类水解的影响因素
考点一 盐类水解原理
考向2 考查盐类水解的应用
【夯基·必备基础知识梳理】 考向3 考查水解常数的应用与计算
知识点1 盐类水解
知识点2 盐类水解规律 考点三 水溶液中粒子的数量关系
知识点3 盐类水解方程式的书写
【提升·必考题型归纳】 【夯基·必备基础知识梳理】
考向1 考查盐类的水解及溶液的酸碱性 知识点1 电解质溶液中的三大守恒
考向2 考查盐类水解规律及应用 知识点2 电解质溶液中粒子浓度大小比较
知识点3 水溶液中函数图像分析
考点二 盐类水解的影响因素及应用 【提升·必考题型归纳】
考向1 考查单一溶液中粒子浓度大小比较
【夯基·必备基础知识梳理】 考向2 考查混合溶液中粒子浓度大小比较
知识点1 影响盐类水解的因素
真题感悟
考点要 考题统计 考情分析
求
2023浙江1月卷2题,2分 分析近三年的高考试题,高考命题在本讲有以下规律:
1.从考查题型和内容上看,高考命题以选择题为主来呈现,考
盐类水 2022北京卷1题,3分
查内容主要有以下两个方面:
解原理 2021北京卷12题,3分 (1)考查盐类水解的基本概念,依托实验背景,考查水解平衡的
影响因素。
盐类水 2023北京卷3题,3分 (2)与工农业生产相结合,考查盐类水解的应用。
解的应 2022浙江6月卷19题,2分
(3)以单一溶液和混合溶液为背景,考查溶液中粒子浓度关系。
(4)借助图像的形式考查①水解方程式的书写;②结合滴定图像判
用 2021河北卷6题,3分
断离子浓度关系;③电离平衡常数与水解常数的转化关系和应
用。
2.从命题思路上看,
水溶液
(1)侧重以具体物质的反应和变化为载体,考查盐类水解的基本
2023天津卷10题,3分
中粒子 概念、水解规律、水解平衡的移动和影响因素;以实际情境为
2022浙江1月卷23题,2分 载体,考查水解的应用。
的数量
(2)侧重考查二元或多元酸与碱反应过程中,溶液中粒子浓度之
2021广东卷8题,2分
关系 间的关系。考查粒子浓度大小比较、三大守恒、对水电离的影
响等。
(3)以一些新物质、新图像为载体考查有关水解常数的计算3.根据高考题的命题特点和规律,复习时要注意以下几个方面:
(1)影响盐类水解的因素;
(2)水解常数与电离常数的关系;
(3)盐类水解在实验室中的应用和在工农业生产中的应用。
(4)盐溶液中离子浓度的大小比较。
考点一 盐类水解原理
知识点1 盐类水解
1.定义:在溶液中盐电离出来的离子跟水电离产生的H+或OH-结合生成弱电解质的反应。
2.条件:可溶性盐必须有弱酸根离子或弱碱阳离子
3.实质:
盐电离→→破坏了水的电离平衡→水的电离程度增大→溶液呈碱性、酸性或中性。
4.特点
(1)可逆:水解反应是可逆反应;
(2)吸热:水解反应是酸碱中和反应的逆反应;
(3)微弱:水解反应程度很微弱。
知识点2 盐类水解规律
1. 盐的分类与盐溶液的酸碱性
盐的类型 强酸强碱盐 强酸弱碱盐 弱酸强碱盐 弱酸弱碱盐是否水解 不水解 水解 水解 水解
比较Ka和Kb的大小确定
溶液的酸碱性 中性 酸性 碱性
溶液的酸性碱性
NaCl 、 NH Cl 、 NaS 、 CHCOONH ( 中 性 溶
代表物 4 2 3 4
KNO CuSO NaCO 液)
3 4 2 3
酸式盐不能通过简单分类来判断其溶液的酸碱性:
NaHSO 不水解,但是其溶液显酸性;
4
注意
NaHSO 电离大于水解,其溶液显酸性;
3
NaHCO 水解大于电离,其溶液显酸性。
3
2.盐类水解规律:
“有弱才水解、无弱不水解、越弱越水解、都弱都水解、越热越水解、越稀越水解、谁强显谁性、同强是
中性”。
知识点3 盐类水解方程式的书写
1.一般要求
水解记三点:①水写分子式,②中间用可逆( ),③后无沉气出。即盐类水解一般不会产生沉淀和气体,
所以不用符号“↓”和“↑”表示水解产物。如 NH Cl水解的离子方程式为NH+HO NH ·H O+H
4 2 3 2
+。
2.三种类型的盐水解离子方程式的书写
①多元弱酸盐水解:分步进行,水解离子方程式要分步表示,以第一步为主,一般只写第一步水解方程式。
如NaCO 水解的离子方程式为CO+HO HCO+OH-。
2 3 2
②多元弱碱盐水解:水解离子方程式一步写完。
如FeCl 水解的离子方程式为Fe3++3HO Fe(OH) +3H+。
3 2 3
③阴、阳离子相互促进的水解:水解程度较大(即产生沉淀),书写时要用“===”、“↑”、“↓”等。
如NaS溶液与AlCl 溶液混合水解的离子方程式为2Al3++3S2-+6HO===2Al(OH) ↓+3HS↑。
2 3 2 3 2
注意:多元弱酸阴离子分步水解,分步书写;多元弱碱阳离子分步水解,一步书写。
考向1 考查盐类的水解及溶液的酸碱性
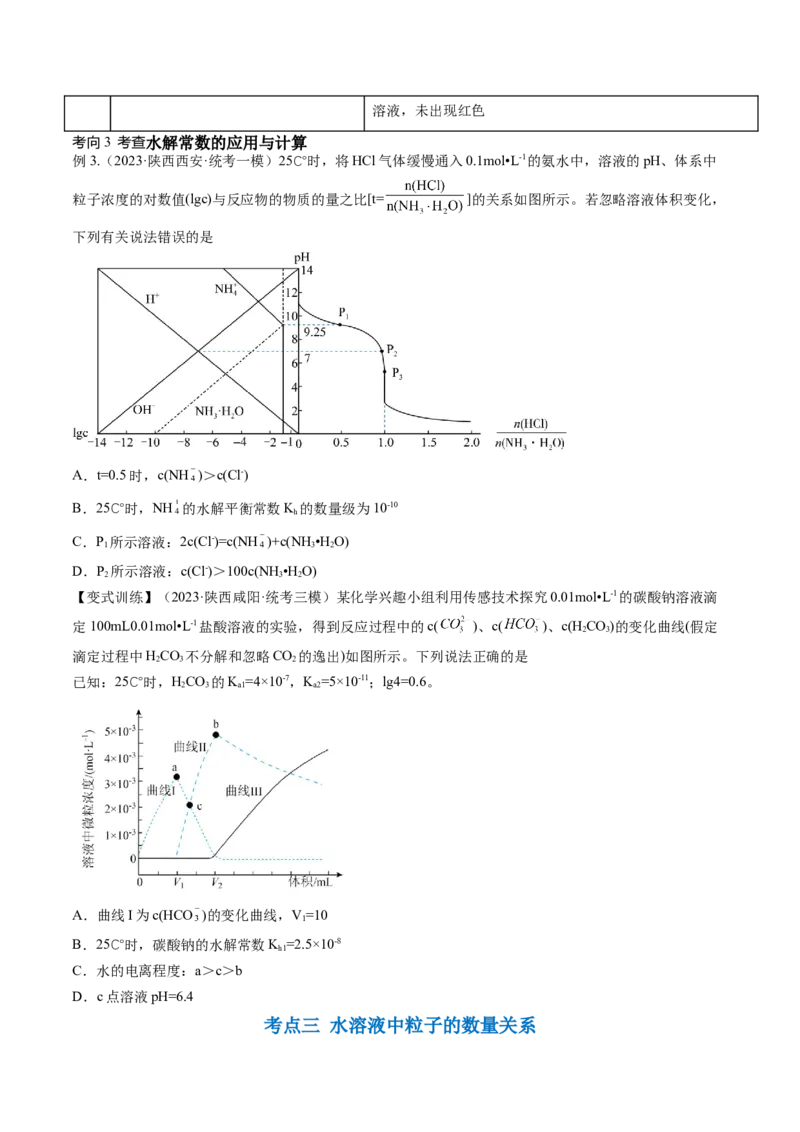
例1.(2023·河北衡水·衡水市第二中学校考三模)实验测得等物质的量浓度的 和 溶液的
pH随温度变化如图所示。下列说法正确的是A.曲线①是 溶液变化曲线
B.C点之前,升高温度两条曲线pH均减小,说明水解程度减弱
C.D点时的溶质为
D.若将D点降温至25℃,其pH范围为8.62c(ClO- )D.25 °C时,pH=7的NaClO和HClO混合溶液中存在:c(HClO)c(H PO -)>c(HPO 2-)>c(PO 3-)。
3 4 2 4 4 4
(2)多元弱酸的正盐溶液:多元弱酸的酸根离子分步水解,水解程度逐级减弱。
如在NaCO 溶液中:c(Na+)>c(CO 2-)>c(OH-)>c(HCO-)。
2 3 3 3
(3)多元弱酸酸式盐:分析酸式酸根电离与水解大小。
如NaHCO 溶液中HCO -水解大于电离,则;c(Na+)>c(HCO-)>c(OH-)>c(H CO)>c(H+)>c(CO 2-)。
3 3 3 2 3 3
NaHSO 溶液中HSO -电离大于水解,则c(Na+)>c(HSO -)c(H+)>c(SO2-)>c(OH-)>c(H SO )。
3 3 3 3 2 3
2.混合溶液中各离子浓度的比较
混合溶液要综合分析电离、水解等因素。如在0.1 mol·L-1 NH Cl溶液和0.1 mol·L-1的氨水混合溶液中,
4
各离子浓度大小的顺序为c(NH +)>c(Cl-)>c(OH-)>c(H+)。
43.不同溶液中同一离子浓度的比较
不同溶液要看溶液中其他离子对该离子的影响。如在相同物质的量浓度的下列溶液中:
①NH Cl②CHCOONH ③NH HSO ,c(NH +)由大到小的顺序为③>①>②。
4 3 4 4 4 4
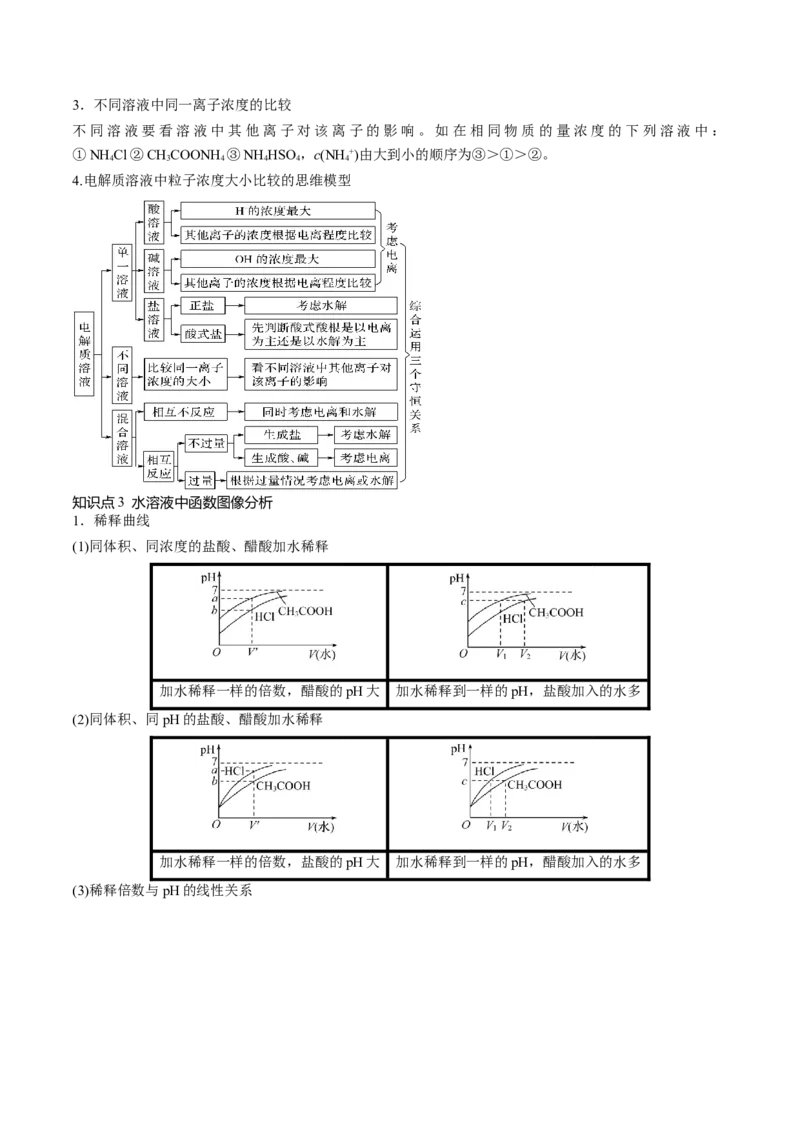
4.电解质溶液中粒子浓度大小比较的思维模型
知识点3 水溶液中函数图像分析
1.稀释曲线
(1)同体积、同浓度的盐酸、醋酸加水稀释
加水稀释一样的倍数,醋酸的pH大 加水稀释到一样的pH,盐酸加入的水多
(2)同体积、同pH的盐酸、醋酸加水稀释
加水稀释一样的倍数,盐酸的pH大 加水稀释到一样的pH,醋酸加入的水多
(3)稀释倍数与pH的线性关系①HY为强酸、HX为弱酸 ① MOH 为强碱、ROH 为弱
②ab两点的溶液中:c(X-)=c(Y 碱
-) ②c(ROH)>c(MOH)
③水的电离程度:d>c>a=b ③水的电离程度:a>b
2.滴定曲线
氢氧化钠滴定等浓度等体积的盐酸、醋酸的滴定曲线 盐酸滴定等浓度等体积的氢氧化钠、氨水的滴定曲线
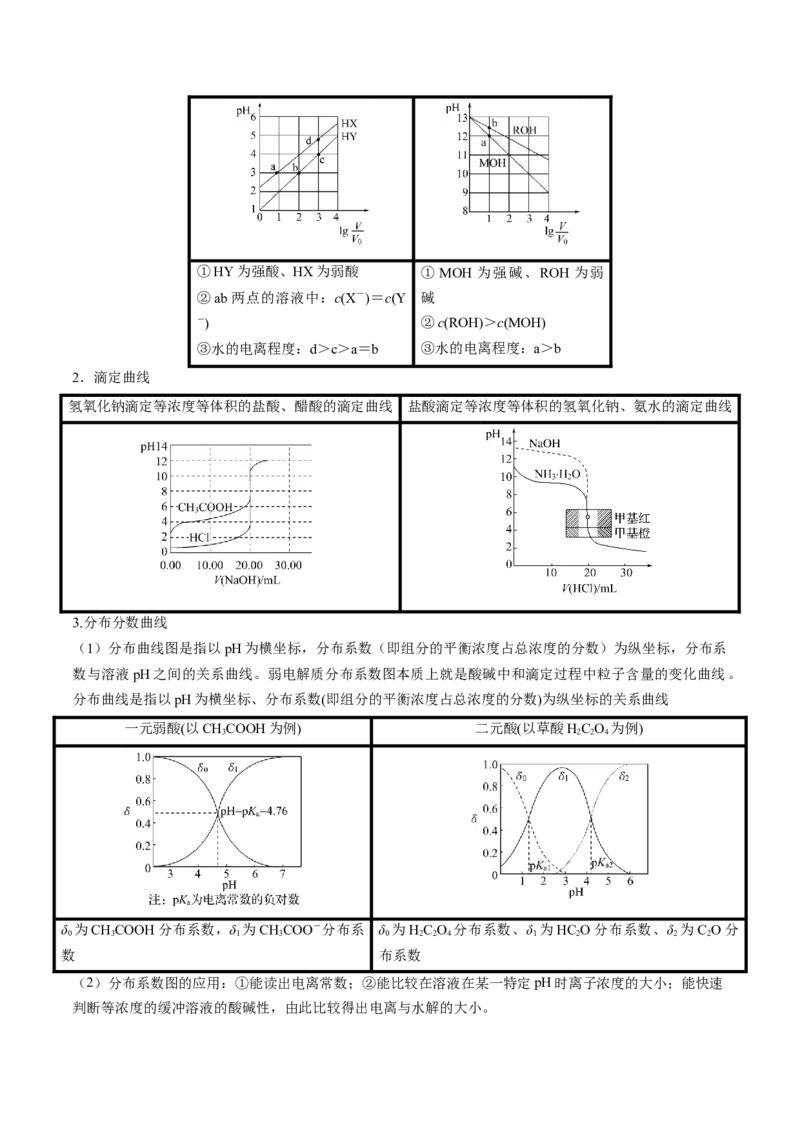
3.分布分数曲线
(1)分布曲线图是指以pH为横坐标,分布系数(即组分的平衡浓度占总浓度的分数)为纵坐标,分布系
数与溶液pH之间的关系曲线。弱电解质分布系数图本质上就是酸碱中和滴定过程中粒子含量的变化曲线。
分布曲线是指以pH为横坐标、分布系数(即组分的平衡浓度占总浓度的分数)为纵坐标的关系曲线
一元弱酸(以CHCOOH为例) 二元酸(以草酸HC O 为例)
3 2 2 4
δ 为CHCOOH分布系数,δ 为CHCOO-分布系 δ 为HC O 分布系数、δ 为HC O分布系数、δ 为C O分
0 3 1 3 0 2 2 4 1 2 2 2
数 布系数
(2)分布系数图的应用:①能读出电离常数;②能比较在溶液在某一特定pH时离子浓度的大小;能快速
判断等浓度的缓冲溶液的酸碱性,由此比较得出电离与水解的大小。考向1 考查单一溶液中粒子浓度大小比较
例1.(2023·广东·统考模拟预测)测定 溶液升温过程中的pH(不考虑水的蒸发、溶液体积
的变化),数据如下。
温度/℃ 25 40 60 80
pH 11.90 11.68 11.54 11.42
下列说法错误的是
A.25℃时, 的一级水解常数 的数量级为
B.温度升高后 溶液碱性减弱
C.溶液中
D.温度升高pH变小是K 增大与水解平衡移动共同作用的结果
w
【变式训练】(2023·广东惠州·统考模拟预测) 是一种弱碱,可与盐酸反应生成 。下列叙
述正确的是
A.常温时,0.1mol/L 水溶液的
B.0.1mol/L 水溶液加水稀释, 升高
C.0.1mol/L 水溶液中:
D. 水溶液中:
考向2 考查混合溶液中粒子浓度大小比较
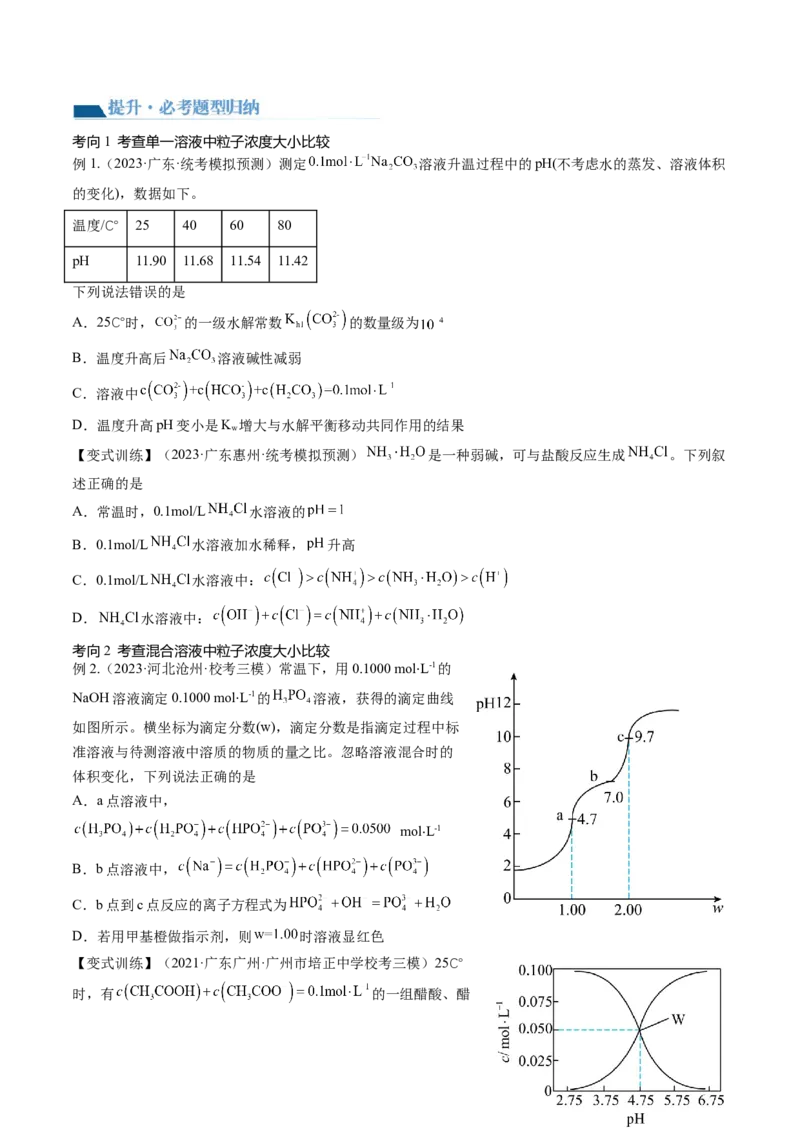
例2.(2023·河北沧州·校考三模)常温下,用0.1000 molL-1的
NaOH溶液滴定0.1000 molL-1的 溶液,获得的滴定⋅ 曲线
如图所示。横坐标为滴定分⋅数(w),滴定分数是指滴定过程中标
准溶液与待测溶液中溶质的物质的量之比。忽略溶液混合时的
体积变化,下列说法正确的是
A.a点溶液中,
molL-1
⋅
B.b点溶液中,
C.b点到c点反应的离子方程式为
D.若用甲基橙做指示剂,则 时溶液显红色
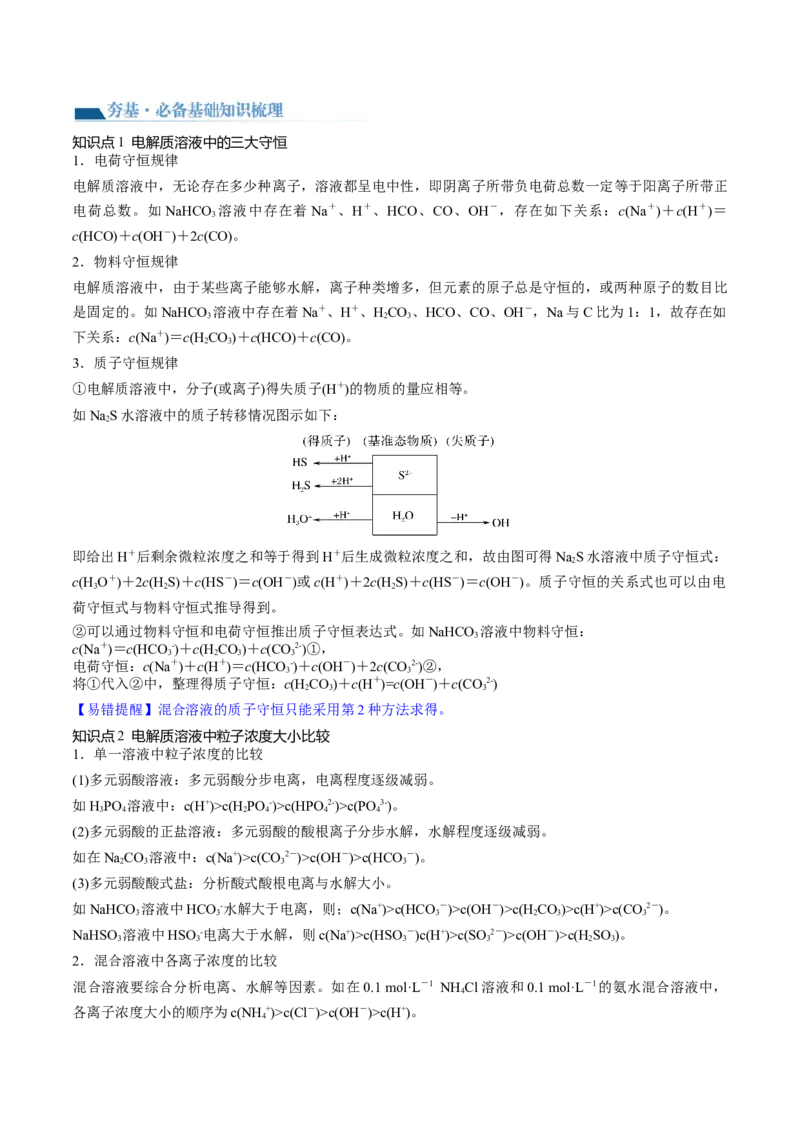
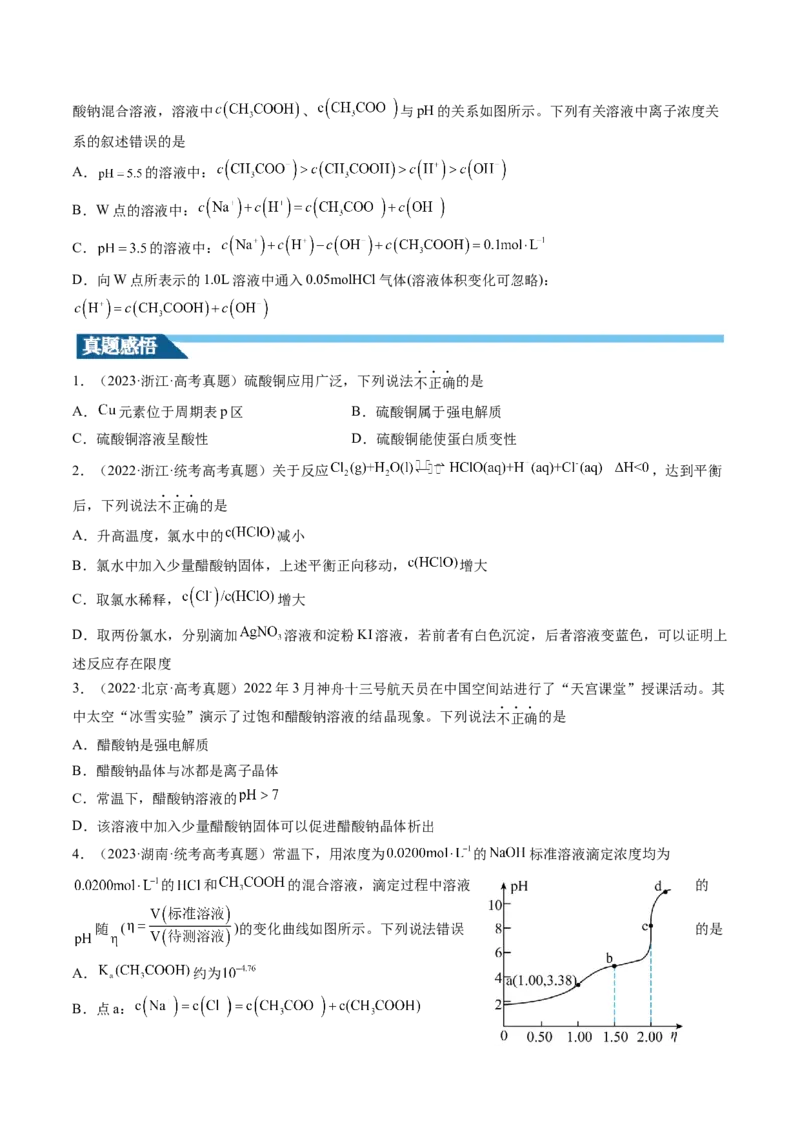
【变式训练】(2021·广东广州·广州市培正中学校考三模)25℃
时,有 的一组醋酸、醋酸钠混合溶液,溶液中 、 与pH的关系如图所示。下列有关溶液中离子浓度关
系的叙述错误的是
A. 的溶液中:
B.W点的溶液中:
C. 的溶液中:
D.向W点所表示的1.0L溶液中通入0.05molHCl气体(溶液体积变化可忽略):
1.(2023·浙江·高考真题)硫酸铜应用广泛,下列说法不正确的是
A. 元素位于周期表p区 B.硫酸铜属于强电解质
C.硫酸铜溶液呈酸性 D.硫酸铜能使蛋白质变性
2.(2022·浙江·统考高考真题)关于反应 ,达到平衡
后,下列说法不正确的是
A.升高温度,氯水中的 减小
B.氯水中加入少量醋酸钠固体,上述平衡正向移动, 增大
C.取氯水稀释, 增大
D.取两份氯水,分别滴加 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明上
述反应存在限度
3.(2022·北京·高考真题)2022年3月神舟十三号航天员在中国空间站进行了“天宫课堂”授课活动。其
中太空“冰雪实验”演示了过饱和醋酸钠溶液的结晶现象。下列说法不正确的是
A.醋酸钠是强电解质
B.醋酸钠晶体与冰都是离子晶体
C.常温下,醋酸钠溶液的
D.该溶液中加入少量醋酸钠固体可以促进醋酸钠晶体析出
4.(2023·湖南·统考高考真题)常温下,用浓度为 的 标准溶液滴定浓度均为
的 和 的混合溶液,滴定过程中溶液 的
随 ( )的变化曲线如图所示。下列说法错误 的是
A. 约为
B.点a:C.点b:
D.水的电离程度: