文档内容
第 32 讲 无机化工流程题的解题策略
(模拟精练+真题演练)
完卷时间:50分钟
一、选择题(共12*5分)
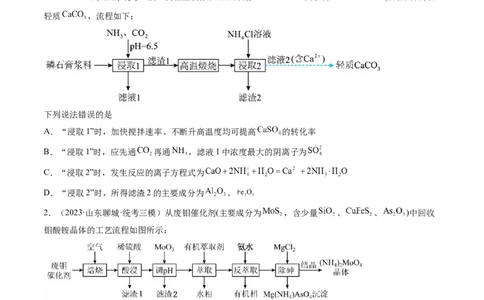
1.(2023·山东聊城·统考一模)实验室模拟以磷石膏(含 及杂质 、 等)为原料制取
轻质 ,流程如下:
下列说法错误的是
A.“浸取1”时,加快搅拌速率、不断升高温度均可提高 的转化率
B.“浸取1”时,应先通 再通 ,滤液1中浓度最大的阴离子为
C.“浸取2”时,发生反应的离子方程式为
D.“浸取2”时,所得滤渣2的主要成分为 、
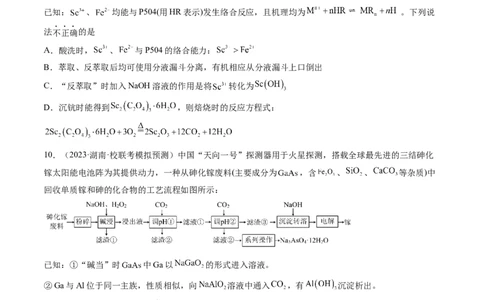
2.(2023·山东聊城·统考三模)从废钼催化剂(主要成分为 ,含少量 、 、 )中回收
钼酸铵晶体的工艺流程如图所示:
注:酸浸后钼元素以 形式存在,溶液中某离子浓度 时,认为沉淀完全;常温下
, 。下列说法错误的是
A.焙烧过程中被氧化的元素有Mo、S、Fe
B.滤渣1的主要成分是
C.“调pH”过程中调节溶液的pH略大于2.83,可除去目标杂质离子
D.反萃取发生的离子方程式为
3.(2023·江西·江西师大附中校联考模拟预测)近日,天津大学钟澄团队制备锌镍电池的负极材料——,流程如下,已知:离心分离是借助于离心力,使比重不同的物质进行分离的方法,下列叙
述错误的是
A.“反应池1”中发生的离子反应为
B.“反应池1”和“反应池2”可通过搅拌加快反应
C.“加热”时选择蒸发皿盛放ZnO和BiOI固体
D.“操作1”可以为离心分离,用于分离固体和液体混合物
4.(2023·山东菏泽·山东省鄄城县第一中学校考三模)加碘食盐中加入的碘酸钾是一种白色结晶粉末,常
温下很稳定,加热至560℃开始分解。在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐
等还原性物质反应。工业上生产碘酸钾的流程如下。
已知:20℃ 的溶解度为8.08g,50℃ 的溶解度为10.20g,100℃ 的溶解度为15.30g。
下列说法不正确的是
A.步骤①反应器发生的反应为
B.步骤②中可用氢氧化钠代替KOH
C.步骤②中氢氧化钾的主要作用是将 转化为
D.步骤③的操作为加热浓缩、冷却结晶
5.(2023·浙江温州·乐清市知临中学校考一模)辉铜矿[ ,含 杂质]合成
目标产物的流程如下。下列说法正确的是
A.步骤Ⅰ在足量 中煅烧产生气体的主要成分:
B.步骤Ⅱ得溶液 中溶质的主要成分: 和
C.步骤Ⅲ的溶液D中存在平衡平衡:D.为得纯净目标产物,步骤Ⅳ的实验操作步骤依次:加热蒸发、冷却结晶、抽滤洗涤。
6.(2023·福建泉州·泉州五中校考一模) 可作白色颜料,利用废液(含有 、 、 、 )
制备 的工艺流程如图所示。下列说法中错误的是
A.“还原”流程中,“滤渣”的成分有铜和铁
B.“水解”流程中,加水能够促进 的水解
C.“水解”流程的离子反应是
D.“洗涤”流程加入的稀盐酸能换成 溶液
7.(2023·山东济南·山东省实验中学校考模拟预测)连二亚硫酸钠( )常用于纺织工业、食品漂白
等领域。工业上生产 的流程如图所示。若在实验室模拟该工艺流程,下列说法错误的是
A.将锌粉投入
水中形成悬浮液主要是为了加快反应速率
B.向 溶液中加入NaCl固体对 的产率无明显影响
C.洗涤 时用乙醇效果好于蒸馏水
D.该流程中涉及化合反应、分解反应、复分解反应
8.(2023·福建泉州·福建省泉州第一中学校考模拟预测)以锆矿石(主要成分为 ,还含有 及钠、
铝、铜的氧化物等杂质)为原料制备工业纯 的工艺流程如图:
下列说法错误的是
A.“高温氯化”结束前通一段时间氧气的目的是除去过量的炭黑
B.“溶液1”中含有的溶质主要为NaCl、NaOH、
C.“碱浸”后分离操作要用到的玻璃仪器有烧杯、玻璃棒、漏斗D.“除杂”的目的是除去铜元素
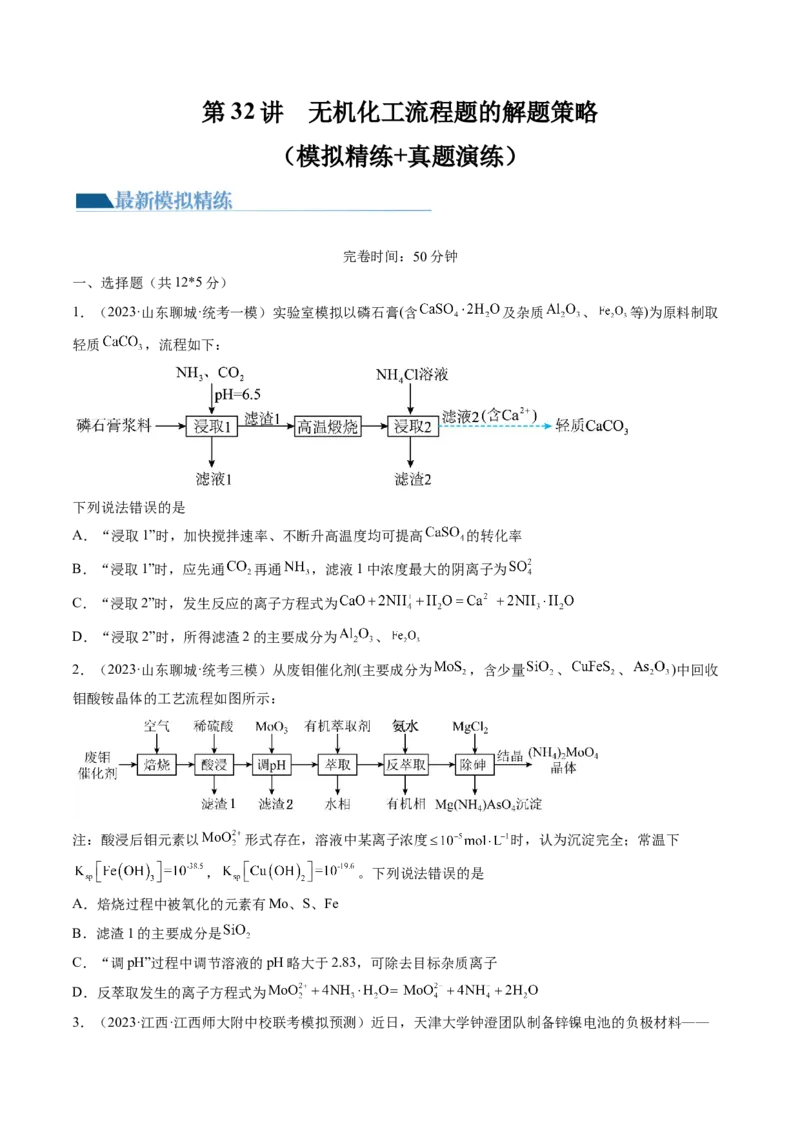
9.(2023·江苏连云港·连云港高中校考模拟预测)氧化钪( )广泛应用于航天、激光等科学领域。利用
钛白酸性废水(含 、 、 等)制备氧化钪的工艺具有较高的经济价值,其流程如下图所示。
已知: 、 均能与P504(用HR表示)发生络合反应,且机理均为 。下列说
法不正确的是
A.酸洗时, 、 与P504的络合能力:
B.萃取、反萃取后均可使用分液漏斗分离,有机相应从分液漏斗上口倒出
C.“反萃取”时加入NaOH溶液的作用是将 转化为
D.沉钪时能得到 ,则焙烧时的反应方程式:
10.(2023·湖南·校联考模拟预测)中国“天向一号”探测器用于火星探测,搭载全球最先进的三结砷化
镓太阳能电池阵为其提供动力,一种从砷化镓废料(主要成分为 ,含 、 、 等杂质)中
回收单质镓和砷的化合物的工艺流程如图所示:
已知:①“碱当”时 中Ga以 的形式进入溶液。
②Ga与Al位于同一主族,性质相似,向 溶液中通入 ,有 沉淀析出。
③离子完全沉淀时的pH: 为8, 为5.6。
下列说法正确的是
A.“碱浸”时, 发生的离子方程式为
B.“滤渣①”的成分为 , ,“滤渣③”的成分为
C.“调pH①”时,为使得杂质离子沉淀完全,可通入过量的
D.“系列操作”为蒸发结晶、过滤、洗涤、干燥
11.(2023·山东聊城·统考三模)用 氧化甲苯制备苯甲酸。实验方法:将甲苯和 溶液在100℃反应一段时间后停止反应,过滤,将含有苯甲酸钾( )和甲苯的滤液按如下流程分离出苯甲
酸和回收未反应的甲苯。下列说法不正确的是
已知:苯甲酸熔点122.4℃,在25℃和95℃时溶解度分别为 和 ;A.操作Ⅰ为分液、操作Ⅱ为过
滤
B.甲苯、苯甲酸分别由A、B获得
C.若B中含有杂质,采用重结晶的方法进一步提纯
D.“系列操作”用到的仪器有铁架台(含铁圈)、蒸发皿、酒精灯、玻璃棒、烧杯
12.(2023·辽宁·校联考模拟预测)氢氧化锆[ ]广泛应用于塑料、橡胶、交换树脂等多种化工行业。
实验室中以含锆废料(含 和少量Cu、Si、Al的氧化物)为原料制备氢氧化锆的工艺流程如下。
下列说法正确的是
A.“熔融”操作可在瓷坩埚中进行
B.“浸取”后通过分液可得到含有 和 的浸液
C. 与 形成配离子的稳定性强于 与 形成配离子的稳定性
D.可用浓 溶液洗涤 粗品
二、主观题(共3小题,共40分)
13.(12分)(2023·海南·校联考一模)以电镀污泥[含Ni(OH) 、Fe(OH) 、Cr(OH) 和SiO]为原料,利用
2 3 3 2
以下工艺可制备硫酸镍晶体(NiSO ·6H O)并获得副产品黄钠铁矾[NaFe (SO )(OH) ]。
4 2 3 4 2 6
已知:黄钠铁矾沉淀易于过滤,相对于Fe(OH) ,沉淀不易吸附Ni2+。
3
请回答下列问题:
(1)①下列措施不能提高“酸浸”过程浸出率的是 (填字母)。
a.适当升高反应温度 b.增大压强 c.不断搅拌②滤渣1的主要成分的化学式为 。
(2)“沉铁”时NaCO 加入速度不宜过快,原因是 。
2 3
(3)“沉铬”过程中发生反应的离子方程式为 。
(4)一系列操作的实验步骤依次如下,请补充相关内容:
i.过滤、洗涤;
ii.将沉淀转移至烧杯中,向其中 ;
iii. ,过滤得 晶体。
14.(14分)(2023·福建宁德·统考一模)钴盐在生活和生产中有着重要应用。
(1)在活性炭的催化作用下,通过氧化CoCl ·6H O制得到[Co(NH )]Cl 流程如下:
2 2 3 6 3
①在“氧化”过程,需水浴控温在50~60℃,温度不能过高,原因是: 。“系列操作”是指在高浓度
的盐酸中使[Co(NH )]Cl 结晶析出,过滤,醇洗,干燥。使用乙醇洗涤产品的具体操作是: 。
3 6 3
②结束后废水中的Co2+,人们常用FeS沉淀剂来处理,原理是 (用离子方程式表示)。
(2)草酸钴是制备钴氧化物的重要原料,常用(NH )C O 溶液和CoCl 溶液制取难溶于水的CoC O·2H O晶
4 2 2 4 2 2 4 2
体。
①常温下,(NH )C O 溶液的pH 7(填“>”、“=”或“<”)。(已知:常温下K(NH ·H O)=1.8×10-5,
4 2 2 4 b 3 2
HC O:K =5.6×10-2,K =5.4×10-5)
2 2 4 a1 a2
②制取CoC O·2H O晶体时,还需加入适量氨水,其作用是 。
2 4 2
③在空气中加热10.98g二水合草酸钴(CoC O·2H O),受热过程中在不同温度范围内分别得到一种固体物
2 4 2
质。已知Co的两种常见化合价为+2价和+3价,M(CoC O·2H O)=183g/mol。
2 4 2
温度范围/℃ 150~210 290~320
固体质量/g 8.82 4.82
i.温度在 范围内,固体物质为 (填化学式);
ii.从 加热到 时生成一种钴的氧化物和CO,此过程发生反应的化学方程式是 。
2
15.(14分)(2023·江西·江西师大附中校联考模拟预测)硫脲 称为硫代尿素,它是制造磺
胺药物的原料,用于合成抗甲状腺功能亢进药物等。150℃时硫脲部分异构化为 ,硫脲能溶于水
和乙醇,但不溶于乙醚等有机溶剂。一种制备硫脲的新工艺如图所示。反应原理:
。回答下列问题:
(1)“过滤”获得滤渣的主要成分是 (填化学式)。
(2)“合成”时,在反应釜中加入石灰氮 和水,边搅拌边通入 ,这样操作的目的是 。洗液、
母液循环回收于“合成”工序,这样操作的目的是 。
(3)宜选择下列试剂 洗涤“硫脲”晶体(填字母)。
A.水 B.75%酒棈 C.乙醚
(4)尿素、硫脲、聚乙烯醇熔融生成固体电解质(SPE)。用丙酮作溶剂(导电性很弱),浸取SPE得到丙酮浸出
液并进行如下实验:
①向浸出液中滴加1%盐酸,测得溶液导电率与盐酸浓度关系如图所示。
实验结果发现:CD段产生沉淀质量最大,用元素分析仪测定该沉淀仅含氮、氢、氯三种元素,进一步实
验发现,该沉淀有固定嫆点,与氢氧化钠浓溶液共热产生一种能使湿润的红色石蕊试纸变蓝色的气体,由
此推知,产生沉淀的成分是 (填化学式);BC段导电率降低的主要原因是 。
②向分离沉淀后的剩余溶液中滴加 溶液,溶液变为 色,说明固体电解质导电阴离子可能是
。
(5)测定固体电解质(SPE)中 含量。称取wg样品溶于水(没有发生化学变化),滴加2~3滴 溶
液,用 溶液滴定至终点,消耗滴定液的体积为VmL。
①则该SPE含 的质量分数为 %。
②如果先加热熔化SPE,再测得 含量,测得结果 (填“偏高”“偏低”或“无影响”)。已知:
滴定反应为 。
1.(2023·湖南·统考高考真题)金属 对 有强吸附作用,被广泛用于硝基或羰基等不饱和基团的催化
氢化反应,将块状 转化成多孔型雷尼 后,其催化活性显著提高。
已知:①雷尼 暴露在空气中可以自燃,在制备和使用时,需用水或有机溶剂保持其表面“湿润”;②邻硝基苯胺在极性有机溶剂中更有利于反应的进行。
某实验小组制备雷尼 并探究其催化氢化性能的实验如下:
步骤1:雷尼 的制备
步骤2:邻硝基苯胺的催化氢化反应
反应的原理和实验装置图如下(夹持装置和搅拌装置略)。装置Ⅰ用于储存 和监测反应过程。
回答下列问题:
(1)操作(a)中,反应的离子方程式是 ;
(2)操作(d)中,判断雷尼 被水洗净的方法是 ;
(3)操作(e)中,下列溶剂中最有利于步骤2中氢化反应的是___________;
A.丙酮 B.四氯化碳 C.乙醇 D.正己烷
(4)向集气管中充入 时,三通阀的孔路位置如下图所示:发生氢化反应时,集气管向装置Ⅱ供气,此时
孔路位置需调节为 ;
(5)仪器M的名称是 ;
(6)反应前应向装置Ⅱ中通入 一段时间,目的是 ;
(7)如果将三颈瓶N中的导气管口插入液面以下,可能导致的后果是 ;
(8)判断氢化反应完全的现象是 。
2.(2023·江苏·统考高考真题)实验室模拟“镁法工业烟气脱硫”并制备 ,其实验过程可表
示为(1)在搅拌下向氧化镁浆料中匀速缓慢通入 气体,生成 ,反应为
,其平衡常数K与 、 、 、
的代数关系式为 ;下列实验操作一定能提高氧化镁浆料吸收 效率的有
(填序号)。
A.水浴加热氧化镁浆料
B.加快搅拌速率
C.降低通入 气体的速率
D.通过多孔球泡向氧化镁浆料中通
(2)在催化剂作用下 被 氧化为 。已知 的溶解度为0.57g(20℃), 氧化溶液中
的离子方程式为 ;在其他条件相同时,以负载钴的分子筛为催化剂,浆料中 被 氧化的
速率随pH的变化如题图甲所示。在pH=6~8范围内,pH增大,浆料中 的氧化速率增大,其主要原
因是 。
(3)制取 晶体。在如题图乙所示的实验装置中,搅拌下,使一定量的 浆料与 溶液
充分反应。 浆料与 溶液的加料方式是 ;补充完整制取 晶体的实验方
案:向含有少量 、 的 溶液中, 。(已知: 、 在 时完全转化为氢氧
化物沉淀;室温下从 饱和溶液中结晶出 , 在150~170℃下干燥得到
,实验中需要使用MgO粉末)
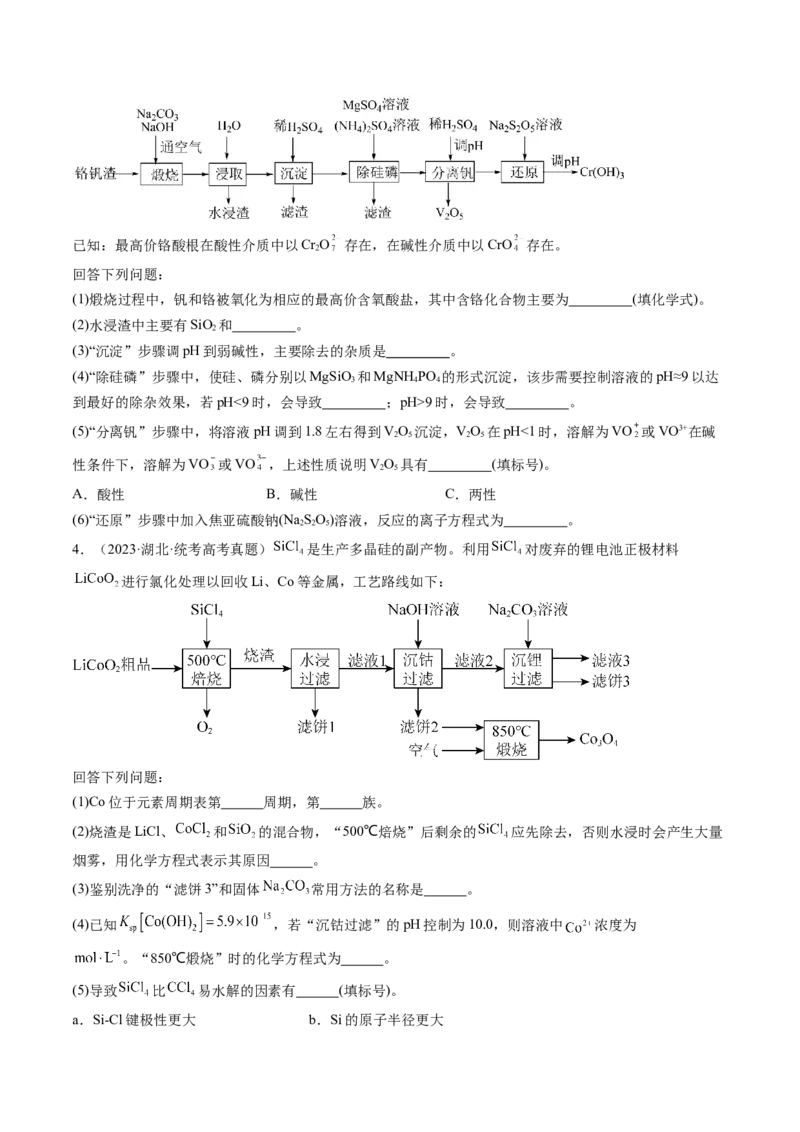
3.(2023·全国·统考高考真题)铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要
杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:已知:最高价铬酸根在酸性介质中以Cr O 存在,在碱性介质中以CrO 存在。
2
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为 (填化学式)。
(2)水浸渣中主要有SiO 和 。
2
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是 。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO 和MgNH PO 的形式沉淀,该步需要控制溶液的pH≈9以达
3 4 4
到最好的除杂效果,若pH<9时,会导致 ;pH>9时,会导致 。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到VO 沉淀,VO 在pH<1时,溶解为VO 或VO3+在碱
2 5 2 5
性条件下,溶解为VO 或VO ,上述性质说明VO 具有 (填标号)。
2 5
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na SO)溶液,反应的离子方程式为 。
2 2 5
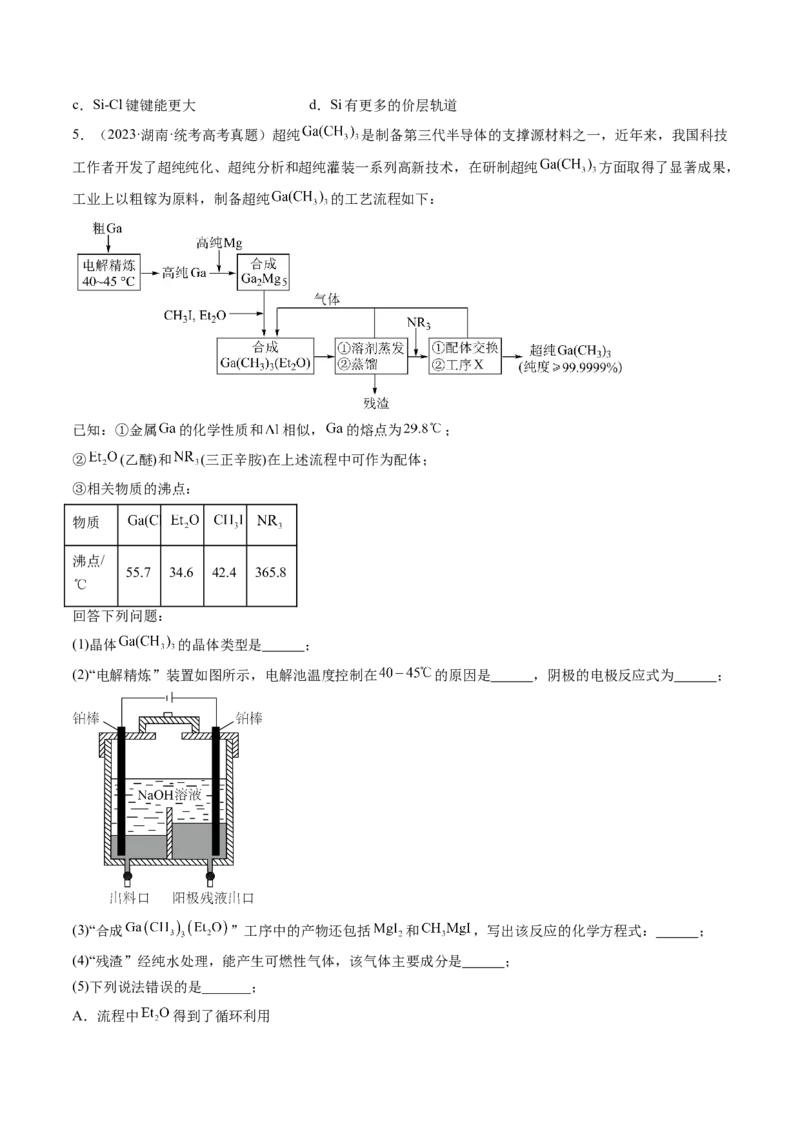
4.(2023·湖北·统考高考真题) 是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
进行氯化处理以回收Li、Co等金属,工艺路线如下:
回答下列问题:
(1)Co位于元素周期表第 周期,第 族。
(2)烧渣是LiCl、 和 的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量
烟雾,用化学方程式表示其原因 。
(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是 。
(4)已知 ,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
。“850℃煅烧”时的化学方程式为 。
(5)导致 比 易水解的因素有 (填标号)。
a.Si-Cl键极性更大 b.Si的原子半径更大c.Si-Cl键键能更大 d.Si有更多的价层轨道
5.(2023·湖南·统考高考真题)超纯 是制备第三代半导体的支撑源材料之一,近年来,我国科技
工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,
工业上以粗镓为原料,制备超纯 的工艺流程如下:
已知:①金属 的化学性质和 相似, 的熔点为 ;
② (乙醚)和 (三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:
物质
沸点/
55.7 34.6 42.4 365.8
回答下列问题:
(1)晶体 的晶体类型是 ;
(2)“电解精炼”装置如图所示,电解池温度控制在 的原因是 ,阴极的电极反应式为 ;
(3)“合成 ”工序中的产物还包括 和 ,写出该反应的化学方程式: ;
(4)“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是 ;
(5)下列说法错误的是_______;
A.流程中 得到了循环利用B.流程中,“合成 ”至“工序X”需在无水无氧的条件下进行
C.“工序X”的作用是解配 ,并蒸出
D.用核磁共振氢谱不能区分 和
(6)直接分解 不能制备超纯 ,而本流程采用“配体交换”工艺制备超纯
的理由是 ;
(7)比较分子中的 键角大小: (填“>”“<”或“=”),其原因是
。