文档内容
必做实验提升(六) 乙醇的催化氧化 酯化反应
实验一 乙醇的催化氧化
实验操作
红色光亮的铜丝灼烧后变为黑色,插入乙醇后铜丝又变为红
实验现象
色。反复几次后,闻到试管中的液体有刺激性气味
实验结论 在催化加热的条件下,乙醇发生了氧化反应
总化学方程式 2CHCH OH + O ――→ 2CH CHO + 2H O
3 2 2 3 2
问题讨论:
1.用化学方程式表示铜丝参与反应的过程:
(1) 2Cu + O ==== = 2CuO ,铜丝变黑。
2
(2) ,铜丝由黑变红。
2.在适当的条件下,生成的乙醛还可以被氧气氧化为乙酸。
3.乙醇还可以被酸性高锰酸钾溶液、重铬酸钾(K Cr O)溶液氧化为乙酸。
2 2 7
实验二 乙酸的酯化反应
在一支试管中加入3 mL乙醇,然后边振荡边慢慢加入2 mL浓硫酸和2 mL
实验操作 乙酸,再加入几片碎瓷片;按下图连接好装置,用酒精灯缓慢加热,将产
生的蒸气经导管通到饱和碳酸钠溶液的上方约0.5 cm处,观察现象
实验装置
实验现象 饱和碳酸钠溶液的液面上有透明的油状液体产生,并可闻到香味
在浓硫酸存在、加热的条件下,乙酸和乙醇发生反应,生成无色、透明、
实验结论
不溶于水、有香味的油状液体
化学方程式 CH COOH + C H OH CH COOC H + H O
3 2 5 3 2 5 2
问题讨论:1.酯化反应操作中的注意事项
(1)试剂加入顺序:乙醇、浓硫酸、乙酸。
(2)加热:对试管进行加热时应用小火缓慢加热,防止乙醇、乙酸大量挥发,提高产物产率。
(3)防暴沸:混合液中加入少量 沸石 ( 或碎瓷片 ),若忘记加 沸石 ( 或碎瓷片 ),应冷却至室温再
补加。
(4)防倒吸的方法:导管末端在 饱和 N aCO 溶液的液面以上或用球形干燥管代替导管。
2 3
2.仪器或药品的作用
(1)长导气管的作用是导气兼冷凝。
(2)浓硫酸在此实验中的作用:催化剂、吸水剂。
(3)饱和NaCO 溶液的作用:①降低乙酸乙酯的溶解度,便于分层得到乙酸乙酯;②中和挥
2 3
发出来的乙酸,便于闻到乙酸乙酯的气味;③溶解挥发出来的乙醇。
3.提高乙酸的转化率和乙酸乙酯产率的措施有哪些?
答案 ①使用浓硫酸作吸水剂;②加热将生成的酯蒸出;③适当增加乙醇的量;④利用长导
气管冷凝回流未反应的乙醇和乙酸。
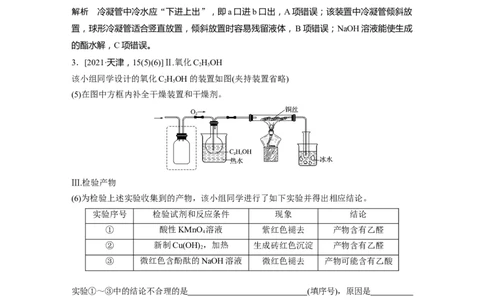
1.(2018·全国卷Ⅰ,9)在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是( )
答案 D
解析 A是生成乙酸乙酯的操作,B是收集乙酸乙酯的操作,C是分离乙酸乙酯的操作,D
是蒸发操作,在生成和纯化乙酸乙酯的实验过程中未涉及。
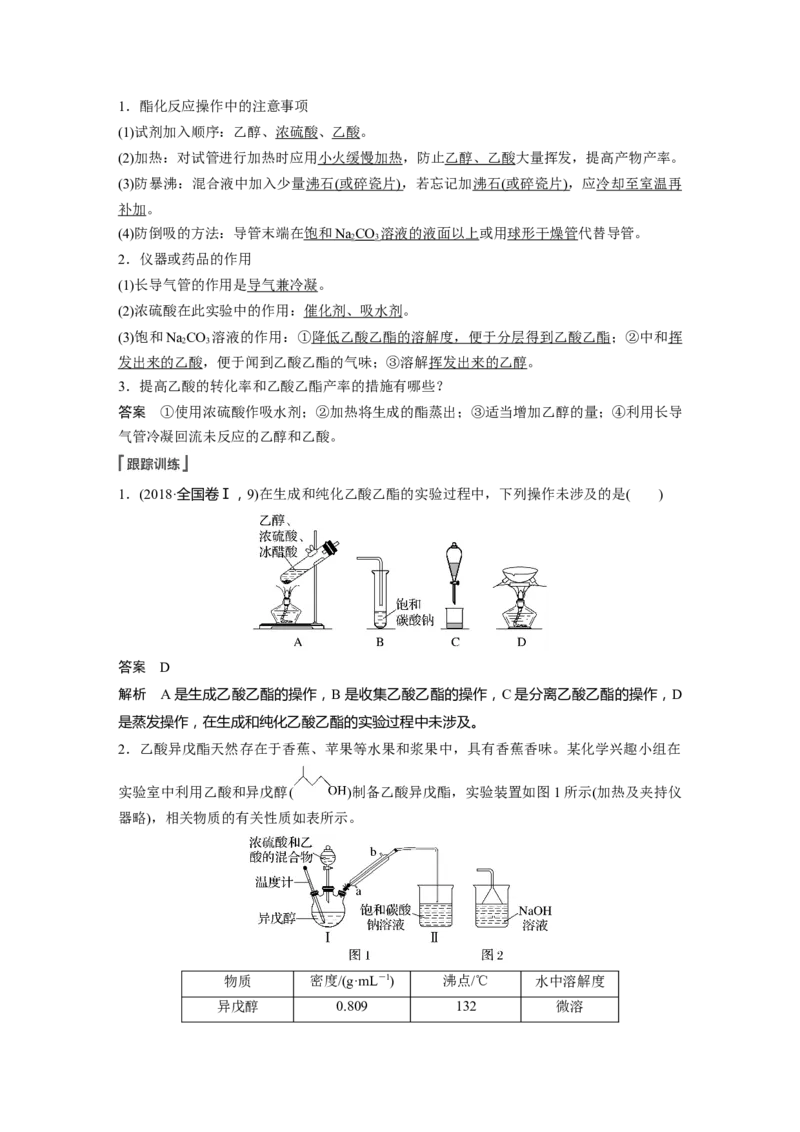
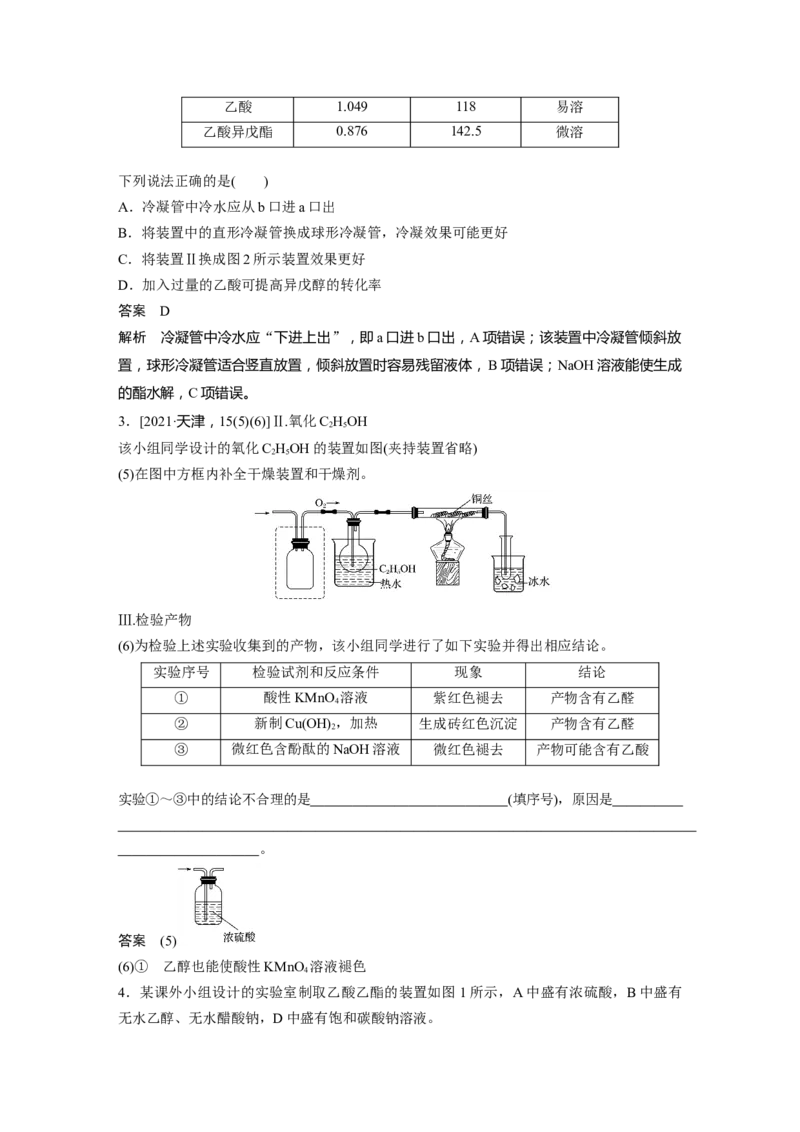
2.乙酸异戊酯天然存在于香蕉、苹果等水果和浆果中,具有香蕉香味。某化学兴趣小组在
实验室中利用乙酸和异戊醇( )制备乙酸异戊酯,实验装置如图1所示(加热及夹持仪
器略),相关物质的有关性质如表所示。
物质 密度/(g·mL-1) 沸点/℃ 水中溶解度
异戊醇 0.809 132 微溶乙酸 1.049 118 易溶
乙酸异戊酯 0.876 142.5 微溶
下列说法正确的是( )
A.冷凝管中冷水应从b口进a口出
B.将装置中的直形冷凝管换成球形冷凝管,冷凝效果可能更好
C.将装置Ⅱ换成图2所示装置效果更好
D.加入过量的乙酸可提高异戊醇的转化率
答案 D
解析 冷凝管中冷水应“下进上出”,即a口进b口出,A项错误;该装置中冷凝管倾斜放
置,球形冷凝管适合竖直放置,倾斜放置时容易残留液体,B项错误;NaOH溶液能使生成
的酯水解,C项错误。
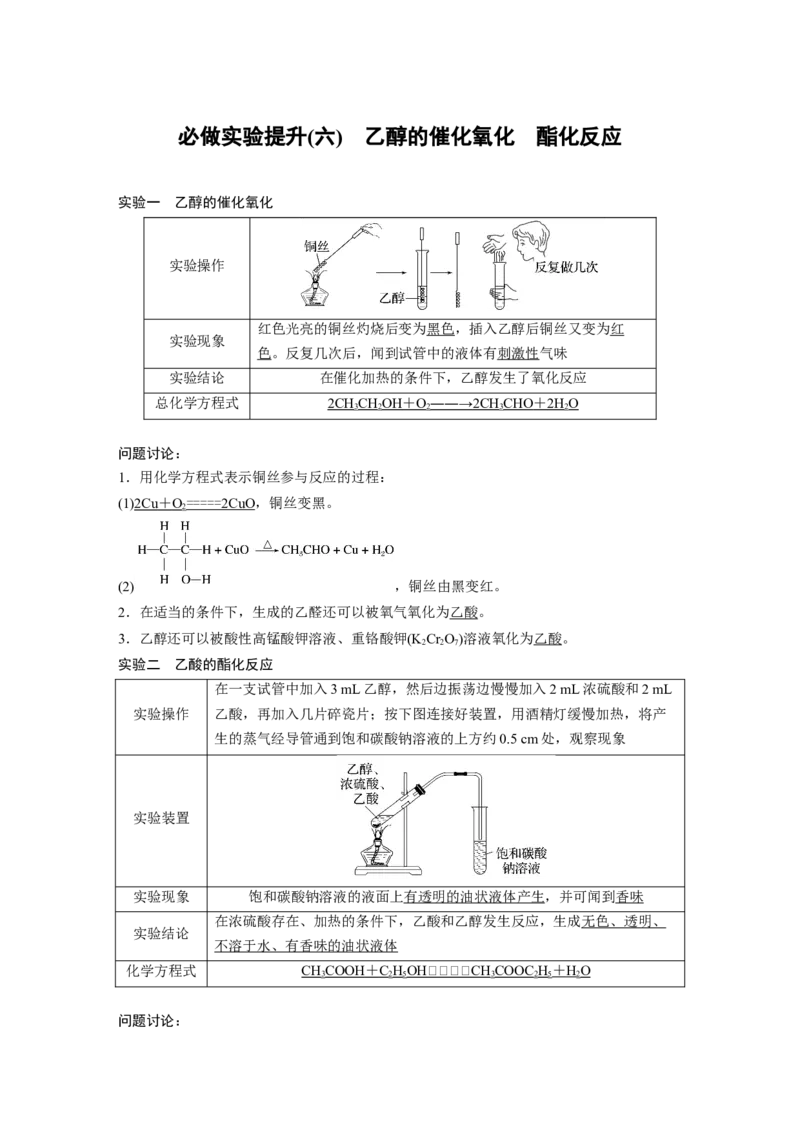
3.[2021·天津,15(5)(6)]Ⅱ.氧化C HOH
2 5
该小组同学设计的氧化C HOH的装置如图(夹持装置省略)
2 5
(5)在图中方框内补全干燥装置和干燥剂。
Ⅲ.检验产物
(6)为检验上述实验收集到的产物,该小组同学进行了如下实验并得出相应结论。
实验序号 检验试剂和反应条件 现象 结论
① 酸性KMnO 溶液 紫红色褪去 产物含有乙醛
4
② 新制Cu(OH) ,加热 生成砖红色沉淀 产物含有乙醛
2
③ 微红色含酚酞的NaOH溶液 微红色褪去 产物可能含有乙酸
实验①~③中的结论不合理的是 (填序号),原因是
。
答案 (5)
(6)① 乙醇也能使酸性KMnO 溶液褪色
4
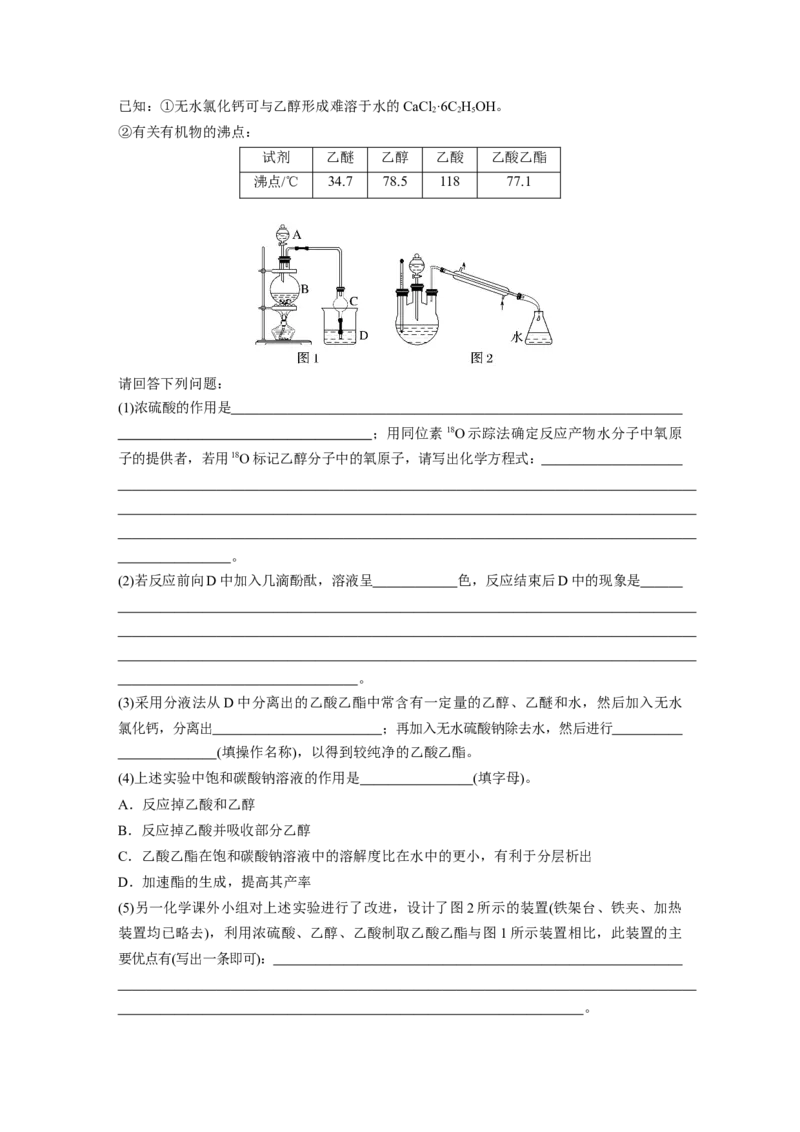
4.某课外小组设计的实验室制取乙酸乙酯的装置如图1所示,A中盛有浓硫酸,B中盛有
无水乙醇、无水醋酸钠,D中盛有饱和碳酸钠溶液。已知:①无水氯化钙可与乙醇形成难溶于水的CaCl ·6C HOH。
2 2 5
②有关有机物的沸点:
试剂 乙醚 乙醇 乙酸 乙酸乙酯
沸点/℃ 34.7 78.5 118 77.1
请回答下列问题:
(1)浓硫酸的作用是
;用同位素18O示踪法确定反应产物水分子中氧原
子的提供者,若用18O标记乙醇分子中的氧原子,请写出化学方程式:
。
(2)若反应前向D中加入几滴酚酞,溶液呈 色,反应结束后D中的现象是
。
(3)采用分液法从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,然后加入无水
氯化钙,分离出 ;再加入无水硫酸钠除去水,然后进行
(填操作名称),以得到较纯净的乙酸乙酯。
(4)上述实验中饱和碳酸钠溶液的作用是 (填字母)。
A.反应掉乙酸和乙醇
B.反应掉乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中的更小,有利于分层析出
D.加速酯的生成,提高其产率
(5)另一化学课外小组对上述实验进行了改进,设计了图2所示的装置(铁架台、铁夹、加热
装置均已略去),利用浓硫酸、乙醇、乙酸制取乙酸乙酯与图1所示装置相比,此装置的主
要优点有(写出一条即可):
。答案 (1)制取乙酸,作催化剂、吸水剂 CHCOOH+CHCH18OHCHCO18OC H +
3 3 2 3 2 5
HO (2)红 溶液分层,上层是无色油状液体,下层溶液颜色变浅 (3)乙醇 蒸馏 (4)BC
2
(5)增加了温度计,有利于控制发生装置中反应液的温度(或增加了冷凝装置,有利于收集产
物乙酸乙酯)
解析 (2)碳酸根离子水解使溶液呈碱性,加入几滴酚酞,溶液呈红色;乙酸乙酯不溶于饱
和碳酸钠溶液,密度比水小,溶液分层,上层是无色油状液体,乙酸和部分碳酸钠反应而使
溶液红色变浅。
(3)由于无水氯化钙可与乙醇形成难溶于水的CaCl ·6C HOH,所以加入无水氯化钙,可分离
2 2 5
出乙醇;再加入无水硫酸钠除去水,由于乙醚与乙酸乙酯的沸点相差较大,因此通过蒸馏可
以得到较纯净的乙酸乙酯。