文档内容
第2讲 物质的量浓度及其溶液的配制
【2020·备考】
最新考纲:1.了解溶液的含义。了解溶解度、饱和溶液的概念。2.了解溶液浓度的表
示方法,理解溶液中溶质的质量分数的概念,并能进行有关计算。3.了解物质的量
浓度的表示方法。掌握配制一定溶质质量分数溶液和物质的量浓度溶液的方法。4.
理解物质的量浓度的概念,并能进行有关计算。
核心素养:1.宏观辨识与微观探析:能从不同层次认识物质的多样性,能根据溶液
体积和溶质的物质的量浓度计算溶质的物质的量、溶质微粒数目。2.科学探究与创
新意识:能从问题和实际出发,确定探究目的,设计配制一定物质的量浓度溶液的
方案,进行实验探究;在探究中学会合作,能够正确分析实验过程中可能存在的误
差问题。
考点一 物质的量浓度及相关计算
(频数:★☆☆ 难度:★★☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师 课堂导语 物
质的量浓度及其计算的考查,一方面出现在阿伏加德罗常数题目的某个选项上,
与电解质溶液结合考查溶液中微粒浓度的变化,另一方面出现在二卷工艺流程或
实验题目上,定量分析所得物质的含量,复习时应在概念理解的基础上强化计算
能力。
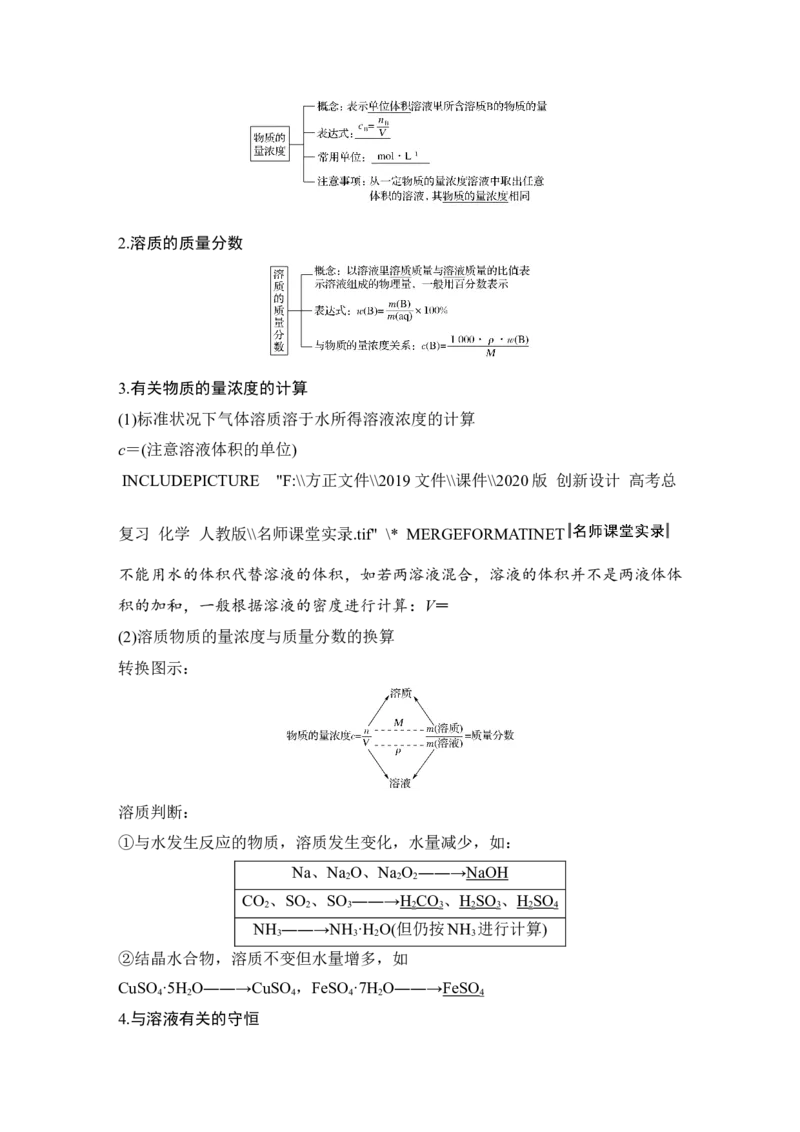
1.物质的量浓度2.溶质的质量分数
3.有关物质的量浓度的计算
(1)标准状况下气体溶质溶于水所得溶液浓度的计算
c=(注意溶液体积的单位)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
不能用水的体积代替溶液的体积,如若两溶液混合,溶液的体积并不是两液体体
积的加和,一般根据溶液的密度进行计算:V=
(2)溶质物质的量浓度与质量分数的换算
转换图示:
溶质判断:
①与水发生反应的物质,溶质发生变化,水量减少,如:
Na、Na O、Na O ――→NaOH
2 2 2
CO 、SO 、SO ――→H CO 、H SO 、H SO
2 2 3 2 3 2 3 2 4
NH ――→NH ·H O(但仍按NH 进行计算)
3 3 2 3
②结晶水合物,溶质不变但水量增多,如
CuSO ·5H O――→CuSO ,FeSO ·7H O――→FeSO
4 2 4 4 2 4
4.与溶液有关的守恒(1)溶液的稀释
①溶质的物质的量守恒,即有c ·V =c ·V 、c ·V +c ·V =c ·V 。
1 1 2 2 1 1 2 2 混 混
②溶质的质量守恒:ρ ·V · +ρ ·V · =(ρ ·V +ρ ·V )· 。
1 1w1 2 2w2 1 1 2 2 w混
(2)电荷守恒,如Na SO 溶液中存在c(Na+)=2c(SO)。
2 4
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
在分析电荷守恒时应注意溶质所形成的离子在溶液中的变化,如:1 mol·L-1
Al (SO ) 溶液中c(SO)=3 mol·L-1,但Al3+由于水解,其浓度小于2 mol·L-1。
2 4 3
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)1 mol·L-1 NaCl溶液是指此溶液中溶质NaCl为1 mol。(×)
(2)从100 mL 5 mol·L-1 H SO 溶液中取出了10 mL,所得硫酸的物质的量浓度为
2 4
0.5 mol·L-1。(×)
(3)标准状况下22.4 L HCl溶于1 L水,盐酸的物质的量浓度为1 mol·L-1。(×)
(4)31 g Na O溶于水,配成1 L溶液,c(Na O)=0.5 mol·L-1。(×)
2 2
(5)将25 g CuSO ·5H O晶体溶于75 g水中所得溶质的质量分数为25%。(×)
4 2
2.(教材改编题)[RJ必修1·P 4改编]将30 mL 0.5 mol·L-1 NaOH溶液加水稀释到
17
500 mL,关于稀释后的溶液叙述不正确的是( )
A.浓度为0.03 mol·L-1
B.从中取出10 mL溶液,其浓度为0.03 mol·L-1
C.稀释后的溶液中含NaOH 0.6 g
D.从中取出10 mL溶液,含NaOH 0.015 mol
解析 溶液稀释前后溶质的物质的量不变。从一定物质的量浓度的溶液中取出任
意体积的溶液,其浓度不变,但所含溶质的物质的量或质量因体积的不同而不同。
答案 D
3.(思维辨析题)观察两个试剂瓶上的标签,回答下列问题。(1)“5%硫酸铜溶液”中的5%是什么含义?
____________________________________________________________________。
答案 5%表示硫酸铜溶液中溶质的质量分数,即 100 g硫酸铜溶液中含有5 g硫
酸铜溶质
(2)0.4 mol·L-1 NaCl溶液中的0.4 mol·L-1表示的含义是什么?
_____________________________________________________________________
。
答案 1 L该NaCl溶液中所含NaCl的物质的量是0.4 molINCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2019·河北邯郸模拟)下列关于物质的量浓度表述正确的是( )
A.0.3 mol·L-1的Na SO 溶液中含有的Na+和SO的总物质的量为0.9 mol
2 4
B.当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol·L-1,只有当22.4 L氨气
溶于水制得1 L氨水时,其浓度才是1 mol·L-1
C.在K SO 和NaCl的中性混合水溶液中,如果Na+和SO的物质的量相等,则K+
2 4
和Cl-的物质的量浓度一定相同
D.10 ℃时,0.35 mol·L-1的KCl饱和溶液100 mL蒸发掉5 g 水,冷却到10 ℃时,
其体积小于100 mL,它的物质的量浓度仍为0.35 mol·L-1
解析 不知道溶液体积,无法计算物质的量,故A错误;22.4 L氨气的温度、压强
不知,物质的量不一定为1 mol,故B错误;K SO 和NaCl的中性混合水溶液中,
2 4
c(H+)=c(OH-),则c(K+)+c(Na+)=c(Cl-)+2c(SO),若Na+和SO物质的量相等,
则K+的浓度必定大于Cl-的浓度,故C错误;同一物质在同一温度下的溶解度一
定,饱和溶液的物质的量浓度恒定,故D正确。
答案 D
2.(2018·福建省德化一中、永安一中、漳平一中联考)若20 g密度为ρg·cm-3的
Ca(NO ) 溶液中含有2 g Ca(NO ) ,则溶液中NO的物质的量浓度为( )
3 2 3 2
A.mol/L B.mol/L
C.mol/L D.mol/L
解析 溶质的物质的量n== mol,溶液的体积V=×
10-3·mL-1=L,Ca(NO ) 的物质的量浓度c===mol·L-1,NO的物质的量浓度为
3 2
mol·L-1×2=mol·L-1。
答案 C
3.(1)在100 g物质的量浓度为c mol·L-1,密度为ρ g·cm-3的硫酸中加入一定量的
水稀释成 mol·L-1的硫酸,则加入水的体积________(填“=”、“>”或“<”,下同)100 mL。
(2)若把(1)中的H SO 改成氨水,应加入水的体积________100 mL。
2 4
(3)若把(1)(2)中的物质的量的浓度均改为溶质的质量分数,则加入水的体积
________100 mL。
解析 (1)·c=·
V =-100
水
由于ρ′<ρ,所以V <100 mL。
水
(2)由于ρ′>ρ,所以V >100 mL。
水
(3)根据质量分数=×100%知,溶质不变,质量分数减半,则溶液质量加倍,所以均
应加入100 mL水。
答案 (1)< (2)> (3)=
【规律总结】
1.同溶质不同物质的量浓度溶液的混合计算
(1)混合后溶液体积保持不变时,c V +c V =c ×(V +V )。
1 1 2 2 混 1 2
(2)混合后溶液体积发生改变时,c V +c V =c V ,其中V =。
1 1 2 2 混 混 混
2.溶质相同、质量分数不同的两溶液的混合规律
(1)等体积混合:当溶液密度大于1 g·cm-3时,混合后质量分数 >(a%+b%);
w
当溶液密度小于1 g·cm-3时,混合后质量分数 <(a%+b%)。
w
(2)等质量混合:混合后溶液中溶质的质量分数 =(a%+b%)。
w
[B组 考试能力过关]
4.(海南卷)把V L含有MgSO 和K SO 的混合溶液分成两等份,一份加入含a mol
4 2 4
NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl 的
2
溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为(
)
A.mol·L-1 B.mol·L-1
C.mol·L-1 D.mol·L-1
解析 设每份中镁离子的物质的量为x,硫酸根离子的物质的量为y,
则由Mg2++2OH-===Mg(OH) ↓可知,
21 2
x a mol
=,解得x=0.5a mol,
由Ba2++SO===BaSO ↓可知,
4
1 1
b mol y
=,解得y=b mol,
忽略溶液中的H+和OH-,由电荷守恒知,b×2=c(K+)+0.5a×2,溶液中K+的物
质的量为(b-0.5a)×2 mol=(2b-a)mol,又由于混合溶液分成两等份,则原溶液
中的K+的物质的量为2(2b-a)mol,则原混合溶液中钾离子的浓度为=mol·L-1,
故选D。
答案 D
5.[2017·课标全国Ⅰ,26(5)改动]凯氏定氮法是测定蛋白质中氮含量的经典方法,
其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,然后通过滴定测
量。已知:NH +H BO ===NH ·H BO ;NH ·H BO +HCl===NH Cl+ H BO 。
3 3 3 3 3 3 3 3 3 4 3 3
现取某甘氨酸(C H NO )样品m克进行测定,滴定时消耗浓度为c mol·L-1的盐酸
2 5 2
V mL,则样品中氮的质量分数为________%,样品的纯度≤________%。
解析 C H NO ~NH ~NH ·H BO ~HCl,样品中氮的质量分数为×100%=%。
2 5 2 3 3 3 3
样品的纯度≤×100%=%。
答案
考点二 一定物质的量浓度溶液的配制
(频数:★☆☆ 难度:★★☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 一
定物质的量浓度溶液的配制是高中重要的定量实验,容量瓶也是常考的重要仪器,
复习时在掌握配制过程的基础上,要学会从多个角度分析实验所产生的误差。
1.配制主要仪器——容量瓶
(1)构造及用途
(2)查漏操作
(3)注意事项
①选择容量瓶时遵循“大而近”的原则,所需溶质的量按所选用的容量瓶的规格
进行计算,不能配制任意体积的溶液。
②不能将固体或浓溶液直接在容量瓶中溶解或稀释,不能作为反应器或用来长期
贮存溶液。
③不能将过冷或过热的溶液转移到容量瓶中,因为容量瓶的容积是在瓶身所标温
度下确定。
④向容量瓶中注入液体时,要用玻璃棒引流;且玻璃棒下端要靠在容量瓶的刻度
线以下的瓶颈壁上。
2.配制辅助仪器
(1)托盘天平:称量前先调零,称量时药品放在左盘,砝码放在右盘,读数精确到0.1
g。
(2)胶头滴管:在试验中往试管或其他容器中滴入少量试剂,或用于量筒和容量瓶
的定容。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.一般情况下,托盘天平的最小砝码是游码的最大量程。
2.胶头滴管不能倒置,也不能平放于桌面上,应插入干净的瓶中或试管内。胶头滴
管加液时,不能伸入容器,更不能接触容器。
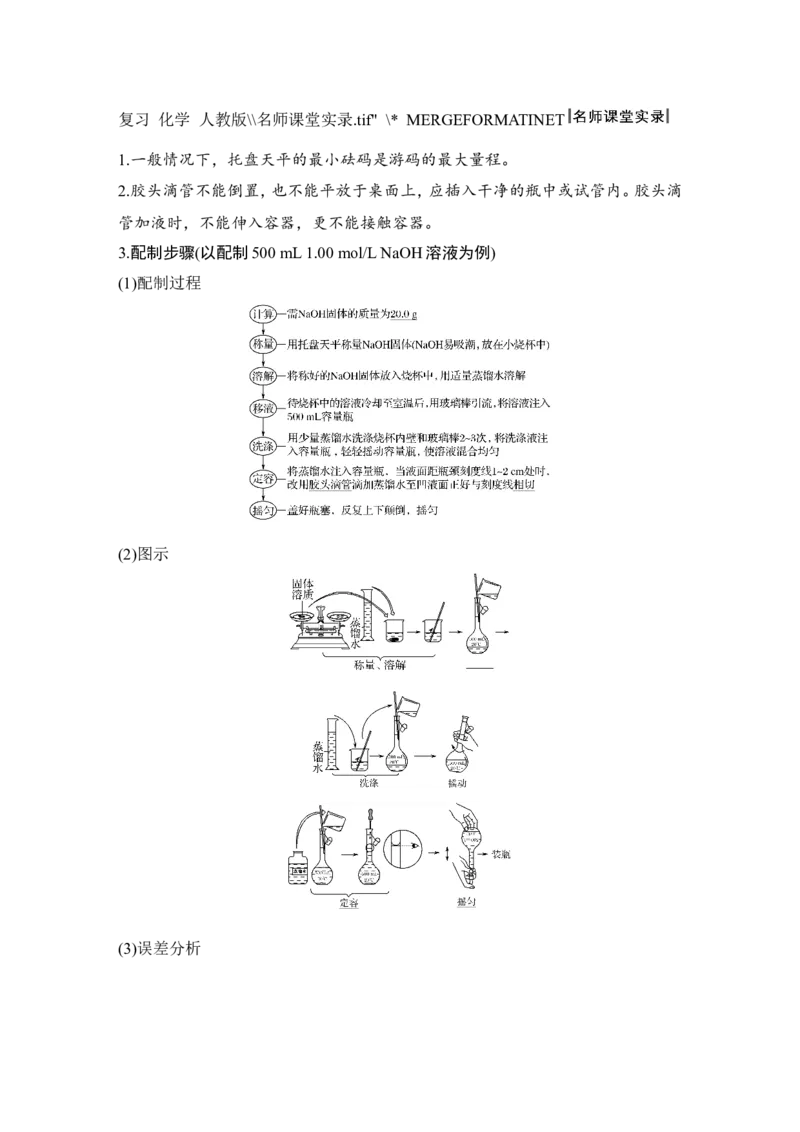
3.配制步骤(以配制500 mL 1.00 mol/L NaOH溶液为例)
(1)配制过程
(2)图示
(3)误差分析[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)使用托盘天平称量药品,都不能直接放在托盘中,均应放在两张相同的纸片上。
(×)
(2)为了配制方便,可将固体或浓溶液直接在容量瓶(或量筒)中进行溶解(或稀释)。
(×)
(3)配制溶液定容时,俯视容量瓶刻度会使溶液浓度偏高。(√)
(4)洗净的锥形瓶和容量瓶可以放进烘箱中烘干。(×)
(5)用固体NaCl配制0.5 mol·L-1的溶液,所用的仪器是烧杯、玻璃棒、胶头滴管、
容量瓶。(×)
2.(根据教材图示改编)下图是配制一定物质的量浓度溶液过程示意图中的几步,回
答下列问题:
(1)图示中几步正确的先后顺序应是________。
A.①②③④ B.③④②①
C.③②④① D.③④①②
(2)其中第①步表示的操作方法为________________________________________
____________________________________________________________________。
答案 (1)B (2)将蒸馏水缓缓注入容量瓶中,液面离容量瓶颈刻度线1~2 cm时
改用胶头滴管,滴加蒸馏水至凹液面与刻度线相切
3.(思维探究)(1)如何配制100 g 10%的NaCl溶液?
___________________________________________________________________________________________________________________________________________
。
(2)如何用浓硫酸配制50 mL体积比为1∶4的稀硫酸?
_____________________________________________________________________
____________________________________________________________________。
答案 (1)用托盘天平称取10 g NaCl固体,放入100 mL的烧杯中,再用100 mL量
筒量取90 mL的水注入烧杯中,然后用玻璃棒搅拌使之溶解
(2)用50 mL的量筒量取40 mL的水注入到100 mL的烧杯中,再用10 mL的量筒
量取10 mL浓硫酸,然后沿烧杯内壁缓缓注入烧杯中,并用玻璃棒不停搅拌
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(黑龙江模考)下列说法正确的是( )
A.现需480 mL 0.1 mol·L-1硫酸铜溶液,则使用容量瓶配制溶液需要7.68 g 硫酸
铜固体
B.配制1 mol·L-1 NaOH溶液100 mL,用托盘天平称量 4 g NaOH固体放入100
mL容量瓶中溶解
C.制备Fe(OH) 胶体,可向沸水中滴加FeCl 饱和溶液并继续煮沸至红褐色
3 3
D.使用量筒量取一定体积的浓硫酸配制一定物质的量浓度的稀硫酸,将浓硫酸转
移至烧杯后需用蒸馏水洗涤量筒,并将洗涤液一并转移至烧杯
解析 实验室没有480 mL的容量瓶,选择大于480 mL且相近规格的容量瓶,故
应选择500 mL容量瓶,配制500 mL 0.1 mol·L-1硫酸铜溶液需要硫酸铜的质量为
0.5 L×0.1 mol·L-1×160 g·mol-1=8.0 g,A错误;氢氧化钠固体应该在烧杯中溶
解,冷却后再转移至容量瓶,B错误;制备Fe(OH) 胶体时,向沸水中滴加FeCl 饱
3 3
和溶液并继续煮沸至红褐色即得到氢氧化铁胶体,C正确;量筒是量出式仪器,量
取的液体倒出的量就是所读的量,不能洗涤,如果洗涤并将洗涤液一并转移至烧
杯,实际量取浓硫酸的体积偏大,所配溶液的浓度偏高,D错误。
答案 C2.下列实验操作会导致实验结果偏低的是( )
①配制100 g 10%的Na CO 溶液,称取10.0 g碳酸钠晶体溶于90.0 g水中 ②测
2 3
定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮 ③配制一定物质的
量浓度的溶液时,药品与砝码放反了,游码读数为0.2 g,所得溶液的浓度 ④用酸
式滴定管取用98%、密度为1.84 g·cm-3的浓硫酸配制200 mL 2 mol·L-1的稀硫酸
时,先平视后仰视
A.只有① B.只有②
C.②③④ D.①③④
解析 ①10.0 g碳酸钠晶体中含Na CO 的质量小于10.0 g;②碳酸钠晶体已经受
2 3
潮时,其中的含水量增加,结果偏高;③中所称样品的质量比实际所需质量小0.4
g;④用酸式滴定管量取液体时,先平视后仰视,则量取的液体体积偏小,所配溶液
浓度偏低。
答案 D
3.(2019·陕西省西安中学第一次摸底考试)已知某“84消毒液”瓶体部分标签如
图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
(1)该“84消毒液”的物质的量浓度约为________mol·L-1。(保留小数点后一位)
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=
________ mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质
量分数为25%的消毒液。
下列说法正确的是________(填字母)。
A.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
C.需要称量NaClO固体的质量为143.0 g
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密
度为1.84 g·cm-3)的浓硫酸配制2 L 2.3 mol·L-1的稀硫酸用于增强“84消毒液”
的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为________mol·L-1。
②需用浓硫酸的体积为________mL。
解析 (1)由c=得,c(NaClO)=≈4.0(mol·L-1)。(2)稀释前后溶液中NaClO的物质
的量不变,则有100 mL×10-3L·mL-1×4.0 mol·L-1=100 mL×100×10-3L·mL-
1×c(NaClO),解得稀释后c(NaClO)=0.04 mol·L-1,
c(Na+)=c(NaClO)=0.04 mol·L-1。(3)选项A,配制过程中需要加入水,所以未洗涤
干净的容量瓶不必烘干后再使用。选项 B,未洗涤烧杯和玻璃棒将导致配制的溶
液中溶质的物质的量减小,结果偏低。选项C,应选取500 mL的容量瓶进行配制,
然后取出480 mL即可,所以需要NaClO的质量为0.5 L×0.4 mol·L-1×
74.5 g·mol-1=149.0 g。(4)①根据H SO 的组成可知,溶液中c(H+)=2c(H SO )=
2 4 2 4
4.6 mol·L-1。②2 L 2.3 mol·L-1的稀硫酸中溶质的物质的量为2 L×2.3 mol·L-1=
4.6 mol,设需要 98%(密度为 1.84 g·cm-3)的浓硫酸的体积为 V mL,则有=4.6
mol,解得V=250。
答案 (1)4.0 (2)0.04 (3)B (4)①4.6 ②250
【归纳总结】
观察液体体积时仰视或俯视引起误差分析
1.配制定容时,视线引起误差分析
(1)仰视刻度线(图1),导致溶液体积偏大,结果偏低。
(2)俯视刻度线(图2),导致溶液体积偏小,结果偏高。
2. 不同仪器的仰视和俯视
(1)了解仪器的构造,特别是刻度是由下而上,还是由上而下。
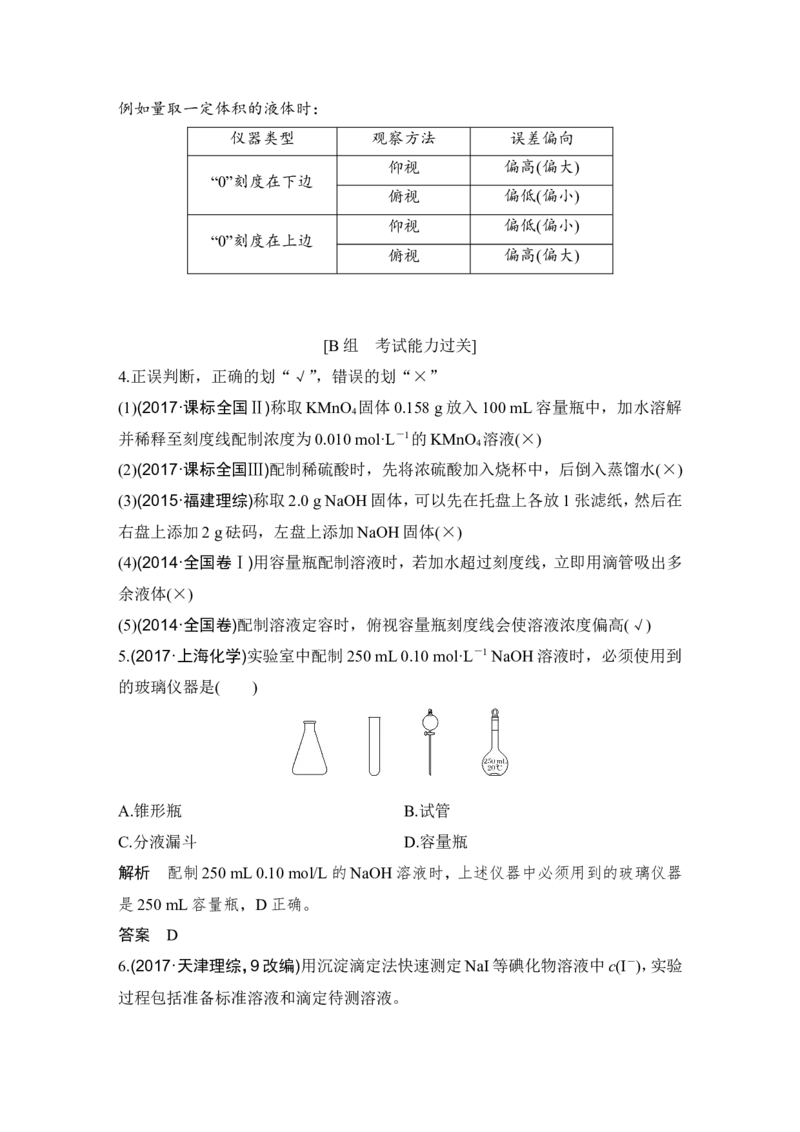
(2)先画出正确的读数方法及数值,再比较仰视和俯视的情况。例如量取一定体积的液体时:
仪器类型 观察方法 误差偏向
仰视 偏高(偏大)
“0”刻度在下边
俯视 偏低(偏小)
仰视 偏低(偏小)
“0”刻度在上边
俯视 偏高(偏大)
[B组 考试能力过关]
4.正误判断,正确的划“√”,错误的划“×”
(1)(2017·课标全国Ⅱ)称取KMnO 固体0.158 g放入100 mL容量瓶中,加水溶解
4
并稀释至刻度线配制浓度为0.010 mol·L-1的KMnO 溶液(×)
4
(2)(2017·课标全国Ⅲ)配制稀硫酸时,先将浓硫酸加入烧杯中,后倒入蒸馏水(×)
(3)(2015·福建理综)称取2.0 g NaOH固体,可以先在托盘上各放1张滤纸,然后在
右盘上添加2 g砝码,左盘上添加NaOH固体(×)
(4)(2014·全国卷Ⅰ)用容量瓶配制溶液时,若加水超过刻度线,立即用滴管吸出多
余液体(×)
(5)(2014·全国卷)配制溶液定容时,俯视容量瓶刻度线会使溶液浓度偏高(√)
5.(2017·上海化学)实验室中配制250 mL 0.10 mol·L-1 NaOH溶液时,必须使用到
的玻璃仪器是( )
A.锥形瓶 B.试管
C.分液漏斗 D.容量瓶
解析 配制250 mL 0.10 mol/L的NaOH溶液时,上述仪器中必须用到的玻璃仪器
是250 mL容量瓶,D正确。
答案 D
6.(2017·天津理综,9改编)用沉淀滴定法快速测定NaI等碘化物溶液中c(I-),实验
过程包括准备标准溶液和滴定待测溶液。准备标准溶液
a.准确称取AgNO 基准物4.246 8 g(0.0250 mol)后,配制成250 mL标准溶液,放
3
在棕色试剂瓶中避光保存,备用。
b.配制并标定100 mL 0.100 0 mol·L-1 NH SCN标准溶液,备用。
4
(1)将称得的 AgNO 配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有
3
_____________________________________________________________________。
(2)AgNO 标 准 溶 液 放 在 棕 色 试 剂 瓶 中 避 光 保 存 的 原 因 是
3
____________________________________________________________________。
(3)若在配制AgNO 标准溶液时,烧杯中的溶液有少量溅出,则配制的AgNO 浓度
3 3
________(填“偏高”、“偏低”、“无影响”),则对 c(I-)测定结果的影响是
________。
答案 (1)250 mL(棕色)容量瓶、胶头滴管
(2)避免AgNO 见光分解
3
(3)偏低 偏高
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\分层课时作业.TIF" \* MERGEFORMATINET
[A级 全员必做题]
1.用浓盐酸配制1∶1(体积比)的稀盐酸(约6 mol/L)100 mL,应选用的定量仪器是(
)
A.量筒 B.滴定管
C.50 mL容量瓶 D.100 mL容量瓶
解析 用浓盐酸配制1∶1(体积比)的稀盐酸(约6 mol/L)100 mL,操作为用量筒分
别量取浓盐酸50 mL和水50 mL,将两者混合得到溶液,所以应选择量筒。
答案 A
2.(2019·山西太原模拟)配制一定物质的量浓度的NaCl溶液时,下列操作不正确
的是( )解析 称量固体时,当接近称量质量时,应用左手拿药匙,右手轻轻振动左手手腕,
图示操作正确,故A不选;为防止溶解和洗涤时所用蒸馏水的体积超过容量瓶容
积,溶解时应用量筒控制所加蒸馏水的量,图示操作正确,故B不选;移液时,玻璃
棒应插在刻度线以下,故选C;定容时,当液面接近刻度线1~2 cm时,用胶头滴
管滴加蒸馏水至刻度线,图示操作正确,故D不选。
答案 C
3.配制100 mL 1.0 mol·L-1 Na CO 溶液,下列操作正确的是( )
2 3
A.称取10.6 g 无水碳酸钠,加入100 mL容量瓶中,加水溶解、定容
B.称取10.6 g无水碳酸钠置于烧杯中,加入100 mL蒸馏水,搅拌、溶解
C.转移Na CO 溶液时,未用玻璃棒引流,直接倒入容量瓶中
2 3
D.定容后,塞好瓶塞,反复倒转、摇匀
解析 固体不能直接在容量瓶中溶解,A项错误;配制100 mL 1 mol·L-1 Na CO
2 3
溶液,所用水的体积并不是100 mL,而是加水至100 mL,B项错误;转移液体时,
要用玻璃棒引流,C项错误。
答案 D
4.(2019·洛阳模拟)下列溶液中Cl-的物质的量浓度最大的是( )
A.200 mL 2.5 mol·L-1 MgCl 溶液
2
B.1 000 mL 2.5 mol·L-1 NaCl溶液
C.250 mL 1 mol·L-1 AlCl 溶液
3
D.300 mL 5 mol·L-1 KClO 溶液
3
解析 溶液中c(Cl-)=溶质的物质的量浓度×化学式中氯离子个数,与溶液的体积无关。200 mL 2.5 mol·L-1 MgCl 溶液中c(Cl-)=2c(MgCl )=2.5 mol·L-1×2=5
2 2
mol·L-1;1 000 mL 2.5 mol·L-1 NaCl溶液中c(Cl-)=c(NaCl)=2.5 mol·L-1;250
mL 1 mol·L-1 AlCl 溶液中c(Cl-)=3c(AlCl )=1 mol·L-1×3=3 mol·L-1;氯酸钾
3 3
溶液中不含氯离子,所以氯离子的物质的量浓度是0。
答案 A
5.取100 mL 0.3 mol·L-1和300 mL 0.25 mol·L-1的硫酸注入500 mL容量瓶中,加
水稀释至刻度线,该混合溶液中H+的物质的量浓度是( )
A.0.21 mol·L-1 B.0.42 mol·L-1
C.0.56 mol·L-1 D.0.26 mol·L-1
解析 容量瓶中 n(H+)=(0.1 L×0.3 mol·L-1+0.3 L×0.25 mol·L-1)×2=0.21
mol,所以c(H+)==0.42 mol·L-1。
答案 B
6.(2018·安徽模拟)某乙醇水溶液的质量分数为 %,物质的量浓度为c mol·L-1,
w
密度为d g·mL-1,1 kg 这种溶液中含有的乙醇是( )
A.46c g B.c/d mol
C.c mol D.1 000d g
w
解析 乙醇的质量为 m=1 000 g× %=10 g;溶液的体积为 V=1 000 g÷d
w w
g·mL-1=(1 000÷d)mL=1/d L。所以乙醇的物质的量为n=c·V=c mol·L-1×1/d L
=c/d mol。故选B。
答案 B
7.(2018·江苏徐州模拟)下列关于0.2 mol·L-1Ba(NO ) 溶液的说法中,正确的是(
3 2
)
A.溶液中含有的阴、阳离子总数为0.6 mol
B.在0.5 L该溶液中,Ba2+的浓度为0.1 mol·L-1
C.在500 mL该溶液中,含有0.2 mol NO
D.取1 L该溶液稀释到10 L时,NO的浓度为0.02 mol·L-1
解析 由于缺少溶液体积,无法计算硝酸钡的物质的量,也就不能求出阴、阳离子
总数,故A项错误;c(Ba2+)=c[Ba(NO ) ]=0.2 mol·L-1,c(Ba2+)=0.2 mol·L-1,不
3 2随溶液体积而发生变化,故 B项错误;n(NO)=2c[Ba(NO ) ]·V=2×0.2 mol·L-
3 2
1×0.5 L=0.2 mol,故 C 项正确;0.2 mol·L-1Ba(NO ) 溶液中 NO 的浓度为 0.4
3 2
mol·L-1,取1 L该溶液稀释到10 L时,稀释过程中溶质的物质的量不变,c(NO)=
=0.04 mol·L-1,故D项错误。
答案 C
8.利用碳酸钠晶体(Na CO ·10H O)来配制0.5 mol/L的碳酸钠溶液1 000 mL,假如
2 3 2
其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是( )
A.称取碳酸钠晶体100 g
B.定容时俯视刻度线
C.移液时,没有对用于溶解碳酸钠晶体的烧杯进行冲洗
D.定容、摇匀、静置后发现液面低于刻度线,于是又加入少量水至刻度线
解析 配制0.5 mol/L的碳酸钠溶液1 000 mL需称取Na CO ·10H O 143 g,称取
2 3 2
100 g 碳酸钠晶体,浓度偏低;定容时俯视刻度线,会造成所配溶液的体积偏小,浓
度偏高,B符合题意;未冲洗溶解碳酸钠晶体的烧杯,会造成碳酸钠损失,浓度偏
低;发现液面低于刻度线,又加少量水导致浓度偏低。
答案 B
9.(2018·潍坊质检)有硫酸镁溶液500 mL,它的密度是1.20 g·cm-3,其中镁离子的
质量分数是4.8%,则有关该溶液的说法不正确的是( )
A.溶质的质量分数是24.0%
B.溶液的物质的量浓度是2.4 mol·L-1
C.溶质和溶剂的物质的量之比是1∶40
D.硫酸根离子的质量分数是19.2%
解析 由Mg2+的质量分数知MgSO 的质量分数为×4.8%=24.0%,其浓度为c=
4
=2.4 mol·L-1,溶质与溶剂的物质的量之比为∶≈1∶21,SO 的质量分数为
×4.8%=19.2%。
答案 C
10.在花瓶中加入“鲜花保鲜剂”可延长鲜花的寿命。下表是1 L“鲜花保鲜剂”的
成分,阅读后回答下列问题:
成分 质量/g 摩尔质量/(g·mol-1)
蔗糖 50.00 342硫酸钾 0.50 174
阿司匹林 0.35 180
高锰酸钾 0.50 158
硝酸银 0.04 170
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是________(填写名称)。
(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林中不含K+)________(只要
求写表达式,不需计算)mol·L-1。
(3)下图所示的仪器中,在配制“鲜花保鲜剂”溶液时肯定不需要的是
________(填字母),还缺少的仪器有________(填仪器名称)。
(4)配制过程中,下列操作对配制结果没有影响的是________(双选;填选项字母)。
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视液面
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)欲确定“鲜花保鲜剂”中硝酸银的浓度,则加入的试剂中应含有________(填
化学符号)。
解析 通过n=m÷M可以计算1 L“鲜花保鲜剂”中含有的各种成分的物质的量,
会得到其中含有的蔗糖的物质的量最大,故其浓度最大。(2)“鲜花保鲜剂”中K+
的物质的量为n(K+)=2n(K SO )+n(KMnO )=mol,所以c(K+)=mol·L-1。(3)配
2 4 4
制一定浓度的溶液必需的仪器:烧杯、玻璃棒、胶头滴管、容量瓶,故答案为a、c,
还缺少的仪器有托盘天平、烧杯、玻璃棒。(4)容量瓶在使用前未干燥,里面有少量
蒸馏水,对溶液的浓度不产生任何影响,A项正确;定容时仰视液面,溶液的体积
偏大,使溶液的浓度偏低,B项错误;容量瓶在使用前刚刚配制完一定物质的量浓
度的NaCl溶液而未洗净,NaCl与AgNO 反应,会使溶液的浓度偏小,C项错误;
3
定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理,对配制的溶液的浓
度不产生任何影响,D项正确;(5)欲确定“鲜花保鲜剂”中硝酸银的浓度,可利用
反应:Ag++Cl-===AgCl↓,加入的试剂中需含有Cl-。答案 (1)蔗糖 (2)2×+ (3)ac 托盘天平、玻璃棒、烧杯 (4)AD (5)Cl-
11.(2018·莱芜一中检测)在标准状况下,将224 L HCl气体溶于635 mL水中,所得
盐酸的密度为1.18 g·cm-3。试计算:
(1)所得盐酸的质量分数和物质的量浓度分别是________、________。
(2)取这种盐酸100 mL,稀释至1.18 L,所得稀盐酸的物质的量浓度是________。
(3)在40.0 mL 0.065 mol·L-1 Na CO 溶液中,逐滴加入上述稀释后的稀盐酸,边加
2 3
边振荡。若使反应不产生 CO 气体,加入稀盐酸的体积的量最多不超过
2
________mL。
解析 (1)n(HCl)==10 mol,
m(HCl)=10 mol×36.5 g·mol-1=365 g,
盐酸的质量分数 =×100%=36.5%,
w
c(HCl)==
=11.8 mol·L-1。
(2)由c(浓)·V(浓)=c(稀)·V(稀)可知,
c(稀)=11.8 mol·L-1×=1 mol·L-1。
(3)n(Na CO )=0.040 L×0.065 mol·L-1=0.002 6 mol,设加入稀盐酸的体积最多不
2 3
超过 x mL,则 n(HCl)=1 mol·L-1×0.001x L=0.001x mol,根据反应 Na CO +
2 3
HCl===NaHCO +NaCl得0.002 6=0.001x,x=2.6。
3
答案 (1)36.5% 11.8 mol·L-1 (2)1 mol·L-1 (3)2.6
[B级 拔高选做题]
12.(2019·哈尔滨师范大学附属中学月考)质量分数为a的某物质的溶液 m g与质
量分数为b的该物质的溶液ng混合后,蒸发掉p g水,得到的溶液每毫升质量为q
g,物质的量浓度为c。则该溶质的相对分子质量为( )
A. B.
C. D.
解析 混合后的溶液中该物质的总质量为(am+bn)g,设该物质的摩尔质量为M
g/mol,则总物质的量为mol。混合后溶液的体积为L,所以可得物质的量浓度c=
mol/L,整理得M=g/mol,又因为当摩尔质量的单位为g/mol时,物质的相对分子
质量与物质的摩尔质量在数值上相等,故C项正确。综上所述,本题正确答案为C。
答案 C
13.在t ℃时,将a g CH COOH完全溶于水,得到V mL溶液,设该溶液的密度为ρ
3
g·cm-3,质量分数为 ,其中含CH COO-的物质的量为b mol。下列叙述不正确的
w 3
是( )
A.溶质质量分数 =×100%
w
B.溶质物质的量浓度c=mol·L-1
C.溶液中c(H+)=mol·L-1+c(OH-)
D.再加入V mL水后,溶质质量分数大于0.5
w
解析 溶质质量分数 =×100%,A错误;物质的量浓度c=mol·L-1
w
=mol·L-1,B正确;c(H+)=c(CH COO-)+c(OH-)=mol·L-1+c(OH-),C正确;醋
3
酸溶液的密度大于纯水的密度,混合后溶质的质量不变而溶液的质量小于原溶液
的2倍,故混合溶液中溶质的质量分数大于原溶液的一半,D正确。
答案 A
14.人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量
的草酸铵[(NH ) C O ]溶液,可析出草酸钙(CaC O )沉淀,将此草酸钙沉淀洗涤后
4 2 2 4 2 4
溶于强酸可得草酸(H C O ),再用KMnO 溶液滴定即可测定血液样品中Ca2+的浓
2 2 4 4
度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
【配制KMnO 标准溶液】如图是配制50 mL KMnO 标准溶液的过程示意图。
4 4(1)请你观察图示判断,其中不正确的操作有________(填序号)。
(2)其中确定50 mL溶液体积的容器是________(填名称)。
(3)如果用图示的操作配制溶液,所配制的溶液浓度将________(填“偏大”或
“偏小”)。
【测定血液样品中Ca2+的浓度】抽取血样20.00 mL,经过上述处理后得到草酸,再
用0.020 mol/LKMnO 溶液滴定,使草酸转化成CO 逸出,这时共消耗12.00 mL
4 2
KMnO 溶液。
4
(4)已知草酸跟KMnO 溶液反应的离子方程式为2MnO+5H C O +6H+===2Mnx
4 2 2 4
++10CO ↑+8H O则方程式中的x=________。
2 2
(5)经过计算,血液样品中Ca2+的浓度为________mg/cm3。
解析 (1)由图示可知②⑤操作不正确。②不能在量筒中溶解固体,⑤定容时应平
视刻度线,至溶液凹液面最低处与刻度线相切。(2)应该用50 mL容量瓶准确确定
50 mL溶液的体积。(3)如果用图示的操作配制溶液,由于仰视刻度线,会使溶液体
积偏大,所配制的溶液浓度将偏小。(4)根据电荷守恒,草酸跟KMnO 溶液反应的
4
离子方程式为2MnO+5H C O +6H+===2Mn2++10CO ↑+8H O。(5)据方程式
2 2 4 2 2
及 CaC O 化 学 式 存 在 如 下 关 系 : n(Ca2 + ) = n(H C O ) = n(KMnO ) =
2 4 2 2 4 4
×0.02×12.00×10-3mol=6×10-4mol,Ca2+的质量为6×10-4×40 g=0.024 g,则
血液中Ca2+的浓度==1.2 mg/cm3。
答案 (1)②⑤ (2)50 mL容量瓶 (3)偏小 (4)2 (5)1.2