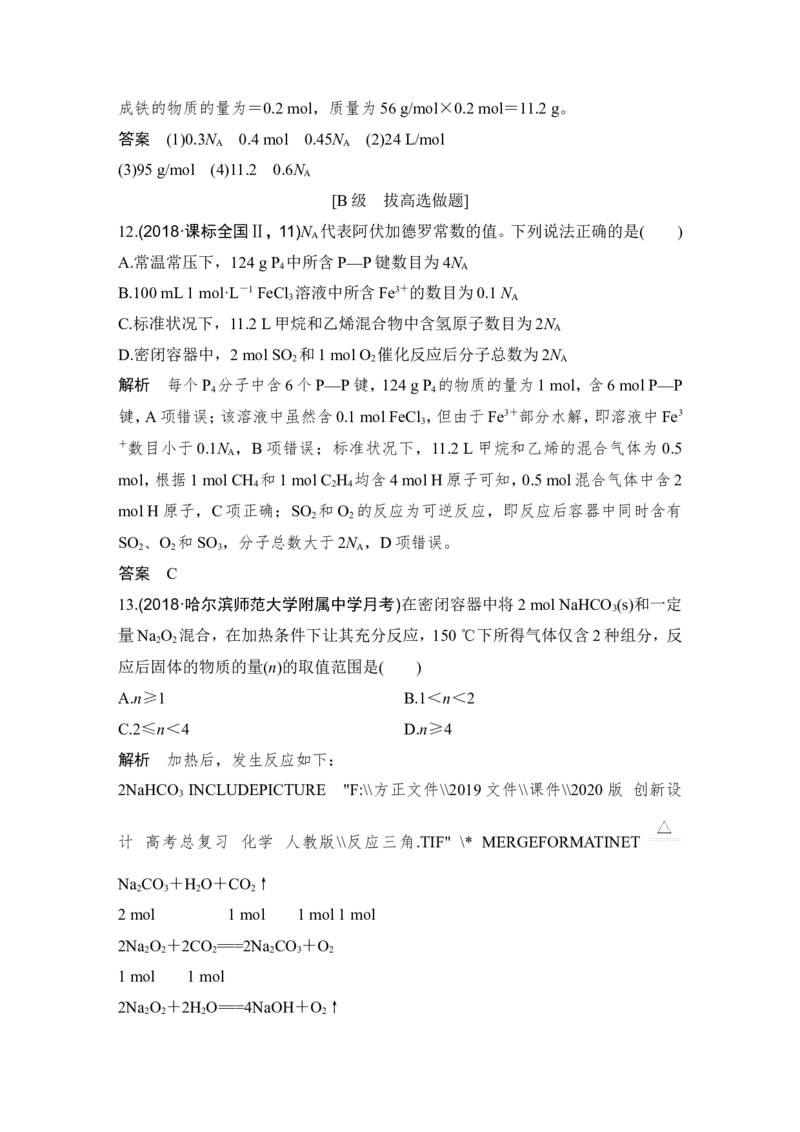文档内容
INCLUDEPICTURE "F:\\方正文件\\2019 文
件\\课件\\2020 版 创新设计 高考总复习
化 学 人 教 版 \\ 第 一 章 .tif" \*
MERGEFORMATINET
第1讲 物质的量 气体摩尔体积
【2020·备考】
最新考纲:1.了解物质的量(n)及其单位摩尔(mol)、摩尔质量(M)、气体摩尔体积
(V )、阿伏加德罗常数(N )的含义。2.能根据微粒(原子、分子、离子等)物质的量、数
m A
目、气体体积(标准状况下)之间的相互关系进行有关计算。
核心素养:1.宏观辨识与微观探析:认识物质的量是联系宏观物质和微观粒子的重
要工具,能从宏观和微观相结合的视角分析与解决实际问题。2.证据推理与模型认
知:在有关物质的量计算过程中,通过分析、推理等方法认识计算的方法,建立阿
伏加德罗常数、气体摩尔体积等题目解答的模型。考点一 物质的量 摩尔质量
(频数:★☆☆ 难度:★☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 物
质的量、摩尔质量属于识记性的基础知识,在高考中很少单独命题,常以某个题支
形式呈现在选择题中或结合阿伏加德罗常数、化学方程式进行与物质的量有关的
计算。复习时我们要在做好概念辨析的基础上,加强以物质的量为中心的计算能
力的强化训练。
1.物质的量、摩尔、阿伏加德罗常数
(1)基本概念间的关系
(2)物质的量的表示方法
例如:0.2 mol H ,3 mol H O等。
2 2
(3)物质的量与微粒个数、阿伏加德罗常数之间的关系
n=。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.物质的量作为研究微观粒子与宏观物质的桥梁,其单位摩尔后面应为确切的微
粒名称;如1 mol氢(不确切)和1 mol大米(宏观物质)皆为错误说法。
2.6.02×1023是个纯数值没有任何物理意义,它与阿伏加德罗常数(N )的关系应理
A
解为:6.02×1023是阿伏加德罗常数(N )的数值的近似值。
A
2.摩尔质量
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
涉及摩尔质量的辨析或判断的问题经常在单位上设错考查,摩尔质量、相对分子
质量、1 mol物质的质量在数值上是相同的,但含义不同,三者的单位不同。摩尔质
量的单位是g·mol-1,相对原子(分子)质量的单位是1,1 mol物质的质量单位是g。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)1 mol H O中含有2 mol氢和1 mol氧(×)
2
(2)0.012 kg 12C中含有约6.02×1023 个碳原子(√)
(3)NaOH的摩尔质量为40 g(×)
(4)1 mol OH-的质量为17 g·mol-1(×)
(5)2 mol H O的摩尔质量是1 mol H O的摩尔质量的2倍(×)
2 2
(6)1 mol H PO 与1 mol H SO 的质量相同,溶于水后电离出的阴离子数目也相同
3 4 2 4
(×)
2.(教材改编题)[RJ必修1·P 改编]在0.5 mol Na SO 中含有离子和氧原子的物质
17 2 4
的量分别是( )
A.1.5 mol 0.5 mol B.1.5 mol 2 molC.0.5 mol 4 mol D.1 mol 2 mol
答案 B
3.(拓展应用题)有一瓶氯化钠试剂的标签如图所示,仔细观察该标签,然后回答下
列问题:
(1)该瓶未开封的试剂中含氯化钠的物质的量为________。
(2)从上述试剂瓶中取出0.5 g样品配成溶液,溶液中Na+与Cl-总数为________。
解析 (1)≈8.21 mol。
(2)×2×6.02×1023mol-1≈9.88×1021。
答案 (1)8.21 mol (2)9.88×1021(或 0.016N ) INCLUDEPICTURE "F:\\方正文
A
件\\2019文件\\课件\\2020版 创新设计 高考总复习 化学 人教版\\题组诊断.tif"
\* MERGEFORMATINET
[A组 基础知识巩固]
1.据央视新闻报道,在政府工作报告中指出,建设一批光网城市,推进5万个行政
村通光纤,让更多城乡居民享受数字化生活。光缆的主要成分为SiO 。下列叙述正
2
确的是( )
A.SiO 的摩尔质量为60
2
B.标准状况下,15 g SiO 的体积为5.6 L
2
C.SiO 中Si与O的质量比为7∶8
2
D.相同质量的SiO 和CO 中含有的氧原子数相同
2 2
解析 摩尔质量的单位为g·mol-1,A项错误。标准状况下,SiO 为固体,B项错误。
2SiO 中Si与O的质量比为28∶32=7∶8,C项正确。SiO 和CO 的摩尔质量不同,
2 2 2
D项错误。
答案 C
2.(原创题)中国地质调查局宣称,我国将加速布局,推进“可燃冰”产业化进程。
“可燃冰”是由水和甲烷在一定条件下形成的类冰结晶化合物。
(1)1 mol甲烷中含有________个CH 分子,含有________个氢原子。
4
(2)甲烷的摩尔质量是________,32 g甲烷和________g水所含氢原子数相同。
(3)0.3 mol CH 分子中所含质子数与________个H O分子中所含质子数相等。1.5 g
4 2
CH中的电子数为________。
(4)已知:1.6 g“可燃冰”( CH ·xH O)的物质的量与6.02×1021个水分子的物质的
4 2
量 相 等 , 则 该 “ 可 燃 冰 ” 的 摩 尔 质 量 为 ________________ , x 值 为
________________。
答案 (1)N (或6.02×1023) 4N (或2.408×1024)
A A
(2)16 g·mol-1 72
(3)0.3N (或1.806×1023) 0.8N
A A
(4)160 g·mol-1 8
【练后反思】
1.掌握好一种计算方法:摩尔质量的计算
2.利用好一个转换“纽带”[B组 考试能力过关]
3.(2018·课标全国Ⅰ,10)N 是阿伏加德罗常数的值。下列说法正确的是( )
A
A.16.25 g FeCl 水解形成的Fe(OH) 胶体粒子数为0.1N
3 3 A
B.22.4 L(标准状况)氩气含有的质子数为18N
A
C.92.0 g甘油(丙三醇)中含有羟基数为1.0N
A
D.1.0 mol CH 与Cl 在光照下反应生成的CH Cl分子数为1.0N
4 2 3 A
解析 16.25 g FeCl 的物质的量n(FeCl )=0.1 mol,如果氯化铁完全水解,则生成
3 3
0.1 mol Fe(OH) ,而氢氧化铁胶体粒子由许多氢氧化铁聚集而成,故氢氧化铁胶体
3
粒子数远小于0.1N ,A项错误;氩气是单原子分子,1 mol Ar含18 mol质子,B项
A
正确;甘油(丙三醇)的分子式为C H O ,相对分子质量为92,1 mol(92.0 g)甘油含3
3 8 3
mol羟基,C项错误;甲烷与氯气在光照下反应会生成四种有机产物,即1.0 mol甲
烷反应后生成的CH Cl、CH Cl 、CHCl 、CCl 共为1 mol,D项错误。
3 2 2 3 4
答案 B
4.(2017·上海卷)下列叙述正确的是( )
A.1 mol O 的质量是32 g/mol
2
B.OH-的摩尔质量是17 g
C.1 mol H O的质量是18 g/mol
2
D.CO 的摩尔质量是44 g/mol
2
解析 质量的单位是g,A、C错误;摩尔质量的单位是g/mol,B错误,D正确。
答案 D
5.(2016·海南卷)利用太阳能分解水制氢气,若光解0.02 mol水,下列说法正确的
是( )
A.可生成H 的质量为0.02 g
2
B.可生成氢原子的个数为2.408×1023个
C.可生成H 的体积为0.224 L(标准状况)
2
D.生成H 的量理论上等于0.04 mol Na与水反应产生H 的量
2 2
解析 根据方程式2H O===2H ↑+O ↑知,光解0.02 mol H O,可产生0.02 mol
2 2 2 2
H 和0.01 mol O 。A项,可生成H 的质量为0.04 g,错误;B项,可生成氢原子的个
2 2 2数为2.408×1022个,错误;C项,可生成标准状况下H 的体积为0.448 L,错误;D
2
项,0.04 mol Na与水反应产生0.02 mol H ,正确。
2
答案 D
6.(2015·全国卷Ⅰ)乌洛托品在合成、医药、染料等工业中有广泛用途,其结构简式
如图所示。将甲醛水溶液与氨水混合蒸发可制得乌洛托品。若原料完全反应生成
乌洛托品,则甲醛与氨的物质的量之比应为( )
A.1∶1 B.2∶3
C.3∶2 D.2∶1
解析 根据乌洛托品的结构简式可知分子式为C H N ,碳原子来自HCHO,氮原
6 12 4
子来自NH ,发生的反应为6HCHO+4NH ―→C H N +6H O,根据原子守恒,则
3 3 6 12 4 2
甲醛与氨的物质的量之比为3∶2。
答案 C
考点二 气体摩尔体积 阿伏加德罗定律
(频数:★★★ 难度:★★☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 气
体摩尔体积和阿伏加德罗定律在高考中常结合阿伏加德罗常数进行考查,考题一
般有意设置一些易错易混的“陷阱”,如常见的误认为气体的非气体物质(HF、SO
3
等),考生一不留神便会成为命题设计者的“猎物”。复习时一定要抓住气体摩尔体
积的使用范围和阿伏加德罗定律的内涵及拓展重点落实。
1.影响物质体积的因素2.气体摩尔体积
3.阿伏加德罗定律
(2)适用范围:单一气体或相互不反应的混合气体。
(3)推论(可通过pV=nRT及n=、ρ=导出)
结论
公式 语言叙述
同温、同压下,气体的体积与其物质的量
T、p相同 =
成正比
同温、同压下,气体的密度与其摩尔质量
T、p相同 =
(或相对分子质量)成正比
温度、体积相同的气体,其压强与其物质
T、V相同 =
的量成正比
备注 n为物质的量,M为摩尔质量,V为气体体积,ρ为密度,p为压强
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
1.阿伏加德罗定律所叙述的“任何气体”,既包括单一气体,也包括互不反应的混合气体。
2.阿伏加德罗定律及其推论没有必要死记硬背,可由理想气体状态方程pV=nRT
进行推导。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)在标准状况下,1 mol O 与1 mol SO 的体积相同。(×)
2 3
(2)在标准状况下,1 mol气体的体积约是22.4 L,在非标准状况下,1 mol气体的体
积则一定不是22.4 L。(×)
(3)同温同压下,等体积的两种单质气体一定具有相同的原子数。(×)
(4)标准状况下,氢气的气体摩尔体积为22.4 L。(×)
(5)同温同体积条件下,等质量的SO 和O 对应的压强之比为1∶2。(√)
2 2
2.(教材改编题)[RJ必修1·P 4改编]下列各组物质中,所含电子数相同的是( )
20
A.0.5 mol 37Cl 和16 g O
2 2
B.5.6 L N (标准状况)和11 g CO
2 2
C.20 g D O和10 g H
2 2
D.224 mL D 和0.1 mol N
2 2
答案 C
3.(思维探究题)由阿伏加德罗常数(N )和一个水分子的质量(m )、一个水分子的体
A 水
积(V )不能确定的物理量是________。
水
①1摩尔水的质量 ②1摩尔水蒸气的质量 ③1摩尔水蒸气的体积
答案 ③
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.标准状况下,5.6 L O 中含有N个氧原子,则阿伏加德罗常数的值为( )
2
A.4N B.
C.2N D.解析 根据题意知,=,故N =2N mol-1,C项正确。
A
答案 C
2.(2019·广西模考)同温同压下,甲容器中充满35Cl ,乙容器中充满37Cl ,下列叙述
2 2
不正确的是( )
A.若两种气体体积相等,则甲、乙两容器中气体密度之比为35∶37
B.若两种气体体积相等,则甲、乙两容器中气体分子数之比为35∶37
C.若两种气体质量相等,则甲、乙两容器中气体所含质子数之比为37∶35
D.若两种气体体积相等,则甲、乙两容器中气体所含中子数之比为9∶10
解析 同温同压下,若两种气体体积相等,则两种气体物质的量相等(气体分子数
也相等),两种气体质量之比为35∶37,而ρ=,m=Mn,故甲、乙两容器中气体密
度之比为35∶37,甲、乙两容器中气体所含中子数之比为(35-17)∶(37-17)=
9∶10,A、D项正确,B项错误;同温同压下,若两种气体质量相等,则甲、乙两容
器中气体物质的量之比为∶=37∶35,故甲、乙两容器中气体所含质子数之比为
37∶35,C项正确。
答案 B
3.(1)2 mol O 和3 mol O 的质量之比为________,分子数之比为________;同温同
3 2
压下的密度之比为________,含氧原子数之比为________,体积之比为________。
(2)在标准状况下,由CO和CO 组成的混合气体6.72 L,质量为12 g。此混合物中
2
CO和CO 分子数目之比是________,混合气体的平均摩尔质量是________,对氢
2
气的相对密度是________。
(3)气体化合物A的化学式可表示为O F ,已知同温同压下10 mL A受热分解生成
x y
15 mL O 和 10 mL F , 则 A 的 化 学 式 为 ________ , 推 断 的 依 据 是
2 2
_____________________________________________________________________。
(4)在标准状况下,15.6 g Na O 投入足量水中,可产生O 的体积为________。
2 2 2
答案 (1)1∶1 2∶3 3∶2 1∶1 2∶3
(2)1∶3 40 g·mol-1 20
(3)O F 阿伏加德罗定律和质量守恒定律
3 2
(4)2.24 L
4.(2018·陕西省西安中学第一次摸底考试)设N 为阿伏加德罗常数的值,下列说法
A
正确的是( )A.标准状况下,2.24 L乙醇中碳氢键的数目为0.5N
A
B.1 L 0.1 mol·L-1硫酸钠溶液中含有的氧原子数为0.4N
A
C.0.1 mol KI与0.1 mol FeCl 在溶液中反应转移的电子数为0.2N
3 A
D.0.1 mol乙烯和乙醇的混合物完全燃烧所消耗的氧分子数为0.3N
A
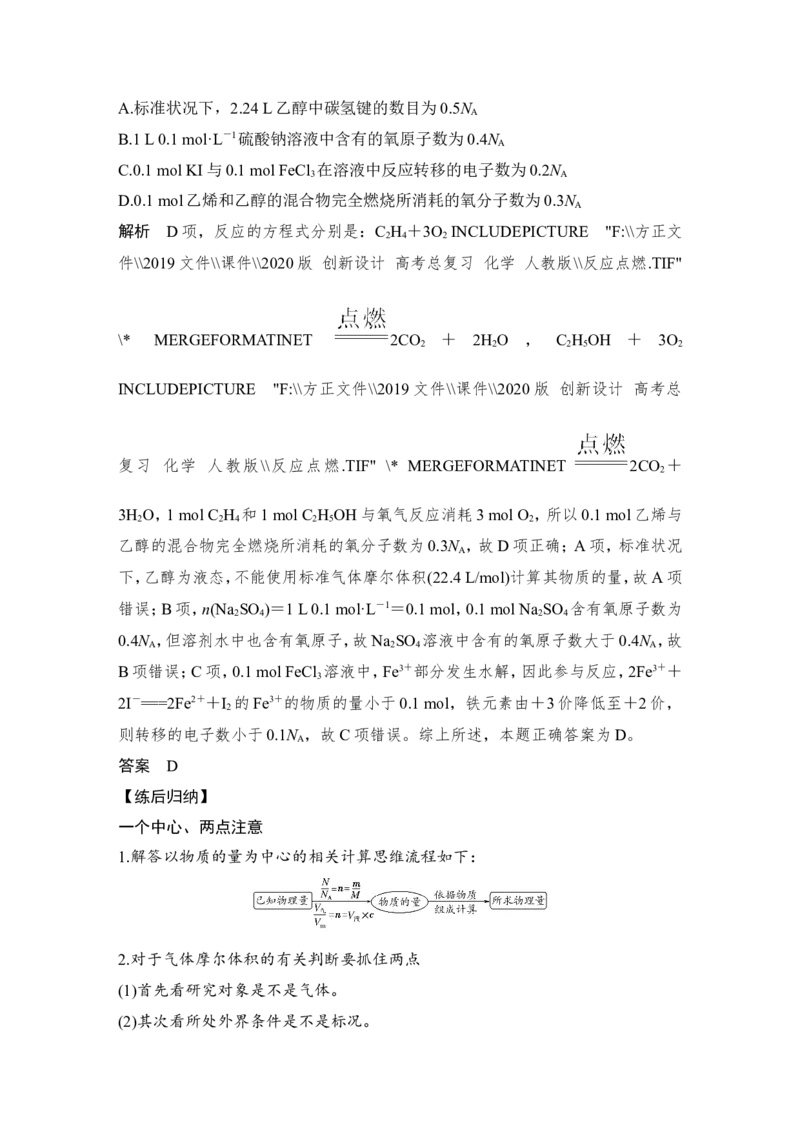
解析 D项,反应的方程式分别是:C H +3O INCLUDEPICTURE "F:\\方正文
2 4 2
件\\2019文件\\课件\\2020版 创新设计 高考总复习 化学 人教版\\反应点燃.TIF"
\* MERGEFORMATINET 2CO + 2H O , C H OH + 3O
2 2 2 5 2
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\反应点燃.TIF" \* MERGEFORMATINET 2CO +
2
3H O,1 mol C H 和1 mol C H OH与氧气反应消耗3 mol O ,所以0.1 mol乙烯与
2 2 4 2 5 2
乙醇的混合物完全燃烧所消耗的氧分子数为0.3N ,故D项正确;A项,标准状况
A
下,乙醇为液态,不能使用标准气体摩尔体积(22.4 L/mol)计算其物质的量,故A项
错误;B项,n(Na SO )=1 L 0.1 mol·L-1=0.1 mol,0.1 mol Na SO 含有氧原子数为
2 4 2 4
0.4N ,但溶剂水中也含有氧原子,故Na SO 溶液中含有的氧原子数大于0.4N ,故
A 2 4 A
B项错误;C项,0.1 mol FeCl 溶液中,Fe3+部分发生水解,因此参与反应,2Fe3++
3
2I-===2Fe2++I 的Fe3+的物质的量小于0.1 mol,铁元素由+3价降低至+2价,
2
则转移的电子数小于0.1N ,故C项错误。综上所述,本题正确答案为D。
A
答案 D
【练后归纳】
一个中心、两点注意
1.解答以物质的量为中心的相关计算思维流程如下:
2.对于气体摩尔体积的有关判断要抓住两点
(1)首先看研究对象是不是气体。
(2)其次看所处外界条件是不是标况。[B组 考试能力过关]
5.判断下列说法是否正确
(1)标准状况下,2.24 L N 和O 的混合气体中分子数为0.2N (×)
2 2 A
(2017·课标全国Ⅱ,8C)
(2)标准状况下,5.6 L CO 与足量Na O 反应转移的电子数为0.5N (×)
2 2 2 A
(2015·四川理综,5C)
(3)标准状况下,22.4 L氨水含有N 个NH 分子(×)
A 3
(2014·广东理综,10C)
6.(全国卷)下列关于同温同压下的两种气体12C18O和14N 的判断正确的是( )
2
A.体积相等时密度相等
B.原子数相等时具有的中子数相等
C.体积相等时具有的电子数相等
D.质量相等时具有的质子数相等
解析 依据阿伏加德罗定律可知在同温同压下的两种气体体积相同,分子数相同,
而每个CO和N 分子所含电子数相同,C项正确;同温同压同体积条件下密度之
2
比等于摩尔质量之比,12C18O 的摩尔质量为 30 g·mol-1,14N 的摩尔质量为 28
2
g·mol-1,A项错误;1个12C18O分子中所含中子数为16,1个14N 分子中所含中子
2
数为14,B项错误;n=,m相同、M不同,n不同,D项错误。
答案 C
7.(2017·课标全国Ⅲ,10)N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.0.1 mol的11B中,含有0.6N 个中子
A
B.pH=1的H PO 溶液中,含有0.1N 个H+
3 4 A
C.2.24 L(标准状况)苯在O 中完全燃烧,得到0.6N 个CO 分子
2 A 2
D.密闭容器中1 mol PCl 与1 mol Cl 反应制备PCl (g),增加2N 个P—Cl键
3 2 5 A
解析 硼原子的质子数为5,11B的中子数为6,故0.1 mol的11B中含有中子数为
0.6N ;未指明溶液体积,无法计算H+ 的个数;标准状况下苯为液体,故2.24 L(标
A
准状况)苯的物质的量不为 0.1 mol,生成的 CO 分子也不是 0.6N ;PCl +
2 A 3
Cl PCl ,这是一个可逆反应,1mol PCl 与1mol Cl 不可能完全反应生成1 mol
2 5 3 2
PCl ,故增加的P-Cl键数目小于2N ,错误。
5 A
答案 AINCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\分层课时作业.TIF" \* MERGEFORMATINET
[A级 全员必做题]
1.(2018·山东烟台模拟)下列叙述正确的是( )
A.NaCl的摩尔质量是58.5 g
B.64 g氧气中含有2 mol氧
C.4 g氦气中含有2 mol氦原子
D.0.1 mol CO 中含有6.02×1022个CO 分子
2 2
解析 NaCl的摩尔质量是58.5 g·mol-1;B项未指明微粒的名称;4 g氦气中应含
有 1 mol 氦原子;0.1 mol CO 中所含 N(CO )=6.02×1023mol-1×0.1 mol=
2 2
6.02×1022。
答案 D
2.空气中的自由电子附着在分子或原子上形成空气负离子,被称为“空气维生素”
O就是一种空气负离子,其摩尔质量为( )
A.33 g B.32 g
C.33 g·mol-1 D.32 g·mol-1
解析 O相对分子质量为32,故摩尔质量为32 g·mol-1。
答案 D
3.某气体的摩尔质量为M g·mol-1,N 表示阿伏加德罗常数,在一定的温度和压强
A
下,体积为V L的该气体所含有的分子数为x。则表示的是( )
A.V L该气体的质量(以g为单位)
B.1 L该气体的质量(以g为单位)
C.1 mol该气体的体积(以L为单位)
D.1 L该气体中所含的分子数
解析 x除以N 为该气体的物质的量,然后乘以M表示其质量,再除以V表示1
A
L该气体的质量。
答案 B
4.一定温度和压强下,30 L某种气态纯净物中含有6.02×1023个分子,这些分子由1.204×1024个原子组成,下列有关说法中不正确的是( )
A.该温度和压强可能是标准状况
B.标准状况下该纯净物若为气态,其体积约是22.4 L
C.该气体中每个分子含有2个原子
D.若O 在该条件下为气态,则1 mol O 在该条件下的体积也为 30 L
2 2
解析 由分子数和原子数的关系可知该分子为双原子分子,且其物质的量为 1
mol,若该物质为气态,则其在标准状况下的体积为22.4 L,故该温度和压强不可
能是标准状况下,在此状况下,V =30 L·mol-1。
m
答案 A
5.人造空气(氧气与氦气的混合气)可用于减轻某些病痛或供深水潜水员使用。标准
状况下,5.6 L“人造空气”的质量是2.4 g,其中氧气与氦气的质量比是( )
A.1∶1 B.1∶4
C.2∶1 D.2∶3
解析 设O 和He的质量分别为x g和y g,则解得x=1.6 g,y=0.8 g,x∶y=1.6
2
g∶0.8 g=2∶1。
答案 C
6.下列有关C H 和C H 的叙述错误的是( )
2 2 6 6
A.二者碳元素的质量分数相同
B.在标准状况下,等体积的两种物质含有的分子数相等
C.等物质的量时,二者质量之比为=
D.等质量时,二者完全燃烧消耗相同状况下的氧气体积相等
解析 C H 与C H 的最简式均为CH,故二者碳元素的质量分数相同,A项正确;
2 2 6 6
标准状况下,C H 为非气体,等体积的两种物质的物质的量不相等,所以含有的分
6 6
子数也不相等,B项错误;等物质的量时,二者质量之比为=,故C不合题意;二者
的最简式相同,则等质量的两种物质完全燃烧消耗相同状况下的氧气体积相等,
故D不合题意。
答案 B
7.(2019·湖南省浏阳市第二、五、六中学三校期中联考)下列示意图中,白球代表氢
原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其
质量忽略不记)。其中能表示等质量的氢气与氦气的是( )解析 设氢气与氦气都为m g,则二者的物质的量之比为∶=2∶1,则体积之比为
2∶1; A、白球代表氢原子,黑球代表氦原子,符合物质的量之比为2∶1,体积之比
为2∶1,故A正确; B、白球代表氢原子,黑球代表氦原子,物质的量之比为
2∶1,体积之比为2∶1,但氦气是单原子构成的分子,故B错误; C、白球代表氢
原子,黑球代表氦原子,物质的量之比为2∶1,但体积之比为1∶2,故C错误;
D、白球代表氢原子,黑球代表氦原子,物质的量之比为1∶1,体积之比为2∶1,
故D错误。
答案 A
8.等温等压下,有质子数相等的CO、N 、C H 三种气体,下列叙述中正确的是(
2 2 2
)
A.体积之比为13∶13∶14 B.密度之比为14∶14∶13
C.质量之比为1∶1∶1 D.原子数之比为1∶1∶1
解析 A项,三种气体分子的质子数均为14,质子数相等的CO、N 、C H 三种气
2 2 2
体,物质的量相等,等温等压下,气体的体积与其物质的量成正比,所以三者体积
之比为1∶1∶1,错误;B项,CO、N 、C H 摩尔质量分别为28 g·mol-1、28 g·mol-
2 2 2
1、26 g·mol-1,等温等压下,气体摩尔体积相同,根据ρ==知,密度与摩尔质量成
正比,则密度之比为28∶28∶26=14∶14∶13,正确;C项,三种气体分子的物质
的量相等,CO、N 、C H 摩尔质量分别为28 g·mol-1、28 g·mol-1、26 g·mol-1,根据
2 2 2
m=nM知:质量之比与摩尔质量成正比为28∶28∶26=14∶14∶13,错误;D项,
1 分子 CO、N 、C H 分别含原子数为 2、2、4,所以三种气体原子数之比为
2 2 2
1∶1∶2,错误。
答案 B
9.(2019·湖南省郴州市高三一检,4)设N 表示阿伏加德罗常数的值,下列说法正
A
确的是( )
A.80 ℃时,1 L pH=1的硫酸溶液中,含有的OH-数目为10-13N
AB.向含有FeI 的溶液中通入适量氯气,当有1 mol Fe2+被氧化时,该反应转移电子
2
数目为3N
A
C.100 g质量分数为46%的乙醇水溶液中氧原子数为4N
A
D.以Mg、Al为电极,NaOH溶液为电解质溶液的原电池中,导线上流过N 个电子
A
解析 A.80 ℃时,K >1×10-14,1 LpH=1的硫酸溶液中,c(OH-)=>mol/L=
w
1×10-13mol/L,含有的OH-数目大于10-13N ,故A错误;B.还原性:I->Fe2+,向
A
含有FeI 的溶液中通入适量氯气,当有1 mol Fe2+被氧化时,I-已经完全被氧化,
2
该反应转移电子数目不能确定,故B错误;C.100 g质量分数为46%的乙醇水溶液
中含有46 g即1 mol乙醇和54 g即3 mol水,氧原子数为4N ,故C正确;D. 以
A
Mg、Al为电极,NaOH溶液为电解质溶液的原电池中,导线上流过的电子数无法
确定,故D错误。故选C。
答案 C
10.标准状况下15 g CO与CO 的混合气体,体积为11.2 L。则:
2
(1)混合气体的密度是________。
(2)混合气体的平均摩尔质量是________。
(3)CO 和CO的体积之比是________。
2
(4)CO的体积分数是________。
(5)CO 和CO的质量之比是________。
2
(6)CO的质量分数是________。
(7)混合气体中所含氧原子的物质的量是________。
(8)混合气体中所含碳原子的物质的量是________。
解析 (1)ρ==≈1.339 g·L-1。
(2)解法一:n==0.5 mol,M===30 g·mol-1。
解法二:M=ρ·V =1.339 g·L-1×22.4 L·mol-1≈30 g·mol-1。
m
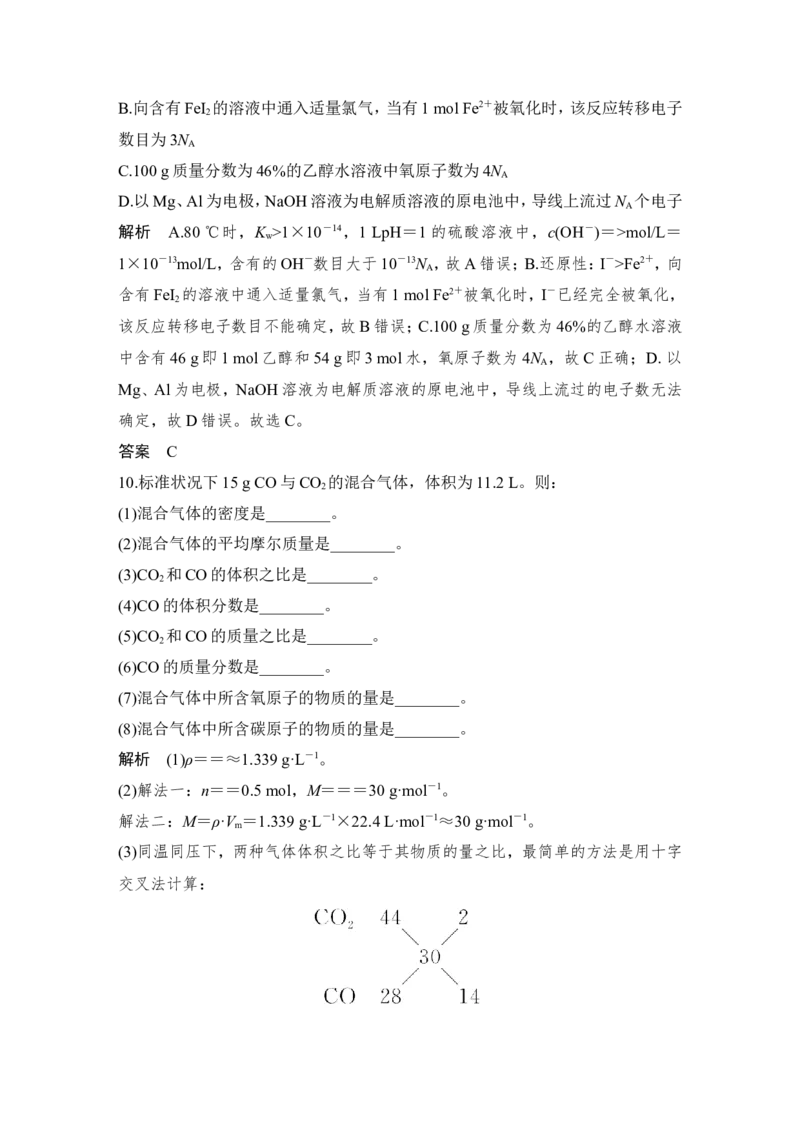
(3)同温同压下,两种气体体积之比等于其物质的量之比,最简单的方法是用十字
交叉法计算:=。
(4)CO的体积分数=×100%=87.5%。
(5)===11∶49。
(6)CO的质量分数=×100%≈81.7%。
(7)n(O)=2n(CO )+n(CO)=2×0.5 mol×+0.5 mol×=0.562 5 mol。
2
(8)n(C)=n(CO )+n(CO)=0.5 mol。
2
答案 (1)1.339 g·L-1
(2)30 g·mol-1
(3)1∶7 (4)87.5% (5)11∶49
(6)81.7% (7)0.562 5 mol (8)0.5 mol
11.物质的量是高中化学常用的物理量,请完成以下有关计算(设N 为阿伏加德罗
A
常数的值):
(1)2.3 g乙醇含有________个H原子,所含共价键的物质的量为________,其中官
能团羟基所含的电子数为________。
(2)某条件下,8 g 氧气所占的体积为 6 L,则在该条件下的气体摩尔体积为
________。
(3)9.5 g 某二价金属的氯化物中含有 0.2 mol Cl-,则此氯化物的摩尔质量为
________。
(4)6.72 L CO(标准状况)与一定量的Fe O 恰好完全反应(生成Fe与CO )后,生成
2 3 2
Fe的质量为________g,转移的电子数目为________。
解析 (1)2.3 g乙醇的物质的量为=0.05 mol,0.05 mol乙醇分子中含有H原子的
物质的量为0.05 mol×6=0.3 mol,含有H原子数为0.3N ;乙醇分子共含有8条
A
共价键,则0.05 mol乙醇分子中含共价键的物质的量为 0.05 mol×8=0.4 mol;
0.05 mol 乙醇分子中含 0.05 mol 羟基,0.05 mol 羟基含有电子的物质的量为
9×0.05 mol=0.45 mol,含有电子数为 0.45N ;(2)8 g氧气的物质的量为=0.25
A
mol,0.25 mol氧气在该条件下的体积为6 L,则该条件下的气体摩尔体积为=24
L/mol。(3)9.5 g某二价金属的氯化物中含有0.2 mol Cl-,该氯化物的物质的量为
0.1 mol,则此氯化物的摩尔质量为=95 g/mol;(4)标准状况下6.72 L一氧化碳的物
质的量为=0.3 mol,0.3 mol CO完全反应生成二氧化碳失去的电子的物质的量为
0.3 mol×(4-2)=0.6 mol,转移电子的数目为0.6N ,根据得失电子守恒,反应生
A成铁的物质的量为=0.2 mol,质量为56 g/mol×0.2 mol=11.2 g。
答案 (1)0.3N 0.4 mol 0.45N (2)24 L/mol
A A
(3)95 g/mol (4)11.2 0.6N
A
[B级 拔高选做题]
12.(2018·课标全国Ⅱ,11)N 代表阿伏加德罗常数的值。下列说法正确的是( )
A
A.常温常压下,124 g P 中所含P—P键数目为4N
4 A
B.100 mL 1 mol·L-1 FeCl 溶液中所含Fe3+的数目为0.1 N
3 A
C.标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2N
A
D.密闭容器中,2 mol SO 和1 mol O 催化反应后分子总数为2N
2 2 A
解析 每个P 分子中含6个P—P键,124 g P 的物质的量为1 mol,含6 mol P—P
4 4
键,A项错误;该溶液中虽然含0.1 mol FeCl ,但由于Fe3+部分水解,即溶液中Fe3
3
+数目小于0.1N ,B项错误;标准状况下,11.2 L甲烷和乙烯的混合气体为0.5
A
mol,根据1 mol CH 和1 mol C H 均含4 mol H原子可知,0.5 mol混合气体中含2
4 2 4
mol H原子,C项正确;SO 和O 的反应为可逆反应,即反应后容器中同时含有
2 2
SO 、O 和SO ,分子总数大于2N ,D项错误。
2 2 3 A
答案 C
13.(2018·哈尔滨师范大学附属中学月考)在密闭容器中将2 mol NaHCO (s)和一定
3
量Na O 混合,在加热条件下让其充分反应,150 ℃下所得气体仅含2种组分,反
2 2
应后固体的物质的量(n)的取值范围是( )
A.n≥1 B.1<n<2
C.2≤n<4 D.n≥4
解析 加热后,发生反应如下:
2NaHCO INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设
3
计 高考总复习 化学 人教版\\反应三角.TIF" \* MERGEFORMATINET
Na CO +H O+CO ↑
2 3 2 2
2 mol 1 mol 1 mol 1 mol
2Na O +2CO ===2Na CO +O
2 2 2 2 3 2
1 mol 1 mol
2Na O +2H O===4NaOH+O ↑
2 2 2 21 mol 1 mol 2 mol
由反应方程式可知,150 ℃时所得气体中仅含有两种组分,则气体为氧气和水蒸气,
二氧化碳全部反应,2 mol NaHCO 分解生成1 mol Na CO ;若2 mol NaHCO 分解
3 2 3 3
生成二氧化碳全部被吸收,则1 mol CO 与Na O 反应生成1 mol Na CO ,所以固
2 2 2 2 3
体的物质的量最少为2 mol Na CO ;若2 mol NaHCO 分解生成的H O和CO 被
2 3 3 2 2
足量的Na O 吸收时,还可生成1 mol Na CO 和2 mol NaOH,所以固体最多不超
2 2 2 3
过4 mol,答案选C。
答案 C
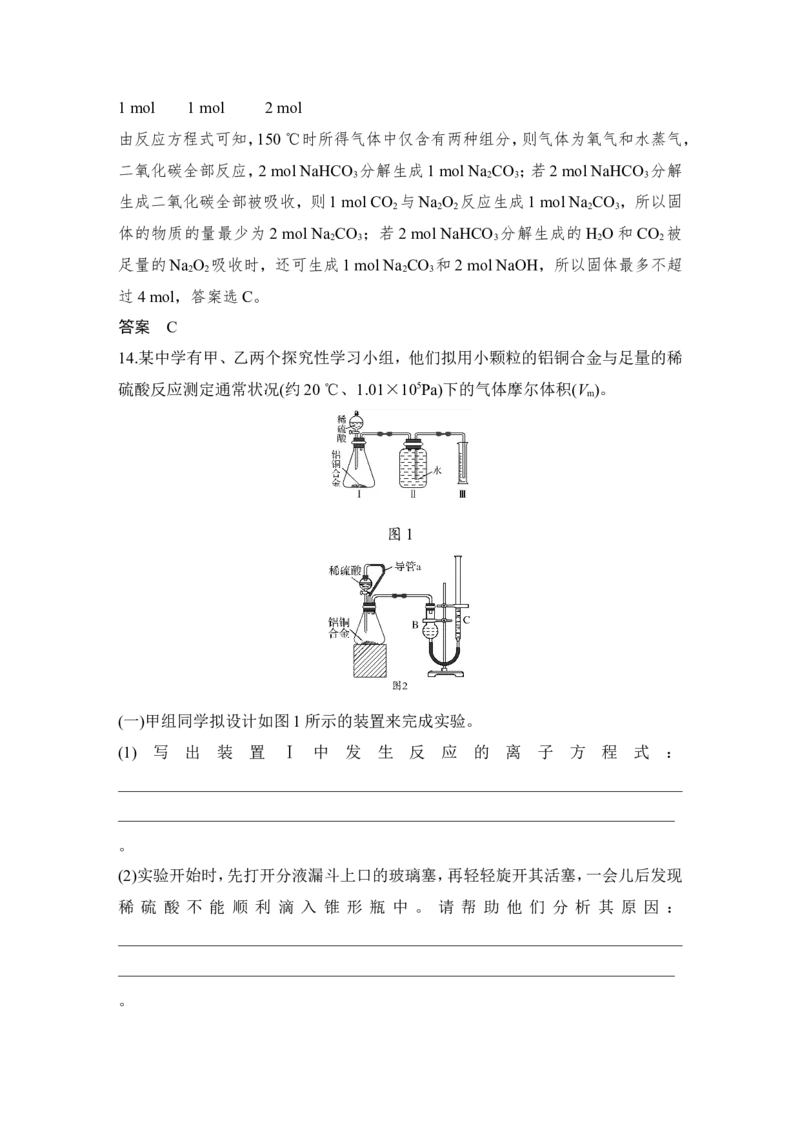
14.某中学有甲、乙两个探究性学习小组,他们拟用小颗粒的铝铜合金与足量的稀
硫酸反应测定通常状况(约20 ℃、1.01×105Pa)下的气体摩尔体积(V )。
m
图1
(一)甲组同学拟设计如图1所示的装置来完成实验。
(1) 写 出 装 置 Ⅰ 中 发 生 反 应 的 离 子 方 程 式 :
______________________________________________________________________
_____________________________________________________________________
。
(2)实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻旋开其活塞,一会儿后发现
稀 硫 酸 不 能 顺 利 滴 入 锥 形 瓶 中 。 请 帮 助 他 们 分 析 其 原 因 :
______________________________________________________________________
_____________________________________________________________________
。(3)实验结束时,生成氢气的体积近似等于________。
(4)锥形瓶中残存的氢气对实验结果是否有影响:________(填“有”“没有”或
“不能判断”),简述理由:_____________________________________________
_____________________________________________________________________
。
(二)乙组同学仔细分析了甲组同学的实验装置后以为,稀硫酸滴入锥形瓶中,即使
不生成氢气,也会将瓶中的空气排出,使所测氢气的体积偏大;实验结束后,连接
广口瓶和量筒的导管中有少量水存在,使所测氢气的体积偏小,于是他们设计了
如图2所示的实验装置。
实验中准确测定出4个数据,如下表:
实验前 实验后
铝铜合金质量(g) m m
1 2
量液管(C)体积(mL) V V
1 2
利用上述数据计算通常状况下的气体摩尔体积:V =________。
m
解析 (一)(1)铝和稀硫酸反应生成硫酸铝和氢气,其离子方程式为 2Al+6H+
===2Al3++3H ↑。
2
(2)铝与稀硫酸反应产生的氢气使锥形瓶内气压增大,锥形瓶内的压强大于大气压
所以稀硫酸不能顺利滴入锥形瓶中。
(3)气体产生的压强导致水从集气瓶中排出,且氢气不易溶于水,所以收集到的水
的体积近似等于氢气的体积。
(4)装置中有空气存在,生成的氢气不溶于水,在相同温度和压强下,生成的氢气的
体积与排出空气的体积相等,所以没有影响。
(二)2Al+6H+===2Al3++3H ↑
2
2 mol 3 mol
mol
V =L/mol。
m
答案 (一)(1)2Al+6H+===2Al3++3H ↑
2
(2)铝与稀硫酸反应产生的氢气使锥形瓶内气压增大
(3)收集到水的体积
(4)没有 相同温度和压强下,生成氢气的体积与排出空气的体积相等(二)L/mol