文档内容
1.下列叙述或操作正确的是( )
A.浓硫酸具有强氧化性,稀硫酸无氧化性
B.浓硫酸不慎沾到皮肤上,立即用NaOH溶液冲洗
C.稀释浓硫酸时应将水沿着烧杯壁慢慢地注入盛有浓硫酸的烧杯中,并不断搅拌
D.浓硫酸与铜的反应中,浓硫酸不仅表现强氧化性,还表现酸性
2.(2024·武汉高三模拟)硫酸钙用途广泛,下列说法不正确的是( )
A.CaSO·2H O俗名:熟石膏
4 2
B.CaSO 属于强电解质
4
C.CaSO 中既含离子键又含共价键
4
D.石膏可用来调节水泥硬化速度
3.下列关于鉴别1 mol·L-1稀硫酸和98%的浓硫酸的叙述正确的是( )
A.常温下测定两溶液的导电能力,导电能力强的是浓硫酸
B.常温下可以用铜片鉴别两种溶液
C.常温下不能用铝片鉴别两种溶液
D.两溶液敞口在空气中放置一段时间后质量明显增大的是浓硫酸
4.实验室用如图装置制备HCl气体。推压注射器活塞将浓盐酸慢慢注入浓硫酸中,可制备少
量干燥HCl气体,其原理分析不正确的是( )
A.混合时放热使HCl溶解度减小
B.浓硫酸具有吸水性,吸收了盐酸中水分
C.浓盐酸具有挥发性,利于HCl气体逸出
D.浓盐酸中HCl以分子形式存在,利于HCl气体逸出
5.(2023·北京,7)蔗糖与浓硫酸发生作用的过程如图所示。下列关于该过程的分析不正确的是( )
A.过程①白色固体变黑,主要体现了浓硫酸的脱水性
B.过程②固体体积膨胀,与产生的大量气体有关
C.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
D.过程中蔗糖分子发生了化学键的断裂
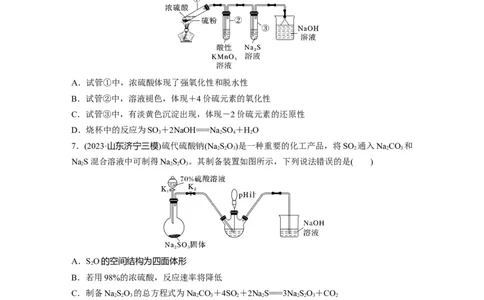
6.(2023·广州高三统考)我国科学家被遴选为“全球青年化学家元素周期表硫元素代言人”。
某小组同学利用反应S+2HSO (浓)=====3SO ↑+2HO进行如图所示的含硫物质的转化实
2 4 2 2
验(夹持装置略)。下列说法正确的是( )
A.试管①中,浓硫酸体现了强氧化性和脱水性
B.试管②中,溶液褪色,体现+4价硫元素的氧化性
C.试管③中,有淡黄色沉淀出现,体现-2价硫元素的还原性
D.烧杯中的反应为SO +2NaOH===NaSO +HO
3 2 4 2
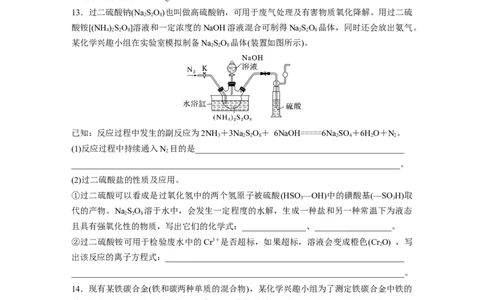
7.(2023·山东济宁三模)硫代硫酸钠(Na SO)是一种重要的化工产品,将SO 通入NaCO 和
2 2 3 2 2 3
NaS混合溶液中可制得NaSO。其制备装置如图所示,下列说法错误的是( )
2 2 2 3
A.SO的空间结构为四面体形
2
B.若用98%的浓硫酸,反应速率将降低
C.制备NaSO 的总方程式为NaCO+4SO +2NaS===3NaSO+CO
2 2 3 2 3 2 2 2 2 3 2
D.为增大三颈烧瓶中加入原料的利用率,可通入过量SO
2
8.连二亚硫酸钠(Na SO)俗称保险粉,工业上可用于纸浆漂白,该物质的还原性比NaSO
2 2 4 2 3
强,其水溶液能被空气中的氧气氧化,在碱性介质中相对稳定。下列说法不正确的是( )
A.连二亚硫酸钠可以用于除去废水中的重铬酸根离子,使Cr O转化为Cr3+
2
B.连二亚硫酸钠溶液敞口放置,可能会发生反应的化学方程式为 2NaSO +O +
2 2 4 2
2HO===4NaHSO
2 3
C.连二亚硫酸钠用于纸浆漂白的原理与ClO 的漂白原理相同
2
D.在包装保存保险粉时加入少量NaCO 固体,可以提高保险粉的稳定性
2 39.下列四支试管中分别盛有固体NaBr、NaCl、NaSO 、Cu,分别向这四支试管中加入适
2 3
量浓硫酸,部分现象如图所示:
下列判断正确的是( )
A.反应①和②的现象说明还原性:Br->Cl-
B.浓硫酸与NaCl不反应,白雾是浓硫酸吸水所致
C.反应③的现象说明氧化性:浓硫酸>Na SO
2 3
D.反应④的现象除产生刺激性气味的气体外,溶液中还析出蓝色晶体
10.NaSO 是常用的防腐剂和漂白剂,通常由NaHSO 过饱和溶液经结晶脱水制得。可利
2 2 5 3
用烟道气中的SO 生产NaSO,其流程如下:
2 2 2 5
下列说法正确的是( )
A.上述制备过程所涉及的物质中只有一种酸性氧化物
B.NaSO 作防腐剂和SO 作漂白剂时,均表现还原性
2 2 5 2
C.上述流程中的NaCO 饱和溶液和NaCO 固体不可互换
2 3 2 3
D.实验室模拟“结晶脱水”时用到的仪器只有蒸发皿、玻璃棒
11.某实验小组同学探究不同金属和浓硫酸的反应,向三等份浓硫酸中分别加入大小相同的
不同金属片,加热,用生成的气体进行下表实验操作并记录实验现象。
实验现象
实验操作
铜 锌 铝
点燃 不燃烧 燃烧 燃烧
通入酸性KMnO 溶液 褪色 褪色 褪色
4
通入CuSO 溶液 无明显变化 无明显变化 出现黑色沉淀
4
通入品红溶液 褪色 褪色 不褪色
已知:HS+CuSO ===CuS↓+HSO (CuS为黑色固体);HS可燃。
2 4 2 4 2
下列说法不正确的是( )
A.加入铜片的实验中,使酸性KMnO 溶液褪色的气体是SO
4 2
B.加入铝片的实验中,燃烧现象能证明生成气体中一定含HS
2C.加入锌片的实验中,生成的气体一定是混合气体
D.金属与浓硫酸反应的还原产物与金属活动性强弱有关
12.将一定量的锌放入200 mL 18.4 mol·L-1浓硫酸中加热,充分反应后锌完全溶解,同时
生成气体X 44.8 L(标准状况)。将反应后的溶液稀释至0.8 L,测得溶液c(H+)=0.2 mol·L-
1,下列判断错误的是( )
A.气体X为SO 和H 的混合物
2 2
B.反应中共转移4 mol电子
C.气体X中SO 与H 的体积比为1∶4
2 2
D.反应中共消耗Zn 130 g
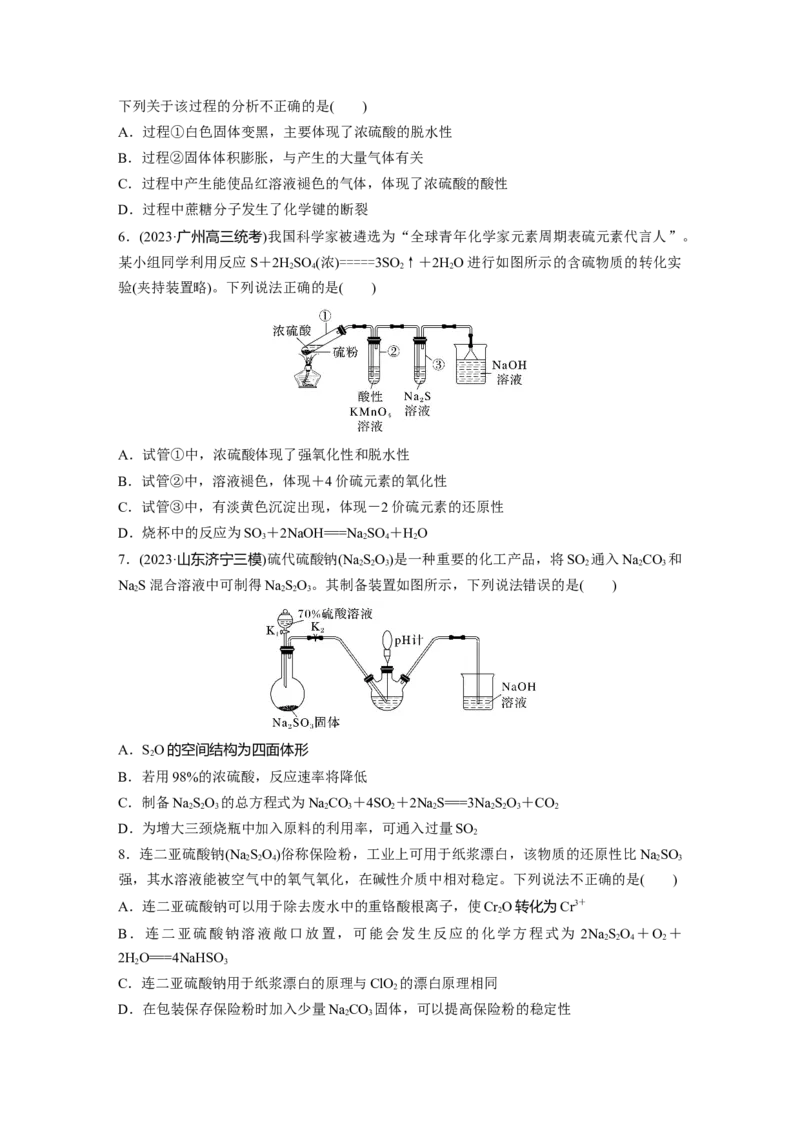
13.过二硫酸钠(Na SO)也叫做高硫酸钠,可用于废气处理及有害物质氧化降解。用过二硫
2 2 8
酸铵[(NH )SO]溶液和一定浓度的NaOH溶液混合可制得NaSO 晶体,同时还会放出氨气。
4 2 2 8 2 2 8
某化学兴趣小组在实验室模拟制备NaSO 晶体(装置如图所示)。
2 2 8
已知:反应过程中发生的副反应为2NH +3NaSO+ 6NaOH=====6NaSO +6HO+N。
3 2 2 8 2 4 2 2
(1)反应过程中持续通入N 目的是_________________________________________________
2
_____________________________________________________________________________。
(2)过二硫酸盐的性质及应用。
①过二硫酸可以看成是过氧化氢中的两个氢原子被硫酸(HSO —OH)中的磺酸基(—SO H)取
3 3
代的产物。NaSO 溶于水中,会发生一定程度的水解,生成一种盐和另一种常温下为液态
2 2 8
且具有强氧化性的物质,写出它们的化学式:_______________、__________________。
②过二硫酸铵可用于检验废水中的Cr3+是否超标,如果超标,溶液会变成橙色(CrO) ,写
2
出该反应的离子方程式:________________________________________________________
______________________________________________________________________________。
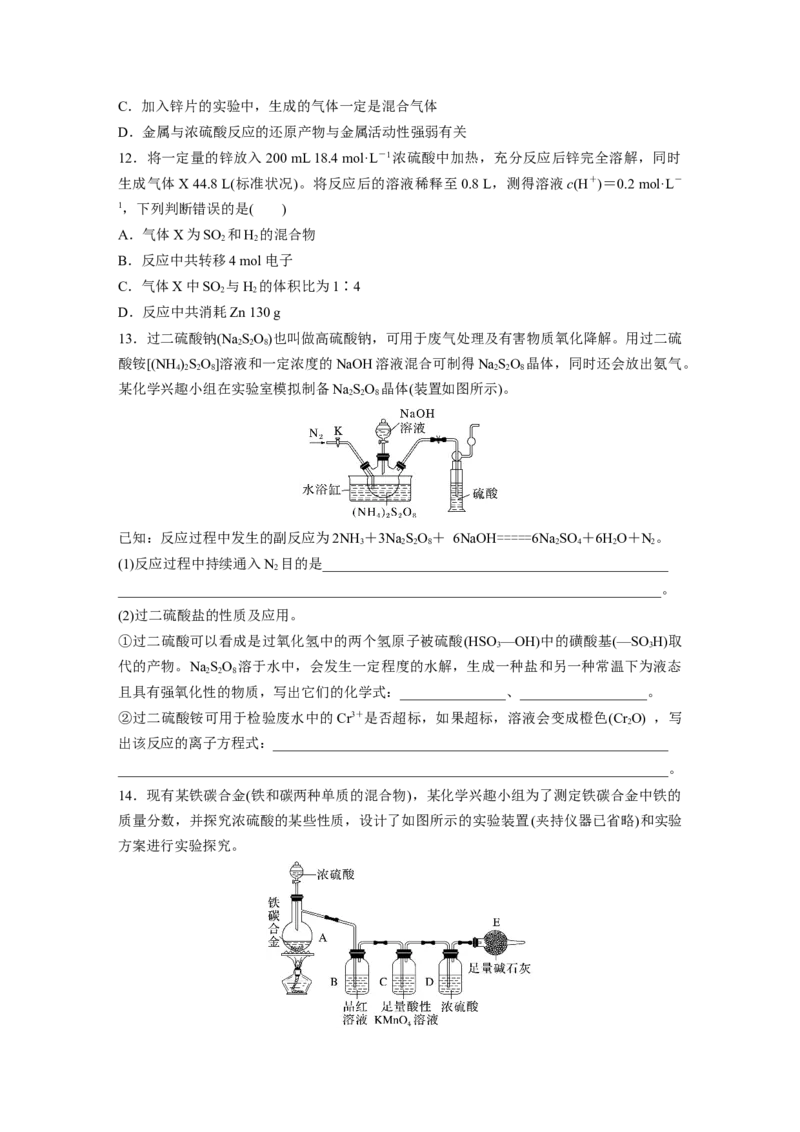
14.现有某铁碳合金(铁和碳两种单质的混合物),某化学兴趣小组为了测定铁碳合金中铁的
质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置(夹持仪器已省略)和实验
方案进行实验探究。Ⅰ.测定铁的质量分数
(1)检查上述装置气密性的一种方法:关闭分液漏斗的活塞,在 E装置后面连上一根导管,
然 后
______________________________________________________________________________
______________________________________________________________________________,
则证明装置的气密性良好。
(2)称量E的质量,并将a g铁碳合金样品放入装置A中,再加入足量的浓硫酸,待A中不
再逸出气体时,停止加热,拆下 E 并称重,E 增重 b g。铁碳合金中铁的质量分数为
____________________________________________________________________(写表达式)。
(3)装置C的作用:_____________________________________________________________
______________________________________________________________________________。
(4)甲同学认为,依据此实验测得的数据计算合金中铁的质量分数可能会偏低,原因是空气
中 CO 、 水 蒸 气 进 入 E 使 b 增 大 。 你 认 为 改 进 的 方 法 是
2
___________________________________。
(5)乙同学认为,即使甲同学认为的偏差得到改进,依据此实验测得合金中铁的质量分数也
可 能 会 偏 高 。 你 认 为 其 中 的 原 因 是
___________________________________________________
______________________________________________________________________________。
Ⅱ.探究浓硫酸的某些性质
(6)往 A 中滴加足量的浓硫酸,未点燃酒精灯前,A、B 均无明显现象,其原因是
______________________________________________________________________________
______________________________________________________________________________。
(7)A中铁与足量浓硫酸发生反应的化学方程式是____________________________________。