文档内容
1.下列关于硫的叙述正确的是( )
A.硫的非金属性较强,在自然界中只以化合态存在
B.可用水溶解过滤分离硝酸钾和硫黄的混合物
C.硫与金属或非金属反应时都作氧化剂
D.硫的氧化性比氯气强
2.下列说法错误的是( )
A.残留在试管内壁上的硫可用热的NaOH溶液除去
B.硫单质与变价金属反应时一般生成低价态的金属硫化物
C.汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理
D.单质硫或含硫物质燃烧时,氧气少量时生成SO ,氧气足量时生成SO
2 3
3.下列有关硫及其化合物的说法或描述正确的是( )
A.硫黄矿制备硫酸经历两步:S―――→SO ――→HSO
3 2 4
B.酸雨与土壤中的金属氧化物反应后,硫元素以单质的形式进入土壤中
C.在燃煤中加入石灰石可减少SO 的排放,发生的反应为2CaCO +2SO +O=====2CO +
2 3 2 2 2
2CaSO
4
D.土壤中的闪锌矿(ZnS)遇到硫酸铜溶液转化为铜蓝(CuS),说明CuS很稳定,不具有还原
性
4.(2023·豫北名校高三调研)正交硫(也称菱形硫、斜方硫)与单斜硫是硫元素的两种常见单质,
均由S 分子(结构如图所示)组成,两者结构中S 分子的排列方式不同,相互之间可以转化:
8 8
单斜硫正交硫。下列有关说法错误的是( )
A.正交硫与单斜硫互为同素异形体
B.S 分子中每个“S”均满足8电子结构
8
C.正交硫转化为单斜硫发生了化学变化
D.正交硫与单斜硫均完全燃烧生成SO 时,单斜硫放出的能量多
2
5.下列关于SO 、SO 的说法正确的是( )
2 3
A.SO 与SO 均为极性分子
2 3
B.SO 能与水形成分子间氢键
3
C.SO 分子中S的杂化方式为sp3
3
D.SO 分子中键角小于SO 分子中的键角
2 3
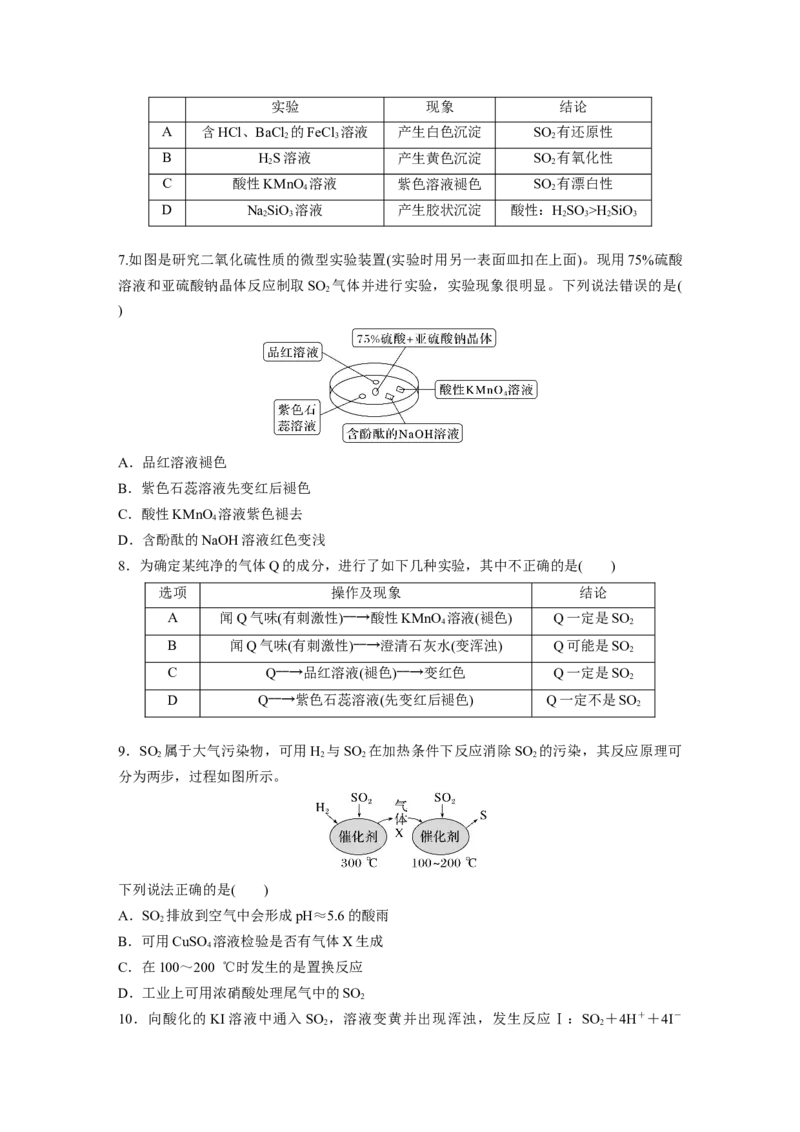
6.根据SO 通入不同溶液中的实验现象,所得结论不正确的是( )
2实验 现象 结论
A 含HCl、BaCl 的FeCl 溶液 产生白色沉淀 SO 有还原性
2 3 2
B HS溶液 产生黄色沉淀 SO 有氧化性
2 2
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
D NaSiO 溶液 产生胶状沉淀 酸性:HSO >H SiO
2 3 2 3 2 3
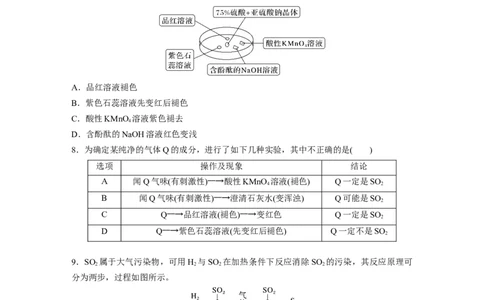
7.如图是研究二氧化硫性质的微型实验装置(实验时用另一表面皿扣在上面)。现用75%硫酸
溶液和亚硫酸钠晶体反应制取SO 气体并进行实验,实验现象很明显。下列说法错误的是(
2
)
A.品红溶液褪色
B.紫色石蕊溶液先变红后褪色
C.酸性KMnO 溶液紫色褪去
4
D.含酚酞的NaOH溶液红色变浅
8.为确定某纯净的气体Q的成分,进行了如下几种实验,其中不正确的是( )
选项 操作及现象 结论
A 闻Q气味(有刺激性)――→酸性KMnO 溶液(褪色) Q一定是SO
4 2
B 闻Q气味(有刺激性)――→澄清石灰水(变浑浊) Q可能是SO
2
C Q――→品红溶液(褪色)――→变红色 Q一定是SO
2
D Q――→紫色石蕊溶液(先变红后褪色) Q一定不是SO
2
9.SO 属于大气污染物,可用H 与SO 在加热条件下反应消除SO 的污染,其反应原理可
2 2 2 2
分为两步,过程如图所示。
下列说法正确的是( )
A.SO 排放到空气中会形成pH≈5.6的酸雨
2
B.可用CuSO 溶液检验是否有气体X生成
4
C.在100~200 ℃时发生的是置换反应
D.工业上可用浓硝酸处理尾气中的SO
2
10.向酸化的KI溶液中通入SO ,溶液变黄并出现浑浊,发生反应Ⅰ:SO +4H++4I-
2 2===2I +S↓+2HO,继续通入SO ,溶液变为无色,发生反应Ⅱ:I +SO +2HO===SO+
2 2 2 2 2 2
4H++2I-。下列说法错误的是( )
A.SO 、I 的氧化性强弱与外界条件有关
2 2
B.每生成0.1 mol SO,整个过程中转移0.4 mol电子,同时消耗0.2 mol KI
C.该过程的总反应为3SO +2HO===2SO+S↓+4H+
2 2
D.该反应过程中KI作催化剂
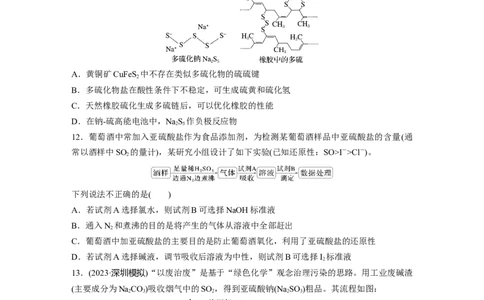
11.多硫化物是指含有硫硫键的化合物,在电池、橡胶等多种工业中均有重要用途,其结构
如图。下列推测不正确的是( )
A.黄铜矿CuFeS 中不存在类似多硫化物的硫硫键
2
B.多硫化物盐在酸性条件下不稳定,可生成硫黄和硫化氢
C.天然橡胶硫化生成多硫链后,可以优化橡胶的性能
D.在钠-硫高能电池中,NaS 作负极反应物
2 5
12.葡萄酒中常加入亚硫酸盐作为食品添加剂,为检测某葡萄酒样品中亚硫酸盐的含量(通
常以酒样中SO 的量计),某研究小组设计了如下实验(已知还原性:SO>I->Cl-)。
2
下列说法不正确的是( )
A.若试剂A选择氯水,则试剂B可选择NaOH标准液
B.通入N 和煮沸的目的是将产生的气体从溶液中全部赶出
2
C.葡萄酒中加亚硫酸盐的主要目的是防止葡萄酒氧化,利用了亚硫酸盐的还原性
D.若试剂A选择碱液,调节吸收后溶液为中性,则试剂B可选择I 标准液
2
13.(2023·深圳模拟)“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣
(主要成分为NaCO)吸收烟气中的SO ,得到亚硫酸钠(Na SO )粗品。其流程如图:
2 3 2 2 3
(1) 为 加 快 工 业 废 碱 渣 中 NaCO 的 溶 解 , 可 采 取 的 措 施 是
2 3
_____________________________(写出一种即可)。
(2)过程①进行的操作是____________。
(3)上述流程中,加入NaOH后,发生反应的化学方程式为_____________________________。
(4)亚硫酸钠粗品中含有少量NaSO ,原因是_________________________________________。
2 4(5)设计实验证明亚硫酸钠粗品中含有少量NaSO 的方案:在一支试管中,加入少量亚硫酸
2 4
钠粗品,用适量蒸馏水溶解,_____________________________________________________
______________________________________________________________________________,
出现白色沉淀,则证明含有NaSO 。
2 4
14.碳、硫的含量对钢铁性能影响很大,其含量的一种测定方法是将钢样中碳、硫转化为气
体,再用测碳、测硫装置进行测定。实验流程如图:
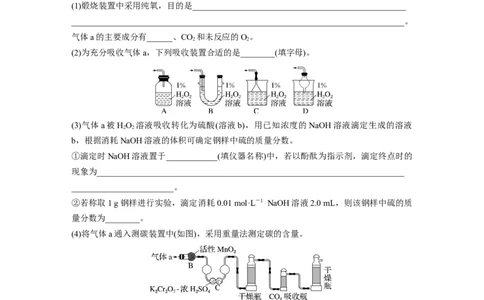
(1)煅烧装置中采用纯氧,目的是__________________________________________________
______________________________________________________________________________。
气体a的主要成分有______、CO 和未反应的O。
2 2
(2)为充分吸收气体a,下列吸收装置合适的是________(填字母)。
(3)气体a被HO 溶液吸收转化为硫酸(溶液b),用已知浓度的NaOH溶液滴定生成的溶液
2 2
b,根据消耗NaOH溶液的体积可确定钢样中硫的质量分数。
①滴定时NaOH溶液置于____________(填仪器名称)中,若以酚酞为指示剂,滴定终点时的
现象为________________________________________________________________________
________________________。
②若称取1 g钢样进行实验,滴定消耗0.01 mol·L-1 NaOH溶液2.0 mL,则该钢样中硫的质
量分数为________。
(4)将气体a通入测碳装置中(如图),采用重量法测定碳的含量。
①气体a通过B和C的目的是除去SO ,通过所用试剂判断该法所利用的 SO 的性质是
2 2
____________________________________________________________________________。
②计算钢样中碳的质量分数,应测量的数据是____________________________________。