文档内容
1.许多物质性质上都存在着递变规律,下列有关说法正确的是( )
A.卤化银的颜色按AgCl、AgBr、AgI的顺序依次变浅
B.卤化氢的键长按H—F、H—Cl、H—Br、H—I的顺序依次增大
C.卤化氢的沸点按HF、HCl、HBr、HI的顺序依次升高
D.卤素单质与氢气化合按F、Cl、Br 、I 的顺序由难变易
2 2 2 2
2.下列说法正确的是( )
A.Fe Cl 根据化合价规律可表示为FeCl ·2FeCl ,则Fe I 也可表示为FeI·2FeI
3 8 2 3 3 8 2 3
B.第ⅦA族元素的非金属性:F>Cl,所以第ⅦA族元素氢化物的酸性:HF>HCl
C.Cl、Br 、I 的单质颜色逐渐变深
2 2 2
D.根据卤族元素性质的递变规律可知,砹易溶于水,难溶于CCl
4
3.已知NaCN溶液呈碱性;(CN) 与卤素单质的性质相似;CN-的还原性介于Br-、I-之间。
2
下列变化不能发生的是( )
A.HCNH++CN-
B.(CN) + CH===CH―→ NC—CH —CH—CN
2 2 2 2 2
C.(CN) +2Br-===2CN-+Br
2 2
D.(CN) + 2OH-===CN-+ CNO-+ HO
2 2
4.下列关于卤素的叙述正确的是( )
①卤素的钾盐中,最易被氧化的是氟化钾 ②溴中溶有少量氯气,可以加入溴化钠再用汽油
萃取的方法提纯 ③溴化银具有感光性,碘化银不具有感光性 ④某溶液与淀粉-KI溶液反
应出现蓝色,则证明该溶液是氯水或溴水 ⑤氟气与氯化钠水溶液反应,一定有氟化氢和氧
气生成 ⑥氯气与水反应时,水既不是氧化剂也不是还原剂
A.①③⑤ B.②③⑥
C.②⑤⑥ D.①③④
5.下列能够检验出KI中是否含有Br-的实验是( )
A.加入足量的新制氯水,溶液变色则有Br-
B.加入酸性KMnO 溶液,观察溶液颜色是否褪去
4
C.加入少量的碘水,再加入CCl 振荡,有机层有色,则有Br-
4
D.加入足量FeCl 溶液,用CCl 萃取后,取无色的水层并加入AgNO 溶液,有浅黄色沉淀
3 4 3
生成,则含有Br-
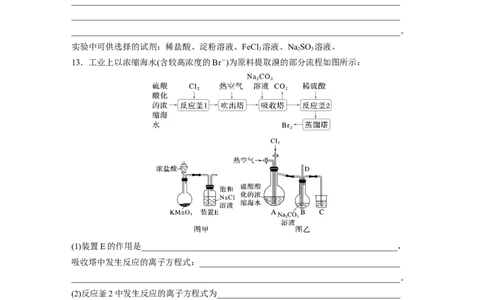
6.某小组比较Cl-、Br-、I- 的还原性,实验如下:
实验1 实验2 实验3装置
溶液颜色无明显变化;把蘸
溶液变黄;把湿润的淀粉- 溶液变深紫色;经
现象 有浓氨水的玻璃棒靠近试管
KI试纸靠近试管口,变蓝 检验溶液含单质碘
口,产生白烟
下列对实验的分析不合理的是( )
A.实验1中,白烟是NH Cl
4
B.根据实验1和实验2判断还原性:Br->Cl-
C.根据实验3判断还原性:I->Br-
D.上述实验利用了浓HSO 的氧化性、难挥发性等性质
2 4
7.某同学向一支试管中按一定的顺序分别加入下列几种物质(一种物质只加一次):a.KI溶
液;b.淀粉溶液;c.NaOH溶液;d.稀硫酸;e.氯水。发现溶液颜色按如下顺序变化:①无色
→②棕黄色→③蓝色→④无色→⑤蓝色。下列对此过程进行的分析中错误的是( )
A.加入以上药品的顺序是a→e→b→c→d
B.③→④反应的化学方程式为3I+6NaOH===5NaI+NaIO +3HO
2 3 2
C.溶液由棕黄色变为蓝色的原因是淀粉溶液遇碘变蓝色
D.④→⑤反应的离子方程式为2I-+Cl===I+2Cl-
2 2
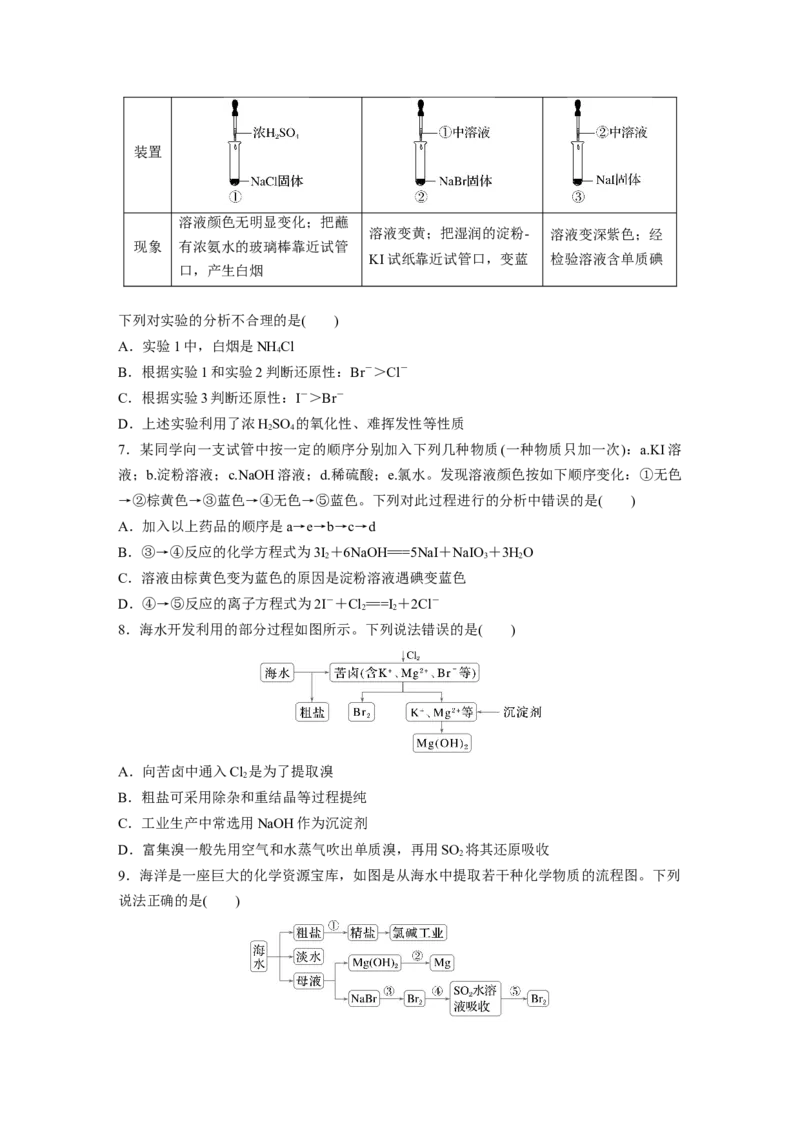
8.海水开发利用的部分过程如图所示。下列说法错误的是( )
A.向苦卤中通入Cl 是为了提取溴
2
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产中常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO 将其还原吸收
2
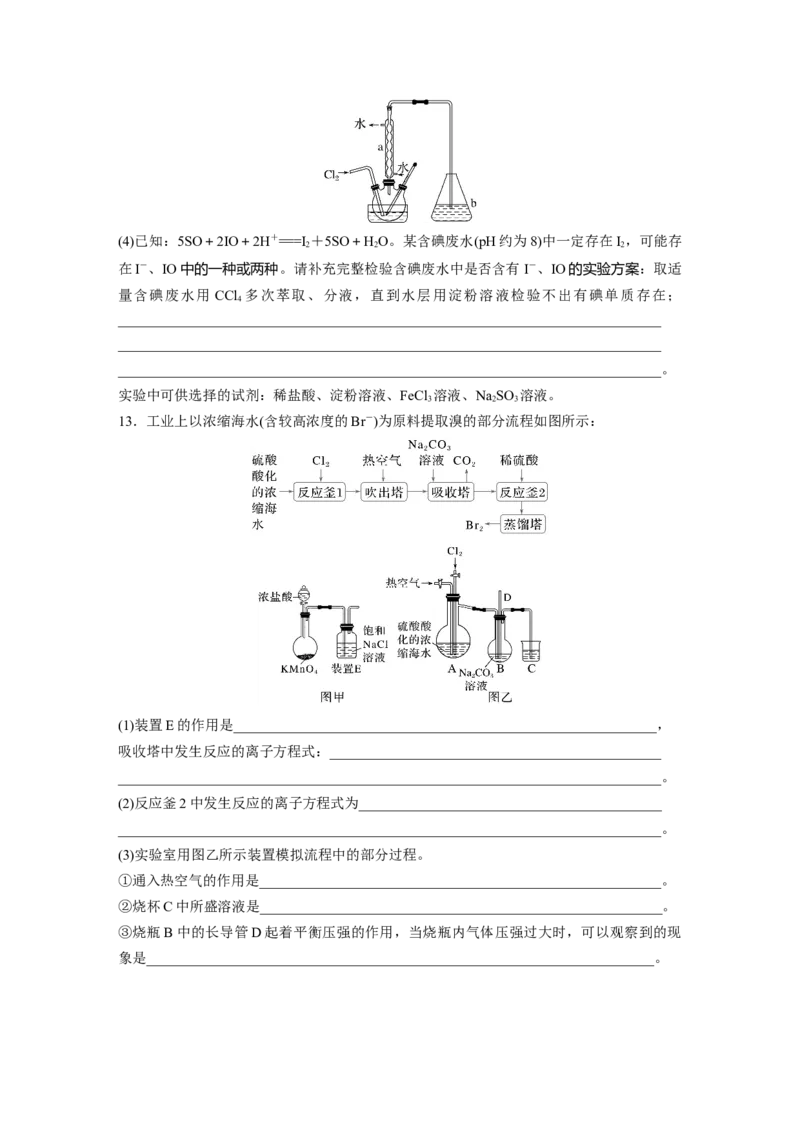
9.海洋是一座巨大的化学资源宝库,如图是从海水中提取若干种化学物质的流程图。下列
说法正确的是( )A.除去粗盐中的SO、Ca2+、Mg2+、Fe3+等杂质,①中加入试剂的顺序为NaCO 溶液
2 3
→NaOH溶液→BaCl 溶液→过滤后加盐酸
2
B.②中包含制取MgCl 溶液、无水MgCl 及电解熔融状态的MgCl 几个阶段
2 2 2
C.氯碱工业可直接得到H、O、NaOH
2 2
D.SO 水溶液吸收Br 的离子方程式为SO +Br +2HO===2H++SO+2HBr
2 2 2 2 2
10.“XY ”表示不同卤素之间靠共用电子对形成的卤素互化物(非金属性:X