文档内容
1.用下列两种途径制取HSO ,某些反应条件和产物已省略,下列有关说法不正确的是(
2 4
)
途径① S――→HSO ;
2 4
途径② S――→SO ――→SO ――→HSO
2 3 2 4
A.途径①反应中体现了浓硝酸的强氧化性和酸性
B.途径②的第二步反应在实际生产中可以通过增大O 的浓度来降低成本
2
C.由途径①和②分别制取1 mol H SO ,理论上各消耗1 mol S,各转移6 mol电子
2 4
D.途径②与途径①相比更能体现“绿色化学”的理念
2.硫在空气中燃烧生成气体A,把A溶于水得溶液B,向B中滴加溴水,溴水褪色,B变
成C,向C中加NaS产生气体D,把D通入B溶液得浅黄色沉淀E。A、B、C、D、E都含
2
同一种元素。下列各物质按A、B、C、D、E顺序排列的是( )
A.SO 、HSO 、HSO 、HS、S
2 2 4 2 3 2
B.SO 、HSO 、HSO 、HS、S
2 2 3 2 4 2
C.SO 、HSO 、HSO 、SO 、NaSO
2 2 3 2 4 3 2 2 3
D.SO 、HSO 、HSO 、SO 、NaSO
3 2 4 2 3 2 2 2 3
3.(2023·长春模拟)在“价—类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及
其定量关系。图中的字母分别代表硫及其常见化合物,下列相关推断不合理的是( )
A.b、d、f既具有氧化性又具有还原性
B.硫酸型酸雨的形成过程涉及b到c的转化
C.a溶液与b溶液反应过程中有淡黄色沉淀生成
D.d在加热条件下与强碱溶液反应生成e和f,且n(e)∶n(f)=1∶2
4.如图是硫元素在自然界中的循环示意图,下列说法不正确的是( )A.海水中的硫元素主要以S2-形式存在
B.煤中含有硫元素,燃煤中加入生石灰可脱硫
C.硫具有弱氧化性,和变价金属反应,通常将金属氧化成低价态
D.硫化氢溶于水得到氢硫酸,氢硫酸是弱酸,能与碱、碱性氧化物反应
5.如图是一种综合处理SO 废气的工艺流程。下列说法正确的是( )
2
A.向溶液B中滴加KSCN溶液,溶液可能变为红色
B.溶液B转化为溶液C发生反应的离子方程式为4H++2Fe2++O===2Fe3++2HO
2 2
C.溶液酸性:A>B>C
D.加氧化亚铁可以使溶液C转化为溶液A
6.“蓝天保卫战”需要持续进行大气治理,有效处理SO 、NO 等大气污染物。化学研究
2 2
为生产、生活处理废气,防止大气污染做出重要贡献。将SO 转化为KSO 的工艺流程如图,
2 2 4
下列说法正确的是( )
A.通入空气的目的是将CO 完全吹出
2
B.反应时应将CaCO 粉碎
3
C.固体产物A是CaSO
3
D.“高温”时只发生CaCO 的分解反应
3
7.(2023·石家庄高三联考)硫及其化合物的“价—类”二维图体现了化学变化之美。下列有
关说法正确的是( )
A.硫在过量的氧气中燃烧直接生成Y
B.将X通入BaCl 溶液中有白色沉淀生成
2
C.M的无水固体粉末显蓝色
D.N与Z反应可生成X
8.硫化氢的转化是资源利用和环境保护的重要研究课题。将 HS和空气的混合气体通入
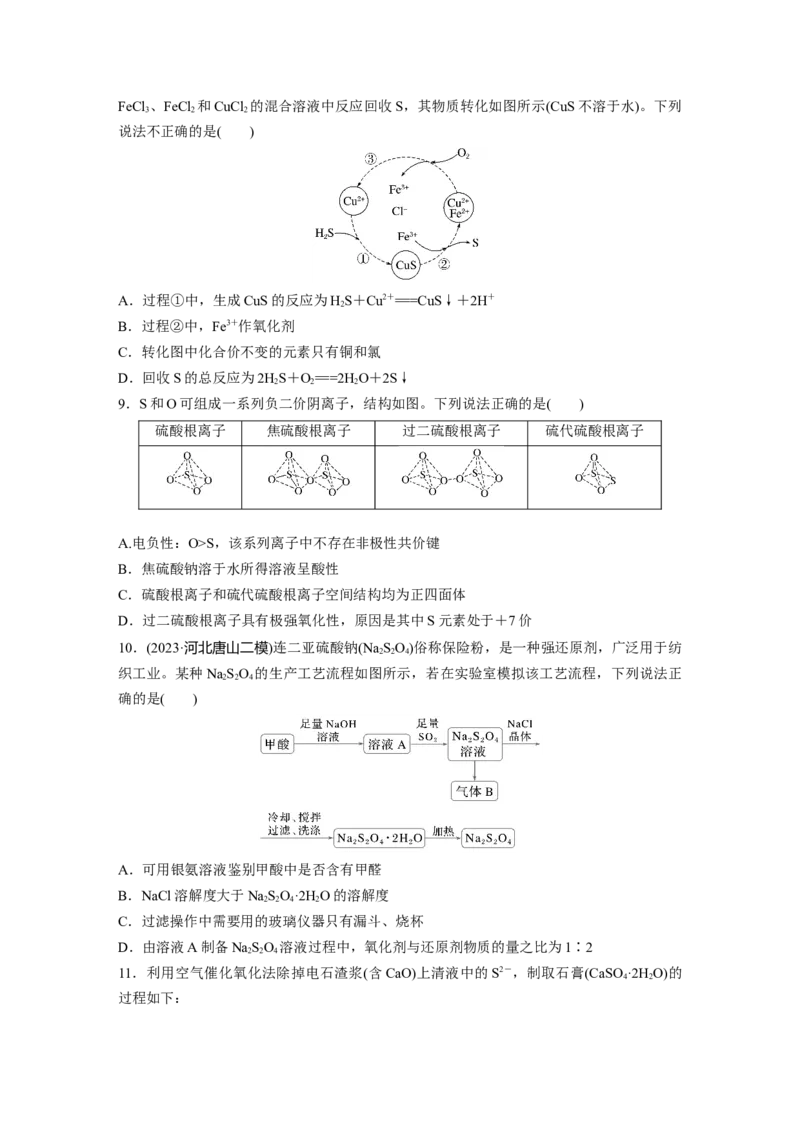
2FeCl 、FeCl 和CuCl 的混合溶液中反应回收S,其物质转化如图所示(CuS不溶于水)。下列
3 2 2
说法不正确的是( )
A.过程①中,生成CuS的反应为HS+Cu2+===CuS↓+2H+
2
B.过程②中,Fe3+作氧化剂
C.转化图中化合价不变的元素只有铜和氯
D.回收S的总反应为2HS+O===2HO+2S↓
2 2 2
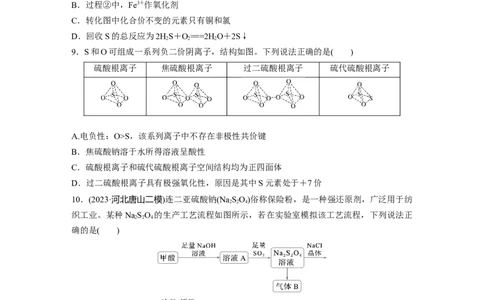
9.S和O可组成一系列负二价阴离子,结构如图。下列说法正确的是( )
硫酸根离子 焦硫酸根离子 过二硫酸根离子 硫代硫酸根离子
A.电负性:O>S,该系列离子中不存在非极性共价键
B.焦硫酸钠溶于水所得溶液呈酸性
C.硫酸根离子和硫代硫酸根离子空间结构均为正四面体
D.过二硫酸根离子具有极强氧化性,原因是其中S元素处于+7价
10.(2023·河北唐山二模)连二亚硫酸钠(Na SO)俗称保险粉,是一种强还原剂,广泛用于纺
2 2 4
织工业。某种NaSO 的生产工艺流程如图所示,若在实验室模拟该工艺流程,下列说法正
2 2 4
确的是( )
A.可用银氨溶液鉴别甲酸中是否含有甲醛
B.NaCl溶解度大于NaSO·2H O的溶解度
2 2 4 2
C.过滤操作中需要用的玻璃仪器只有漏斗、烧杯
D.由溶液A制备NaSO 溶液过程中,氧化剂与还原剂物质的量之比为1∶2
2 2 4
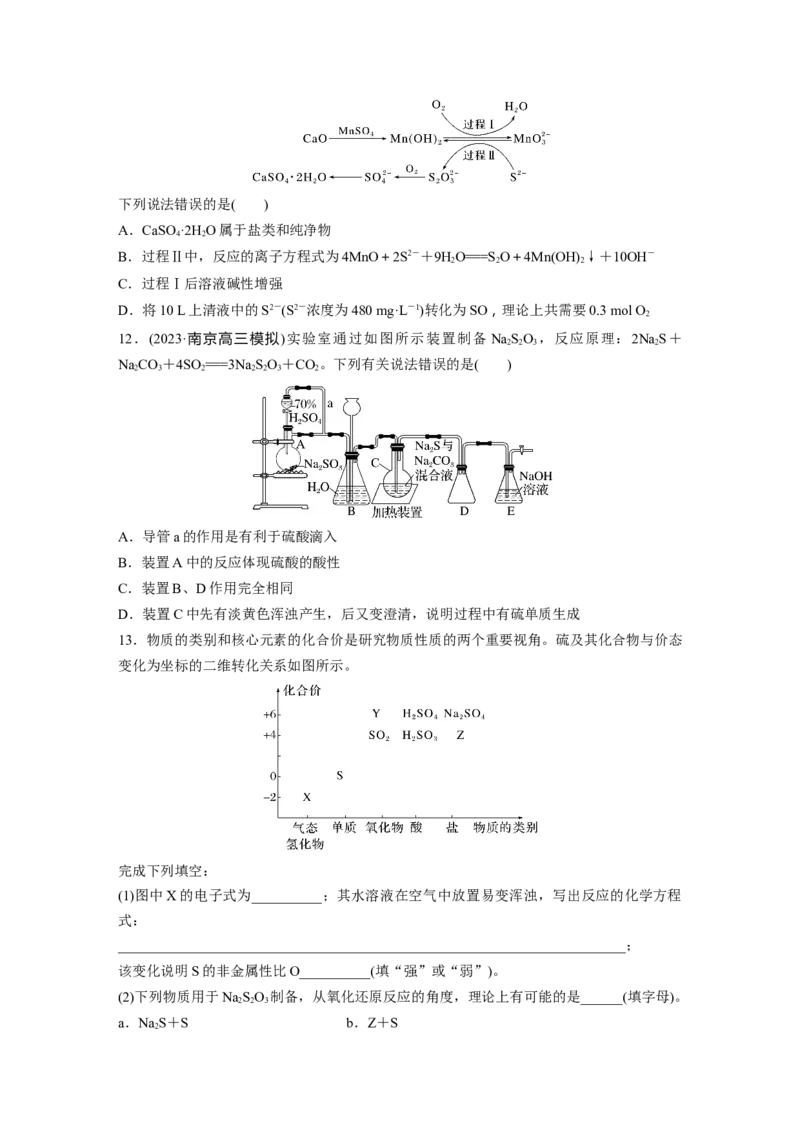
11.利用空气催化氧化法除掉电石渣浆(含CaO)上清液中的S2-,制取石膏(CaSO·2H O)的
4 2
过程如下:下列说法错误的是( )
A.CaSO·2H O属于盐类和纯净物
4 2
B.过程Ⅱ中,反应的离子方程式为4MnO+2S2-+9HO===SO+4Mn(OH) ↓+10OH-
2 2 2
C.过程Ⅰ后溶液碱性增强
D.将10 L上清液中的S2-(S2-浓度为480 mg·L-1)转化为SO,理论上共需要0.3 mol O
2
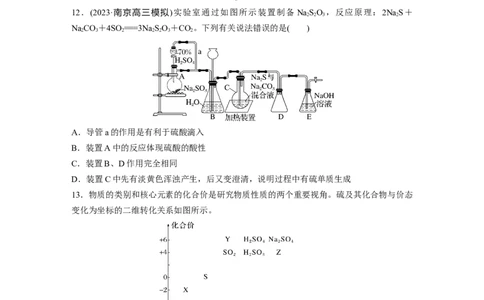
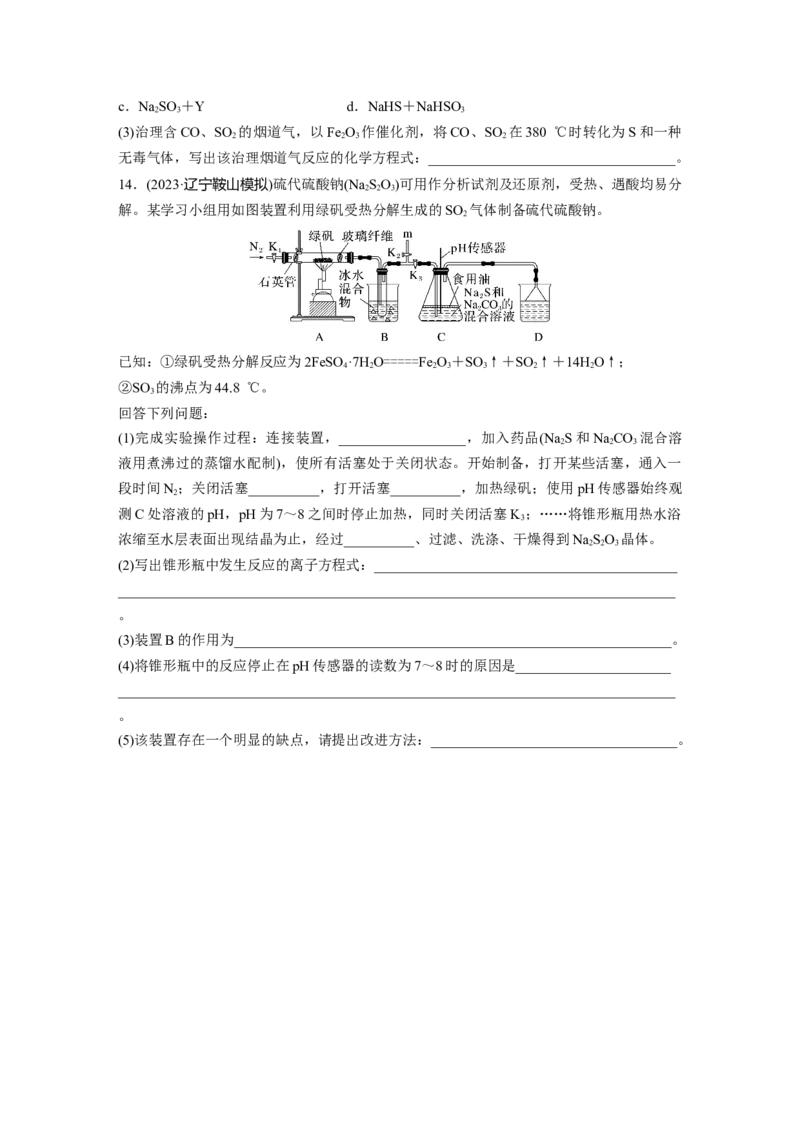
12.(2023·南京高三模拟)实验室通过如图所示装置制备 NaSO ,反应原理:2NaS+
2 2 3 2
NaCO+4SO ===3NaSO+CO。下列有关说法错误的是( )
2 3 2 2 2 3 2
A.导管a的作用是有利于硫酸滴入
B.装置A中的反应体现硫酸的酸性
C.装置B、D作用完全相同
D.装置C中先有淡黄色浑浊产生,后又变澄清,说明过程中有硫单质生成
13.物质的类别和核心元素的化合价是研究物质性质的两个重要视角。硫及其化合物与价态
变化为坐标的二维转化关系如图所示。
完成下列填空:
(1)图中X的电子式为__________;其水溶液在空气中放置易变浑浊,写出反应的化学方程
式:
________________________________________________________________________;
该变化说明S的非金属性比O__________(填“强”或“弱”)。
(2)下列物质用于NaSO 制备,从氧化还原反应的角度,理论上有可能的是______(填字母)。
2 2 3
a.NaS+S b.Z+S
2c.NaSO +Y d.NaHS+NaHSO
2 3 3
(3)治理含CO、SO 的烟道气,以Fe O 作催化剂,将CO、SO 在380 ℃时转化为S和一种
2 2 3 2
无毒气体,写出该治理烟道气反应的化学方程式:___________________________________。
14.(2023·辽宁鞍山模拟)硫代硫酸钠(Na SO)可用作分析试剂及还原剂,受热、遇酸均易分
2 2 3
解。某学习小组用如图装置利用绿矾受热分解生成的SO 气体制备硫代硫酸钠。
2
已知:①绿矾受热分解反应为2FeSO ·7H O=====Fe O+SO ↑+SO ↑+14HO↑;
4 2 2 3 3 2 2
②SO 的沸点为44.8 ℃。
3
回答下列问题:
(1)完成实验操作过程:连接装置,__________________,加入药品(Na S和NaCO 混合溶
2 2 3
液用煮沸过的蒸馏水配制),使所有活塞处于关闭状态。开始制备,打开某些活塞,通入一
段时间N ;关闭活塞__________,打开活塞__________,加热绿矾;使用pH传感器始终观
2
测C处溶液的pH,pH为7~8之间时停止加热,同时关闭活塞K ;……将锥形瓶用热水浴
3
浓缩至水层表面出现结晶为止,经过__________、过滤、洗涤、干燥得到NaSO 晶体。
2 2 3
(2)写出锥形瓶中发生反应的离子方程式:___________________________________________
_______________________________________________________________________________
。
(3)装置B的作用为______________________________________________________________。
(4)将锥形瓶中的反应停止在pH传感器的读数为7~8时的原因是______________________
_______________________________________________________________________________
。
(5)该装置存在一个明显的缺点,请提出改进方法:___________________________________。