文档内容
1.二十四节气是中国历法的独特创造。四月农谚:“雷雨肥田”“雨生百谷”描述的都是
节气谷雨。下列元素在自然界中的转化与“雷雨肥田”有关的是( )
A.K B.N C.P D.C
2.据研究,NO广泛分布于生物体内各组织中,可将积存在血管壁上的脂肪、胆固醇带走,
被称为“血管清道夫”。下列说法中错误的是( )
A.NO极易与氧气反应生成一种红棕色气体
B.实验室中,可利用铜与稀硝酸的反应制取NO
C.人体吸入大量NO气体,可以预防心血管疾病
D.雷雨天气,氮气和氧气能生成NO
3.硝酸被称为“国防工业之母”,是因为它是制取炸药的重要原料。下列实验事实与硝酸
性质对应不准确的一组是( )
A.硝酸能与FeO反应——酸性和氧化性
B.不能用稀硝酸与锌反应制氢气——强氧化性
C.要用棕色试剂瓶盛装浓硝酸——不稳定性
D.能使滴有酚酞的氢氧化钠溶液红色褪去——强氧化性
4.(2023·海口高三联考)下列关于氮及其化合物的探究,结论和解释正确的是( )
操作和现象 结论和解释
A 铜丝溶解于稀HNO,生成无色气体 金属能与强酸反应置换出氢气
3
B NH 能使热的氧化铜产生红色物质 NH 有还原性
3 3
C N 与H 混合加热不反应 N的非金属性弱
2 2
D NO 被NaOH溶液吸收 NO 是酸性氧化物
2 2
5.某集气瓶内装有红棕色气体,加入足量蒸馏水后盖上玻璃片振荡,得橙黄色溶液,气体颜
色消失;再打开玻璃片后,瓶中气体又变为红棕色,则该气体可能是( )
A.N、NO 、Br (g) B.NO 、NO、N
2 2 2 2 2
C.NO 、NO、O D.N、O、Br (g)
2 2 2 2 2
6.(2022·北京,12)某MOFs的多孔材料刚好可将NO“固定”,高能选择性吸附NO 。废
2 4 2
气中的NO 被吸附后,经处理能全部转化为HNO。原理示意图如下。
2 3已知:2NO (g)NO(g) ΔH<0
2 2 4
下列说法不正确的是( )
A.温度升高时不利于NO 吸附
2
B.多孔材料“固定”NO,促进2NO (g)NO(g)平衡正向移动
2 4 2 2 4
C.制备HNO 的原理为:2NO+O+2HO===4HNO
3 2 4 2 2 3
D.每制备0.4 mol HNO ,转移电子数约为6.02×1022
3
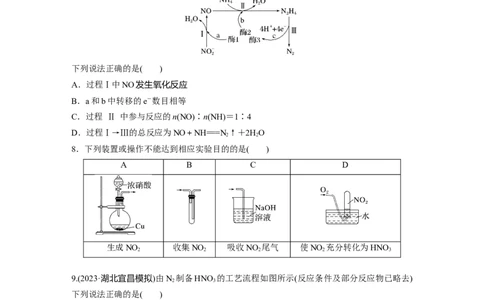
7.(2022·湖南,9)科学家发现某些生物酶体系可以促进H+和e-的转移(如a、b和c),能将
海洋中的NO转化为N 进入大气层,反应过程如图所示。
2
下列说法正确的是( )
A.过程Ⅰ中NO发生氧化反应
B.a和b中转移的e-数目相等
C.过程 Ⅱ 中参与反应的n(NO)∶n(NH)=1∶4
D.过程Ⅰ→Ⅲ的总反应为NO+NH===N↑+2HO
2 2
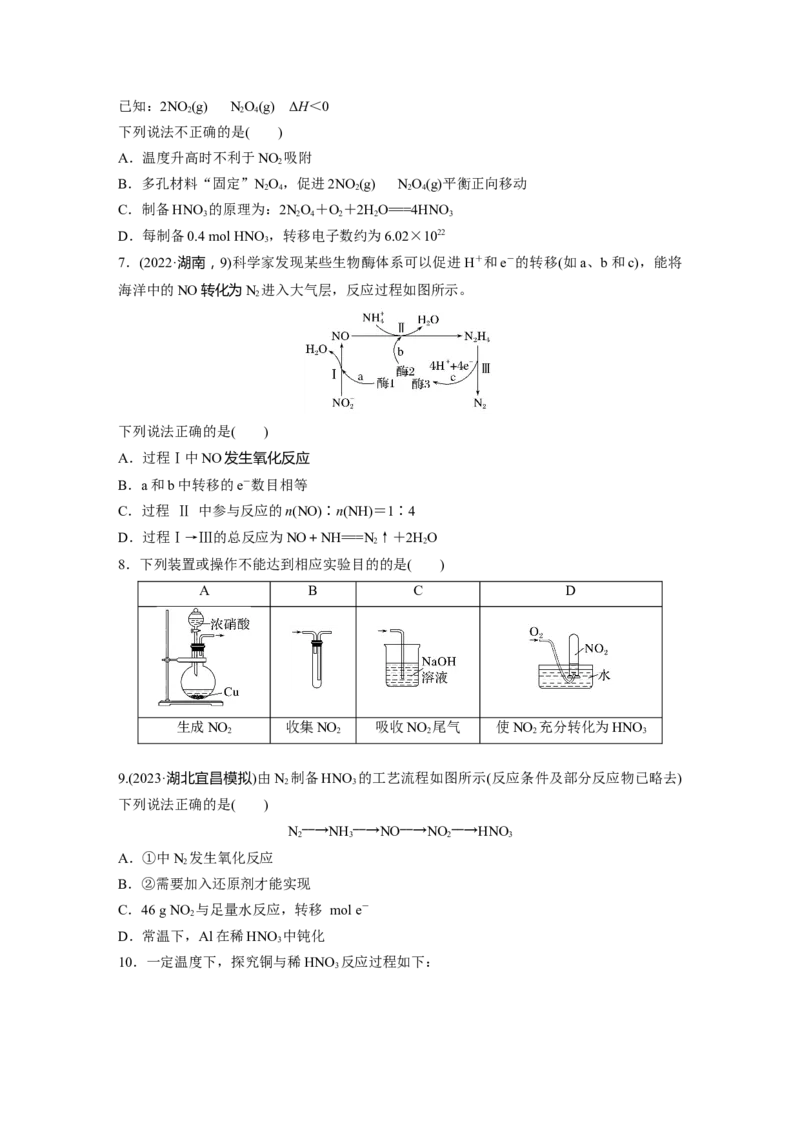
8.下列装置或操作不能达到相应实验目的的是( )
A B C D
生成NO 收集NO 吸收NO 尾气 使NO 充分转化为HNO
2 2 2 2 3
9.(2023·湖北宜昌模拟)由N 制备HNO 的工艺流程如图所示(反应条件及部分反应物已略去)
2 3
下列说法正确的是( )
N――→NH ――→NO――→NO ――→HNO
2 3 2 3
A.①中N 发生氧化反应
2
B.②需要加入还原剂才能实现
C.46 g NO 与足量水反应,转移 mol e-
2
D.常温下,Al在稀HNO 中钝化
3
10.一定温度下,探究铜与稀HNO 反应过程如下:
3下列说法不正确的是( )
A.过程Ⅰ中生成无色气体的离子方程式是3Cu+2NO+8H+===3Cu2++2NO↑+4HO
2
B.步骤Ⅲ反应速率比Ⅰ快的原因是NO 溶于水,使c(HNO)增大
2 3
C.由实验可知,NO 对该反应具有催化作用
2
D.当活塞不再移动时,再抽入空气,铜可以继续溶解
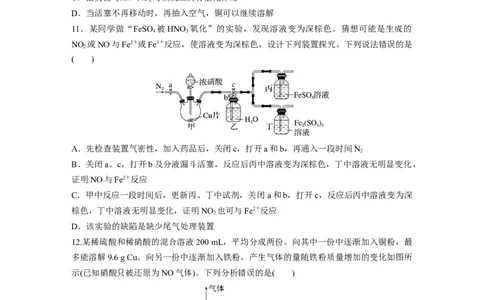
11.某同学做“FeSO 被HNO 氧化”的实验,发现溶液变为深棕色。猜想可能是生成的
4 3
NO 或NO与Fe2+或Fe3+反应,使溶液变为深棕色,设计下列装置探究。下列说法错误的是
2
( )
A.先检查装置气密性,加入药品后,关闭c,打开a和b,再通入一段时间N
2
B.关闭a、c,打开b及分液漏斗活塞,反应后丙中溶液变为深棕色,丁中溶液无明显变化,
证明NO与Fe2+反应
C.甲中反应一段时间后,更新丙、丁中试剂,关闭a和b,打开c,反应后丙中溶液变为深
棕色,丁中溶液无明显变化,证明NO 也可与Fe2+反应
2
D.该实验的缺陷是缺少尾气处理装置
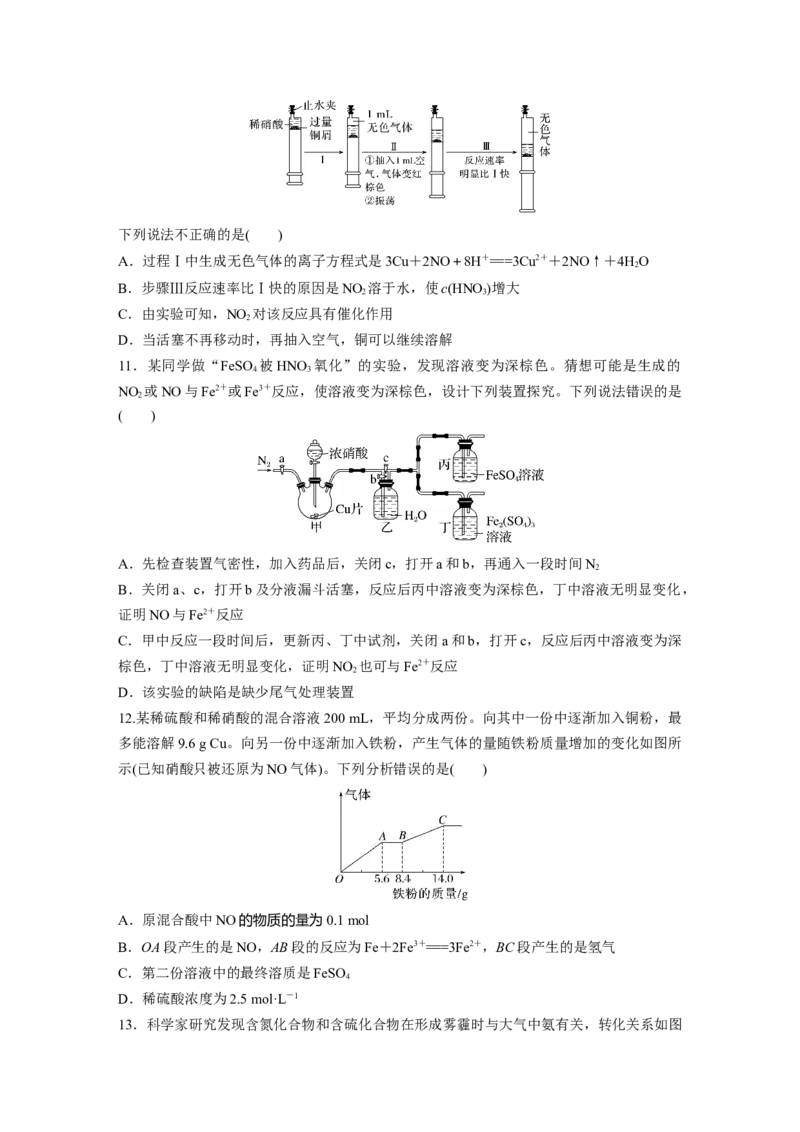
12.某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最
多能溶解9.6 g Cu。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所
示(已知硝酸只被还原为NO气体)。下列分析错误的是( )
A.原混合酸中NO的物质的量为0.1 mol
B.OA段产生的是NO,AB段的反应为Fe+2Fe3+===3Fe2+,BC段产生的是氢气
C.第二份溶液中的最终溶质是FeSO
4
D.稀硫酸浓度为2.5 mol·L-1
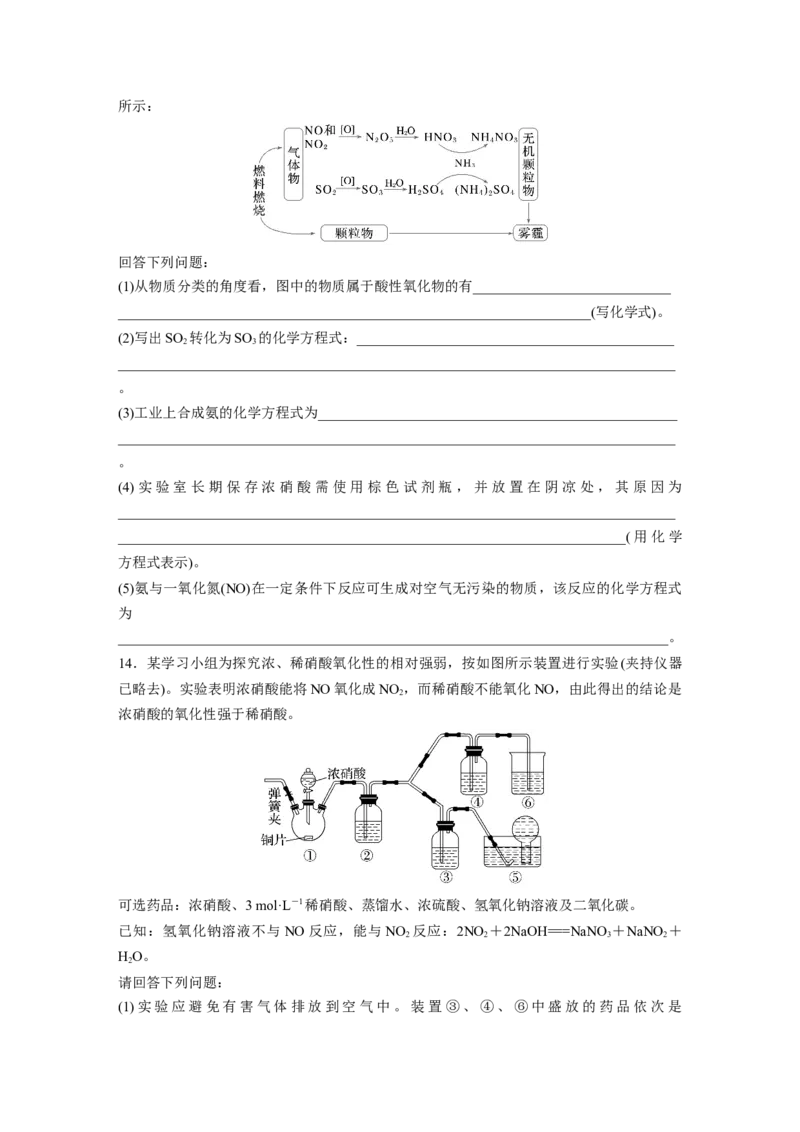
13.科学家研究发现含氮化合物和含硫化合物在形成雾霾时与大气中氨有关,转化关系如图所示:
回答下列问题:
(1)从物质分类的角度看,图中的物质属于酸性氧化物的有____________________________
___________________________________________________________________(写化学式)。
(2)写出SO 转化为SO 的化学方程式:_____________________________________________
2 3
_______________________________________________________________________________
。
(3)工业上合成氨的化学方程式为___________________________________________________
_______________________________________________________________________________
。
(4)实验室长期保存浓硝酸需使用棕色试剂瓶,并放置在阴凉处,其原因为
_______________________________________________________________________________
________________________________________________________________________(用化学
方程式表示)。
(5)氨与一氧化氮(NO)在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式
为
______________________________________________________________________________。
14.某学习小组为探究浓、稀硝酸氧化性的相对强弱,按如图所示装置进行实验(夹持仪器
已略去)。实验表明浓硝酸能将NO氧化成NO ,而稀硝酸不能氧化NO,由此得出的结论是
2
浓硝酸的氧化性强于稀硝酸。
可选药品:浓硝酸、3 mol·L-1稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳。
已知:氢氧化钠溶液不与NO反应,能与NO 反应:2NO +2NaOH===NaNO +NaNO +
2 2 3 2
HO。
2
请回答下列问题:
(1)实验应避免有害气体排放到空气中。装置 ③、④、⑥中盛放的药品依次是___________________________________________________________________________。
(2) 实 验 的 具 体 操 作 : 先 检 查 装 置 的 气 密 性 , 再 加 入 药 品 , 然 后
____________________________
____________________________________________________,最后滴加浓硝酸。
(3)装置①中发生反应的化学方程式是_______________________________________________
_______________________________________________________________________________
。
(4)装置②的作用是_____________________________________________________________,
发生反应的化学方程式是_________________________________________________________
_______________________________________________________________________________
。
(5)该小组得出的结论所依据的实验现象是___________________________________________
_______________________________________________________________________________
。
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝
酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了
以下4个实验方案来判断两种看法是否正确。这些方案中可行的是________(填字母)。
a.加热该绿色溶液,观察颜色变化
b.加水稀释该绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变