文档内容
1.清代《本草纲目拾遗》中关于“鼻冲水(氨水)”的记载明确指出:“鼻冲水,……贮以
玻璃瓶,紧塞其口,勿使泄气,则药力不减……唯以此水瓶口对鼻吸其气,即遍身麻颤出汗
而愈,虚弱者忌之。宜外用,勿服。”下列有关“鼻冲水”的推断不正确的是( )
A.鼻冲水是弱电解质
B.鼻冲水滴入酚酞溶液中,溶液变红色
C.鼻冲水中含有分子和离子的种类为6种
D.存在平衡:NH +HONH ·H ONH+OH-
3 2 3 2
2.下列离子方程式书写正确的是( )
A.实验室用氯化铵和熟石灰制氨:NH+OH-=====NH ↑+HO
3 2
B.NaOH溶液与NH Cl溶液混合加热:NH+OH-=====NH ·H O
4 3 2
C.氨水中加盐酸:NH ·H O+H+===NH+HO
3 2 2
D.氨水中加入氯化铁溶液:Fe2++2NH ·H O===2NH+Fe(OH) ↓
3 2 2
3.如图所示是NH 的两个性质实验,下列有关说法正确的是( )
3
A.两个实验均表现了NH 易溶于水
3
B.两个实验均表现了NH 易挥发
3
C.两个实验均表现了NH 是碱性气体
3
D.两个实验均表现了NH 是还原性气体
3
4.下列根据实验现象得出的结论不正确的是( )
A.将集有氨的试管倒扣于盛有水的水槽中,液体迅速充满试管,说明氨极易溶于水
B.将湿润的红色石蕊试纸放入集有氨的集气瓶中,试纸由红色变为蓝色,说明氨水呈碱性
C.将蘸有浓氨水和浓硝酸的玻璃棒靠近,观察到白烟,说明氨易与酸化合生成铵盐
D.将红热的Pt丝伸入盛有浓氨水的锥形瓶中,瓶口出现少量红棕色气体,说明氨的直接氧
化产物为NO
2
5.某同学探究氨气和铵盐的性质,对相关实验操作及现象描述正确的是( )
A.室温下测定等浓度的氨水和NaOH溶液的pH,比较NH ·H O和NaOH的碱性强弱
3 2
B.向试管中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口,若试纸不变蓝,则原溶液中无NH
C.液氨作为清洁能源的反应原理是4NH +5O=====4NO+6HO
3 2 2
D.加热可除去NH Cl中的少量NaHCO
4 3
6.(2023·广东肇庆二模)如图装置中,干燥烧瓶内盛有某种气体,烧杯和胶头滴管内盛放某种
溶液。挤压胶头滴管的胶头,下列与实验事实不相符的是( )
A.CO(NaHCO 溶液)/无色喷泉
2 3
B.NH (H O中含酚酞)/红色喷泉
3 2
C.NH (H O中含甲基橙)/黄色喷泉
3 2
D.HCl(AgNO 溶液)/白色喷泉
3
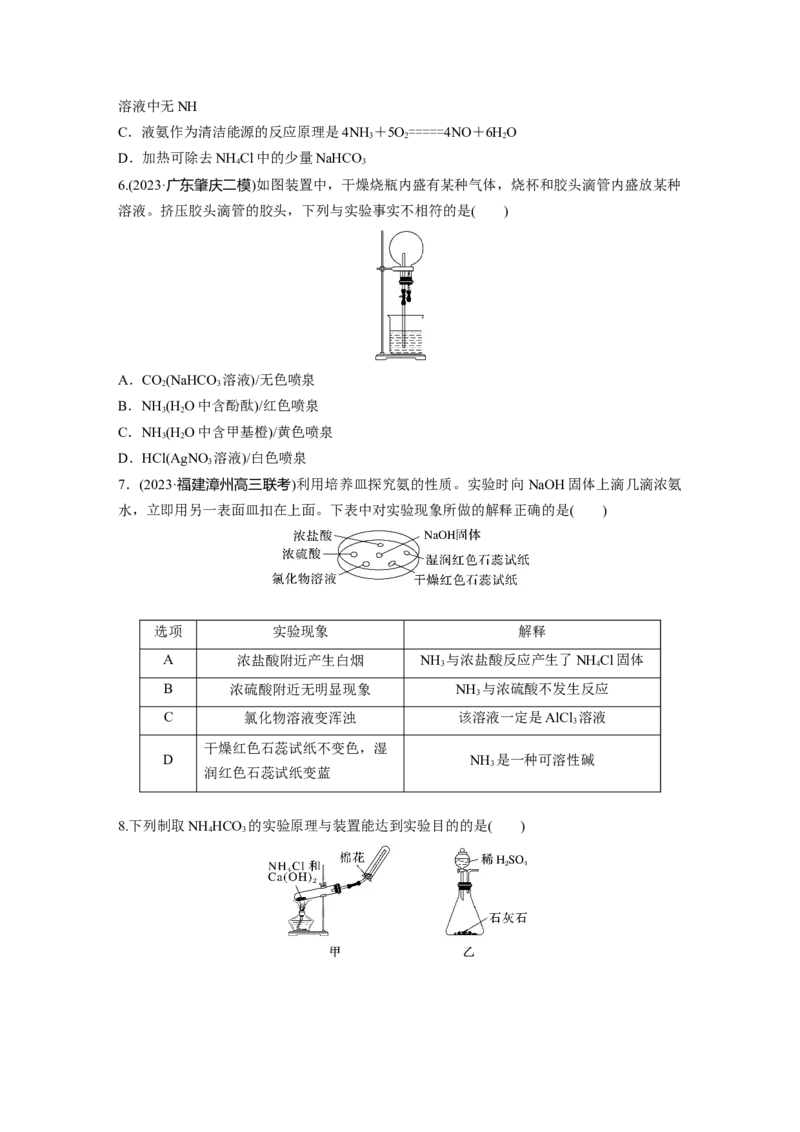
7.(2023·福建漳州高三联考)利用培养皿探究氨的性质。实验时向NaOH固体上滴几滴浓氨
水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是( )
选项 实验现象 解释
A 浓盐酸附近产生白烟 NH 与浓盐酸反应产生了NH Cl固体
3 4
B 浓硫酸附近无明显现象 NH 与浓硫酸不发生反应
3
C 氯化物溶液变浑浊 该溶液一定是AlCl 溶液
3
干燥红色石蕊试纸不变色,湿
D NH 是一种可溶性碱
3
润红色石蕊试纸变蓝
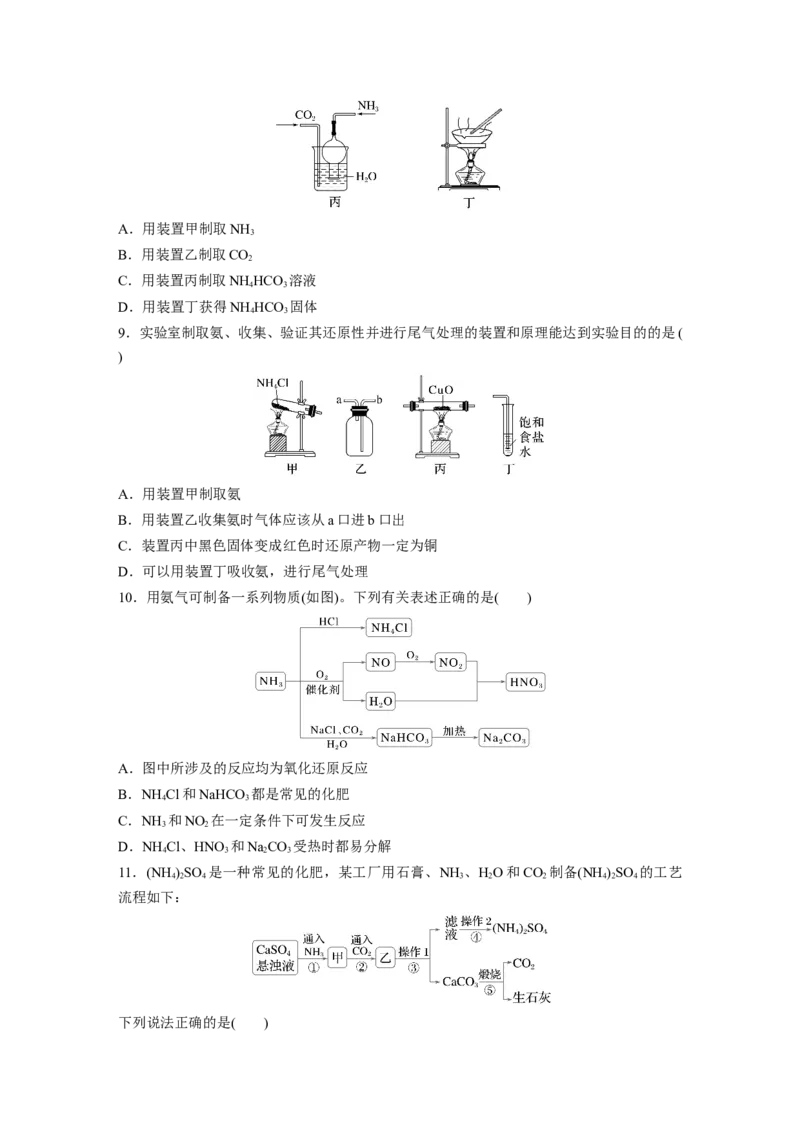
8.下列制取NH HCO 的实验原理与装置能达到实验目的的是( )
4 3A.用装置甲制取NH
3
B.用装置乙制取CO
2
C.用装置丙制取NH HCO 溶液
4 3
D.用装置丁获得NH HCO 固体
4 3
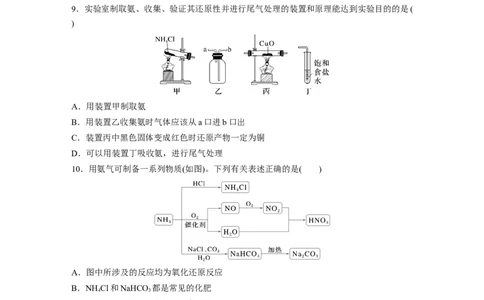
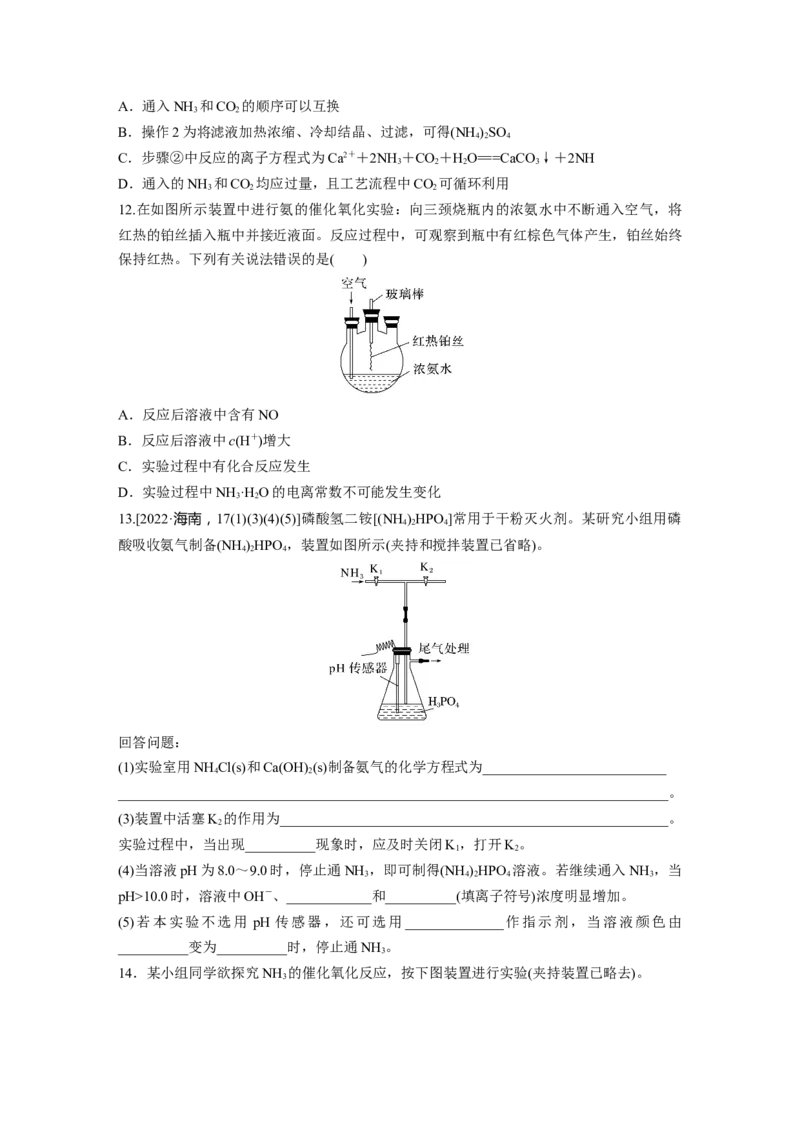
9.实验室制取氨、收集、验证其还原性并进行尾气处理的装置和原理能达到实验目的的是(
)
A.用装置甲制取氨
B.用装置乙收集氨时气体应该从a口进b口出
C.装置丙中黑色固体变成红色时还原产物一定为铜
D.可以用装置丁吸收氨,进行尾气处理
10.用氨气可制备一系列物质(如图)。下列有关表述正确的是( )
A.图中所涉及的反应均为氧化还原反应
B.NH Cl和NaHCO 都是常见的化肥
4 3
C.NH 和NO 在一定条件下可发生反应
3 2
D.NH Cl、HNO 和NaCO 受热时都易分解
4 3 2 3
11.(NH )SO 是一种常见的化肥,某工厂用石膏、NH 、HO和CO 制备(NH )SO 的工艺
4 2 4 3 2 2 4 2 4
流程如下:
下列说法正确的是( )A.通入NH 和CO 的顺序可以互换
3 2
B.操作2为将滤液加热浓缩、冷却结晶、过滤,可得(NH )SO
4 2 4
C.步骤②中反应的离子方程式为Ca2++2NH +CO+HO===CaCO ↓+2NH
3 2 2 3
D.通入的NH 和CO 均应过量,且工艺流程中CO 可循环利用
3 2 2
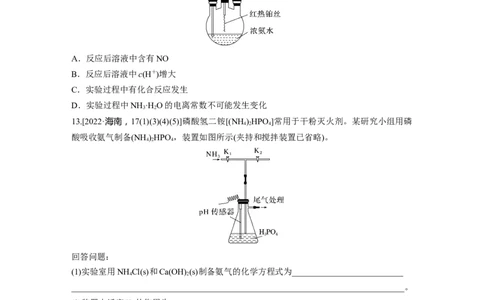
12.在如图所示装置中进行氨的催化氧化实验:向三颈烧瓶内的浓氨水中不断通入空气,将
红热的铂丝插入瓶中并接近液面。反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终
保持红热。下列有关说法错误的是( )
A.反应后溶液中含有NO
B.反应后溶液中c(H+)增大
C.实验过程中有化合反应发生
D.实验过程中NH ·H O的电离常数不可能发生变化
3 2
13.[2022·海南,17(1)(3)(4)(5)]磷酸氢二铵[(NH )HPO ]常用于干粉灭火剂。某研究小组用磷
4 2 4
酸吸收氨气制备(NH )HPO ,装置如图所示(夹持和搅拌装置已省略)。
4 2 4
回答问题:
(1)实验室用NH Cl(s)和Ca(OH) (s)制备氨气的化学方程式为__________________________
4 2
______________________________________________________________________________。
(3)装置中活塞K 的作用为_______________________________________________________。
2
实验过程中,当出现__________现象时,应及时关闭K,打开K。
1 2
(4)当溶液pH为8.0~9.0时,停止通NH ,即可制得(NH )HPO 溶液。若继续通入NH ,当
3 4 2 4 3
pH>10.0时,溶液中OH-、____________和__________(填离子符号)浓度明显增加。
(5)若本实验不选用 pH 传感器,还可选用______________作指示剂,当溶液颜色由
__________变为__________时,停止通NH 。
3
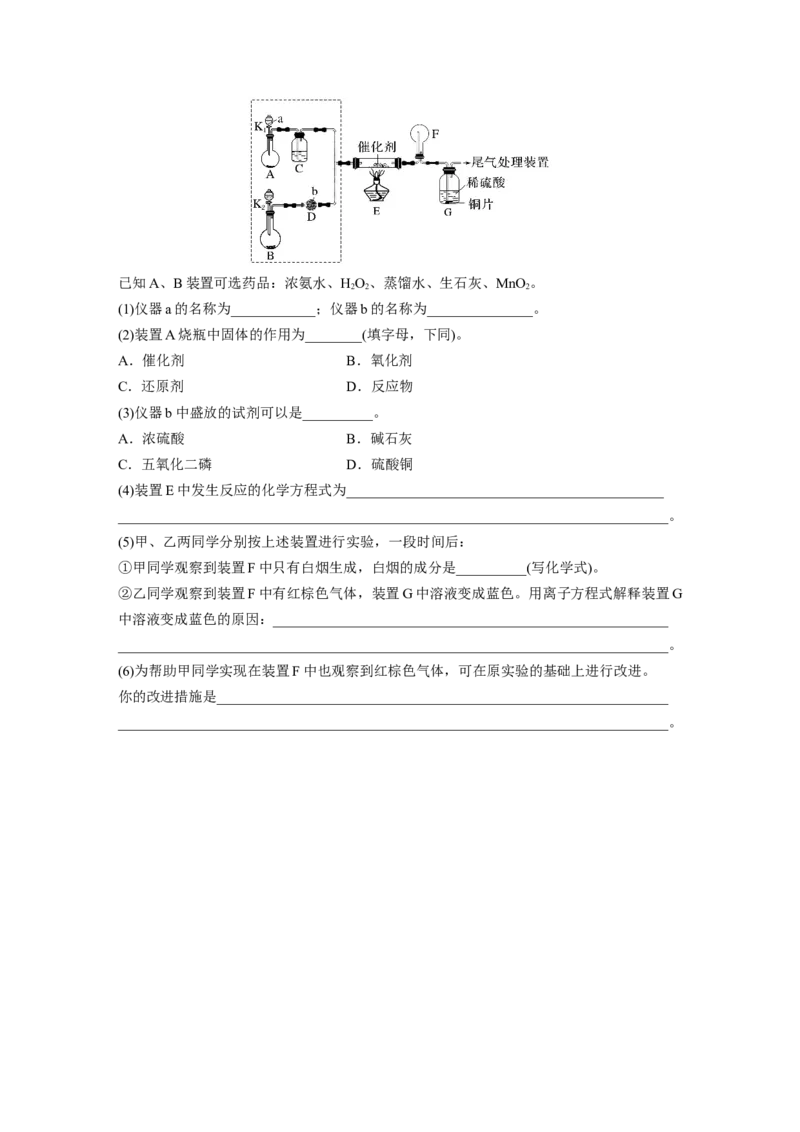
14.某小组同学欲探究NH 的催化氧化反应,按下图装置进行实验(夹持装置已略去)。
3已知A、B装置可选药品:浓氨水、HO、蒸馏水、生石灰、MnO 。
2 2 2
(1)仪器a的名称为____________;仪器b的名称为_______________。
(2)装置A烧瓶中固体的作用为________(填字母,下同)。
A.催化剂 B.氧化剂
C.还原剂 D.反应物
(3)仪器b中盛放的试剂可以是__________。
A.浓硫酸 B.碱石灰
C.五氧化二磷 D.硫酸铜
(4)装置E中发生反应的化学方程式为_____________________________________________
______________________________________________________________________________。
(5)甲、乙两同学分别按上述装置进行实验,一段时间后:
①甲同学观察到装置F中只有白烟生成,白烟的成分是__________(写化学式)。
②乙同学观察到装置F中有红棕色气体,装置G中溶液变成蓝色。用离子方程式解释装置G
中溶液变成蓝色的原因:________________________________________________________
______________________________________________________________________________。
(6)为帮助甲同学实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进。
你的改进措施是________________________________________________________________
______________________________________________________________________________。