文档内容
答案和解析
1.【答案】A
【解析】解:A、化学反应不能改变元素种类,该选项说法不正确;
B、铜、铁硬度较大,比较坚固,该选项说法正确;
C、燃烧的条件之一是需要可燃物,该选项说法正确;
D、金在高温下难与其它物质反应,该选项说法正确。
故选:A。
A、化学反应前后元素种类不变;
B、铜、铁硬度较大,比较坚固;
C、燃烧条件:可燃物,与氧气接触,温度达到着火点;
D、金的化学性质不活泼。
本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、
判断,从而得出正确的结论。
2.【答案】B
【解析】解:A、试管用于少量液体试剂的加热,一般不用作溶解固体、配制溶液,
故A错误;
B、烧杯可以用来溶解固体、配制溶液、加热较多量液体试剂,故B正确;
C、集气瓶用于收集气体,不能用于配制溶液、加热较多量液体及反应容器,故C错
误;
D、量筒只用来量取液体,而一定不能用来溶解固体、配制溶液,故D错误。
故选:B。
根据实验室常见仪器的用途分析即可,
烧杯:用作配制溶液、溶解固体和加热较多量液体试剂。
试管:用于少量液体试剂的加热。
量筒:量取液体体积,不能加热。
集气瓶:适用于收集气体。
此题看起来简单,但同学们的答分并不高,同学们对这些仪器的使用范围很模糊,这
就需要同学们注重课本,留意常见仪器的使用规则,同时做实验时要严格要求自己。
3.【答案】D
【解析】解:A、碳酸氢钠是盐,硫酸是酸,该选项分类不正确;
B、二氧化硫是氧化物,高锰酸钾是盐,该选项分类不正确;
C、氧化铜是黑色固体,氧化铁是红棕色固体,该选项分类不正确;
D、碳和氢气都具有还原性,该选项分类正确。
故选:D。
A、电离生成的阳离子都是氢离子的化合物是酸,由金属离子和酸根离子组成的化合
物是盐;
B、由氧元素和另外一种元素组成的化合物是氧化物;
C、氧化铜是黑色固体,氧化铁是红棕色固体;
D、碳、氢气和一氧化碳具有还原性。
本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、
判断,从而得出正确的结论。
4.【答案】C
第 页,共 页
1 2【解析】解:A、由化学式可知,羟氯喹中含有C、H、Cl、N、O五种元素,选项说
法正确;
B、相对分子质量的单位是1,一般省略不写,故B错误;
C、羟氯喹中碳、氢、氯、氮、氧五种元素的质量比为(12×18):(1×26):35.5:
(14×3):(16×1)=432:52:71:84:32,则羟氯喹中碳元素的质量分数最大,选
项说法正确。
D、C、H、Cl、N、O的原子序数分别为:6、1、17、7、8,故氯元素的原子序数最
大正确;
故选:C。
A.根据化学式的宏观意义来分析;
B.根据相对分子质量的单位为1来分析
C.根据化合物中元素的质量比来分析;
D.根据各个原子的原子序数来分析;
本题难度不大,考查同学们结合新信息、灵活运用有机物的概念、化学式的含义与有
关计算进行分析问题、解决问题的能力。
5.【答案】C
【解析】解:A.氢氧化钠是一种碱,盐酸是一种酸,酸碱作用生成盐和水的反应属于
中和反应,选项说法正确;
B.a点所示溶液的pH<7,溶液显酸性,能使紫色的石蕊试液变红色,选项说法正确;
C.b点所示溶液的pH=7,呈中性,说明HCl与NaOH恰好完全反应,化学方程式以
及物质间的质量关系为:
NaOH+HCl=NaCl+H O
2
40 36.5
由此可知,恰好反应时,HCl与NaOH质量并不相等,选项说法错误;
D.c点所示溶液的pH>7,溶液呈碱性,即溶液中的溶质是氯化钠和氢氧化钠,选项说
法正确。
故选:C。
A.根据中和反应的概念来分析;
B.根据溶液的酸碱性来分析;
C.根据所示溶液的pH以及化学方程式来分析;
D.根据溶液的酸碱性来分析。
在解此类题时,首先分析题中的反应原理,然后将题中信息和课本知识的联系,看清
每步操作的目的或反应实质即可较快解答。
6.【答案】C
【解析】解:A.碳酸铵能与氢氧化钙反应生成有刺激性气味的氨气,而硫酸钾与熟石
灰不反应,现象不同,所以可以将二者鉴别开,不合题意;
B.碳酸铵能与盐酸反应生成二氧化碳气体,而硫酸钾与盐酸不反应,现象不同,所以
可以将二者鉴别开,不合题意;
C.碳酸铵和硫酸钾均能与氯化钡反应生成白色沉淀,所以现象相同,无法鉴别,符合
题意;
D.碳酸铵能与氢氧化钡反应生成碳酸钡白色沉淀,同时产生有刺激性气味的氨气,而
硫酸钾与氢氧化钡反应只能产生白色沉淀,现象不同,所以可以将二者鉴别开,不合
题意。
故选:C。
根据物质的不同性质、物质间反应的现象来分析解答。
本题难度不是很大,但涉及知识点较多,熟悉常见离子的检验方法是解答本题的关键。
第 页,共 页
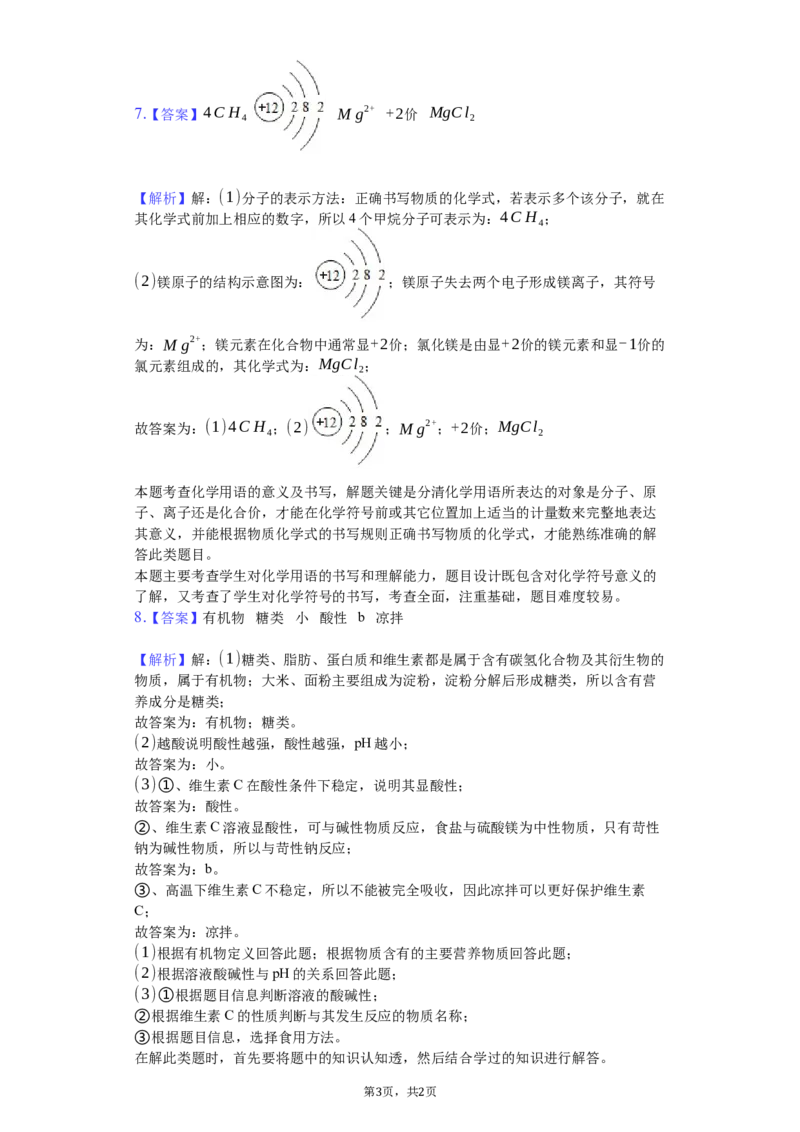
2 107.【答案】4CH M g2+ +2价 MgCl
4 2
【解析】解:(1)分子的表示方法:正确书写物质的化学式,若表示多个该分子,就在
其化学式前加上相应的数字,所以4个甲烷分子可表示为:4CH ;
4
(2)镁原子的结构示意图为: ;镁原子失去两个电子形成镁离子,其符号
为:M g2+;镁元素在化合物中通常显+2价;氯化镁是由显+2价的镁元素和显-1价的
氯元素组成的,其化学式为:MgCl ;
2
故答案为:(1)4CH ;(2) ;M g2+;+2价;MgCl
4 2
本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原
子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达
其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解
答此类题目。
本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的
了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易。
8.【答案】有机物 糖类 小 酸性 b 凉拌
【解析】解:(1)糖类、脂肪、蛋白质和维生素都是属于含有碳氢化合物及其衍生物的
物质,属于有机物;大米、面粉主要组成为淀粉,淀粉分解后形成糖类,所以含有营
养成分是糖类;
故答案为:有机物;糖类。
(2)越酸说明酸性越强,酸性越强,pH越小;
故答案为:小。
(3)①、维生素C在酸性条件下稳定,说明其显酸性;
故答案为:酸性。
②、维生素C溶液显酸性,可与碱性物质反应,食盐与硫酸镁为中性物质,只有苛性
钠为碱性物质,所以与苛性钠反应;
故答案为:b。
③、高温下维生素C不稳定,所以不能被完全吸收,因此凉拌可以更好保护维生素
C;
故答案为:凉拌。
(1)根据有机物定义回答此题;根据物质含有的主要营养物质回答此题;
(2)根据溶液酸碱性与pH的关系回答此题;
(3)①根据题目信息判断溶液的酸碱性;
②根据维生素C的性质判断与其发生反应的物质名称;
③根据题目信息,选择食用方法。
在解此类题时,首先要将题中的知识认知透,然后结合学过的知识进行解答。
第 页,共 页
3 29.【答案】不饱和 40g c
【解析】解:(1)饱和溶液是指一定温度下不能继续溶解某种溶质的溶液,①能继续
溶解这种溶质,所以是不饱和溶液,故答案为:不饱和;
(2)根据题中的实验可知100g水中加入了2次每次加入20g氯化钾即共40g氯化钾后所
得溶液不能再溶解氯化钾,所以该温度下100g水中加入40g氯化钾正好饱和,故该温
度下氯化钾的溶解度是40g,故答案为:40g;
(3)根据图示可知100g水中加入60g氯化钾所得溶液质量为140g,说明只溶解了
40g
40g,所以该温度下的溶解度是40g;实验③溶液的质量分数为 ×100%≈28.6%,
140g
故答案为:c。
(1)根据饱和溶液是指一定温度下不能继续溶解某种溶质的溶液分析;
(2)根据固体的溶解度是指一定温度下100g溶剂水中达到饱和状态所溶解的这种溶质
的质量就是该温度下该物质在水中的溶解度分析;
(3)根据一定温度下,100g水中溶解氯化钾的质量考虑。
本题考查了固体的溶解度、饱和溶液、不饱和溶液的概念和溶质质量分数的计算相关
问题,注重应用侧重能力。
10.【答案】HCl+N H =N H Cl 小
3 4
【解析】解:(1)盐酸与氨气反应生成氯化铵,书写化学方程式注意配平;
故答案为:HCl+N H ⋅H O=N H Cl+H O。
3 2 4 2
(2)盐酸中溶质为HCl,相对分子质量为36.5,氨水中挥发出分子为N H ,相对分子
3
质量为17,在A处先有白烟生成,说明氨分子先运动到A处与氯化氢分子接触反生反
应,所以相对分子质量越大,分子运动速率越小;
故答案为:小。
(1)盐酸与氨气反应生成氯化铵,据此书写化学方程式;
(2)根据实验现象总结实验结论。
在解此类题时,首先要将题中的知识认知透,然后结合学过的知识进行解答。
11.【答案】O 化合 3NO +H O=2HNO +NO NO N H 种类和个数
2 2 2 3 3
【解析】解:(1)氮气和单质X反应生成一氧化氮,故X是氧气,故填:O ;
2
(2)反应②是一氧化氮和氧气反应生成二氧化氮,属于化合反应,故填:化合;
(3)反应③是二氧化氮和水反应生成硝酸和一氧化氮,故填:
3NO +H O=2HNO +NO;
2 2 3
(4)根据图示可以看出,可以循环利用的物质是一氧化氮,故填:NO;
(5)化学反应前后原子的种类和个数不变,该反应前含有10个O原子,反应后含有4
个N原子,10个O原子,12个H原子,故反应前含有4□中含有4个N原子,12个H
原子,故□中含有1个N原子,3个H原子,其化学式为:N H ,故填:N H ;种类
3 3
和个数。
根据题干提供的信息,氮气和单质X反应生成一氧化氮,故X是氧气,一氧化氮和氧
气反应生成二氧化氮,结合物质间的反应进行分析解答即可。
本题考查的是物质的制备的知识,完成此题,可以依据题干提供的信息结合物质的性
质进行。
12.【答案】CaCO +2HCl=CaCl +H O+CO ↑ B 检查装置的气密性 紫色变
3 2 2 2
红色 干燥的石蕊试纸 二氧化碳的密度比空气大 二氧化碳既不能燃烧,也不能支持
燃烧
第 页,共 页
4 10【解析】解:(1)实验室制取CO ,是在常温下,用大理石或石灰石和稀盐酸制取的,
2
碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,因此不需要加热;故答案为:
CaCO +2HCl=CaCl +H O+CO ↑;
3 2 2 2
(2)C装置中实验所需二氧化碳,应选用A、B发生装置中的B装置获得。在仪器组装
后、加入药品前,需要进行的操作是:检查装置的气密性;故答案为:B;检查装置的
气密性;
(3)制得的CO 干燥后利用C装置进行实验,b处的实验现象是:紫色变红色;若要证
2
明b处二氧化碳与水发生了反应,可在a处放置石蕊溶液染成紫色的干燥的小花或干
燥的石蕊试纸;故答案为:紫色变红色;干燥的石蕊试纸;
(4)根据烧杯中的实验现象,能得出的结论是:二氧化碳的密度比空气大;二氧化碳既
不能燃烧,也不能支持燃烧;故答案为:二氧化碳的密度比空气大;二氧化碳既不能
燃烧,也不能支持燃烧;
(1)实验室制取CO ,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐
2
酸反应生成氯化钙和水和二氧化碳,因此不需要加热。二氧化碳能溶于水,密度比空
气的密度大,因此只能用向上排空气法收集。
(2)检查装置的气密性;
(3)二氧化碳的性质;
(4)根据烧杯中的实验现象,能得出的结论是:二氧化碳的密度比空气大;二氧化碳既
不能燃烧,也不能支持燃烧。
本考点主要考查了检查装置的气密性、气体的制取装置和收集装置的选择,同时也考
查了化学方程式的书写、二氧化碳的性质等,综合性比较强。气体的制取装置的选择
与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有
关。本考点是中考的重要考点之一,主要出现在实验题中。
13.【答案】小 低 碱性 2Na+2H O=2NaOH+H ↑
2 2
2NaOH+CuSO =Cu(OH) ↓+Na SO 隔绝氧气和水
4 2 2 4
【解析】解:【进行实验】实验一:根据“金属钠漂浮于水面上”可得:金属钠的密
度比水的小;根据“不规则钠慢慢熔化成一个光亮的小球”可知反应放热,金属钠的
熔点低;故填:小;低;
实验二:取少量反应后的溶液于试管中,滴加几滴无色酚酞溶液,溶液变红,说明反
应后的溶液呈碱性;钠和水反应生成氢氧化钠和氢气,反应的化学方程式为:
2Na+2H O=2NaOH+H ↑;故填:碱性;2Na+2H O=2NaOH+H ↑;
2 2 2 2
实验三:钠和水反应生成氢氧化钠和氢气,氢氧化钠与硫酸铜反应生成硫酸钠和氢氧
化铜,所以试管中出现蓝色絮状沉淀的化学方程式为:
2NaOH+CuSO =Cu(OH) ↓+Na SO ;故填:
4 2 2 4
2NaOH+CuSO =Cu(OH) ↓+Na SO ;
4 2 2 4
【拓展思考】由于金属钠能与空气和水发生反应,且密度比水小。所以保存时,要隔
绝氧气(或空气)和水。故填:隔绝氧气和水。
【进行实验】实验一:根据实验现象分析;
实验二:酚酞在碱性溶液中显红色;
实验三:氢氧化钠与硫酸铜反应生成硫酸钠和氢氧化铜;
【拓展思考】根据金属钠的化学性质进行回答。
本题重点考查了学生分析信息,结合相关知识及操作中的描述和反应现象,分析解决
问题的能力。
14.【答案】催化作用
【解析】解:(1)由催化剂的定义可知,二氧化锰作为催化剂在化学反应中起催化作用,
前后本身的质量和化学性质都没有发生变化;
第 页,共 页
5 2(2)根据质量守恒定律,反应产生氧气的质量=68g+2g-66.8g=3.2g
设产生3.2g氧气需要H O 的质量为x
2 2
MnO
2
- 68 32
2H O 2H O+O ↑
2 2 ❑ 2 2
x 3.2g
68 32
= 解得:x=6.8g
x 3.2g
6.8g
过氧化氢溶液的溶质质量分数= ×100%=10%。
68g
答:过氧化氢溶液的质量分数是10%。
故答案为:(1)催化作用;(2)10%。
(1)根据催化剂的定义分析回答;
(2)过氧化氢在二氧化锰催化下分解生成水和氧气,由于气体放出而使反应后剩余物质
的质量减小,利用质量守恒定律,反应前后物质总质量的差即为放出氧气的质量;根
据反应的化学方程式,由放出氧气的质量计算出过氧化氢的质量,然后求出过氧化氢
溶液的溶质质量分数即可。
解答本题时需要首先使用质量守恒定律,找出题中隐含条件,然后再由化学方程式及
溶液的溶质质量分数进行计算,有较强的综合性,需要有清晰的解题思路。
第 页,共 页
6 10