文档内容
1.下表物质与其所含化学键类型、所属化合物类型完全正确的一组是( )
选项 A B C D
物质 MgCl CO HCl NaOH
2 2
所含化学键类型 离子键、共价键 共价键 离子键 离子键、共价键
所属化合物类型 离子化合物 共价化合物 离子化合物 共价化合物
2.下列有关电子式表示正确的是( )
①次氯酸的电子式:
②甲醛的电子式:
③HCl的电子式:
④由Na和Cl形成离子键的过程:
A.①③ B.①④ C.②③ D.②④
3.在下列变化中,既有离子键被破坏又有共价键被破坏的是( )
A.将NH 通入水中 B.氢氧化钠熔化
3
C.将HBr通入水中 D.硫酸氢钾溶于水
4.关于σ键和π键的形成过程,下列说法不正确的是( )
A.HCl分子中的σ键为两个s轨道“头碰头”重叠形成
B.N 分子中的π键为p-p π键,π键不能绕键轴旋转
2
C.CH 中的碳原子为sp3杂化,4个sp3杂化轨道分别与氢原子s轨道形成σ键
4
D.乙烯(CH==CH)中碳碳之间形成1个σ键和1个π键
2 2
5.下列有关化学键类型的叙述正确的是( )
A.化合物NH 所有原子最外层均满足2个或8个电子的稳定结构,则1 mol NH 中含有5N
5 5 A
个N—H σ键(N 表示阿伏加德罗常数的值)
A
B.乙烯酮的结构简式为CH==C==O,其分子中含有极性共价键和非极性共价键,且 σ键
2
与π键数目之比为1∶1
C.已知乙炔的结构式为H—C≡C—H,则乙炔中存在2个σ键(C—H)和3个π键(C≡C)
D.乙烷分子中只存在σ键,不存在π键
6.关于键长、键能和键角,下列说法错误的是( )
A.键角是描述分子空间结构的重要参数B.键长的大小与成键原子的半径和成键数目有关
C.C===C键能等于C—C键能的2倍
D.因为O—H的键能小于H—F的键能,所以O、F 与H 反应的能力逐渐增强
2 2 2
7.(2023·石家庄模拟)我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧
化,其反应如下:HCHO+O――→CO+HO。下列有关说法正确的是( )
2 2 2
A.CO 只含有非极性共价键
2
B.0.5 mol HCHO含有1 mol σ键
C.HCHO、CO 分子中只含有σ键
2
D.HO中含有极性键
2
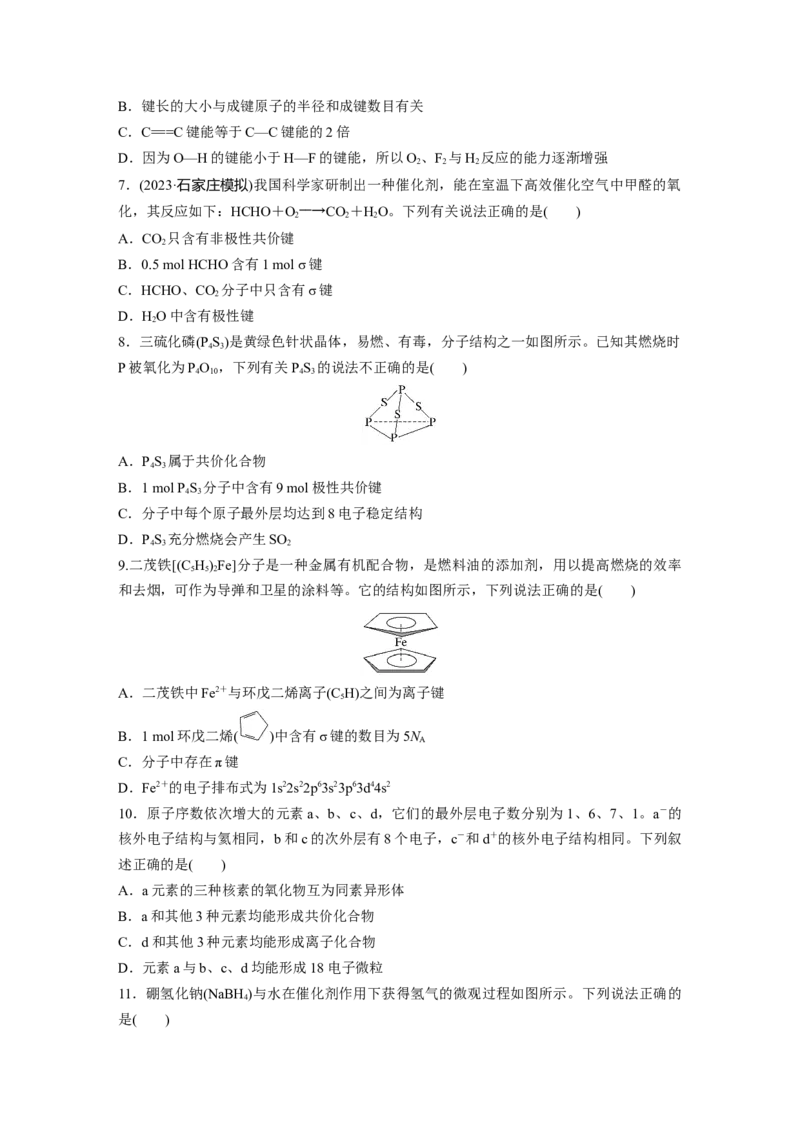
8.三硫化磷(P S)是黄绿色针状晶体,易燃、有毒,分子结构之一如图所示。已知其燃烧时
4 3
P被氧化为PO ,下列有关PS 的说法不正确的是( )
4 10 4 3
A.PS 属于共价化合物
4 3
B.1 mol P S 分子中含有9 mol极性共价键
4 3
C.分子中每个原子最外层均达到8电子稳定结构
D.PS 充分燃烧会产生SO
4 3 2
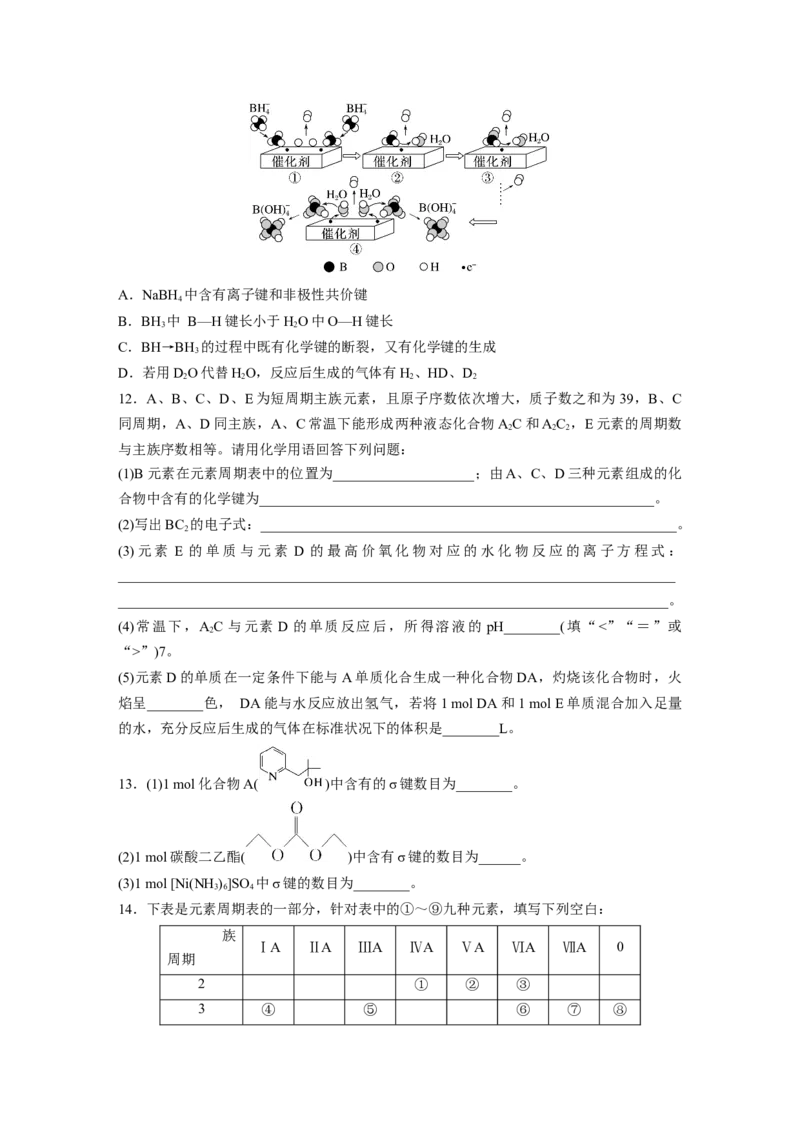
9.二茂铁[(C H)Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率
5 5 2
和去烟,可作为导弹和卫星的涂料等。它的结构如图所示,下列说法正确的是( )
A.二茂铁中Fe2+与环戊二烯离子(C H)之间为离子键
5
B.1 mol环戊二烯( )中含有σ键的数目为5N
A
C.分子中存在π键
D.Fe2+的电子排布式为1s22s22p63s23p63d44s2
10.原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。a-的
核外电子结构与氦相同,b和c的次外层有8个电子,c-和d+的核外电子结构相同。下列叙
述正确的是( )
A.a元素的三种核素的氧化物互为同素异形体
B.a和其他3种元素均能形成共价化合物
C.d和其他3种元素均能形成离子化合物
D.元素a与b、c、d均能形成18电子微粒
11.硼氢化钠(NaBH )与水在催化剂作用下获得氢气的微观过程如图所示。下列说法正确的
4
是( )A.NaBH 中含有离子键和非极性共价键
4
B.BH 中 B—H键长小于HO中O—H键长
3 2
C.BH→BH 的过程中既有化学键的断裂,又有化学键的生成
3
D.若用DO代替HO,反应后生成的气体有H、HD、D
2 2 2 2
12.A、B、C、D、E为短周期主族元素,且原子序数依次增大,质子数之和为 39,B、C
同周期,A、D同主族,A、C常温下能形成两种液态化合物AC和AC ,E元素的周期数
2 2 2
与主族序数相等。请用化学用语回答下列问题:
(1)B元素在元素周期表中的位置为____________________;由A、C、D三种元素组成的化
合物中含有的化学键为________________________________________________________。
(2)写出BC 的电子式:___________________________________________________________。
2
(3)元素 E 的单质与元素 D 的最高价氧化物对应的水化物反应的离子方程式:
_______________________________________________________________________________
______________________________________________________________________________。
(4)常温下,AC 与元素 D 的单质反应后,所得溶液的 pH________(填“<”“=”或
2
“>”)7。
(5)元素D的单质在一定条件下能与A单质化合生成一种化合物DA,灼烧该化合物时,火
焰呈________色, DA能与水反应放出氢气,若将1 mol DA和1 mol E单质混合加入足量
的水,充分反应后生成的气体在标准状况下的体积是________L。
13.(1)1 mol化合物A( )中含有的σ键数目为________。
(2)1 mol碳酸二乙酯( )中含有σ键的数目为______。
(3)1 mol [Ni(NH )]SO 中σ键的数目为________。
3 6 4
14.下表是元素周期表的一部分,针对表中的①~⑨九种元素,填写下列空白:
族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
2 ① ② ③
3 ④ ⑤ ⑥ ⑦ ⑧4 ⑨
(1)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是________,碱性最强的
化合物的电子式是____________________。
(2)用电子式表示元素④与⑥形成的化合物的过程:__________________________________,
该化合物属于________(填“共价”或“离子”)化合物。
(3)①与⑦形成的化合物的电子式:________________________________________________。
(4)判断④⑤⑥原子半径的大小顺序:______________________________________________
(用元素符号或化学式表示,下同 ),比较③和⑥的简单氢化物的稳定性:
_____________________________________________________________________________。