文档内容
1.下列关于化学反应速率的说法正确的是( )
A.因是同一反应,所以用不同物质表示化学反应速率时,所得数值是相同的
B.根据化学反应速率的大小可以知道化学反应进行的快慢
C.化学反应速率为“1 mol·L-1·min-1”表示的意思是时间为1 min时,某物质的浓度为1
mol·L-1
D.金属钠与水的反应中,可用钠或者水的浓度变化来表示化学反应速率
2.下列有关化学反应速率的认识错误的是( )
①可以测定某一反应的瞬时速率
②只能用单位时间内物质的量浓度变化值表示
③任何化学反应都可以通过反应现象判断化学反应的快慢
④溶液中发生的反应,速率的快慢主要由温度、浓度决定
A.只有① B.只有①②
C.只有③④ D.均错误
3.一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如
图所示:
下列描述正确的是( )
A.反应开始到10 s,用Z表示的反应速率为0.158 mol·L-1·s-1
B.反应开始到10 s,X的物质的量浓度减少了0.79 mol·L-1
C.反应开始到10 s时,Y的转化率为79%
D.反应的化学方程式为X(g)+Y(g)Z(g)
4.反应3Fe(s)+4HO(g)=====Fe O(s)+4H(g)在一容积可变的密闭容器中进行,下列条件
2 3 4 2
的改变能使反应速率加快的是( )
①增加铁的量 ②将容器的体积缩小一半
③保持体积不变,充入N 使体系压强增大
2
④保持体积不变,充入水蒸气使体系压强增大
A.①④ B.②③ C.③④ D.②④
5.下列说法正确的是( )A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增多
B.有气体参加的化学反应,若增大压强(即缩小反应容器的容积),可增大活化分子的百分
数,从而使反应速率增大
C.升高温度能使化学反应速率增大的主要原因是减小了反应物分子中活化分子的百分数
D.催化剂能增大单位体积内活化分子的百分数,从而增大反应速率
6.如图表示某化学反应在使用催化剂(b曲线)和未使用催化剂(a曲线)时,反应过程和能量
的对应关系。下列说法一定正确的是( )
A.a与b相比,b的活化能更高
B.该反应反应物断键吸收的总能量小于生成物成键释放的总能量
C.a与b相比,a中活化分子的百分数更高
D.a与b相比,a的反应速率更快
7.乙醛在少量I 存在下发生的分解反应为CHCHO(g)―→CH(g)+CO(g)。某温度下,测得
2 3 4
CHCHO的浓度变化情况如下表:
3
t/s 42 105 242 384 665 1 070
c(CHCHO)/ (mol·L-1) 6.68 5.85 4.64 3.83 2.81 2.01
3
下列说法不正确的是( )
A.42~242 s,消耗CHCHO的平均反应速率为1.02×10-2 mol·L-1·s-1
3
B.第384 s时的瞬时速率大于第665 s时的瞬时速率是受c(CHCHO)的影响
3
C.反应至105 s时,测得混合气体的体积为168.224 L(标准状况)
D.I 为催化剂降低了反应的活化能,使活化分子百分数增加,有效碰撞次数增多
2
8.(2023·安徽省卓越县中联盟高三第一次联考)一定温度下,在2 L恒容密闭容器中投入1
mol CO (g)与4 mol H (g)制备CHOH(g),不考虑副反应,其物质的量随时间变化的关系如
2 2 3
图所示:
下列说法正确的是( )
A.该反应的化学方程式为CO(g)+3H(g)===CHOH(g) +HO(g)
2 2 3 2B.0~30 min内,用H 表示的平均反应速率为0.05 mol·L-1·min-1
2
C.逆反应速率:a点大于b点
D.CO 的平衡转化率是50%
2
9.已知:2KMnO +5HC O +3HSO ===2MnSO +KSO +10CO↑+8HO。某化学小组
4 2 2 4 2 4 4 2 4 2 2
欲探究HC O 溶液和酸性KMnO 溶液反应过程中浓度、温度对化学反应速率的影响,进行
2 2 4 4
了如下实验(忽略溶液体积变化):
0.01 mol·L-1酸性 0.1 mol·L-1 HC O 溶 水的体 反应温 反应时
2 2 4
实验
KMnO 溶液体积/mL 液体积/mL 积/mL 度/℃ 间/min
4
Ⅰ 2 2 0 20 2.1
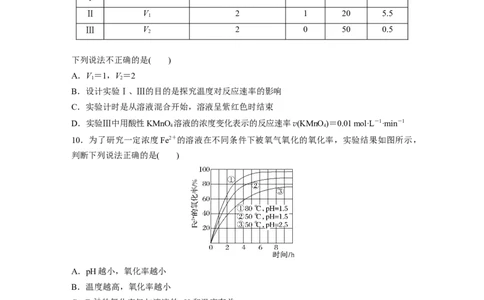
Ⅱ V 2 1 20 5.5
1
Ⅲ V 2 0 50 0.5
2
下列说法不正确的是( )
A.V=1,V=2
1 2
B.设计实验Ⅰ、Ⅲ的目的是探究温度对反应速率的影响
C.实验计时是从溶液混合开始,溶液呈紫红色时结束
D.实验Ⅲ中用酸性KMnO 溶液的浓度变化表示的反应速率v(KMnO)=0.01 mol·L-1·min-1
4 4
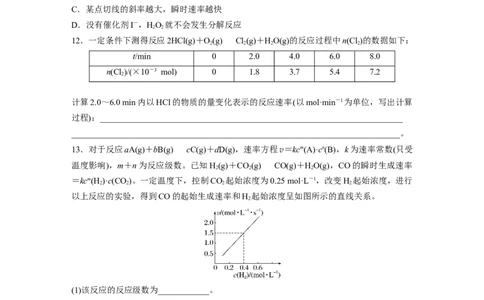
10.为了研究一定浓度Fe2+的溶液在不同条件下被氧气氧化的氧化率,实验结果如图所示,
判断下列说法正确的是( )
A.pH越小,氧化率越小
B.温度越高,氧化率越小
C.Fe2+的氧化率仅与溶液的pH和温度有关
D.实验说明降低pH、升高温度有利于提高Fe2+的氧化率
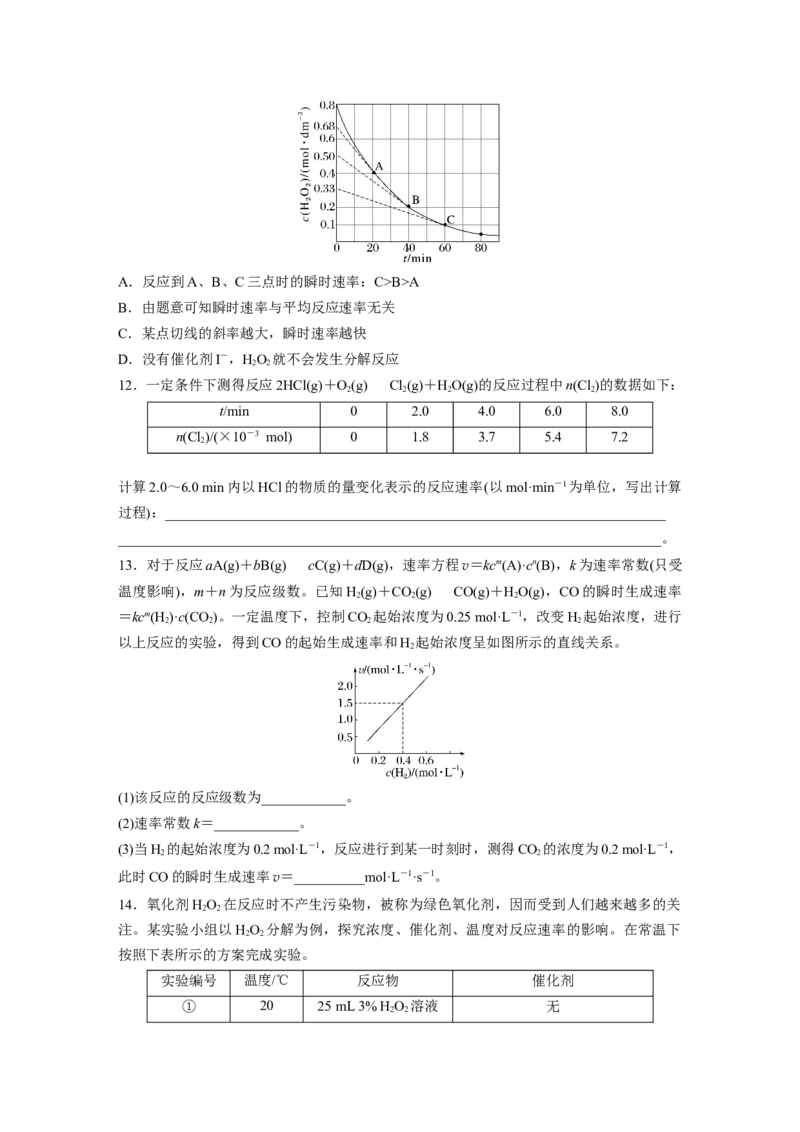
11.25 ℃,HO 分解反应的方程式为HO(aq)=====HO(l)+O(g),HO 分解反应的浓度与
2 2 2 2 2 2 2 2
时间的关系曲线如图所示,=,当观察的时间间隔无限小,平均速率的极值即为化学反应在
t时的瞬时速率,即lim[]=,A点切线的斜率为=0.014 mol·dm-3·min-1,表示在第20 min,
当HO 浓度为0.4 mol·dm-3时,瞬时速率为0.014 mol·dm-3·min-1(斜率、速率均取绝对值),
2 2
则下列说法正确的是( )A.反应到A、B、C三点时的瞬时速率:C>B>A
B.由题意可知瞬时速率与平均反应速率无关
C.某点切线的斜率越大,瞬时速率越快
D.没有催化剂I-,HO 就不会发生分解反应
2 2
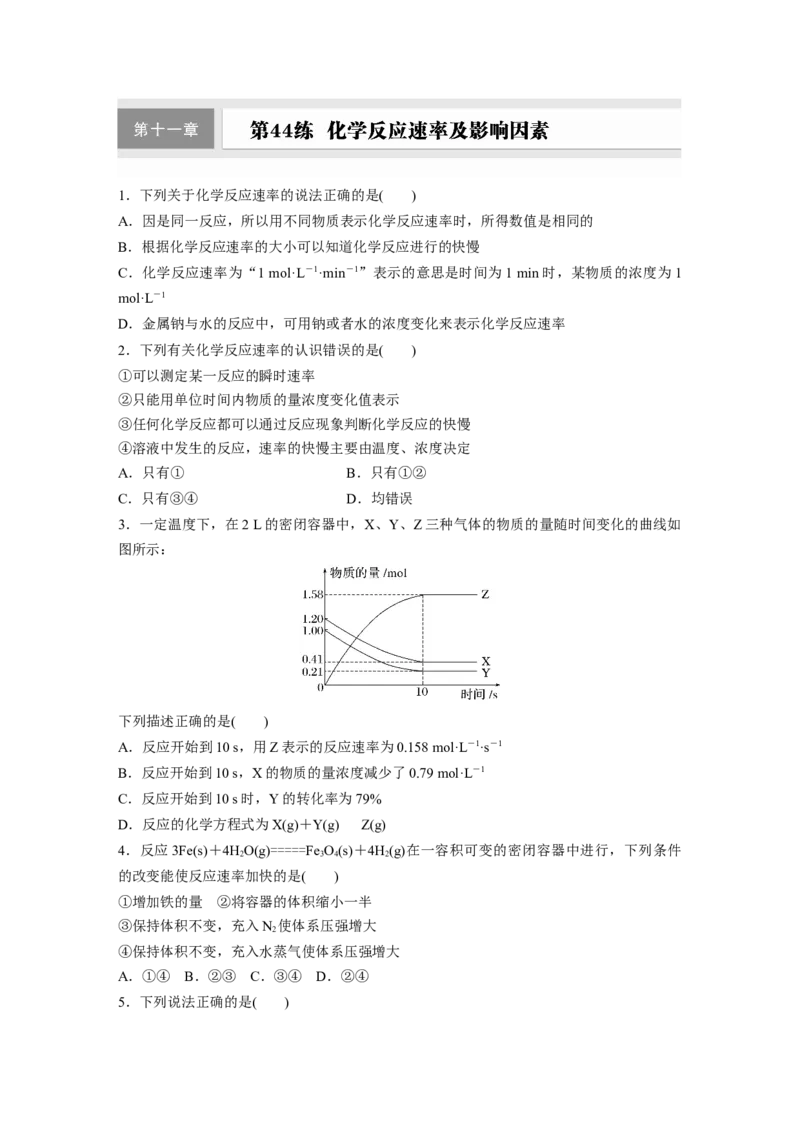
12.一定条件下测得反应2HCl(g)+O(g)Cl(g)+HO(g)的反应过程中n(Cl )的数据如下:
2 2 2 2
t/min 0 2.0 4.0 6.0 8.0
n(Cl )/(×10-3 mol) 0 1.8 3.7 5.4 7.2
2
计算2.0~6.0 min内以HCl的物质的量变化表示的反应速率(以mol·min-1为单位,写出计算
过程):_______________________________________________________________________
_____________________________________________________________________________。
13.对于反应aA(g)+bB(g)cC(g)+dD(g),速率方程v=kcm(A)·cn(B),k为速率常数(只受
温度影响),m+n为反应级数。已知H(g)+CO(g)CO(g)+HO(g),CO的瞬时生成速率
2 2 2
=kcm(H )·c(CO)。一定温度下,控制CO 起始浓度为0.25 mol·L-1,改变H 起始浓度,进行
2 2 2 2
以上反应的实验,得到CO的起始生成速率和H 起始浓度呈如图所示的直线关系。
2
(1)该反应的反应级数为____________。
(2)速率常数k=____________。
(3)当H 的起始浓度为0.2 mol·L-1,反应进行到某一时刻时,测得CO 的浓度为0.2 mol·L-1,
2 2
此时CO的瞬时生成速率v=__________mol·L-1·s-1。
14.氧化剂HO 在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关
2 2
注。某实验小组以HO 分解为例,探究浓度、催化剂、温度对反应速率的影响。在常温下
2 2
按照下表所示的方案完成实验。
实验编号 温度/℃ 反应物 催化剂
① 20 25 mL 3% HO 溶液 无
2 2② 20 25 mL 5% HO 溶液 无
2 2
③ 20 25 mL 5% HO 溶液 0.1 g MnO
2 2 2
④ 20 25 mL 5% HO 溶液 1~2滴1 mol·L-1 FeCl 溶液
2 2 3
⑤ 30 25 mL 5% HO 溶液 0.1 g MnO
2 2 2
(1)实验①和②的目的是________________________________。同学甲在进行实验①和②时
并没有观察到明显现象。资料显示,通常条件下过氧化氢稳定,不易分解。为了达到实验目
的,可采取的改进方法是______________________________(写出一种即可)。
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如图甲所示。分析该图能得出的结
论是____________________________________________________________________________,
____________________________________________________________________________。
(3)同学乙设计了如图乙所示的实验装置对过氧化氢的分解速率进行定量分析,以生成20 mL
气体为准,其他影响实验的因素均已忽略。实验中需要测量的数据是__________________
____________________________________________________________________________。