文档内容
1.已知反应:2NO(g)+Br (g)2NOBr(g) ΔH=-a kJ·mol-1(a>0),其反应机理如下:
2
①NO(g)+Br (g)NOBr (g) 快
2 2
②NO(g)+NOBr (g)2NOBr(g) 慢
2
下列有关该反应的说法正确的是( )
A.该反应的反应速率主要取决于反应①的快慢
B.NOBr 是该反应的催化剂
2
C.增大Br (g)浓度能增大活化分子百分数,加快反应速率
2
D.正反应的活化能比逆反应的活化能小a kJ·mol-1
2.科学家结合实验与计算机模拟结果,研究出了均相催化的思维模型。
总反应:A+B―→AB(K为催化剂),
①A+K―→AK E ,
a1
②AK+B―→AB+K E 。
a2
下列说法错误的是( )
A.第①步为决速步骤
B.升高温度,该反应的速率加快
C.该反应的ΔH=-E kJ·mol-1
a
D.催化剂降低了活化能,加快了反应速率
3.异丁烯[CH===C(CH)]是一种重要的化工原料,常用于制备丁基橡胶、甲基丙烯腈等。
2 3 2
资料表明,异丁烷在固体杂多酸盐(用S表示)作用下制备异丁烯和H 的反应机理如下:
2
过程ⅰ.CH —CH(CH )—CH+S―→CH—CH(CH )—CH…S;
3 3 3 3 3 3
过程ⅱ.CH —CH(CH )—CH…S+S―→CH==C(CH)…S+H…S;
3 3 3 2 3 2 2
过程ⅲ.CH ==C(CH)…S―→CH===C(CH)+S;
2 3 2 2 3 2
过程ⅳ.H …S―→H(g)+S。
2 2
下列说法错误的是( )
A.总反应的化学方程式为CH—CH(CH )—CH――→CH==C(CH)+H
3 3 3 2 3 2 2
B.固体杂多酸盐是反应的催化剂,降低了总反应的活化能C.CH==C(CH)…S和H…S均为催化剂
2 3 2 2
D.过程ⅲ表示的是异丁烯在固体杂多酸盐表面的脱附过程
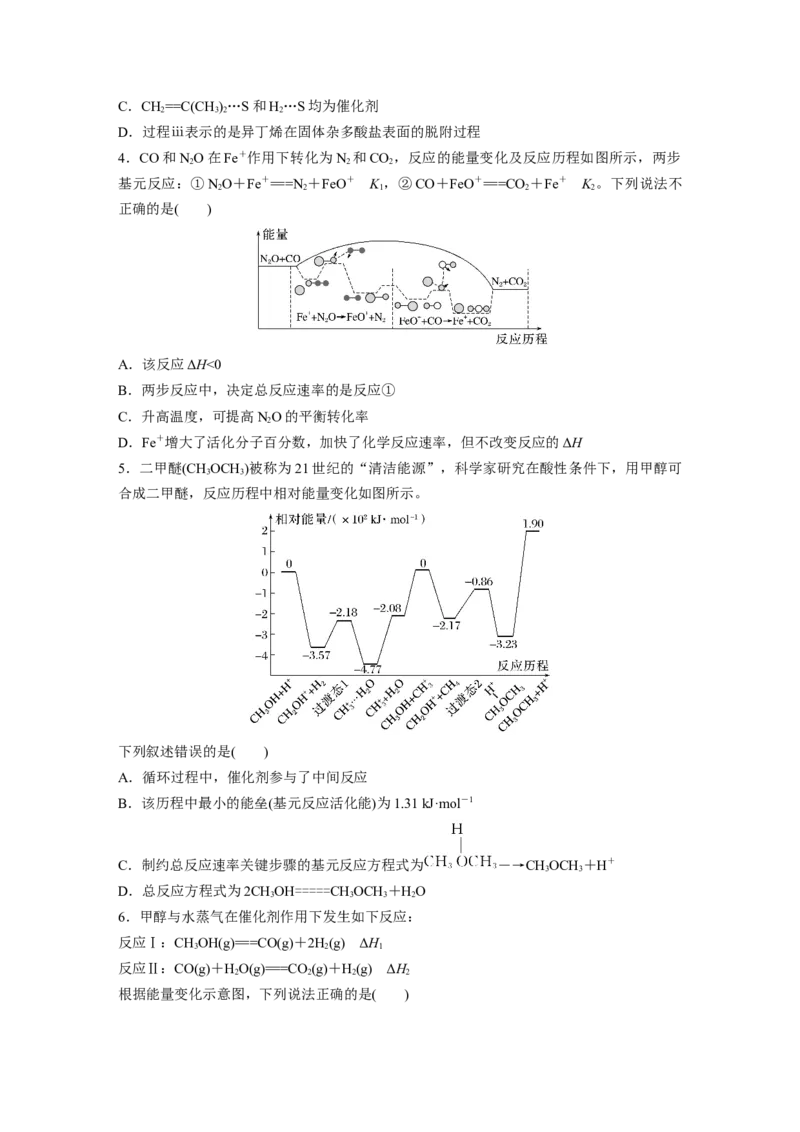
4.CO和NO在Fe+作用下转化为N 和CO ,反应的能量变化及反应历程如图所示,两步
2 2 2
基元反应:①NO+Fe+===N +FeO+ K ,②CO+FeO+===CO +Fe+ K 。下列说法不
2 2 1 2 2
正确的是( )
A.该反应ΔH<0
B.两步反应中,决定总反应速率的是反应①
C.升高温度,可提高NO的平衡转化率
2
D.Fe+增大了活化分子百分数,加快了化学反应速率,但不改变反应的ΔH
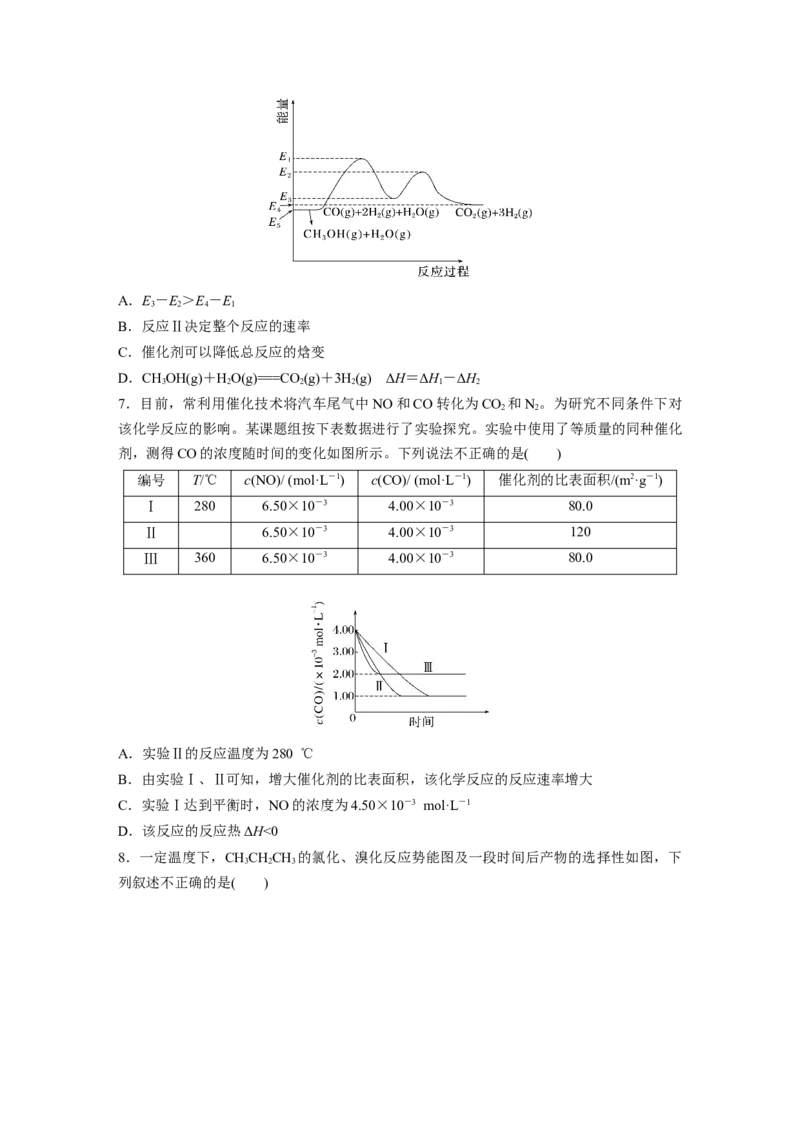
5.二甲醚(CHOCH )被称为21世纪的“清洁能源”,科学家研究在酸性条件下,用甲醇可
3 3
合成二甲醚,反应历程中相对能量变化如图所示。
下列叙述错误的是( )
A.循环过程中,催化剂参与了中间反应
B.该历程中最小的能垒(基元反应活化能)为1.31 kJ·mol-1
C.制约总反应速率关键步骤的基元反应方程式为 ―→CHOCH +H+
3 3
D.总反应方程式为2CHOH=====CHOCH +HO
3 3 3 2
6.甲醇与水蒸气在催化剂作用下发生如下反应:
反应Ⅰ:CHOH(g)===CO(g)+2H(g) ΔH
3 2 1
反应Ⅱ:CO(g)+HO(g)===CO(g)+H(g) ΔH
2 2 2 2
根据能量变化示意图,下列说法正确的是( )A.E-E>E-E
3 2 4 1
B.反应Ⅱ决定整个反应的速率
C.催化剂可以降低总反应的焓变
D.CHOH(g)+HO(g)===CO(g)+3H(g) ΔH=ΔH-ΔH
3 2 2 2 1 2
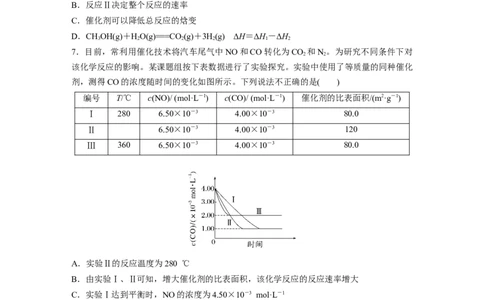
7.目前,常利用催化技术将汽车尾气中NO和CO转化为CO 和N 。为研究不同条件下对
2 2
该化学反应的影响。某课题组按下表数据进行了实验探究。实验中使用了等质量的同种催化
剂,测得CO的浓度随时间的变化如图所示。下列说法不正确的是( )
编号 T/℃ c(NO)/ (mol·L-1) c(CO)/ (mol·L-1) 催化剂的比表面积/(m2·g-1)
Ⅰ 280 6.50×10-3 4.00×10-3 80.0
Ⅱ 6.50×10-3 4.00×10-3 120
Ⅲ 360 6.50×10-3 4.00×10-3 80.0
A.实验Ⅱ的反应温度为280 ℃
B.由实验Ⅰ、Ⅱ可知,增大催化剂的比表面积,该化学反应的反应速率增大
C.实验Ⅰ达到平衡时,NO的浓度为4.50×10-3 mol·L-1
D.该反应的反应热ΔH<0
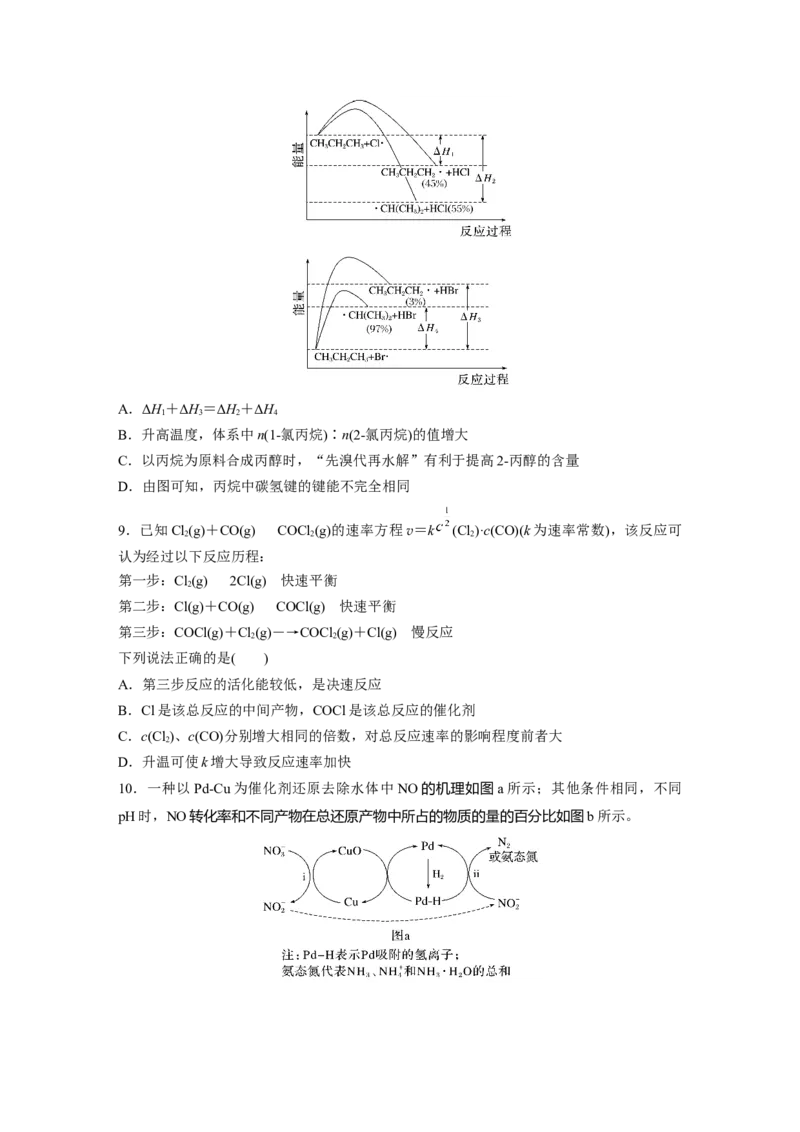
8.一定温度下,CHCHCH 的氯化、溴化反应势能图及一段时间后产物的选择性如图,下
3 2 3
列叙述不正确的是( )A.ΔH+ΔH=ΔH+ΔH
1 3 2 4
B.升高温度,体系中n(1-氯丙烷)∶n(2-氯丙烷)的值增大
C.以丙烷为原料合成丙醇时,“先溴代再水解”有利于提高2-丙醇的含量
D.由图可知,丙烷中碳氢键的键能不完全相同
9.已知Cl(g)+CO(g)COCl (g)的速率方程v=k (Cl )·c(CO)(k为速率常数),该反应可
2 2 2
认为经过以下反应历程:
第一步:Cl(g)2Cl(g) 快速平衡
2
第二步:Cl(g)+CO(g)COCl(g) 快速平衡
第三步:COCl(g)+Cl(g)―→COCl (g)+Cl(g) 慢反应
2 2
下列说法正确的是( )
A.第三步反应的活化能较低,是决速反应
B.Cl是该总反应的中间产物,COCl是该总反应的催化剂
C.c(Cl )、c(CO)分别增大相同的倍数,对总反应速率的影响程度前者大
2
D.升温可使k增大导致反应速率加快
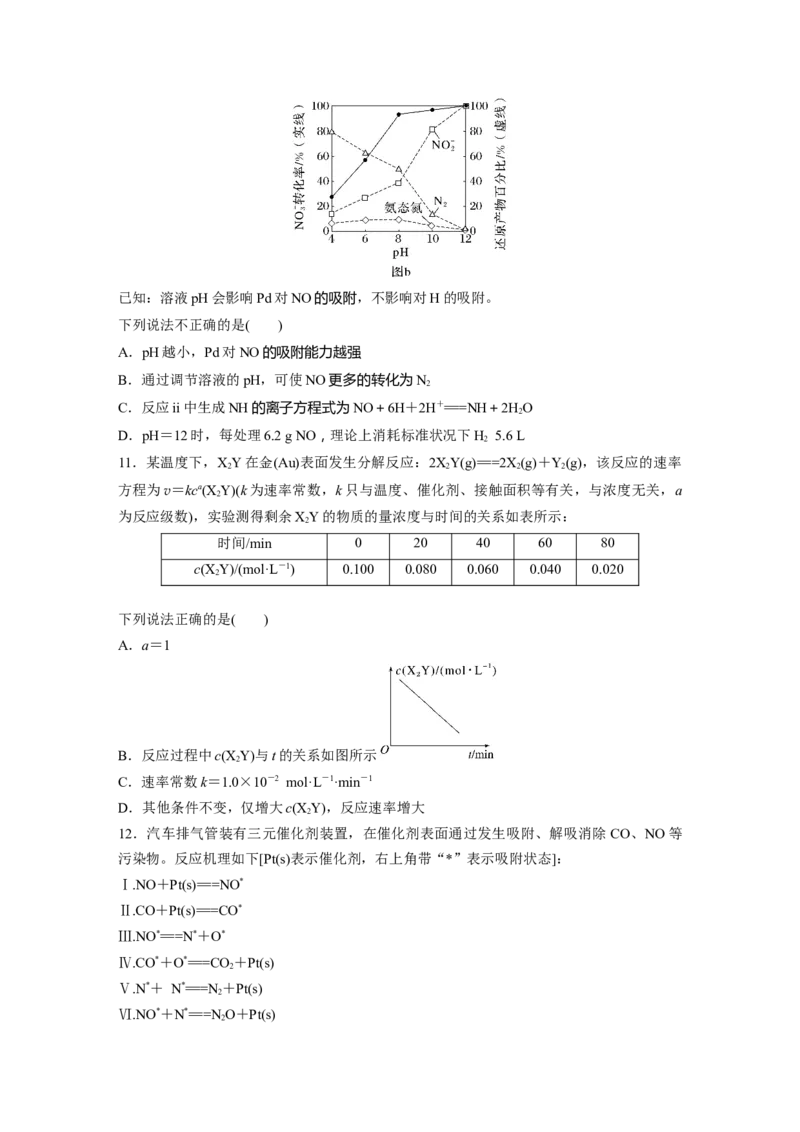
10.一种以Pd-Cu为催化剂还原去除水体中NO的机理如图a所示;其他条件相同,不同
pH时,NO转化率和不同产物在总还原产物中所占的物质的量的百分比如图b所示。已知:溶液pH会影响Pd对NO的吸附,不影响对H的吸附。
下列说法不正确的是( )
A.pH越小,Pd对NO的吸附能力越强
B.通过调节溶液的pH,可使NO更多的转化为N
2
C.反应ii中生成NH的离子方程式为NO+6H+2H+===NH+2HO
2
D.pH=12时,每处理6.2 g NO,理论上消耗标准状况下H 5.6 L
2
11.某温度下,XY在金(Au)表面发生分解反应:2XY(g)===2X(g)+Y(g),该反应的速率
2 2 2 2
方程为v=kca(X Y)(k为速率常数,k只与温度、催化剂、接触面积等有关,与浓度无关,a
2
为反应级数),实验测得剩余XY的物质的量浓度与时间的关系如表所示:
2
时间/min 0 20 40 60 80
c(X Y)/(mol·L-1) 0.100 0.080 0.060 0.040 0.020
2
下列说法正确的是( )
A.a=1
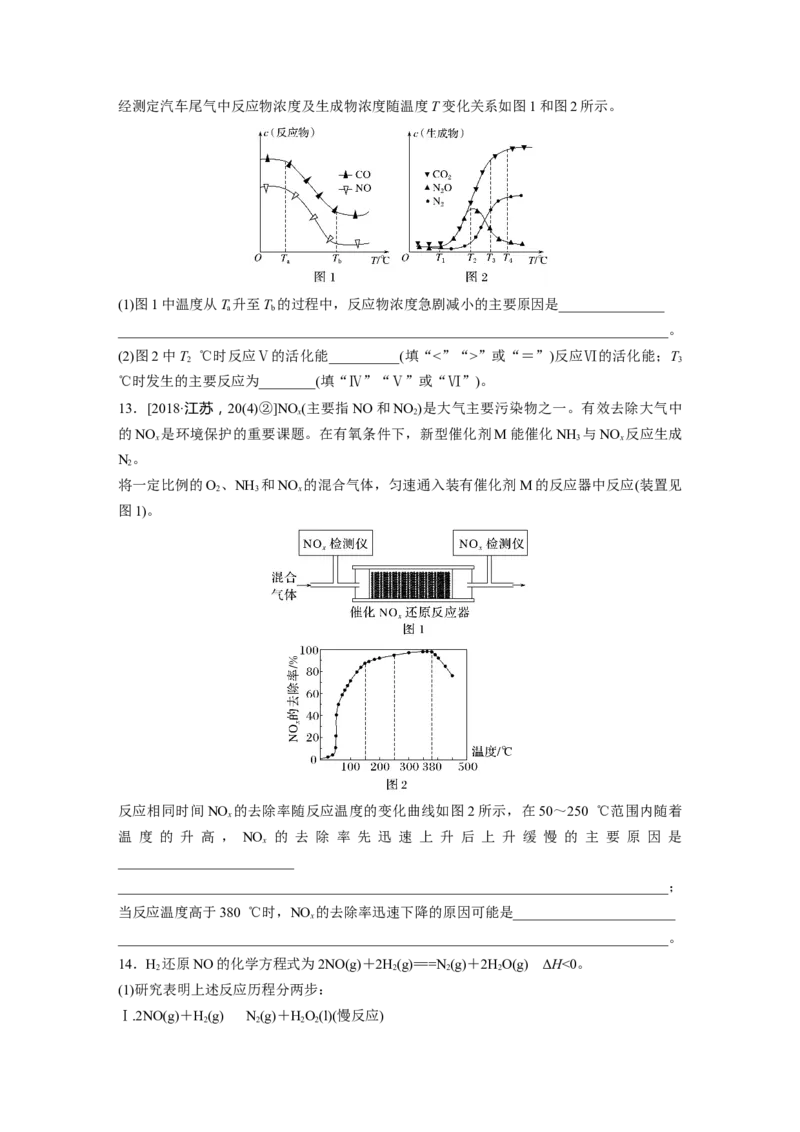
B.反应过程中c(X Y)与t的关系如图所示
2
C.速率常数k=1.0×10-2 mol·L-1·min-1
D.其他条件不变,仅增大c(X Y),反应速率增大
2
12.汽车排气管装有三元催化剂装置,在催化剂表面通过发生吸附、解吸消除 CO、NO等
污染物。反应机理如下[Pt(s)表示催化剂,右上角带“*”表示吸附状态]:
Ⅰ.NO+Pt(s)===NO*
Ⅱ.CO+Pt(s)===CO*
Ⅲ.NO*===N*+O*
Ⅳ.CO*+O*===CO+Pt(s)
2
Ⅴ.N*+ N*===N+Pt(s)
2
Ⅵ.NO*+N*===NO+Pt(s)
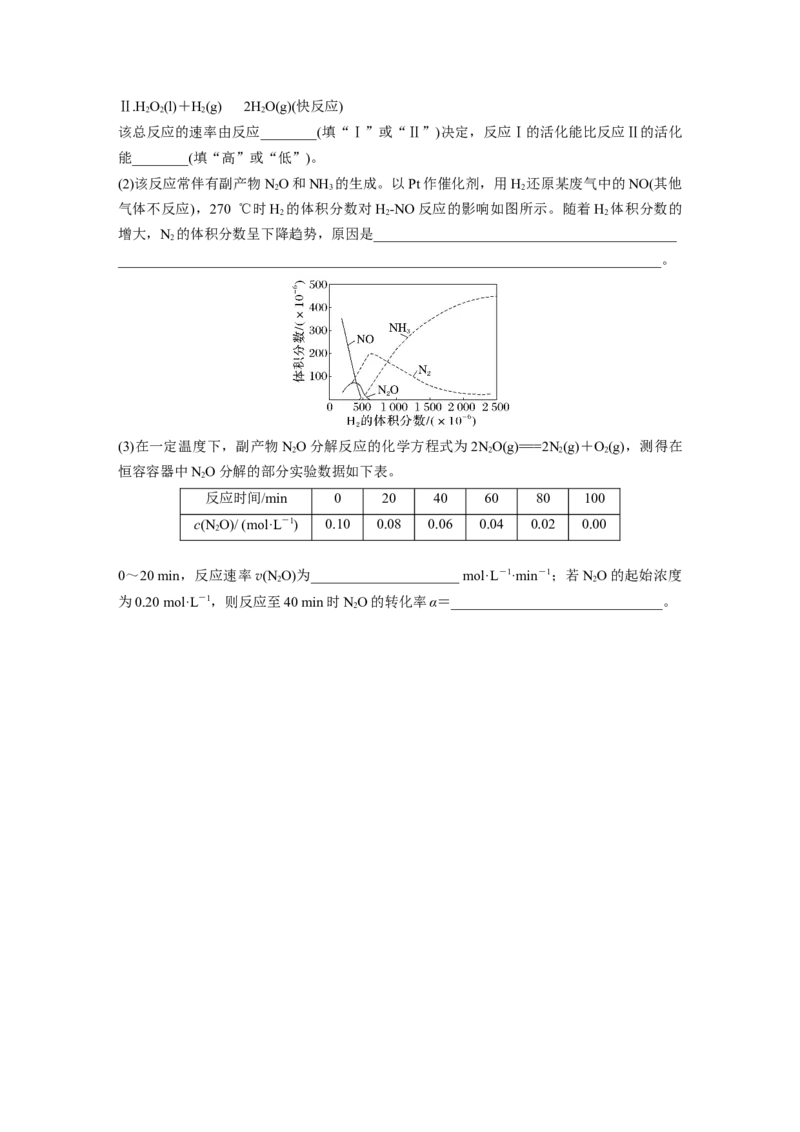
2经测定汽车尾气中反应物浓度及生成物浓度随温度T变化关系如图1和图2所示。
(1)图1中温度从T升至T 的过程中,反应物浓度急剧减小的主要原因是_______________
a b
______________________________________________________________________________。
(2)图2中T ℃时反应Ⅴ的活化能__________(填“<”“>”或“=”)反应Ⅵ的活化能;T
2 3
℃时发生的主要反应为________(填“Ⅳ”“Ⅴ”或“Ⅵ”)。
13.[2018·江苏,20(4)②]NO(主要指NO和NO )是大气主要污染物之一。有效去除大气中
x 2
的NO 是环境保护的重要课题。在有氧条件下,新型催化剂M能催化NH 与NO 反应生成
x 3 x
N。
2
将一定比例的O 、NH 和NO 的混合气体,匀速通入装有催化剂M的反应器中反应(装置见
2 3 x
图1)。
反应相同时间NO 的去除率随反应温度的变化曲线如图2所示,在50~250 ℃范围内随着
x
温 度 的 升 高 , NO 的 去 除 率 先 迅 速 上 升 后 上 升 缓 慢 的 主 要 原 因 是
x
_________________________
______________________________________________________________________________;
当反应温度高于380 ℃时,NO 的去除率迅速下降的原因可能是_______________________
x
______________________________________________________________________________。
14.H 还原NO的化学方程式为2NO(g)+2H(g)===N(g)+2HO(g) ΔH<0。
2 2 2 2
(1)研究表明上述反应历程分两步:
Ⅰ.2NO(g)+H(g)N(g)+HO(l)(慢反应)
2 2 2 2Ⅱ.H O(l)+H(g)2HO(g)(快反应)
2 2 2 2
该总反应的速率由反应________(填“Ⅰ”或“Ⅱ”)决定,反应Ⅰ的活化能比反应Ⅱ的活化
能________(填“高”或“低”)。
(2)该反应常伴有副产物NO和NH 的生成。以Pt作催化剂,用H 还原某废气中的NO(其他
2 3 2
气体不反应),270 ℃时H 的体积分数对H-NO反应的影响如图所示。随着H 体积分数的
2 2 2
增大,N 的体积分数呈下降趋势,原因是___________________________________________
2
_____________________________________________________________________________。
(3)在一定温度下,副产物NO分解反应的化学方程式为2NO(g)===2N(g)+O(g),测得在
2 2 2 2
恒容容器中NO分解的部分实验数据如下表。
2
反应时间/min 0 20 40 60 80 100
c(N O)/ (mol·L-1) 0.10 0.08 0.06 0.04 0.02 0.00
2
0~20 min,反应速率v(N O)为_____________________ mol·L-1·min-1;若NO的起始浓度
2 2
为0.20 mol·L-1,则反应至40 min时NO的转化率α=______________________________。
2