文档内容
考点 10 铁及其重要化合物
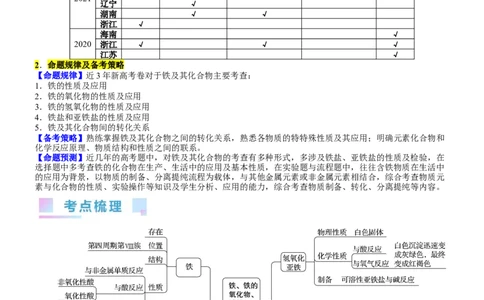
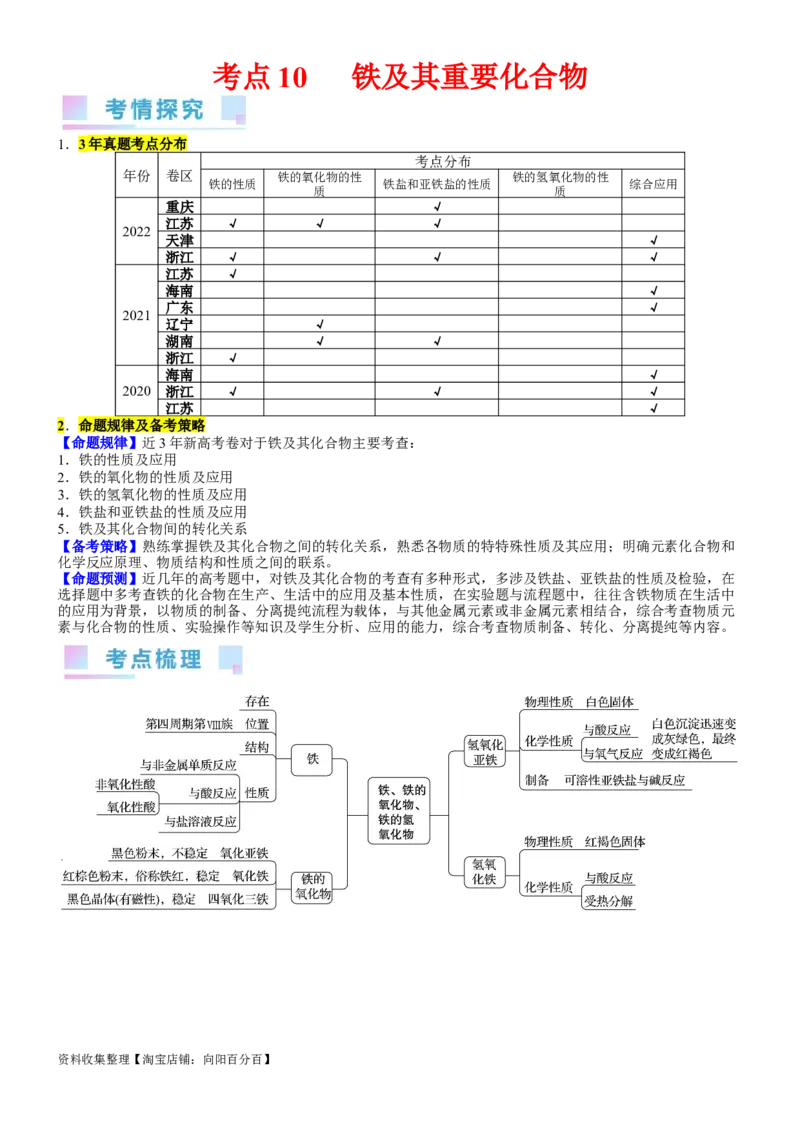
1.3年真题考点分布
考点分布
年份 卷区 铁的氧化物的性 铁的氢氧化物的性
铁的性质 铁盐和亚铁盐的性质 综合应用
质 质
重庆 √
江苏 √ √ √
2022
天津 √
浙江 √ √ √
江苏 √
海南 √
广东 √
2021
辽宁 √
湖南 √ √
浙江 √
海南 √
2020 浙江 √ √ √
江苏 √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于铁及其化合物主要考查:
1.铁的性质及应用
2.铁的氧化物的性质及应用
3.铁的氢氧化物的性质及应用
4.铁盐和亚铁盐的性质及应用
5.铁及其化合物间的转化关系
【备考策略】熟练掌握铁及其化合物之间的转化关系,熟悉各物质的特特殊性质及其应用;明确元素化合物和
化学反应原理、物质结构和性质之间的联系。
【命题预测】近几年的高考题中,对铁及其化合物的考查有多种形式,多涉及铁盐、亚铁盐的性质及检验,在
选择题中多考查铁的化合物在生产、生活中的应用及基本性质,在实验题与流程题中,往往含铁物质在生活中
的应用为背景,以物质的制备、分离提纯流程为载体,与其他金属元素或非金属元素相结合,综合考查物质元
素与化合物的性质、实验操作等知识及学生分析、应用的能力,综合考查物质制备、转化、分离提纯等内容。
资料收集整理【淘宝店铺:向阳百分百】考法 1 单质铁
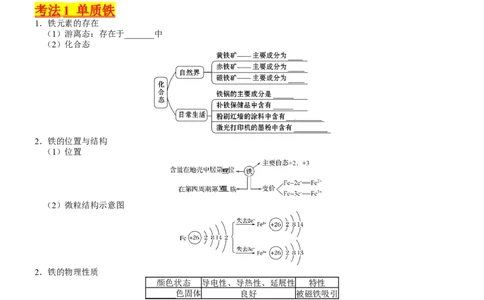
1.铁元素的存在
(1)游离态:存在于_______中
(2)化合态
2.铁的位置与结构
(1)位置
(2)微粒结构示意图
2.铁的物理性质
颜色状态 导电性、导热性、延展性 特性
_______色固体 良好 被磁铁吸引
3.铁的化学性质
(1)Fe与Cl 反应:_____________________
2
(2)Fe与S反应:____________________________
(3)Fe与水蒸气反应:___________________________________
(4)Fe与氧化性酸(如HNO)反应的离子方程式
3
①Fe与过量稀HNO 的反应:_____________________
3
资料收集整理【淘宝店铺:向阳百分百】②Fe与少量稀HNO 的反应:___________________________________
3
(5)Fe与FeCl 溶液的反应:____________________________
3
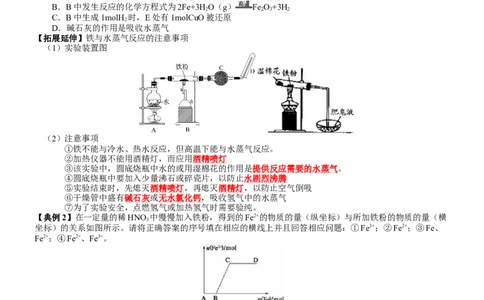
【典例1】某化学兴趣小组利用如图装置进行“铁与水蒸气反应”的实验,并检验产物的性质,下列说法正确
的是( )。
A.实验时,应先点燃B处的酒精喷灯,再点燃A处的酒精灯
B.B中发生反应的化学方程式为2Fe+3H O(g) Fe O+3H
2 2 3 2
C.B中生成1molH 时,E处有1molCuO被还原
2
D.碱石灰的作用是吸收水蒸气
【拓展延伸】铁与水蒸气反应的注意事项
(1)实验装置图
(2)注意事项
①铁不能与冷水、热水反应,但高温下能与水蒸气反应。
②加热仪器不能用酒精灯,而应用酒精喷灯
③该实验中,圆底烧瓶中水的或用湿棉花的作用是 提供反应需要的 水蒸气 。
④圆底烧瓶中要加入少量沸石或碎瓷片,以防止水剧烈沸腾
⑤实验结束时,先熄灭酒精喷灯,再熄灭酒精灯,以防止空气倒吸
⑥干燥管中盛有碱石灰或无水氯化钙,吸收氢气中的水蒸气
⑦为了实验安全,点燃氢气或加热氢气时需要验纯。
【典例2】在一定量的稀HNO 中慢慢加入铁粉,得到的Fe2+的物质的量(纵坐标)与所加铁粉的物质的量(横
3
坐标)的关系如图所示。请将正确答案的序号填在相应的横线上并且回答相应问题:①Fe3+;②Fe2+;③Fe、
Fe2+;④Fe2+、Fe3+。
(1)AB段铁元素以__________形式存在。
(2)BC段铁元素以__________形式存在。
(3)CD段铁元素以__________形式存在,将该段溶液中的离子按照浓度由大到小的顺序排列_______________。
(4)若将14g铁粉溶于1L稀硝酸中恰好完全反应,放出NO气体后称量所得溶液,发现比原溶液质量增加
8g,则原溶液中硝酸的物质的量浓度是___________。
【拓展延伸】铁与稀硝酸反应规律
1.反应方程式
(1)HNO 过量:Fe+4HNO =Fe(NO )+NO↑+2H O
3 3 3 3 2
(2)Fe过量:3Fe+8HNO =3Fe(NO )+2NO↑+4H O
3 3 2 2
2.产物和相对量的关系
资料收集整理【淘宝店铺:向阳百分百】(1) ≤ ,产物仅有Fe(NO ),HNO 可能有剩余;
3 3 3
(2) ≥ ,产物仅有Fe(NO ),Fe可能有剩余;
3 2
(3) < < ,产物为Fe(NO ) 和Fe(NO ),Fe和HNO 都反应完全。
3 3 3 2 3
3.硝酸的物质的量与气体的物质的量关系: =
1.西周晚期,我国已掌握了冶铁技术。下列有关铁的化学反应的叙述正确的是( )。
A.室温下,过量Fe与浓硫酸反应生成FeSO
4
B.加热时,过量Fe与氯气反应生成FeCl
2
C.高温下,铁与水蒸气反应有Fe O 生成
3 4
D.高温下,铁粉与氧化铝粉末反应生成单质铝
2.(2023·龙岩模拟)下列叙述不正确的是:①Fe与S混合加热生成Fe S;②Fe与稀硝酸、稀硫酸反应均有
2 3
气泡产生,说明Fe与两种酸均发生置换反应;③过量的铁与浓硝酸加热反应有气体生成;④FeCl 溶液能与Cu
3
反应,可用于刻蚀印刷电路板( )。
A.①③ B.①② C.②④ D.②③
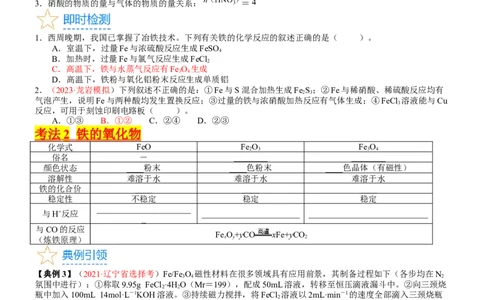
考法 2 铁的氧化物
化学式 FeO Fe O Fe O
2 3 3 4
俗名 - ________ ________
颜色状态 ____粉末 ____色粉末 ____色晶体(有磁性)
溶解性 难溶于水 难溶于水 难溶于水
铁的化合价 ____ ____ ____
稳定性 不稳定 稳定 稳定
______________________
与H+反应 _______________________ ____________________________
_
与CO的反应
FeO+yCO xFe+yCO
(炼铁原理) x y 2
【典例3】(2021·辽宁省选择考)Fe/Fe O 磁性材料在很多领域具有应用前景,其制备过程如下(各步均在N
3 4 2
氛围中进行):①称取9.95g FeCl ·4H O(Mr=199),配成50mL溶液,转移至恒压滴液漏斗中。②向三颈烧
2 2
瓶中加入100mL 14mol·L-1KOH溶液。③持续磁力搅拌,将FeCl 溶液以2mL·min-1的速度全部滴入三颈烧瓶
2
中,100℃下回流3h。④冷却后过滤,依次用热水和乙醇洗涤所得黑色沉淀,在40℃干燥。⑤管式炉内焙烧
2h,得产品3.24g。部分装置如图:
回答下列问题:
(1)仪器a的名称是____________;使用恒压滴液漏斗的原因是___________________________。
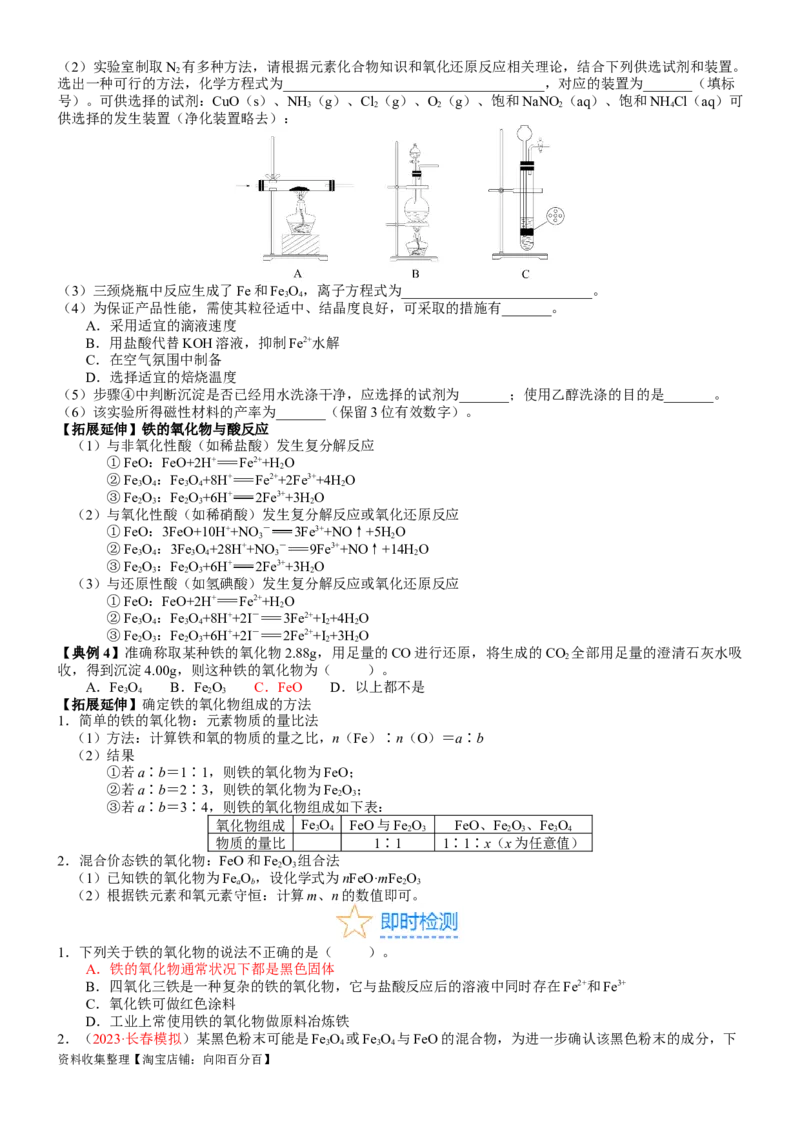
资料收集整理【淘宝店铺:向阳百分百】(2)实验室制取N 有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和装置。
2
选出一种可行的方法,化学方程式为_____________________________________,对应的装置为_______(填标
号)。可供选择的试剂:CuO(s)、NH (g)、Cl(g)、O(g)、饱和NaNO (aq)、饱和NH Cl(aq)可
3 2 2 2 4
供选择的发生装置(净化装置略去):
(3)三颈烧瓶中反应生成了Fe和Fe O,离子方程式为___________________________。
3 4
(4)为保证产品性能,需使其粒径适中、结晶度良好,可采取的措施有_______。
A.采用适宜的滴液速度
B.用盐酸代替KOH溶液,抑制Fe2+水解
C.在空气氛围中制备
D.选择适宜的焙烧温度
(5)步骤④中判断沉淀是否已经用水洗涤干净,应选择的试剂为_______;使用乙醇洗涤的目的是_______。
(6)该实验所得磁性材料的产率为_______(保留3位有效数字)。
【拓展延伸】铁的氧化物与酸反应
(1)与非氧化性酸(如稀盐酸)发生复分解反应
①FeO:FeO+2H+ Fe2++H O
2
②Fe O:Fe O+8H+ Fe2++2Fe3++4H O
3 4 3 4 2
③Fe O:Fe O+6H+ 2Fe3++3H O
2 3 2 3 2
(2)与氧化性酸(如稀硝酸)发生复分解反应或氧化还原反应
①FeO:3FeO+10H++NO - 3Fe3++NO↑+5H O
3 2
②Fe O:3Fe O+28H++NO - 9Fe3++NO↑+14H O
3 4 3 4 3 2
③Fe O:Fe O+6H+ 2Fe3++3H O
2 3 2 3 2
(3)与还原性酸(如氢碘酸)发生复分解反应或氧化还原反应
①FeO:FeO+2H+ Fe2++H O
2
②Fe O:Fe O+8H++2I- 3Fe2++I +4H O
3 4 3 4 2 2
③Fe O:Fe O+6H++2I- 2Fe2++I +3H O
2 3 2 3 2 2
【典例4】准确称取某种铁的氧化物2.88g,用足量的CO进行还原,将生成的CO 全部用足量的澄清石灰水吸
2
收,得到沉淀4.00g,则这种铁的氧化物为( )。
A.Fe O B.Fe O C.FeO D.以上都不是
3 4 2 3
【拓展延伸】确定铁的氧化物组成的方法
1.简单的铁的氧化物:元素物质的量比法
(1)方法:计算铁和氧的物质的量之比,n(Fe)∶n(O)=a∶b
(2)结果
①若a∶b=1∶1,则铁的氧化物为FeO;
②若a∶b=2∶3,则铁的氧化物为Fe O;
2 3
③若a∶b=3∶4,则铁的氧化物组成如下表:
氧化物组成 Fe O FeO与Fe O FeO、Fe O、Fe O
3 4 2 3 2 3 3 4
物质的量比 1∶1 1∶1∶x(x为任意值)
2.混合价态铁的氧化物:FeO和Fe O 组合法
2 3
(1)已知铁的氧化物为Fe O,设化学式为nFeO·mFe O
a b 2 3
(2)根据铁元素和氧元素守恒:计算m、n的数值即可。
1.下列关于铁的氧化物的说法不正确的是( )。
A.铁的氧化物通常状况下都是黑色固体
B.四氧化三铁是一种复杂的铁的氧化物,它与盐酸反应后的溶液中同时存在Fe2+和Fe3+
C.氧化铁可做红色涂料
D.工业上常使用铁的氧化物做原料冶炼铁
2.(2023·长春模拟)某黑色粉末可能是Fe O 或Fe O 与FeO的混合物,为进一步确认该黑色粉末的成分,下
3 4 3 4
资料收集整理【淘宝店铺:向阳百分百】列实验方案不可行的是( )。
A.准确称量一定质量的黑色粉末,用H 充分还原,并用干燥剂收集所得水,获得水的准确质量,进行计
2
算
B.准确称量一定质量的黑色粉末,溶解于足量盐酸,加热蒸干溶液并在空气中灼烧至质量不变,称量所
得粉末质量,进行计算
C.准确称量一定质量的黑色粉末,用CO充分还原,在CO气流中冷却后准确称量剩余固体的质量,计算
D.准确称量一定质量的黑色粉末,与一定量铝粉混合后点燃,充分反应后冷却,准确称量剩余固体质量,
进行计算
考法 3 铁的氢氧化物
化学式 Fe(OH) Fe(OH)
2 3
色态 _____固体 _____固体
溶解性 _____溶于水 _____溶于水
与H+反
___________________________________ _____________________________
应
热分解 - _____________________________
可溶性亚铁盐与碱反应: 可溶性铁盐与碱反应:
制法
Fe2++2OH-=Fe(OH)↓ Fe3++3OH-=Fe(OH)↓
2 3
Fe(OH) 在空气中能够非常迅速地被氧气氧化成Fe(OH),现象是_____沉淀迅速
转化 2 3
变成_____色,最后变成_____色,化学方程式:_____________________________
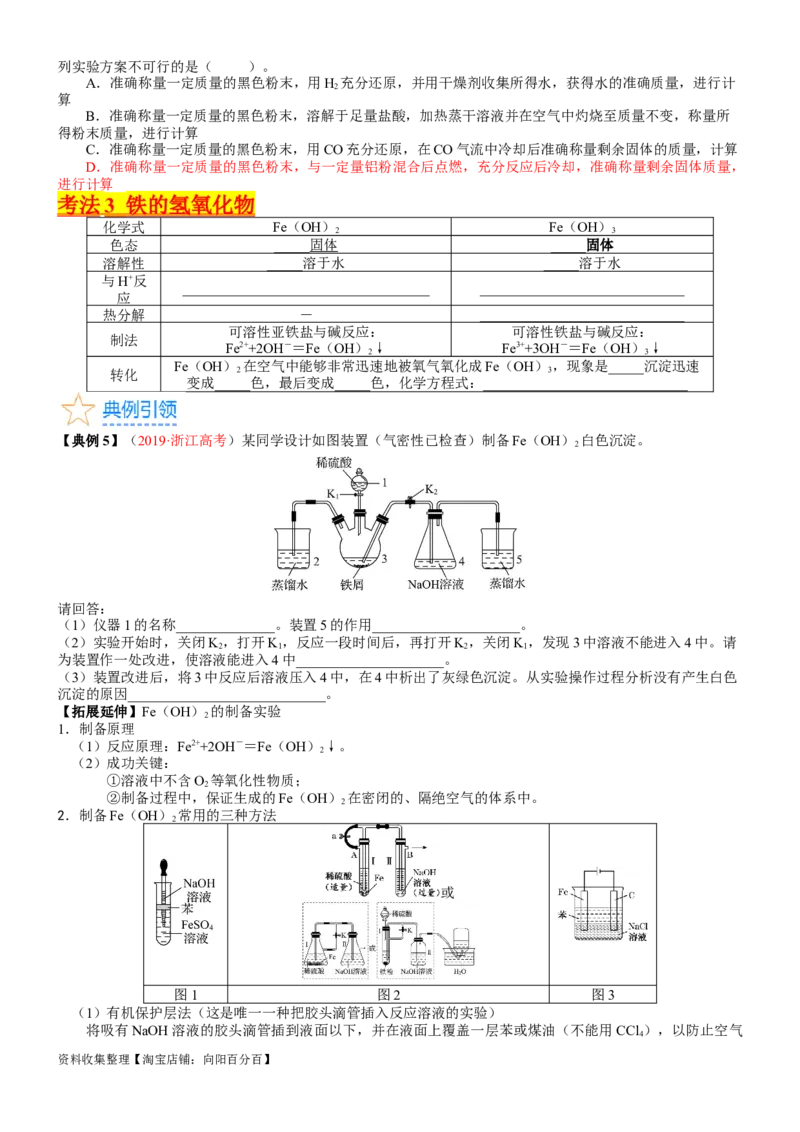
【典例5】(2019·浙江高考)某同学设计如图装置(气密性已检查)制备Fe(OH) 白色沉淀。
2
请回答:
(1)仪器1的名称______________。装置5的作用_____________________。
(2)实验开始时,关闭K,打开K,反应一段时间后,再打开K,关闭K,发现3中溶液不能进入4中。请
2 1 2 1
为装置作一处改进,使溶液能进入4中_____________________。
(3)装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色
沉淀的原因____________________________。
【拓展延伸】Fe(OH) 的制备实验
2
1.制备原理
(1)反应原理:Fe2++2OH-=Fe(OH)↓。
2
(2)成功关键:
①溶液中不含O 等氧化性物质;
2
②制备过程中,保证生成的Fe(OH) 在密闭的、隔绝空气的体系中。
2
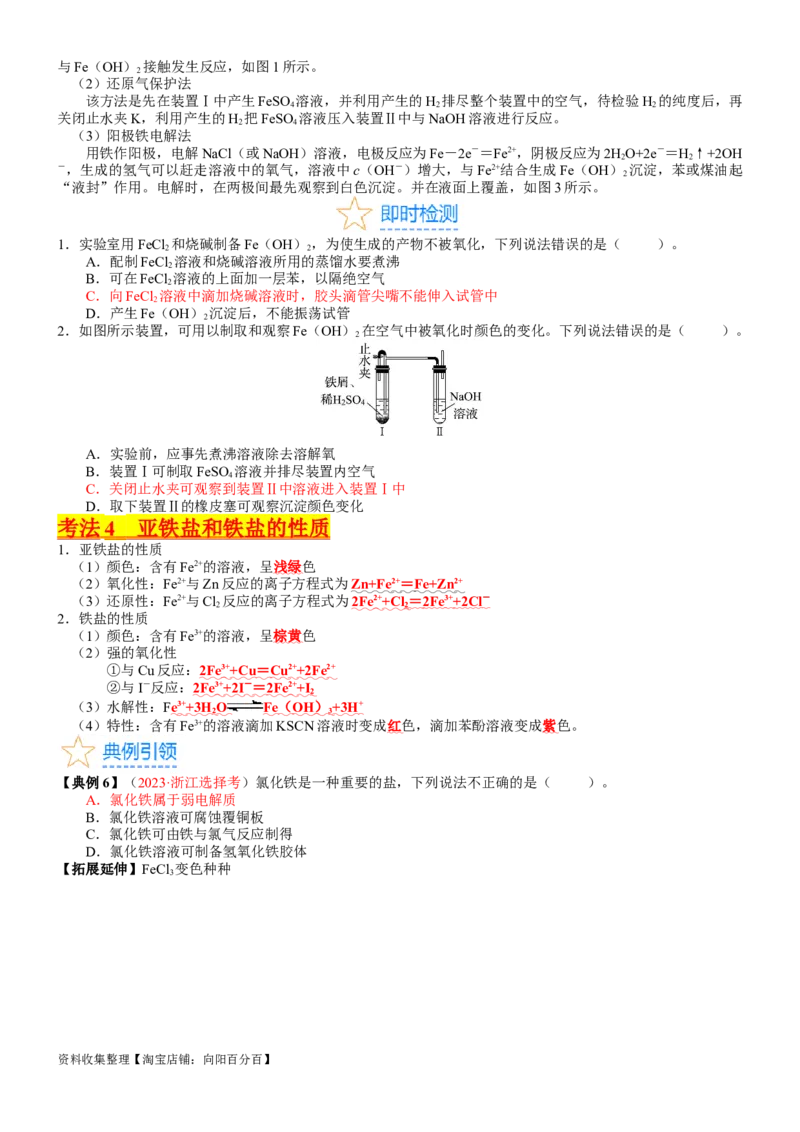
2.制备Fe(OH) 常用的三种方法
2
或
图1 图2 图3
(1)有机保护层法(这是唯一一种把胶头滴管插入反应溶液的实验)
将吸有NaOH溶液的胶头滴管插到液面以下,并在液面上覆盖一层苯或煤油(不能用CCl ),以防止空气
4
资料收集整理【淘宝店铺:向阳百分百】与Fe(OH) 接触发生反应,如图1所示。
2
(2)还原气保护法
该方法是先在装置Ⅰ中产生FeSO 溶液,并利用产生的H 排尽整个装置中的空气,待检验H 的纯度后,再
4 2 2
关闭止水夹K,利用产生的H 把FeSO 溶液压入装置Ⅱ中与NaOH溶液进行反应。
2 4
(3)阳极铁电解法
用铁作阳极,电解NaCl(或NaOH)溶液,电极反应为Fe-2e-=Fe2+,阴极反应为2HO+2e-=H↑+2OH
2 2
-,生成的氢气可以赶走溶液中的氧气,溶液中c(OH-)增大,与Fe2+结合生成Fe(OH) 沉淀,苯或煤油起
2
“液封”作用。电解时,在两极间最先观察到白色沉淀。并在液面上覆盖,如图3所示。
1.实验室用FeCl 和烧碱制备Fe(OH),为使生成的产物不被氧化,下列说法错误的是( )。
2 2
A.配制FeCl 溶液和烧碱溶液所用的蒸馏水要煮沸
2
B.可在FeCl 溶液的上面加一层苯,以隔绝空气
2
C.向FeCl 溶液中滴加烧碱溶液时,胶头滴管尖嘴不能伸入试管中
2
D.产生Fe(OH) 沉淀后,不能振荡试管
2
2.如图所示装置,可用以制取和观察Fe(OH) 在空气中被氧化时颜色的变化。下列说法错误的是( )。
2
A.实验前,应事先煮沸溶液除去溶解氧
B.装置Ⅰ可制取FeSO 溶液并排尽装置内空气
4
C.关闭止水夹可观察到装置Ⅱ中溶液进入装置Ⅰ中
D.取下装置Ⅱ的橡皮塞可观察沉淀颜色变化
考法 4 亚铁盐 和 铁盐的性质
1.亚铁盐的性质
(1)颜色:含有Fe2+的溶液,呈浅绿色
(2)氧化性:Fe2+与Zn反应的离子方程式为 Zn+Fe 2+ = Fe+Zn 2+
(3)还原性:Fe2+与Cl 反应的离子方程式为 2Fe 2+ +Cl = 2F e 3 + +2C l -
2 2
2.铁盐的性质
(1)颜色:含有Fe3+的溶液,呈棕黄色
(2)强的氧化性
①与Cu反应: 2Fe 3+ +Cu = C u 2+ +2Fe 2+
②与I-反应: 2Fe 3+ +2I - = 2Fe 2+ +I
2
(3)水解性:F e 3+ +3H O Fe ( OH ) +3H +
2 3
(4)特性:含有Fe3+的溶液滴加KSCN溶液时变成红色,滴加苯酚溶液变成紫色。
【典例6】(2023·浙江选择考)氯化铁是一种重要的盐,下列说法不正确的是( )。
A.氯化铁属于弱电解质
B.氯化铁溶液可腐蚀覆铜板
C.氯化铁可由铁与氯气反应制得
D.氯化铁溶液可制备氢氧化铁胶体
【拓展延伸】FeCl 变色种种
3
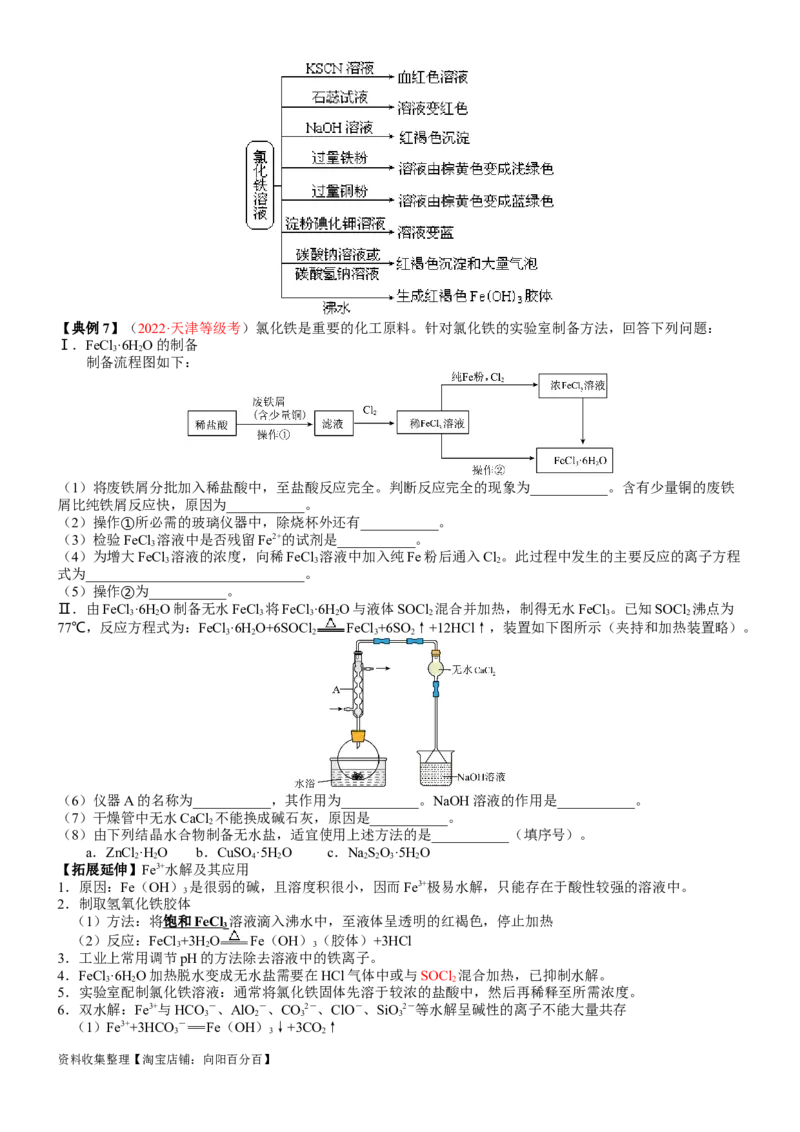
资料收集整理【淘宝店铺:向阳百分百】【典例7】(2022·天津等级考)氯化铁是重要的化工原料。针对氯化铁的实验室制备方法,回答下列问题:
Ⅰ.FeCl ·6HO的制备
3 2
制备流程图如下:
(1)将废铁屑分批加入稀盐酸中,至盐酸反应完全。判断反应完全的现象为___________。含有少量铜的废铁
屑比纯铁屑反应快,原因为___________。
(2)操作①所必需的玻璃仪器中,除烧杯外还有___________。
(3)检验FeCl 溶液中是否残留Fe2+的试剂是___________。
3
(4)为增大FeCl 溶液的浓度,向稀FeCl 溶液中加入纯Fe粉后通入Cl。此过程中发生的主要反应的离子方程
3 3 2
式为_______________________________。
(5)操作②为___________。
Ⅱ.由FeCl ·6HO制备无水FeCl 将FeCl ·6HO与液体SOCl 混合并加热,制得无水FeCl 。已知SOCl 沸点为
3 2 3 3 2 2 3 2
77℃,反应方程式为:FeCl ·6HO+6SOCl FeCl +6SO ↑+12HCl↑,装置如下图所示(夹持和加热装置略)。
3 2 2 3 2
(6)仪器A的名称为___________,其作用为___________。NaOH溶液的作用是___________。
(7)干燥管中无水CaCl 不能换成碱石灰,原因是___________。
2
(8)由下列结晶水合物制备无水盐,适宜使用上述方法的是___________(填序号)。
a.ZnCl·HO b.CuSO ·5HO c.NaSO·5HO
2 2 4 2 2 2 3 2
【拓展延伸】Fe3+水解及其应用
1.原因:Fe(OH) 是很弱的碱,且溶度积很小,因而Fe3+极易水解,只能存在于酸性较强的溶液中。
3
2.制取氢氧化铁胶体
(1)方法:将 饱和 FeC l 溶液滴入沸水中,至液体呈透明的红褐色,停止加热
3
(2)反应:FeCl +3H O Fe(OH)(胶体)+3HCl
3 2 3
3.工业上常用调节pH的方法除去溶液中的铁离子。
4.FeCl ·6HO加热脱水变成无水盐需要在HCl气体中或与SOCl 混合加热,已抑制水解。
3 2 2
5.实验室配制氯化铁溶液:通常将氯化铁固体先溶于较浓的盐酸中,然后再稀释至所需浓度。
6.双水解:Fe3+与HCO -、AlO-、CO2-、ClO-、SiO2-等水解呈碱性的离子不能大量共存
3 2 3 3
(1)Fe3++3HCO - Fe(OH)↓+3CO↑
3 3 2
资料收集整理【淘宝店铺:向阳百分百】