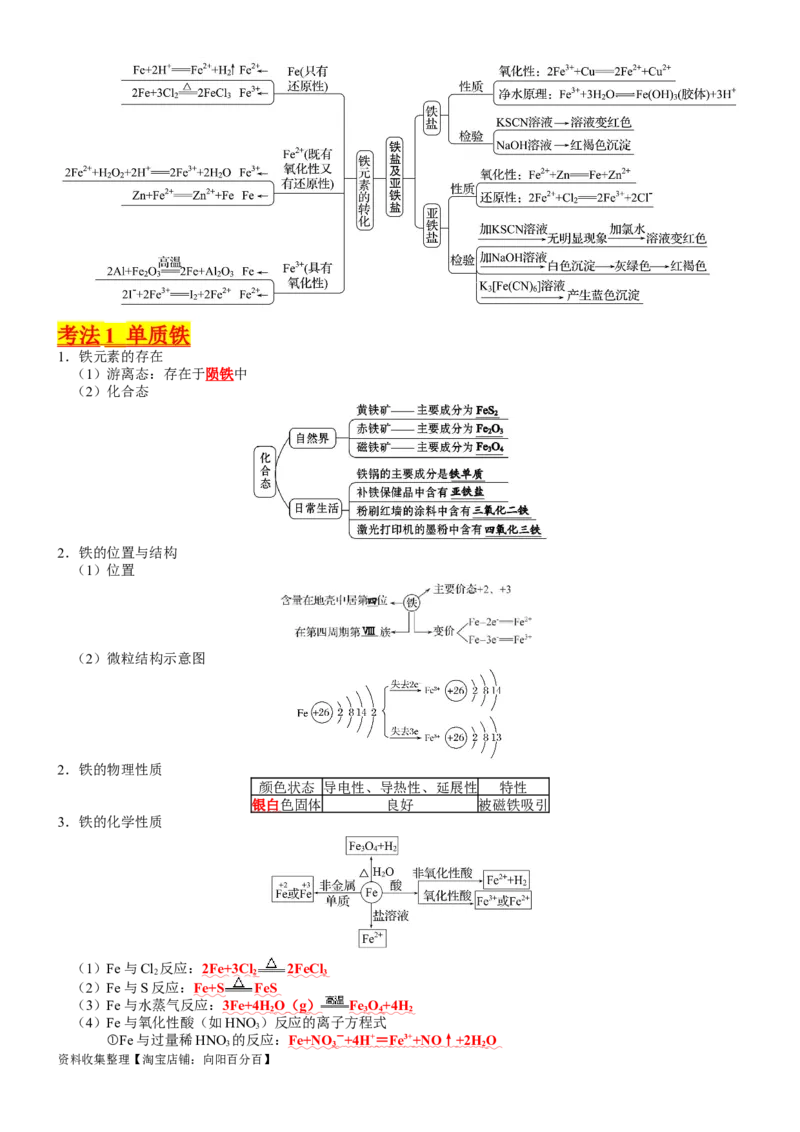
文档内容
考点 10 铁及其重要化合物
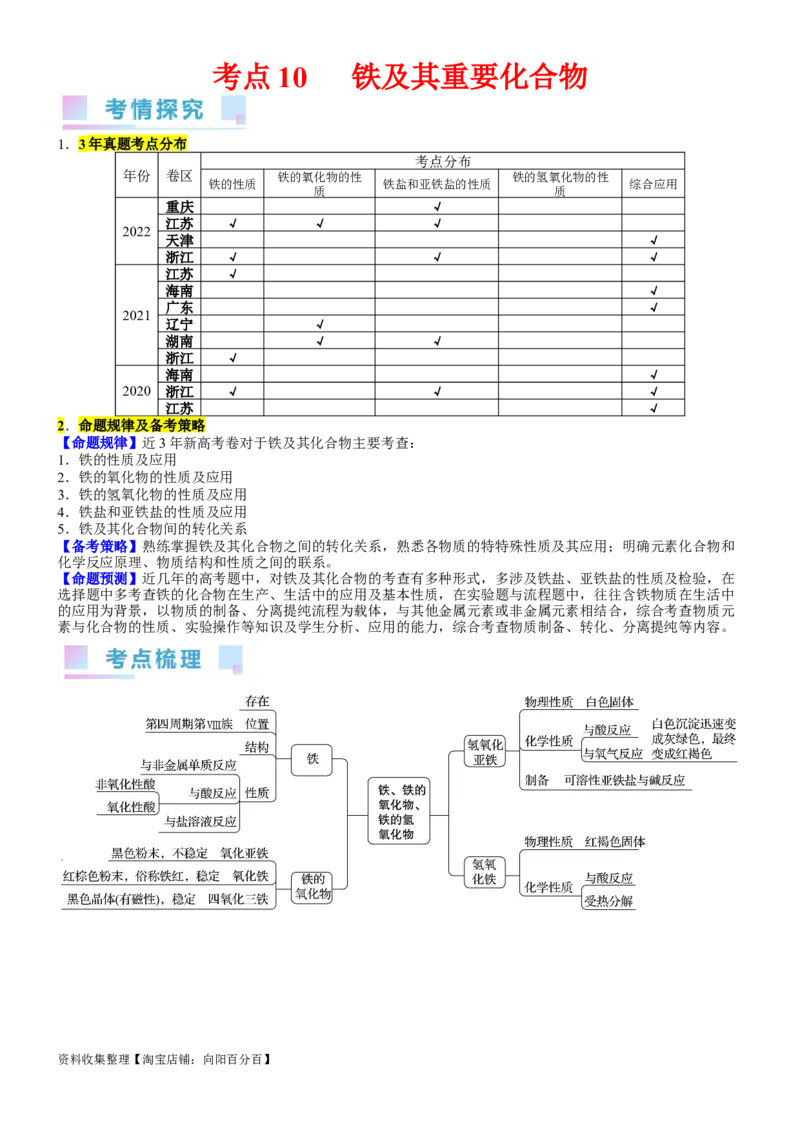
1.3年真题考点分布
考点分布
年份 卷区 铁的氧化物的性 铁的氢氧化物的性
铁的性质 铁盐和亚铁盐的性质 综合应用
质 质
重庆 √
江苏 √ √ √
2022
天津 √
浙江 √ √ √
江苏 √
海南 √
广东 √
2021
辽宁 √
湖南 √ √
浙江 √
海南 √
2020 浙江 √ √ √
江苏 √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于铁及其化合物主要考查:
1.铁的性质及应用
2.铁的氧化物的性质及应用
3.铁的氢氧化物的性质及应用
4.铁盐和亚铁盐的性质及应用
5.铁及其化合物间的转化关系
【备考策略】熟练掌握铁及其化合物之间的转化关系,熟悉各物质的特特殊性质及其应用;明确元素化合物和
化学反应原理、物质结构和性质之间的联系。
【命题预测】近几年的高考题中,对铁及其化合物的考查有多种形式,多涉及铁盐、亚铁盐的性质及检验,在
选择题中多考查铁的化合物在生产、生活中的应用及基本性质,在实验题与流程题中,往往含铁物质在生活中
的应用为背景,以物质的制备、分离提纯流程为载体,与其他金属元素或非金属元素相结合,综合考查物质元
素与化合物的性质、实验操作等知识及学生分析、应用的能力,综合考查物质制备、转化、分离提纯等内容。
资料收集整理【淘宝店铺:向阳百分百】考法 1 单质铁
1.铁元素的存在
(1)游离态:存在于陨铁中
(2)化合态
2.铁的位置与结构
(1)位置
(2)微粒结构示意图
2.铁的物理性质
颜色状态 导电性、导热性、延展性 特性
银白色固体 良好 被磁铁吸引
3.铁的化学性质
(1)Fe与Cl 反应:2Fe+3Cl 2FeCl
2 2 3
(2)Fe与S反应:Fe+S FeS
(3)Fe与水蒸气反应:3Fe+4H O ( g ) FeO+4H
2 3 4 2
(4)Fe与氧化性酸(如HNO)反应的离子方程式
3
①Fe与过量稀HNO 的反应:Fe+NO - +4H + = F e 3 + +NO ↑ +2H O
3 3 2
资料收集整理【淘宝店铺:向阳百分百】②Fe与少量稀HNO 的反应:3Fe+2NO - +8H + = 3F e 2 + +2NO ↑ +4H O
3 3 2
(5)Fe与FeCl 溶液的反应: Fe+2Fe 3+ = 3Fe 2+
3
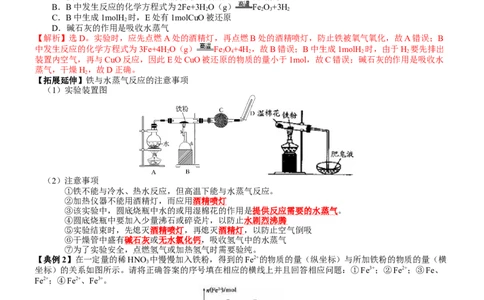
【典例1】某化学兴趣小组利用如图装置进行“铁与水蒸气反应”的实验,并检验产物的性质,下列说法正确
的是( )。
A.实验时,应先点燃B处的酒精喷灯,再点燃A处的酒精灯
B.B中发生反应的化学方程式为2Fe+3H O(g) Fe O+3H
2 2 3 2
C.B中生成1molH 时,E处有1molCuO被还原
2
D.碱石灰的作用是吸收水蒸气
【解析】选D。实验时,应先点燃A处的酒精灯,再点燃B处的酒精喷灯,防止铁被氧气氧化,故A错误;B
中发生反应的化学方程式为3Fe+4H O(g) Fe O+4H ,故B错误;B中生成1molH 时,由于H 要先排出
2 3 4 2 2 2
装置内空气,再与CuO反应,因此E处CuO被还原的物质的量小于1mol,故C错误;碱石灰的作用是吸收水
蒸气,干燥H,故D正确。
2
【拓展延伸】铁与水蒸气反应的注意事项
(1)实验装置图
(2)注意事项
①铁不能与冷水、热水反应,但高温下能与水蒸气反应。
②加热仪器不能用酒精灯,而应用酒精喷灯
③该实验中,圆底烧瓶中水的或用湿棉花的作用是 提供反应需要的 水蒸气 。
④圆底烧瓶中要加入少量沸石或碎瓷片,以防止水剧烈沸腾
⑤实验结束时,先熄灭酒精喷灯,再熄灭酒精灯,以防止空气倒吸
⑥干燥管中盛有碱石灰或无水氯化钙,吸收氢气中的水蒸气
⑦为了实验安全,点燃氢气或加热氢气时需要验纯。
【典例2】在一定量的稀HNO 中慢慢加入铁粉,得到的Fe2+的物质的量(纵坐标)与所加铁粉的物质的量(横
3
坐标)的关系如图所示。请将正确答案的序号填在相应的横线上并且回答相应问题:①Fe3+;②Fe2+;③Fe、
Fe2+;④Fe2+、Fe3+。
(1)AB段铁元素以__________形式存在。
(2)BC段铁元素以__________形式存在。
(3)CD段铁元素以__________形式存在,将该段溶液中的离子按照浓度由大到小的顺序排列_______________。
(4)若将14g铁粉溶于1L稀硝酸中恰好完全反应,放出NO气体后称量所得溶液,发现比原溶液质量增加
8g,则原溶液中硝酸的物质的量浓度是___________。
【解析】硝酸具有强氧化性,能够被铁氧化成Fe3+,反应的离子方程式为:Fe+4H++NO -=Fe3++NO↑+2HO。
3 2
所以向稀HNO 中加入铁粉,开始时稀HNO 过量应生成Fe3+(AB段),随加入铁粉量的增加,HNO 反应完全
3 3 3
后,开始发生反应2Fe3++Fe=3Fe2+,Fe3+部分被还原成Fe2+(BC段),最后全部转化为Fe2+(CD段)。CD段
得到的溶液是Fe(NO ) 溶液,因为c(NO -)是c(Fe2+)的两倍,所以c(NO -)>c(Fe2+),因为Fe2+在
3 2 3 3
资料收集整理【淘宝店铺:向阳百分百】溶液中存在微弱的水解:Fe2++2HO Fe(OH)+2H+,所以c(H+)>c(OH-),即c(NO -)>c
2 2 3
(Fe2+)>c(H+)>c(OH-)。(4)根据质量守恒定律:m(Fe)+m(HNO)=m(溶液)+m(NO),则
3
溶液增重:△m(溶液)=m(溶液)-m(HNO)=m(Fe)-m(NO)=8g,即14g-m(NO)=8g,解得
3
6g
30g/mol
m(NO)=6g,n(NO)= =0.2mol。铁粉和稀硝酸可能发生如下两个反应:Fe+4HNO (稀) Fe
3
(NO )+NO↑+2H O,3Fe+8HNO (稀) 3Fe(NO )+2NO↑+4H O,无论发生哪一个反应恒有如下关
3 3 2 3 3 2 2
0.8mol
系:n(HNO)∶n(NO)=4∶1,则n(HNO)=4n(NO)=4×0.2mol=0.8mol,c(HNO)= 1L =
3 3 3
0.8mol/L。
【答案】(1)① (2)④ (3)③ c(NO -)>c(Fe2+)>c(H+)>c(OH-)(4)0.8mol/L
3
【拓展延伸】铁与稀硝酸反应规律
1.反应方程式
(1)HNO 过量:Fe+4HNO =Fe(NO )+NO↑+2H O
3 3 3 3 2
(2)Fe过量:3Fe+8HNO =3Fe(NO )+2NO↑+4H O
3 3 2 2
2.产物和相对量的关系
(1) ≤ ,产物仅有Fe(NO ),HNO 可能有剩余;
3 3 3
(2) ≥ ,产物仅有Fe(NO ),Fe可能有剩余;
3 2
(3) < < ,产物为Fe(NO ) 和Fe(NO ),Fe和HNO 都反应完全。
3 3 3 2 3
3.硝酸的物质的量与气体的物质的量关系: =
1.西周晚期,我国已掌握了冶铁技术。下列有关铁的化学反应的叙述正确的是( )。
A.室温下,过量Fe与浓硫酸反应生成FeSO
4
B.加热时,过量Fe与氯气反应生成FeCl
2
C.高温下,铁与水蒸气反应有Fe O 生成
3 4
D.高温下,铁粉与氧化铝粉末反应生成单质铝
【解析】选C。室温下,过量Fe与浓硫酸发生钝化,应加热下反应,故A错误;氯气具有强氧化性,加热时,
过量Fe与氯气反应生成FeCl ,故B错误;高温下Fe与水蒸气反应生成四氧化三铁和氢气,叙述合理,故C正
3
确;Al比Fe的活泼性强,则Fe与氧化铝不反应,故D错误。
2.(2023·龙岩模拟)下列叙述不正确的是:①Fe与S混合加热生成Fe S;②Fe与稀硝酸、稀硫酸反应均有
2 3
气泡产生,说明Fe与两种酸均发生置换反应;③过量的铁与浓硝酸加热反应有气体生成;④FeCl 溶液能与Cu
3
反应,可用于刻蚀印刷电路板( )。
A.①③ B.①② C.②④ D.②③
【解析】选B。Fe是变价金属,遇强氧化剂(如HNO、Cl 等)生成+3价铁,遇弱氧化剂(如S或I 等)生成
3 2 2
+2价铁,故Fe与S混合加热生成FeS,①错误;Fe与稀硝酸反应生成的气体为NO,该反应不是置换反应,②
错误。
考法 2 铁的氧化物
化学式 FeO Fe O Fe O
2 3 3 4
俗名 - 铁红 磁性氧化铁
颜色状态 黑色粉末 红棕色粉末 黑色晶体(有磁性)
溶解性 难溶于水 难溶于水 难溶于水
铁的化合价 +2 +3 +2 、 +3
稳定性 不稳定 稳定 稳定
与H+反应 FeO+2H + = Fe 2+ +H O FeO +6H + = 2Fe 3+ +3H O FeO +8H + = Fe 2+ +2Fe 3+ +4H O
2 2 3 2 3 4 2
资料收集整理【淘宝店铺:向阳百分百】与CO的反应
(炼铁原 FeO+yCO xFe+yCO
x y 2
理)
【典例3】(2021·辽宁省选择考)Fe/Fe O 磁性材料在很多领域具有应用前景,其制备过程如下(各步均在N
3 4 2
氛围中进行):①称取9.95g FeCl ·4H O(Mr=199),配成50mL溶液,转移至恒压滴液漏斗中。②向三颈烧
2 2
瓶中加入100mL 14mol·L-1KOH溶液。③持续磁力搅拌,将FeCl 溶液以2mL·min-1的速度全部滴入三颈烧瓶
2
中,100℃下回流3h。④冷却后过滤,依次用热水和乙醇洗涤所得黑色沉淀,在40℃干燥。⑤管式炉内焙烧
2h,得产品3.24g。部分装置如图:
回答下列问题:
(1)仪器a的名称是____________;使用恒压滴液漏斗的原因是___________________________。
(2)实验室制取N 有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和装置。
2
选出一种可行的方法,化学方程式为_____________________________________,对应的装置为_______(填标
号)。可供选择的试剂:CuO(s)、NH (g)、Cl(g)、O(g)、饱和NaNO (aq)、饱和NH Cl(aq)可
3 2 2 2 4
供选择的发生装置(净化装置略去):
(3)三颈烧瓶中反应生成了Fe和Fe O,离子方程式为___________________________。
3 4
(4)为保证产品性能,需使其粒径适中、结晶度良好,可采取的措施有_______。
A.采用适宜的滴液速度
B.用盐酸代替KOH溶液,抑制Fe2+水解
C.在空气氛围中制备
D.选择适宜的焙烧温度
(5)步骤④中判断沉淀是否已经用水洗涤干净,应选择的试剂为_______;使用乙醇洗涤的目的是_______。
(6)该实验所得磁性材料的产率为_______(保留3位有效数字)。
【解析】(1)根据仪器的构造与用途可知,仪器a的名称是(球形)冷凝管;恒压滴液漏斗在使用过程中可保
持气压平衡,使液体顺利流下。(2)实验室中制备少量氮气的基本原理是用适当的氧化剂将氨或铵盐氧化,常
见的可以是将氨气通入灼热的氧化铜中反应,其化学方程式为:2NH +3CuO N+3Cu+3H O;可选择气体通
3 2 2
入硬质玻璃管与固体在加热条件下发生反应,即选择A装置。还可利用饱和NaNO (aq)和饱和NH Cl(aq)
2 4
在加热下发生氧化还原反应制备氮气,反应的化学方程式为:NaNO +NHCl NaCl+N ↑+2H O↑,可选择
2 4 2 2
液体与液体加热制备气体型,所以选择B装置。(3)三颈烧瓶中FeCl 溶液与100mL 14mol·L-1KOH溶液发生
2
反应生成了Fe和Fe O,根据氧化还原反应的规律可知,该反应的离子方程式为4Fe2++8OH-
3 4
Fe↓+Fe O↓+4H O;(4)结晶度受反应速率与温度的影响,所以为保证产品性能,需使其粒径适中、结晶度
3 4 2
良好,可采取的措施有采用适宜的滴液速度、选择适宜的焙烧温度,AD项符合题意,若用盐酸代替KOH溶液,
生成的晶体为Fe和Fe O,均会溶解在盐酸中,因此得不到该晶粒,故B不选;若在空气氛围中制备,则亚铁
3 4
离子容易被空气氧化,故D不选;(5)因为反应后溶液中有氯离子,所以在步骤④中判断沉淀是否已经用水
洗涤干净,需取最后一次洗涤液,加入稀硝酸酸化后,再加入硝酸银溶液,若无白色沉淀生成,则证明已洗涤
干净;乙醇易溶于水,易挥发,所以最后使用乙醇洗涤的目的是除去晶体表面水分,便于快速干燥。(6)
资料收集整理【淘宝店铺:向阳百分百】9.95g
199g/mol
9.95g FeCl ·4H O(Mr=199)的物质的量为 =0.05mol,根据发生反应的离子方程式:4Fe2++8OH-
2 2
Fe↓+Fe O↓+4H O,可知理论上所得的Fe和Fe O 的物质的量各自为0.0125mol,所以得到的黑色产品质量应
3 4 2 3 4
3.24g
3.6g
为0.0125mol×(56g/mol +232g/mol)=3.6g,实际得到的产品3.24g,所以其产率为 ×100%=90.0%。
【答案】(1)(球形)冷凝管;平衡气压,便于液体顺利流下
(2)2NH +3CuO N+3Cu+3H O(或NaNO +NHCl NaCl+N ↑+2H O↑);A(或B)
3 2 2 2 4 2 2
(3)4Fe2++8OH- Fe↓+Fe O↓+4H O(4)AD
3 4 2
(5)稀硝酸和硝酸银溶液;除去晶体表面水分,便于快速干燥(6)90.0%
【拓展延伸】铁的氧化物与酸反应
(1)与非氧化性酸(如稀盐酸)发生复分解反应
①FeO:FeO+2H+ Fe2++H O
2
②Fe O:Fe O+8H+ Fe2++2Fe3++4H O
3 4 3 4 2
③Fe O:Fe O+6H+ 2Fe3++3H O
2 3 2 3 2
(2)与氧化性酸(如稀硝酸)发生复分解反应或氧化还原反应
①FeO:3FeO+10H++NO - 3Fe3++NO↑+5H O
3 2
②Fe O:3Fe O+28H++NO - 9Fe3++NO↑+14H O
3 4 3 4 3 2
③Fe O:Fe O+6H+ 2Fe3++3H O
2 3 2 3 2
(3)与还原性酸(如氢碘酸)发生复分解反应或氧化还原反应
①FeO:FeO+2H+ Fe2++H O
2
②Fe O:Fe O+8H++2I- 3Fe2++I +4H O
3 4 3 4 2 2
③Fe O:Fe O+6H++2I- 2Fe2++I +3H O
2 3 2 3 2 2
【典例4】准确称取某种铁的氧化物2.88g,用足量的CO进行还原,将生成的CO 全部用足量的澄清石灰水吸
2
收,得到沉淀4.00g,则这种铁的氧化物为( )。
A.Fe O B.Fe O C.FeO D.以上都不是
3 4 2 3
【解析】选C。4.00g CaCO 沉淀的物质的量为0.04mol,则根据碳元素守恒:参加反应的CO及生成的CO 的物
3 2
质的量也为 0.04mol,增加的氧元素为 n(O)=0.04mol(即铁的氧化物中所有的氧元素),其质量为
0.04mol×16g·mol-1=0.64g,铁的氧化物中氧元素质量为0.64g,铁元素的质量为2.88g-0.64g=2.24g,铁元素
的物质的量为:n(Fe)= =0.04mol,铁的氧化物中铁元素与氧元素的物质的量之比为
0.04mol∶0.04mol=1∶1,则这种铁的氧化物的化学式为FeO。
【拓展延伸】确定铁的氧化物组成的方法
1.简单的铁的氧化物:元素物质的量比法
(1)方法:计算铁和氧的物质的量之比,n(Fe)∶n(O)=a∶b
(2)结果
①若a∶b=1∶1,则铁的氧化物为FeO;
②若a∶b=2∶3,则铁的氧化物为Fe O;
2 3
③若a∶b=3∶4,则铁的氧化物组成如下表:
氧化物组成 Fe O FeO与Fe O FeO、Fe O、Fe O
3 4 2 3 2 3 3 4
物质的量比 1∶1 1∶1∶x(x为任意值)
2.混合价态铁的氧化物:FeO和Fe O 组合法
2 3
(1)已知铁的氧化物为Fe O,设化学式为nFeO·mFe O
a b 2 3
(2)根据铁元素和氧元素守恒:计算m、n的数值即可。
1.下列关于铁的氧化物的说法不正确的是( )。
A.铁的氧化物通常状况下都是黑色固体
B.四氧化三铁是一种复杂的铁的氧化物,它与盐酸反应后的溶液中同时存在Fe2+和Fe3+
C.氧化铁可做红色涂料
D.工业上常使用铁的氧化物做原料冶炼铁
【解析】选A。A项,氧化铁是红棕色粉末,氧化亚铁和四氧化三铁是黑色的,错误;B项,四氧化三铁是一
1 2
种复杂的铁的氧化物,其中3是Fe2+、3 是Fe3+,Fe O 可看作是由FeO、Fe O 组成的化合物[实质是Fe
3 4 2 3
(FeO),偏铁酸亚铁盐],它与盐酸反应后的溶液中同时存在Fe2+和Fe3+,正确;C项,Fe O 可做红色油漆、
2 2 2 3
涂料,正确;D项,工业上常使用铁的氧化物做原料,用CO冶炼铁,正确。
资料收集整理【淘宝店铺:向阳百分百】2.(2023·长春模拟)某黑色粉末可能是Fe O 或Fe O 与FeO的混合物,为进一步确认该黑色粉末的成分,下
3 4 3 4
列实验方案不可行的是( )。
A.准确称量一定质量的黑色粉末,用H 充分还原,并用干燥剂收集所得水,获得水的准确质量,进行计
2
算
B.准确称量一定质量的黑色粉末,溶解于足量盐酸,加热蒸干溶液并在空气中灼烧至质量不变,称量所
得粉末质量,进行计算
C.准确称量一定质量的黑色粉末,用CO充分还原,在CO气流中冷却后准确称量剩余固体的质量,计算
D.准确称量一定质量的黑色粉末,与一定量铝粉混合后点燃,充分反应后冷却,准确称量剩余固体质量,
进行计算
【解析】选D。准确称量一定质量的黑色粉末,用H 充分还原,并用干燥剂收集所得水,获得水的准确质量,
2
计算得到氧元素质量和铁元素质量,依据铁元素和氧元素物质的量之比确定化学式,能计算得到物质组成,故
A不选;准确称量一定质量的黑色粉末,溶解于足量盐酸,加热蒸干溶液并在空气中灼烧至质量不变,称量所
得粉末质量,得到氧化铁质量,依据铁元素和氧元素守恒进行计算铁元素和氧元素物质的量之比判断氧化物化
学式,能计算得到物质组成,故B不选;准确称量一定质量的黑色粉末,用CO充分还原,在CO气流中冷却
后准确称量剩余固体的质量,依据铁元素和氧元素质量守恒计算铁元素和氧元素物质的量之比分析判断氧化物
的存在形式,能计算得到物质组成,故C不选;准确称量一定质量的黑色粉末,与一定质量铝粉混合后点燃,
充分反应后冷却,准确称量剩余固体质量,反应前后都是固体反应前后固体质量不变,不能计算确定该黑色粉
末的成分,故D选。
考法 3 铁的氢氧化物
化学式 Fe(OH) Fe(OH)
2 3
色态 白色固体 红褐色固体
溶解性 难溶于水 难溶于水
与H+反
Fe ( OH ) +2H + = Fe 2+ +2H O Fe ( OH ) +3H + = Fe 3+ +3H O
应 2 2 3 2
热分解 - 2Fe ( OH ) FeO+3H O
3 2 3 2
可溶性亚铁盐与碱反应: 可溶性铁盐与碱反应:
制法
Fe2++2OH-=Fe(OH)↓ Fe3++3OH-=Fe(OH)↓
2 3
Fe(OH) 在空气中能够非常迅速地被氧气氧化成Fe(OH),现象是白色沉淀迅速变
转化 2 3
成灰绿色,最后变成红褐色,化学方程式: 4Fe ( OH ) +O +2H O = 4Fe ( OH )
2 2 2 3
【典例5】(2019·浙江高考)某同学设计如图装置(气密性已检查)制备Fe(OH) 白色沉淀。
2
请回答:
(1)仪器1的名称______________。装置5的作用_____________________。
(2)实验开始时,关闭K,打开K,反应一段时间后,再打开K,关闭K,发现3中溶液不能进入4中。请
2 1 2 1
为装置作一处改进,使溶液能进入4中_____________________。
(3)装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色
沉淀的原因____________________________。
【解析】该装置制备Fe(OH) 白色沉淀的思路是在排净空气的气氛中,先使铁屑和稀硫酸反应得到FeSO ,
2 4
再利用气体产生气压把FeSO 溶液压至装置4中与NaOH反应,得到Fe(OH),注意所需试剂也需要加热除
4 2
掉溶解氧。(1)仪器1是分液漏斗或滴液漏斗,该反应需要置于无氧环境,注意这里跟防倒吸无关,装置5的
作用是液封,防止空气进入装置4。(2)实验开始时,关闭K,打开K,反应一段时间后,再打开K,关闭
2 1 2
K,发现3中溶液不能进入4中。操作失败的原因是仪器3中产生的H 从左侧导管逸出,没有足够的压强,所
1 2
以不能将FeSO 溶液压入4中,因而在装置2、3之间添加控制开关即可。(3)灰绿色沉淀产生的原因是装置4
4
中空气没有完全排净,Fe(OH) 被空气氧化。
2
【答案】(1)分液漏斗(滴液漏斗)液封,防止空气进入装置4
(2)在装置2、3之间添加控制开关(3)装置4内的空气没有排净
【拓展延伸】Fe(OH) 的制备实验
2
资料收集整理【淘宝店铺:向阳百分百】