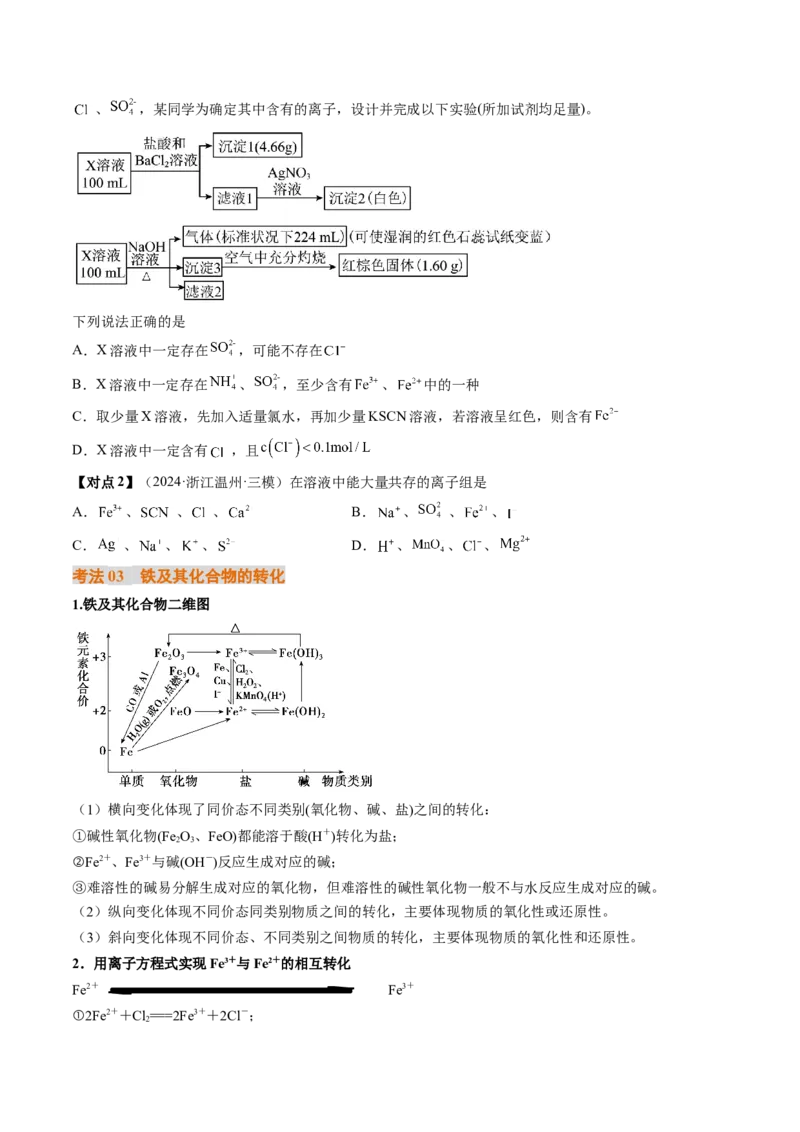
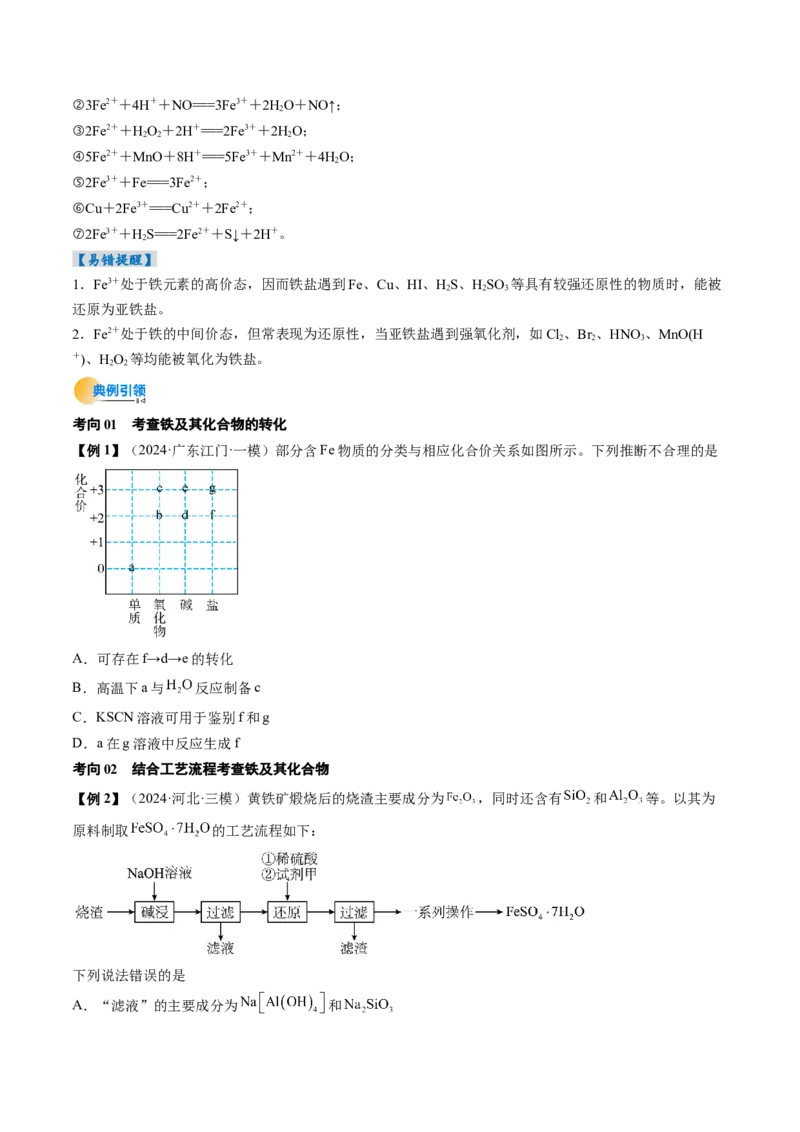
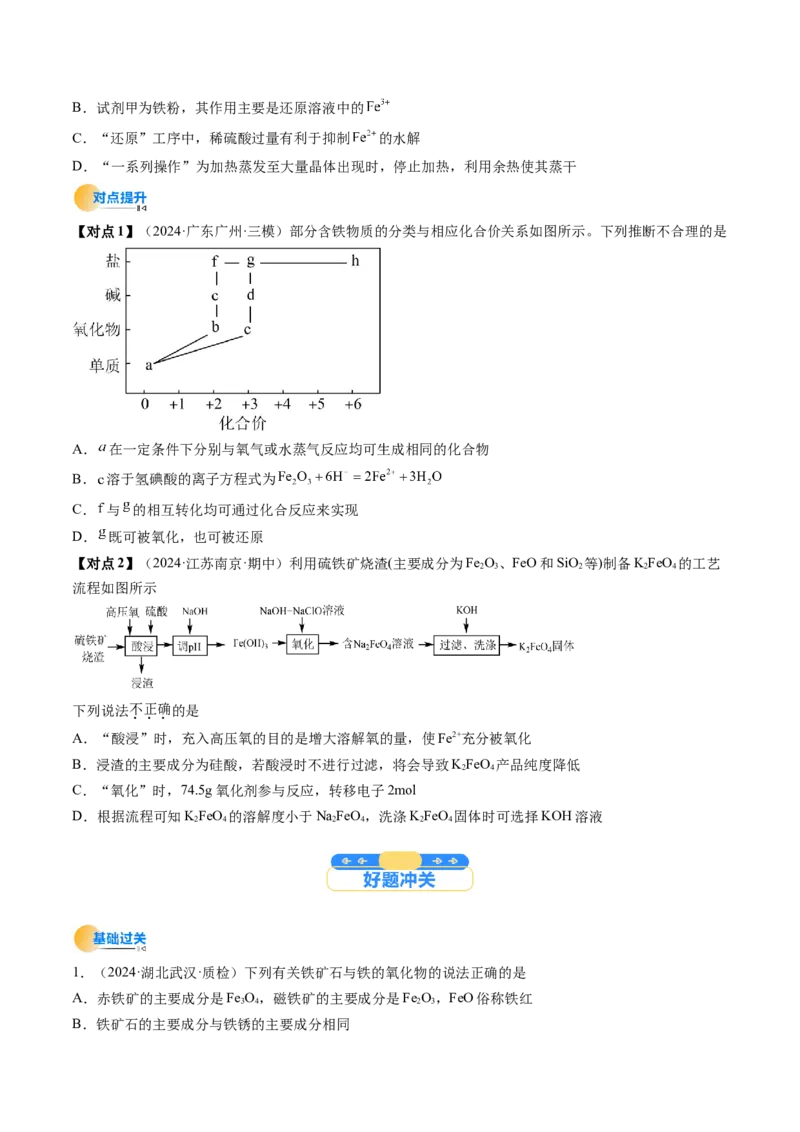
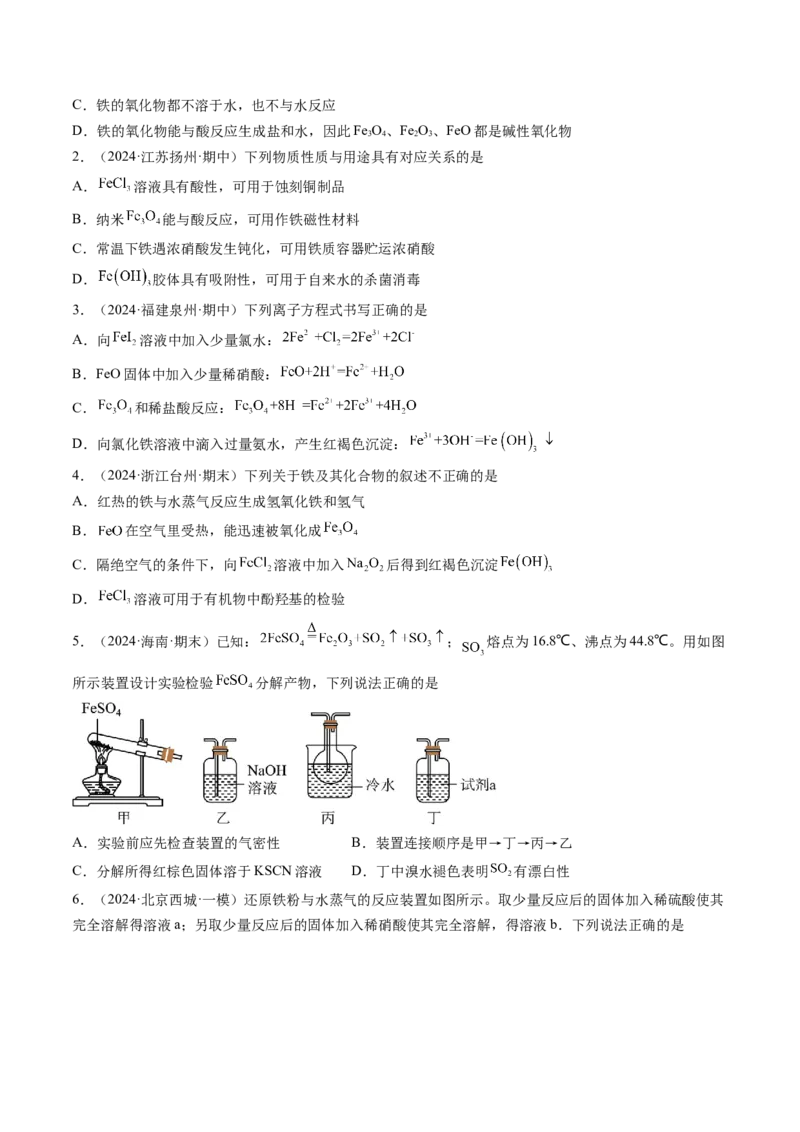
文档内容
考点 10 铁及其重要化合物
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 铁的单质 氧化物 铁的氢氧化物............................................................................................2
考法02 亚铁离子、铁离子的性质及检验................................................................................................6
考法03 铁及其化合物的转化...................................................................................................................9
...........................................................................................................................................11
1.高考真题考点分布
考点内容 考点分布
2024全国新课标卷9题,6分;2023浙江1月卷4题,2分;2023全国卷7题,6
铁及其化合物的 分;
性质及应用 2023广东卷7题,2分;2022浙江卷9题,2分;2022重庆卷4题,3分;
2022浙江卷22题,2分;2022广东卷6题,3分;
Fe2+、Fe3+的检 2023湖南卷7题,3分;2022广东卷11题,3分;2022海南卷6题,2分;
验 2021湖南卷3题,3分;
铁及其化合物的 2024安徽卷4题,3分;2023全国卷11题,6分;2023浙江卷16题,2分;
转化 2023江苏卷11题,3分;2023辽宁卷10题,3分;2023浙江1月卷16题,2分;
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,铁的性质,铁的氧化物、Fe(OH) 和Fe(OH) 的性质、“铁三角”转
2 3
化等仍是高考命题的热点。
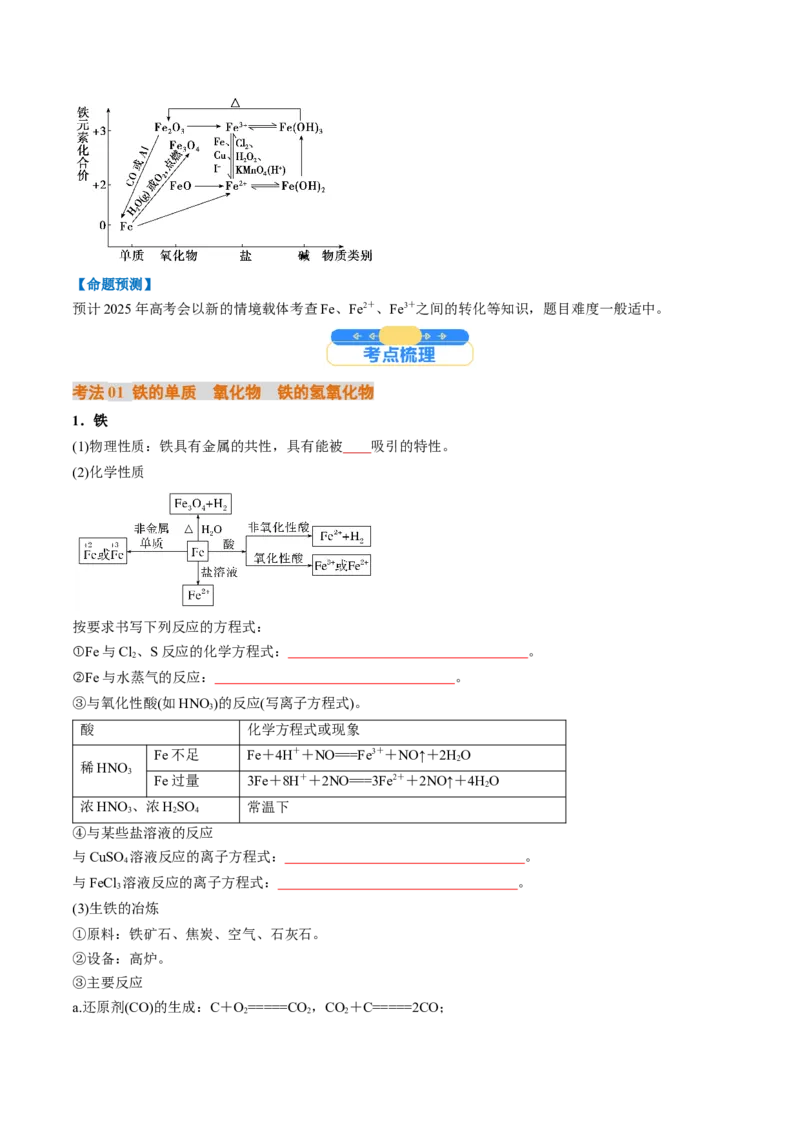
【备考策略】【命题预测】
预计2025年高考会以新的情境载体考查Fe、Fe2+、Fe3+之间的转化等知识,题目难度一般适中。
考法01 铁的单质 氧化物 铁的氢氧化物
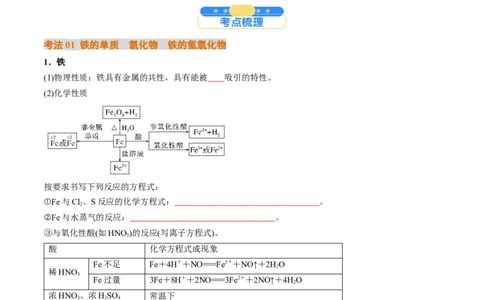
1.铁
(1)物理性质:铁具有金属的共性,具有能被 吸引的特性。
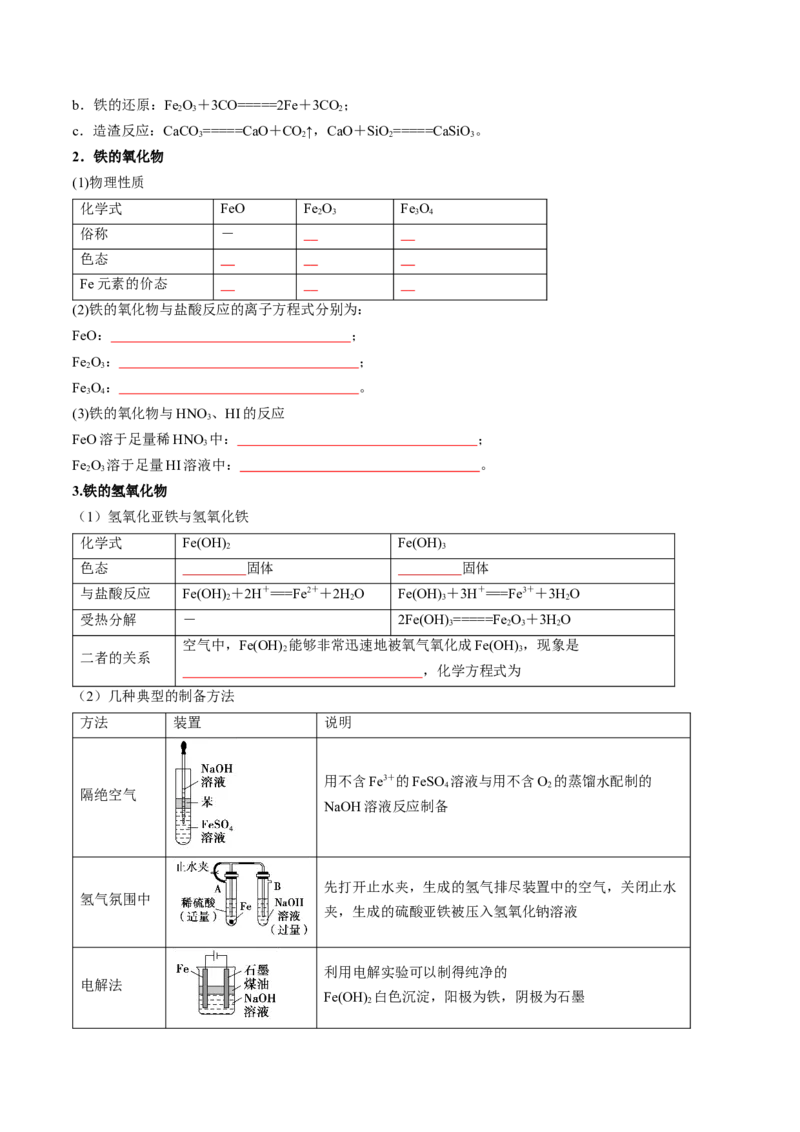
(2)化学性质
按要求书写下列反应的方程式:
①Fe与Cl、S反应的化学方程式: 。
2
②Fe与水蒸气的反应: 。
③与氧化性酸(如HNO)的反应(写离子方程式)。
3
酸 化学方程式或现象
Fe不足 Fe+4H++NO===Fe3++NO↑+2HO
2
稀HNO
3
Fe过量 3Fe+8H++2NO===3Fe2++2NO↑+4HO
2
浓HNO、浓HSO 常温下
3 2 4
④与某些盐溶液的反应
与CuSO 溶液反应的离子方程式: 。
4
与FeCl 溶液反应的离子方程式: 。
3
(3)生铁的冶炼
①原料:铁矿石、焦炭、空气、石灰石。
②设备:高炉。
③主要反应
a.还原剂(CO)的生成:C+O=====CO,CO+C=====2CO;
2 2 2b.铁的还原:Fe O+3CO=====2Fe+3CO;
2 3 2
c.造渣反应:CaCO =====CaO+CO↑,CaO+SiO=====CaSiO 。
3 2 2 3
2.铁的氧化物
(1)物理性质
化学式 FeO Fe O Fe O
2 3 3 4
俗称 -
色态
Fe元素的价态
(2)铁的氧化物与盐酸反应的离子方程式分别为:
FeO: ;
Fe O: ;
2 3
Fe O: 。
3 4
(3)铁的氧化物与HNO、HI的反应
3
FeO溶于足量稀HNO 中: ;
3
Fe O 溶于足量HI溶液中: 。
2 3
3.铁的氢氧化物
(1)氢氧化亚铁与氢氧化铁
化学式 Fe(OH) Fe(OH)
2 3
色态 固体 固体
与盐酸反应 Fe(OH) +2H+===Fe2++2HO Fe(OH) +3H+===Fe3++3HO
2 2 3 2
受热分解 - 2Fe(OH) =====Fe O+3HO
3 2 3 2
空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH) ,现象是
2 3
二者的关系
,化学方程式为
(2)几种典型的制备方法
方法 装置 说明
用不含Fe3+的FeSO 溶液与用不含O 的蒸馏水配制的
4 2
隔绝空气
NaOH溶液反应制备
先打开止水夹,生成的氢气排尽装置中的空气,关闭止水
氢气氛围中
夹,生成的硫酸亚铁被压入氢氧化钠溶液
利用电解实验可以制得纯净的
电解法
Fe(OH) 白色沉淀,阳极为铁,阴极为石墨
2请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)铁的化学性质比较活泼,所以铁在自然界中全部以化合态形式存在。( )
(2)Fe分别与氯气和盐酸反应所得氯化物相同。( )
(3)Fe与稀HNO、稀HSO 反应均有气泡产生,说明Fe与两种酸均发生置换反应。( )
3 2 4
(4)常温下可用铁制容器储存、运输浓硝酸、浓硫酸。( )
(5)铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe O。( )
3 4
(6)氧化铁能与酸反应,所以可用于制作红色颜料。( )
(7)Fe O 可用FeO·Fe O 表示,故Fe O 为混合物。( )
3 4 2 3 3 4
(8)在空气中,白色的Fe(OH) 迅速转变成灰绿色,最终变成红褐色。( )
2
(9)氢氧化铁与HI溶液反应的离子方程式为Fe(OH) +3H+===Fe3++3HO。( )
3 2
(10)Fe O 不能与水反应生成Fe(OH) ,所以不能通过化合反应生成Fe(OH) 。( )
2 3 3 3
考向01 考查铁的性质
【例1】(2024·江苏泰州·模拟)铁及其化合物的转化具有重要应用。在指定条件下,下列物质间转化能实
现的是
A.
B.
C.
D.
【思维建模】
(1)铁的氧化规律
铁与弱氧化剂(如S、FeCl 、CuSO 、I 等)反应时被氧化为Fe2+,铁与强氧化剂(如Cl 、Br 、HNO 、浓
3 4 2 2 2 3
HSO 等)反应时被氧化为Fe3+。
2 4
(2)铁与酸反应的规律
①Fe与一般酸反应时只生成Fe2+,与氧化性酸(HNO)反应时Fe少量生成Fe3+,Fe过量生成Fe2+。
3
②Fe与浓硫酸、浓硝酸作用时常温钝化(形成致密氧化膜),加热可以持续反应。
考向02 考查铁的氧化物
【例2】(2024·江苏南京·二模)关于铁的三种氧化物(FeO、Fe O、Fe O)的下列叙述中正确的是( )
2 3 3 4
A.铁的三种氧化物中铁元素的化合价完全相同
B.都是碱性氧化物,都能与盐酸反应生成氯化铁和水
C.氧化亚铁在空气中加热可生成更稳定的四氧化三铁D.四氧化三铁中铁元素有+2价和+3价,它是一种混合物
考向03 考查铁的氢氧化物
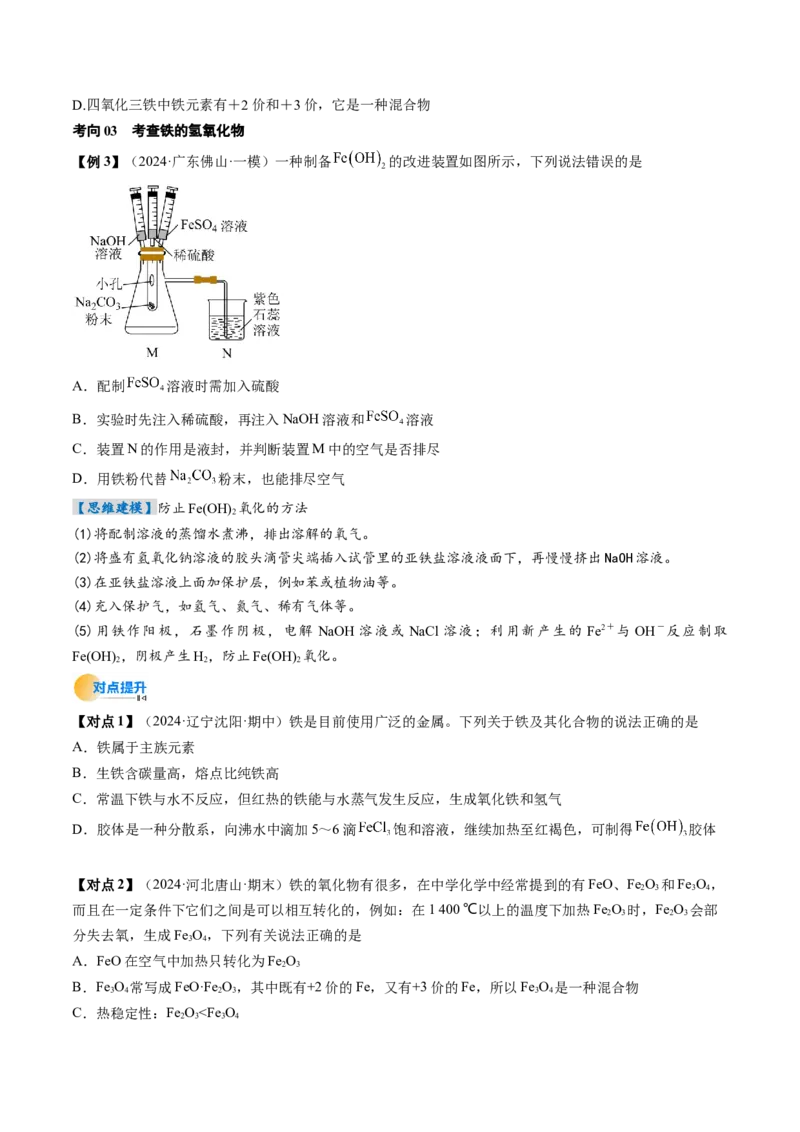
【例3】(2024·广东佛山·一模)一种制备 的改进装置如图所示,下列说法错误的是
A.配制 溶液时需加入硫酸
B.实验时先注入稀硫酸,再注入NaOH溶液和 溶液
C.装置N的作用是液封,并判断装置M中的空气是否排尽
D.用铁粉代替 粉末,也能排尽空气
【思维建模】防止Fe(OH) 氧化的方法
2
(1)将配制溶液的蒸馏水煮沸,排出溶解的氧气。
(2)将盛有氢氧化钠溶液的胶头滴管尖端插入试管里的亚铁盐溶液液面下,再慢慢挤出NaOH溶液。
(3)在亚铁盐溶液上面加保护层,例如苯或植物油等。
(4)充入保护气,如氢气、氮气、稀有气体等。
(5)用铁作阳极,石墨作阴极,电解 NaOH 溶液或 NaCl 溶液;利用新产生的 Fe2+与 OH-反应制取
Fe(OH) ,阴极产生H,防止Fe(OH) 氧化。
2 2 2
【对点1】(2024·辽宁沈阳·期中)铁是目前使用广泛的金属。下列关于铁及其化合物的说法正确的是
A.铁属于主族元素
B.生铁含碳量高,熔点比纯铁高
C.常温下铁与水不反应,但红热的铁能与水蒸气发生反应,生成氧化铁和氢气
D.胶体是一种分散系,向沸水中滴加5~6滴 饱和溶液,继续加热至红褐色,可制得 胶体
【对点2】(2024·河北唐山·期末)铁的氧化物有很多,在中学化学中经常提到的有FeO、Fe O 和Fe O,
2 3 3 4
而且在一定条件下它们之间是可以相互转化的,例如:在1 400 ℃以上的温度下加热Fe O 时,Fe O 会部
2 3 2 3
分失去氧,生成Fe O,下列有关说法正确的是
3 4
A.FeO在空气中加热只转化为Fe O
2 3
B.Fe O 常写成FeO·Fe O,其中既有+2价的Fe,又有+3价的Fe,所以Fe O 是一种混合物
3 4 2 3 3 4
C.热稳定性:Fe O