文档内容
考点 13 钠及其化合物
(好题冲关)
【基础过关】
1.(2023·广东省汕头市二模)2023年1月23日,汕头迎春大型焰火晚会点亮了汕头湾,为汕头发展注
入强心剂。下列焰火颜色与钾元素相关的是( )
A.黄色 B.紫色 C.绿色 D.洋红色
【答案】B
【解析】钾的焰色为紫色火焰,所以B正确;故选B。
2.(2023·重庆市高三三模)向下列物质中加入NaOH溶液并加热,其成分不发生改变的是( )
A.用聚四氟乙烯制成的实 B.用于通信的光导 C.用于焙制糕点的小 D.从餐厨废弃物中提取
验仪器 纤维 苏打 的地沟油
【答案】A
【解析】A项,聚四氟乙烯不和氢氧化钠溶液反应,故A符合题意;B项,光导纤维的主要成分是二氧
化硅,二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,离子方程式为SiO+2OH- =SiO 2-+H O,故B不符
2 3 2
合题意;C项,小苏打的主要成分是碳酸氢钠,碳酸氢钠与氢氧化钠反应生成碳酸钠和水,离子方程式为:
HCO -+OH-=CO 2-+H O,故C不符合题意;D项,“地沟油”的成分是油脂,与碱溶液反应生成高级脂肪
3 3 2
酸盐和甘油,故D不符合题意;故选A。
3.下列关于钠的化合物的说法中,正确的是( )
A.NaCO 和NaHCO 均能与盐酸和NaOH溶液反应
2 3 3
B.NaCO 固体中含有的NaHCO 可用加热的方法除去
2 3 3
C.NaO 和NaO均为白色固体,与CO 反应均放出O
2 2 2 2 2
D.分别向NaO 和NaO与水反应后的溶液中立即滴入酚酞溶液,两者的现象相同
2 2 2
【答案】B
【解析】NaCO 不能与NaOH反应,A项错误;NaHCO 加热分解生成NaCO ,可以用加热的方法除
2 3 3 2 3
去NaCO 固体中含有的 NaHCO ,B项正确;NaO 是淡黄色固体,与 CO 反应生成NaCO 与O ,但
2 3 3 2 2 2 2 3 2
NaO与CO 反应生成NaCO,没有氧气生成,C项错误;NaO 与水反应生成NaOH与O,反应后的溶液
2 2 2 3 2 2 2
中含有过氧化氢,过氧化氢具有强氧化性,立即滴入酚酞,现象是溶液先变红,后退色,NaO与水反应生
2
成NaOH,滴入酚酞,溶液变为红色,现象不相同,D项错误。
资料收集整理【淘宝店铺:向阳百分百】4.下列有关NaO和NaO 的叙述中,正确的是( )
2 2 2
A.NaO比NaO 稳定
2 2 2
B.只用水来确定某NaO粉末中是否含有NaO
2 2 2
C.NaO、NaO 分别与CO 反应,产物相同
2 2 2 2
D.将足量的NaO 比NaO分别加到酚酞溶液中,最终溶液均为红色
2 2 2
【答案】B
【解析】A项,NaO在空气中加热时会转化为NaO,故NaO 比NaO稳定,故A错误; B项,
2 2 2 2 2 2
NaO 与水反应会产生气泡,有明显的现象,所以可用水来确定某NaO粉末中是否含有NaO,故B正确;
2 2 2 2 2
C项,NaO与CO 反应生成碳酸钠,NaO 与CO 反应生成碳酸钠和氧气,产物不同,故C错误; D项,
2 2 2 2 2
NaO、NaO 加到酚酞溶液中,二者均先与溶液中的水反应生成碱而使溶液变为红色,但NaO 具有漂白
2 2 2 2 2
性,又会将红色溶液漂白,故D错误;故选B。
5.下列关于NaHCO 和NaCO 的描述不正确的是( )
3 2 3
A.NaHCO 俗称小苏打
3
B.NaCO 溶液显碱性,所以NaCO 属于碱
2 3 2 3
C.热稳定性:NaHCO <NaCO
3 2 3
D.等物质的量的NaHCO 和NaCO 分别与足量盐酸反应,生成的CO 的量相等
3 2 3 2
【答案】B
【解析】A项,NaHCO 是碳酸与氢氧化钠形成的酸式盐,俗称小苏打,A正确;B项,尽管NaCO
3 2 3
溶液显碱性,但NaCO 电离产生金属阳离子和酸根阴离子,因此属于盐而不是属于碱,B错误;C项,
2 3
NaHCO 不稳定,受热反应产生NaCO、CO、HO,NaCO 受热不分解,因此物质的热稳定性:NaHCO
3 2 3 2 2 2 3 3
<NaCO,C正确;D项,等物质的量的NaHCO 和NaCO 中含有的C的物质的量相同,因此二者分别与
2 3 3 2 3
足量盐酸反应,根据C元素守恒可知反应生成的CO 的量相等,D正确;故选B。
2
6.下列关于钠及其化合物的说法中错误的是( )
A.碳酸氢钠药片是抗酸药,服用时喝些醋能提高药效
B.NaO 与CO 反应放出氧气,可用于制作呼吸面具
2 2 2
C.分别将少量钠投入到盛有水和乙醇的烧杯中,可比较水与乙醇中氢的活泼性
D.用铂丝蘸取某溶液灼烧,火焰呈黄色,证明其中含有
【答案】A
【解析】A项,碳酸氢钠能与醋酸反应,服用碳酸氢钠时喝些醋能会使药效降低,故A错误;B项,
NaO 与CO 反应放出氧气,可以用作供氧剂,可用于制作呼吸面具,故B正确;C项,钠和水反应较剧
2 2 2
烈,和乙醇反应比较缓慢,故分别将少量钠投入到盛有水和乙醇的烧杯中,可比较水与乙醇中氢的活泼性,
故C正确;D项,钠的焰色反应为黄色,用铂丝蘸取某溶液灼烧,且钠元素在溶液只能以离子形式存在,
资料收集整理【淘宝店铺:向阳百分百】火焰呈黄色,证明其中含有Na+,故D正确;故选A。
7.用铂丝蘸取某混合液进行焰色实验,下列说法正确的是( )
A.焊在玻璃棒上的铂丝可用光洁无锈的铁丝代替
B.焰色反应有发光现象,所以是化学变化
C.透过蓝色钴玻璃观察到紫色火焰,证明原溶液有钾元素无钠元素
D.每次实验结束可用水洗净铂丝并在外焰上灼烧至没有颜色
【答案】A
【解析】A项,洁净的铁丝,放在酒精灯上灼烧至无色,本身并无颜色,可用来进行颜色反应,故A
正确;B项,焰色反应是某些金属元素在灼烧时表现的性质,属于物理变化,故B错误;C项,透过蓝色
钴玻璃的目的是滤去黄光的干扰,所以透过蓝色钴玻璃观察到紫色火焰,证明原溶液有钾元素,但不能说
明没有钠元素,故C错误;D项,不能用水洗净铂丝,应该用盐酸,盐酸易挥发,其盐高温时也易挥发,
铂丝蘸盐酸灼烧时,盐酸及其盐可一起挥发掉,可以达到洗净的目的,故D错误;故选A。
8.NaCl 是一种化工原料,可以制备一系列物质。下列说法正确的是
A.25℃,NaHCO 在水中的溶解度比 NaCO 的大
3 2 3
B.石灰乳与 Cl 的反应中,Cl 既是氧化剂,又是还原剂
2 2
C.常温下干燥的 Cl 能用钢瓶贮存
2
D.如图所示转化反应都是氧化还原反应
【答案】BC
【解析】A项,25℃,饱和碳酸钠溶液中通入二氧化碳生成碳酸氢钠晶体,则NaHCO 在水中的溶解
3
度比NaCO 的小,故A错误;B项,石灰乳与Cl 的反应为2Ca(OH) +2Cl=Ca(ClO) +CaCl +2H O,反应
2 3 2 2 2 2 2 2
中Cl的化合价既升高又降低,故Cl 既是氧化剂,又是还原剂,故B正确;C项,常温下干燥的Cl 与Fe
2 2
不反应,故能用钢瓶贮存,故C正确;D项,图中转化:NaCl+NH +H O+CO=NHCl+NaHCO ,2NaHCO
3 2 2 4 3 3
NaCO+H O+CO↑均为非氧化还原反应,故D错误;故选BC。
2 3 2 2
9.(2023·天津市和平区高三模拟)侯德榜是我国杰出的化学家,“侯氏制碱法”的创始人。1926年,
塘沽“红三角”牌纯碱在万国博览会获金质奖章。反应:NaCl +CO +NH+H O= NHCl+ NaHCO ↓,是
2 3 2 4 3
“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解,其中不正确的是(
)
资料收集整理【淘宝店铺:向阳百分百】A.小韩同学说:该条件下NaHCO 的溶解度较小
3
B.小韦同学说:NaHCO 不是纯碱
3
C.小羊同学说:析出NaHCO 固体后的溶液中只含氯化铵,可做化肥
3
D.小任同学说:该反应是在饱和食盐水中先通入氨气,再通入二氧化碳
【答案】C
【解析】A项,反应中只有碳酸氢钠沉淀生成,所以该条件下NaHCO 的溶解度较小,首先达到饱和
3
析出,故A正确;B项,纯碱是NaCO,NaHCO 是小苏打,故B正确;C项,析出 NaHCO 固体后的溶
2 3 3 3
液仍是NaHCO 的饱和溶液,含氯化铵、NaHCO 等,故C错误;D项,在饱和食盐水中先通入氨气使溶
3 3
液呈碱性,再通入二氧化碳,增大二氧化碳的溶解度,故D正确;故选C。
10.某些氧化物在一定条件下能与NaO 反应,且反应极有规律,如NaO+SO=Na SO 、
2 2 2 2 2 2 4
2NaO+2SO(g)= 2Na SO +O ,。据此判断下列反应方程式错误的是( )
2 2 3 2 4 2
A.2NaO+2N O=4NaNO +O B.NaO+2NO=2NaNO
2 2 2 3 2 2 2 2 2 3
C.2NaO+2N O═4NaNO+O D.2NaO+2Mn O=4NaMnO+O
2 2 2 5 3 2 2 2 2 7 4 2
【答案】A
【解析】根据题给信息可知:NaO 可与某些元素的最高价氧化物反应,生成对应的盐(或碱)和O,
2 2 2
NaO 具有强氧化性,与所含元素不是最高价态的氧化物反应时,生成其最高价的盐,而不生成O。A项,
2 2 2
NO 中的氮也不是最高价,所以不产生氧气,不符合上述规律,故A错误;B项,NO 中N元素的化合价
2 3 2
为+4价,不是最高价态,与NaO 反应时不生成O,反应的化学方程式为NaO+2NO=2NaNO ,故B正
2 2 2 2 2 2 3
确;C项,NO 中N元素的化合价为+5价,是最高价态,与NaO 反应时生成O,反应的化学方程式为
2 5 2 2 2
2NaO+2N O═4NaNO+O ,故C正确;D项,MnO 中Mn元素的化合价为+7价,处于最高价态,与
2 2 2 5 3 2 2 7
NaO 反应时生成O,反应的化学方程式为2NaO+2Mn O=4NaMnO+O ,故D正确;故选A。
2 2 2 2 2 2 7 4 2
11.下列钠及其化合物的性质与用途具有对应关系的是( )
A.Na有导电性,可用作快中子反应堆的热交换剂
B.NaO 有强氧化性,可用于漂白
2 2
C.NaOH显碱性,可用作干燥剂
D.NaHCO 受热易分解,可用于治疗胃酸过多
3
【答案】B
【解析】A项,因为钠为金属,具有良好的导热性,所以可用作快中子反应堆的热交换剂,A错误;B
资料收集整理【淘宝店铺:向阳百分百】项,NaO 具有漂白性,是因为其具有强氧化性,B正确;C项,NaOH具有吸水性,而作干燥剂,C错误;
2 2
D项,NaHCO 可以与胃酸中的HCl反应,故可用于治疗胃酸过多,D错误。故选B。
3
12.将一定量的NaHCO 和NaO 的混合物置于密闭容器中充分加热,反应中转移电子的物质的量为
3 2 2
1mol,下列说法一定正确的是( )
A.容器中一定有0.5molO
2
B.反应后,容器中一定没有HO
2
C.反应后,容器中的固体只有NaCO
2 3
D.混合物中NaHCO 和NaO 的物质的量一定相等
3 2 2
【答案】A
【解析】加热时NaHCO 分解:2NaHCO NaCO+CO ↑+H O,然后发生:
3 3 2 3 2 2
2NaO+2CO =2Na CO+O 、2NaO+2H O=4NaOH+O ↑,由方程式可知,转移1mol电子,则生成
2 2 2 2 3 2 2 2 2 2
0.5molO,可知反应1molNa O,如过氧化钠过量,则产物生成NaCO 和NaOH,如过氧化钠不足,则产
2 2 2 2 3
物为NaCO,可能有NaOH,不一定有水。故选A。
2 3
13.为探究NaO 与HO的反应,某学习小组将1~2mL水滴入盛有1~2g过氧化钠固体的试管中,下
2 2 2
列有关说法不正确的是( )
A.该实验可以用带火星的木条来检验生成的气体是否为氧气
B.该实验可以直接用手轻轻触摸试管外壁来感受反应的热效应
C.该实验可以用pH试纸来检验生成的溶液是否显碱性
D.该实验可以说明过氧化钠可在潜水艇中作为氧气的来源
【答案】C
【解析】A项,带火星的木条复燃,可检验NaO 与HO反应生成氧气,故A正确;B项,NaO 与
2 2 2 2 2
HO反应放出热量,用手轻轻触摸试管外壁来感受反应的热效应,故B正确;C项,NaO 与HO反应生
2 2 2 2
成过氧化物,具有漂白性,pH试纸颜色漂白,不能检验溶液的酸碱性,故C错误;D项,NaO 与HO反
2 2 2
应生成氧气,可在潜水艇中作为氧气的来源,故D正确;故选C。
14.为除去括号内的杂质,所选用的试剂或方法错误的是( )
A.CO 气体(HCl):饱和NaHCO 溶液
2 3
B.NaCO 固体(NaHCO ):加热至不再产生气体
2 3 3
C.NaHCO 溶液(Na CO):通过量CO
3 2 3 2
D.NaCO 溶液(Na SO ):加入适量Ba(OH) 溶液,过滤
2 3 2 4 2
【答案】D
【解析】A项,二氧化碳与碳酸氢钠不反应,氯化氢能与碳酸氢钠反应生成二氧化碳,故A正确;B
项,碳酸氢钠加热分解生成碳酸钠,碳酸钠受热不分解,则加热法可除杂,故B正确;C项,碳酸钠溶液
资料收集整理【淘宝店铺:向阳百分百】吸收二氧化碳转化为碳酸氢钠,则用二氧化碳能除去碳酸氢钠溶液中的碳酸钠,故C正确;D项,二者都
与氢氧化钡反应生成沉淀,主要物质也被除去了,故D错误;故选D。
15.金属钠溶解于液氨中形成氨合钠离子和氨合电子,向该溶液中加入穴醚类配体L,得到首个含碱
金属阴离子的黄金化合物[NaL]+Na-。下列说法错误的是( )
A.Na-的半径比Mg大 B.钠的液氨溶液有强的还原性
C.Na-的第一电离能比H-大 D.该事实表明钠也可表现非金属性
【答案】C
【解析】A项,已知Na-与Mg具有相同的核外电子排布,且Na的核电荷数小于Mg,则Na-的半径比
Mg大,A正确;B项,由题干信息可知,钠的液氨溶液中形成氨合钠离子和氨合电子,其中氨合电子具有
强还原性,B正确;C项,由于H-形成有2个电子的稳定结构,而Na-核外最外形上是2个电子的不稳定结
构,则 Na-的第一电离能比H-小,C错误; D项,由题干信息可知,Na也可以形成Na-,则说明Na也可
以结合电子形成阴离子,即该事实表明钠也可表现非金属性,D正确;故选C。
16.已知甲、乙、丙三种物质均含有同种元素X,其转化关系如下:
的
下列说法错误 是( )
A.若A为NaOH溶液,乙为白色沉淀,则X可能为短周期金属元素
B.若A为硝酸,X为金属元素,则甲与乙反应可生成丙
C.若A为氧气,丙在通常状况下为红棕色气体,则甲可能为非金属单质
D.若乙为NaHCO ,则甲或丙可能是CO
3 2
【答案】B
【解析】A项,若A为NaOH溶液,甲是AlCl ,乙是Al(OH) 白色沉淀,丙是NaAlO ,X为短周期
3 3 2
金属元素铝,符合题意,A正确;B项,若A为硝酸,X为金属元素,X应是变价金属,则甲是Fe,乙是
Fe(NO ) ,丙是Fe(NO ) ,甲与乙不反应,B错误;C项,若A为氧气,丙在通常状况下为红棕色气体即
3 2 3 3
NO ,则甲是N ,乙是NO,C正确;D项,若乙为NaHCO ,甲是CO ,A是NaOH,丙是NaCO ,或者
2 2 3 2 2 3
甲是NaCO,乙是NaHCO ,A是HCl,丙是CO,D正确。故选B。
2 3 3 2
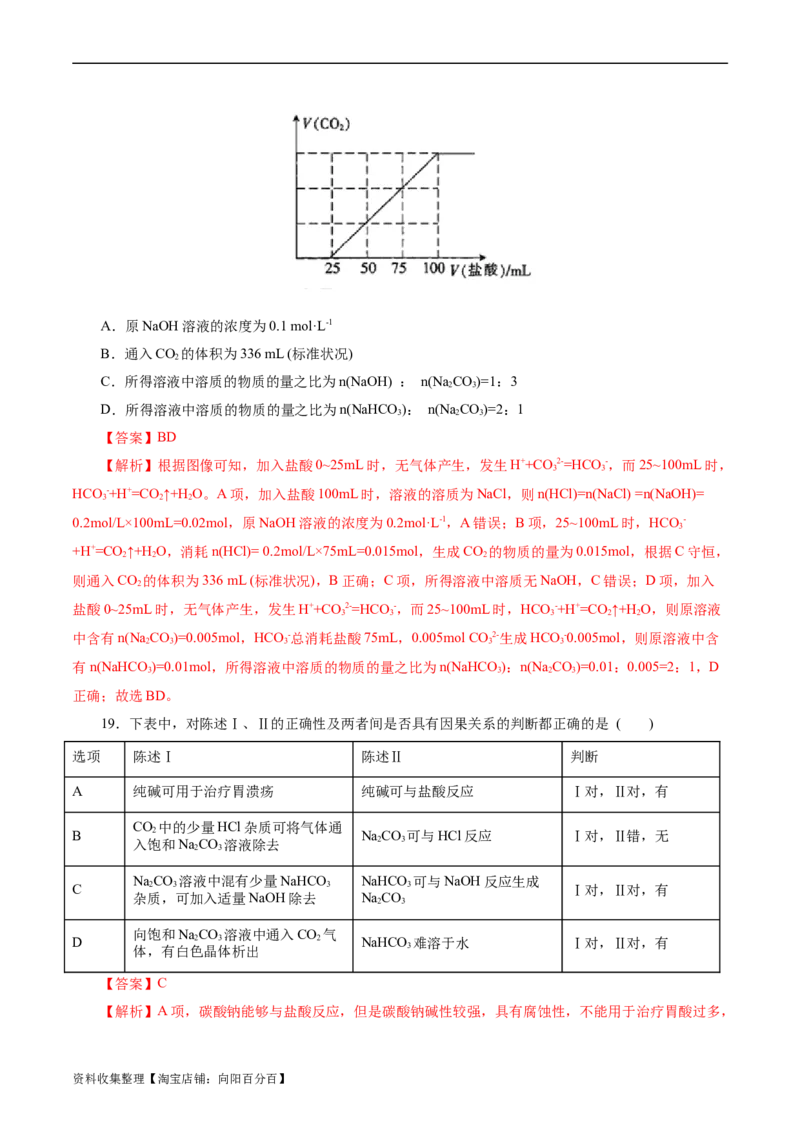
17.向体积均为10mL且物质的量浓度相同的两份NaOH溶液中分别通入一定量的CO 得到溶液甲和
2
乙。向甲、乙两溶液中分别滴加0.1 mol·L-1盐酸。此时反应生成CO 体积(标准状况)与所加盐酸体积间的关
2
系如图所示。则下列叙述中正确的是( )
资料收集整理【淘宝店铺:向阳百分百】A.乙溶液中含有的溶质是NaCO、NaHCO
2 3 3
B.当0