文档内容
考点 15 氮及其化合物
目录
................................................................................................................................................1
1.高考真题考点分布......................................................................................................................................1
2.命题规律及备考策略..................................................................................................................................1
................................................................................................................................................2
考法01 氮及其氧化物 硝酸......................................................................................................................2
考法02 氨 铵盐..........................................................................................................................................7
考法03 氮及其化合物的转化关系...........................................................................................................10
..............................................................................................................................................12
1.高考真题考点分布
考点内容 考点分布
氮及其氧化物 2023湖北卷1题,3分;2022天津卷4题,3分;2022北京卷12题,4分;
2023新课标卷12题,6分;2023辽宁卷3题,3分;2023浙江1月5题,2分;
氨气、铵盐
2022天津卷4题,3分;2021全国甲卷9题,6分;2021浙江1月10题,2分
硝酸的性质 2024·湖北卷8题,3分;2023山东卷2题,2分;2022山东卷12题,4分;
不同价态氮的 2023湖南卷1题,3分;2022江苏卷8题,3分;2022北京卷12题,3分;
物质相互转化 2022湖南卷9题,3分;2021河北卷10题,3分;2021浙江6月16题,2分
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,氮的固定、氮氧化物性质、硝酸、氨气、铵盐仍是高考命题的热
点。
【备考策略】
氮元素“价-类”二维图【命题预测】
预计2025年高考会以新的情境载体考查氨气、铵盐的性质及用途、掌握氨气的实验室制法、含氮化合物的
转化、有关硝酸的实验和计算等知识,题目难度一般适中。
考法01 氮及其氧化物 硝酸
1.氮的固定
2.氮气
(1)物理性质: 色 味的气体,密度比空气略小, 溶于水。
(2)化学性质
① 。
② 。
③ 。
3.氮的氧化物
(1)氮有多种价态的氧化物,氮元素从+1→+5价都有对应的氧化物,如NO、NO、NO、NO (或NO)、
2 2 3 2 2 4
NO,其中属于酸性氧化物的是NO、NO。
2 5 2 3 2 5
(2)NO和NO 的比较
2
性质 NO NO
2
色、味、态 的气体 的气体
水溶性 溶于水 溶于水毒性 有毒,大气污染物之一 有毒,大气污染物之一
与水反应 不反应
与氧气反应 不反应
4.硝酸物理性质
硝酸是 、 挥发、 气味的液体。
5.硝酸化学性质
(1)不稳定性
反应: 。
(2)强氧化性
硝酸无论浓、稀都具有强氧化性,而且浓度越大,氧化性越强。
①与金属反应
稀硝酸与铜反应的化学方程式: ;
浓硝酸与铜反应的化学方程式: 。
②与非金属反应
浓硝酸与C反应的化学方程式: 。
③与还原性化合物反应
硝酸可氧化HS、SO 、NaSO 、HI、Fe2+等还原性物质。
2 2 2 3
稀硝酸与FeSO 溶液反应的离子方程式: 。
4
(3)与有机物反应
①硝化反应(与 反应):
+HNO――→ +HO。
3 2
②显色反应:含有苯环的蛋白质遇到浓硝酸加热后变黄色。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
1.固氮反应一定属于氧化还原反应( )
2.N 与O 在放电条件下直接化合成NO ( )
2 2 2
3.可用NO 与水反应制取硝酸,故NO 是酸性氧化物( )
2 2
4.NO 通入FeSO 溶液中始终无明显现象( )
2 45.高温、高压、催化剂条件下氮气与氢气反应时,氮气作还原剂( )
6.NO 溶于水时,NO 是氧化剂,水是还原剂( )
2 2
7.NO易溶于水,所以只能用排空气法收集( )
8.试管内壁上的银镜可用稀HNO 除去,也可用氨水除去( )
3
9.浓HNO 和氯水均用棕色试剂瓶保存,其原理相同( )
3
10.浓HNO 溅到皮肤上,皮肤会变黄( )
3
考向01 考查氮氧化物的性质
【例1】1.(2024·北京·三模)在一支 注射器里充入 ,然后吸入 水,用乳胶管和弹簧
夹封住管口,振荡注射器,静置后观察现象①。打开弹簧夹,快速吸入 空气后夹上弹簧夹,观察现
象②。振荡注射器,静置后再观察现象③。
下列关于该过程的分析不正确的是
A.现象①②,主要体现了 难溶于水、还原性
B.现象②③,针筒示数:
C.过程中若将空气 改成 ,③能观察到针筒内无气体剩余
D.此实验启示工业上制硝酸时充入适量 可以提高氮原子利用率
【思维建模】氮氧化物溶于水的问题分析
无论是单一气体(NO ),还是NO、NO 、O 中的两者的混合气体,反应的实质是3NO +HO===2HNO +
2 2 2 2 2 3
NO,2NO+O===2NO,故若有气体剩余只能是NO或O,不可能是NO 。
2 2 2 2
(1)若NO和O 通入水中,总关系式为4NO+3O+2HO===4HNO (4∶3)。
2 2 2 3
(2)若NO 和O 通入水中,总关系式为4NO +O+2HO===4HNO (4∶1)。
2 2 2 2 2 3
(3)NO 、NO、O 三种混合气体通入水中:
2 2
①可先将NO和O 转化为NO ,再按上述各种情况分别处理。
2 2
②也可先将NO 和HO反应转化为NO,再按4NO+3O+2HO===4HNO 情况处理。
2 2 2 2 3
考向02 考查硝酸的性质与用途
【例2】(2024·陕西铜川·模拟预测)实验室利用以下装置配制2 的稀硝酸并制取NO,其中装置及
操作均正确且能达到实验目的的是A.用装置甲制备NO气体 B.用装置乙收集NO气体
C.用装置丙进行NO的尾气吸收 D.用装置丁配制100mL2 溶液
考向03 金属与硝酸反应的计算
【例3】在100 mL 稀HNO 和稀HSO 组成的混合溶液中,两种酸的物质的量浓度之和为0.4 mol·L-1。向
3 2 4
该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中Cu2+的物质的量浓度最大值为(反应前后溶液
体积变化忽略不计)( )
A.0.15 mol·L-1 B.0.24 mol·L-1
C.0.30 mol·L-1 D.0.36 mol·L-1
【思维建模】
(1)金属与硝酸反应计算的思维模型
(2)金属与硝酸反应的计算方法
①电子守恒法:金属失电子数=n(NO )+3n(NO)。
2
②原子守恒法:n(HNO)=xn[M(NO)]+n(NO )+n(NO)(x代表金属元素的化合价)。
3 3 x 2
若向反应后溶液中加入NaOH溶液恰好使Mx+沉淀完全,此时溶质为NaNO ,则存在:
3
n(Na+)=n(NO)=n(HNO)-n(NO)-n(NO )。
3 2
③电荷守恒法:HNO 过量时反应后溶液中(不考虑OH-)有c(NO)=c(H+)+x×c(Mx+)。起酸性作用的HNO
3 3
的物质的量是金属的物质的量和金属所带电荷数的乘积,可表示为 n(HNO) =xn(Mx+)=n(e-)(Mn+代表
3 酸性
金属离子)。
④离子方程式计算法:金属与硫酸、硝酸的混合酸反应时,由于硝酸盐中NO在硫酸提供H+的条件下能继
续与金属反应,故此类题目应用离子方程式来计算3Cu+8H++2NO===3Cu2++2NO↑+4HO。先作过量判
2
断,然后根据完全反应的金属或H+或NO进行相关计算,且要符合电荷守恒。【对点1】(2024·广东·二模)NH 可用作脱硝剂。某科研小组探究NO 被NH 还原的反应,涉及的部分装
3 2 3
置如图所示。
下列说法正确的是
A.用甲装置制备NH
3
B.乙装置中反应的n(还原剂)∶n(氧化剂)=2∶1
C.丙装置盛放无水CaCl 用于干燥NH
2 3
D.在丁装置中为了更好混合反应气体,应先通入NO
2
【对点2】(2024·江西·二模)铜与足量浓硝酸反应的装置如下图所示,下列说法错误的是
A.具支试管A中会出现红棕色气体,溶液呈绿色
B.装置B的作用是缓冲气流并收集
C.该反应体现了浓硝酸的强氧化性和酸性
D.烧杯中反应的离子方程式为
【对点3】(2024·河北唐山·期末)向含x mol HNO 和y mol HSO 的混合稀溶液中缓慢加入铁粉,其氧化产
3 2 4
物与所加铁粉的物质的量关系如图所示:
下列有关说法正确的是( )A.x=0.2,y=0.1
B.a点之前的反应离子方程式为3Fe+8H++2NO===3Fe2++2NO↑+4HO
2
C.向b点所得溶液中加入Cu粉,最多可溶解1.92 g
D.反应至c点,可收集到气体4.48 L(标准状况)
考法02 氨 铵盐
1.氨的结构特征
2.氨的物理性质
无色、有 气味的气体,密度比空气的 ,易 ,液氨可作 ,极易溶于水(1∶700),可由喷
泉实验证明。
3.氨的化学性质
(1)较稳定:N的 强,N—H的 大,因而NH 比较稳定。
3
(2)
(3)较强的配位能力
Cu(OH) 溶于氨水:Cu(OH) +4NH ===[Cu(NH)]2++2OH-。
2 2 3 3 4
(4)还原性
催化氧化:4NH +5O=====4NO+6HO。
3 2 2
4.铵盐
(1)物理性质
铵盐大多数是 固体,绝大多数易溶于水。
(2)化学性质
5.NH的检验步骤
未知液―――→产生使 的红色石蕊试纸变 的气体,则证明含NH。6.氨的实验室制法
(1 ) NH Cl和Ca(OH) 的固体混合物制取氨气
4 2
简易装置示意图如图。
(2)用浓氨水制备氨气
方法 化学方程式(或原理) 发生装置
加热浓氨水
浓氨水+固 NaOH溶于水放热,促使氨水分解,且OH-浓度的增大有利于NH 的放
3
体NaOH 出
浓氨水+固 CaO与水反应,使溶剂(水)减少;反应放热,促使氨水分解。化学方程式
体CaO 为NH ·H O+CaO===NH↑+Ca(OH)
3 2 3 2
请判断下列说法的正误(正确的打“√”,错误的打“×”)
1.向AlCl 溶液中逐滴加入过量的氨水,先产生白色沉淀,最后白色沉淀溶解( )
3
2.氨溶于水显弱碱性是因为氨气分子能电离出OH-( )
3.氨极易溶于水,因此氨水比较稳定(不容易分解)( )
4.氨水和液氨不同,氨水是混合物,液氨是纯净物( )
5.氨水中物质的量浓度最大的粒子是NH ·H O(水除外)( )
3 2
6.加热盛有NH Cl固体的试管,试管底部固体消失,试管口有晶体凝结,说明NH Cl固体可以升华( )
4 4
7.用浓氯化铵溶液处理过的舞台幕布不易着火,其原因是氯化铵分解吸收热量,降低了温度;氯化铵分
解产生的气体隔绝了空气( )
8.草木灰(含KCO)与铵盐混用降低肥效( )
2 3
9.铵盐加热均易分解产生NH ( )
3
10.某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性( )
考向01 氨和铵盐
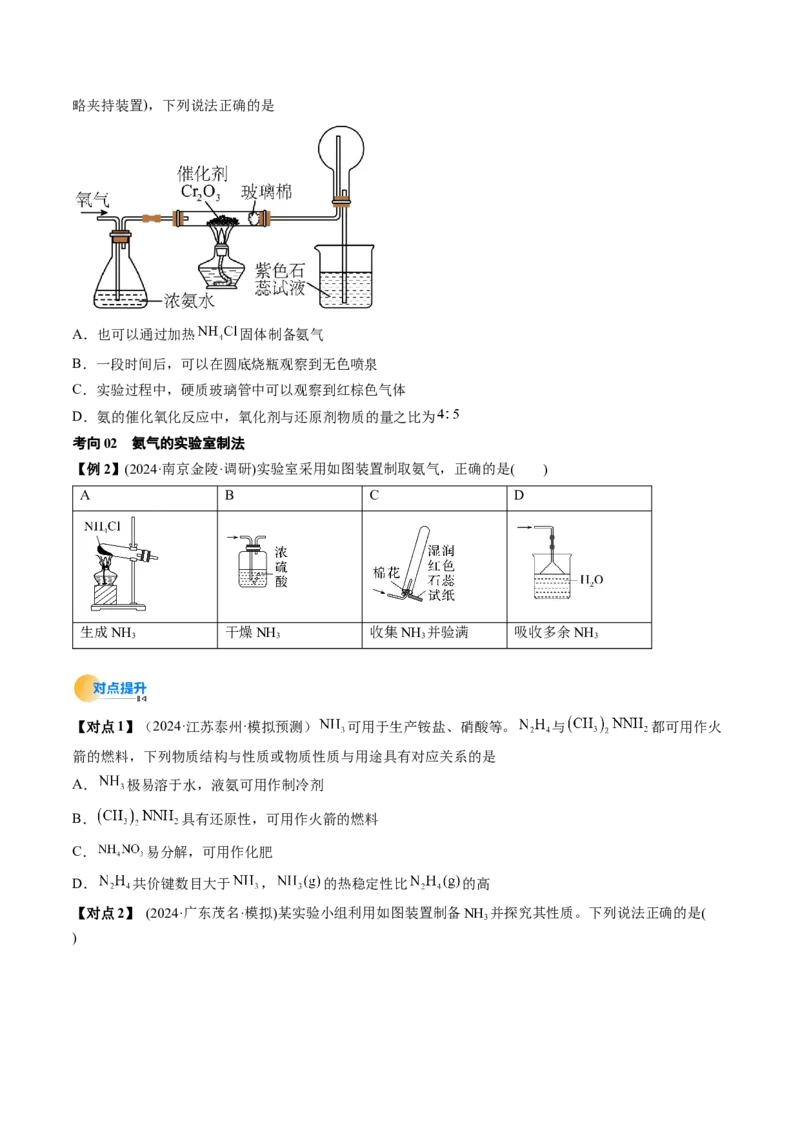
【例1】(2024·广东广州·模拟预测)利用氨的催化氧化原理制备硝酸并进行喷泉实验,装置如图所示(省略夹持装置),下列说法正确的是
A.也可以通过加热 固体制备氨气
B.一段时间后,可以在圆底烧瓶观察到无色喷泉
C.实验过程中,硬质玻璃管中可以观察到红棕色气体
D.氨的催化氧化反应中,氧化剂与还原剂物质的量之比为
考向02 氨气的实验室制法
【例2】(2024·南京金陵·调研)实验室采用如图装置制取氨气,正确的是( )
A B C D
生成NH 干燥NH 收集NH 并验满 吸收多余NH
3 3 3 3
【对点1】(2024·江苏泰州·模拟预测) 可用于生产铵盐、硝酸等。 与 都可用作火
箭的燃料,下列物质结构与性质或物质性质与用途具有对应关系的是
A. 极易溶于水,液氨可用作制冷剂
B. 具有还原性,可用作火箭的燃料
C. 易分解,可用作化肥
D. 共价键数目大于 , 的热稳定性比 的高
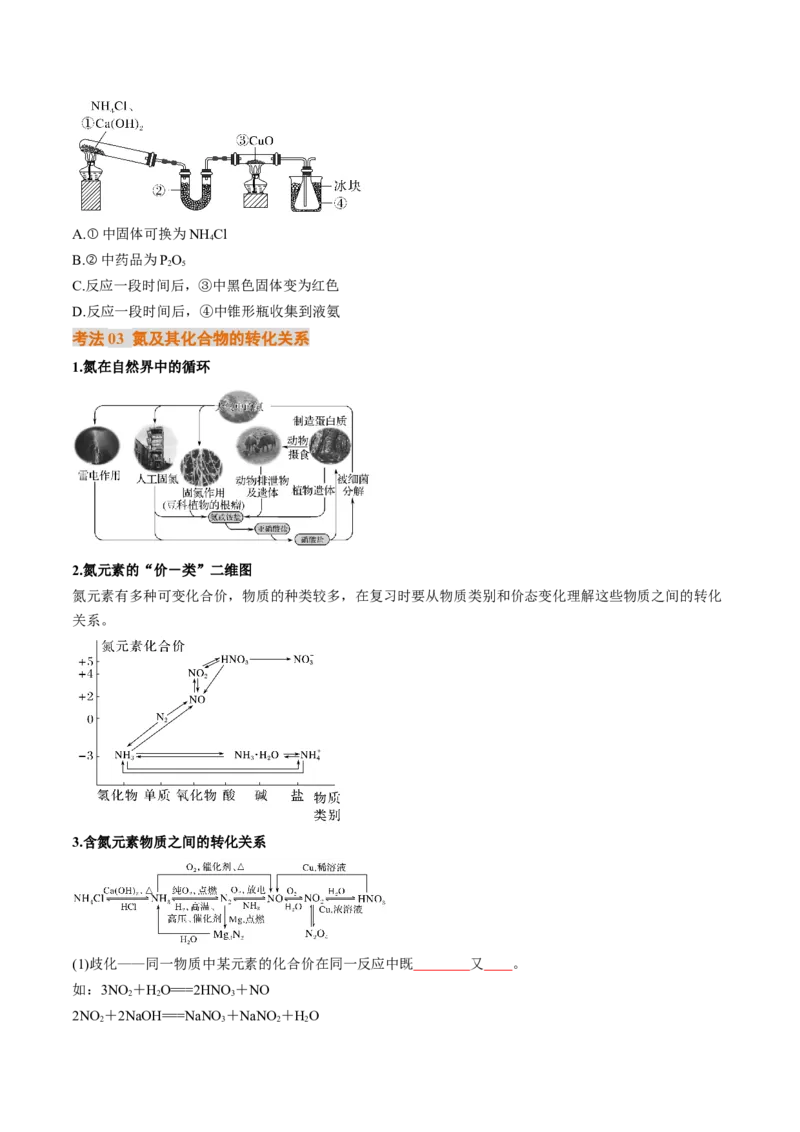
【对点2】 (2024·广东茂名·模拟)某实验小组利用如图装置制备NH 并探究其性质。下列说法正确的是(
3
)A.①中固体可换为NH Cl
4
B.②中药品为PO
2 5
C.反应一段时间后,③中黑色固体变为红色
D.反应一段时间后,④中锥形瓶收集到液氨
考法03 氮及其化合物的转化关系
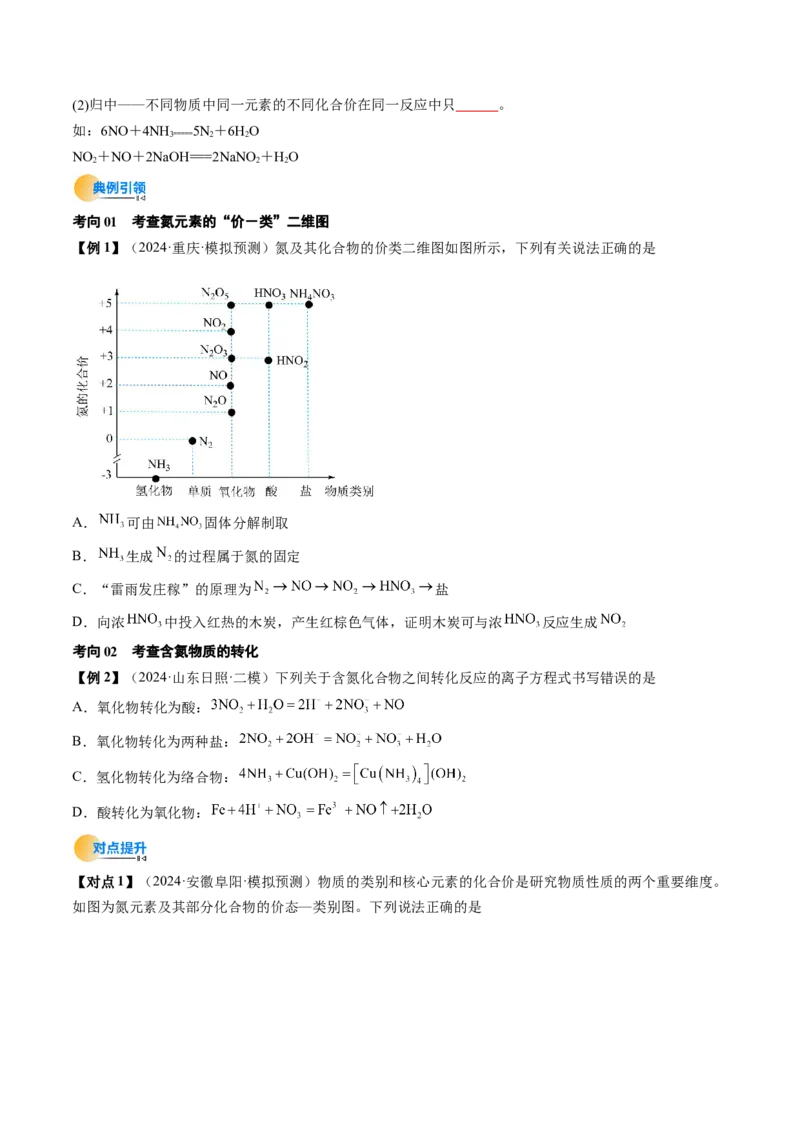
1.氮在自然界中的循环
2.氮元素的“价-类”二维图
氮元素有多种可变化合价,物质的种类较多,在复习时要从物质类别和价态变化理解这些物质之间的转化
关系。
3.含氮元素物质之间的转化关系
(1)歧化——同一物质中某元素的化合价在同一反应中既 又 。
如:3NO +HO===2HNO +NO
2 2 3
2NO +2NaOH===NaNO +NaNO +HO
2 3 2 2(2)归中——不同物质中同一元素的不同化合价在同一反应中只 。
如:6NO+4NH 5N+6HO
3===== 2 2
NO +NO+2NaOH===2NaNO +HO
2 2 2
考向01 考查氮元素的“价-类”二维图
【例1】(2024·重庆·模拟预测)氮及其化合物的价类二维图如图所示,下列有关说法正确的是
A. 可由 固体分解制取
B. 生成 的过程属于氮的固定
C.“雷雨发庄稼”的原理为 盐
D.向浓 中投入红热的木炭,产生红棕色气体,证明木炭可与浓 反应生成
考向02 考查含氮物质的转化
【例2】(2024·山东日照·二模)下列关于含氮化合物之间转化反应的离子方程式书写错误的是
A.氧化物转化为酸:
B.氧化物转化为两种盐:
C.氢化物转化为络合物:
D.酸转化为氧化物:
【对点1】(2024·安徽阜阳·模拟预测)物质的类别和核心元素的化合价是研究物质性质的两个重要维度。
如图为氮元素及其部分化合物的价态—类别图。下列说法正确的是A.图中各物质均参与自然界循环
B.c、d均为酸性氧化物
C.f不能检验氯气管道是否漏气
D.实验室可用g的固体与NaOH固体加热制备f
【对点2】(2024·湖北黄石·一模)工业制取硝酸的过程如下图:
下列说法正确的是
A.工业上的转化①使用的催化剂为VO
2 5
B.转化②中,每生成1molNO,转移电子数目为10N
A
C.NO、NO 的混合气体能被足量烧碱溶液完全吸收的条件是n(NO)≤n(NO)
2 2
D.转化④中,相同条件下V(NO):V(O )=4:3时,理论上NO 全部转化为HNO
2 2 2 3
1.下列有关硝酸的说法正确的是( )
A.工业硝酸的质量分数约为69%,常因溶有少量NO而略显黄色
B.硝酸是一种氧化性很强的酸,可以与金、铂等金属反应
C.将木炭放入浓硝酸中,可立即观察到有气泡生成
D.工业制备硝酸第三步为用水吸收二氧化氮生成硝酸
2.(2023·湖南邵阳·二模)实验室制取少量 ,下列方法不能达到目的的是
A.加热分解氯化铵固体
B.加热分解浓氨水
C.将浓氨水滴入到碱石灰上
D.加热氯化铵和氢氧化钙的固体混合物
3.(2024·河北·一模)利用下列实验装置能达到相应实验目的的是
选项 A B实验装
置
实验目
除去乙酸乙酯中的乙酸 制备氨气
的
选项 C D
实验装
置
实验目
除去 中的 通过观察气泡验证 能否催化 分解
的
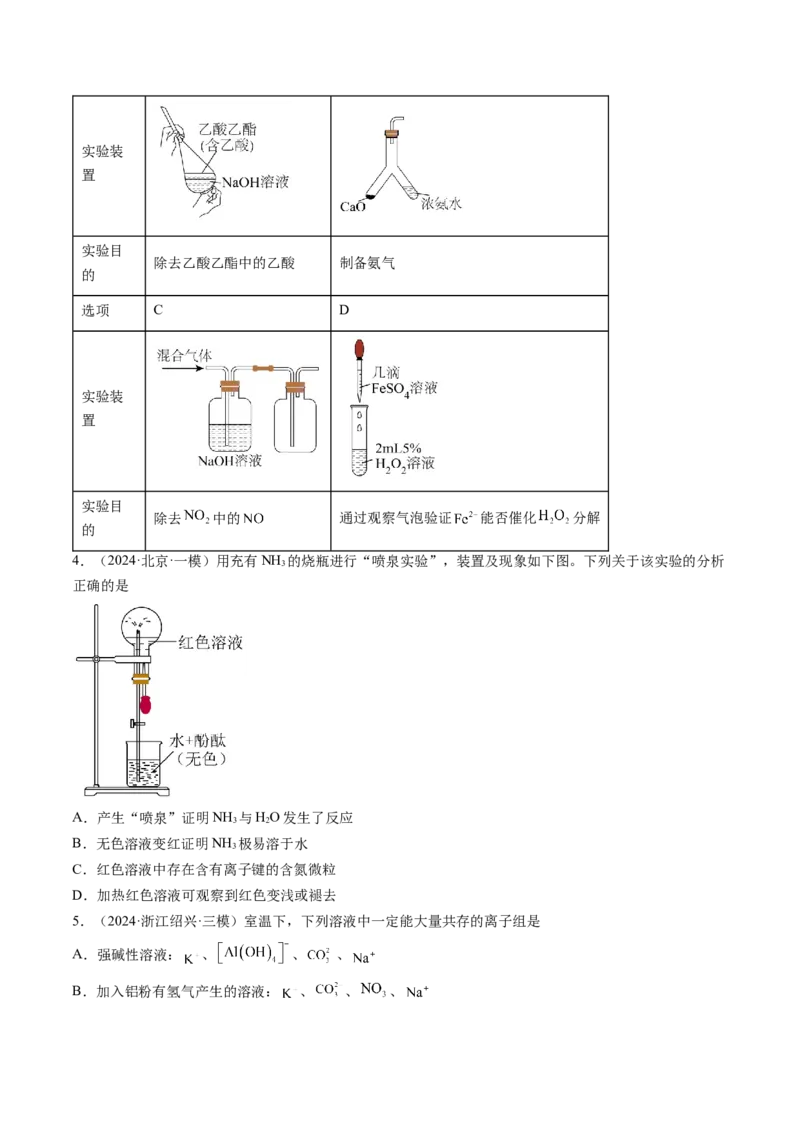
4.(2024·北京·一模)用充有NH 的烧瓶进行“喷泉实验”,装置及现象如下图。下列关于该实验的分析
3
正确的是
A.产生“喷泉”证明NH 与HO发生了反应
3 2
B.无色溶液变红证明NH 极易溶于水
3
C.红色溶液中存在含有离子键的含氮微粒
D.加热红色溶液可观察到红色变浅或褪去
5.(2024·浙江绍兴·三模)室温下,下列溶液中一定能大量共存的离子组是
A.强碱性溶液: 、 、 、
B.加入铝粉有氢气产生的溶液: 、 、 、C.中性溶液: 、 、 、
D.强酸性溶液: 、 、 、
6.(2024·广东深圳·模拟预测)下列离子方程式书写正确的是
A.浓硝酸和铁在常温下反应:Fe+6H++3 =Fe3++3NO↑+3H O
2 2
B.实验室制氨气: +OH-=NH↑
3
C.向含有1.5molFeI 的溶液中通入2molCl :2Fe2++6I-+4Cl=2Fe3++3I +8Cl-
2 2 2 2
D.向NaClO溶液中通入少量SO :ClO-+SO+H O= +Cl-+2H+
2 2 2
7.(2024·海南·三模)如图装置可用于收集气体并验证其某些化学性质,能达到目的的是
选
气体 试剂 现象 结论
项
A 酚酞试液 溶液变红色 氨水显碱性
B 紫色石蕊试液 溶液先变红后褪色 有酸性和漂白性
C 溴水 溶液褪色 分子中含碳碳双键
D 淀粉-KI溶液 溶液变蓝 有氧化性
8.(2024·海南·三模)部分含N的纯净物的“价-类”二维图如图所示。下列叙述正确的是
A.a只有还原性,没有氧化性 B.一定条件下,a和c反应可生成b
C.a的催化氧化可直接生成c D.c和水反应生成b和d
9.(2024·河北·一模)大气中NO达到一定浓度时,会对人体造成伤害。NO在大气中转化过程如下图所
示,下列说法正确的是A. 在转化过程中表现出强氧化性,与 互为同位素
B. 是大气污染物,在大气中有可能形成硝酸型酸雨或光化学烟雾
C. 是一种酸性氧化物,酸性氧化物都可以和水反应生成相应的酸
D. 是一种直线形分子,电子式为
10.(2024·湖南娄底·模拟) 某学习小组设计了如图的实验装置(夹持装置已省略)模拟常压下工业合成氨,并
检验氨的生成。Y形管左侧支管中盛有NH Cl与NaNO 的混合溶液,加热后生成N 及少量NH 。下列有
4 2 2 3
关描述不正确的是( )
A.实验时,点燃a处酒精灯一段时间后,再点燃c处酒精喷灯
B.b处装置可用盛有碱石灰的U形管代替
C.硬质玻璃管中的石棉可以增大混合气体与铁粉的接触面积
D.若d处锥形瓶中溶液变红,则说明硬质玻璃管中有NH 生成
3
11.足量铜溶于一定量浓硝酸,产生NO 、NO、NO的混合气体,这些气体若与1.12 L O (标准状况)混合
2 2 4 2
后通入水中,气体被水完全吸收。若向原所得溶液中加入5 mol·L-1 HSO 溶液100 mL,则继续溶解的Cu
2 4
的质量为( )
A.6.4 g B.9.6 g
C.19.2 g D.24 g
12.(2024·山东日照·二模)部分含氮物质的分类与相应化合物关系如图所示。下列说法错误的是
A.b具有碱性和还原性
B.反应Ⅰ中氧化产物和还原产物的物质的量之比为1∶1C.反应Ⅱ过程中生成0.1mol 时,转移1mol电子
D.反应Ⅲ能有效降低水体中的氮元素含量
13.(2024·河北·二模)下列离子的检验方案、现象及结论不正确的是
选
检验方案 现象 结论
项
原溶液中含有
A 向某溶液中滴加 溶液 出现蓝色沉淀
向某溶液中加入淀粉溶液后再滴入适量过氧化氢 原溶液中不含
B 溶液始终不变蓝
溶液
向硫酸酸化的 溶液中滴加 溶液,再 被氧化成
C 出现白色沉淀
滴加 溶液
产生能使湿润的红色石蕊试纸 原溶液中含有
D 向某盐溶液中加足量 后加热
变蓝的气体
14.(2024·北京门头沟·一模)为吸收工业尾气中的 和 ,设计如图流程,同时还能获得连二亚硫酸
钠( ,其结晶水合物又称保险粉)和 产品。( 为铈元素)
下列说法不正确的是
A.工业尾气中的 和 排放到大气中会形成酸雨
B.装置Ⅱ的作用是吸收
C. 从阴极口流出回到装置Ⅱ循环使用
D.装置Ⅳ中氧化 ,至少需要标准状况下
15.(2024·河南周口·模拟预测)某兴趣小组设计实验验证铜与浓硝酸、稀硝酸的反应,装置如图所示(夹
持装置未画出):实验一:验证铜与浓硝酸的反应
按图示连接好装置,_______后,装入药品,关闭 、 ,打开 ,一段时间后,再关闭 ,打开 ,
加入足量的浓 。
实验二:验证铜与稀硝酸的反应
待装置B中反应完全后……
回答下列有关问题:
(1)实验一中的横线上应填入的内容是 ;装置B中装浓硝酸的仪器名称是 。
(2)实验一中“关闭 、 ,打开 ”的目的是
(3)装置B中发生反应的离子方程式为
(4)实验二的后续操作顺序为 (填标号),打开止水夹后装置C的具支试管中的现象为 。
a.打开止水夹 b.打开 c.打开 ,加入蒸馏水 d.关闭 e.插入铜丝。
(5)实验结束后,有同学观察到装置B中溶液呈绿色,装置C中溶液呈蓝色。小组同学认为颜色不同的原因
可能如下:
猜想1:硝酸铜溶液的物质的量浓度不同,溶液颜色不同,浓度小时呈蓝色,浓度大时呈绿色。
猜想2: 溶解在硝酸铜溶液中,导致溶液颜色不同。
继续实验,打开 ,一段时间后,装置B中溶液变为蓝色,说明 可能成立,请设计实验验证另一
猜想的可能性: 。
1.(2024·湖北卷,8,3分)结构决定性质,性质决定用途。下列事实解释错误的是( )
事实 解释
A 甘油是黏稠液体 甘油分子间的氢键较强
B 王水溶解铂 浓盐酸增强了浓硝酸的氧化性
C 冰的密度小于干冰 冰晶体中水分子的空间利用率相对较低
D 石墨能导电 未杂化的p轨道重叠使电子可在整个碳原子平面内运动2.(2023•湖北省选择性考试,1)2023年5月10日,天舟六号货运飞船成功发射,标志着我国航天事业进
入到高质量发展新阶段。下列不能作为火箭推进剂的是( )
A.液氮-液氢 B.液氧-液氢C.液态NO -肼 D.液氧-煤油
2
3.(2023·山东,2)实验室中使用盐酸、硫酸和硝酸时,对应关系错误的是( )
A.稀盐酸:配制AlCl 溶液
3
B.稀硫酸:蔗糖和淀粉的水解
C.稀硝酸:清洗附有银镜的试管
D.浓硫酸和浓硝酸的混合溶液:苯的磺化
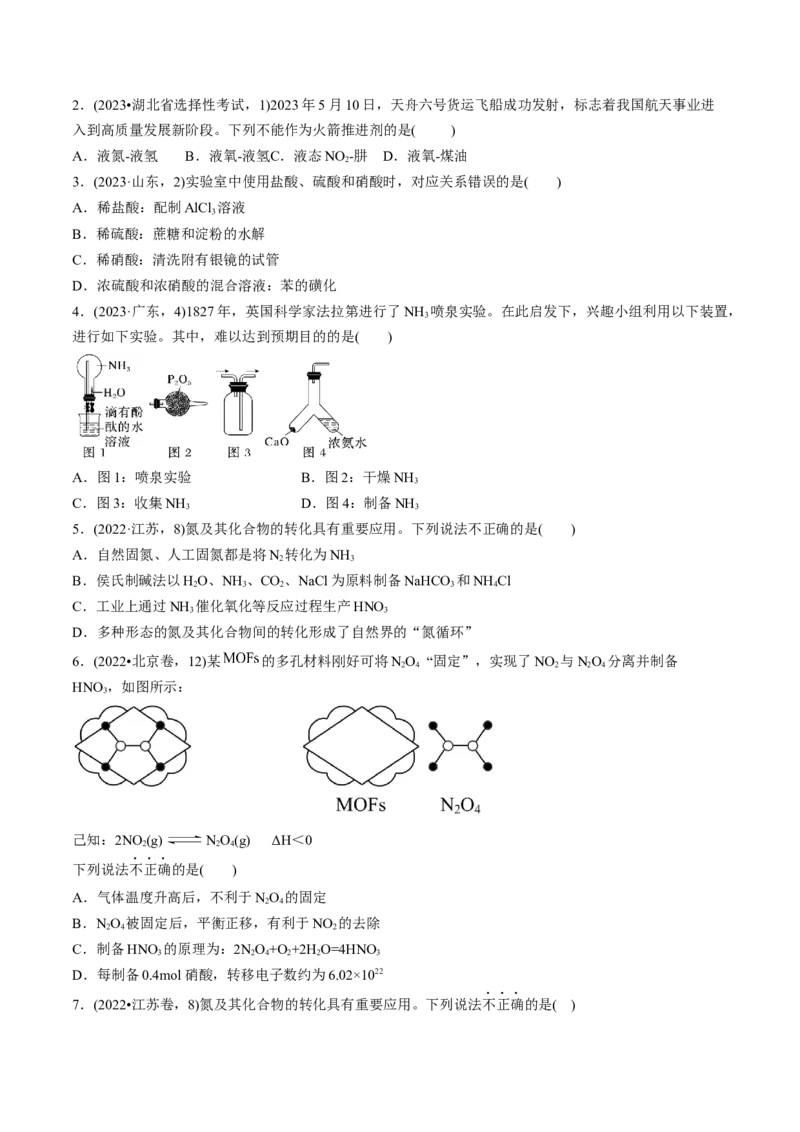
4.(2023·广东,4)1827年,英国科学家法拉第进行了NH 喷泉实验。在此启发下,兴趣小组利用以下装置,
3
进行如下实验。其中,难以达到预期目的的是( )
A.图1:喷泉实验 B.图2:干燥NH
3
C.图3:收集NH D.图4:制备NH
3 3
5.(2022·江苏,8)氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A.自然固氮、人工固氮都是将N 转化为NH
2 3
B.侯氏制碱法以HO、NH 、CO、NaCl为原料制备NaHCO 和NH Cl
2 3 2 3 4
C.工业上通过NH 催化氧化等反应过程生产HNO
3 3
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
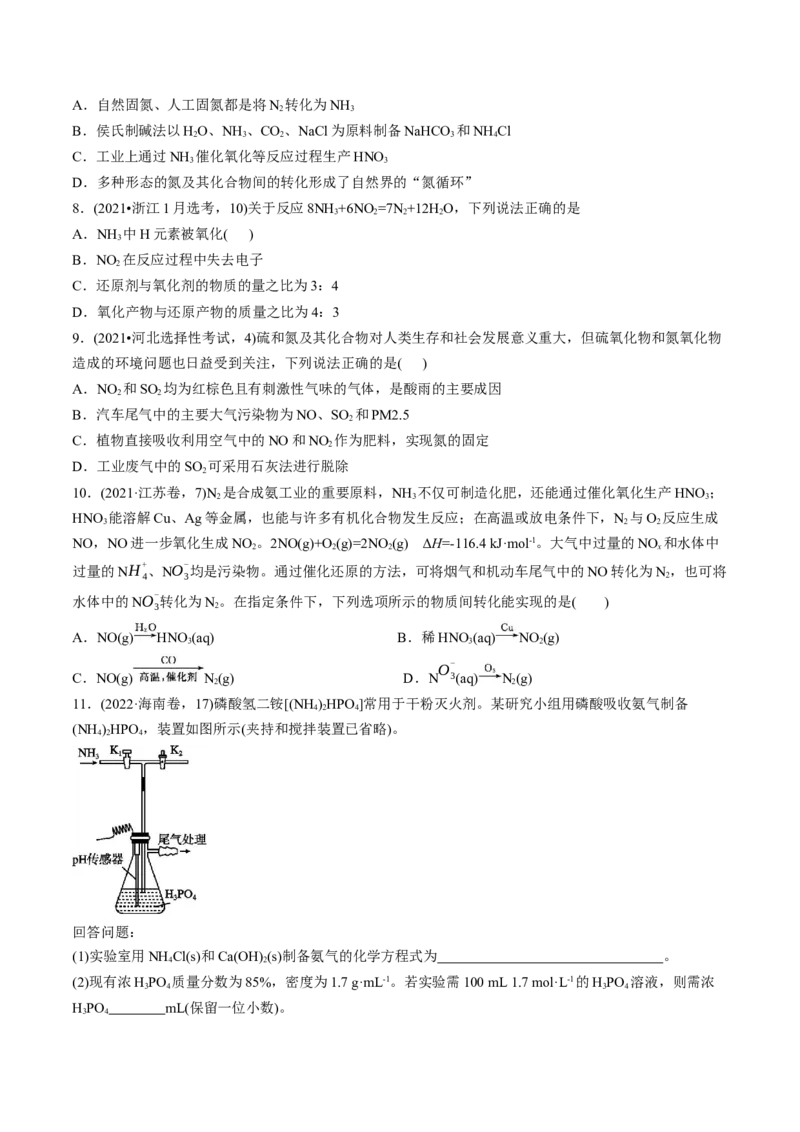
6.(2022•北京卷,12)某 的多孔材料刚好可将NO “固定”,实现了NO 与NO 分离并制备
2 4 2 2 4
HNO,如图所示:
3
己知:2NO (g) NO(g) ΔH<0
2 2 4
下列说法不正确的是( )
A.气体温度升高后,不利于NO 的固定
2 4
B.NO 被固定后,平衡正移,有利于NO 的去除
2 4 2
C.制备HNO 的原理为:2NO+O +2H O=4HNO
3 2 4 2 2 3
D.每制备0.4mol硝酸,转移电子数约为6.02×1022
7.(2022•江苏卷,8)氮及其化合物的转化具有重要应用。下列说法不正确的是( )A.自然固氮、人工固氮都是将N 转化为NH
2 3
B.侯氏制碱法以HO、NH 、CO、NaCl为原料制备NaHCO 和NH Cl
2 3 2 3 4
C.工业上通过NH 催化氧化等反应过程生产HNO
3 3
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
8.(2021•浙江1月选考,10)关于反应8NH +6NO=7N +12H O,下列说法正确的是
3 2 2 2
A.NH 中H元素被氧化( )
3
B.NO 在反应过程中失去电子
2
C.还原剂与氧化剂的物质的量之比为3:4
D.氧化产物与还原产物的质量之比为4:3
9.(2021•河北选择性考试,4)硫和氮及其化合物对人类生存和社会发展意义重大,但硫氧化物和氮氧化物
造成的环境问题也日益受到关注,下列说法正确的是( )
A.NO 和SO 均为红棕色且有刺激性气味的气体,是酸雨的主要成因
2 2
B.汽车尾气中的主要大气污染物为NO、SO 和PM2.5
2
C.植物直接吸收利用空气中的NO和NO 作为肥料,实现氮的固定
2
D.工业废气中的SO 可采用石灰法进行脱除
2
10.(2021·江苏卷,7)N 是合成氨工业的重要原料,NH 不仅可制造化肥,还能通过催化氧化生产HNO;
2 3 3
HNO 能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N 与O 反应生成
3 2 2
NO,NO进一步氧化生成NO 。2NO(g)+O (g)=2NO (g) ΔH=-116.4 kJ·mol-1。大气中过量的NO 和水体中
2 2 2 x
过量的NH+ 、NO-
均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N,也可将
4 3 2
水体中的NO-
转化为N。在指定条件下,下列选项所示的物质间转化能实现的是( )
3 2
A.NO(g) HNO(aq) B.稀HNO(aq) NO (g)
3 3 2
O-
C.NO(g) N(g) D.N 3(aq) N(g)
2 2
11.(2022·海南卷,17)磷酸氢二铵[(NH )HPO ]常用于干粉灭火剂。某研究小组用磷酸吸收氨气制备
4 2 4
(NH )HPO ,装置如图所示(夹持和搅拌装置已省略)。
4 2 4
回答问题:
(1)实验室用NH Cl(s)和Ca(OH) (s)制备氨气的化学方程式为 。
4 2
(2)现有浓HPO 质量分数为85%,密度为1.7 g·mL-1。若实验需100 mL 1.7 mol·L-1的HPO 溶液,则需浓
3 4 3 4
HPO mL(保留一位小数)。
3 4(3)装置中活塞K 的作用为 。实验过程中,当出现 现象时,应及时关闭K,打开
2 1
K。
2
(4)当溶液pH为8.0~9.0时,停止通NH ,即可制得(NH )HPO 溶液。若继续通入NH ,当pH>10.0时,溶
3 4 2 4 3
液中OH-、 和 (填离子符号)浓度明显增加。
(5)若本实验不选用pH传感器,还可选用 作指示剂,当溶液颜色由 变为 时,停
止通NH 。
3