文档内容
考点 17 元素周期表 元素周期律
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 元素周期表的结构.......................................................................................................................2
考法02 元素周期律...................................................................................................................................5
考法03 元素位构性的应用.......................................................................................................................9
...........................................................................................................................................12
1.高考真题考点分布
考点内容 考点分布
2024·甲卷,4分;2024·江苏卷,3分;2023天津卷5题,4分;
元素周期律
2021北京卷4题,4分
2024·甘肃卷,3分;2023全国甲卷11题,6分;2023全国乙卷10题,6分;
文字叙述型元素推 2023广东卷14题,3分;2023浙江1月10题,3分;2023浙江6月11题,3分;
断 2023湖北卷6题,3分;2023湖南卷6题,3分;2022浙江1月16题,2分;
2022浙江6月16题,2分;2022海南卷10题,4分;2022辽宁卷5题,3分;
周期表片段型元素
2022年广东7题,2分;2021浙江1月15题,2分
推断
物质结构式型元素 2023辽宁卷9题,3分;2022全国乙卷11题,6分;2022湖南卷5题,3分;
推断 2021河北卷12题,4分;2021广东卷13题,4分;2021辽宁卷14题,3分;
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,应用元素周期律和元素周期表,推断原子的结构,预测元素的性
质,如金属性、非金属性的变化,半径的变化,仍是高考命题的热点。
【备考策略】
元素“位”“构”“性”三者关系的题型会继续以元素及其化合物知识为载体,用物质结构理论,解释现
象、定性推断、归纳总结相结合。通过编排元素周期表考查的抽象思维能力和逻辑思维能力;通过对元素原子结构、位置间的关系的推导,培养学生的分析和推理能力。
【命题预测】
预计2025年高考会以新的情境载体考查同周期、同主族元素性质的递变规律,理清元素“位—构—性”的
关系,特别是金属性、非金属性强弱以及原子或离子半径大小判断知识,题目难度一般适中。
考法01 元素周期表的结构
1.编排原则
(1)周期:把电子层数相同的元素,按 递增的顺序,从左至右排成的横行。
(2)族:把最外层电子数相同的元素,按 递增的顺序,从上至下排成的纵行。
2.元素周期表的结构
(1)周期
短周期 长周期
序号 1 2 3 4 5 6 7
元素种数 不完全周期,最多容
0族元素 纳32种元素,目前
原子序数 排了26种元素
(2)族
①主族:由短周期元素和长周期元素共同组成的族(第18列除外)
列序 1 2 13 14 15 16 17
主族序数 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
②副族:仅由长周期元素组成的族(第8、9、10列除外)
列序 3 4 5 6 7 11 12
族序数 ⅢB ⅣB ⅤB ⅥB ⅦB ⅠB ⅡB
③Ⅷ族:包括 三个纵列。
④0族:第18纵列,该族元素又称为稀有气体元素。
3.元素周期表中的特殊位置
(1)分区
①分界线:沿着元素周期表中铝、锗、锑、钋与硼、硅、砷、碲、砹的交界处画一条斜线,即为金属元素区和非金属元素区分界线(氢元素除外)。线的左边是 元素(氢除外),线的右边是 元素。非金
属元素主要集中在元素周期表右上角的三角区内(如图所示)。处于 与 分界线(又称梯形线)
附近的非金属元素具有一定的 性,又称为半金属、类金属或准金属,但不能叫两性非金属。
②各区位置:分界线左面为金属元素区,分界线右面为非金属元素区。
③分界线附近元素的性质:既表现金属元素的性质,又表现非金属元素的性质。
④对角线规则
在元素周期表中,某些主族元素与右下方的主族元素(如图)的有些性质是相似的(如锂和镁在过量的氧
气中燃烧均生成正常氧化物,而不是过氧化物),这种相似性被称为 规则。
(2)过渡元素:元素周期表中部从ⅢB族到ⅡB族10个纵列共六十多种元素,这些元素都是金属元素。
(3)镧系:元素周期表第6周期中,57号元素镧到71号元素镥共15种元素。
(4)锕系:元素周期表第7周期中,89号元素锕到103号元素铹共15种元素。
(5)超铀元素:在锕系元素中92号元素铀(U)以后的各种元素。
4.元素周期表的“三大”应用
(1)科学预测:为新元素的发现及预测它们的原子结构和性质提供了线索。
(2)寻找新材料:
(3)用于工农业生产
地球中化学元素的分布与它们在元素周期表中的位置关系对探矿有指导意义。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)包含元素种数最多的族是第ⅠA族。( )(2)原子的最外层有2个电子的元素一定是第ⅡA族元素。( )
(3)第ⅠA族元素都是碱金属元素,在化学反应中均易失去1个电子。( )
(4)过渡元素都是金属元素,且均由副族元素组成。( )
(5)两种短周期元素的原子序数相差8,则周期序数一定相差1。( )
(6)元素周期表中位于金属与非金属分界线附近的元素属于过渡元素( )
(7)第ⅠA族全部是金属元素( )
(8)元素周期表中镧系元素和锕系元素都占据同一格,它们是同位素( )
(9)形成化合物种数最多的元素在ⅣA族( )
考向01 考查周期表的结构
【例1】(2024·广东深圳·一模)IUPAC(国际纯粹与应用化学联合会)宣布,第112号化学元素正式名称为
“Copernicium”,元素符号为“Cn”,以纪念著名天文学家哥白尼,该元素的一种核素含有的中子数为
165。下列关于Cn的说法正确的是( )
A.Cn位于第六周期ⅡB族
B.Cn是过渡元素
C.Cn是非金属元素
D.Cn元素的核外电子数为165
考向02 考查周期表的应用
【例2】(2024·山东淄博·二模)部分元素在周期表中的分布如图所示(虚线为金属元素与非金属元素的分
界线),下列说法不正确的是( )
A.虚线左侧是金属元素
B.As处于第五周期第ⅤA族
C.Si、Ge可作半导体材料
D.Sb既有金属性又有非金属性
【对点1】(2024·河北保定·模拟)中国科学院院士张青莲教授曾主持测定的铟( In)等9种元素相对原子质
49
量的新值,被采用为国际新标准。In与Al同主族。下列说法正确的是( )
A.In是第四周期ⅢA族元素B.In与In互为同素异形体
C.原子半径:Rb>In
D.碱性:In(OH) <Al(OH)
3 3
【对点2】(2024·浙江台州·模拟)下列说法正确的是( )
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.原子最外层电子数为2的元素一定处于周期表第ⅡA族
C.同周期中金属性最强的元素是ⅠA族金属元素
D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
考法02 元素周期律
1.元素周期律
(1)概念:元素的性质随元素原子的核电荷数递增发生 递变的规律。
(2)实质:元素性质的周期性变化是元素原子 周期性变化的必然结果。
2.主族元素的周期性变化规律
项目 同周期(左→右) 同主族(上→下)
核电荷数 逐渐增大 逐渐增大
电子层数 相同 逐渐增多
原子
原子半径 逐渐减小 逐渐增大
结构
阳离子逐渐减小阴离子逐渐减小
离子半径 逐渐增大
r(阴离子)>r(阳离子)
最高正化合价由+1→+7(O、F除 相同,最高正化合价=主族序
化合价
外)负化合价=-(8-主族序数) 数(O、F除外)
元素的金属性和非金 金属性逐渐减弱 金属性逐渐增强
属性 非金属性逐渐增强 非金属性逐渐减弱
性质 离子的氧化性、还原 阳离子氧化性逐渐增强 阳离子氧化性逐渐减弱
性 阴离子还原性逐渐减弱 阴离子还原性逐渐增强
气态氢化物的稳定性 逐渐增强 逐渐减弱
最高价氧化物对应的 碱性逐渐减弱 碱性逐渐增强
水化物的酸碱性 酸性逐渐增强 酸性逐渐减弱
3.元素周期表、元素周期律的应用
(1)根据元素周期表中的位置寻找未知元素
(2)预测元素的性质(由递变规律推测)
①比较不同周期、不同主族元素的性质
如:金属性:Mg>Al、Ca>Mg,则碱性:Mg(OH) >Al(OH) 、Ca(OH) >Mg(OH) ,则Ca(OH) >
2 3 2 2 2
Al(OH) (填“>”“<”或“=”)。
3
②推测未知元素的某些性质
如:已知Ca(OH) 微溶,Mg(OH) 难溶,可推知Be(OH) 难溶;再如:已知卤族元素的性质递变规律,可
2 2 2
推知元素砹(At)应为有色固体,与氢难化合,HAt不稳定,水溶液呈酸性,AgAt不溶于水等。(3)启发人们在一定区域内寻找新物质
①半导体元素在金属与非金属分界线附近,如:Si、Ge、Ga等。
②农药中常用元素在右上方,如:F、Cl、S、P、As等。
③催化剂和耐高温、耐腐蚀合金材料主要在过渡元素中找,如:Fe、Ni、Rh、Pt、Pd等。
4.微粒半径大小比较方法
5.元素金属性和非金属性强弱的判断方法
本质 原子越易失电子,金属性越强(与原子失电子数目无关)
①在金属活动性顺序表中越靠前,金属性越强
②单质与水或非氧化性酸反应越剧烈,金属性越强
金属性
③单质还原性越强或阳离子氧化性越弱,金属性越强
比较 判断方法
④最高价氧化物对应水化物的碱性越强,金属性越强
⑤若Xn++Y―→X+Ym+,则Y比X的金属性强
⑥元素在周期表中的位置:左边或下方元素的金属性强
本质 原子越易得电子,非金属性越强(与原子得电子数目无关)
①与H 化合越容易,气态氢化物越稳定,非金属性越强
2
非金属
②单质氧化性越强或阴离子还原性越弱,非金属性越强
性比较 判断方法
③最高价氧化物对应水化物的酸性越强,非金属性越强
④元素在周期表中的位置:右边或上方元素的非金属性强
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)元素的氧化物对应水化物的酸性越强,非金属性越强,碱性越强,金属性越强。( )
(2)元素的气态氢化物越稳定,非金属性越强,其水溶液的酸性越强,还原性越弱。( )
(3)元素的原子得电子越多,非金属性越强,失电子越多,金属性越强。( )
(4)同周期元素,从左到右,原子半径逐渐减小,离子半径也逐渐减小。( )
(5)第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性( )
(6)元素的氧化物对应的水化物酸性越强,非金属性越强,碱性越强,金属性越强( )(7)元素的气态氢化物越稳定,非金属性越强,其水溶液的酸性越强,还原性越弱( )
考向01 考查微粒半径大小比较
【例1】(2024·辽宁沈阳·一模)短周期元素X、Y,若原子半径X>Y,则下列选项中一定正确的是(
)
A.若X、Y均在ⅣA族,则单质熔点X>Y
B.若X、Y均在ⅥA族,则气态氢化物的热稳定性X>Y
C.若X、Y均属于第二周期非金属元素,则简单离子半径X>Y
D.若X、Y均属于第三周期金属元素,则元素的最高正价X>Y
【思维建模】
考向02 考查元素金属性和非金属性强弱
【例2】(2024·河北隆尧·模拟)W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外电子
总数满足X+Y=W+Z;化合物XW 与WZ相遇会产生白烟。下列叙述正确的是( )
3
A.非金属性:W>X>Y>Z
B.原子半径:Z>Y>X>W
C.元素X的含氧酸均为强酸
D.Y的氧化物水化物为强碱
【思维建模】
元素的金属性强弱比较 元素的非金属性强弱比较
最高价氧化物对应水化物的碱性越强,对应元素的 最高价氧化物对应水化物的酸性越强,对应元素
金属性越强 的非金属性越强
单质与水、酸反应越容易或越剧烈,对应元素的金 单质与H 反应越容易,生成的简单氢化物越稳
2
属性越强 定,对应元素的非金属性越强
单质的还原性越强,对应元素的金属性越强 单质的氧化性越强,对应元素的非金属性越强
阳离子氧化性越强,对应元素的金属性越弱 简单阴离子的还原性越强,对应元素的非金属性越弱
原电池:负极材料对应元素的金属性通常强于正极。电解池:在阴极首先放电的阳离子,其对应元素的
金属性弱;在阳极首先放电的阴离子,其对应元素的非金属性弱
置换反应:强的置换出弱的,适用于金属也适用于非金属
【对点1】(2024·山东潍坊·模拟)如表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与
X的最高化合价之和为8。下列说法错误的是( )
W
X Y Z
A.原子半径:W<X
B.常温常压下,Y单质为固态
C.气态氢化物热稳定性:Z<W
D.X的最高价氧化物的水化物是强碱
【对点2】(2024·湖北黄冈·模拟)下列事实不能说明元素的金属性或非金属性相对强弱的是( )
选项 事实 结论
A 与冷水反应,Na比Mg强烈 金属性:Na>Mg
B Ca(OH) 的碱性强于Mg(OH) 金属性:Ca>Mg
2 2
C SO 与NaHCO 溶液反应生成CO 非金属性:S>C
2 3 2
t ℃时,Br +H 2HBr K=5.6×107
2 2
D 非金属性:Br>I
I+H 2HI K=43
2 2
考法03 元素位构性的应用
1.结合元素周期表结构推断的思维模型
(1)依据原子结构特点推断
3≤N<8,元素属于ⅢA族~ⅦA族;N=1或2,元素属于ⅠA族、ⅡA族、副族
原子最外层电
(Pd除外)、0族(氦);N=8,元素属于0族(He除外);N>次外层电子数,元
子数(N)
素属于第二周期(Li、Be除外)
“阴三阳四” 某元素对应简单离子的最外层电子数与次外层电子数相等,若为阴离子,则该元素位
规律 于第三周期;若为阳离子,则该元素位于第四周期
“阴上阳下” 电子层结构相同的离子,若电性相同,则位于同周期;若电性不同,则阳离子对应元
规律 素位于阴离子对应元素的下一周期
(2)依据元素在周期表中的相对位置推断
直接相邻的
“┳”型、 ①“┻”型、 ②
“╋”型相对
位置关系
③
注:Z为某元素的原子序数
“对角线”规 有些元素在周期表中虽然既非同周期,又非同主族,但其单质与同类化合物的化学性质
则 却很相似,如Li和Mg、Be和Al等
2.元素周期表结构与元素性质的关系
考向01 结合原子结构进行推断
【例1】(2023·湖南卷)日光灯中用到的某种荧光粉的主要成分为3W(ZX)·WY。已知:X、Y、Z和
3 4 2 2
W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子
数相等,基态X、Y、Z原子的未成对电子数之比为2∶1∶3。下列说法正确的是( C )
A.电负性:X>Y>Z>W
B.原子半径:X<Y<Z<W
C.Y和W的单质都能与水反应生成气体
D.Z元素最高价氧化物对应的水化物具有强氧化性
考向02 结合“特殊微粒结构”进行推断
【例2】(2024·江苏常州·一模)X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元素的最高正
价为+4价,Y元素与Z、M元素相邻,且与M元素同主族;化合物ZX 的电子总数为18个;Q元素的原
2 4
子最外层电子数比次外层少一个电子。下列说法不正确的是( )
A.原子半径:Z<Y<M
B.最高价氧化物对应水化物的酸性:Z>Y>M
C.X Z-ZX 易溶于水,其水溶液呈碱性
2 2
D.X、Z和Q三种元素形成的化合物一定是共价化合物
考向03 结合元素周期表结构进行推断【例3】(2024·湖南长沙·联考)短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素
原子的最外层电子数之和为21。下列关系正确的是( )
W X
Y Z
A.氢化物沸点:W<Z
B.氧化物对应水化物的酸性:Y>W
C.化合物熔点:YX<YZ
2 3 3
D.简单离子的半径:Y<X
考向04 结合元素化合物的性质推断
【例4】(2022·全国乙卷)化合物(YWXZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z
4 5 8 2
为短周期元素,原子序数依次增加,且加和为21。YZ 分子的总电子数为奇数,常温下为气体。该化合物
2
的热重曲线如图所示,在200 ℃以下热分解时无刺激性气体逸出。下列叙述正确的是( D )
A.W、X、Y、Z的单质常温下均为气体
B.最高价氧化物的水化物的酸性:Y<X
C.100~200 ℃阶段热分解失去4个WZ
2
D.500 ℃热分解后生成固体化合物XZ
2 3
【对点1】(2023·全国乙卷)一种矿物由短周期元素W、X、Y组成,溶于稀盐酸有无色无味气体生成。
W、X、Y原子序数依次增大。简单离子X2-与Y2+具有相同的电子结构。下列叙述正确的是( )
A.X的常见化合价有-1、-2
B.原子半径大小为Y>X>W
C.YX的水合物具有两性
D.W单质只有4种同素异形体
【对点2】(2024·湖南常德·模拟)W、X、Y、Z为原子序数依次增大的短周期主族元素,Y的原子序数
等于W与X的原子序数之和,Z的最外层电子数为K层的一半,W与X可形成原子个数比为2∶1的18e-
分子。下列说法错误的是( )
A.简单离子半径:Z>X>Y
B.W与Y能形成含有非极性键的化合物
C.X和Y的最简单氢化物的沸点:X<YD.Y的单质可从X的简单氢化物中置换出X的单质
【对点3】(2024·北京顺义·二模)下表为元素周期表的一部分,其中X、Y、W、Z为短周期元素,W的
单质常温下为黄绿色气体。下列说法不正确的是( )
Y Z
X W
R T
A.X、Y的单质均存在同素异形体
B.Y、Z的简单氢化物的稳定性逐渐增强
C.R的单质可用于制造半导体材料
D.工业上电解NaW溶液制W 可使用阴离子交换膜
2
【对点4】(2024·福建厦门·联考)W、X、Y、Z均为短周期元素且原子序数依次增大,元素X和Z同族。
盐YZW与浓盐酸反应,有黄绿色气体产生,此气体同冷烧碱溶液作用,可得到含YZW的溶液。下列说法
正确的是( )
A.原子半径大小为W<X<Y<Z
B.X的氢化物水溶液酸性强于Z的
C.Y W 与ZW均含有非极性共价键
2 2 2
D.标准状况下W的单质状态与X的相同
1.(2024·黑龙江大庆·一模)根据元素周期表和元素周期律,判断下列叙述正确的是
A.氢卤酸的酸性由强到弱的顺序:HF>HCl>HBr
B.同周期第ⅡA族和第ⅢA族元素原子序数可能相差1、11、25
C.铁元素位于元素周期表中第四周期第ⅧA族
D.主族元素都有最高正价,且都等于该元素原子的最外层电子数
2.(2024·云南保山·一模)下列关于原子核外电子排布和元素周期律的说法,正确的是
A.同一周期中,第ⅡA与第ⅢA族元素原子的核电荷数相差1或10或25
B.氧的非金属性比碳强,所以 的熔沸点比 高
C. 是卤族元素最高价含氧酸中酸性最强的酸
D.元素周期表纵向看,由16个纵列构成
3.(2024·天津河西·三模)下列叙述正确的是
A.第二周期主族元素原子半径从左到右依次减小
B.第三周期元素的氯化物所属晶体类型相同
C.短周期第IA族与VIIA族元素构成的物质均含离子键D.元素周期表中位于金属与非金属分界线附近的元素属于过渡元素
4.(2024·浙江·三模)如图,X、Y、Z、W四种短周期元素的原子最外层电子数之和为21.下列说法正确
的是
X Y
W Z
T
A.原子半径(r):r(Z)>r(Y)>r(X)
B.X的氢化物一定比Y的氢化物的沸点要低
C.WY、WZ、WX均有熔点高、硬度大的特性
2 4
D.某病毒DNA链中有T元素,可能是T取代了普通DNA链中的P元素
5.(2024·四川雅安·模拟预测)X、Y、Q、M、N均为短周期主族元素,这五种元素在周期表中的相对位
置如下图所示。已知X、Q、M三种元素的核电荷数之和比Y和N的核电荷数之和多10。下列说法正确的
是
X Y
Q M N
A.Q、M、N形成的单质硬度都很大
B. 不能从溶液中制得
C.X、Q、M、N的所有氧化物都能与氢氧化钠溶液反应
D.含氧酸酸性由大到小的顺序为
6.(2024·湖南·模拟预测)已知X、Y、Z、W、M为短周期元素且原子序数依次增大,W原子核外s能级
上的电子总数与p能级上的电子总数相等,0.1molM单质与足量稀硫酸作用,在标准状况下能产生
3.36LH ;常温下,M的单质与Z的最高价氧化物对应的水化物的浓溶液作用,M的表面会形成一层致密
2
的氧化膜。在化合物YX、ZX、XW 中,相应分子内各原子最外层电子都满足稳定结构,下列说法正
2 6 2 4 2 2
确的是
A.电解熔融MCl 可以得到单质M
3
B.XW 中既有极性键又有非极性键
2 2
C.Z的氢化物的沸点大于Y的氢化物沸点
D.原子半径:M>W>Z>Y
7.(2024·重庆·模拟预测)主族元素X、Y、Z、W、R分别处于三个短周期,原子序数依次增加,且原子
序数之和为38,R和W最外层电子数相等,在元素周期表中W和Z相邻,下列叙述一定正确的是
A.原子半径: Y>Z>R>W>X
B.简单氢化物的热稳定性:W>Z
C.X、Y、Z形成的化合物是极性分子
D.W与R组成的二元化合物均为酸性氧化物8.(2024·湖北武汉·一模)X、Y、Z、W、M是原子序数依次增大的短周期主族元素,且位于三个不同周
期,Z与Y和W都相邻,且Y、Z、W三种元素原子的最外层电子数之和为16,下列说法错误的是
A.原子半径:Z>W>M>X
B.Z和W都有多种同素异形体
C.最高价氧化物对应水化物的酸性:YZ
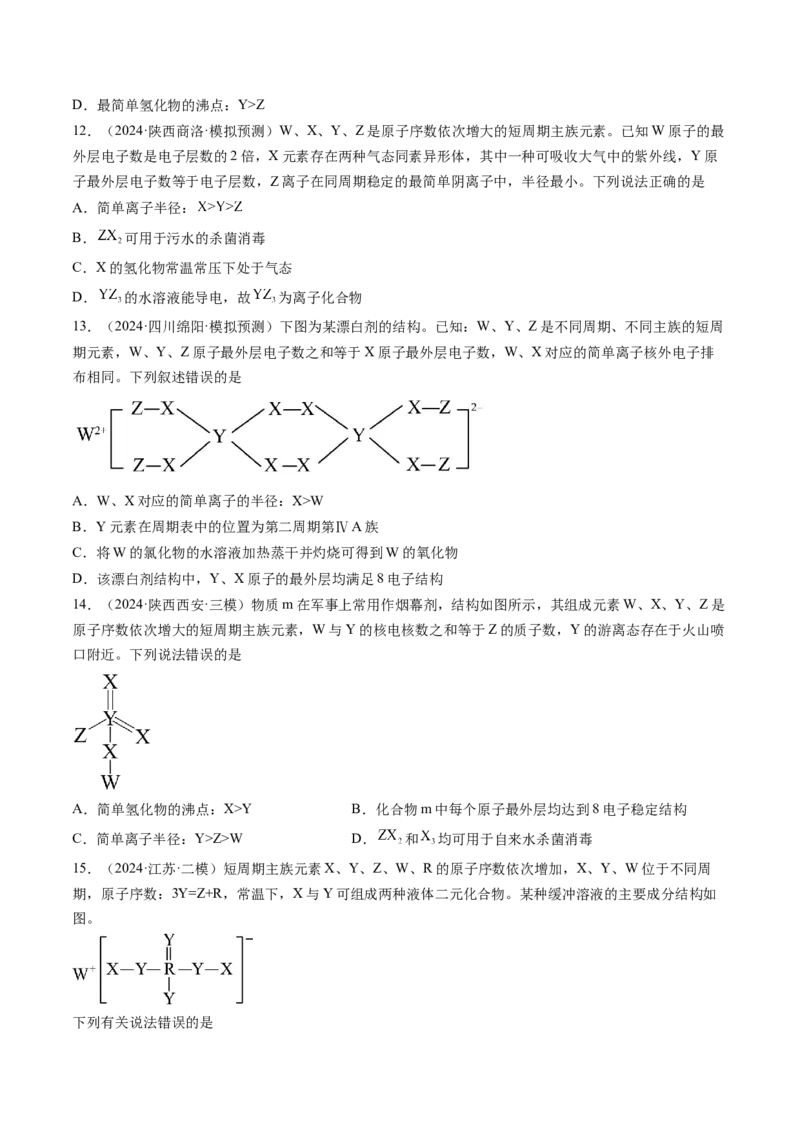
12.(2024·陕西商洛·模拟预测)W、X、Y、Z是原子序数依次增大的短周期主族元素。已知W原子的最
外层电子数是电子层数的2倍,X元素存在两种气态同素异形体,其中一种可吸收大气中的紫外线,Y原
子最外层电子数等于电子层数,Z离子在同周期稳定的最简单阴离子中,半径最小。下列说法正确的是
A.简单离子半径:
B. 可用于污水的杀菌消毒
C.X的氢化物常温常压下处于气态
D. 的水溶液能导电,故 为离子化合物
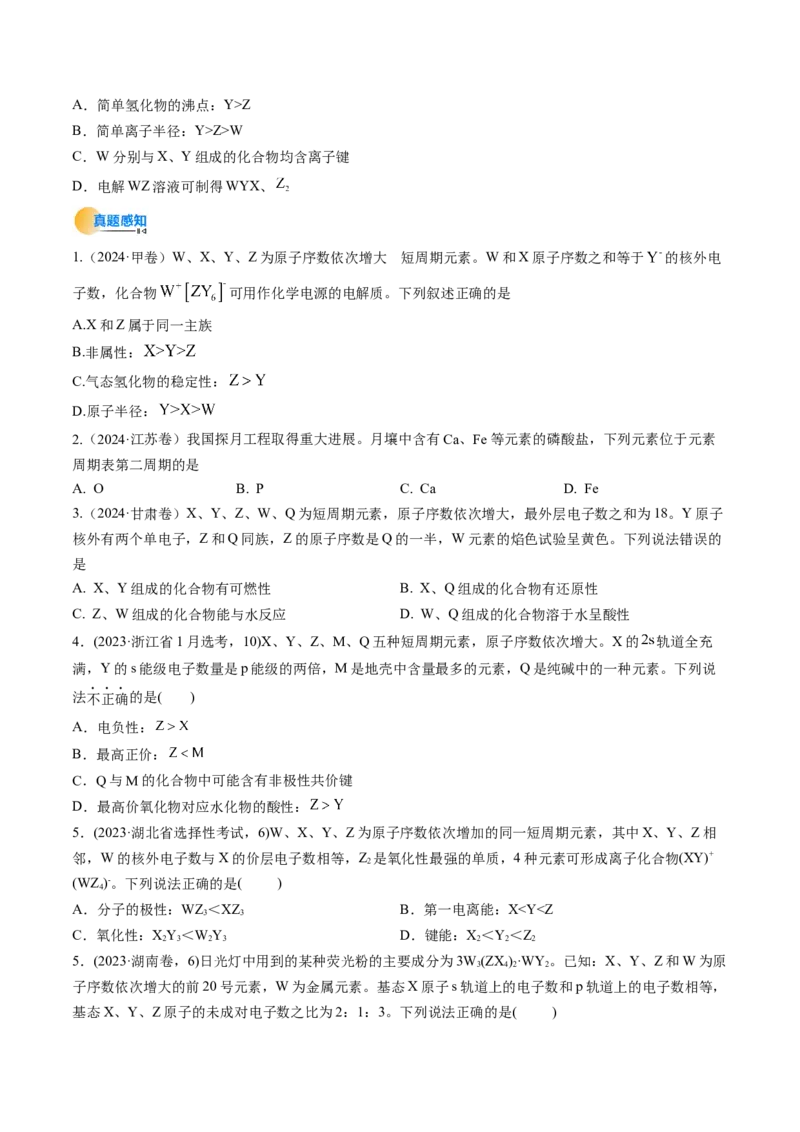
13.(2024·四川绵阳·模拟预测)下图为某漂白剂的结构。已知:W、Y、Z是不同周期、不同主族的短周
期元素,W、Y、Z原子最外层电子数之和等于X原子最外层电子数,W、X对应的简单离子核外电子排
布相同。下列叙述错误的是
A.W、X对应的简单离子的半径:X>W
B.Y元素在周期表中的位置为第二周期第ⅣA族
C.将W的氯化物的水溶液加热蒸干并灼烧可得到W的氧化物
D.该漂白剂结构中,Y、X原子的最外层均满足8电子结构
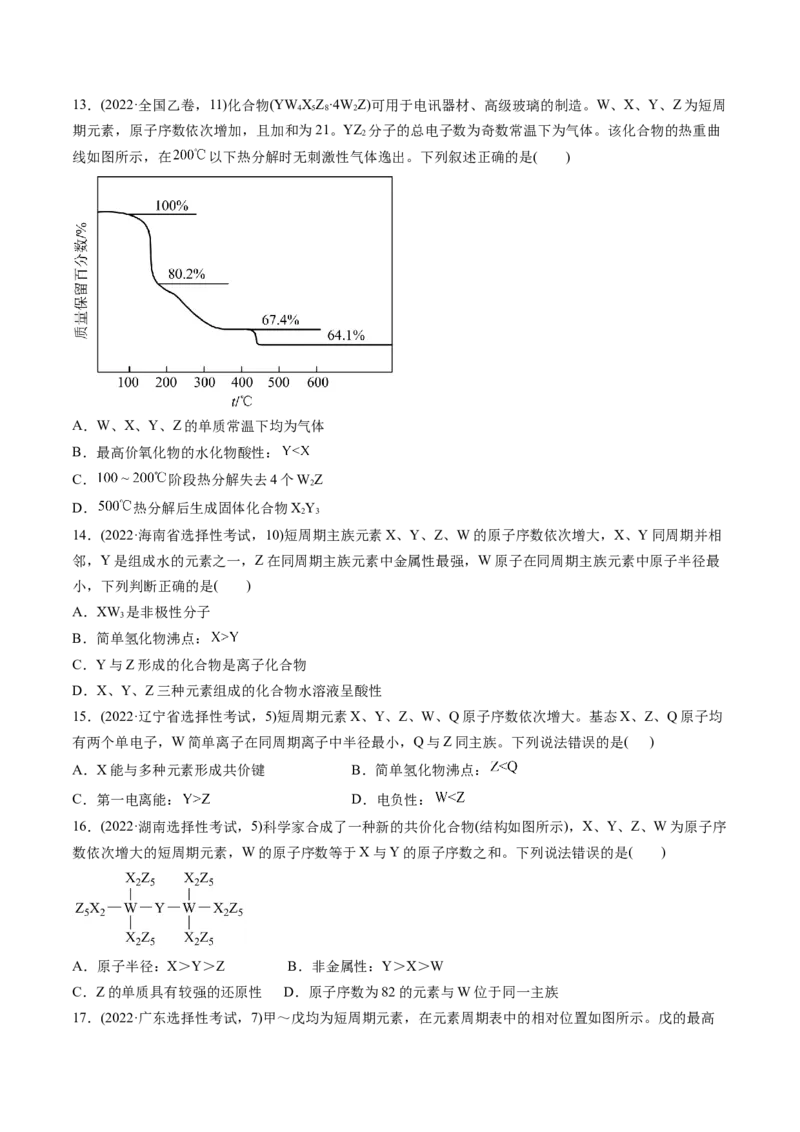
14.(2024·陕西西安·三模)物质m在军事上常用作烟幕剂,结构如图所示,其组成元素W、X、Y、Z是
原子序数依次增大的短周期主族元素,W与Y的核电核数之和等于Z的质子数,Y的游离态存在于火山喷
口附近。下列说法错误的是
A.简单氢化物的沸点:X>Y B.化合物m中每个原子最外层均达到8电子稳定结构
C.简单离子半径:Y>Z>W D. 和 均可用于自来水杀菌消毒
15.(2024·江苏·二模)短周期主族元素X、Y、Z、W、R的原子序数依次增加,X、Y、W位于不同周
期,原子序数:3Y=Z+R,常温下,X与Y可组成两种液体二元化合物。某种缓冲溶液的主要成分结构如
图。
下列有关说法错误的是A.简单氢化物的沸点:Y>Z
B.简单离子半径:Y>Z>W
C.W分别与X、Y组成的化合物均含离子键
D.电解WZ溶液可制得WYX、
1.(2024·甲卷)W、X、Y、Z为原子序数依次增大 短的周期元素。W和X原子序数之和等于 的核外电
子数,化合物 可用作化学电源的电解质。下列叙述正确的是
A.X和Z属于同一主族
B.非属性:
C.气态氢化物的稳定性:
D.原子半径:
2.(2024·江苏卷)我国探月工程取得重大进展。月壤中含有Ca、Fe等元素的磷酸盐,下列元素位于元素
周期表第二周期的是
A. O B. P C. Ca D. Fe
3.(2024·甘肃卷)X、Y、Z、W、Q为短周期元素,原子序数依次增大,最外层电子数之和为18。Y原子
核外有两个单电子,Z和Q同族,Z的原子序数是Q的一半,W元素的焰色试验呈黄色。下列说法错误的
是
A. X、Y组成的化合物有可燃性 B. X、Q组成的化合物有还原性
C. Z、W组成的化合物能与水反应 D. W、Q组成的化合物溶于水呈酸性
4.(2023·浙江省1月选考,10)X、Y、Z、M、Q五种短周期元素,原子序数依次增大。X的 轨道全充
满,Y的s能级电子数量是p能级的两倍,M是地壳中含量最多的元素,Q是纯碱中的一种元素。下列说
法不正确的是( )
A.电负性:
B.最高正价:
C.Q与M的化合物中可能含有非极性共价键
D.最高价氧化物对应水化物的酸性:
5.(2023·湖北省选择性考试,6)W、X、Y、Z为原子序数依次增加的同一短周期元素,其中X、Y、Z相
邻,W的核外电子数与X的价层电子数相等,Z 是氧化性最强的单质,4种元素可形成离子化合物(XY)+
2
(WZ)-。下列说法正确的是( )
4
A.分子的极性:WZ<XZ B.第一电离能:XY>Z>W B.原子半径:X