文档内容
考点 17 化学反应的热效应
(核心考点精讲精练)
一、3年真题考点分布
考点内容 考题统计
能源及其综合利用 2021全国乙卷卷1题,6分;2022广东卷3题,2分;
2022浙江6月选考18题,2分;2021浙江1月选考20
反应热的计算
题,2分;
盖斯定律运用
2022浙江1月选考18题,2分;2021浙江6月选考21
题,2分;2021北京卷14题,3分;
2023浙江1月选考14题,3分;2021浙江1月选考24
化学反应历程与反应机理图像分析 题,2分;2021广东卷14题,4分;2021湖北卷12题,3
分;
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,
化学反应与能量属于高考频考知识点,该考点主要在化学与生活、化学反应原理综合题型中出现,其
考查方式主要涉及:①利用盖斯定律求反应热,②利用盖斯定律书写热化学方程式,③能量大小比较,④
能源及其分析、环保,⑤热力学。熟练运用盖斯定律计算反应热是关键能力。
【备考策略】
化学变化的本质是有新物质的生成,并伴有能量的变化,能多角度、动态地分析热化学方程式,运用
化学原理解决实际问题。
(1)提高陌生文本的阅读能力,提高有效信息的提取能力;
(2)能够从微粒角度(微粒变化、化学键变化)分析物质的变化规律,并能够运用规律解决新问题;
(3)不同的省份应根据本省命题规律进行针对性地备考。
【命题预测】
预测2024年高考中仍会以综合题中的某一设问为主,也不排除以选择题的形式对盖斯定律的应及 ΔH
的大小比较进行考查。新课标明确了焓变与反应热的关系,反应热的考查内容将不断拓宽,对热化学方程
式的书写及盖斯定律的应用要求会有所提高,另外试题可能更加关注能源问题,以期引导考生形成与环境
和谐共处,合理利用自然资源的观念。训练时要对以图象、图表为背景考查能量变化、化学键键能、正逆
资料收集整理【淘宝店铺:向阳百分百】反应的活化能关系及简单计算多加关注。
考法 1 焓变
1.反应热(焓变)
(1)概念:在恒压条件下进行的反应的热效应。
符号:ΔH。
单位:kJ·mol-1或kJ/mol。
(2)表示方法
吸热反应:ΔH>0;放热反应:ΔH<0。
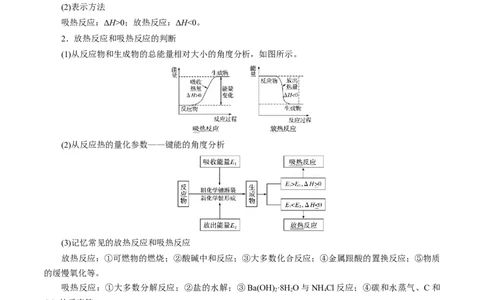
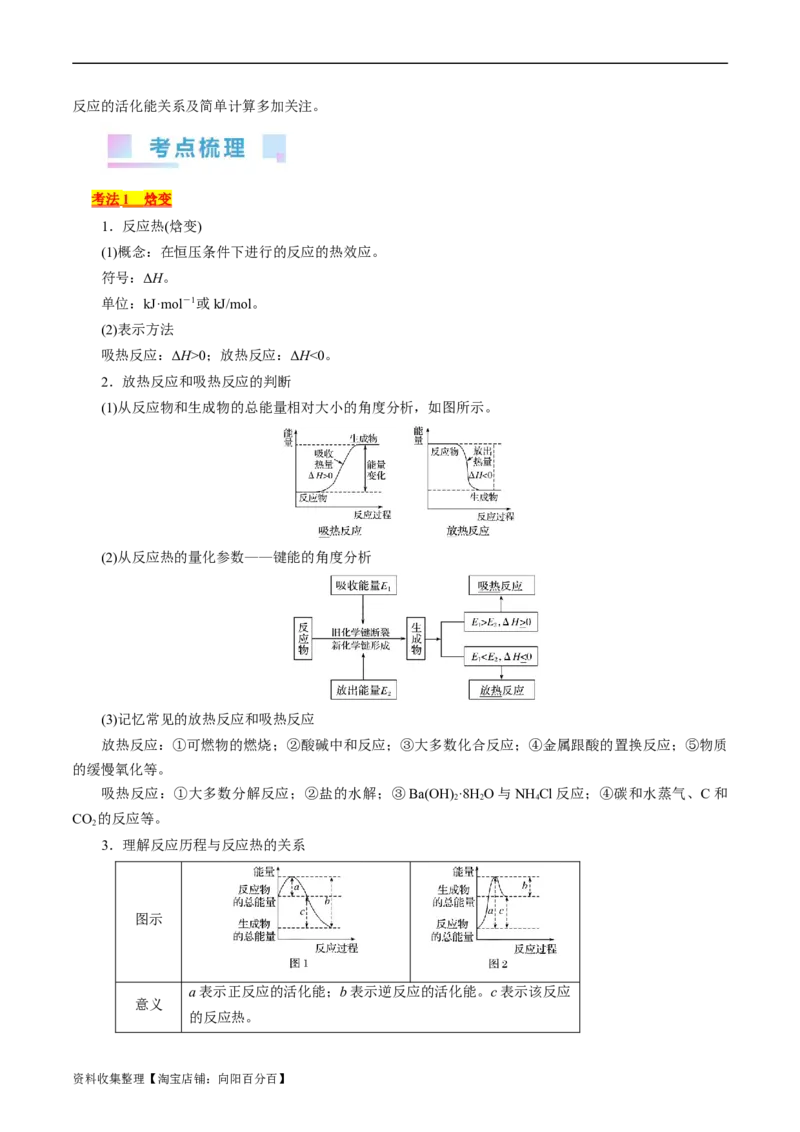
2.放热反应和吸热反应的判断
(1)从反应物和生成物的总能量相对大小的角度分析,如图所示。
(2)从反应热的量化参数——键能的角度分析
(3)记忆常见的放热反应和吸热反应
放热反应:①可燃物的燃烧;②酸碱中和反应;③大多数化合反应;④金属跟酸的置换反应;⑤物质
的缓慢氧化等。
吸热反应:①大多数分解反应;②盐的水解;③Ba(OH) ·8H O与NH Cl反应;④碳和水蒸气、C和
2 2 4
CO 的反应等。
2
3.理解反应历程与反应热的关系
图示
a表示正反应的活化能;b表示逆反应的活化能。c表示该反应
意义
的反应热。
资料收集整理【淘宝店铺:向阳百分百】图1:ΔH=(a-b) kJ·mol-1=-c kJ·mol-1,表示放热反应
ΔH
图2:ΔH=(a-b) kJ·mol-1=c kJ·mol-1,表示吸热反应
1.熟记反应热ΔH的基本计算公式
ΔH=生成物的总能量-反应物的总能量
ΔH=反应物的总键能之和-生成物的总键能之和
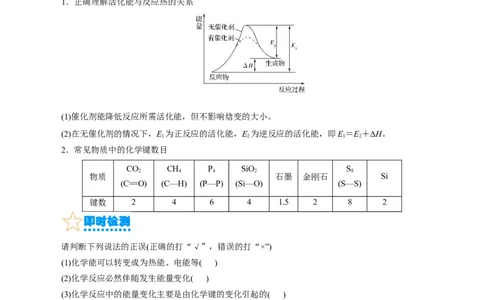
1.正确理解活化能与反应热的关系
(1)催化剂能降低反应所需活化能,但不影响焓变的大小。
(2)在无催化剂的情况下,E 为正反应的活化能,E 为逆反应的活化能,即E=E+ΔH。
1 2 1 2
2.常见物质中的化学键数目
CO CH P SiO S
2 4 4 2 8
物质 石墨 金刚石 Si
(C==O) (C—H) (P—P) (Si—O) (S—S)
键数 2 4 6 4 1.5 2 8 2
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)化学能可以转变成为热能、电能等( )
(2)化学反应必然伴随发生能量变化( )
(3)化学反应中的能量变化主要是由化学键的变化引起的( )
(4)化学反应中能量变化的多少与反应物的质量无关( )
(5)放热反应不需要加热就能反应,吸热反应不加热就不能反应( )
(6)吸热反应在任何条件下都不能发生( )
(7)活化能越大,表明反应断裂旧化学键需要克服的能量越高( )
(8)吸热反应中,反应物化学键断裂吸收的总能量高于生成物形成化学键放出的总能量( )
(9)同温同压下,反应H(g)+Cl(g)===2HCl(g)在光照和点燃条件下的ΔH不同( )
2 2
(10)可逆反应的ΔH表示完全反应时的热量变化,与反应是否可逆无关( )
(11)水蒸气变为液态水时放出的能量就是该变化的反应热( )
资料收集整理【淘宝店铺:向阳百分百】(12)同温同压下,反应H(g)+Cl(g)===2HCl(g)在光照和点燃条件下的ΔH不同( )
2 2
(13)可逆反应的ΔH表示完全反应时的热量变化,与反应是否可逆无关( )
答案:(1)√ (2)√ (3)√ (4)× (5)× (6)× (7)√ (8)√ (9)× (10)√ (11)× (12)× (13)√
例1 (2022·浙江省6月选考)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O HO HO
2 2 2 2 2
24
能量/ kJ·mol-l 218 39 10 0 0
9
可根据HO(g)+HO(g)= H O(g)计算出HO 中氧氧单键的键能为214 kJ·mol-l。下列说法不正确的是(
2 2 2 2
)
A.H 的键能为436 kJ·mol-l
2
B.O 的键能大于HO 中氧氧单键的键能的两倍
2 2 2
C.解离氧氧单键所需能量: HOO<HO
2 2
D.HO(g)+O(g)= H O(g) ΔH=-143kJ·mol−1
2 2 2
【答案】C
【解析】A项,根据表格中的数据可知,H 的键能为218×2=436 kJ·mol-l,A正确;
2
B项,由表格中的数据可知O 的键能为:249×2=498 kJ·mol-l,由题中信息可知HO 中氧氧单键的键能为
2 2 2
214 kJ·mol-l,则O 的键能大于HO 中氧氧单键的键能的两倍,B正确;C项,由表格中的数据可知
2 2 2
HOO=HO+O,解离其中氧氧单键需要的能量为249+39-10=278 kJ·mol-l,HO 中氧氧单键的键能为214
2 2
kJ·mol-l,C错误;D项,由表中的数据可知HO(g)+O(g)= H O(g)的 ,D
2 2 2
正确;故选C。
例2 (2020•浙江7月选考)关于下列ΔH的判断正确的是( )
CO(aq)+H+(aq)===HCO(aq) ΔH
1
CO(aq)+HO(l)HCO(aq)+OH−(aq) ΔH
2 2
OH−(aq)+H+(aq)===HO(l) ΔH
2 3
OH−(aq)+CHCOOH(aq)===CHCOO−(aq)+HO(l) ΔH
3 3 2 4
A.ΔH<0 ΔH<0 B.ΔH<ΔH C.ΔH<0 ΔH>0 D.ΔH>ΔH
1 2 1 2 3 4 3 4
【答案】B
【解析】碳酸氢根的电离属于吸热过程,则CO(aq)+H+(aq)=HCO- (aq)为放热反应,所以△H<0;
3 1
CO(aq)+H O(l) HCO - (aq)+OHˉ(aq)为碳酸根的水解离子方程式,CO的水解反应为吸热反应,所以
2 3
△H>0;OHˉ(aq)+H+(aq)=H O(l)表示强酸和强碱的中和反应,为放热反应,所以△H<0;醋酸与强碱的中
2 2 3
资料收集整理【淘宝店铺:向阳百分百】和反应为放热反应,所以△H<0;但由于醋酸是弱酸,电离过程中会吸收部分热量,所以醋酸与强碱反应
4
过程放出的热量小于强酸和强碱反应放出的热量,则△H> H;综上所述,只有△H< H 正确,故选
4 3 1 2
B。 △ △
对点1 某反应2A=3B,它的反应能量变化曲线如图所示,下列有关叙述正确的是( )
A.该反应为吸热反应 B.A比B更稳定
C.加入催化剂会改变反应的焓变 D.整个反应的ΔH=E -E
1 2
【解析】A项,由图象可知物质A、B的能量相对大小,A比B能量高,所以A→B释放能量,是放
热反应,A错误;B项,B能量比A的低,故B更稳定,B错误;C项,催化剂能改变反应途径和活化能
大小,但不能改变焓变,C错误;D项,整个反应先吸收E 的能量,再放出E 的能量,所以ΔH=E-E ,D
1 2 1 2
正确;故选D。
对点2 某化学反应A(g)+B (g)=2AB(g)的能量变化如图所示,则下列说法中正确的是( )
2 2
A.该反应为放热反应,无需加热就可以发生
B.断裂1molA-A键和1molB-B键要吸收xkJ的能量
C.根据图示可知生成1molAB (g)放出 的能量
D.三种物质A(g)、B (g)、AB(g)中,最稳定的物质一定是AB(g)
2 2
【答案】B
【解析】A项,由图可知反应物总能量高于生成物能量为放热反应,但A-A键和B-B键断裂需要吸收
能量,可能需要加热破坏反应物化学键以发生反应,反应放热与反应是否需要加热无关,选项A错误;B
项,断裂1moLA-A键和1molB-B键要吸收xkJ的能量,选项B正确;C项,根据图示可知生成1mol AB
资料收集整理【淘宝店铺:向阳百分百】(g)放出 的能量,选项C错误;D项,物质能量越低越稳定,由图知A(g)和B (g)的总能量高
2 2
于2 AB (g)的能量,但不知单独物质的能量大小,所以无法确定谁最稳定,选项D错误;故选B。
考法 2 热化学方程式
1.概念
表示参加反应物质的量和反应热的关系的化学方程式。
2.意义
表明了化学反应中的物质变化和能量变化。
如:2H(g)+O(g)===2H O(l) ΔH=-571.6 kJ·mol-1
2 2 2
表示:2 mol氢气和1 mol氧气反应生成2 mol液态水时放出571.6 kJ的热量。
3.书写要求
(1)注明反应的温度和压强(25 ℃、101 kPa下进行的反应可不注明)。
(2)注明反应物和生成物的状态:固态(s)、液态(l)、水溶液(aq)、气态(g)。
(3)热化学方程式中各物质的化学计量数只表示物质的物质的量,而不表示分子个数(或原子个数),因
此可以写成分数。
(4)热化学方程式中不用“↑”和“↓”。
(5)由于ΔH与反应物的物质的量有关,所以热化学方程式中物质的化学计量数必须与 ΔH相对应,如
果化学计量数加倍,则ΔH也要加倍。当反应向逆反应方向进行时,其反应热与正反应的反应热数值相等,
符号相反。
1.书写热化学方程式的程序
2.书写热化学方程式要“五查”
(1)查热化学方程式是否配平。
(2)查各物质的聚集状态是否正确。
(3)查ΔH的“+”“-”符号是否正确。
(4)查反应热的单位是否为kJ·mol-1。
资料收集整理【淘宝店铺:向阳百分百】(5)查反应热的数值与化学计量数是否对应。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)热化学方程式中,化学计量数只代表物质的量,不代表分子数( )
(2)对于可逆反应,热化学方程式后的ΔH代表前面的化学计量数对应物质的量的物质完全反应时的热
效应( )
(3)正逆反应的ΔH相等( )
(4)反应条件(点燃或加热)对热效应有影响,所以热化学方程式必须注明反应条件( )
(5)比较ΔH大小,只需比较数值,不用考虑正负号( )
(6)热化学方程式中的化学计量数与ΔH成正比( )
(7)物质的状态不同ΔH的数值也不同( )
(8)当反应逆向进行时,其反应热与正反应热的反应热数值相等,符号相反( )
(9)2H O(l)===2H (g)+O(g) ΔH>0( )
2 2 2
(10)C(石墨,s)===C(金刚石,s) ΔH>0,说明石墨比金刚石稳定( )
答案:(1) √ (2)√ (3)× (4)× (5)× (6)√ (7)√ (8)√ (9)√ (10)√
例1 已知一定温度和压强下:2H(g)+O(g)===2H O(g) ΔH =-a kJ·mol-1,下列叙述不正确的是(
2 2 2 1
)
A.2 mol H (g)和1 mol O (g)完全反应生成2 mol H O(g)时放出a kJ的热量
2 2 2
B.2 mol H O(g)完全分解为2 mol H (g)和1 mol O (g)时吸收a kJ的热量
2 2 2
C.2 mol H (g)和1 mol O (g)完全反应生成2 mol H O(l)时放出的热量小于a kJ
2 2 2
D.1 mol H (g)和0.5 mol O(g)完全反应生成1 mol H O(g)时放出0.5a kJ的热量
2 2 2
【答案】C
【解析】由热化学方程式知,A正确;反应逆向发生时热量的数值不变,B正确;等量的反应物生成
液态水比生成气态水放出的热量多,C错误;反应物的物质的量减半,反应热也减半,D正确。
例2 工业生产硫酸过程中,SO 在接触室中被催化氧化为SO 气体,已知该反应为放热反应。现将2
2 3
mol SO 、1 mol O 充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO 的转化率为50%,则下列
2 2 2
热化学方程式正确的是( )
A.2SO (g)+O(g) 2SO (g) ΔH=+196.6 kJ·mol-1
2 2 3
B.2SO (g)+O(g) 2SO (g) ΔH=-98.3 kJ·mol-1
2 2 3
C.SO (g)+ O(g) SO (g) ΔH=-98.3 kJ·mol-1
2 2 3
资料收集整理【淘宝店铺:向阳百分百】D.SO (g)+ O(g) SO (g) ΔH=-196.6 kJ·mol-1
2 2 3
【答案】C
【解析】2mol SO 、1mol O 充入恒容容器中,达平衡时,SO 的转化率为50%,则反应了的SO 的物
2 2 2 2
质的量为1mol,放出热量98.3kJ,则每反应1molSO ,放出98.3kJ的热量,故热化学方程式为:2SO (g)
2 2
+O (g) 2SO (g) H=-196.6 kJ•mol-1或SO (g)+ O(g) SO (g),△H=-98.3 kJ•mol-1,由此判
2 3 2 2 3
△
断各选项热化学方程式正误。A项,反应是放热反应,ΔH小于0,故A错误;B项,热化学方程式中反应
热和对应二氧化硫的量不符合,故B错误;C项,选项中的热化学方程式符合题意,故C正确;D项,热
化学方程式中反应热和对应二氧化硫的量不符合,故D错误;故选C。
对点1 下列热化学方程式正确的是( )
选项 已知条件 热化学方程式
A H 的燃烧热为a kJ·mol-1 H+Cl=====2HCl ΔH=-a kJ·mol-1
2 2 2
1 mol SO 、0.5 mol O 完全反应,放 2SO (g)+O(g) 2SO (g) ΔH=-98.3
B 2 2 2 2 3
出热量98.3 kJ kJ·mol-1
H+(aq)+OH-(aq)=== HSO (aq)+Ba(OH) (aq)===
2 4 2
C
HO(l) ΔH=-57.3 kJ·mol-1 BaSO(s)+2HO(l) ΔH=-114.6 kJ·mol-1
2 4 2
P(白磷,s)===4P(红磷,s)
4
D 31 g白磷比31 g红磷能量多b kJ
ΔH=-4b kJ·mol-1
【答案】D
【解析】选项A中符合已知条件的应是H 和O 反应,A错;ΔH应为-196.6 kJ·mol-1,B错;选项C
2 2
中由于生成BaSO 沉淀,放出的热量大于114.6 kJ,C错。
4
对点2 根据如图所给信息,得出的结论正确的是( )
资料收集整理【淘宝店铺:向阳百分百】A.48 g碳完全燃烧放出热量为1 574 kJ/mol
B.2C(s)+O(g)===2CO(g) ΔH=-221.0 kJ/mol
2
C.2CO(g)===2CO(g)+O(g) ΔH=+283.0 kJ/mol
2 2
D.C(s)+O(g)===CO (s) ΔH=-393.5 kJ/mol
2 2
【答案】B
【解析】48 g C完全燃烧放热为393.5 kJ/mol×4 mol=1 574 kJ,不是1 574 kJ/mol,故A错误;据图示
可知,1 mol C燃烧生成CO放热393.5 kJ-283.0 kJ=110.5 kJ,所以2 mol C燃烧生成CO放热221.0 kJ,
故B正确;1 mol CO燃烧生成1 mol二氧化碳放热283.0 kJ,所以2CO(g)===2CO(g)+O(g) ΔH=+
2 2
566.0 kJ/mol,故C错误;应该生成二氧化碳气体,不是固态,故D错误。
考法 3 燃烧热、中和热、能源
1.标准燃烧热
(1)概念:在101 kPa时,1 mol纯物质完全燃烧生成稳定的氧化物时的反应热。标准燃烧热的单位一般
用kJ·mol-1表示。
标准燃烧热的限定词有恒压(101 kPa时)、可燃物的物质的量(1 mol)、完全燃烧、稳定的氧化物等,其
中的“完全燃烧”,是指物质中下列元素完全转变成对应的氧化物:C→CO(g),H→H O(l),S→SO (g)等。
2 2 2
(2)表示的意义:例如:C的标准燃烧热为393.5 kJ·mol-1,表示在101 kPa时,1 mol C完全燃烧生成
CO 气体时放出393.5 kJ的热量。
2
(3)书写热化学方程式:标准燃烧热是以1 mol物质完全燃烧所放出的热量来定义的,因此在书写它的
热化学方程式时,应以燃烧 1 mol 物质为标准来配平其余物质的化学计量数。例如:C H (l)+
8 18
O(g)===8CO (g)+9HO(l) ΔH=-5 518 kJ·mol-1,即C H 的标准燃烧热ΔH为-5 518 kJ·mol-1。
2 2 2 8 18
(4)标准燃烧热的计算:可燃物完全燃烧放出的热量的计算方法为Q =n(可燃物)×|ΔH|。式中:Q 为
放 放
可燃物燃烧反应放出的热量;n为可燃物的物质的量;ΔH为可燃物的标准燃烧热。
2.中和热
(1)概念:在稀溶液中,强酸跟强碱发生中和反应生成1mol液态HO时的反应热。
2
(2)注意几个限定词:①稀溶液;②产物是1 mol液态HO;③用热化学方程式可表示为OH-(aq)+H+
2
(aq)===H O(l) ΔH=-57.3 kJ·mol-1。
2
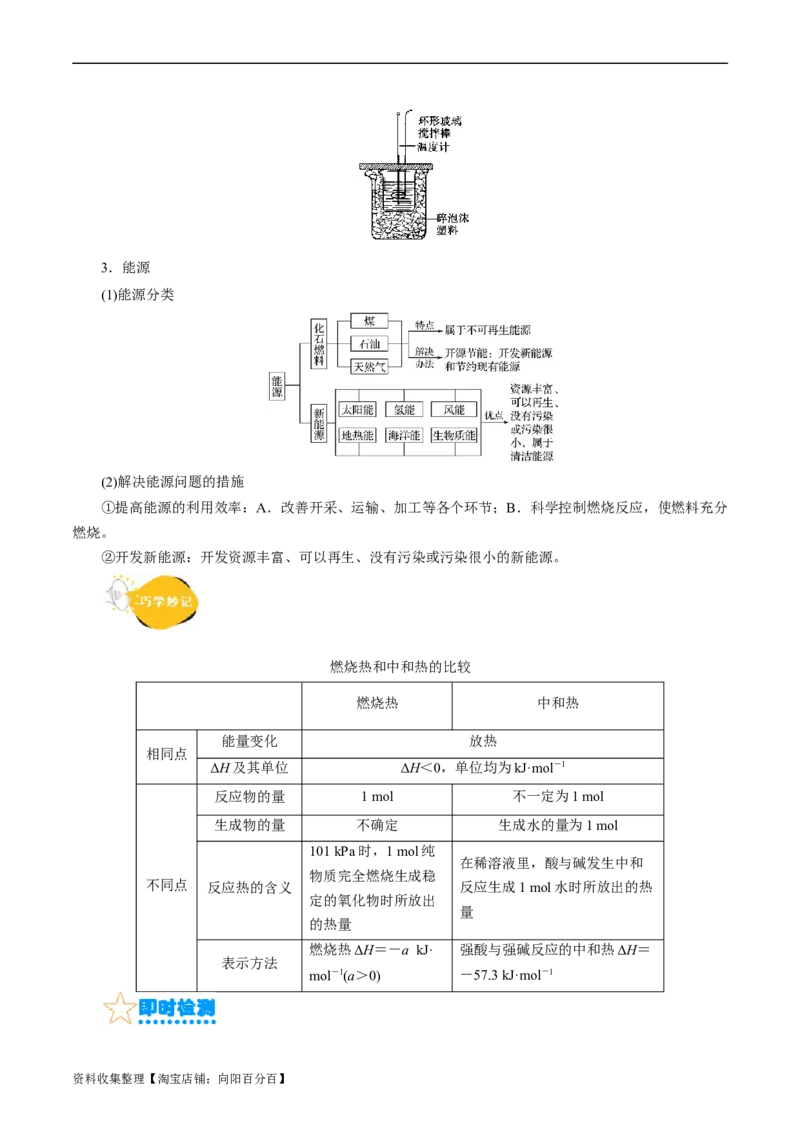
(3)中和热的测定
①测定原理:ΔH=-
c=4.18 J·g-1·℃-1=4.18×10-3 kJ·g-1·℃-1;n为生成HO的物质的量。
2
②装置如图
资料收集整理【淘宝店铺:向阳百分百】3.能源
(1)能源分类
(2)解决能源问题的措施
①提高能源的利用效率:A.改善开采、运输、加工等各个环节;B.科学控制燃烧反应,使燃料充分
燃烧。
②开发新能源:开发资源丰富、可以再生、没有污染或污染很小的新能源。
燃烧热和中和热的比较
燃烧热 中和热
能量变化 放热
相同点
ΔH及其单位 ΔH<0,单位均为kJ·mol-1
反应物的量 1 mol 不一定为1 mol
生成物的量 不确定 生成水的量为1 mol
101 kPa时,1 mol纯
在稀溶液里,酸与碱发生中和
物质完全燃烧生成稳
不同点 反应热的含义 反应生成1 mol水时所放出的热
定的氧化物时所放出
量
的热量
燃烧热ΔH=-a kJ· 强酸与强碱反应的中和热ΔH=
表示方法
mol-1(a>0) -57.3 kJ·mol-1
资料收集整理【淘宝店铺:向阳百分百】