文档内容
考点 17 化学反应的热效应
【基础过关】
1.化学反应中的能量变化,通常主要表现为热量的变化。下列相关表述正确的是( )
A.一定条件下,将0.5molH(g)和0.5molI (g)置于密闭容器中充分反应生成 放热 ,其热化学方
2 2
程式为:I(g )+H (g) 2HI(g) H=-2akJ•mol-1
2 2
△
B.在101kPa时,2 g H 完全燃烧生成液态水,放出 热量,表示氢气燃烧热的热化学方程式
2
表示为:
C.S(g)+ O (g)=SO(g) ΔH S(g)+ O (g)=SO(g) ΔH ΔH>ΔH
2 2 1 2 2 2 1 2
D.HCl和NaOH反应的中和热 ,则0.5molHSO 和足量Ba(OH) 反应的
2 4 2
【答案】B
【解析】A项, 一定条件下,将0.5molH(g)和0.5molI (g)置于密闭容器中充分反应生成HI放热于
2 2
akJ,则I 和H 反应生成1molHI(g)时放热大于akJ,放热焓变为负,则其热化学方程式I(g )+H (g)
2 2 2 2
2HI(g) H<-2akJ•mol-1,故A错误; B项,燃烧热是指在一定压强下,1 mol的可燃物完全燃烧生成稳定
的氧化△物的时候所放出的热量;在101kPa时,2 gH
2
完全燃烧生成液态水,放出于285.8akJ热量,表示氢
气燃烧热的热化学方程式表示为: ,B正确;C项,硫蒸气的能
量比等质量的固态硫能量高、则等量的硫蒸汽燃烧生成二氧化硫气体比固态硫燃烧放出的热量多,焓变为
负值时,放出热量越多,焓变越小,则S(g)+ O (g)=SO(g) ΔH S(g)+ O (g)=SO(g) ΔH ΔH<ΔH,
2 2 1 2 2 2 1 2
故C错误;D项,HCl和NaOH反应的中和热ΔH =-57.3kJ•mol-1,硫酸和足量Ba(OH) 反应生成硫酸钡沉
2
淀和水,由于生成沉淀,也要放热,则0.5molHSO 和足量Ba(OH) 反应放出的热量大于盐酸和氢氧化钠
2 4 2
反应1mol液态HO时放出的热量、即大于57.3kJ,则0.5molHSO 和足量Ba(OH) 反应的ΔH
2 2 4 2
<-57.3kJ•mol-1,故D错误;故选B。
2.根据以下热化学方程式,ΔH 和ΔH 的大小比较错误的是( )
1 2
A.Br (g)+H(g)=2HBr(g) ΔH ,Br (l)+H (g)=2HBr(g) ΔH ,则有ΔH<ΔH
2 2 1 2 2 2 1 2
B.2HS(g)+3O(g)=2SO(g)+2HO(l) ΔH ,2HS(g)+O(g)=2S(s)+2HO(l) ΔH ,则有ΔH>ΔH
2 2 2 2 1 2 2 2 2 1 2
C.4Al(s)+3O (g)=2Al O(s) ΔH ,4Fe(s)+3O (g)=2Fe O(s) ΔH ,则有ΔH<ΔH
2 2 3 1 2 2 3 2 1 2
D.C(s)+O(g)=CO (g) ΔH ,C(s)+O(g)=CO(g) ΔH ,则有ΔH<ΔH
2 2 1 2 2 1 2
【答案】B
资料收集整理【淘宝店铺:向阳百分百】【解析】A项,依据盖斯定律分析,液态溴变化为气态溴需要吸收热量,反应是放热反应,焓变是负
值,所以△H<△H,A正确;B项,S燃烧生成二氧化硫放热,反应是放热反应,焓变是负值,所以
1 2
△H<△H,B错误;C项,铝活泼性大于铁,能量高于铁,反应是放热反应,焓变是负值,△H<
1 2 1
△H,C正确;D项,碳完全燃烧放出的热量大于不完全燃烧生成CO放出的热量,反应是放热反应,焓
2
变是负值,所以△H<△H,D正确;故选B。
1 2
3.(2023·湖北省部分学校高三联考)下列对热化学方程式的解读或书写正确的是( )
A.已知 ΔH>0,则石墨比金刚石稳定
B.已知①S(g)+O(g) SO (g) ΔH;②S(s)+O (g) SO (g) ΔH,则ΔH>ΔH
2 2 1 2 2 2 1 2
C.已知甲烷燃烧热为 ,则甲烷燃烧的热化学方程式可以表示为CH (g)+
4
2O(g)=CO (g)+ 2HO(g) ΔH=-890.3 kJ·mol-1
2 2 2
D.已知中和热 ,则1mol硫酸和足量稀NaOH溶液反应的反应热就是中和热
【答案】A
【解析】A项, 已知 ΔH>0,说明石墨的能量较低,金刚石的能量高,能
量越高越不稳定,所以石墨比金刚石稳定,A正确;B项,气态硫比固态硫能量大,故燃烧时要放出更多
的热量,所以ΔH 的数值大,燃烧放热,焓变都是负值,数值越大,负数反而越小,所以ΔH<ΔH,B错
1 1 2
误;C项,甲烷燃烧的热化学方程式中,应该生成液态水,C错误;D项,1mol硫酸和足量稀NaOH溶液
反应生成2molH O,不是中和热,D错误;故选A。
2
4.(2023·河北省邯郸市部分学校高三联考)依据下列含硫物质转化的热化学方程式,得出的相关结论
正确的是( )
①S(g)+CO(g) SO (g) ΔH
2 2 1
②S(s)+CO(g) SO (g) ΔH
2 2 2
③2HS(g)+ O(g) 2S(s)+ HO(1) ΔH
2 2 2 3
④2HS(g)+3 O(g) 2SO (g)+ HO(1) ΔH
2 2 2 2 4
⑤2HS(g)+SO(g) 3S(s)+ 2HO(1) ΔH
2 2 2 5
A.ΔH>ΔH B.ΔH<ΔH
1 2 3 4
C.ΔH=ΔH+ΔH D.2ΔH=3ΔH-ΔH
4 2 3 5 3 4
【答案】D
【解析】A项, 气态S的能量比固体S的大,所以气态S燃烧时放出的热量多,放热反应的ΔH为负
数,绝对值大的ΔH反而小,故A错误;B项,反应③是HS的不完全燃烧,反应④是HS的完全燃烧,
2 2
完全燃烧放出的热量多,放热反应的ΔH为负数,绝对值大的ΔH反而小,所以ΔH>ΔH,故B错误;C
3 4
资料收集整理【淘宝店铺:向阳百分百】项,根据盖斯定律,②×2+③得2HS(g)+3 O (g) 2SO (g)+ H O(1) ΔH=2ΔH+ΔH,故C错误;D
2 2 2 2 4 2 3
项,根据盖斯定律[③×3-④] 得 ,故D正确;故
选D。
5.(2023·广东省蕉岭县蕉岭中学高三第二次质检)已知:2CO(g)+O(g)=2CO (g) ΔH=-566kJ/mol
2 2
2NaO(s)+2CO(g)=2Na CO(s)+O(g) ΔH=-452kJ/mol
2 2 2 2 3 2
下列说法正确的是( )
A.28克CO完全燃烧,放出热量为283J
B.NaO(s)+CO(g)=Na CO(s)+ O(g) ΔH=+226kJ/mol
2 2 2 2 3 2
C.CO(g)与NaO(s)反应放出509kJ热量时,电子转移数为1.204×1024
2 2
D.CO的燃烧热为283kJ/mol
【答案】D
【解析】A项, 28克CO完全燃烧,相当于1molCO完全燃烧。第一个热化学方程式中ΔH是
2molCO完全燃烧所产生的的热量,所以由此可知1molCO完全燃烧,放出的热量为 KJ,故A
错误;B项,NaO(s)+CO(g)=Na CO(s)+ O(g)与第二个热化学方程式有关,相当于第二个热化学方程
2 2 2 2 3 2
式除以2,所以NaO(s)+CO(g)=Na CO(s)+ O(g) ΔH=-226kJ/mol ,故B错误;C项,①2CO(g)+
2 2 2 2 3 2
O(g)=2CO(g) ΔH=-566 kJ/mol、②NaO(s)+CO(g)=NaCO(s)+ O(g) ΔH=-226 kJ/mol,则根据
2 2 2 2 2 2 3 2
盖斯定律可知①× +②即得到NaO(s)+CO(g)=NaCO(s),所以该反应的反应热△H=-566 kJ/mol×
2 2 2 3
-226 kJ/mol=-509kJ/mol。在反应中碳元素化合价从+2价升高到+4价,失去2个电子。因此CO(g)与
NaO(s)反应放出509 kJ热量时,电子转移数为2×6.02×1023 ,但CO(g)与NaO(s)反应未指明生成物状态,
2 2 2 2
故C错误;D项,燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量,①2CO(g)+O(g)=
2
2CO(g) ΔH=-566 kJ/mol,所以CO的燃烧热为△H=-566 kJ/mol× =-283 kJ/mol ,故D正确; 故选
2
D。
6.(2023·河南省濮阳市南乐一高高三月考)下列示意图表示正确的是( )
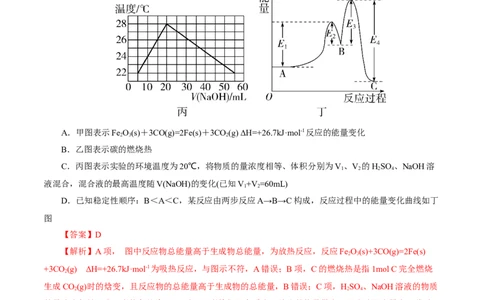
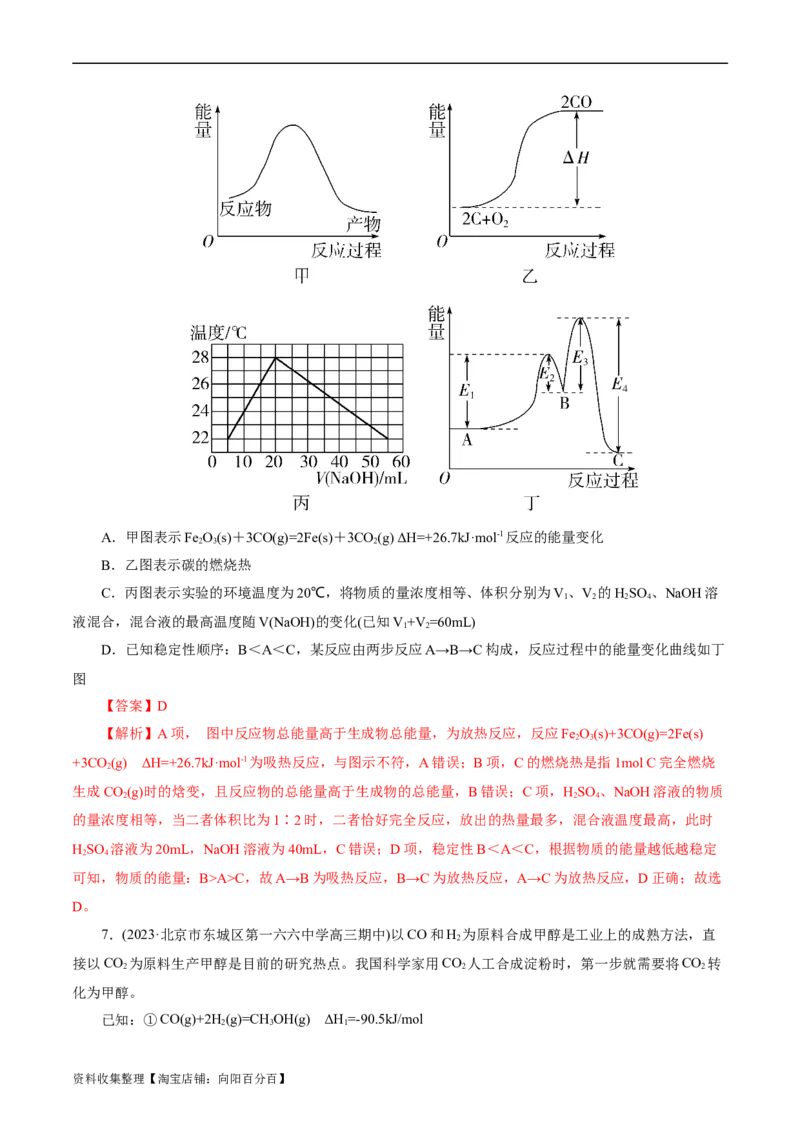
资料收集整理【淘宝店铺:向阳百分百】A.甲图表示Fe O(s)+3CO(g)=2Fe(s)+3CO(g) ΔH=+26.7kJ·mol-1反应的能量变化
2 3 2
B.乙图表示碳的燃烧热
C.丙图表示实验的环境温度为20℃,将物质的量浓度相等、体积分别为V、V 的HSO 、NaOH溶
1 2 2 4
液混合,混合液的最高温度随V(NaOH)的变化(已知V+V =60mL)
1 2
D.已知稳定性顺序:B<A<C,某反应由两步反应A→B→C构成,反应过程中的能量变化曲线如丁
图
【答案】D
【解析】A项, 图中反应物总能量高于生成物总能量,为放热反应,反应Fe O(s)+3CO(g)=2Fe(s)
2 3
+3CO (g) ΔH=+26.7kJ·mol-1为吸热反应,与图示不符,A错误;B项,C的燃烧热是指1mol C完全燃烧
2
生成CO(g)时的焓变,且反应物的总能量高于生成物的总能量,B错误;C项,HSO 、NaOH溶液的物质
2 2 4
的量浓度相等,当二者体积比为1∶2时,二者恰好完全反应,放出的热量最多,混合液温度最高,此时
HSO 溶液为20mL,NaOH溶液为40mL,C错误;D项,稳定性B<A<C,根据物质的能量越低越稳定
2 4
可知,物质的能量:B>A>C,故A→B为吸热反应,B→C为放热反应,A→C为放热反应,D正确;故选
D。
7.(2023·北京市东城区第一六六中学高三期中)以CO和H 为原料合成甲醇是工业上的成熟方法,直
2
接以CO 为原料生产甲醇是目前的研究热点。我国科学家用CO 人工合成淀粉时,第一步就需要将CO 转
2 2 2
化为甲醇。
已知:①CO(g)+2H(g)=CH OH(g) ΔH =-90.5kJ/mol
2 3 1
资料收集整理【淘宝店铺:向阳百分百】②CO(g)+HO(g)=CO(g)+H(g) ΔH =-41.1kJ/mol
2 2 2 2
③2H(g)+ O (g)=2HO(g) ΔH =-483.6kJ/mol
2 2 2 3
下列说法不正确的是( )
A.若温度不变,反应①中生成1 mol CH OH(l)时,放出的热量大于90.5 kJ
3
B.CO 与H 合成甲醇的热化学方程式为:CO(g)+3H(g)=CH OH(g)+H O(g) ΔH=-49.4kJ/mol
2 2 2 2 3 2
C.通过电解制H 和选用高效催化剂,可降低CO 与H 合成甲醇反应的焓变
2 2 2
D.以CO 和HO为原料合成甲醇,同时生成O,该反应需要吸收能量
2 2 2
【答案】C
【解析】A项,1mol CHOH(g)能量高于 1mol CHOH(l),反应物的总能量相同,根据能量守恒定律,
3 3
若温度不变,反应国中生成1mol CHOH(l)时,放出的热量大于90.5kJ,故 A 正确;B项,根据盖斯定律,
3
①—②得CO(g)+3H(g)=CH OH(g)+H O(g) ΔH=ΔH -ΔH =-49.4kJ/mol,故B正确;C项,催化剂可降低
2 2 3 2 1 1
CO 与H 合成甲醇反应的活化能,但不改变反应的焓变,故C错误;D项,已知反应④CO(g)
2 2 2
+3H (g)=CH OH(g)+H O(g) ΔH=-49.4kJ/mol,根据盖斯定律④×2—③×3得2CO(g)+4HO(g)=2CHOH(g)
2 3 2 2 2 3
+3O (g) ΔH=2ΔH -3ΔH =1352kJ/mol>0,,则该反应需要吸收能量,故 D 正确;故选C。
2 4 3
8.(2023·浙江省温州市高三第一次适应性考试)标准状态下,1mol纯物质的相对能量及解离为气态原
子时所消耗的能量如下表所示:
物质 O(g) N(g) NO g) C(s,石墨) CH(g) CO(g)
2 2 2 4 2
相对能量/ kJ·mol−1 0 0 x 0 -75 -393.5
解离总耗能/kJ 498 946 632 717 1656 y
下列说法正确的是( )
A.x =180
B.逐级断开CH(g)中的每摩尔C—H所消耗的能量均为414kJ
4
C.解离每摩尔C(s,石墨)中的碳碳键平均耗能为239kJ
D.根据NO(g)+CH(g) CO(g)+N(g)+2H O(g)的ΔH可计算出H—O键能
4 2 2
【答案】D
【解析】A项,焓变=生成物总能量-反应物总能量,则N(g)+O(g) 2NO(g) ΔH=2x
2 2
kJ·mol−1,焓变=反应物总键能-生成物总键能,即498+946-632×2=2x,x =90,故A错误;B项,逐级断开
CH(g)中的每摩尔C—H所消耗的能量不相等,故B错误;C项,石墨晶体中每个碳原子形成3条共价键,
4
两个碳原子形成1条键,则1mol石墨含有1.5molC-C键,解离每摩尔C(s,石墨)中的碳碳键平均耗能为
478kJ,故C错误;D项,焓变=反应物总键能-生成物总键能,C(s,石墨)+O (g) CO(g)的ΔH可计算
2 2
出y值,再根据NO(g)+CH(g) CO(g)+N(g)+2H O(g)的ΔH可计算出H—O键能,故D正确;故选
4 2 2
资料收集整理【淘宝店铺:向阳百分百】D。
9.(2023·浙江省浙南名校联盟高三第二次联考)已知有如下三个烯烃加成反应
Ⅰ kJmol
⋅
Ⅱ kJmol
⋅
Ⅲ kJmol
⋅
则下列说法不正确的是( )
A.由题可知丁烯稳定性是Ⅲ>Ⅱ>Ⅰ
B.由题可知断裂碳碳π键和氢氢σ键所消耗的能量总是小于形成两个碳氢σ键所放出的能量
C.由题可知烯烃的稳定性与双键碳上的取代基和构型有关
D.由题可知,由于Ⅰ、Ⅱ、Ⅲ断键和成键都一样,因此反应的 不能由键能计算得到
【答案】D
【解析】A项,根据物质的能量越低越稳定,由热化学方程式可知放出的能量Ⅰ>Ⅱ>Ⅲ,说明丁烯
的能量大小为Ⅰ>Ⅱ>Ⅲ,稳定性为Ⅲ>Ⅱ>Ⅰ,故A正确;B项,三个反应都是放热反应,由题可知断
裂碳碳π键和氢氢σ键所消耗的能量总是小于形成两个碳氢σ键所放出的能量,故B正确;C项,由题可
知烯烃的稳定性与双键碳上的取代基和构型有关,取代基越多,越稳定,反式比顺式结构稳定,故C正确;
D项,反应的ΔH能由键能计算得到,反应焓变ΔH=反应物总键能-生成物总键能,故D错误;故选D。
10.(2023·浙江省诸暨市高三适应性考试)甲醇与水蒸气在催化剂作用下发生如下反应:
反应Ⅰ:CHOH(g) CO (g)+ 2H(g) ΔH
3 2 1
反应Ⅱ:CO (g)+ HO(g) CO (g)+ H(g) ΔH
2 2 2 2
根据能量变化示意图,下列说法正确的是( )
A.E-E >E-E
3 2 4 1
资料收集整理【淘宝店铺:向阳百分百】B.反应Ⅱ决定整个反应的速率
C.催化剂可以降低总反应的焓变
D.CHOH(g)+HO(g) CO(g)+3H(g) ΔH=ΔH -ΔH
3 2 2 2 1 2
【答案】A
【解析】A项,由于绝对值 ,该值为负值,去掉绝对值后,E-E >E-E ,A正确;
3 2 4 1
B项,由图可知,反应I正反应的活化能为E-E ,反应II的活化能为E-E ,反应I的活化能较大,则反应
1 5 2 3
I的反应速率慢于反应II,反应I决定整个反应的速率,B错误;C项,催化剂可改变反应的活化能,反应
的焓变由始态和终态决定,催化剂不改变焓变,C错误;D项,根据盖斯定律,反应I+II可得目标方程
CHOH(g)+HO(g) CO(g)+3H(g) ΔH=ΔH +ΔH ,D错误;故选A。
3 2 2 2 1 2
11.在一定温度压强下,依据图示关系,下列说法不正确的是( )
A.C(石墨)+ CO (g) =2CO(g) ΔH=ΔH-ΔH
2 1 2
B.1mol C(石墨)和1mol C(金刚石)分别与足量O 反应全部转化为CO(g) ,前者放热多
2 2
C.ΔH=ΔH-ΔH
5 1 3
D.化学反应的△H,只与反应体系的始态和终态有关,与反应途径无关
【答案】B
【解析】A项,由题干信息可知,反应I:C(石墨)+ (g)=CO(g) ΔH 反应II:CO(g)+
1
(g)=CO (g) ΔH,则反应I-反应II得C(石墨)+ CO (g) =2CO(g),根据盖斯定律可知ΔH=ΔH-ΔH,A正确;
2 2 2 1 2
B项,由题干信息可知,C(石墨)= C(金刚石) ΔH<0,即1molC(石墨)具有的总能量低于1molC(金刚石),
5
则1mol C(石墨)和1mol C(金刚石)分别与足量O 反应全部转化为CO(g),后者放热多,B错误;C项,由
2 2
题干信息可知,反应I:C(石墨)+ (g)=CO(g) ΔH,反应III:C(金刚石)+ (g)=CO(g) 则反应I-反应
1
III得C(石墨)= C(金刚石),根据盖斯定律可知,ΔH=ΔH-ΔH,C正确;D项,根据盖斯定律可知,化学
5 1 3
反应的△H,只与反应体系的始态和终态有关,与反应途径无关,D正确;故选B。
12. MgCO 和CaCO 的能量关系如图所示(M=Ca、Mg):
3 3
资料收集整理【淘宝店铺:向阳百分百】已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是( )
A.ΔH(MgCO )>ΔH(CaCO)>0
1 3 1 3
B.ΔH(MgCO )=ΔH (CaCO)>0
2 3 2 3
C.ΔH(CaCO)-ΔH (MgCO )=ΔH (CaO)-ΔH (MgO)
1 3 1 3 3 3
D.对于MgCO 和CaCO ,ΔH+ΔH >ΔH
3 3 1 2 3
【答案】C
【解析】根据盖斯定律可得ΔH=ΔH+ΔH +ΔH ,又易知Ca2+半径大于Mg2+半径,所以CaCO 的离子键
1 2 3 3
强度弱于MgCO ,CaO的离子键强度弱于MgO。A项,ΔH 表示断裂CO2-和M2+的离子键所吸收的能量,
3 1 3
离子键强度越大,吸收的能量越大,因而ΔH(MgCO )>ΔH(CaCO)>0,A项正确;B项,ΔH 表示断裂
1 3 1 3 2
CO2-中共价键形成O2-和CO 吸收的能量,与M2+无关,因而ΔH(MgCO )=ΔH (CaCO)>0,B项正确;C
3 2 2 3 2 3
项,由上可知ΔH(CaCO)-ΔH (MgCO )<0,而ΔH 表示形成MO离子键所放出的能量,ΔH 为负值,CaO
1 3 1 3 3 3
的离子键强度弱于MgO,因而ΔH(CaO)>ΔH(MgO),ΔH(CaO)-ΔH (MgO)>0,C项错误;D项,
3 3 3 3
ΔH+ΔH >0,ΔH<0,故ΔH+ΔH >ΔH,D项正确。故选C。
1 2 3 1 2 3
13.(2023·安徽省皖优联盟高三第二次阶段测试)已知[ΔH、ΔH、ΔH 对应的反应中O(g)已省略,且
2 3 5 2
ΔH>ΔH]:
2 5
下列说法正确的是( )
A.ΔH>0 B.ΔH 的值是CHCHCHCH(g)的燃烧热
1 3 3 2 2 3
C.ΔH+ΔH=ΔH+ΔH D.稳定性:正丁烷>异丁烷
1 2 3 4
【答案】C
【解析】A项,ΔH、ΔH 分别表示异丁烷与正丁烷的燃烧热,若ΔH>ΔH,说明燃烧1 mol两种物
2 3 2 5
质时前者释放的热量较后者少,由此知异丁烷的能量较低,则正丁烷转化为异丁烷是放热反应,故A错误;
B项,燃烧热是1mol纯物质完全燃烧生成指定产物时放出的热量,含H元素的物质燃烧生成的指定产物为
资料收集整理【淘宝店铺:向阳百分百】液态水,所以ΔH 的值不是正丁烷的燃烧热,故B错误;C项,ΔH+ΔH 和ΔH+ΔH 的始态和终态相同,
3 1 2 3 4
由盖斯定律可知,ΔH+ΔH=ΔH+ΔH,故C正确;D项,相同条件下,能量越低越稳定,则稳定性:正丁
1 2 3 4
烷<异丁烷,故D错误;故选C。
14.(2023·浙江省北斗星盟高三联考)下面是丙烷(用 表示)的氯化和溴化反应时的相对能量变化图
(已知 )及产率关系。有关说法不正确的是( )
A.1molRH(g)完全生成1molRCl(g)放热1.6×10-19(a-b) J
B. 比 稳定
C.以丙烷、卤素、氢氧化钠溶液为原料制备2-丙醇,Br 优于Cl
2 2
D.溴代和氯代第一步都是决速反应
【答案】A
【解析】A项,由图可知,1个RH(g)分子转化成RCl(g)放热1.6×10-19(a-b) J,则1molRH(g)完全生成
1molRCl(g)放热N ×1.6×10-19(a-b) J,故A错误;B项,由图可知, 的能量比 低,则 比 稳定,
A
故B正确;C项,由题目信息可知,丙烷和Br 发生取代反应时相比和Cl 发生取代反应更加容易生成
2 2
CHCH(X)CH,CHCH(X)CH 在NaOH水溶液中发生水解反应可以得到2-丙醇,则以丙烷、卤素、氢氧化
2 3 2 3
钠溶液为原料制备2-丙醇,Br 优于Cl,故C正确;D项,由图可知,溴代和氯代第一步反应活化能大于
2 2
第二步,说明第一步反应速率小于第二步,则溴代和氯代第一步都是决速反应,故D正确;故选A。
15.(2023·浙江省精诚联盟高三三模)XH和O 反应生成X或XO的能量-历程变化如图。在恒温恒容
2
的密闭容器中加入一定量的XH和O,t min时测得c(XO)<c(X),下列有关说法不正确的是( )
2 1
资料收集整理【淘宝店铺:向阳百分百】A.t min时容器内的压强比初始状态更大
1
B.
C.只改变反应温度,t min时可能出现c(X)<c(XO)
1
D.相同条件下,在t min (t >t)时测定,可能出现c(X)<c(XO)
2 2 1
【答案】D
【解析】由图可知XH和O 反应生成X或XO都是放热反应,相对而言生成XO的活化能更低,反应
2
速率更快,时间上要出现c(X)<c(XO)时间上要比t min 更短。A项,据图可知生成1molXO气体物质的
1
量减小生成1mol,生成1molX气体物质的量增加2mol,因为t min时测得c(XO)<c(X),所以t min时气
1 1
体总的物质的量是增大的,因此t min时容器内的压强比初始状态更大,A正确;B项,由图可知,B正
1
确;C项,XH和O 反应生成X或XO都是放热反应,相对而言生成XO的活化能更低,反应速率更快,
2
只改变反应温度,t min时可能出现c(X)<c(XO),C正确;D项,根据题干信息t min时测得c(XO)<
1 1
c(X),说明XO是动力学产物,时间上要出现c(X)<c(XO)时间上要比t min 更短,D错误;故选D。
1
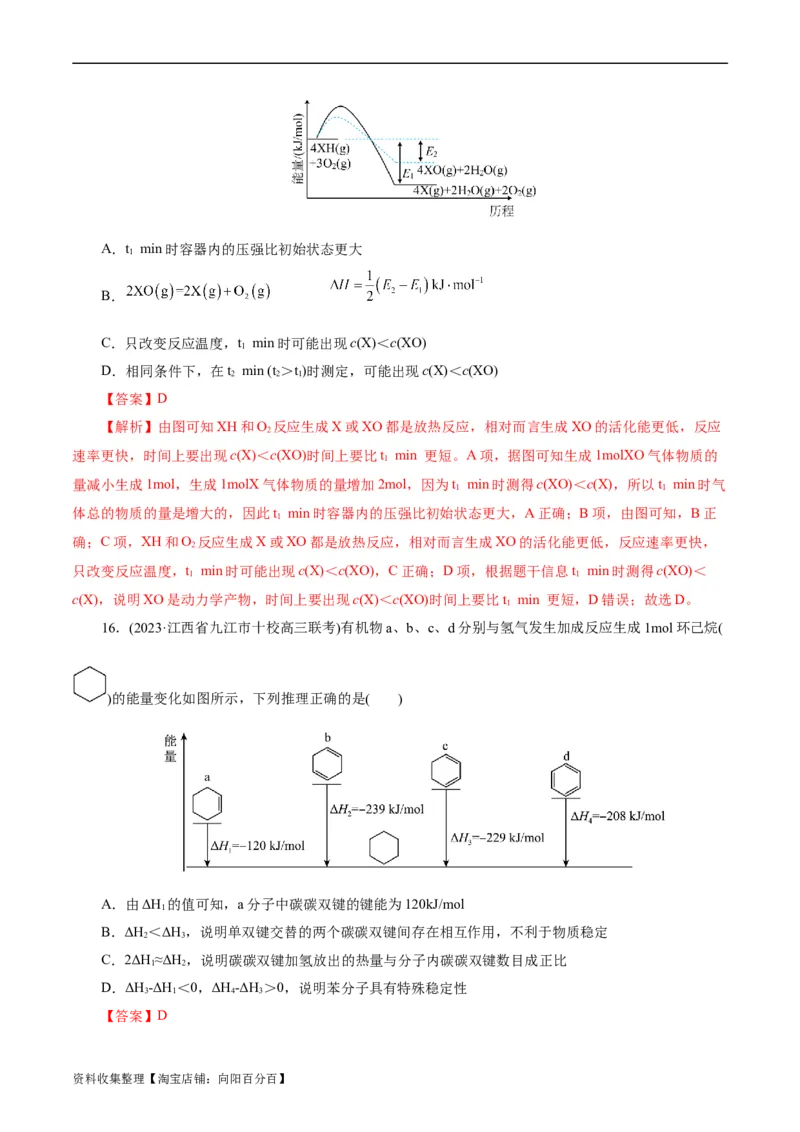
16.(2023·江西省九江市十校高三联考)有机物a、b、c、d分别与氢气发生加成反应生成1mol环己烷(
)的能量变化如图所示,下列推理正确的是( )
A.由ΔH 的值可知,a分子中碳碳双键的键能为120kJ/mol
1
B.ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,不利于物质稳定
2 3
C.2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
D.ΔH-ΔH <0,ΔH-ΔH >0,说明苯分子具有特殊稳定性
3 1 4 3
【答案】D
资料收集整理【淘宝店铺:向阳百分百】【解析】A项, 由ΔH 的值可知,2摩尔碳氢键和1摩尔碳碳单键的键能和比1摩尔氢氢键的键能和
1
1摩尔碳碳双键之和多120千焦,A错误;B项,ΔH<ΔH,即单双键交替的物质能量低,更稳定,说明
2 3
单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定,B错误;C项,虽然2ΔH≈ΔH,但两者并
1 2
不相等,说明碳碳双键加氢放出的热量与分子内碳碳双键数目、双键的位置有关,不能简单的说碳碳双键
加氢放出的热量与分子内碳碳双键数目成正比,C错误;D项,由图示可知,反应I为: (l)+H (g)→
2
(l) ΔH ,反应III为: (l)+2H (g) → (l) ΔH 反应IV为: +3H (g)→ (l) ΔH ,ΔH-
1 2 3, 2 4 3
ΔH<0即 (l)+H (g) → (l) ΔH<0,ΔH-ΔH >0即 +H (g)→ (l) ΔH>0,则说明 具
1 2 4 3 2
有的总能量小于 ,能量越低越稳定,则说明苯分子具有特殊稳定性,D正确;故选D。
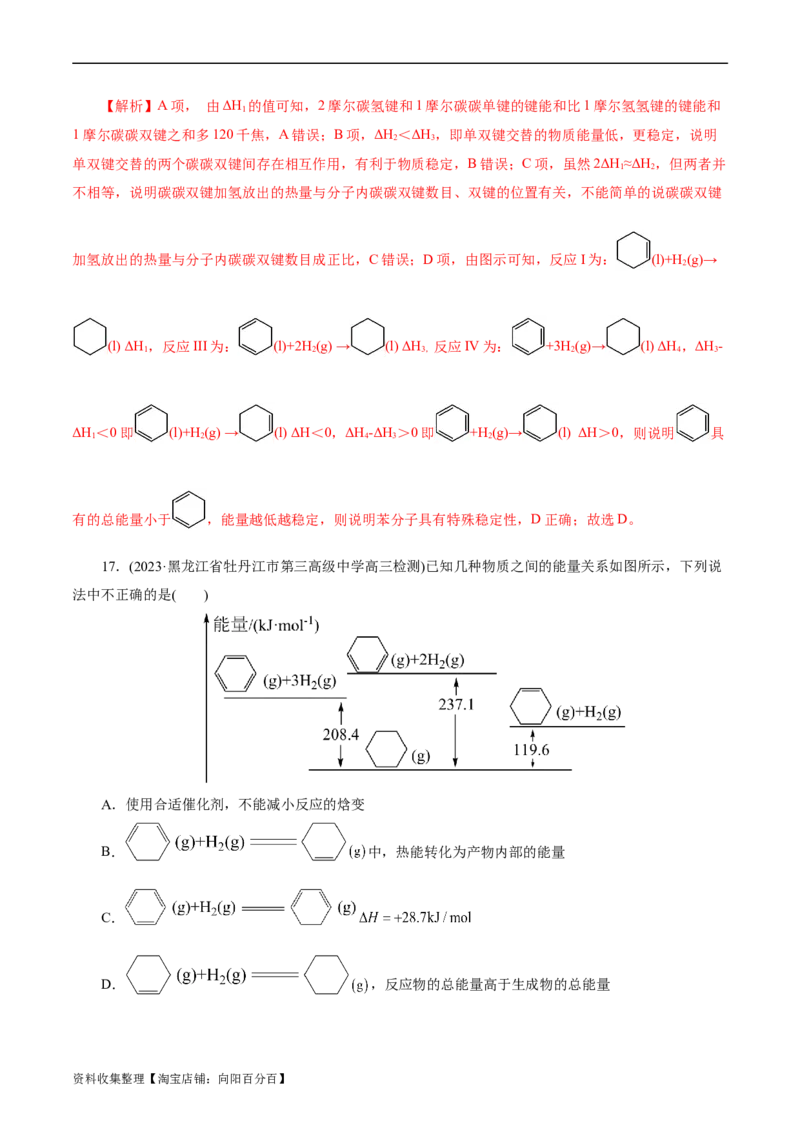
17.(2023·黑龙江省牡丹江市第三高级中学高三检测)已知几种物质之间的能量关系如图所示,下列说
法中不正确的是( )
A.使用合适催化剂,不能减小反应的焓变
B. 中,热能转化为产物内部的能量
C.
D. ,反应物的总能量高于生成物的总能量
资料收集整理【淘宝店铺:向阳百分百】【答案】B
【解析】A项, 使用合适催化剂可降低反应的活化能,但不能减小反应的焓变,故A正确;B项,
ΔH=119.6kJ/mol-208.4kJ/mol=-88.8kJ/mol中,产物内部的能量转化为
热能,故B错误;C项,
ΔH=237.1kJ/mol-208.4kJ/mol=+28.7kJ/mol,故C正确;D项,
ΔH=-119.6kJ/mol,反应为放热反应,反应物的总能量高于生成物的总能量,故D正确;故选B。
18.(2023·浙江省浙里卷天下高三联考)甲烷与氯气发生取代反应分别生成1mol相关有机物的能量变
化如图所示:
已知Cl-Cl、C-Cl键能分别为243 kJ·mol-1、327 kJ·mol-1,下列说法不正确的是( )
A.1mol CH(g)的能量比1mol CHCl(g)的能量多197kJ
4 2 2
B.CH 与Cl 的取代反应是放热反应
4 2
C. ,说明CH 与Cl 的四步取代反应,难易程度相当
4 2
D.CH(g)+ Cl·(g)→ CH·(g)+HCl(g) ΔH=-15 kJ·mol-1
4 3
【答案】A
【解析】A项,由图可知,甲烷和氯气反应生成CHCl(g)的同时还会生成氯化氢,故不能说明1mol
2 2
CH(g)的能量比1mol CHCl(g)的能量多197kJ,A错误;B项,由图可知,焓变均为负值,则为放热反应,
4 2 2
资料收集整理【淘宝店铺:向阳百分百】B正确; C项, ,说明CH 与Cl 的四步取代反应每多取代1个氢原子的难
4 2
易程度相当,C正确;D项,CH(g)+ Cl·(g)→ CH ·(g)+HCl(g)反应中,断裂了1molC-H键,形成了1molH-
4 3
Cl键,已知Cl-Cl、C-Cl键能分别为243 kJ·mol-1、327 kJ·mol-1,则CH(g)+ Cl·(g)→ CH ·(g)+HCl(g)的焓
4 3
变为 ,即
, ,D正
确;故选A。
19.(2023·湘豫名校联盟高三联考)苯与卤素发生取代反应可细分为:
①C H(苯)+∙X+X→C H∙+X +HX H
6 6 2 6 5 2 1
②C
6
H
5
∙+X
2
+HX→C
6
H
5
X+HX+∙X △H
2
下图1、2表示反应中部分物质的含
△
量(测量反应过程中多个时间点的各物质含量,去除开始时与结束
前的极端值后取平均值),已知图1为使用催化剂前,图2为使用催化剂后,下表为相关△H的数据。
X Cl Br
H(kJ∙mol-1) 10 20
1
△H(kJ∙mol-1) -111 -100
2
下列说法正确的是△( )
A.可推知H-Cl键的键能比H-Br键的键能大10 kJ∙mol-1
B.1mol苯与1mol氯气反应将会向环境释放101kJ热量
C.使用催化剂后会改变△H,但不会改变△H+ H
1 1 2
D.反应②为总反应的决速步,催化剂的机理为降
△
低反应②的活化能
【答案】A
【解析】A项, 从表中可以得出,△H(Cl)- H(Br)=(10-20) kJ∙mol-1=-10 kJ∙mol-1,两个过程中其它键
1 1
△
资料收集整理【淘宝店铺:向阳百分百】的断裂情况相同,只有形成H-Cl键和比H-Br键不同,由此可推知H-Cl键的键能比H-Br键的键能大10
kJ∙mol-1,A正确;B项,利用盖斯定律,将反应①+②,可得出C H(苯)+X →C HX+HX
6 6 2 6 5
H= H+ H=-101 kJ∙mol-1,由于苯与氯气发生的反应为可逆反应,所以1mol苯与1mol氯气反应向环境
1 2
△释放△的热量△小于101kJ,B不正确;C项,使用催化剂后,只能改变反应的活化能,不能改变△H
1
和
△H,也不会改变△H+ H,C不正确;D项,从图中可以看出,加入催化剂后,C H∙的百分含量增大较
2 1 2 6 5
少,而C
6
H
5
X的百分含量△增大很多,则表明反应①的反应速率慢,反应②的反应速率快,从而确定反应②
为总反应的决速步,催化剂的机理为降低反应②的活化能,D不正确;故选A。
20.(2023·浙江省金、丽、衢十二校高三二模)氮肥保障了现代农业的丰收。根据下图的循环过程,有
关硫酸铵和氯化铵的说法正确的是( )
A.ΔH=+3kJ·mol−1
5
B.硫酸铵晶体中只含离子键不含共价键
C.氯化铵晶体溶于水的过程:ΔS<0
D.可以通过NH Cl的受热分解实验测得ΔH=+698kJ·mol−1的数据
4 1
【答案】A
【解析】A项,① ;②
;③ ;④
;⑤ ;⑥
;则根据盖斯定律④+②+⑥-①-③得⑤,得到ΔH=+3kJ·mol−1,A
5
项正确;B项,硫酸铵晶体中既含离子键又含共价键,B项错误;C项,氯化铵晶体溶于水的过程中混乱
度增大,即熵增大,ΔS>0,C项错误;D项,氯化铵受热分解为氯化氢和氨气,氯化氢和氨气又会重新
结合生成氯化铵,不能用氯化铵的受热分解实验测 的数据,D项
资料收集整理【淘宝店铺:向阳百分百】错误;故选A。
21.(2023·浙江省七彩阳光联盟、金华十二校高三联考)25℃,有关物质的能量转化图如图,又已知
RO 是 的稳定氧化物,试分析计算并回答下列说法不正确的是( )
2
A.25℃时,单质 的标准燃烧热:ΔH=-393.5kJ·mol−1
B.若RO的摩尔质量为 ,则RO的热值为
C.转化Ⅱ的热化学方程式为:2RO(g)+O(g)=2RO (g) ΔH=-282.9kJ·mol−1
2 2
D.由R→RO的热化学方程式为:2R(s)+O(g)=2RO(g) ΔH=-221.2kJ·mol−1
2
【答案】C
【解析】A项,25℃时,R的燃烧热为1 mol R完全燃烧生成R的稳定氧化物放出的热量,所以R的
标准燃烧热:ΔH=-393.5kJ·mol−1,故A正确;B项,转化Ⅱ为1molRO和0.5molO 生成1 mol RO 放出
2 2
282.9kJ热量,若 的摩尔质量为 ,则 的热值为 ,故B正确;C项,
转化Ⅱ为1molRO和0.5molO 生成1molRO 放出282.9kJ热量,则2molRO和1molO 生成2molRO 放出
2 2 2 2
565.8kJ热量,则转化Ⅱ的热化学方程式为:2RO(g)+O(g)=2RO (g) ΔH=-565.8kJ·mol−1,故C错误;D
2 2
项,根据图知,1molR反应转化为1molRO时放出热量为393.5kJ-282.9kJ=110.6kJ,所以由R转化为 的
热化学方程式为:2R(s)+O(g)=2RO(g) ΔH=-221.2kJ·mol−1,故D正确;故选C。
2
22.(2023·浙江省天域全国名校协作体高三联考)甲醇和异丁烯(以IB表示)在催化剂作用下合成甲基叔
丁基醚(MTBE):CHOH(g)+IB(g) = MTBE(g) ΔH。反应过程中反应物首先被催化剂吸附,再经历过渡态
3
(I、Ⅱ、Ⅲ)最终得到产物,相对能量与反应历程的关系如图所示(其中N 表示甲醇和异丁烯同时被吸附,
1
N 表示甲醇先被吸附,N 表示异丁烯先被吸附)。
2 3
资料收集整理【淘宝店铺:向阳百分百】下列说法不正确的是
A.该反应的ΔH=-4QkJ/mol
B.三种反应历程中,N 反应速率最快
1
C.过渡态I比另两种过渡态稳定
D.同温同压下,只要起始投料相同,三种途径MTBE的转化率相同
【答案】D
【解析】A项,该反应的焓变△H为生成物的总能量减去反应物的总能量,则△H=(1-5)QkJ/
mol=-4QkJ/mol, 该反应的热化学方程式为该条件下反应的热化学方程式为:CH OH(g)+IB(g) = MTBE(g)
3
ΔH=-4QkJ/mol,A正确;B项,N、N、 N 三种反应历程的活化能分别为(6-2)QkJ/mol=4 QkJ/mol、(9-
1 2 3
3)QkJ/mol=6QkJ/mol、(10-4)QkJ/mol=6QkJ/mol,则N 反应速率最快,B正确;C项,过渡态I的能量最低,
1
能量越低越稳定,故过渡态I比另两种过渡态稳定,C正确;D项,N、N、N 三种反应历程的活化能不
1 2 3
相等,则同温同压下,只有起始投料相同,相同时间三种途径MTBE的转化率不相同,D错误;故选D。
23.(2023·浙江省Z20名校联盟高三第三次联考)我国科学家研究化合物M(s)催化CO 氢化生成甲酸的
2
机理,其中由化合物M(s)生成化合物N(s)过程的机理和相对能量曲线如下图所示。 均为过渡态。
下列说法正确的是
A.过渡态TS1比化合物Р更稳定
B.过程M→P为化合物M生成化合物N的决速步骤
C.化合物M催化CO 氢化生成甲酸的反应过程中一定有Fe-O键的生成和断裂
2
D.由M(s)生成N(s)的热化学方程式:M(s)+CO (g)=N(s)ΔH=-0.51kJmol-1
2
⋅
资料收集整理【淘宝店铺:向阳百分百】【答案】C
【解析】A项,由图可知,过渡态TS1比P能量高,则P更稳定,A错误;B项,由图可知,过程
P→TS2为两步反应中活化能较大的反应,为慢反应,即为化合物M生成化合物N的决速步骤,B错误;
C项,化合物M为催化剂,反应前后结构不会改变,比较M、N的结构可知,当Fe-O键的断裂重新连接
氢原子生成M,所以一定有Fe-O键的生成和断裂,C正确;D项,图示为一个二氧化碳分子反应过程,能
量变化为-11.63eV,所以当有1mol二氧化碳反应能量变化为-11.63eV×1.6×10-19J/
eV×6.02×1023=1.12×106J=1120kJ,则该过程的热化学方程式为:M(s)+CO (g)=N(s)ΔH=-1120kJ mol-1,D错
2
误;故选C。 ⋅
24.(2023·浙江省稽阳联谊学校高三联考)一定条件下,2,3-二甲基-1,3-丁二烯与溴单质发生液相加
成反应(1,2-加成和1,4-加成同时存在),已知体系中两种产物可通过中间产物 互相
转化,反应历程及能量变化如图所示:
下列说法正确的是( )
A. 比 稳定,因此任意条件下主产物均为
B.由 小于 可知,升温有利于 →
C.
资料收集整理【淘宝店铺:向阳百分百】D.由反应历程及能量变化图可知,该加成反应为放热反应
【答案】C
【解析】A项,低温下的主产物为1,2-加成,高温下的主要产物是1,4-加成,故A错误;B项,温度升
高对活化能大的反应影响更大,因此升温有利于得到 ,故B错误;C项,根据图像可以得
到 ,故C正确;D项,由反应历程及能量变化图无法判断该加成反应为
放热反应,故D错误;故选C
【能力提升】
25.(2023·浙江省温州市高三第三次模拟适应性考试)标准状态下,气态反应物、生成物及活化分子
[A(B)表示“A+B→产物”的活化分子]的相对能量如表所示:
物质 NO(g) NO (g) SO (g) SO (g) O(g) O(g) NO(O) SO (O )
2 2 3 2 3 3 2 3
相对能量/ 91.3 33.2 -296.8 -395.7 0 142.7 237.2 -96.1
下列说法不正确的是( )
A.NO (g)+SO (g) NO (g)+ SO (g) ΔH=-40.8 kJ·mol-1
2 2 3
B.3O(g) 2O(g)反应不能自发进行
2 3
C.相同条件下,SO (g)+O(g) O (g)+ SO (g)比NO (g)+O(g) O (g)+ NO (g)速率快
2 3 2 3 3 2 2
D.1mol NO (g)的总键能大于1mol NO(g)总键能
2
【答案】C
【解析】A项,NO (g)+SO(g) NO (g)+ SO (g) ΔH=生成物总能量-反应物总能量=91.3kJ/mol+
2 2 3
(-395.7kJ/mol)-[33.2kJ/mol+(-296.8kJ/mol)]=-40.8kJ/mol,故A正确;B项,3O(g) 2O(g) H=生成物
2 3
总能量-反应物总能量=+285.4kJ/mol>0,且 S<0,则任何温度下 H-T S>0,即反应3O(g)
2
2O(g)不能自发进行,故B正确;C项,反应SO (g)+O(g) O (g)+ SO (g)的活化能=活化分子能量-
3 2 3 2 3
反应物总能量=-96.1kJ/mol-(-296.8kJ/mol+142.7kJ/mol)=58kJ/mol,反应NO (g)+O(g) O (g)+ NO (g)
3 2 2
的活化能为237.2kJ/mol-(91.3kJ/mol+142.7kJ/mol)=3.2kJ/mol<58kJ/mol,反应的活化能越高,反应速率越慢,
则相同条件下,SO (g)+O(g) O (g)+ SO (g)比NO (g)+O(g) O (g)+ NO (g)速率慢,故C错
2 3 2 3 3 2 2
误;D项,反应2NO (g)+O(g) 2NO (g)ΔH=生成物总能量-反应物总能
2 2
量=2×33.2kJ/mol-2×91.3kJ/mol-0kJ/mol=-116.2kJ/mol,为放热反应,焓变△H=反应物总键能-生成物总键能,
则该反应反应物总键能<生成物总键能,即1molNO(g)和0.5molO 总键能<1molNO (g)的总键能,所以
2 2
1molNO (g)的总键能大于1molNO(g)总键能,故D正确;故选C。
2
资料收集整理【淘宝店铺:向阳百分百】