文档内容
考点 17 化学反应的热效应
【基础过关】
1.化学反应中的能量变化,通常主要表现为热量的变化。下列相关表述正确的是( )
A.一定条件下,将0.5molH(g)和0.5molI (g)置于密闭容器中充分反应生成 放热 ,其热化学方
2 2
程式为:I(g )+H (g) 2HI(g) H=-2akJ•mol-1
2 2
△
B.在101kPa时,2 g H 完全燃烧生成液态水,放出 热量,表示氢气燃烧热的热化学方程式
2
表示为:
C.S(g)+ O (g)=SO(g) ΔH S(g)+ O (g)=SO(g) ΔH ΔH>ΔH
2 2 1 2 2 2 1 2
D.HCl和NaOH反应的中和热 ,则0.5molHSO 和足量Ba(OH) 反应的
2 4 2
2.根据以下热化学方程式,ΔH 和ΔH 的大小比较错误的是( )
1 2
A.Br (g)+H(g)=2HBr(g) ΔH ,Br (l)+H (g)=2HBr(g) ΔH ,则有ΔH<ΔH
2 2 1 2 2 2 1 2
B.2HS(g)+3O(g)=2SO(g)+2HO(l) ΔH ,2HS(g)+O(g)=2S(s)+2HO(l) ΔH ,则有ΔH>ΔH
2 2 2 2 1 2 2 2 2 1 2
C.4Al(s)+3O (g)=2Al O(s) ΔH ,4Fe(s)+3O (g)=2Fe O(s) ΔH ,则有ΔH<ΔH
2 2 3 1 2 2 3 2 1 2
D.C(s)+O(g)=CO (g) ΔH ,C(s)+O(g)=CO(g) ΔH ,则有ΔH<ΔH
2 2 1 2 2 1 2
3.(2023·湖北省部分学校高三联考)下列对热化学方程式的解读或书写正确的是( )
A.已知 ΔH>0,则石墨比金刚石稳定
B.已知①S(g)+O(g) SO (g) ΔH;②S(s)+O (g) SO (g) ΔH,则ΔH>ΔH
2 2 1 2 2 2 1 2
C.已知甲烷燃烧热为 ,则甲烷燃烧的热化学方程式可以表示为CH (g)+
4
2O(g)=CO (g)+ 2HO(g) ΔH=-890.3 kJ·mol-1
2 2 2
D.已知中和热 ,则1mol硫酸和足量稀NaOH溶液反应的反应热就是中和热
4.(2023·河北省邯郸市部分学校高三联考)依据下列含硫物质转化的热化学方程式,得出的相关结论
正确的是( )
①S(g)+CO(g) SO (g) ΔH
2 2 1
②S(s)+CO(g) SO (g) ΔH
2 2 2
③2HS(g)+ O(g) 2S(s)+ HO(1) ΔH
2 2 2 3
④2HS(g)+3 O(g) 2SO (g)+ HO(1) ΔH
2 2 2 2 4
⑤2HS(g)+SO(g) 3S(s)+ 2HO(1) ΔH
2 2 2 5
资料收集整理【淘宝店铺:向阳百分百】 1A.ΔH>ΔH B.ΔH<ΔH
1 2 3 4
C.ΔH=ΔH+ΔH D.2ΔH=3ΔH-ΔH
4 2 3 5 3 4
5.(2023·广东省蕉岭县蕉岭中学高三第二次质检)已知:2CO(g)+O(g)=2CO (g) ΔH=-566kJ/mol
2 2
2NaO(s)+2CO(g)=2Na CO(s)+O(g) ΔH=-452kJ/mol
2 2 2 2 3 2
下列说法正确的是( )
A.28克CO完全燃烧,放出热量为283J
B.NaO(s)+CO(g)=Na CO(s)+ O(g) ΔH=+226kJ/mol
2 2 2 2 3 2
C.CO(g)与NaO(s)反应放出509kJ热量时,电子转移数为1.204×1024
2 2
D.CO的燃烧热为283kJ/mol
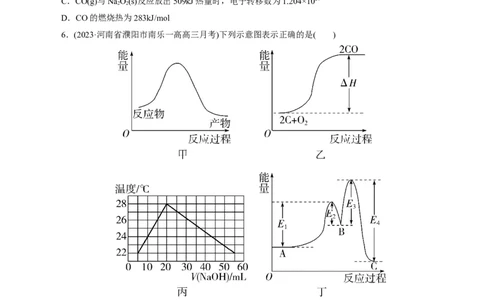
6.(2023·河南省濮阳市南乐一高高三月考)下列示意图表示正确的是( )
A.甲图表示Fe O(s)+3CO(g)=2Fe(s)+3CO(g) ΔH=+26.7kJ·mol-1反应的能量变化
2 3 2
B.乙图表示碳的燃烧热
C.丙图表示实验的环境温度为20℃,将物质的量浓度相等、体积分别为V、V 的HSO 、NaOH溶
1 2 2 4
液混合,混合液的最高温度随V(NaOH)的变化(已知V+V =60mL)
1 2
D.已知稳定性顺序:B<A<C,某反应由两步反应A→B→C构成,反应过程中的能量变化曲线如丁
图
7.(2023·北京市东城区第一六六中学高三期中)以CO和H 为原料合成甲醇是工业上的成熟方法,直
2
资料收集整理【淘宝店铺:向阳百分百】 2接以CO 为原料生产甲醇是目前的研究热点。我国科学家用CO 人工合成淀粉时,第一步就需要将CO 转
2 2 2
化为甲醇。
已知:①CO(g)+2H(g)=CH OH(g) ΔH =-90.5kJ/mol
2 3 1
②CO(g)+HO(g)=CO(g)+H(g) ΔH =-41.1kJ/mol
2 2 2 2
③2H(g)+ O (g)=2HO(g) ΔH =-483.6kJ/mol
2 2 2 3
下列说法不正确的是( )
A.若温度不变,反应①中生成1 mol CH OH(l)时,放出的热量大于90.5 kJ
3
B.CO 与H 合成甲醇的热化学方程式为:CO(g)+3H(g)=CH OH(g)+H O(g) ΔH=-49.4kJ/mol
2 2 2 2 3 2
C.通过电解制H 和选用高效催化剂,可降低CO 与H 合成甲醇反应的焓变
2 2 2
D.以CO 和HO为原料合成甲醇,同时生成O,该反应需要吸收能量
2 2 2
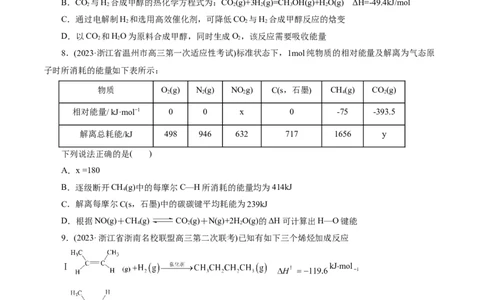
8.(2023·浙江省温州市高三第一次适应性考试)标准状态下,1mol纯物质的相对能量及解离为气态原
子时所消耗的能量如下表所示:
物质 O(g) N(g) NO g) C(s,石墨) CH(g) CO(g)
2 2 2 4 2
相对能量/ kJ·mol−1 0 0 x 0 -75 -393.5
解离总耗能/kJ 498 946 632 717 1656 y
下列说法正确的是( )
A.x =180
B.逐级断开CH(g)中的每摩尔C—H所消耗的能量均为414kJ
4
C.解离每摩尔C(s,石墨)中的碳碳键平均耗能为239kJ
D.根据NO(g)+CH(g) CO(g)+N(g)+2H O(g)的ΔH可计算出H—O键能
4 2 2
9.(2023·浙江省浙南名校联盟高三第二次联考)已知有如下三个烯烃加成反应
Ⅰ kJmol
⋅
Ⅱ kJmol
⋅
Ⅲ kJmol
⋅
则下列说法不正确的是( )
A.由题可知丁烯稳定性是Ⅲ>Ⅱ>Ⅰ
B.由题可知断裂碳碳π键和氢氢σ键所消耗的能量总是小于形成两个碳氢σ键所放出的能量
资料收集整理【淘宝店铺:向阳百分百】 3C.由题可知烯烃的稳定性与双键碳上的取代基和构型有关
D.由题可知,由于Ⅰ、Ⅱ、Ⅲ断键和成键都一样,因此反应的 不能由键能计算得到
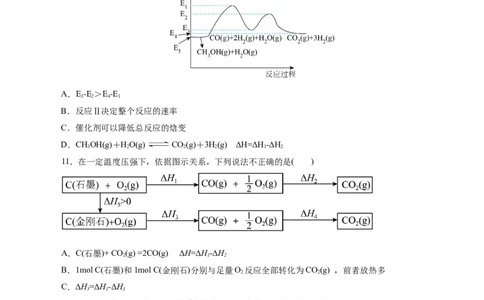
10.(2023·浙江省诸暨市高三适应性考试)甲醇与水蒸气在催化剂作用下发生如下反应:
反应Ⅰ:CHOH(g) CO (g)+ 2H(g) ΔH
3 2 1
反应Ⅱ:CO (g)+ HO(g) CO (g)+ H(g) ΔH
2 2 2 2
根据能量变化示意图,下列说法正确的是( )
A.E-E >E-E
3 2 4 1
B.反应Ⅱ决定整个反应的速率
C.催化剂可以降低总反应的焓变
D.CHOH(g)+HO(g) CO(g)+3H(g) ΔH=ΔH -ΔH
3 2 2 2 1 2
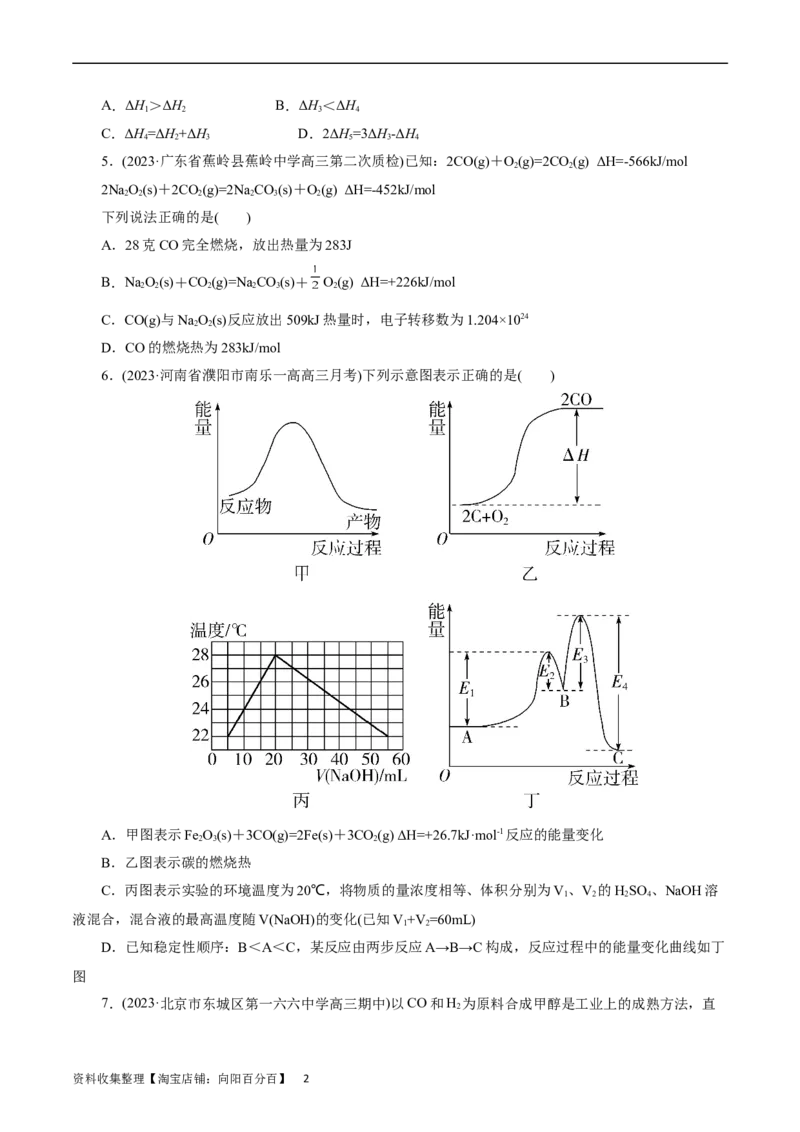
11.在一定温度压强下,依据图示关系,下列说法不正确的是( )
A.C(石墨)+ CO (g) =2CO(g) ΔH=ΔH-ΔH
2 1 2
B.1mol C(石墨)和1mol C(金刚石)分别与足量O 反应全部转化为CO(g) ,前者放热多
2 2
C.ΔH=ΔH-ΔH
5 1 3
D.化学反应的△H,只与反应体系的始态和终态有关,与反应途径无关
12. MgCO 和CaCO 的能量关系如图所示(M=Ca、Mg):
3 3
已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是( )
资料收集整理【淘宝店铺:向阳百分百】 4A.ΔH(MgCO )>ΔH(CaCO)>0
1 3 1 3
B.ΔH(MgCO )=ΔH (CaCO)>0
2 3 2 3
C.ΔH(CaCO)-ΔH (MgCO )=ΔH (CaO)-ΔH (MgO)
1 3 1 3 3 3
D.对于MgCO 和CaCO ,ΔH+ΔH >ΔH
3 3 1 2 3
13.(2023·安徽省皖优联盟高三第二次阶段测试)已知[ΔH、ΔH、ΔH 对应的反应中O(g)已省略,且
2 3 5 2
ΔH>ΔH]:
2 5
下列说法正确的是( )
A.ΔH>0 B.ΔH 的值是CHCHCHCH(g)的燃烧热
1 3 3 2 2 3
C.ΔH+ΔH=ΔH+ΔH D.稳定性:正丁烷>异丁烷
1 2 3 4
14.(2023·浙江省北斗星盟高三联考)下面是丙烷(用 表示)的氯化和溴化反应时的相对能量变化图
(已知 )及产率关系。有关说法不正确的是( )
A.1molRH(g)完全生成1molRCl(g)放热1.6×10-19(a-b) J
B. 比 稳定
C.以丙烷、卤素、氢氧化钠溶液为原料制备2-丙醇,Br 优于Cl
2 2
D.溴代和氯代第一步都是决速反应
资料收集整理【淘宝店铺:向阳百分百】 515.(2023·浙江省精诚联盟高三三模)XH和O 反应生成X或XO的能量-历程变化如图。在恒温恒容
2
的密闭容器中加入一定量的XH和O,t min时测得c(XO)<c(X),下列有关说法不正确的是( )
2 1
A.t min时容器内的压强比初始状态更大
1
B.
C.只改变反应温度,t min时可能出现c(X)<c(XO)
1
D.相同条件下,在t min (t >t)时测定,可能出现c(X)<c(XO)
2 2 1
16.(2023·江西省九江市十校高三联考)有机物a、b、c、d分别与氢气发生加成反应生成1mol环己烷(
)的能量变化如图所示,下列推理正确的是( )
A.由ΔH 的值可知,a分子中碳碳双键的键能为120kJ/mol
1
B.ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,不利于物质稳定
2 3
C.2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
D.ΔH-ΔH <0,ΔH-ΔH >0,说明苯分子具有特殊稳定性
3 1 4 3
17.(2023·黑龙江省牡丹江市第三高级中学高三检测)已知几种物质之间的能量关系如图所示,下列说
法中不正确的是( )
资料收集整理【淘宝店铺:向阳百分百】 6A.使用合适催化剂,不能减小反应的焓变
B. 中,热能转化为产物内部的能量
C.
D. ,反应物的总能量高于生成物的总能量
18.(2023·浙江省浙里卷天下高三联考)甲烷与氯气发生取代反应分别生成1mol相关有机物的能量变
化如图所示:
已知Cl-Cl、C-Cl键能分别为243 kJ·mol-1、327 kJ·mol-1,下列说法不正确的是( )
A.1mol CH(g)的能量比1mol CHCl(g)的能量多197kJ
4 2 2
B.CH 与Cl 的取代反应是放热反应
4 2
C. ,说明CH 与Cl 的四步取代反应,难易程度相当
4 2
D.CH(g)+ Cl·(g)→ CH·(g)+HCl(g) ΔH=-15 kJ·mol-1
4 3
19.(2023·湘豫名校联盟高三联考)苯与卤素发生取代反应可细分为:
①C H(苯)+∙X+X→C H∙+X +HX H
6 6 2 6 5 2 1
②C
6
H
5
∙+X
2
+HX→C
6
H
5
X+HX+∙X △H
2
△
资料收集整理【淘宝店铺:向阳百分百】 7下图1、2表示反应中部分物质的含量(测量反应过程中多个时间点的各物质含量,去除开始时与结束
前的极端值后取平均值),已知图1为使用催化剂前,图2为使用催化剂后,下表为相关△H的数据。
X Cl Br
H(kJ∙mol-1) 10 20
1
△H(kJ∙mol-1) -111 -100
2
下列说法正确的是△( )
A.可推知H-Cl键的键能比H-Br键的键能大10 kJ∙mol-1
B.1mol苯与1mol氯气反应将会向环境释放101kJ热量
C.使用催化剂后会改变△H,但不会改变△H+ H
1 1 2
D.反应②为总反应的决速步,催化剂的机理为降
△
低反应②的活化能
20.(2023·浙江省金、丽、衢十二校高三二模)氮肥保障了现代农业的丰收。根据下图的循环过程,有
关硫酸铵和氯化铵的说法正确的是( )
A.ΔH=+3kJ·mol−1
5
B.硫酸铵晶体中只含离子键不含共价键
C.氯化铵晶体溶于水的过程:ΔS<0
D.可以通过NH Cl的受热分解实验测得ΔH=+698kJ·mol−1的数据
4 1
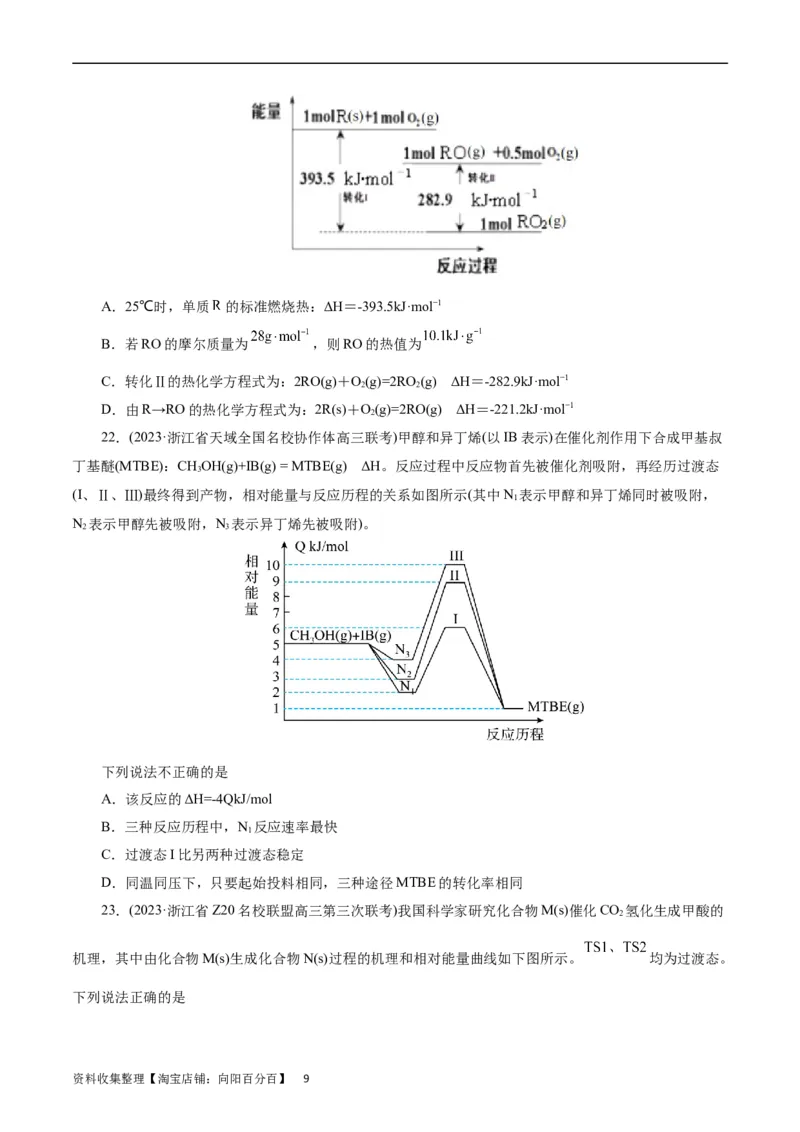
21.(2023·浙江省七彩阳光联盟、金华十二校高三联考)25℃,有关物质的能量转化图如图,又已知
RO 是 的稳定氧化物,试分析计算并回答下列说法不正确的是( )
2
资料收集整理【淘宝店铺:向阳百分百】 8A.25℃时,单质 的标准燃烧热:ΔH=-393.5kJ·mol−1
B.若RO的摩尔质量为 ,则RO的热值为
C.转化Ⅱ的热化学方程式为:2RO(g)+O(g)=2RO (g) ΔH=-282.9kJ·mol−1
2 2
D.由R→RO的热化学方程式为:2R(s)+O(g)=2RO(g) ΔH=-221.2kJ·mol−1
2
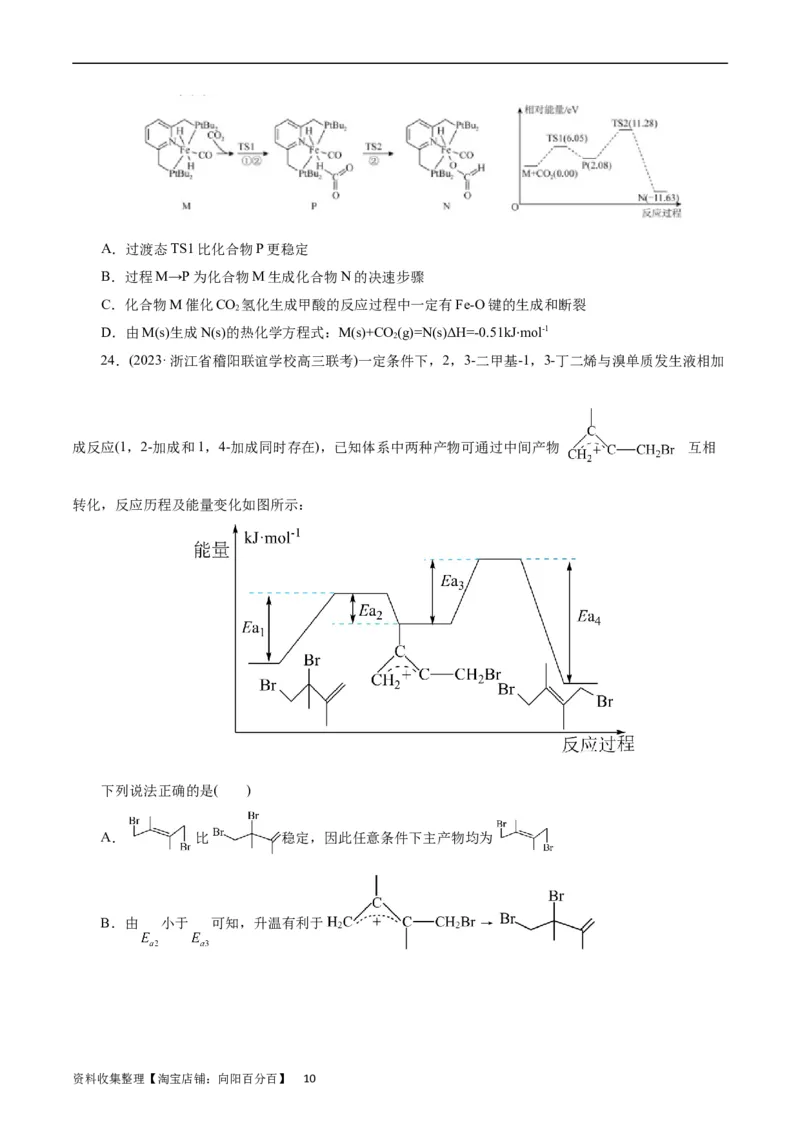
22.(2023·浙江省天域全国名校协作体高三联考)甲醇和异丁烯(以IB表示)在催化剂作用下合成甲基叔
丁基醚(MTBE):CHOH(g)+IB(g) = MTBE(g) ΔH。反应过程中反应物首先被催化剂吸附,再经历过渡态
3
(I、Ⅱ、Ⅲ)最终得到产物,相对能量与反应历程的关系如图所示(其中N 表示甲醇和异丁烯同时被吸附,
1
N 表示甲醇先被吸附,N 表示异丁烯先被吸附)。
2 3
下列说法不正确的是
A.该反应的ΔH=-4QkJ/mol
B.三种反应历程中,N 反应速率最快
1
C.过渡态I比另两种过渡态稳定
D.同温同压下,只要起始投料相同,三种途径MTBE的转化率相同
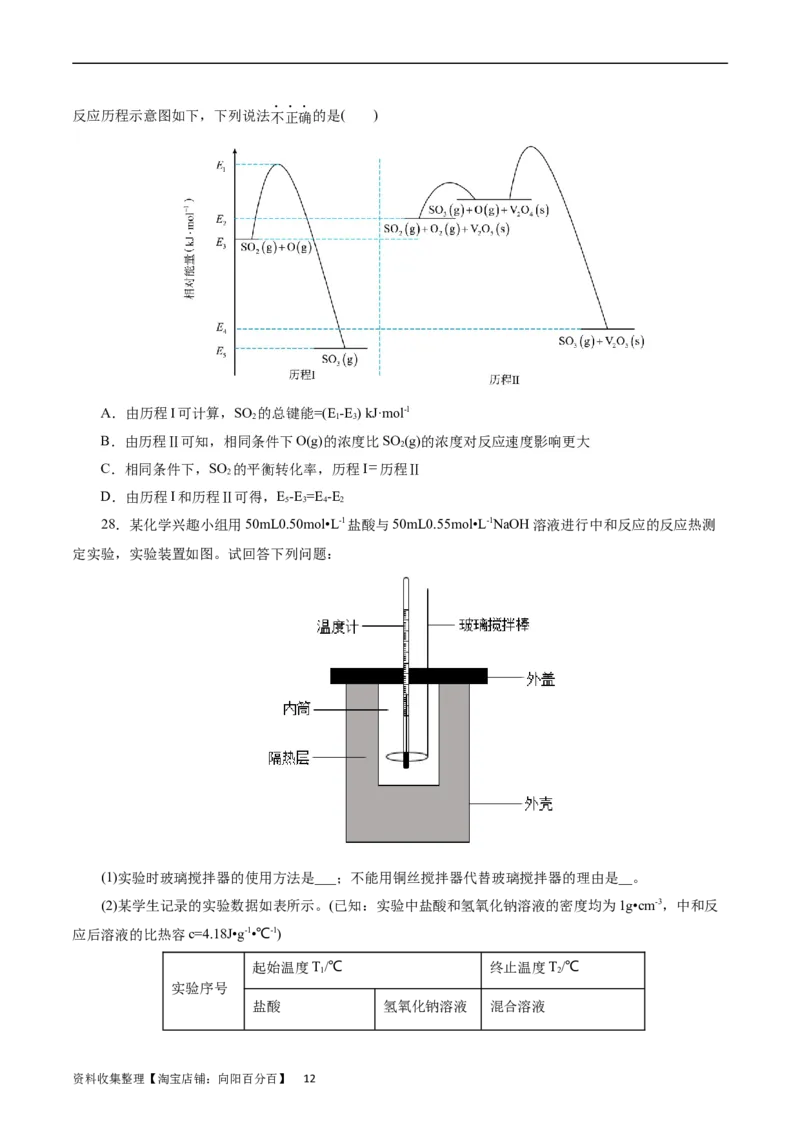
23.(2023·浙江省Z20名校联盟高三第三次联考)我国科学家研究化合物M(s)催化CO 氢化生成甲酸的
2
机理,其中由化合物M(s)生成化合物N(s)过程的机理和相对能量曲线如下图所示。 均为过渡态。
下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】 9A.过渡态TS1比化合物Р更稳定
B.过程M→P为化合物M生成化合物N的决速步骤
C.化合物M催化CO 氢化生成甲酸的反应过程中一定有Fe-O键的生成和断裂
2
D.由M(s)生成N(s)的热化学方程式:M(s)+CO (g)=N(s)ΔH=-0.51kJmol-1
2
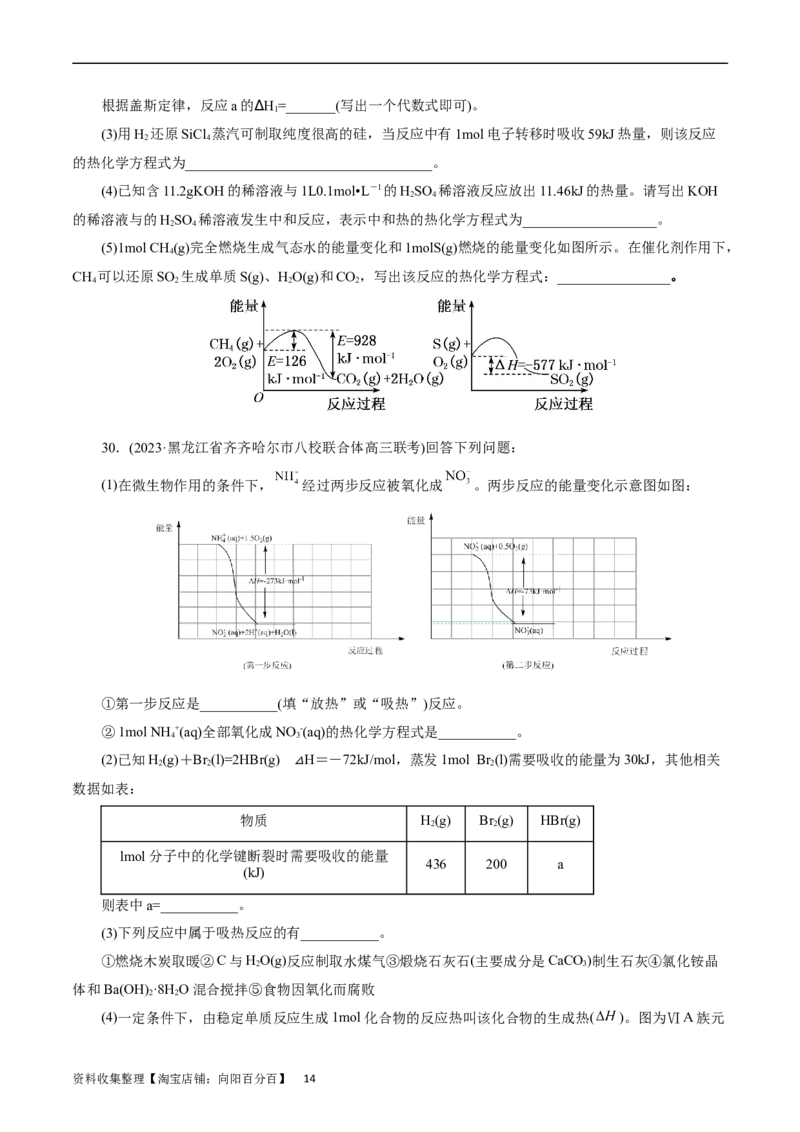
24.(2023·浙江省稽阳联谊学校高三联考)一定条件下,2,3-二甲基⋅-1,3-丁二烯与溴单质发生液相加
成反应(1,2-加成和1,4-加成同时存在),已知体系中两种产物可通过中间产物 互相
转化,反应历程及能量变化如图所示:
下列说法正确的是( )
A. 比 稳定,因此任意条件下主产物均为
B.由 小于 可知,升温有利于 →
资料收集整理【淘宝店铺:向阳百分百】 10C.
D.由反应历程及能量变化图可知,该加成反应为放热反应
【能力提升】
25.(2023·浙江省温州市高三第三次模拟适应性考试)标准状态下,气态反应物、生成物及活化分子
[A(B)表示“A+B→产物”的活化分子]的相对能量如表所示:
物质 NO(g) NO (g) SO (g) SO (g) O(g) O(g) NO(O) SO (O )
2 2 3 2 3 3 2 3
相对能量/ 91.3 33.2 -296.8 -395.7 0 142.7 237.2 -96.1
下列说法不正确的是( )
A.NO (g)+SO (g) NO (g)+ SO (g) ΔH=-40.8 kJ·mol-1
2 2 3
B.3O(g) 2O(g)反应不能自发进行
2 3
C.相同条件下,SO (g)+O(g) O (g)+ SO (g)比NO (g)+O(g) O (g)+ NO (g)速率快
2 3 2 3 3 2 2
D.1mol NO (g)的总键能大于1mol NO(g)总键能
2
26.(2023·浙江省临海、新昌两地高三适应性考试5月模考)叔丁基溴在乙醇中反应的能量变化如图所
示:
反应1:(CH)CBr→(CH)C=CH +HBr
3 3 3 2 2
反应2:C HOH+(CH )CBr→(CH)COC H+HBr
2 5 3 3 3 3 2 5
下列说法不正确的是( )
A.过渡态能量:①>②>③
B.(CH)COC H 可以逆向转化为(CH)CBr,但不会转化为(CH)C=CH
3 3 2 5 3 3 3 2 2
C.若将上述反应体系中的叔丁基溴改为叔丁基氯,则E—E 的值增大
4 3
D.向(CH)CBr的乙醇溶液中加入NaOH并适当升温,可以得到较多的(CH)C=CH
3 3 3 2 2
27.(2023·浙江省杭州地区(含周边)重点中学高三联考化)一定条件下,反应物和生成物的相对能量与
资料收集整理【淘宝店铺:向阳百分百】 11反应历程示意图如下,下列说法不正确的是( )
A.由历程I可计算,SO 的总键能=(E-E ) kJ·mol-l
2 1 3
B.由历程Ⅱ可知,相同条件下O(g)的浓度比SO (g)的浓度对反应速度影响更大
2
C.相同条件下,SO 的平衡转化率,历程I 历程Ⅱ
2
D.由历程I和历程Ⅱ可得,E-E =E-E
5 3 4 2
28.某化学兴趣小组用50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行中和反应的反应热测
定实验,实验装置如图。试回答下列问题:
(1)实验时玻璃搅拌器的使用方法是___;不能用铜丝搅拌器代替玻璃搅拌器的理由是__。
(2)某学生记录的实验数据如表所示。(已知:实验中盐酸和氢氧化钠溶液的密度均为1g•cm-3,中和反
应后溶液的比热容c=4.18J•g-1•℃-1)
起始温度T/℃ 终止温度T/℃
1 2
实验序号
盐酸 氢氧化钠溶液 混合溶液
资料收集整理【淘宝店铺:向阳百分百】 121 20.0 20.2 23.3
2 20.2 20.4 23.4
3 20.4 20.6 23.8
依据该学生的实验数据计算,该实验测得反应放出的热量为__J。
(3)下列操作会导致实验结果出现偏差的是___(填标号)。
a.用量筒量取盐酸的体积时仰视读数
b.把量筒中的氢氧化钠溶液分多次倒入盐酸中
c.将50mL0.55mol•L-1氢氧化钠溶液取成了50mL0.55mol•L-1氢氧化钾溶液
d.做本实验的当天室温较高
e.大烧杯的杯盖中间小孔太大
(4)某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和喊的温度,你是否同
意该同学的观点,为什么?___。
(5)如果将NaOH溶液换成等量的NaOH固体,那么实验中测得中和反应的反应热( H)___(填“偏大”、
“偏小”或“不变”)。 △
(6)如果用60mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行实验,与上述实验相比,二者所放
出的热量___(填“相等”或“不相等”,下同),所求的中和反应H+(aq)+OH-(aq)=H O(1) H的反应热
2
( H)___。 △
△
29.(2023·宁夏石嘴山市模拟)回答下列问题
(1)“世上无难事,九天可揽月”,我国的航空航天事业取得了举世瞩目的成就。碳酰肼类化合物
[Mn(L) ]( ClO ) 是种优良的含能材料,可作为火箭推进剂的组分,其相关反应的能量变化如图所示,已知
3 4 2
△H= -299kJ/mol,则△H (kJ/mol )为_____________
2 1
(2)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO 重整是CO 利用的研究热点
4 2 2
之一、该重整反应体系主要涉及以下反应:
(a)CH(g)+CO (g) 2CO(g)+2H(g) ∆H
4 2 2 1
(b)CO (g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
(c)CH(g) C(s)+2H(g) ∆H
4 2 3
(d)2CO(g) CO(g)+C(s) ∆H
2 4
(e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5
资料收集整理【淘宝店铺:向阳百分百】 13根据盖斯定律,反应a的∆H=_______(写出一个代数式即可)。
1
(3)用H 还原SiCl 蒸汽可制取纯度很高的硅,当反应中有1mol电子转移时吸收59kJ热量,则该反应
2 4
的热化学方程式为___________________________________。
(4)已知含11.2gKOH的稀溶液与1L0.1mol•L-1的HSO 稀溶液反应放出11.46kJ的热量。请写出KOH
2 4
的稀溶液与的HSO 稀溶液发生中和反应,表示中和热的热化学方程式为___________________。
2 4
(5)1mol CH (g)完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化如图所示。在催化剂作用下,
4
CH 可以还原SO 生成单质S(g)、HO(g)和CO,写出该反应的热化学方程式:________________。
4 2 2 2
30.(2023·黑龙江省齐齐哈尔市八校联合体高三联考)回答下列问题:
(1)在微生物作用的条件下, 经过两步反应被氧化成 。两步反应的能量变化示意图如图:
①第一步反应是___________(填“放热”或“吸热”)反应。
②1mol NH +(aq)全部氧化成NO -(aq)的热化学方程式是___________。
4 3
(2)已知H(g)+Br(l)=2HBr(g) H=-72kJ/mol,蒸发1mol Br(l)需要吸收的能量为30kJ,其他相关
2 2 2
数据如表: △
物质 H(g) Br(g) HBr(g)
2 2
lmol分子中的化学键断裂时需要吸收的能量
436 200 a
(kJ)
则表中a=___________。
(3)下列反应中属于吸热反应的有___________。
①燃烧木炭取暖②C与HO(g)反应制取水煤气③煅烧石灰石(主要成分是CaCO)制生石灰④氯化铵晶
2 3
体和Ba(OH) ·8H O混合搅拌⑤食物因氧化而腐败
2 2
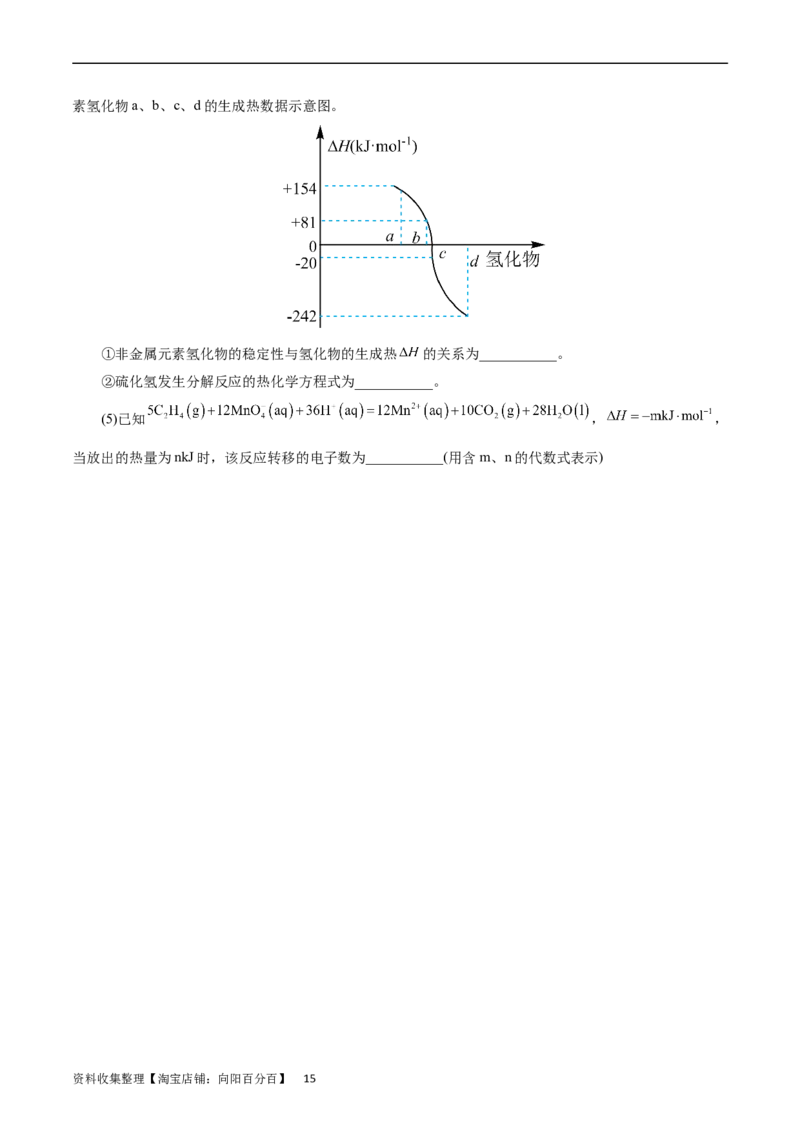
(4)一定条件下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热( )。图为ⅥA族元
资料收集整理【淘宝店铺:向阳百分百】 14素氢化物a、b、c、d的生成热数据示意图。
①非金属元素氢化物的稳定性与氢化物的生成热 的关系为___________。
②硫化氢发生分解反应的热化学方程式为___________。
(5)已知 , ,
当放出的热量为nkJ时,该反应转移的电子数为___________(用含m、n的代数式表示)
资料收集整理【淘宝店铺:向阳百分百】 15