文档内容
解密 03 离子反应
1.(2022·上海交大附中高三阶段练习)下列物质的水溶液能导电,但属于非电解质的是
A.CHCOOH B.Cl C.NH NO D.SO
3 2 4 3 2
2.(2022·甘肃·兰州一中高三期中)分类是科学研究的重要方法。下列物质分类正确的是
A. 都是碱性氧化物 B.磁铁矿、矿泉水、漂白粉都是混合物
C.乙醇、四氯化碳、氯气都是非电解质 D. 都是酸性氧化物
3.(2022·全国·高三专题练习)下列说法正确的是
A. 溶于水得到的氯水能导电,所以 是电解质
B.只有在电流作用下 才能电离成 、 和
C.强电解质溶液的导电能力不一定都强;弱电解质溶液的导电能力不一定都弱
D. 难溶于水,故B 是弱电解质;醋酸铅易溶于水,故醋酸铅是强电解质
4.(2022·河北深州市中学高三阶段练习)下列由NaCl的实验事实得出的结论不正确的是
选
A B C D
项
实
验
事
实
NaCl固体不导
NaCl溶于水 NaCl溶液通电 熔融NaCl能导电
电
NaCl在水中发生
结 NaCl不是电解 a离子是Na+,通电后 NaCl熔融时能电离
电离:NaCl=Na+
论 质 a、b离子定向移动 出自由移动的离子
+Cl-
A.A B.B C.C D.D
5.(2022·全国·高三专题练习)KSO 的电离方程式书写正确的是
2 4
A.KSO =K++SO B.KSO =2K++SO
2 4 2 4
C.KSO =K++2SO D.KSO =K2++SO
2 4 2 4
6.(2021·浙江·高三开学考试)下列物质熔融状态时不导电的是A.MgF B.KCl C.HSO D.NaOH
2 2 4
7.(2022·浙江省普陀中学高三阶段练习)下列物质中,能够导电的电解质是
A.Fe B.熔融的MgCl C.液态纯硫酸 D.蔗糖
2
8.(2022·甘肃武威·高三阶段练习)下列电离方程式正确的是
A.Ba(OH) Ba+2+2OH- B.CHCOOH CHCOO-+H+
2 3 3
C.HPO 3H++PO D.BaCO Ba2++CO
3 4 3
9.(2022·山东·滨州市沾化区实验高级中学高三阶段练习)离子方程式
+2H+=H O+CO↑表示
2 2
A.碳酸盐与盐酸之间的反应 B.一切碳酸盐与一切酸之间的反应
C.可溶性碳酸盐与酸之间的反应 D.可溶性碳酸盐与强酸之间的反应
10.(2022·浙江·高三专题练习)下列有关反应中不属于离子反应的是( )
A.NaCO 溶液与澄清石灰水的反应
2 3
B.氢氧化铜与稀硫酸的反应
C.锌与氯化铜溶液的反应
D.二氧化碳与生石灰作用生成碳酸钙的反应
11.(2022·江西·南昌二中高三阶段练习)下列离子方程式正确的是
A.向含 的 溶液中加入适量 :
B.向 溶液中加入过量氨水:
C. 加入足量稀硝酸中:
D.向漂白粉溶液中通入过量的SO :ClO-+SO +HO= +HClO
2 2 2
12.(2022·山西吕梁·高三阶段练习)宏观辨识和微观探析是化学学科的核心素养之一,
下列指定反应的离子方程式书写正确的是
A.向NaAlO 溶液中加入过量稀盐酸:AlO +H++H O=Al(OH) ↓
2 2 3
B.向CaCl 溶液中通入CO:Ca2++H O+CO=CaCO ↓+2H+
2 2 2 2 3
C.KI溶液久置空气中变黄色:4I-+O +2H O=2I +4OH-
2 2 2
D.明矾(KAl(SO)•12H O)溶液中加入过量Ba(OH) 溶液:Al3++SO +Ba2++3OH-
4 2 2 2
=Al(OH) ↓+BaSO ↓
3 4
13.(2022·辽宁·沈阳二中高三期中)下列离子反应方程式书写正确的是
A.CuSO 与过量浓氮水反应的离子方程式:Cu2++2NH·H O=Cu(OH) +2
4 3 2 2
B.惰性电极电解氯化镁溶液:2C1-+2H O H↑+Cl↑+2OH-
2 2 2
C.向Mg(HCO ) 溶液中加入过量NaOH溶液,产生白色沉淀:Mg2++2 +2OH-
3 2
=MgCO+ +2H O
3 2D.向NH Fe(SO ) 溶液中加入少量Ba(OH) 溶液:2Fe2++3 +3Ba2++6OH-
4 4 2 2
=3BaSO ↓+2Fe(OH) ↓
4 3
14.(2022·江西·南昌二中高三阶段练习)常温下,下列有关溶液组成的描述合理的是
A.在碱性溶液中可以大量存在: 、 、 、
B.在 溶液中可以大量存在: 、 、 、
C.在滴加甲基橙显红色的溶液中可以大量存在: 、 、 、
D.在 的溶液中可以大量存在: 、Cu2+、 、
15.(2022·吉林长春·高三阶段练习)某无色溶液中可能存在
七种离子中的几种。现取该溶液进行实验,得到如
下现象:
①向溶液中滴加足量氯水后,溶液无色变橙色,且有无色气泡冒出;
②向①所得溶液中加入足量 溶液,无明显现象;
③向②所得溶液中继续滴加淀粉溶液,无明显现象。
已知:
据此可以判断,该溶液中一定不存在的离子组是
A. B.
C. D.
16.(2022·湖北·高三期中)向某可能含有 、 、 、 、 的溶液中逐滴
加入NaOH溶液,产生沉淀的物质的量随所加NaOH溶液的体积的变化图像如图所示。图
中各点对应的溶液中离子可以大量共存的是
A.a点: 、 、 B.b点: 、 、
C.c点: 、 、 D.d点: 、 、
1.(2022·浙江温州·三模)25℃时,下列有关电解质溶液的说法正确的是
A.pH、体积均相同的NH Cl和HCl溶液,导电能力相同
4
B.用CHCOOH溶液做导电实验,灯泡很暗,说明CHCOOH是弱酸
3 3C.将1molNH NO 溶于稀氨水中,使溶液呈中性,溶液中n(NH )=n(NO )
4 3
D.物质的量浓度相同的NH Cl溶液和NH HCO 溶液中c(NH ):前者小于后者
4 4 3
2.(2022·河南洛阳·模拟预测)下列各组物质的分类正确的是
选项 混合物 电解质 酸性氧化物 化合物
A 氯水 乙醇 NO CaCl
2 5 2
B 氨水 冰醋酸 MnO NaOH
2 7
C 水玻璃 石膏 SO HD
2
D 水银 氟化氢 CO HCl
2
A.A B.B C.C D.D
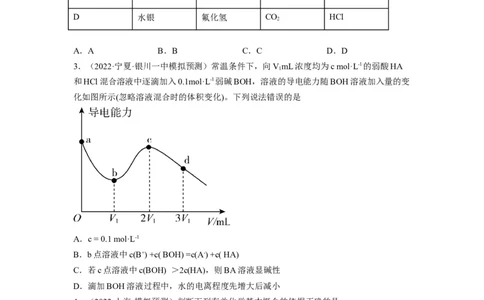
3.(2022·宁夏·银川一中模拟预测)常温条件下,向VmL浓度均为c mol·L-1的弱酸HA
1
和HCl混合溶液中逐滴加入0.1mol·L-1弱碱BOH,溶液的导电能力随BOH溶液加入量的变
化如图所示(忽略溶液混合时的体积变化)。下列说法错误的是
A.c = 0.1 mol·L-1
B.b点溶液中c(B+) +c( BOH) =c(A-) +c( HA)
C.若c点溶液中c(BOH) >2c(HA),则BA溶液显碱性
D.滴加BOH溶液过程中,水的电离程度先增大后减小
4.(2022·上海·模拟预测)判断下列有关化学基本概念的依据正确的是
A.共价化合物:是否含有共价键 B.离子晶体:液态时能否导电
C.强弱电解质:溶液的导电能力大小 D.氧化还原反应:元素化合价是否变化
5.(2021·浙江·模拟预测)下列反应的离子方程式或电离方程式正确的是
A. 溶液中加入足量 溶液:
B.向 溶液中加入 溶液至溶液呈中性C. 溶液中加入铁粉:
D. 在水中的电离:
6.(2022·海南·一模)下列指定反应的离子方程式正确的是
A.用NaOH溶液吸收少量SO :
2
B.向稀FeSO 溶液中滴加稀硝酸:
4
C.向AlCl 溶液中加入过量氨水:
3
D.用盐酸、淀粉KI溶液检验含碘盐中的 :
7.(2022·河北·霸州市第一中学模拟预测)下列各组中的两种物质相互反应时,无论哪种
过量,都可用同一个离子方程式表示的是
①氯化铝溶液与氢氧化钠溶液
②过氧化钠与水
③碘化亚铁溶液与氯水
④碳酸氢钙溶液与澄清石灰水
A.①② B.①③ C.③④ D.②④
8.(2022·湖北·模拟预测)下列各组离子在所给定的条件下可以大量共存的是
选项 条件 离子
A lgc(H+)/c(OH-)< 0 CHCOO-、B-r、Na+
3
B 使KI-淀粉试纸变蓝的溶液 S2-、NH 、Mg2+
C 含有Fe2+的溶液 [Fe(CN) ]3-、Cl-、K+
6
D 0.1mol·L-1NaAlO 2 溶液 H 2 PO 、K+、Ba2+
A.A B.B C.C D.D
9.(2022·河南·焦作市第一中学模拟预测)现有一包粉末样品,可能由
中的两种或三种组成。现进行如下实验:
ⅰ.取适量固体样品于试管中,加足量蒸馏水充分振荡,溶液变浑浊;
ⅱ.将ⅰ中的混合物过滤、洗涤;
ⅲ.向滤渣中加入足量稀盐酸,滤渣部分溶解并产生刺激性气味的气体。
则该样品中一定存在的物质是
A. B.
C. D.
10.(2022·天津·二模)常温下,在指定的溶液中一定能大量共存的离子组是A.使pH试纸变蓝的溶液:Al3+、Na+、SO 、Cl-
B. =1×10-12的溶液:K+、AlO 、CO 、Na+
C.加入苯酚显紫色的溶液:Na+、NH 、Cl-、I-
D.c(SO )=0.1mol/L的溶液:K+、MnO 、SO 、H+
11.(2022·上海上海·二模)除去下列物质中的杂质(括号内为杂质),可采用加入过量
NaOH溶液充分反应后,再用过滤方法分离的是
A.AlCl 溶液(FeCl ) B.NaCO 溶液(NaHCO )
3 3 2 3 3
C.Fe O 固体(AlO) D.NaCl溶液(MgCl )
2 3 2 3 2
12.(2020·江西·临川一中一模)向FeCl 溶液中加入NaSO 溶液,测定混合后溶液pH随
3 2 3
混合前溶液中 变化的曲线如图所示。
实验发现:
ⅰ.a 点溶液澄清透明,向其中滴加 NaOH 溶液后,立即产生灰白色沉淀,滴入 KSCN 溶
液显红色;
ⅱ.c 点和 d 点溶液中产生红褐色沉淀,无气体逸出;取其上层清液滴加NaOH溶液后无
明显现象,滴加 KSCN 溶液显红色。
下列分析合理的是
A.检验a点溶液中反应生成的阴离子所需试剂为:稀硝酸和BaCl 溶液
2
B.c点和d点出现上述现象的主要原因是Fe3+和 发生双水解反应
C.b点较a点溶液pH升高的主要原因:2Fe3++ +H O = 2Fe2++ +2H+
2
D.向d点上层清液中滴加 NaOH溶液无明显现象,证明溶液中无Fe3+
13.(2022·江西·赣州市赣县第三中学高三阶段练习)按要求写出下列反应的方程式
(1)氯气和水反应的离子方程式:_______;
(2)Ca(ClO) +CO +H O的化学方程式:_______;
2 2 2
(3)工业上制取氯气的离子方程式:_______;
(4)工业制漂白粉的化学方程式:_______ ;
(5) )胶体制备的离子方程式:_______;(6)向 溶液滴加 溶液至 时的离子方程式:_______ ;
(7)FeSO 的酸性溶液与HO 反应试写出该反应的离子方程式:_______ ;
4 2 2
(8)Fe3+可腐蚀印刷电路板上的铜箔,反应的离子方程式为_______;
(9)向NaClO溶液中通入少量的CO 离子方程式_______;
2
(10)FeBr 溶液中通入等物质的量的Cl 气体,离子方程式为:_______。
2 2
14.(2022·陕西·大荔县教学研究室一模)元素化合物在化工生产和环境科学中有着重要
的用途。
(1)向NH Al(SO ) 溶液中逐滴加入稀NaOH溶液至过量,反应的离子方程式依次为____、
4 4 2
____、____。
(2)自然界中Cr主要以+3价和+6价形式存在。 中的Cr能引起细胞的突变,可以用亚
硫酸钠在酸性条件下将 还原。写出该反应的离子方程式:____。
(3)常温下,氰化钠(NaCN)能与过氧化氢溶液反应生成一种酸式盐和一种能使湿润的红色石
蕊试纸变成蓝色的气体,大大降低其毒性。写出该反应的离子方程式:____。
(4)已知:CCl 与水不相溶且密度比水大,Cl 的CCl 溶液呈黄绿色,Br 的CCl 溶液呈橙红
4 2 4 2 4
色,且Br 易从水溶液中溶入CCl 中。Cl 既能氧化Br-,也能氧化Fe2+。
2 4 2
①取10mL0.1mol/LFeBr 溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量
2
反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl ,振荡后,
4
下层为无色液体。以上实验结论表明还原性:Fe2+____Br- (填“>”或“<”)。
②若在400mL0.1mol/LFeBr 溶液中通入标准状况下672mL的Cl,取少量反应后的溶液加
2 2
入CCl ,振荡后下层液体呈____色,写出该反应的离子方程式____。
4
15.(2022·江西·高三阶段练习)Q溶液中含有如表所示离子中的某5种且浓度均为0.5
(不考虑水的电离与离子水解)。向Q溶液中加入足量稀氢溴酸,有气体R产生。经
分析,反应前后阴离子种类不变。
阳离子 阴离子
、 、 、 、 、 、 、 、 、 、 、 ,
、 、
请回答下列问题:
(1)写出一种检验气体R的方法:_______。写出产生气体R的离子方程式:_______。
(2)由“加入氢溴酸……”、“反应前后阴离子种类不变”推知:Q一定不含_______(填中
文数字)种阴离子。
(3)综合排断,Q一定含离子有_______(填离子符号)。
(4)一定量Q与氯气缓慢反应,实验结果如下:①“血红色溶液”变为蓝色溶液,发生反应的离子方程式为_______。
②V的范围为_______。