文档内容
解密 03 离子反应
考点热度 ★★★★★
【考纲导向】
1.了解离子反应的概念,了解离子反应发生的条件,并会判断离子在溶液中能否大量共存。
2.了解电解质的概念,了解强电解质与弱电解质的概念。
3.理解电解质在水中的电离以及电解质溶液的导电性。
4.能正确书写离子方程式,或结合具体反应对所给离子方程式进行正误判断。
【命题分析】
离子方程式的书写及正误判断、溶液中的离子共存是每年高考的热点,高考再现率为100%。在高考试题中,
大多以选择题形式呈现,但增加了限制条件和隐含条件,基本每一个选项都会有干扰,并且加大氧化还原
反应的考察。选择题常以离子方程式正误判断的形式呈现,非选择题常与氧化还原反应理论、化学工艺流
程、实验滴定(沉淀滴定、氧化还原滴定)相结合,书写相关反应的离子方程式。氧化还原型离子方程式的
书写是近几年全国卷命题的热点内容。离子共存类选择题主要为限定条件下离子能否大量共存的判断。
离子推断类试题Ⅰ卷、Ⅱ卷均有考查,主要利用离子的特征反应,通过定性、定量分析,确定离子存在情
况,进而推断物质。
核心考点一 离子方程式的书写与正误判断
离子方程式中物质的拆分原则
(1)强酸、强碱和可溶性盐写成离子形式。
(2)弱酸、弱碱、难溶盐、单质、氧化物、气体用化学式表示。(3)多元弱酸的酸式盐的酸根离子(如HCO、HSO等)在离子方程式中不能拆开写,多元强酸的酸式盐的酸根
离子(如HSO)在离子方程式中拆开写。
(4)微溶物的处理情况:
①当反应物是微溶物的澄清稀溶液时(如澄清石灰水),微溶物应写成离子形式。
②当反应物是微溶物的浊液或固态时(如石灰乳),微溶物应写化学式。
③生成物中的微溶物按难溶物处理,应写化学式。
(5)固体之间的反应(如消石灰与NH Cl),固体与特定溶液(如Cu与浓硫酸)的反应不能用离子方程式表示。
4
离子方程式正误判断要注意4个两
考法 离子方程式的书写与正误判断(题型预测:选择题)
1.(2022·全国)能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水混合:Al3++4NH+2H O=AlO +4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO +CO +H O=HSiO +HCO
2 2
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO =BaSO ↓+2H O
2 4 4 4 2
与“量”有关的离子方程式的书写方法
(1)先后反应型离子方程式的书写——“假设定序”法
这类反应只要明确了离子反应的先后顺序,书写也就迎刃而解了。如向FeBr 溶液中通入Cl ,在不明确离
2 2
子反应的先后顺序时,可假设Cl 先与Br-反应,则生成的溴单质还要氧化Fe2+生成Fe3+,这样即可确定
2
Cl 先与Fe2+反应, 后与Br-反应,然后再根据量的关系书写即可。
2(2)离子配比型离子方程式的书写——“少定多变”法
就是把相对量较少的物质定为“1 mol”,若少量物质有两种或两种以上离子
“少定”
参加反应,则参加反应的离子的物质的量之比与原物质组成比相符
就是过量的反应物,其离子的化学计量数根据反应实际需求量来确定,不受
“多变”
化学式中的比例制约,是可变的
如少量NaHCO 与足量Ca(OH) 溶液的反应:
3 2
“少定”——即定HCO的物质的量为1 mol;
“多变”——1 mol HCO能与1 mol OH-发生反应,得到1 mol H O和1 mol CO,1 mol CO再与1 mol Ca2+
2
结合生成CaCO 沉淀,离子方程式为HCO+Ca2++OH-===CaCO ↓+HO。
3 3 2
变式1 离子反应的判断
1.(2022·山西预测)根据离子反应发生的条件,判断下列各组物质中不能发生离子反应的是
A.稀HSO 与BaCl 溶液 B.NaOH溶液与CuSO 溶液
2 4 2 4
C.NaOH溶液与KCl溶液 D.NaHCO 溶液与稀HCl
3
变式2 离子方程式的意义
2.(2022·北京)下列方程式与所给事实不相符的是
A.加热 固体,产生无色气体:
B.过量铁粉与稀硝酸反应,产生无色气体:
C.苯酚钠溶液中通入 ,出现白色浑浊:
D.乙醇、乙酸和浓硫酸混合加热,产生有香味的油状液体:
变式3 离子方程式正误判断
3.(2022·浙江)下列反应的离子方程式不正确的是
A.盐酸中滴加 溶液:
B. 溶液中通入过量 :C.乙醇与 酸性溶液反应:
D.溴与冷的 溶液反应:
变式4 与量有关的离子方程式正误判断
4.(2022·浙江)下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
3 2
B.将少量NO 通入NaOH溶液:2NO +2OH-= + +H O
2 2 2
C.将少量SO 通入NaClO溶液:SO +H O+2ClO-= +2HClO
2 2 2
D.向氨水中滴入少量硝酸银溶液:Ag++2NH·H O= +2H O
3 2 2
变式5 定量型离子方程式正误判断
5.(2022·辽宁·高三期中)下列反应的离子方程式书写正确的是
A.向 溶液中逐滴滴加氨水直至过量:
B.澄清石灰水与少量小苏打溶液混合:
C.向 溶液中加入含等物质的量溶质的 溶液:
D.NaClO溶液与HI溶液反应:
1.(2022·四川模拟)依据现有知识分析判断,下列选项中不满足离子反应发生条件的是
A.
B.
C.
D.2.(2022·广东)下列关于 的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:
B.碱转化为两种盐:
C.过氧化物转化为碱:
D.盐转化为另一种盐:
3.(2022·江西·临川一中高三期中)下列离子方程式书写正确的是
A.向FeBr 溶液中通入少量Cl:2Br-+Cl=Br +2Cl-
2 2 2 2
B.向Ca(OH) 溶液中滴加少量的NaHCO 溶液:Ca2++2OH-+2HCO =CaCO ↓+CO +2H O
2 3 3 2
C.向Ba(NO ) 溶液中通入SO 气体产生白色沉淀:Ba2++SO+H O=BaSO↓+2H+
3 2 2 2 2 3
D.向KAl(SO ) 溶液中滴加Ba(OH) 溶液至沉淀质量最大:Al3++2SO +4OH-+2Ba2+=2BaSO ↓+AlO
4 2 2 4
+2H O
2
4.(2022·吉林·抚松县第一中学模拟预测)下列离子方程式书写错误的是
A.将少量 气体通入NaClO溶液中:
B.向含等物质的量的 、 、 的溶液中通入等物质的量的氯气:
C.向 溶液中滴加 溶液:
D.向明矾溶液中滴加 溶液,使沉淀的物质的量最大时:
5.(2022·海南·高三阶段练习)“宏观辨识与微观探析”是化学学科核心素养之一,下列过程中发生反应
的离子方程式正确的是
A.向 溶液中通入过量 :B.过量 通入稀漂白粉溶液中:
C.向 溶液中加入稀硝酸:
D. 溶于HI溶液中:
6.(2022·四川·石室中学高三阶段练习)能正确表示下列反应的离子方程式为
A.过氧化物转化为碱:
B.向 溶液中加入同体积同浓度的 溶液:
C.用醋酸和淀粉 溶液检验加碘盐中的 :
D.向 溶液中通入等物质的量的 :
核心考点二 离子共存与离子推断
1.离子共存题中常考查的离子性质
颜色 MnO(紫红色)、Cu2+(蓝色)、Fe2+(浅绿色)、Fe3+(黄色)
氧化性 MnO(H+)、NO(H+)、Fe3+、ClO-
还原性 Fe2+、I-、S2-(HS-)、SO(HSO)
水解显酸性 NH、 Al3+、Zn2+、Fe2+、Fe3+、Cu2+、Ag+
水解显碱性 AlO、CO、ClO-、SO、S2-、SiO、CHCOO-
3
2.离子不能共存的原因
(1)发生复分解反应
①生成难溶物或微溶物;②生成气体或挥发性物质;③生成难电离物质。
(2)发生氧化还原反应
①具有较强氧化性的离子(如MnO、ClO-、Fe3+等)与具有较强还原性的离子(如Fe2+、S2-、I-、SO等)不
能共存;②NO与I-,S2-与SO,Cl-与ClO-等在酸性条件下不能共存,而在碱性条件下可共存。
(3)发生相互促进的水解反应
某些弱碱阳离子与某些弱酸阴离子因发生相互促进的水解反应而不能大量共存。如 Al3+与AlO、HCO、
CO、S2-,Fe3+与AlO、HCO、CO等发生相互促进的水解反应生成沉淀或气体。
(4)发生络合反应若离子间发生络合反应,则这些离子不能共存。如Fe3+与SCN-不能共存。
3.溶液酸碱性的三类描述(室温下)
(1)pH<7或c(H+)>c(OH-)或c(H+)>10-7 mol·L-1
(2)能使pH试纸显红色的溶液
酸性溶液
(3)能使甲基橙显红色或橙色的溶液
(4)能使紫色石蕊溶液显红色的溶液
(1)pH>7或c(H+)10-7 mol·L-1
(2)能使酚酞溶液显红色的溶液
碱性溶液
(3)能使紫色石蕊溶液显蓝色的溶液
(4)能使pH试纸显蓝色的溶液
可能为酸
性溶液也 (1)与Al反应放出H 的溶液
2
可能为碱 (2)常温下,水电离出的c(H+)或c(OH-)浓度不是10-7 mol·L-1
性溶液
4.离子共存题目的3步解题流程
5.解离子推断题依据4项基本原则,确定离子是否存在
(1)肯定原则:根据实验现象,推出肯定存在或肯定不存在的离子。
(2)互斥原则:即相互反应的离子不能大量共存。
①根据“互斥原则”,若推出溶液中已存在某离子,那么能与该离子反应的离子则不能大量存在。
②可以根据“互斥原则”,先确定离子间的组合,这样可以大大减少思维量。例如Ag+只能为AgNO ,碳
3
酸盐只能为NaCO、KCO、(NH )CO 等。
2 3 2 3 4 2 3
(3)进出原则:即加入试剂时带入(“进”)的离子和发生反应时消耗(“出”)的离子,对后续实验是否有影
响。
(4)守恒原则:即溶液中电荷守恒。
考法 离子共存与离子推断(题型预测:选择题)
1.(2022·重庆一中高三阶段练习)下列各组离子在指定溶液中一定能大量共存的是A.澄清透明的溶液中: 、 、 、
B.酸度 的溶液中: 、 、 、
C.久置的氯水中: 、 、 、
D.加入铝粉能产生 的溶液中: 、 、 、
2.(2022·辽宁·高三阶段练习)某无色混合气体中可能含有Cl、O、SO 、NO、NO 中的一种或几种。现
2 2 2 2
将此混合气体通过品红溶液后,品红溶液褪色,向剩余气体中通入空气,很快变为红棕色。下列对原混合
气体成分的判断正确的是
A.肯定只有SO B.肯定没有Cl、O 和SO
2 2 2 2
C.可能有Cl 和O D.肯定只有NO、SO
2 2 2
1.审离子共存题目中的5大易忽视点
(1)注意判断离子共存的情况:“能、不能”,“一定、可能、一定不能”。
(2)注意题干中提示的溶液酸碱性:酸性溶液应考虑H+的存在,碱性溶液应考虑OH-的存在。
(3)注意题干中提示的溶液颜色:溶液无色时,有色离子不能存在。
(4)注意正确理解“透明溶液”,如NaCl溶液、KOH溶液为无色透明溶液,CuSO 溶液、FeCl 溶液是有色
4 3
透明溶液,不能认为“有色”就不透明。
(5)注意题干中提示的水的电离程度:当由水电离出的c(H+)或c(OH-)小于1×10-7 mol·L-1时,溶液可能
为酸性溶液或碱性溶液;当由水电离出的c(H+)或c(OH-)大于1×10-7 mol·L-1 时,溶液可能为弱酸盐溶
液或弱碱盐溶液。
2.解离子推断时的注意事项
(1)注意有颜色的离子与溶液的颜色是否一致。
(2)根据某现象推出含有的某种离子,该离子是否为前面的操作引入的。
(3)注意离子共存问题。
①离子是否能存在于溶液中,要特别注意溶液的性质(如酸碱性、氧化性、还原性)与离子的性质。
②推断结果中的离子是否能共存于同一溶液中。
③离子是否会隐蔽转化,如Al3+遇到过量的强碱转化为AlO,AlO遇到过量的强酸转化为Al3+。
变式1 常见限制条件的离子共存
1.(2022·天津河北·高三期中)常温下,下列各组离子在指定溶液中能大量共存的是A. 的溶液中: 、 、 、
B.无色溶液中: 、 、 、
C.含有 的溶液中: 、 、 、
D. 的溶液中: 、 、 、
变式2 隐含条件的离子共存
2.(2022·江西吉安·高三阶段练习)常温下,下列离子在指定条件下的溶液中一定可以大量共存的是
A. 的溶液:
B.加入 淀粉溶液后会变蓝色的溶液:
C. 的溶液:
D.滴加盐酸有气泡产生的溶液:
变式3 离子的推断
3.(2022·黑龙江·哈尔滨七十三中高三阶段练习)在一含Na+的澄清溶液中,可能还存在NH 、Fe2+、I-、
Br-、CO 、SO 离子中的几种:①在原来溶液中滴加足量的饱和氯水,有气泡生成,溶液呈现橙黄色②
向呈橙黄色的溶液中加入BaCl 溶液时无沉淀生成③橙黄色溶液不能使淀粉溶液变蓝色。根据上述实验事
2
实推断,下列说法不正确的是
A.溶液中一定存在Br-、CO B.溶液中可能存在NH
C.溶液中一定不存在Fe2+、I-、SO D.溶液一定呈碱性
变式4 混合物成分的分析与推断
4.(2022·湖南·长沙一中高三阶段练习)某澄清透明溶液中可能含有 、 、 、 、 、
、 、 中的几种离子,其离子浓度均为 。某化学社的成员进行如下实验:下列说法正确的是
A.无法确定原溶液中是否含有 、
B.滤液X中大量存在的阳离子有 、 和
C.沉淀C为
D.原溶液中存在的离子为 、 、 、
1.(2022·宁夏·银川二中高三阶段练习)下列各组离子在给定溶液中能大量共存的是
A.在0.1mol/L氨水中:Cu2+、Na+、NO 、S2- B.在0.1mol/L氯化钠溶液中:I-、Fe3+、HCO
C.在0.1mol/L硝酸溶液中:Cl-、Fe2+、SO D.在0.1mol/L醋酸溶液中:K+、NO 、SO
2.(2022·山西运城·高三期中)下列各组离子在指定的溶液中可能大量共存的是
A.0.1mol/L硫酸: 、 、 、
B.使酚酞变红色的溶液: 、 、 、
C.加入铝产生氢气的溶液: 、 、 、
D.0.1mo/L 溶液: 、 、 、
3.(2023·广东佛山·高三阶段练习)下列微粒在所给条件下,能大量共存的是
A.滴加KSCN溶液后显红色的溶液中: 、 、 、
B.遇酚酞显红色的溶液中: 、 、 、
C.澄清透明的酸性溶液中: 、 、 、D.常温下, 的溶液中: 、 、 、
4.(2022·黑龙江·牡丹江市第三高级中学高三阶段练习)常温下,下列各组离子在指定溶液中一定能大量
共存的是
A.某无色溶液中: 、 、 、
B.加入足量过氧化钠后的溶液中: 、 、 、
C.在 的溶液中: 、 、 、
D.由水电离的 的溶液中: 、 、 、
5.(2022·四川省内江市第六中学高三阶段练习)某溶液中可能存在Br-、 、 、Al3+、I-、Mg2+、
Na+7种离子中的几种。现取该溶液进行实验,得到如下实验现象:①向溶液中滴加足量氯水后,溶液变橙
色,且有无色气泡冒出;②向所得橙色溶液中加入足量BaCl 溶液,无沉淀生成;③向所得溶液中滴加淀
2
粉溶液,溶液不变蓝色。据此可以推断,该溶液中肯定不存在的离子是
A.Al3+、Na+、 、I- B.Mg2+、Na+、 、I-
C.Al3+、Mg2+、I-、 D.Al3+、 、Br-、I-
6.(2022·辽宁·沈阳二中高三期中)常温下pH=1的某溶液A中含有 、K+、Na+、Fe3+、Al3+、Fe2+、
、 、Cl-、I-、 中的几种,且溶液中各离子的物质的量浓度均为0.1moL/L,现取该溶液进行有
关实验,实验结果如图所示:下列有关说法正确的是
A.该溶液中一定有上述离子中的 、Al3+、 、Cl-四种离子
B.实验消耗Cu14.4g,则生成气体丁的体积为3.36LC.可用焰色试验确定原溶液中是否含有Na+,若含有Na+灼烧时火焰呈黄色,是因为基态的电子跃迁激发
态若未见黄色火焰则无Na+
D.一定没有Fe3+,但是无法确定是否含有I-
7.(2022·湖南省祁东县育贤中学高三阶段练习)若向含有 , 的混合溶液中逐滴加入
150mL 的HCl溶液,测得溶液中某几种离子的物质的量的变化情况如右图所示。则下列说法中,
不正确的是
A.结合 的能力:
B.在M点发生的反应为
C.原混合溶液中, 与 的物质的量浓度相同
D.若原混合溶液与盐酸充分反应,最终消耗盐酸体积的最大值为300mL
8.(2022·辽宁实验中学模拟预测)一种以黑钨矿(主要成分是FeWO 和MnWO ,还含有Si、As等元素的
4 4
杂质)为原料制备钨酸(H WO)的工业流程如图所示。
2 4
已知:“水浸”后滤液中主要阴离子为 、 、 和
下列说法错误的是
A.滤渣的成分是HSiO
2 3
B.“焙烧”过程中,Fe、Mn元素被氧化
C.“氧化”过程发生反应的离子方程式是 +ClO-= +Cl-D.“沉钨”过程,用Ca(OH) 溶液代替CaCl 溶液效果更好
2 2
【考点拓展】离子反应其它考查方式
拓展一 离子反应与图象相结合
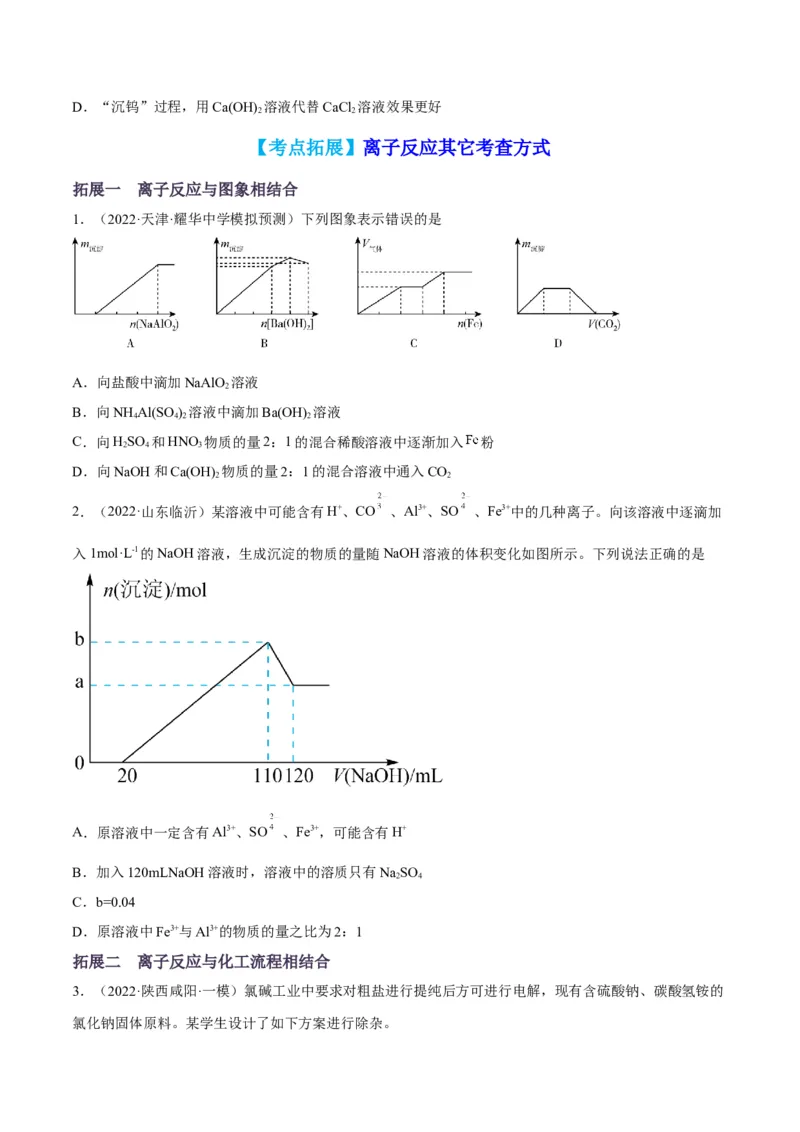
1.(2022·天津·耀华中学模拟预测)下列图象表示错误的是
A.向盐酸中滴加NaAlO 溶液
2
B.向NH Al(SO ) 溶液中滴加Ba(OH) 溶液
4 4 2 2
C.向HSO 和HNO 物质的量2:1的混合稀酸溶液中逐渐加入 粉
2 4 3
D.向NaOH和Ca(OH) 物质的量2:1的混合溶液中通入CO
2 2
2.(2022·山东临沂)某溶液中可能含有H+、CO 、Al3+、SO 、Fe3+中的几种离子。向该溶液中逐滴加
入1mol·L-1的NaOH溶液,生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列说法正确的是
A.原溶液中一定含有Al3+、SO 、Fe3+,可能含有H+
B.加入120mLNaOH溶液时,溶液中的溶质只有NaSO
2 4
C.b=0.04
D.原溶液中Fe3+与Al3+的物质的量之比为2:1
拓展二 离子反应与化工流程相结合
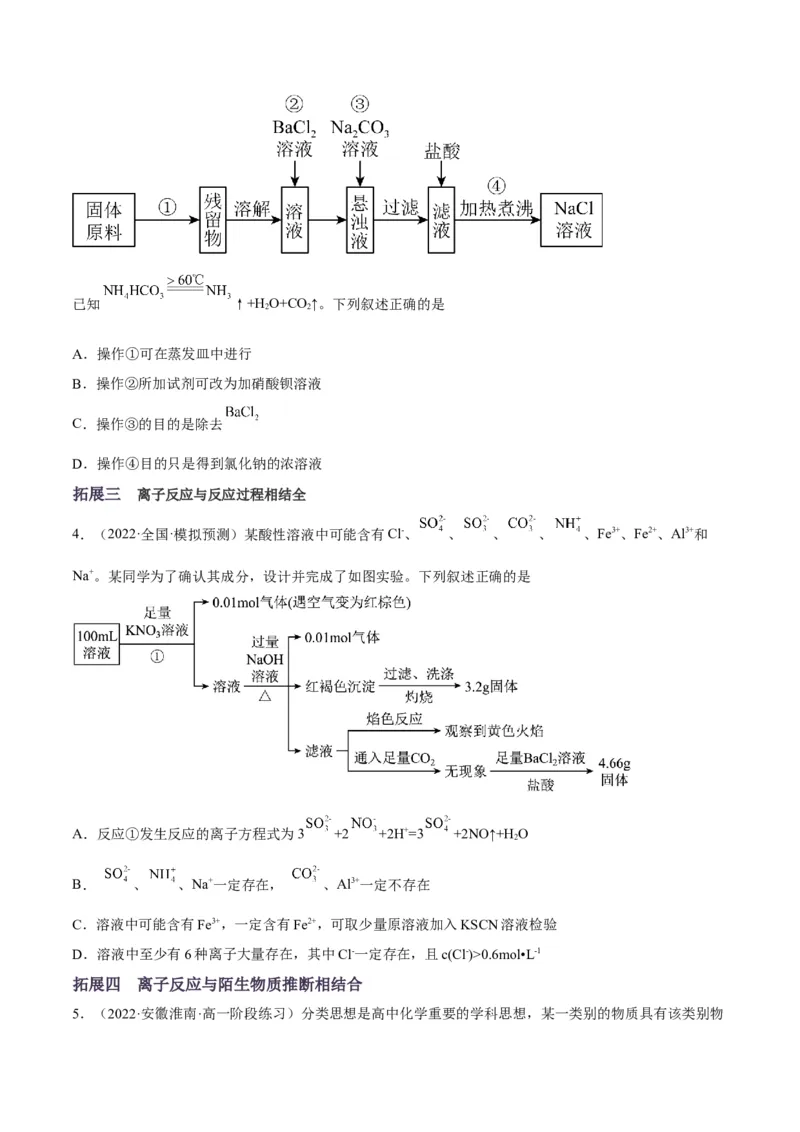
3.(2022·陕西咸阳·一模)氯碱工业中要求对粗盐进行提纯后方可进行电解,现有含硫酸钠、碳酸氢铵的
氯化钠固体原料。某学生设计了如下方案进行除杂。已知 ↑+H O+CO↑。下列叙述正确的是
2 2
A.操作①可在蒸发皿中进行
B.操作②所加试剂可改为加硝酸钡溶液
C.操作③的目的是除去
D.操作④目的只是得到氯化钠的浓溶液
拓展三 离子反应与反应过程相结全
4.(2022·全国·模拟预测)某酸性溶液中可能含有Cl-、 、 、 、 、Fe3+、Fe2+、Al3+和
Na+。某同学为了确认其成分,设计并完成了如图实验。下列叙述正确的是
A.反应①发生反应的离子方程式为3 +2 +2H+=3 +2NO↑+HO
2
B. 、 、Na+一定存在, 、Al3+一定不存在
C.溶液中可能含有Fe3+,一定含有Fe2+,可取少量原溶液加入KSCN溶液检验
D.溶液中至少有6种离子大量存在,其中Cl-一定存在,且c(Cl-)>0.6mol•L-1
拓展四 离子反应与陌生物质推断相结合
5.(2022·安徽淮南·高一阶段练习)分类思想是高中化学重要的学科思想,某一类别的物质具有该类别物质的通性。因此,可以通过物质类别判断、预测陌生物质的性质及反应。无机化合物按照组成和性质可进
行如下分类:
无机化合物
酸 碱 盐 氧化物
③_______
实 ①HCl ⑤
④ ⑦_______
例
②_______ ⑥_______
(其中②、③、⑥均由N、H、O中的3种元素组成)
(1)写出表中物质的化学式:②_______,③_______,⑥_______。
(2)酸、碱、盐在水溶液中发生复分解反应的条件是_______;利用表格中物质间的反应,写出两个生成气
体的离子反应方程式:_______,_______
(3)⑦是硫元素的最高价氧化物,其化学式是_______,它属于_______(填“酸”或“碱”)性氧化物。实验
室中可以用NaOH溶液吸收该氧化物,写出该反应的离子方程式:_______。