文档内容
题型 18 化学反应原理综合题
目 录
题型综述
解题攻略
题组 01 反应热+化学平衡的小综合
题组 02 反应热+反应速率+化学平衡的小综合
题组 03 反应热+反应机理+反应速率+化学平衡大综合
题组 04 反应热+反应速率+化学平衡+电化学大综合
题组 05 反应热+反应速率+化学平衡+电解质溶液大综合
高考练场
化学反应原理综合题是高考必考题型,承载着宏观辨识与微观探析、变化观念与平衡思想、证据推理
与模型认知等核心素养,及变化观、微粒观等重要学科思想,常与生产、生活、科技等紧密联系的物质为
背景材料,把热化学、电化学及四大平衡知识融合在一起命制,题目设问较多,涉及内容也较多,多数题
目含有图像或图表,导致思维转换角度较大,对考生思维能力的要求较高。根据对近几 年的高考试题分析
来看,从考点设置的角度,可将本专题分为四个题组:一是反应热+化学平衡的小综合;二是反应热+反应
速率+化学平衡的小综合;三是反应热+反应机理+反应速率+化学平衡大综合,四是反应热+反应速率+化学平
衡+电化学大综合,五是反应热+反应速率+化学平衡+电解质溶液大综合。
题组 01 反应热+化学平衡的小综合
【例 1-1】(2024·山东卷)水煤气是 的主要来源,研究 对 体系制 的影响,涉及主要反应如
下:
/回答下列问题:
(1) 的焓变 (用代数式表示)。
(2)压力 p 下, 体系达平衡后,图示温度范围内 已完全反应, 在 温度时完全
分解。气相中 , 和 摩尔分数随温度的变化关系如图所示,则 a 线对应物质为 (填化学式)。
当温度高于 时,随温度升高 c 线对应物质摩尔分数逐渐降低的原因是 。
(3)压力 p 下、温度为 时,图示三种气体的摩尔分数分别为 0.50,0.15,0.05,则反应
的平衡常数 ;此时气体总物质的量为 ,则 的
物质的量为 ;若向平衡体系中通入少量 ,重新达平衡后,分压 将 (填“增
大”“减小”或“不 将 (填“增大”“减小”或“不
变”), 变”)。
【例 1-2】(2024·江西卷)石油开采的天然气含有 HS。综合利用天然气制氢是实现“碳中和”的重要途径。
2
CH 和 H S 重整制氢的主要反应如下:
4 2
反应Ⅰ:CH 4(g)+2H 2S(g)⇌CS 2(g)+4H 2(g) ΔH 1=+260kJ/mol
反应Ⅱ:CH 4(g)⇌C(s)+2H 2(g) ΔH 2=+90kJ/mol
反应Ⅲ:2H 2S(g)⇌S 2(g)+2H 2(g) ΔH 3=+181kJ/mol
回答下列问题:
(1)HS 分子的电子式为 。
2
(2)反应Ⅳ:CS 2(g)⇌S 2(g)+C(s)ㅤΔH 4= kJ/mol。
(3)保持反应器进料口总压为 100kPa.分别以 8kPaCH 、24kPaH S(He 作辅气)与 25kPaCH 、75kPaH S 进
4 2 4 2
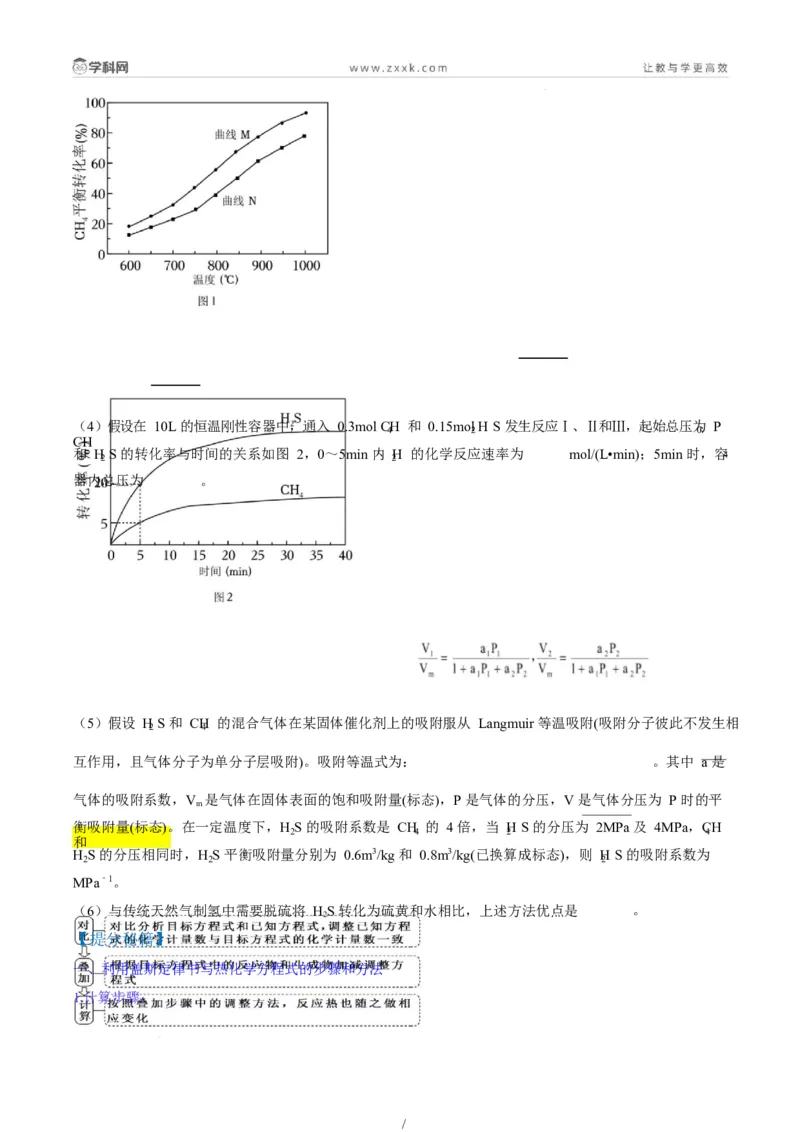
料。CH 平衡转化率与温度的关系如图 1,含有 He 的曲线为 ,理由是 。
4
/(4)假设在 10L 的恒温刚性容器中,通入 0.3mol CH 和 0.15mol H S 发生反应Ⅰ、Ⅱ和Ⅲ,起始总压为 P
4 2 0.
CH
和 H
2
S 的转化率与时间的关系如图 2,0~5min 内
2
H 的化学反应速率为 mol/(L•min);5min 时,容4
器内总压为 。
(5)假设 H S 和 CH 的混合气体在某固体催化剂上的吸附服从 Langmuir 等温吸附(吸附分子彼此不发生相
2 4
互作用,且气体分子为单分子层吸附)。吸附等温式为: 。其中 a 是
气体的吸附系数,V 是气体在固体表面的饱和吸附量(标态),P 是气体的分压,V 是气体分压为 P 时的平
m
衡吸附量(标态)。在一定温度下,H S 的吸附系数是 CH 的 4 倍,当 H S 的分压为 2MPa 及 4MPa,CH
2 4 2 4
和
H S 的分压相同时,H S 平衡吸附量分别为 0.6m3/kg 和 0.8m3/kg(已换算成标态),则 H S 的吸附系数为
2 2 2
MPa﹣1。
(6)与传统天然气制氢中需要脱硫将 HS 转化为硫黄和水相比,上述方法优点是 。
2
【提分秘籍】
一、利用盖斯定律书写热化学方程式的步骤和方法
1.计算步骤:
/2.计算方法
二、平衡转化率大小变化分析技巧
1.转化率问题首先看是否是平衡转化率,若为非平衡状态的转化率,则侧重分析温度、压强、浓度对反应快
慢、催化剂对反应快慢及选择性(主副反应)的影响;若为平衡转化率,则侧重分析温度、压强、浓度对化学
平衡的影响,有时也涉及温度对催化活性的影响。
2.判断反应物转化率的变化时,不要把平衡正向移动与反应物转化率提高等同起来,要视具体情况而定。常
见有以下几种情形:
反应类型 条件的改变 反应物转化率的变化
恒容时只增加反
反应物 A 的转化率减小,反应物 B 的转化率增大
应物 A 的用量
恒温恒压条件下 反应物转化率不变
有多种反应物的可逆 反应物 A 和 B 的转化率
m+n>p+q
反应:mA(g)+nB(g) 同等倍数地增大 均增大
pC(g)+qD(g) 反应物 A、B 的 恒温恒容 反应物 A 和 B 的转化率
m+n<p+q
量 条件下 均减小
反应物 A 和 B 的转化率
m+n=p+q
均不变
恒温恒压
反应物转化率不变
只有一种反应物的可 条件下
增加反应物 A 的
逆反应:mA(g) m>n+p 反应物 A 的转化率增大
用量 恒温恒容
nB(g)+pC(g) m<n+p 反应物 A 的转化率减小
条件下
m=n+p 反应物 A 的转化率不变
【变式演练】
【变式 1-1】(2024·河南·三模)氨是重要化工原料,其工业合成原理为
。回答下列问题:
/(1)已知:ⅰ. ;
ⅱ. (a、b 都大于 0)。
则反应 的 (用含 a、b 的代数式表示),利于该反应正向进行的
条件为 (填“低温”“高温”或“任意温
度”)。
(2)向恒温恒容密闭容器中充入体积比 的 和 ,发生反应 。下列情况
表明该反应一定达到平衡状态的是___________(填字母,下同)。
A.气体密度不随时间变化 B.气体平均摩尔质量不随时间变化
C.气体总压强不随时间变化 D. 体积分数不随时间变化
(3)下列关于 的叙述正确的是 。
A. 生成速率等于 消耗速率的 2 倍
B.若加入高效催化剂,平衡常数和反应热都会增大
C.若起始按体积比 投入 和 ,则 和 的转化率相等
(4)向 刚性密闭容器中充入 和 合成氨,经历相同时间测得 转化率与温度及时间的关
系如图 1 所示。
①温度: (填“>”或“<”)。
② 温度下,合成氨反应的平衡常数 为 (结果保留三位有效数字)。
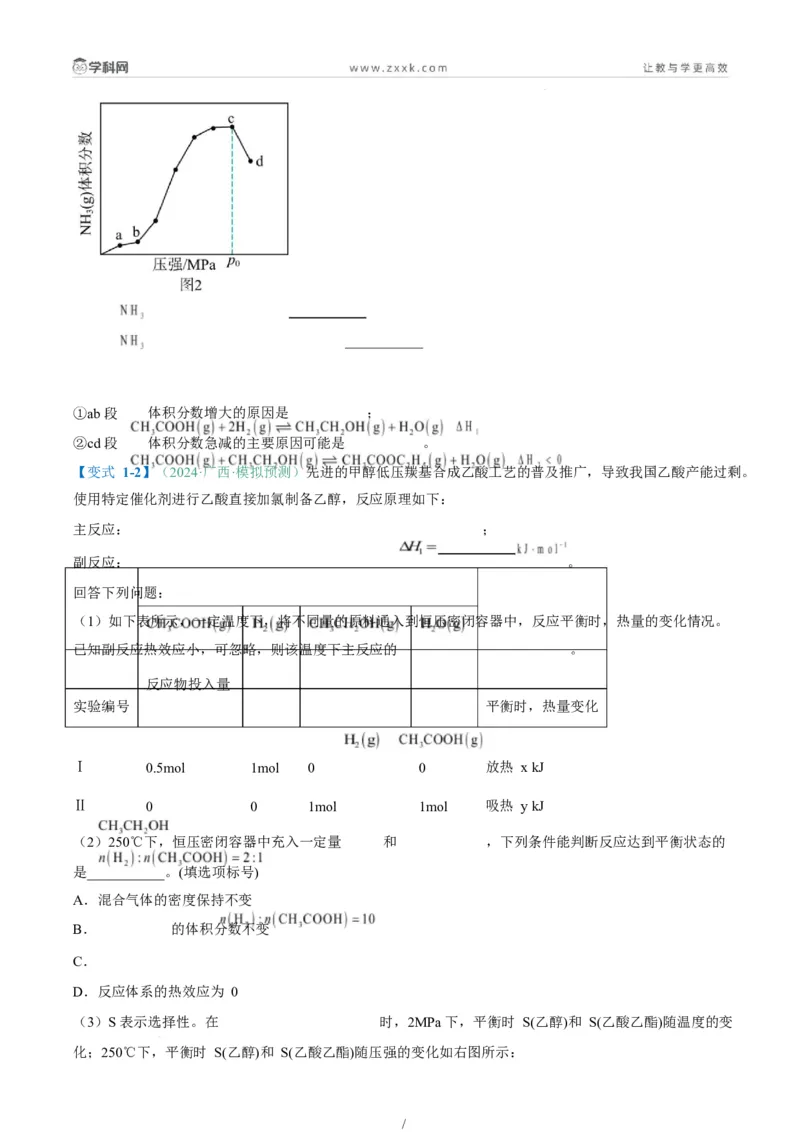
(5)一定温度下,向体积可变的密闭容器中充入 和 ,合成 ,测得 体积分数与压强
关系如图 2 所示。
/①ab 段 体积分数增大的原因是 ;
②cd 段 体积分数急减的主要原因可能是 。
【变式 1-2】(2024·广西·模拟预测)先进的甲醇低压羰基合成乙酸工艺的普及推广,导致我国乙酸产能过剩。
使用特定催化剂进行乙酸直接加氯制备乙醇,反应原理如下:
主反应: ;
副反应: 。
回答下列问题:
(1)如下表所示,一定温度下,将不同量的原料通入到恒压密闭容器中,反应平衡时,热量的变化情况。
已知副反应热效应小,可忽略,则该温度下主反应的 。
反应物投入量
实验编号 平衡时,热量变化
Ⅰ 0.5mol 1mol 0 0 放热 x kJ
Ⅱ 0 0 1mol 1mol 吸热 y kJ
(2)250℃下,恒压密闭容器中充入一定量 和 ,下列条件能判断反应达到平衡状态的
是___________。(填选项标号)
A.混合气体的密度保持不变
B. 的体积分数不变
C.
D.反应体系的热效应为 0
(3)S 表示选择性。在 时,2MPa 下,平衡时 S(乙醇)和 S(乙酸乙酯)随温度的变
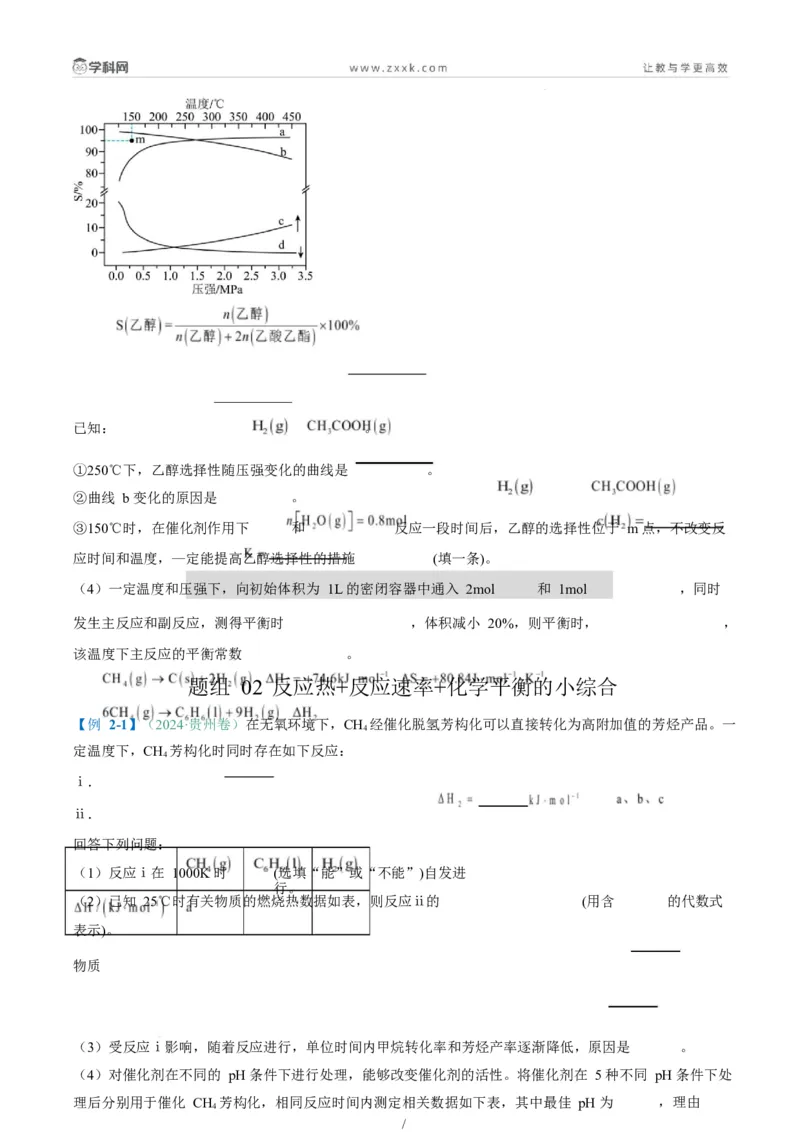
化;250℃下,平衡时 S(乙醇)和 S(乙酸乙酯)随压强的变化如右图所示:
/已知: 。
①250℃下,乙醇选择性随压强变化的曲线是 。
②曲线 b 变化的原因是 。
③150℃时,在催化剂作用下 和 反应一段时间后,乙醇的选择性位于 m 点,不改变反
应时间和温度,—定能提高乙醇选择性的措施 (填一条)。
(4)一定温度和压强下,向初始体积为 1L 的密闭容器中通入 2mol 和 1mol ,同时
发生主反应和副反应,测得平衡时 ,体积减小 20%,则平衡时, ,
该温度下主反应的平衡常数 。
题组 02 反应热+反应速率+化学平衡的小综合
【例 2-1】(2024·贵州卷)在无氧环境下,CH 经催化脱氢芳构化可以直接转化为高附加值的芳烃产品。一
4
定温度下,CH 芳构化时同时存在如下反应:
4
ⅰ.
ⅱ.
回答下列问题:
(1)反应ⅰ在 1000K 时 (选填“能”或“不能”)自发进
行。
(2)已知 25℃时有关物质的燃烧热数据如表,则反应ⅱ的 (用含 的代数式
表示)。
物质
(3)受反应ⅰ影响,随着反应进行,单位时间内甲烷转化率和芳烃产率逐渐降低,原因是 。
(4)对催化剂在不同的 pH 条件下进行处理,能够改变催化剂的活性。将催化剂在 5 种不同 pH 条件下处
理后分别用于催化 CH 芳构化,相同反应时间内测定相关数据如下表,其中最佳 pH 为 ,理由
4
/是 。
pH CH 平均转化率/% 芳烃平均产率/% 产物中积碳平均含量/%
4
2.4 9.60 5.35 40.75
4.0 9.80 4.60 45.85
7.0 9.25 4.05 46.80
10.0 10.45 6.45 33.10
12.0 9.95 4.10 49.45
(5) 下,在某密闭容器中按 充入气体,发生反应
,平衡时 与 的分压比为 4:1,则 的平衡转化率
为 ,平衡常数 K= (用平衡分压代替平衡浓度计算,分压 总压 物质的量分数,列出计算式
p
即可)。
(6)引入丙烷可促进甲烷芳构化制备苯和二甲苯,反应如下:
(两个反应可视为同级数的平行反应)
对于同级数的平行反应有 ,其中 v、k 分别为反应速率和反应速率常数,E 为反应活
a
化能,A 、A 为定值,R 为常数,T 为温度,同一温度下 是定值。已知 ,若要提高苯的产
1 2
率,可采取的措施有 。
【例 2-2】(2024·湖南卷)丙烯腈( )是一种重要的化工原料。工业上以 为载气,用 作催
化剂生产 的流程如下:
已知:①进料混合气进入两釜的流量恒定,两釜中反应温度恒定:
②反应釜Ⅰ中发生的反应:
ⅰ:
③反应釜Ⅱ中发生的反应:
ⅱ:
ⅲ:
/④在此生产条件下,酯类物质可能发生水解。
回答下列问题:
(1)总反应
(用含 、 、和 的代数式表示);
(2)进料混合气中 ,出料中四种物质( 、
、 、 )的流量,(单位时间内出料口流出的物质的量)随时间变化关系如图:
①表示 的曲线是 (填“a”“b”或“c”);
②反应釜Ⅰ中加入 的作用是 。
③出料中没有检测到 的原因是 。
④反应 后,a、b、c 曲线对应物质的流量逐渐降低的原因是 。
(3)催化剂 再生时会释放 ,可用氨水吸收获得 。现将一定量的 固体(含
水)置于密闭真空容器中,充入 和 ,其中 的分压为 ,在 ℃下进行干燥。为保证
不分解, 的分压应不低于 (已知 ,
分解的平衡常数 );
(4)以 为原料,稀硫酸为电解液,Sn 作阴极,用电解的方法可制得 ,其阴
极反应式 。
【提分秘籍】
一、三种平衡常数的计算
a A(g)+b B(g) c C(g)+d D(g)
1.浓度平衡常数:K=
c
①平衡量必须为平衡时的浓度
/②等体积反应:可以用平衡时的物质的量代替平衡时的浓度
③恒压条件下:先计算平衡体积,再算平衡常数
2.压强平衡常数:K =
p
①平衡量为平衡时的浓度、物质的量、体积等均可
②分压 P=P ×x=P × =(P +P +P +…)×
i 总 i 总
1 2 3
③恒容条件下:先计算平衡总压,再算平衡常数或直接根据分压计算
3.物质的量分数平衡常数:K=
x
①平衡量为平衡时的浓度、物质的量、体积等均可
②物质的量分数:x=
i
二、多重平衡体系化学平衡常数的计算
1.多重平衡是指相互关联的若干平衡同时存在于一个平衡系统中,且至少有一种物质同时参与几个相互关联
的平衡。
多重平衡涉及的反应多,看似杂乱,但各个平衡之间存在内在联系,要么连续,要么竞争,这样可将
三个平衡简化为两个平衡,从而快速解答。也可以从元素守恒入手,只要抓住起始状态与平衡状态即可,
可以忽略复杂的反应过程,从而使复杂问题简单化。
2.同一容器内的多平衡体系,相同组分的平衡浓度相同
①化学平衡:a A(g) b B(g)+c C(g),c C(g) d D(g)+e E(g)
②特点:计算 K 、K 时,用到的 c(C)相同
1 2
3.计算方法
(1)元素守恒法:根据某元素守恒,计算出平衡时相应组分的浓度
(2)设未知数法
①有几个平衡假设几个未知数(变化量)
②用这些未知数表示出平衡时相应组分的浓度
③根据相关等量计算出未知数,带入平衡常数表达式求解
【变式演练】
【变式 2-1】(2024·山西晋中·二模)煤的气化与液化是实现煤清洁利用的基本途径; 的资源化利用有利
于碳中和目标的实现。回答下列问题:
(1)煤制备乙烯的途径之一如下:
;
/;
。
已知:① ;
② 。
则 ,反应 的自发性与温度的关系是 。
(2) 催化加氢可得到甲烷: ,从速率与
平衡移动两方面考虑,反应温度不宜过低或过高,理由是 。
(3)向某密闭容器中充入一定量的 和 ,在 条件下发生反应:
。当充入量 时 的平衡转化率~ 的关系与 时 的平衡
转化率~ 的关系如图所示:
①表示 时 平衡转化率~ 的关系是 (填“Ⅰ”或
“Ⅱ”)。
②当充入量 、温度为 时,反应开始后经过 达到平衡状态,若最初充人 ,则
内 ;实际生产中从反应炉出来的气体中
的转化率总是低于图中表示的相应值,最可能的原因是 。
③下列事实不能说明在一定温度下该反应已经达到平衡状态的是 (填选项字母)。
A.容器中气体总体积保持不变
B.混合气体的平均相对分子质量保持不变
C.相同时间内 键与 键断裂的数目相等
D. 与 比值保持不变
/【变式 2-2】(2024·山东济南·一模)天然气、石油钻探过程会释放出 CO 、H S 等气体。某种将 CO 和 H
2 2 2 2
S
共活化的工艺涉及如下反应:
①
②
③
④
回答下列问题:
(1)已知:298K 时,18g 气态水转化为液态水释放出 44kJ 的能量;HS(g)的标准摩尔燃烧焓(△H)为-586kJ·
2
mol-1,则 COS(g)的标准摩尔燃烧焓( )为 kJ·mol-1,反应②在 (填“高温”“低
温”
或“任意温度”)下能自发进行。
(2)一定条件下,向起始压强为 200kPa 的恒容密闭容器中通入等物质的量的 CO (g)和 H S(g)混合气体,
2 2
发生上述反应,25min 时,测得体系总压强为 210kPa,S(g)的平均反应速率为 kPa·min-1.达到平
2
衡时,测得体系总压强为 230kPa, ,此时 HS(g)的平衡转化率为 ,
2
反应②的标准平衡常数 (已知:分压=总压×该组分物质的量分数,对于反应
, ,其中 , 、 、 、 为各组分
的平衡分压)。
(3)将等物质的量的 CO (g)和 H S(g)混合气体充入恒压密闭容器中,发生上述反应,反应物的平衡转化率、
2 2
COS 或 HO 的选择性与温度关系如图所示。COS 的选择性 ,HO 的选择性
2 2
。
/①表示“COS 的选择性”的曲线是 (填“曲线 a”或“曲线
b”);
②温度低于 500℃时,H S 的转化率与 CO 的相等,原因是 。
2 2
题组 03 反应热+反应机理+反应速率+化学平衡大综合
【例 3-1】(2023·河北卷)氮是自然界重要元素之一,研究氮及其化合物的性质以及氮的循环利用对解决环
境和能源问题都具有重要意义。
已知: 物质中的化学键断裂时所需能量如下表。
物质
能量/ 945 498 631
回答下列问题:
(1)恒温下,将 空气( 和 的体积分数分别为 0.78 和 0.21,其余为惰性组分)置于容积为 的恒
容密闭容器中,假设体系中只存在如下两个反应:
i
ii
① 。
②以下操作可以降低上述平衡体系中 浓度的有 (填标号)。
A.缩小体积 B.升高温度 C.移除 D.降低 浓度
③若上述平衡体系中 ,则 (写出含
a、b、V 的计算式)。
(2)氢气催化还原 作为一种高效环保的脱硝技术备受关注。高温下氢气还原 反应的速率方程为
为速率常数。在一定温度下改变体系中各物质浓度,测定结果如下表。
/组号
1 0.10 0.10 r
2 0.10 0.20
3 0.20 0.10
4 0.05 0.30 ?
表中第 4 组的反应速率为 。(写出含 r 的表达式)
(3)①以空气中的氮气为原料电解合成氨时, 在 (填“阴”或“阳”)极上发生反应, 。
产生
②氨燃料电池和氢燃料电池产生相同电量时,理论上消耗 和 的质量比为 ,则在碱性介质中氨燃
料电池负极的电极反应式为 。
③我国科学家研究了水溶液中三种催化剂(a、b、c)上 电还原为 (图 1)和 电还原为 (图 2)反应
历程中的能量变化,则三种催化剂对 电还原为 的催化活性由强到弱的顺序为 (用字母 a、b、
c 排序)。
【例 3-2】(2023·湖北卷)纳米碗 是一种奇特的碗状共轭体系。高温条件下, 可以由 分
子经过连续 5 步氢抽提和闭环脱氢反应生成。 的反应机理和能量变化如
下:
/回答下列问题:
(1)已知 中的碳氢键和碳碳键的键能分别为 和 ,H-H 键能为
。估算 的 。
(2)图示历程包含 个基元反应,其中速率最慢的是第 个。
(3) 纳米碗中五元环和六元环结构的数目分别为 、 。
(4)1200K 时,假定体系内只有反应 发生,反应过程中压强恒定为 (即
的初始压强),平衡转化率为α,该反应的平衡常数 为 (用平衡分压代替平衡浓度计算,分
压=总压×物质的量分数)。
(5) 及 反应的 ( 为平衡常数)随温度倒
数的关系如图所示。已知本实验条件下, (R 为理想气体常数,c 为截距)。图中两条线几乎平行,
从结构的角度分析其原因是 。
(6)下列措施既能提高反应物的平衡转化率,又能增大生成 的反应速率的是 (填标号)。
a.升高温度 b.增大压强 c.加入催化剂
【提分秘籍】
一、能量图像的分析方法
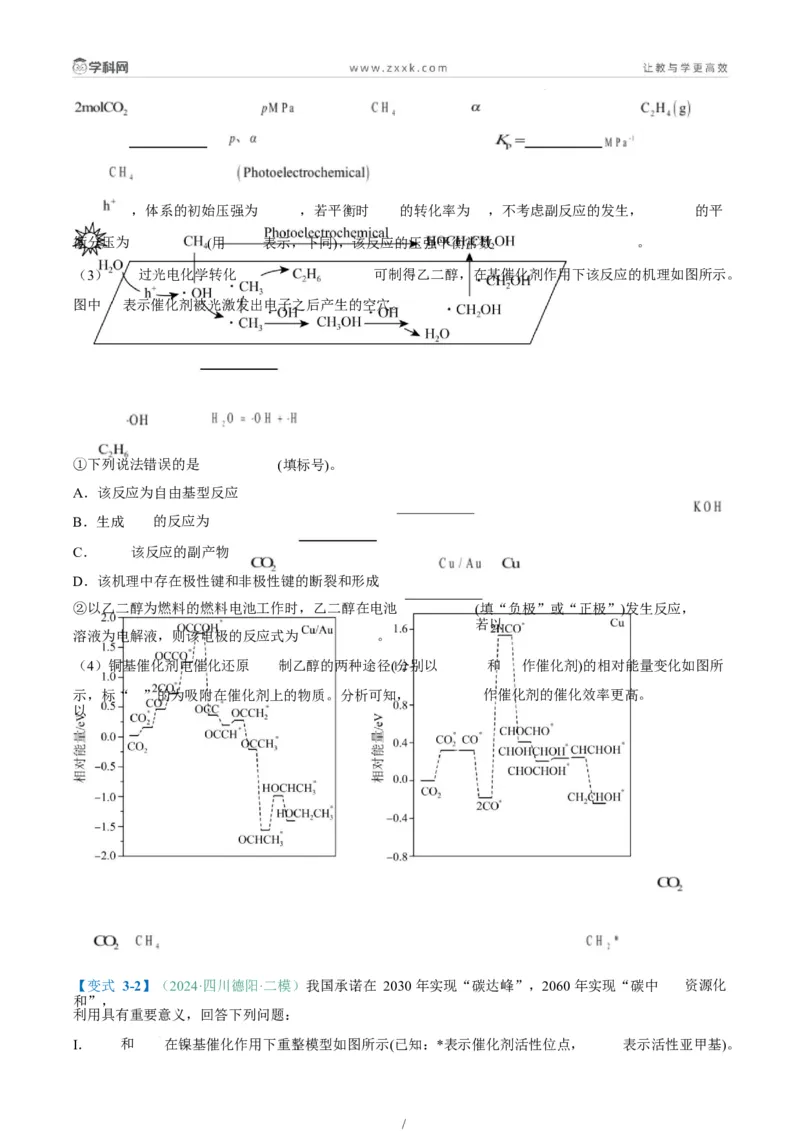
/二、“环式”反应催化机理的分析
“环式”反应过程图如下:
“入环”的物质为反应物,如图中的①④;位于“环上”的物质为催化剂或中间体,如图中的⑤⑥⑦⑧;
“出
环”的物质为生成物,如图中的②③;由反应物和生成物可快速得出总反应方程式。
1.明确反应物:最重要的要看清图示中的箭头,明确哪些物质进行循环体系,哪些物质离子循环体系,进行
循环体系的物质为总反应的反应物,离子循环体系的物质为总反应的生成物。
2.明确催化剂和中间产物:从循环图示中找出分解的若干反应,通过分步反应区分哪些是催化剂,哪些是中
间产物。
3.写出总反应:依据质量守恒定律,确定循环 图示中没标出的物质,利用氧化还原反应的配平方法进行配
平,写出总反应,同时标出催化剂和反应条件。
三、 “直线式”催化剂表面“吸附”“脱附”机
理分析
1.过程分析
/上述是合成氨的催化反应机理的一般过程(简化的过程):
①反应物扩散到催化剂表面;
②反应物被吸附在催化剂表面;
③被吸附的反应物发生化学反应生成产物;
④产物的解吸。
2.过程中能量变化分析
催化剂的催化过程是一个能量变化的过程,其中有能量升高(称为吸热)、也有能量降低(称为放热)。
吸热的过程就是“爬坡”的过程,就是能垒,最大能垒就是活化能。能垒是指必须要克服的能量障碍,才能
达到化学反应的转化状态。催化剂吸附一般是吸热的,而催化剂脱附是表征催化剂反应过程中,催化剂表
面上被吸附物质释放出去的反应步骤之一。脱附并非是必须要克服的能量障碍,因此,催化剂脱附不能算
作是能垒。但是,在实际的催化剂反应中,由于催化剂的活性中心部分与反应物之间的相互作用强度较大,
因此,在某些情况下,催化剂脱附所需要的能量也是催化反应中的一种能垒之一。
例如:我国科学家结合实验与计算机模拟结果,研究了在铁掺杂 W18049 纳米反应器催化剂表面上实
现常温低电位合成氨,获得较高的氮产量和法拉第效率。反应历程如图所示,其中吸附在催化剂表面的物
种用*标注。
需要吸收能量最大的能量(活化能)E= ev,该步骤的化学方程式为 。若通入 体积分数过大
时导致催化剂效率降低的原因是 。
【答案】1.54 NH *+NH =2NH H 占据催化剂活性中心过多或 H 体积分数过大时,催化剂吸附了较多的
3 3 3 2 2
H ,阻碍了 N 与催化剂的接触,导致催化剂催化效率降低。
2 2
【解析】根据图示,吸收能量最大能垒,即相对能量的差最大为-1.02-(-2.56)=1.54;根据图示,该步反应的
方程式为 NH *+NH =2NH ;若通入 H 的体积分数过大,H 占据催化剂活性中心过多或 H 体积分数过大时,
3 3 3 2 2 2
/催化剂吸附了较多的 H ,阻碍了 N 与催化剂的接触,导致催化剂催化效率降低;
2 2
也就是说,脱附就看是吸热还是放热,吸热的话考虑能垒问题。
四、能垒与决速步骤的关系
能垒:简单可以理解为从左往右进行中,向上爬坡最高的为能垒,而包含此能垒的反应我们称之为决
速步骤,也称为慢反应。例如下图中,从第一个中间态到过渡态 2 的能量就是能垒,而 HCOO
*+H*=CO +2H*是在 Rh 做催化剂时该历程的决速步骤 。
2
【特别提醒】①最大能垒是指反应历程各步变化中起始相对能量和过渡态相对能量的最大差值。
②能垒越大,反应速率越小,即多步反应中能垒最大的反应为决速反应。
③用不同催化剂催化化学反应,催化剂使能垒降低幅度越大,说明催化效果越好。
④相同反应物同时发生多个竞争反应,其中能垒越小的反应,反应速率越大,产物占比越高。
⑤书写总反应化学方程式只看始态和终态的物质,并删去二者中相同的物质,不考虑各步骤中的“中间物质”。
⑥若吸附在催化剂表面的物种用“*”标注,则物种“吸附”放热,而“脱附”吸热。
【变式演练】
【变式 3-1】(2024·河北沧州·二模)二氧化碳和甲烷是两种温室效应气体,将二者进行转化,可得到具有高
附加值的化学品或清洁燃料。
(1) 和 催化重整制取 和
主反应:①
副反应:②
③
④
主反应的 ,该反应在 (填“较高温度”或“较低温度”)下可自发进
行。
(2) 和 反应可制取乙烯,反应的化学方程式为
。一定温度下,向某恒容密闭容器中充入 和
/,体系的初始压强为 ,若平衡时 的转化率为 ,不考虑副反应的发生, 的平
衡分压为 (用 表示,下同),该反应的压强平衡常数 。
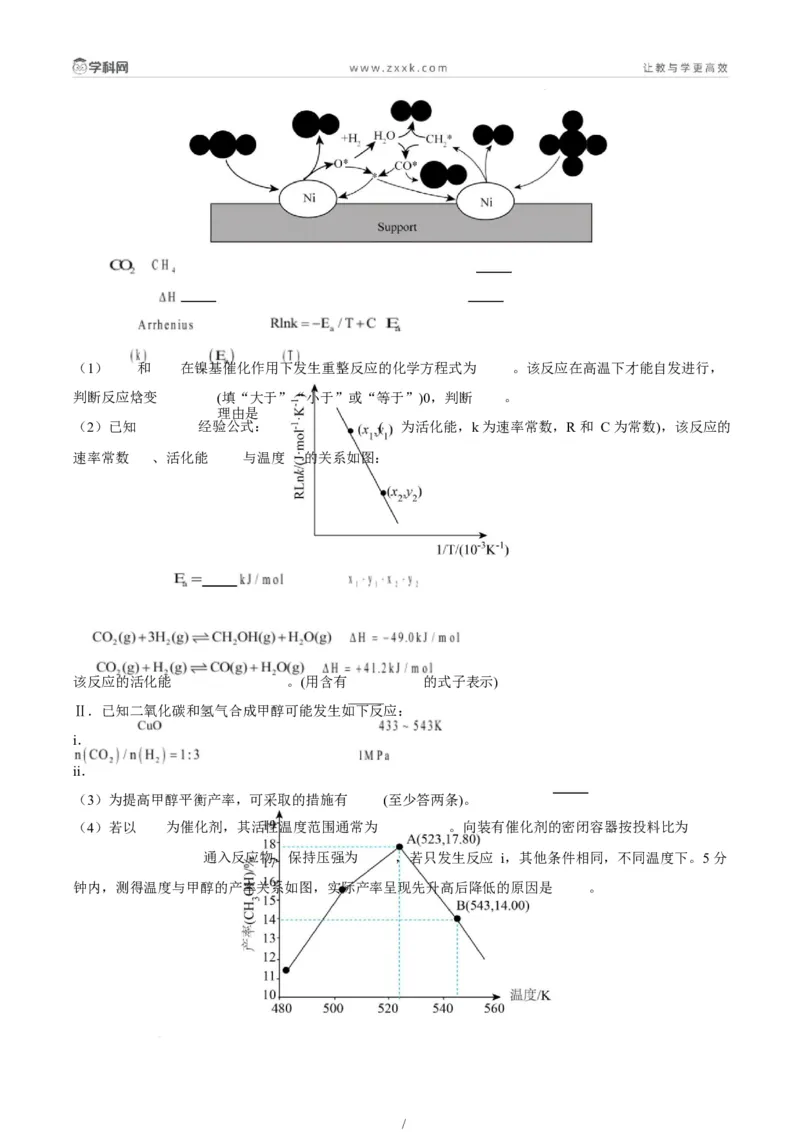
(3) 过光电化学转化 可制得乙二醇,在某催化剂作用下该反应的机理如图所示。
图中 表示催化剂被光激发出电子之后产生的空穴。
①下列说法错误的是 (填标号)。
A.该反应为自由基型反应
B.生成 的反应为
C. 该反应的副产物
D.该机理中存在极性键和非极性键的断裂和形成
②以乙二醇为燃料的燃料电池工作时,乙二醇在电池 (填“负极”或“正极”)发生反应,
若以
溶液为电解液,则该电极的反应式为 。
(4)铜基催化剂电催化还原 制乙醇的两种途径(分别以 和 作催化剂)的相对能量变化如图所
示,标“ ”的为吸附在催化剂上的物质。分析可知, 作催化剂的催化效率更高。
以
【变式 3-2】(2024·四川德阳·二模)我国承诺在 2030 年实现“碳达峰”,2060 年实现“碳中 资源化
和”,
利用具有重要意义,回答下列问题:
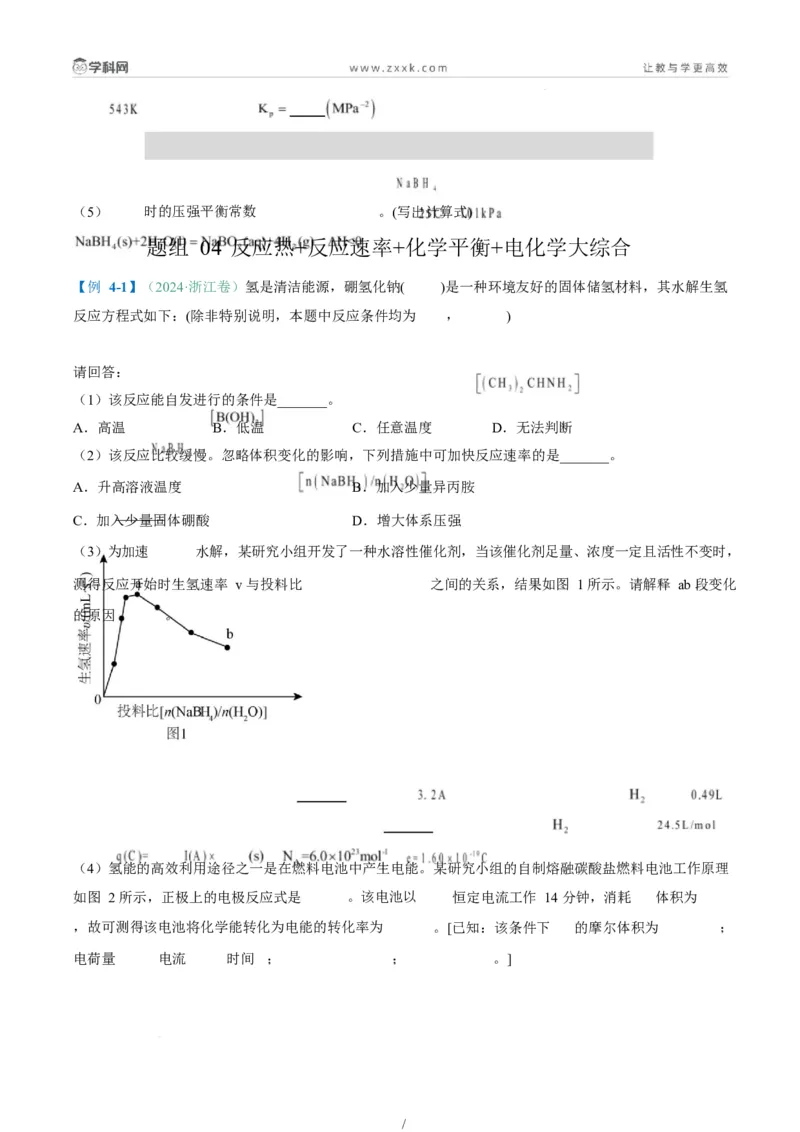
I. 和 在镍基催化作用下重整模型如图所示(已知:*表示催化剂活性位点, 表示活性亚甲基)。
/(1) 和 在镍基催化作用下发生重整反应的化学方程式为 。该反应在高温下才能自发进行,
判断反应焓变 (填“大于”“小于”或“等于”)0,判断 。
理由是
(2)已知 经验公式: ( 为活化能,k 为速率常数,R 和 C 为常数),该反应的
速率常数 、活化能 与温度 的关系如图:
该反应的活化能 。(用含有 的式子表示)
Ⅱ.已知二氧化碳和氢气合成甲醇可能发生如下反应:
i.
ii.
(3)为提高甲醇平衡产率,可采取的措施有 (至少答两条)。
(4)若以 为催化剂,其活性温度范围通常为 。向装有催化剂的密闭容器按投料比为
通入反应物,保持压强为 ,若只发生反应 i,其他条件相同,不同温度下。5 分
钟内,测得温度与甲醇的产率关系如图,实际产率呈现先升高后降低的原因是 。
/(5) 时的压强平衡常数 。(写出计算式)
题组 04 反应热+反应速率+化学平衡+电化学大综合
【例 4-1】(2024·浙江卷)氢是清洁能源,硼氢化钠( )是一种环境友好的固体储氢材料,其水解生氢
反应方程式如下:(除非特别说明,本题中反应条件均为 , )
请回答:
(1)该反应能自发进行的条件是_______。
A.高温 B.低温 C.任意温度 D.无法判断
(2)该反应比较缓慢。忽略体积变化的影响,下列措施中可加快反应速率的是_______。
A.升高溶液温度 B.加入少量异丙胺
C.加入少量固体硼酸 D.增大体系压强
(3)为加速 水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,
测得反应开始时生氢速率 v 与投料比 之间的关系,结果如图 1 所示。请解释 ab 段变化
的原因 。
(4)氢能的高效利用途径之一是在燃料电池中产生电能。某研究小组的自制熔融碳酸盐燃料电池工作原理
如图 2 所示,正极上的电极反应式是 。该电池以 恒定电流工作 14 分钟,消耗 体积为
,故可测得该电池将化学能转化为电能的转化率为 。[已知:该条件下 的摩尔体积为 ;
电荷量 电流 时间 ; ; 。]
/(5)资源的再利用和再循环有利于人类的可持续发展。选用如下方程式,可以设计能自发进行的多种制备
方法,将反应副产物偏硼酸钠( )再生为 。(已知: 是反应的自由能变化量,其计算方法也
遵循盖斯定律,可类比 计算方法;当 时,反应能自发进行。)
I.
II.
III.
请书写一个方程式表示 再生为 的一种制备方法,并注明 。(要求:反应物不超过
三种物质;氢原子利用率为 。)
【例 4-2】(2024·浙江卷)通过电化学、热化学等方法,将 转化为 等化学品,是实现“双碳”目
标的途径之一。请回答:
(1)某研究小组采用电化学方法将 转化为 ,装置如图。电极 B 上的电极反应式是 。
(2)该研究小组改用热化学方法,相关热化学方程式如下:
:
Ⅱ:
Ⅲ:
① 。
②反应Ⅲ在恒温、恒容的密闭容器中进行, 和 的投料浓度均为 ,平衡常数 ,
/则 的平衡转化率为 。
③用氨水吸收 ,得到 氨水和 甲酸铵的混合溶液, 时该混合溶液的
。[已知: 时,电离常数 、 ]
(3)为提高效率,该研究小组参考文献优化热化学方法,在如图密闭装置中充分搅拌催化剂 M 的 (有
机溶剂)溶液, 和 在溶液中反应制备 ,反应过程中保持 和 的压强不变,总反应
的反应速率为 v,反应机理如下列三个基元反应,各反应的活化能 (不考
虑催化剂活性降低或丧失)。
Ⅳ:
V:
VI:
①催化剂 M 足量条件下,下列说法正确的是 。
A.v 与 的压强无关 B.v 与溶液中溶解 的浓度无关
C.温度升高,v 不一定增大 D.在溶液中加入 ,可提高 转化率
②实验测得: , 下,v 随催化剂 M 浓度 c 变化如图。 时,v 随 c 增大而
增大: 时,v 不再显著增大。请解释原因 。
【提分秘籍】
一、燃料电池电极反应式的书写
第一步:写出电池总反应式。
燃料电池的总反应与燃料燃烧的反应一致,若产物能和电解质反应,则总反应为加合后的反应。如甲烷燃
料电池(电解质溶液为 NaOH 溶液)的反应如下:
/CH +2O ===CO +2H O①
4 2 2 2
CO +2NaOH===Na CO +H O②
2 2 3 2
①+②可得甲烷燃料电池的总反应式:CH +2O +2NaOH===Na CO +3H O。
4 2 2 3 2
第二步:写出电池的正极反应式。
根据燃料电池的特点,一般在正极上发生还原反应的物质都是 O,因电解质溶液不同,故其电极反应也会
2
有所不同:
燃料电池电解质 正极反应式
酸性电解质 O +4H++4e-===2H O
2
2
碱性电解质 O +2H O+4e-===4OH-
2 2
固体电解质(高温下能传导 O2-) O+4e-===2O2-
2
熔融碳酸盐(如熔融 K CO ) O +2CO +4e-===2CO2-3
2 3 2 2
第三步:电池的总反应式-电池的正极反应式=电池的负极反应式。
二、电解池电极反应式的书写步骤
微提醒:通常电极反应可以根据阳极材料和电解质溶液的性质进行判断,但在高考题中往往需要结合题给
信息进行判断。
三、有关离子交换膜的类型及其应用
(1)阳离子交换膜(只允许阳离子和水分子通过,阻止阴离子和气体通过)
以锌铜原电池为例,中间用阳离子交换膜隔开
①负极反应式:Zn-2e-=Zn2+
②正极反应式:Cu2++2e-=Cu
③Zn2+通过阳离子交换膜进入正极区
④阳离子→透过阳离子交换膜→原电池正极(或电解池的阴极)
(2)阴离子交换膜(只允许阴离子和水分子通过,阻止阳离子和气体通过)
/以 Pt 为电极电解淀粉KI 溶液,中间用阴离子交换膜隔开
①阴极反应式:2H O+2e=H ↑+2OH
2 2
②阳极反应式:2I_2e=I
2
③阴极产生的 OH移向阳极与阳极产物反应:3I +6OH=IO +5I
2 3
+3HO
2
④阴离子→透过阴离子交换膜→电解池阳极(或原电池的负极)
(3)质子交换膜(只允许 H+和水分子通过)
在微生物作用下电解有机废水(含 CHCOOH),可获得清洁能源 H
3 2
①阴极反应式:2H++2e=H ↑
2
②阳极反应式:CH COOH8e+2H O=2CO ↑+8H+
3 2 2
③阳极产生的 H+通过质子交换膜移向阴极
④H+→透过质子交换膜→原电池正极(或电解池的阴极)
(4)双极膜
双极膜
由一张阳膜和一张阴膜复合制成。该
膜特点是在直流电的作用下,阴、阳
膜复合层间的 HO 解离成 H+和 OH
2
-并通过阳膜和阴膜分别向两极区移
动,作为 H+和 OH-的离子源
【变式演练】
【变式 4-1】(2024·河南·三模)几种物质的燃烧热如下表所示。
可燃物
燃烧热
回答下列问题:
(1)写出表示 燃烧热的热化学方程式: 。
(2) 。
(3)某水煤气含 、 、 和 ,其中 、 体积分数分别为 、 。标准状况下, 这
种水煤气完全燃烧生成液态水和二氧化碳时放出的热量为 。该水煤气中 、 的物质的量分别
为 、 。
(4)在如图 1 坐标系中补全 燃烧反应的能量变化图 。
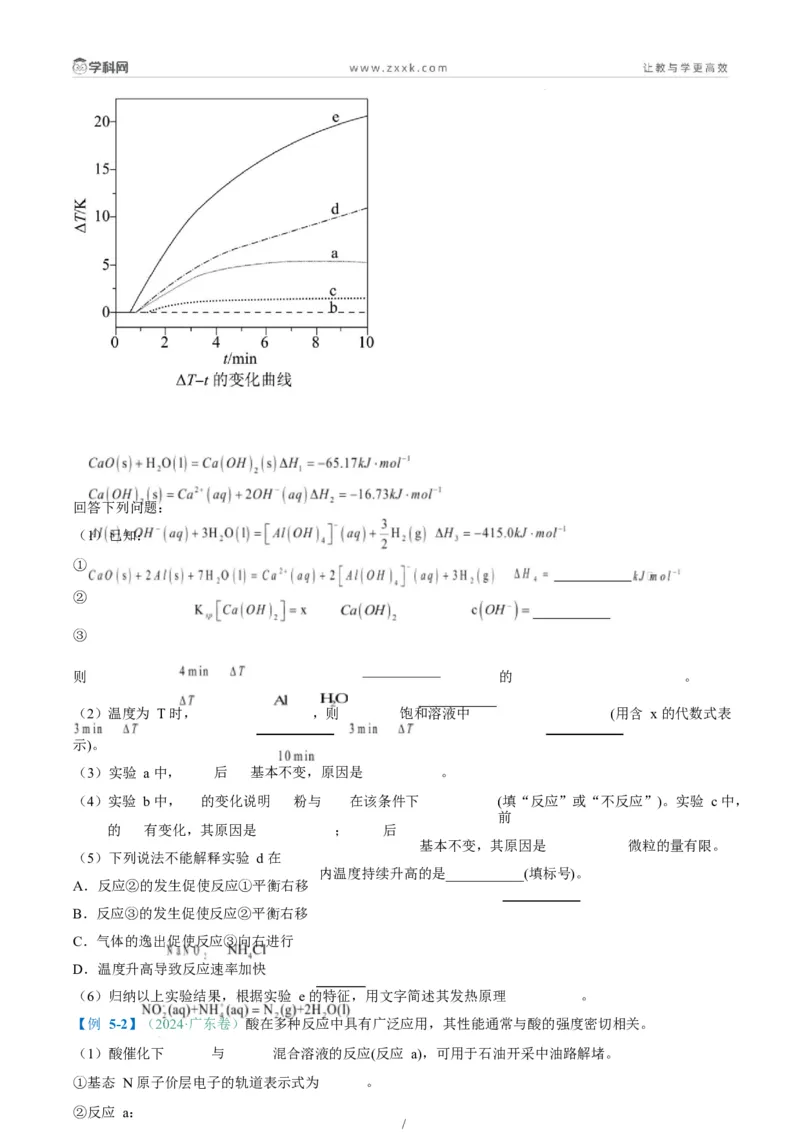
/(5)已知: 催化氢化制 的反应历程及能量变化如图 2 所示。
①控速反应式为 。
②下列叙述正确的是 (填字母)。
A.升高温度,总反应平衡常数变大
B.正反应在任何温度下都能自发
C.总反应分六个基元反应
(6)工业上用甲醇燃料电池采用电解法处理含 和 的碱性废水,将 转化为 、 ,其工作原
理如图 3、图 4 所示。
/① 极电极反应式为 。
② 转化为 、 的离子方程式为 。
【变式 4-2】(2025·四川·一模)乙醛、乙醇都是常见的有机物,在生产、生活中都有广泛的用途。请回答下
列问题:
(1)在 25℃,101kPa 下,取一定量的无水乙醇完全燃烧,放出的热量为 QkJ,燃烧产生的 通入过量
饱和石灰水中,生成了 。则表示乙醇燃烧热的热化学方程式为 。
(2)已知: 的速率方程 (k 为速率常数,只与温度、
催化剂有关;n 为反应级数)。为了测定反应级数(n),实验测得 在一系
列不同浓度时的初始反应速率数据如下:
0.1 0.2 0.3 0.4
0.02 0.08 0.18 0.32
则该总反应为 ,级反应;速率常数
(3)一定温度下,保持总压强为 100kPa,向反应器充入 和 的混合气体( 不参与反应)发生
反应 ,测得 平衡转化率与起始投料比
的关系如图所示。
①由图可知: 的平衡转化率随着投料比增大而减小,其原因是 。
②该温度下,上述反应在 A 点的平衡常数 kPa( 为用分压计算的平衡常数,分压=总压×物质
的量分数)。
(4)用乙醇电催化氧化制备乙醛的原理如下图所示。
/①电解过程中电极室 A 中溶液的 pH (填“增大”、“减小”或“不
变”)。
②电极 A 的电极反应式为 。
③当生成 时,理论上 A、B 两室溶液质量变化之和为 g。
题组 05 反应热+反应速率+化学平衡+电解质溶液大综合
【例 5-1】(2022·湖北卷)自发热材料在生活中的应用日益广泛。某实验小组为探究“ ”体系
的发热原理,在隔热装置中进行了下表中的五组实验,测得相应实验体系的温度升高值( )随时间(t)的变
化曲线,如图所示。
实验编号 反应物组成
粉末
a
粉
b
粉
c
饱和石灰水
粉
d
石灰乳
粉
e 粉末
/回答下列问题:
(1)已知:
①
②
③
则 的 。
(2)温度为 T 时, ,则 饱和溶液中 (用含 x 的代数式表
示)。
(3)实验 a 中, 后 基本不变,原因是 。
(4)实验 b 中, 的变化说明 粉与 在该条件下 (填“反应”或“不反应”)。实验 c 中,
前
的 有变化,其原因是 ; 后
基本不变,其原因是 微粒的量有限。
(5)下列说法不能解释实验 d 在
内温度持续升高的是___________(填标号)。
A.反应②的发生促使反应①平衡右移
B.反应③的发生促使反应②平衡右移
C.气体的逸出促使反应③向右进行
D.温度升高导致反应速率加快
(6)归纳以上实验结果,根据实验 e 的特征,用文字简述其发热原理 。
【例 5-2】(2024·广东卷)酸在多种反应中具有广泛应用,其性能通常与酸的强度密切相关。
(1)酸催化下 与 混合溶液的反应(反应 a),可用于石油开采中油路解堵。
①基态 N 原子价层电子的轨道表示式为 。
②反应 a:
/已知:
则反应 a 的 。
③某小组研究了 3 种酸对反应 a 的催化作用。在相同条件下,向反应体系中滴加等物质的量的少量酸,测
得体系的温度 T 随时间 t 的变化如图。
据图可知,在该过程中 。
A.催化剂酸性增强,可增大反应焓变
B.催化剂酸性增强,有利于提高反应速率
C.催化剂分子中含 H 越多,越有利于加速反应
D.反应速率并不始终随着反应物浓度下降而减小
(2)在非水溶剂中,将 转化为化合物ⅱ(一种重要的电子化学品)的催化机理示意图如图,其中的催化
剂有 和 。
(3)在非水溶剂中研究弱酸的电离平衡具有重要科学价值。一定温度下,某研究组通过分光光度法测定了
两种一元弱酸 (X 为 A 或 B)在某非水溶剂中的 。
a.选择合适的指示剂其钾盐为 , ;其钾盐为 。
b.向 溶液中加入 ,发生反应: 。 起始的物质的量为 ,加入 的物
质的量为 ,平衡时,测得 随 / 的变化曲线如图。已知:该溶剂本身不电离,钾盐在该溶剂中完全电离。
①计算 。(写出计算过程,结果保留两位有效数字)
②在该溶剂中, ; 。(填“>”“<”或“=”)
【提分秘籍】
一、电离常数的计算
(1)特定条件下的 K 或 K 的有关计算
a b
25℃ 时,a mol·L-1 弱酸盐 NaA 溶液与 b mol·L-1 的强酸 HB 溶液等体积混合,溶液呈中性,则 HA 的电离
常数 K 求算三步骤:
a
①电荷守恒:c(Na+)+c(H+)=c(OH-)+c(A-)+c(B-)⇨c(A-)=c(Na+)-c(B-)=a-b2。
②物料守恒:c(HA)+c(A-)=a2 ⇨c(HA)=b2。
③K=c(H+)·c(A-)c(HA)=10-7(a-b)b。
a
(2)根据图像求电离常数的思路(以 HA 为例)
分析图像 ――→寻找 特殊点:c(HA)=c(A-)―→pH 或 c(H+)――→Ka 表达式 Ka=10-pH
=c
(H+)
二、有关溶度积常数的计算
(1)已知溶度积求溶液中的某种离子的浓度,如 K =a 的饱和 AgCl 溶液中 c(Ag+)=c(Cl-)=a mol·L-1。
sp
(2)已知溶度积溶液中某离子的浓度,求溶液中的另一种离子的浓度,如某温度下 AgCl 的 K =a,在 0.1
sp
mol·L-1 的 NaCl 溶液中加入过量的 AgCl 固体,达到平衡后 c(Ag+)=10a mol·L-1。
(3)沉淀开始和沉淀完全时溶液 pH 的计算方法:[以 Cu(OH) 为例]。
2
室温下,向 2 mol·L-1 CuSO 溶液中逐滴加入 NaOH 溶液调节溶液的 pH 至多少时开始沉淀?调节溶液
4
pH 至多少时 Cu2+沉淀完全?
(已知:室温下 K [Cu(OH) ]=2.0×10-20,离子浓度小于 10-5 mol·L-1 时视为 Cu2+沉淀完全)
sp 2
①沉淀开始时 pH 的求算。
K [Cu(OH) ]=c(Cu2+)·c2(OH-)=2×c2(OH-)=2.0×10-20,
sp 2
c(OH-)=10-20=10-10(mol·L-1),
c(H+)=Kwc(OH-)=10-1410-10=10-4(mol·L-1),
/pH=-lgc(H+)=-lg10-4=4。
②沉淀完全时 pH 的求算。
K [Cu(OH) ]=c(Cu2+)·c2(OH-)=10-5·c2(OH-)=2.0×10-20,c(OH-)=2.0×10-15=20×10-8≈4.47×10-8
sp 2
(mol·L-1),c(H+)=Kwc(OH-)=10-144.47×10-8≈2.24×10-7(mol·L-1),pH=-lgc(H+)=-lg(2.24×10-7
)=7-lg2.24≈6.6。
(4)沉淀先后的计算与判断
①沉淀类型相同,则 K 小的化合物先沉淀;
sp
②沉淀类型不同,则需要根据 K 分别计算出沉淀时所需离子浓度,所需离子浓度小的先沉淀。
sp
(5)根据两种含同种离子的化合物的 K 数据,求溶液中不同离子浓度的比值
sp
如某溶液中含有 I-、Cl-等,向其中滴加 AgNO 溶液,当 AgCl 开始沉淀时,求溶液中 c 平(I-)c
3
平(Cl-),则有 c 平(I-)c 平(Cl-)=c 平(Ag+)·c 平(I-)c 平(Ag+)·c 平(Cl-)=Ksp
(AgI)
Ksp(AgCl)。
(6)判断沉淀的生成或转化
把离子浓度数值代入 K 表达式,若数值大于 K ,沉淀可生成或转化为相应难溶物质。
sp sp
【变式演练】
【变式 5-1】(2024·广东清远·一模)硫是人类认识最早的元素之一,含硫物质在化工生产、日常生活中扮演
了重要的角色。
(1)一种可将 无害化处理的工艺涉及反应如下:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
①基态 S 原子的价层电子排布式为 。
②反应 的 。
(2)已知, 与 可发生催化反应,反应机理如图所示。
/①该反应的催化剂是 。
②物质 A 的电子式为 。
(3)向 的 溶液中通入 气体,含硫微粒在不同 溶液中的分布系数 如图所
示:
① 的电离常数 ;常温下, 溶液显 (填“酸”“碱”或
“中”)性。
②25℃时, 的 。工业生产中常联合处理含 的废气和含 的废水,欲发生反应
,计算该反应的平衡常数 (写出计算过程)。
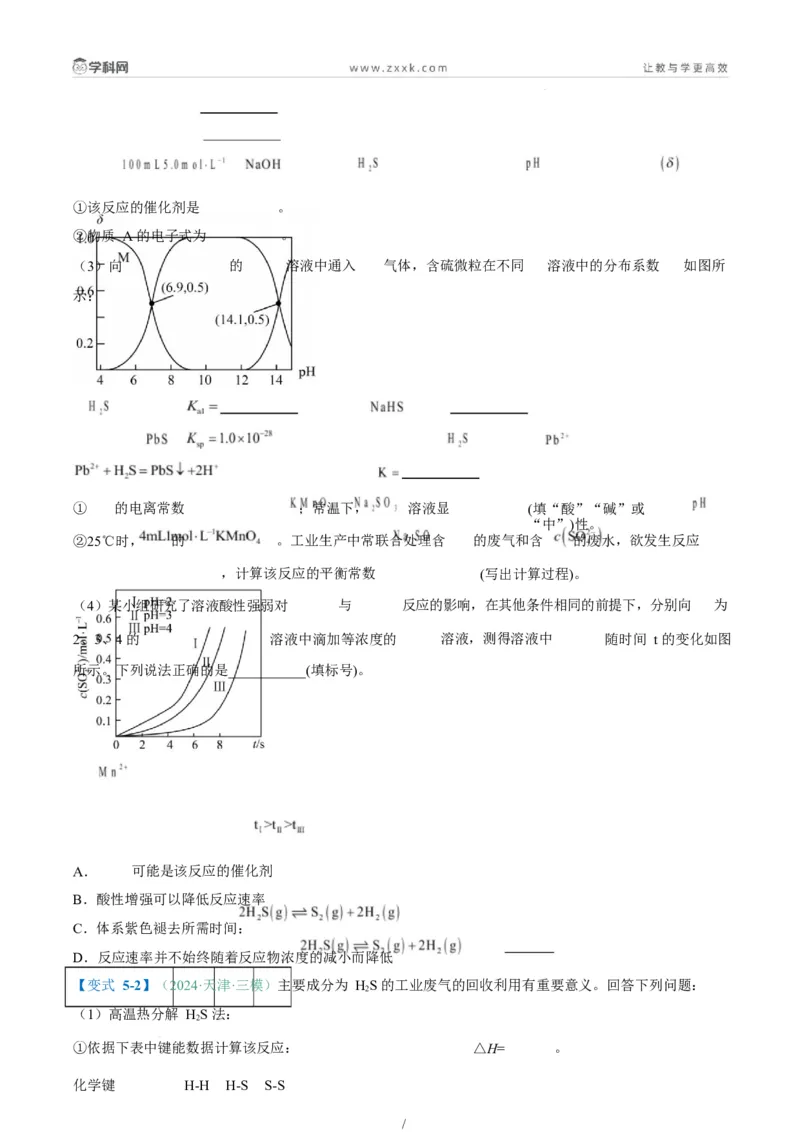
(4)某小组研究了溶液酸性强弱对 与 反应的影响,在其他条件相同的前提下,分别向 为
2、3、4 的 溶液中滴加等浓度的 溶液,测得溶液中 随时间 t 的变化如图
所示。下列说法正确的是___________(填标号)。
A. 可能是该反应的催化剂
B.酸性增强可以降低反应速率
C.体系紫色褪去所需时间:
D.反应速率并不始终随着反应物浓度的减小而降低
【变式 5-2】(2024·天津·三模)主要成分为 HS 的工业废气的回收利用有重要意义。回答下列问题:
2
(1)高温热分解 HS 法:
2
①依据下表中键能数据计算该反应: △H= 。
化学键 H-H H-S S-S
/键能( ) 436 364 414
②某温度下恒容密闭容器中,反应物 HS 转化率达到最大值的依据是 (填字母)。
2
a.气体的压强不发生变化 b.气体的密度不发生变化
c. 不发生变化 d.单位时间里分解的 H S 和生成的 H 的量一样多
2 2
③1470 K、100 kPa 下,将 n(H S):n(Ar)=1:4 的混合气进行 H S 热分解反应。平衡时混合气中 H S 与 H
2 2 2 2
的分压相等,HS 平衡转化率为 ,平衡常数 K = (保留两位有效数字)(K 是以分压代表的平
2 p p
衡常数,分压=总压×物质的量分数)。
(2)常温下,HS 的 、 , 。向含 0.002 mol/L Mn2+废水
2
中通入一定量的 HS,当溶液的 pH=a、c(HS-)=1.0×10-4 mol/L 时,Mn2+开始沉淀,则 a= 。
2
(3)通过电化学循环法可将 H S 转化为 H SO 和 H (如下图左所示)。其中氧化过程发生如下两步反应:
2 2 4 2
H S+H SO =SO +S↓+2H O、S+O =SO 。
2 2 4 2 2 2 2
①电极 上发生反应的电极反应式 。
②理论上 1 mol H S 参加反应可产生 H mol。
2 2
(4)表面喷淋水的活性炭可用于吸附氧化 HS,其原理如上图右所示。其它条件不变时,水膜的酸碱性会
2
影响 H S 的去除率。适当增大活性炭表面的水膜 pH,H S 的氧化去除率增大的原因是 。
2 2
1.(2025·浙江杭州·模拟预测)丙烯是有机化工中的重要原料,可用丙烷直接脱氢工艺和丙烷氧化脱氢工艺
制备。
I.丙烷直接脱氢工艺,以金属 为催化剂,存在以下两个反应:
主反应:
/副反应:
其主反应中有关物质的燃烧热数据如下:
物质
燃烧热 -2219.9 -2058.0 -285.8
回答下列问题:
(1)主反应的 。主反应自发进行的条件是 。
(2)下图为丙烷直接脱氢法中丙烷和丙烯的平衡体积分数与温度、压强的关系(图中的压强分别为
和 )。
① 时,图中表示丙烯的曲线是 (填“i”、“ii”、“iii”或“iv”
)。
② 、500℃时,在密闭容器中进行反应,若只发生上述主反应和副反应,则达平衡时,丙烷的转化
率为 (保留 3 位有效数字)。其他条件不变情况下,以下操作有利于提高平衡时 的操作
有 。
A.恒压通入适量 B.加入适量
C.提高 的表面积 D.加入浸泡了 的硅藻土
II.丙烷氧化脱氢工艺:
(3)在相同温度、压强下进行该工艺,将 、 和 按不同比例投料,控制 浓度不变,改变
。每组实验反应相同时间后, 转化率和 产率如下图所示。已知各组反应均未达平
衡,催化剂活性无明显变化,解释 产率先增后降的原因: 。
/III.工业上可利用丙烯进行电有机合成制备 1,2-丙二醇。
(4)写出以稀硫酸为电解液,丙烯在电极上生成 1,2-丙二醇的电极反应方程式: 。
2.(2024·云南丽江·一模)CO 既是温室气体,也是重要的化工原料,二氧化碳的捕捉和利用是我国能源领
2
域的一个重要战略方向。
(1)用活性炭还原法可以处理汽车尾气中的氮氧化物,某研究小组向 2L 的密闭容器加入一定量的活性炭
和 NO,发生反应 C(s)+2NO(g) N (g)+CO (g) ΔH,在 T ℃时,反应进行到不同时间测得各物质的物质的
2 2 1
量如下:
时间/min 物质的量/mol 0 10 20 30
NO 4.00 2.32 0.80 0.80
N 0 0.84 1.60 1.60
2
CO 0 0.84 1.60 1.60
2
①根据图表数据分析 T ℃时,该反应在 10~20min 内的平均反应速率ν(CO )= 。
1 2
②平衡时测得容器的总压强为 P KPa,则 T ℃时该反应的分压平衡常数 K = (用平衡分压代替平
0 1 p
衡浓度计算,分压=总压×物质的量分数)
③若 30min 后升高温度至 T ℃,达到平衡时,容器中 NO、N 、CO 的浓度之比为 3:5:5,该反应的
2 2 2
ΔH
0(填“>”或“<”)。
④若 30min 后只改变某一条件,NO、N 、CO 的浓度分别变为 0.6mol/L;1.2mol/L;1.2mol/L,则改变的条
2 2
件可能是 (填字母编号)。
A.适当缩小容器的体积 B.通入一定量的 NO
C.加入一定量的活性炭 D.加入合适的催化剂
E.升高温度
(2)向恒容绝热的密闭容器中充入 amolC 与 2amolNO 进行反应 C(s)+2NO(g) N (g)+CO (g),下列能判
2 2
断反应已达化学平衡状态的是 。
①容器中混合气体密度不变②混合气体中 c(N ):c(CO )=1:1 且保持不变
2 2
③v (NO)=v (N )④容器内温度不变⑤容器内压强不变
正 逆 2 /(3)工业上用 CO 和 H 反应合成二甲醚。已知:
2 2
CO (g)+3H (g) CH OH(g)+H O(g) ΔH =-49.1kJ·mol-1
2 2
3 2 1
2CHOH(g) CH OCH (g)+H O(g) ΔH =-24.5kJ·mol-1
3
3 3 2 2
写出 CO (g)和 H (g)转化为 CH OCH (g)和 H O(g)的热化学方程式 。
2 2 3 3 2
(4)二甲醚燃料电池具有能量转化率高、电量大的特点而被广泛应用,某种二甲醚氧气电池(电解质为 KOH
溶液)的负极反应式为 。
3.(2024·甘肃卷) 是制备半导体材料硅的重要原料,可由不同途径制备。
(1)由 制备 :
已知
时,由 制备 硅 (填“吸”或 。升高温度有利
“放”)热
于制备硅的原因是 。
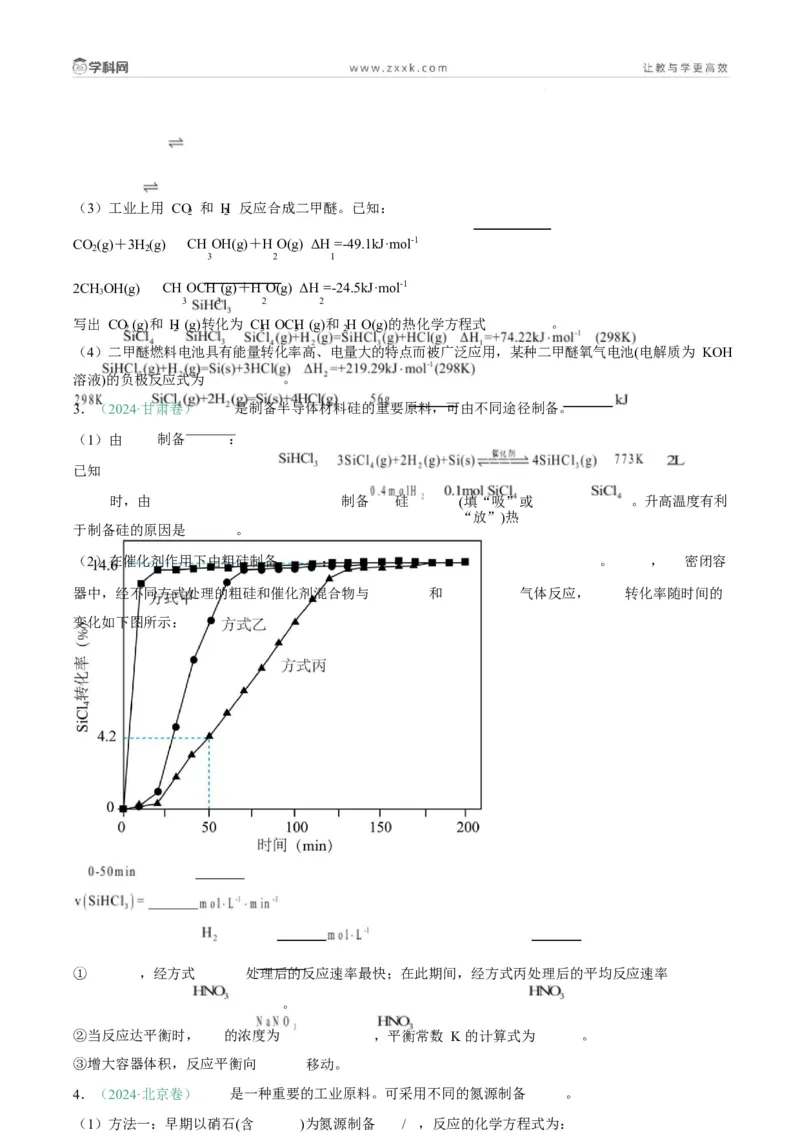
(2)在催化剂作用下由粗硅制备 : 。 , 密闭容
器中,经不同方式处理的粗硅和催化剂混合物与 和 气体反应, 转化率随时间的
变化如下图所示:
① ,经方式 处理后的反应速率最快;在此期间,经方式丙处理后的平均反应速率
。
②当反应达平衡时, 的浓度为 ,平衡常数 K 的计算式为 。
③增大容器体积,反应平衡向 移动。
4.(2024·北京卷) 是一种重要的工业原料。可采用不同的氮源制备 。
(1)方法一:早期以硝石(含 )为氮源制备 / ,反应的化学方程式为:。该反应利用了浓硫酸的性质是酸性和 。
(2)方法二:以 为氮源催化氧化制备 ,反应原理分三步进行。
①第 I 步反应的化学方程式为 。
②针对第Ⅱ步反应进行研究:在容积可变的密闭容器中,充入 和 进行反应。在不同压强
下( 、 ),反应达到平衡时,测得 转化率随温度的变化如图所示。解释 y 点的容器容积小于 x 点的容
器容积的原因 。
(3)方法三:研究表明可以用电解法以 为氮源直接制备 ,其原理示意图如下。
①电极 a 表面生成 的电极反应式: 。
②研究发现: 转化可能的途径为 。电极 a 表面还发生 iii. 。iii 的存在,有利
于途径 ii,原因是 。
(4)人工固氮是高能耗的过程,结合 分子结构解释原因 。方法三为 的直接利用提供了一种新
的思路。
5.(2024·江苏泰州·模拟预测)I.工业废水和废渣中会产生含硫(-II)等污染物,需经处理后才能排放。
(1)废水中的硫化物通常用氧化剂将其氧化为单质 S 进行回收。已知: 溶液中含硫微粒的物质的量分
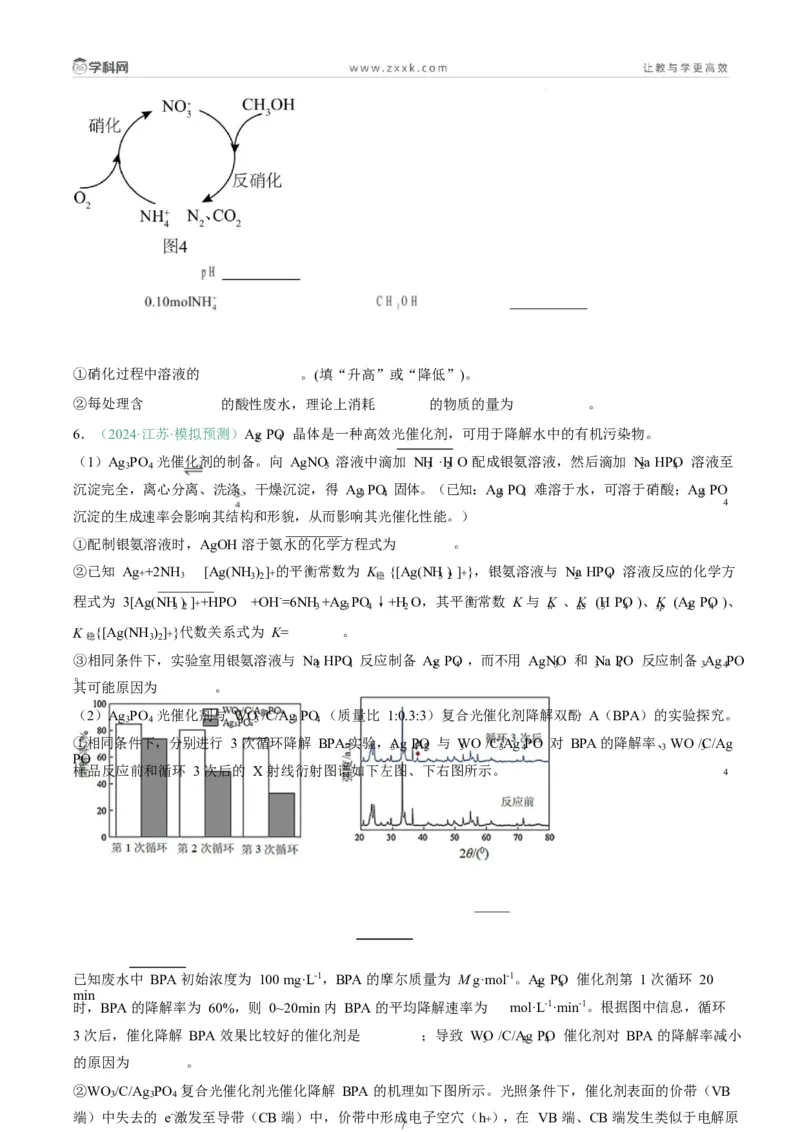
数随 变化情况如图 1 所示。
/图 1 图 2
①向含硫废水中加入稀 调节溶液的 为 6,废水中 。
②控制废水 约为 8,废水中单质硫回收率如图 2 所示。 溶液的加入量大于 时,废水中单
质硫的回收率下降的原因是 。
(2)含硫废渣(硫元素的主要存在形式为 ),可以回收处理并加以利用。沉积物-微生物酸性燃料电池工
作原理如图 3 所示。
碳棒 b 处 S 生成 的电极反应式为 。
II.氨氮废水中含有氨和铵盐,直接排放会造成环境污染。可用以下方法处理:
(3)沉淀法
①“氧化”时在微生物的催化作用下, 被氧化为 。该反应的化学方程式为 。
②“沉淀”中将“氧化”步骤后剩余的 转化为 沉淀,若调节 过大,会降低氨氮
去除率,其原因为 。
(4)生物硝化反硝化法
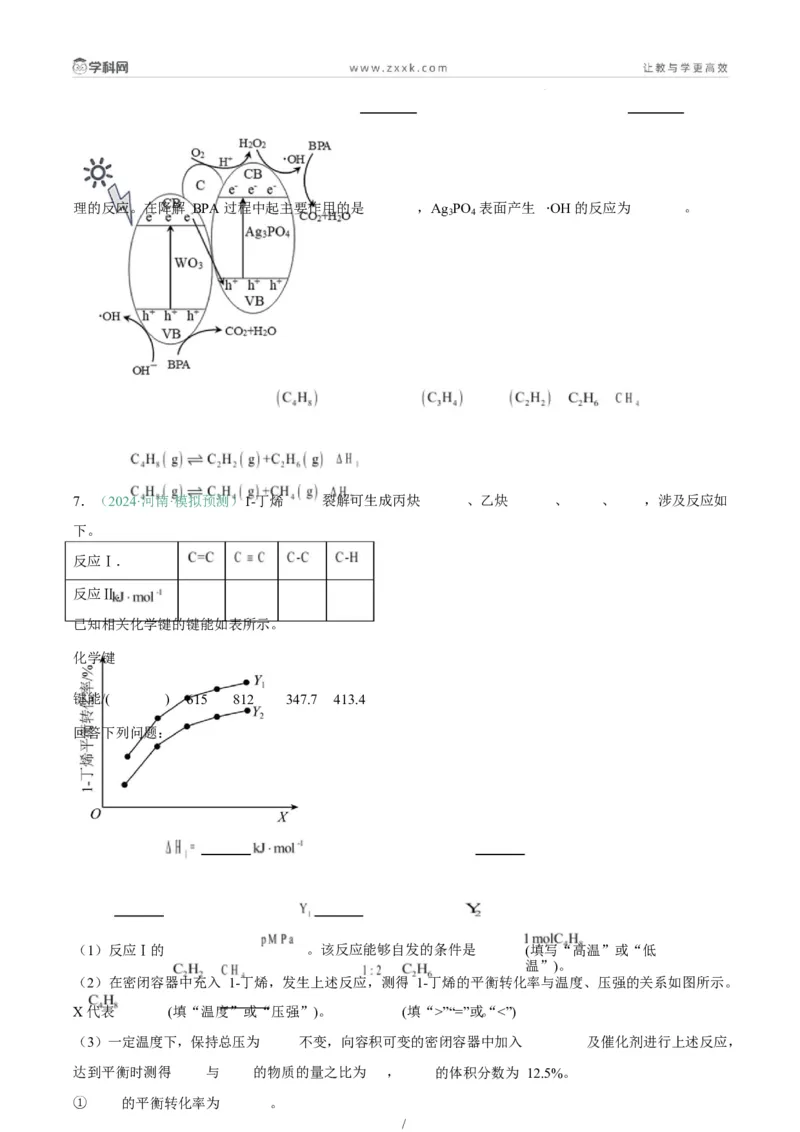
生物硝化反硝化法可将酸性废水中的氨氮转化为氮气,其原理如图 4 所示。
/①硝化过程中溶液的 。(填“升高”或“降低”)。
②每处理含 的酸性废水,理论上消耗 的物质的量为 。
6.(2024·江苏·模拟预测)Ag PO 晶体是一种高效光催化剂,可用于降解水中的有机污染物。
3 4
(1)Ag PO 光催化剂的制备。向 AgNO 溶液中滴加 NH ·H O 配成银氨溶液,然后滴加 Na HPO 溶液至
3 4 3 3 2 2 4
沉淀完全,离心分离、洗涤、干燥沉淀,得 Ag PO 固体。(已知:Ag PO 难溶于水,可溶于硝酸;Ag PO
3 4 3 4 3
4
沉淀的生成速率会影响其结构和形貌,从而影响其光催化性能。)
①配制银氨溶液时,AgOH 溶于氨水的化学方程式为 。
②已知 Ag++2NH
3
[Ag(NH
3
)
2
]+ 的平衡常数为 K
稳
{[Ag(NH
3
)
2
]+},银氨溶液与 N
2
a HPO
4
溶液反应的化学方
程式为 3[Ag(NH
3
)
2
]++HPO +OH-=6NH
3
+Ag
3
PO
4
↓+H
2
O,其平衡常数 K 与 K
w
、K
a3
(H
3
PO
4
)、K
sp
(A
3
g PO
4
)、
K
稳
{[Ag(NH
3
)
2
]+}代数关系式为 K= 。
③相同条件下,实验室用银氨溶液与 Na HPO 反应制备 Ag PO ,而不用 AgNO 和 Na PO 反应制备 Ag PO
2 4 3 4 3 3 4 3 4
。
其可能原因为 。
(2)Ag PO 光催化剂与 WO /C/Ag PO (质量比 1:0.3:3)复合光催化剂降解双酚 A(BPA)的实验探究。
3 4 3 3 4
①相同条件下,分别进行 3 次循环降解 BPA 实验,Ag PO 与 WO /C/Ag PO 对 BPA 的降解率、WO /C/Ag
3 4 3 3 4 3 3
PO
样品反应前和循环 3 次后的 X 射线衍射图谱如下左图、下右图所示。 4
已知废水中 BPA 初始浓度为 100 mg·L-1,BPA 的摩尔质量为 M g·mol-1。Ag PO 催化剂第 1 次循环 20
3 4
min
时,BPA 的降解率为 60%,则 0~20min 内 BPA 的平均降解速率为 mol·L-1·min-1。根据图中信息,循环
3 次后,催化降解 BPA 效果比较好的催化剂是 ;导致 WO /C/Ag PO 催化剂对 BPA 的降解率减小
3 3 4
的原因为 。
②WO /C/Ag PO 复合光催化剂光催化降解 BPA 的机理如下图所示。光照条件下,催化剂表面的价带(VB
3 3 4
端)中失去的 e-激发至导带(CB 端)中,价带中形成
/
电子空穴(h+ ),在 VB 端、CB 端发生类似于电解原理的反应。在降解 BPA 过程中起主要作用的是 ,Ag PO 表面产生 ·OH 的反应为 。
3 4
7.(2024·河南·模拟预测)1-丁烯 裂解可生成丙炔 、乙炔 、 、 ,涉及反应如
下。
反应Ⅰ.
反应Ⅱ.
已知相关化学键的键能如表所示。
化学键
键能/( ) 615 812 347.7 413.4
回答下列问题:
(1)反应Ⅰ的 。该反应能够自发的条件是 (填写“高温”或“低
温”)。
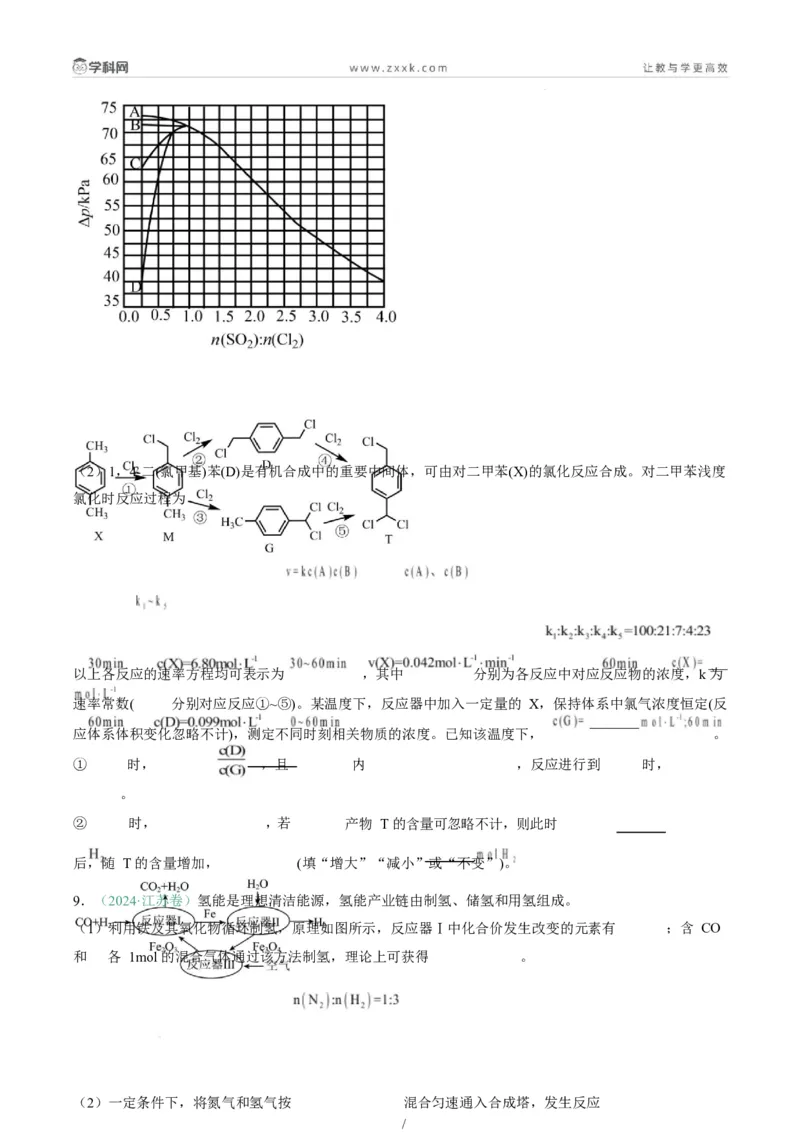
(2)在密闭容器中充入 1-丁烯,发生上述反应,测得 1-丁烯的平衡转化率与温度、压强的关系如图所示。
X 代表 (填“温度”或“压强”)。 (填“>”“=”或。“<”)
(3)一定温度下,保持总压为 不变,向容积可变的密闭容器中加入 及催化剂进行上述反应,
达到平衡时测得 与 的物质的量之比为 , 的体积分数为 12.5%。
① 的平衡转化率为 。
/② 的选择性为 ( 选择性= ,结果保留三位有效数
字)。
③此温度下,反应Ⅱ的平衡常数 MPa(压强代替浓度,分压=总压×物质的量分数)。
(4)1-丁烯可以利用正丁烷催化脱氢制备,催化脱氢分为无氧催化脱氢和有氧催化脱氢,如下表所示。与
无氧脱氢相比,其他条件相同,有氧脱氢( 为氧化剂)平衡转化率高的原因是 。
无氧催化脱氢 有氧催化脱氢
反应Ⅱ.
反应Ⅰ.
平衡转化率:39% 平衡转化率:68%
8.(2024·河北卷)氯气是一种重要的基础化工原料,广泛应用于含氯化工产品的生产。硫酰氯及 1,4-二(氯
甲基)苯等可通过氯化反应制备。
(1)硫酰氯常用作氯化剂和氯磺化剂,工业上制备原理如下:
。
①若正反应的活化能为 ,则逆反应的活化能 (用含 的代数式表示)。
②恒容密闭容器中按不同进料比充入 和其 ,测定 温度下体系达平衡时的
( 为体系初始压强, ,P 为体系平衡压强),结果如图。
上图中温度由高到低的顺序为 ,判断依据为 。M 点 的转化率为 , 温度下用分
压表示的平衡常数 。
③下图曲线中能准确表示 温度下 随进料比变化的是 (填序号)。
/(2)1,4-二(氯甲基)苯(D)是有机合成中的重要中间体,可由对二甲苯(X)的氯化反应合成。对二甲苯浅度
氯化时反应过程为
以上各反应的速率方程均可表示为 ,其中 分别为各反应中对应反应物的浓度,k 为
速率常数( 分别对应反应①~⑤)。某温度下,反应器中加入一定量的 X,保持体系中氯气浓度恒定(反
应体系体积变化忽略不计),测定不同时刻相关物质的浓度。已知该温度下, 。
① 时, ,且 内 ,反应进行到 时,
。
② 时, ,若 产物 T 的含量可忽略不计,则此时
后,随 T 的含量增加, (填“增大”“减小”或“不变”)。
9.(2024·江苏卷)氢能是理想清洁能源,氢能产业链由制氢、储氢和用氢组成。
(1)利用铁及其氧化物循环制氢,原理如图所示,反应器Ⅰ中化合价发生改变的元素有 ;含 CO
和 各 1mol 的混合气体通过该方法制氢,理论上可获得 。
(2)一定条件下,将氮气和氢气按 混合匀速通入合成塔,发生反应
/。海绵状的 作催化剂,多孔 作为 的“骨架”和气体吸附剂。
① 中含有 CO 会使催化剂中毒。 和氨水的混合溶液能吸收 CO 生成
溶液,该反应的化学方程式为 。
② 含量与 表面积、出口处氨含量关系如图所示。 含量大于 ,出口处氨含量下降的原
因是 。
(3)反应 可用于储氢。
①密闭容器中,其他条件不变,向含有催化剂的 溶液中通入 , 产率随温度变
化如图所示。温度高于 , 产率下降的可能原因是 。
②使用含氨基物质(化学式为 ,CN 是一种碳衍生材料)联合 催化剂储氢,可能机理如图所示,
氨基能将 控制在催化剂表面,其原理是 ;用重氢气(D )代替 H ,通过检测是否存在 (填
2 2
化学式)确认反应过程中的加氢方式。
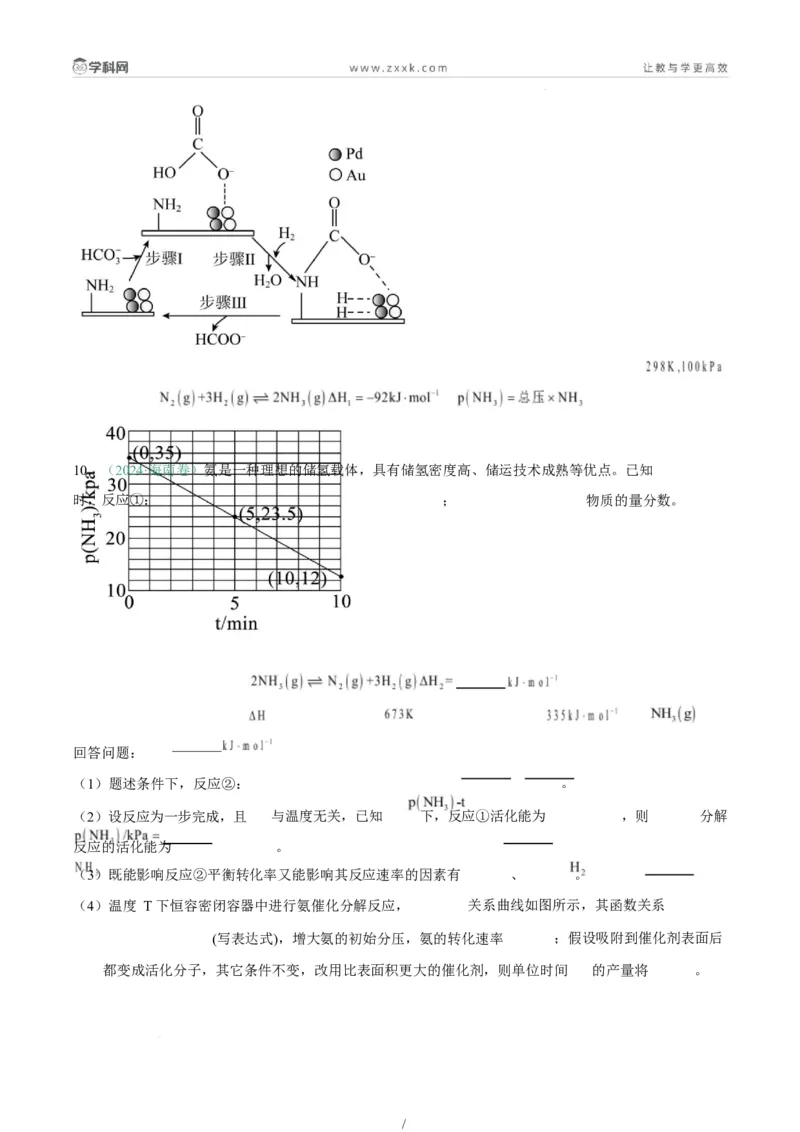
/10.(2024·海南卷)氨是一种理想的储氢载体,具有储氢密度高、储运技术成熟等优点。已知
时,反应①: ; 物质的量分数。
回答问题:
(1)题述条件下,反应②: 。
(2)设反应为一步完成,且 与温度无关,已知 下,反应①活化能为 ,则 分解
反应的活化能为 。
(3)既能影响反应②平衡转化率又能影响其反应速率的因素有 、 。
(4)温度 T 下恒容密闭容器中进行氨催化分解反应, 关系曲线如图所示,其函数关系
(写表达式),增大氨的初始分压,氨的转化速率 ;假设吸附到催化剂表面后
都变成活化分子,其它条件不变,改用比表面积更大的催化剂,则单位时间 的产量将 。
/