文档内容
专题 09 化学反应速率与化学平衡
1.了解化学反应速率的概念、化学反应速率的定量表示方法;
2.了解催化剂在生产、生活和科学研究领域中的重要作用;
3.了解化学反应的可逆性,能用焓变和熵变说明常见简单化学反应的方向;
4.了解化学平衡建立的过程。理解化学平衡常数的含义,能够利用化学平衡常数
考纲
进行简单的计算;
5.理解外界条件(浓度、温度、压强、催化剂等)对反应速率和化学平衡的影响,
认识其一般规律;
6.了解化学反应速率和化学平衡的调控在生活、生产和科学研究领域中的重要作
用。
化学反应速率与化学平衡是高中化学重要理论主干知识,试题难度一般较大,特别是
原理综合题型,将多个知识点组合在一起,客观上增加了思维容量。化学反应速率一
般考查形式如下:一是考查化学反应速率图像问题;二是考查化学反应速率的影响
因素;三是在填空题中综合考查。化学反应进行的方向和限度一般考查形式有:一
考情预测 是在选择题中某个选项考查可逆反应焓变和熵变的大小;二是考查化学平衡状态的
判断;三是与化学平衡相结合考查化学平衡常数的应用等。化学平衡的移动考查形
式固定,一般是以图像或者表格的形式为载体,考查平衡移动、化学平衡的计算、
等效平衡、平衡图像等知识点等,综合性强,难度大,为选择题中的压轴题型。在
填空题中也会结合工农业生产考查平衡状态的判断、平衡图像、化学平衡常数等。
核心素养 变化观念与平衡思想 证据推理与模型认知高频考点一 化学反应速率及影响因素
1.化学反应速率化学反应速率与化学计量数的关系。对于已知反应mA(g)+nB(g)===pC(g)+qD(g),其化学反应速率可用
不同的反应物或生成物来表示,当单位相同时,化学反应速率的数值之比等于方程式中各物质的化学计量数之
比,即v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q。
2.影响化学反应速率的因素
(1)内因
反应物本身的性质是影响化学反应速率的主要因素。如相同条件下Mg、Al与稀盐酸反应的速率大小关系
为:v(Mg)>v(Al)。
(2)外因(其他条件不变,只改变一个条件)
3.理论解释——有效碰撞理论
(1)活化分子:能够发生有效碰撞的分子。
(2)活化能:如图图中:E 为正反应的活化能,使用催化剂时的活化能为E,E 为逆反应的活化能,反应热为E-E。
1 3 2 1 2
(3)有效碰撞:活化分子之间能够引发化学反应的碰撞。
活化分子、有效碰撞与反应速率的关系。
【典例剖析】
【例1】(2022•辽宁省选择性考试)某温度下,在 恒容密闭容器中 发生反应2X(s) Y(g)
+2Z(g),有关数据如下:
时间段/ min 产物Z的平均生成速率/ mol·L-1·min-1
0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是( )
A.1 min时,Z的浓度大于
B.2 min时,加入 ,此时
C.3 min时,Y的体积分数约为33.3%
D.5 min时,X的物质的量为
【答案】B
【解析】A项,反应开始一段时间,随着时间的延长,反应物浓度逐渐减小,产物Z的平均生成速率逐渐
减小,则0~1 min内Z的平均生成速率大于0~2 min内的,故1 min时,Z的浓度大于0.20 mol·L-1,A正确;B项,4 min时生成的Z的物质的量为 ,6min时生成的Z的物质的量为
,故反应在4min时已达到平衡,设达到平衡时生了 ,列三段式:
根据 ,得 ,则Y的平衡浓度为0.3 mol·L-1,Z的平衡浓度为0.6 mol·L-1,平衡常数
,2min时Y的浓度为0.2 mol·L-1,Z的浓度为0.4 mol·L-1,加入 后Z的浓度变
为0.6 mol·L-1, ,反应正向进行,故 ,B错误;C项,反应生成的
Y与Z的物质的量之比恒等于1∶2,反应体系中只有Y和Z为气体,相同条件下,体积之比等于物质的量之
比, ,故Y的体积分数始终约为33.3%,C正确;D项,由B项分析可知5 min时反应处于平衡状态,
此时生成Z为0.6 mol,则X的转化量为0.6 mol,初始X的物质的量为2 mol,剩余X的物质的量为1.4 mol,
D正确;故选B。
【例2】(2022•河北省选择性考试)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为
①X Y;②Y Z。反应①的速率 ,反应②的速率 ,式中 为速率常数。
图甲为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的 曲线。下列说法错误的是( )A.随 的减小,反应①、②的速率均降低
B.体系中
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于T 时,总反应速率由反应②决定
1
【答案】AB
【解析】由图中的信息可知,浓度随时间变化逐渐减小的代表的是X,浓度随时间变化逐渐增大的代表的
是Z,浓度随时间变化先增大后减小的代表的是Y;由图乙中的信息可知,反应①的速率常数随温度升高增大
的幅度小于反应②的。A项,由图甲中的信息可知,随c(X)的减小,c(Y) 先增大后减小,c(Z)增大,因此,反
应①的速率随c(X)的减小而减小,而反应②的速率先增大后减小,A错误;B项,根据体系中发生的反应可知,
在Y的浓度达到最大值之前,单位时间内X的减少量等于Y和Z的增加量,因此,v (X)= v (Y) +v(Z),但是,
在Y的浓度达到最大值之后,单位时间内Z的增加量等于Y和X的减少量,故v (X) + v (Y) = v(Z),B错误;
C项,升高温度可以可以加快反应①的速率,但是反应①的速率常数随温度升高增大的幅度小于反应②的,且
反应②的的速率随着Y的浓度的增大而增大,因此,欲提高Y的产率,需提高反应温度且控制反应时间,C
正确;D项,由图乙信息可知,温度低于T时,k>k,反应②为慢反应,因此,总反应速率由反应②决定,
1 2
D正确;故选AB。
【变式探究】
1.(2021•浙江6月选考)一定温度下:在NO 的四氯化碳溶液(100mL)中发生分解反应:2NO
2 5 2 5
4NO +O 。在不同时刻测量放出的O 体积,换算成NO 浓度如下表:
2 2 2 2 5
171 282
0 600 1200 2220 x
0 0
1.40 0.96 0.66 0.48 0.35 0.24 0.12
下列说法正确的是( )
A.600~1200 s,生成NO 的平均速率为5.0×10-4mol·L-1·s-1
2
B.反应2220 s时,放出的O 体积为11.8L(标准状况)
2
C.反应达到平衡时,v (N O)=2v (NO )
正 2 5 逆 2
D.推测上表中的x为3930
【答案】D
【解析】A项,600~1200 s,NO 的变化量为(0.96-0.66) mol·L-1==0.3 mol·L-1,在此时间段内NO 的变化
2 5 2量为其2倍,即0.6 mol·L-1,因此,生成NO 的平均速率为 1.0×10-3mol·L-1·s-1,A不正确;B
2
项,由表中数据可知,反应2220 s时,NO 的变化量为(1.40-0.35) mol·L-1==1.05 mol·L-1,其物质的量的变化
2 5
量为1.05 mol·L-10.1L=0.105mol,O 的变化量是其 ,即0.0525mol,因此,放出的O 在标准状况下的体积
2 2
为0.0525mol 22.4L/mol=1.176L ,B不正确;C项,反应达到平衡时,正反应速率等于逆反应速率,用不同
物质表示该反应的速率时,其数值之比等于化学计量数之比,2v (N O)=v (NO ),C不正确;D项,分析表
正 2 5 逆 2
中数据可知,该反应经过1110s(600-1710,1710-2820)后NO 的浓度会变为原来的 ,因此,NO 的浓度由
2 5 2 5
0.24 mol·L-1变为0.12 mol·L-1时,可以推测上表中的x为(2820+1110)=3930,D正确。故选D。
2.(2022•浙江省丽水市缙云中学等三校高三联考模拟)为探究HO 对HO 分解是否有催化作用,分别取
2 2 2 2
10mL30% HO (约10 mol·L-1)于四支试管中,控制其它条件相同,进行实验获得如下表数据(氧气为标准状况
2 2
下的体积):
生成氧气体积/(mL)
实验 控制温
所加药品
编号 度/℃
第1个2min 第2个2min 第3个2min
① 20 4.8 5.7 6.8
2mL0.5
② mol·L-1 30 12.8 16.7 20.2
CuSO
4
③ 40 89.6 63.0 28.0
④ 2molH O 40 2.0 3.2 4.3
2
下列有关说法不正确的是( )
A.由以上实验数据可得Cu2+对HO 分解一定有催化作用
2 2
B.温度低于40℃时,CuSO 对HO 分解催化效率随温度升高而降低
4 2 2
C.实验③第1个2min HO 的平均反应速率约为0.8
2 2
D.由实验④可得HO 分解为放热反应
2 2
【答案】D
【解析】A项,实验③④说明Cu2+对HO 分解有催化作用,A正确;B项,温度每升高10°C,速率提高
2 2
2~4倍,实验②③说明,随着温度升高,Cu2+对HO 分解的催化效果明显提高,B正确;C项,实验③第1个
2 2
3min生成氧气平均速率为90mLmin−1,即90×10−3÷22.4mol/min,根据反应2HO=2H O+O↑,HO 的平均反应
2 2 2 2 2 2
⋅速率约为90×10−3÷22.4×2÷10×10−3=0.8molL−1min−1, C正确;D项,随反应的进行,相同时间段内反应速率减
慢,无法说明反应是放热反应,D错误;⋅故选⋅ D。
3.(2021•河北选择性考试)室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:
①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v=kc2(M),反应②的速率可表示为v=kc2(M) (k 、k
1 1 2 2 1 2
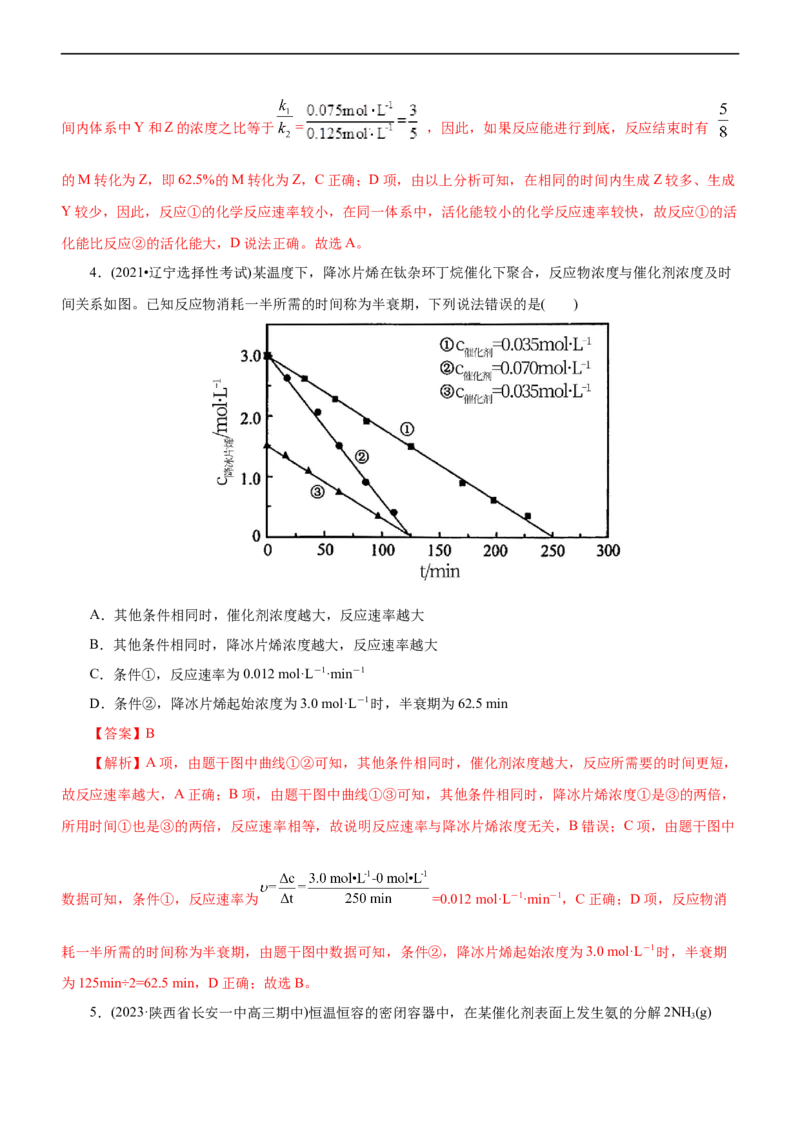
为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是
A.0~30min时间段内,Y的平均反应速率为6.67×10-8mol•L-1•min-1
B.反应开始后,体系中Y和Z的浓度之比保持不变
C.如果反应能进行到底,反应结束时62.5%的M转化为Z
D.反应①的活化能比反应②的活化能大
【答案】A
【解析】A项,由图中数据可知,30 min时,M、Z的浓度分别为0.300 mol•L-1和0.125 mol•L-1,则M的
变化量为0.5 mol•L-1-0.300 mol•L-1=0.200 mol•L-1,其中转化为Y的变化量为0.200 mol•L-1-0.125 mol•L-1=0.075
mol•L-1。因此,0~30 min时间段内,Y的平均反应速率为 ,A不正
确;B项,由题中信息可知,反应①和反应②的速率之比为 ,Y和Z分别为反应①和反应②的产物,且两
者与M的化学计量数相同(化学计量数均为1),因此反应开始后,体系中Y和Z的浓度之比等于 ,由于
k、k 为速率常数,故该比值保持不变,B正确; C项,结合A、B的分析可知因此反应开始后,在相同的时
1 2间内体系中Y和Z的浓度之比等于 = ,因此,如果反应能进行到底,反应结束时有
的M转化为Z,即62.5%的M转化为Z,C正确;D项,由以上分析可知,在相同的时间内生成Z较多、生成
Y较少,因此,反应①的化学反应速率较小,在同一体系中,活化能较小的化学反应速率较快,故反应①的活
化能比反应②的活化能大,D说法正确。故选A。
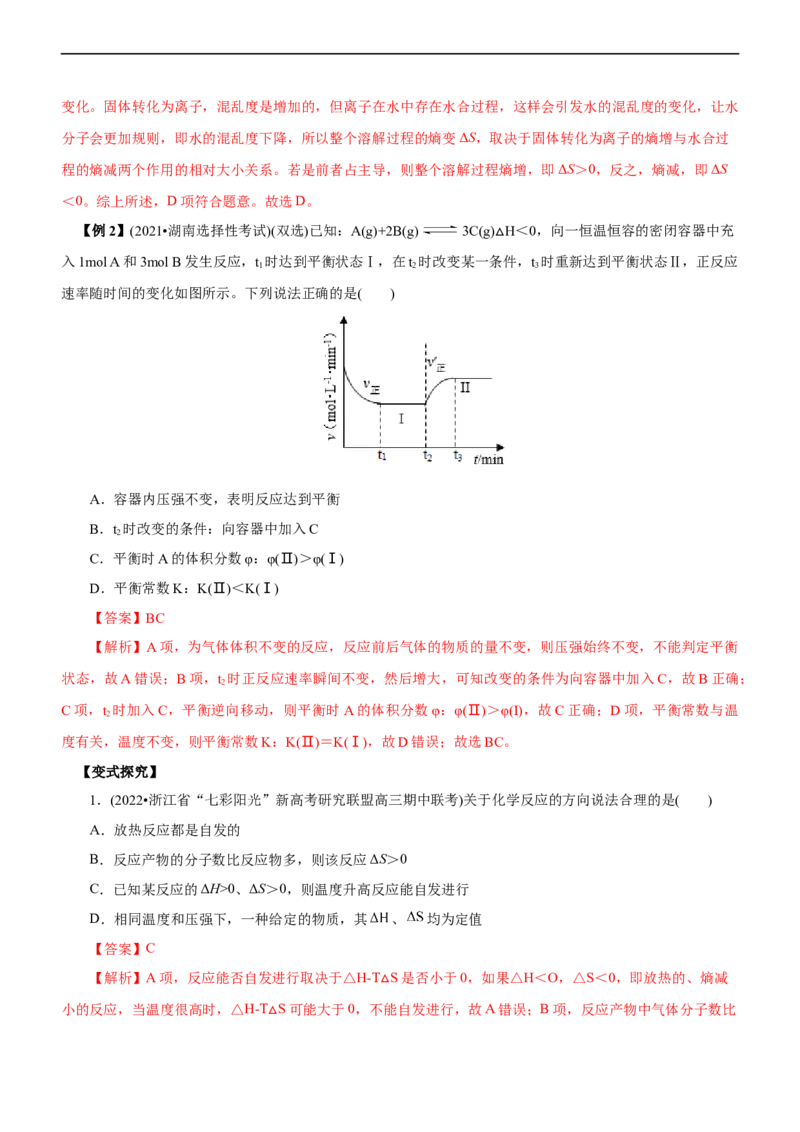
4.(2021•辽宁选择性考试)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓度及时
间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是( )
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为0.012 mol·L-1·min-1
D.条件②,降冰片烯起始浓度为3.0 mol·L-1时,半衰期为62.5 min
【答案】B
【解析】A项,由题干图中曲线①②可知,其他条件相同时,催化剂浓度越大,反应所需要的时间更短,
故反应速率越大,A正确;B项,由题干图中曲线①③可知,其他条件相同时,降冰片烯浓度①是③的两倍,
所用时间①也是③的两倍,反应速率相等,故说明反应速率与降冰片烯浓度无关,B错误;C项,由题干图中
数据可知,条件①,反应速率为 =0.012 mol·L-1·min-1,C正确;D项,反应物消
耗一半所需的时间称为半衰期,由题干图中数据可知,条件②,降冰片烯起始浓度为3.0 mol·L-1时,半衰期
为125min÷2=62.5 min,D正确;故选B。
5.(2023·陕西省长安一中高三期中)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解2NH (g)
3N(g)+3H(g)。测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正
2 2
确的是( )
编号 0 20 40 60 80
① a 2.40 2.00 1.60 1.20 0.80
② a 1.20 0.80 0.40 x
③ 2a 2.40 1.60 0.80 0.40 0.40
A.实验①, ,v(N )=1.0×10-5mol·L-1·min-1
2
B.实验②, 时处于平衡状态,x<0.4
C.相同条件下,增加催化剂的表面积,反应速率增大
D.相同条件下,增加氨气的浓度,反应速率增大
【答案】D
【解析】A项,实验①中,0~20min,氨气浓度变化量为2.40×10-3mol·L-1-2.00×10-4mol·L-1=4.00×10-4
mol·L-1, ,反应速率之比等于化学计量数之比,
,A正确;B项,催化剂表面积大小只影响反应速率,不影响平衡,实验
③中氨气初始浓度与实验①中一样,实验③达到平衡时氨气浓度为4.00×10-4mol·L-1,则实验①达平衡时氨气
浓度也为4.00×10-4mol·L-1,而恒温恒容条件下,实验②相对于实验①为减小压强,平衡正向移动,因此实验
②60min时处于平衡状态,x<0.4,B正确;C项,对比实验①和实验③,氨气浓度相同,实验③中催化剂表面
积是实验①中催化剂表面积的2倍,实验③先达到平衡状态,实验③的反应速率大,说明相同条件下,增加催
化剂的表面积,反应速率增大, C正确;D项,实验①、实验②中0~20min、20min~40min氨气浓度变化量都
是4.00×10-4mol·L-1,实验②中60min时反应达到平衡状态,实验①和实验②催化剂表面积相同,实验①中氨
气初始浓度是实验②中氨气初始浓度的两倍,实验①60min时反应未达到平衡状态,相同条件下,增加氨气浓
度,反应速率并没有增大,D错误;故选D。
分析外界因素对化学反应速率的影响时要注意以下几点
1.对于固体和纯液体反应物,其浓度可视为常数,改变用量速率不变。但固体颗粒的大小决定反应物接触面积的大小,会影响化学反应速率。
2.压强对速率的影响有以下几种情况:
(1)恒温时:增大压强――→体积缩小――→浓度增大――→化学反应速率加快。
(2)恒容时:
①充入气体反应物――→压强增大――→浓度增大――→速率加快。
②充入惰性气体――→总压强增大,但各气体物质的量浓度不变,反应速率不变。
(3)恒压时:压强不变充入惰性气体――→压强不变――→体积增大――→各物质浓度减小――→反应速
率减慢。
3.温度改变对任何反应的速率都有影响。
4.加入催化剂可以同等程度的改变正逆化学反应速率。
高频考点二 化学反应进行的方向与化学平衡状态
1.自发过程
(1)含义
在一定条件下,不需要借助外力作用就能自动进行的过程。
(2)特点
①体系趋向于从高能状态转变为低能状态(体系对外部做功或释放热量)。
②在密闭条件下,体系有从有序转变为无序的倾向性(无序体系更加稳定)。
2.化学反应方向
(1)判据
(2)一般规律:
①ΔH<0,ΔS>0的反应任何温度下都能自发进行;
②ΔH>0,ΔS<0的反应任何温度下都不能自发进行;
③ΔH和ΔS的作用相反,且相差不大时,温度对反应的方向起决定性作用。当 ΔH<0,ΔS<0时低温下反
应能自发进行;当ΔH>0,ΔS>0时,高温下反应能自发进行。
说明:对于一个特定的气相反应,熵变的大小取决于反应前后的气体物质的化学计量数大小。
2.化学平衡状态的判断(1)原则
“体系中一个变化的物理量到某一时刻不再变化”,这个物理量可作为平衡状态的“标志”。
(2)等速标志
v =v 是化学平衡状态的本质特征,对于等速标志的理解,要注意以下两个方面的内容:
正 逆
①用同一种物质来表示反应速率时,该物质的生成速率与消耗速率相等。
②用不同种物质来表示反应速率时必须符合两方面:a.表示两个不同的方向;b.速率之比=浓度的变化量
之比=物质的量的变化量之比=化学计量数之比。
(3)浓度标志
反应混合物中各组分的浓度不变是平衡状态的宏观表现,可逆反应中各组分的物质的量、浓度、百分含量、
气体的体积分数一定时,可逆反应达到平衡状态。
(4)混合气体的平均相对分子质量()标志
①当反应物与生成物均为气体时:对于反应前后气体分子数不等的反应,为定值可作为反应达到平衡状态
的标志;对于反应前后气体分子数相等的反应,为定值不能作为反应达到平衡状态的标志。
②若有非气体参与,无论反应前后气体的分子数是否相等,为定值一定可作为反应达到平衡状态的标志。
(5)混合气体的密度(ρ)标志
①当反应物与生成物均为气体时:在恒容条件下,无论反应前后气体分子数是否相等,ρ为定值,不能作
为反应达到平衡状态的标志;在恒压条件下,对于反应前后气体分子数相等的反应,ρ为定值,不能作为反应
达到平衡状态的标志,对于反应前后气体分子数不等的反应,ρ为定值,可作为反应达到平衡状态的标志。
②当有非气体物质参与反应时:对于恒容体系,ρ为定值,可作为反应达到平衡状态的标志。
(6)混合气体的压强标志
因为恒容、恒温条件下,气体的物质的量n(g)越大则压强p就越大,则无论各成分是否均为气体,只需要
考虑Δn(g)。对于Δn(g)=0的反应,当p为定值时,不能作为反应达到平衡状态的标志;对于Δn(g)≠0的反应,
当p为定值时,可作为反应达到平衡状态的标志。
【典例剖析】
【例1】(2022·浙江省1月选考)AB型强电解质在水中的溶解(可视作特殊的化学反应)表示为AB(s)=An+(aq)
+Bn-(aq),其焓变和熵变分别为ΔH和ΔS。对于不同组成的AB型强电解质,下列说法正确的是( )
A.ΔH和ΔS均大于零 B.ΔH和ΔS均小于零
C.ΔH可能大于零或小于零,ΔS大于零 D.ΔH和ΔS均可能大于零或小于零
【答案】D
【解析】强电解质溶于水有的放热,如硫酸铜等;有的吸热,如碳酸氢钠等,所以在水中溶解对应的ΔH
可能大于零或小于零。熵表示系统混乱程度。体系越混乱,则熵越大。AB型强电解质固体溶于水,存在熵的变化。固体转化为离子,混乱度是增加的,但离子在水中存在水合过程,这样会引发水的混乱度的变化,让水
分子会更加规则,即水的混乱度下降,所以整个溶解过程的熵变ΔS,取决于固体转化为离子的熵增与水合过
程的熵减两个作用的相对大小关系。若是前者占主导,则整个溶解过程熵增,即ΔS>0,反之,熵减,即ΔS
<0。综上所述,D项符合题意。故选D。
【例2】(2021•湖南选择性考试)(双选)已知:A(g)+2B(g) 3C(g) H<0,向一恒温恒容的密闭容器中充
入1mol A和3mol B发生反应,t 时达到平衡状态Ⅰ,在t 时改变某一条△件,t 时重新达到平衡状态Ⅱ,正反应
1 2 3
速率随时间的变化如图所示。下列说法正确的是( )
A.容器内压强不变,表明反应达到平衡
B.t 时改变的条件:向容器中加入C
2
C.平衡时A的体积分数φ:φ(Ⅱ)>φ(Ⅰ)
D.平衡常数K:K(Ⅱ)<K(Ⅰ)
【答案】BC
【解析】A项,为气体体积不变的反应,反应前后气体的物质的量不变,则压强始终不变,不能判定平衡
状态,故A错误;B项,t 时正反应速率瞬间不变,然后增大,可知改变的条件为向容器中加入C,故B正确;
2
C项,t 时加入C,平衡逆向移动,则平衡时A的体积分数φ:φ(Ⅱ)>φ(I),故C正确;D项,平衡常数与温
2
度有关,温度不变,则平衡常数K:K(Ⅱ)=K(Ⅰ),故D错误;故选BC。
【变式探究】
1.(2022•浙江省“七彩阳光”新高考研究联盟高三期中联考)关于化学反应的方向说法合理的是( )
A.放热反应都是自发的
B.反应产物的分子数比反应物多,则该反应ΔS>0
C.已知某反应的ΔH>0、ΔS>0,则温度升高反应能自发进行
D.相同温度和压强下,一种给定的物质,其 、 均为定值
【答案】C
【解析】A项,反应能否自发进行取决于△H-T S是否小于0,如果△H<O,△S<0,即放热的、熵减
小的反应,当温度很高时,△H-T S可能大于0,不△能自发进行,故A错误;B项,反应产物中气体分子数比
△反应物多,则该反应ΔS>0,故B错误;C项,根据△H-T S<0反应能自发进行,某反应的ΔH>0、ΔS>0,
则高温条件反应能自发进行,故C正确;D项,相同温度和△压强下,一种给定的物质,其H、S均为定值,故
D错误;故选C。
2.(2022·河北省百师联盟高三第一轮复习联考)制水煤气的反应为C(s)+HO(g) CO(g)+H(g) ΔH>0,
2 2
现将一定量的原料充入一个容积不变的真空密闭容器中,在恒定温度下使其发生反应,不能说明该反应达到化
学平衡状态的是. ( )
A.CO与H 的物质的量之比不变 B.H 的体积分数不再发生变化
2 2
C.混合气体压强保持不变 D.混合气体的密度不变
【答案】A
【解析】A项,随着反应的进行,生成的CO与H 的物质的量之比始终为1 : 1,因此不能说明达到平
2
衡状态,A错误;B项,H 的体积分数即物质的量分数,随着反应进行H 的体积分数逐渐增大,当不变时说
2 2
明达到平衡状态,B正确 ;C项,随反应的进行,气体的物质的量增大,达到平衡时气体的物质的量不变,
混合气体压强不变,因此压强可作为平衡的标志,C错误;D项,由于反应物C为固体,随着反应进行,气体
质量增大,反应容器体积一定,密度逐渐增大,当混合气体的密度不变时,为达到平衡的标志, D错误;故
选A。
3.(2021•浙江6月选考)相同温度和压强下,关于物质熵的大小比较,合理的是( )
A.1molCH(g)<1molH(g) B.1molHO(g)<2molHO(g)
4 2 2 2
C.1molHO(s)>1molHO(l) D.1molC(s,金刚石)>1molC(s,石黑)
2 2
【答案】B
【解析】A项,CH(g)和H(g)物质的量相同,且均为气态,CH(g)含有的原子总数多,CH(g)的摩尔质量
4 2 4 4
大,所以熵值1molCH (g)>1molH (g),A错误;B项,相同状态的相同物质,物质的量越大,熵值越大,所
4 2
以熵值1molH O(g)<2molH O(g),B正确;C项,等量的同物质,熵值关系为:S(g)>S(l)>S(s),所以熵值
2 2
1molH O(s)<1molH O(l),C错误;D项,从金刚石和石墨的结构组成上来看,金刚石的微观结构更有序,熵
2 2
值更低,所以熵值1molC(s,金刚石)<1molC(s,石黑),D错误;故选B。
4.(2020•江苏卷)反应 可用于纯硅的制备。下列有关该反应的说法正
确的是( )
A.该反应 、
B.该反应的平衡常数C.高温下反应每生成1 mol Si需消耗
D.用E表示键能,该反应
【答案】B
【解析】A项,SiCl 、H、HCl为气体,且反应前气体系数之和小于反应后气体系数之和,因此该反应为
4 2
熵增,即△S>0,故A错误;B项,根据化学平衡常数的定义,该反应的平衡常数K= ,故B
正确;C项,题中说的是高温,不是标准状况下,因此不能直接用22.4L·mol-1计算,故C错误;D项,
△H=反应物键能总和-生成物键能总和,即△H=4E(Si-Cl)+2E(H-H)-4E(H-Cl) -2E(Si-Si),故D错误;
故选B。
5.(2022•浙江省丽水市缙云中学等三校高三联考模拟)在体积为2L的恒容绝热密闭容器中投入1molA和
1molB,发生反应A(s)+B(g) C(g) ΔH<0,2min后达到平衡,此时容器内有0.3molC。下列说法不正
确的是( )
A.若容器内混合气体压强不变,则反应达到平衡状态
B.单位时间内n(B) = n(C)
消耗 生成
生成时,则反应达到平衡状态
C.若开始时在该容器中投入1molA和2molB,则平衡时B的转化率小于30%
D.若将容器的体积压缩到原来的一半,正逆反应速率都增大
【答案】B
【解析】A项,恒容绝热,反应前后气体的物质的量不变、温度升高,则压强增大,当压强不变(即温度
不变)时,该反应处于平衡状态,故A正确;B项,n(B) 与n(C) 均为向正反应方向进行,所以不能用于判断
消 生成
该反应是否处于平衡状态,故B错;C项,根据勒夏特列原理可知,若开始时在该容器中投入1molA和
2molB,增大B的浓度平衡虽然正向移动,但不能完全抵消,所以新平衡时B的转化率小于旧平衡时的转化率
30%,故C正确;D项,若将容器的体积压缩到原来的一半,则反应物和生成物浓度均增加,所以正逆反应速
率均增大,故D正确;故选B。
焓变、熵变和温度对化学反应方向的影响
ΔH ΔS ΔH-TΔS 反应情况
- + 永远是负值 在任何温度下过程均自发进行+ - 永远是正值 在任何温度下过程均非自发进行
+ + 低温为正高温为负 低温时非自发,高温时自发
- - 低温为负高温为正 低温时自发,高温时非自发
高频考点三 化学平衡常数
1.化学平衡常数
(1)概念:
在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常
数,用符号K表示。
(2)表达式:对于反应mA(g)+nB(g) pC(g)+qD(g),K=。
实例:
化学方程式 平衡常数 关系式
N(g)+3H(g) 2NH (g) K = K =
2 2 3 1 2
N(g)+H(g) NH (g) K = (或K )
2 2 3 2 1
2NH (g) N(g)+3H(g) K = K =
3 2 2 3 3
(3)意义:
①K值越大,正反应进行的程度越大,反应物的转化率越大。
②K只受温度影响,与反应物或生成物的浓度变化无关,吸热反应,升高温度,K增大,放热反应,升高
温度,K减小。
2.平衡转化率
对于上例反应中A(g)的平衡转化率可表示为:
α(A)=×100%{c(A)代表A的初始浓度,c (A)代表A的平衡浓度}。
0 平
【典例剖析】
【例1】(2020·三明市普通高中期末质量检测)常温常压下,O 溶于水产生的游离氧原子[O]有很强的杀菌消
3
毒能力,发生的反应如下:
反应①:O O+[O] ΔH>0 平衡常数为K
3 2 1
反应②:[O]+O 2O ΔH<0 平衡常数为K
3 2 2
总反应:2O 3O ΔH<0 平衡常数为K
3 2
下列叙述正确的是( )
A.降低温度,K减小 B.K=K +K
1 2
C.增大压强,K 减小 D.适当升温,可提高消毒效率
2
【答案】D
【解析】A项,降低温度向放热反应移动即正向移动,K增大,故A错误;B项,方程式相加,平衡常数应该相乘,因此K=K ∙K ,故B错误;C项,增大压强,平衡向体积减小的方向移动,即逆向移动,平衡常数
1 2
不变,故C错误;D项,适当升温,反应速率加快,消毒效率提高,故D正确。故选D。
【例2】(2021•全国乙卷)一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用作有
机合成中的碘化剂。回答下列问题:
(1)历史上海藻提碘中得到一种红棕色液体,由于性质相似,Liebig误认为是ICl,从而错过了一种新元素
的发现,该元素是_______。
(2)氯铂酸钡(BaPtCl )固体加热时部分分解为BaCl 、Pt和Cl,376.8℃时平衡常数K=1.0×104Pa2,在一硬
6 2 2 p
质玻璃烧瓶中加入过量BaPtCl ,抽真空后,通过一支管通入碘蒸气(然后将支管封闭),在376.8℃,碘蒸气初
6
始压强为 。376.8℃平衡时,测得烧瓶中压强为32.5 kPa,则P =_______ kPa,反应2ICl(g)=I(g)
Icl 2
+Cl(g)的平衡常数K=_______(列出计算式即可)。
2
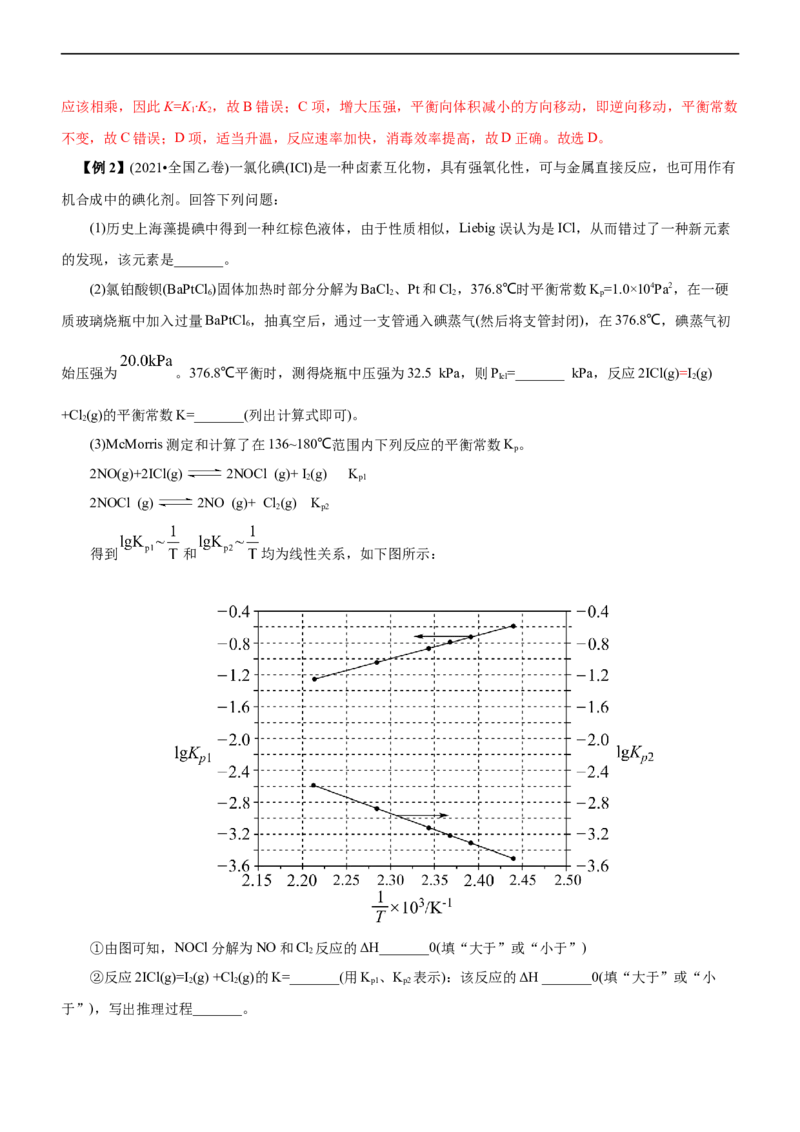
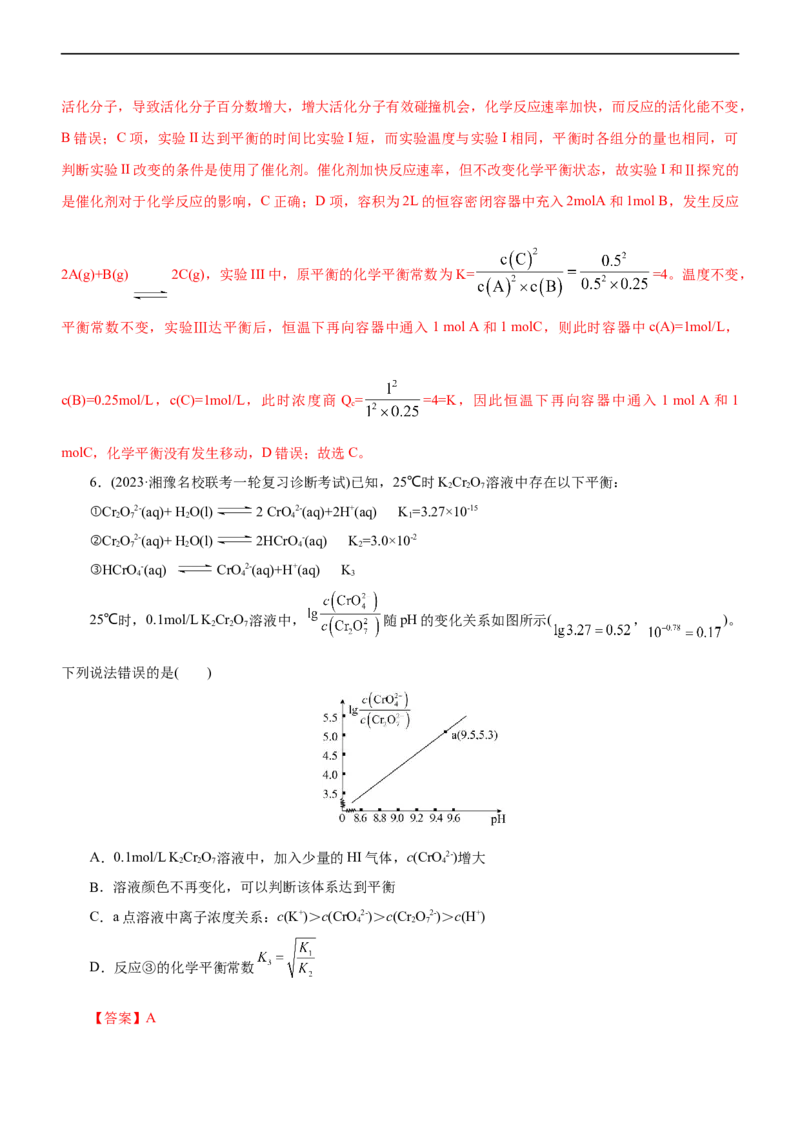
(3)McMorris测定和计算了在136~180℃范围内下列反应的平衡常数K。
p
2NO(g)+2ICl(g) 2NOCl (g)+ I (g) K
2 p1
2NOCl (g) 2NO (g)+ Cl(g) K
2 p2
得到 和 均为线性关系,如下图所示:
①由图可知,NOCl分解为NO和Cl 反应的ΔH_______0(填“大于”或“小于”)
2
②反应2ICl(g)=I (g) +Cl(g)的K=_______(用K 、K 表示):该反应的ΔH _______0(填“大于”或“小
2 2 p1 p2
于”),写出推理过程_______。(4)Kistiakowsky曾研究了NOCl光化学分解反应,在一定频率(v)光的照射下机理为:
NOCl+ →
+NOCl→2NO+Cl
2
其中 表示一个光子能量, 表示NOCl的激发态。可知,分解1mol的NOCl需要吸收
_______mol光子。
【答案】(1)溴(或Br) (3)24.8
(3)①大于 ②K ·K 大于 设T/>T,即 ,由图可知:
p1 p2
则:
,即 ,因此该反应正反应为吸热反应,即ΔH大于0
(4)0.5
【解析】(1)红棕色液体,推测为溴单质,因此错过发现的元素是溴(或Br);
(2)由题意玻376.8℃时璃烧瓶中发生两个反应:BaPtCl (s) BaCl (s)+ Pt (s)+2 Cl (g)、Cl(g)+I (g)
6 2 2 2 2
2ICl(g)。BaPtCl (s) BaCl (s)+ Pt (s)+2 Cl (g)的平衡常数K=1.0×104Pa2,则平衡时p2(Cl )=
6 2 2 p 2
1.0×104Pa2,平衡时p(Cl )=100Pa,设到达平衡时I(g)的分压减小pkPa,则:
2 2
376.8℃平衡时,测得烧瓶中压强为32.5kPa,则0.1+20.0+p=32.5,解得p=12.4,则平衡时
P =2pkPa=2×12.4kPa=24.8kPa;则平衡时,I(g)的分压为(20.0-p)kPa=(20×103-12.4×103)Pa,
Icl 2
24.8kPa=24.8×103Pa,p(Cl )=0.1kPa=100Pa,因此反应2ICl(g)=I (g) +Cl (g)的平衡常数K=
2 2 2;(3)①结合图可知,温度越高, 越小,lgKp 越大,即Kp 越大,说明升高温
2 2
度平衡2NOCl (g) 2NO (g)+ Cl (g)正向移动,则NOCl分解为NO和Cl 反应的大于0;②Ⅰ. 2NO(g)
2 2
+2ICl(g) 2NOCl (g)+ I (g) K ;Ⅱ.2NOCl (g) 2NO (g)+ Cl (g) K ;Ⅰ+Ⅱ得2ICl(g)=I (g)
2 p1 2 p2 2
+Cl(g),则2ICl(g)=I (g) +Cl (g)的K= K ·K ;该反应的ΔH大于0;推理过程如下:设 ,即 ,
2 2 2 p1 p2
由图可知: 则:
,即 ,因此该反应正反应为吸热反应,即ΔH大于
0;(4)Ⅰ. NOCl+ → ,Ⅱ. +NOCl→2NO+Cl ,Ⅰ+Ⅱ得总反应为2NOCl+hv=2NO+Cl ,因此
2 2
2molNOCl分解需要吸收1mol光子能量,则分解1mol的NOCl需要吸收0.5mol光子。
【变式探究】
1.(2022·山东省高三第三次联考)一定温度下,反应MgCl (l) Mg(l) +Cl (g)达到平衡时,下列说法错
2 2
误的是( )
A.该反应的平衡常数K=c(Cl )
2
B.将容器体积压缩为原来一半,当体系再次达到平衡时,Cl 的浓度增大
2
C.减小氯气浓度,平衡正向移动,平衡常数不变
D.温度升高该反应的化学平衡常数K增大
【答案】B
【解析】A项,由化学方程式知,MgCl 和Mg为液态,其浓度是常数,不能写入平衡常数的表达式中,
2
所以该反应的平衡常数K=c(Cl ),A正确;B项,该反应的平衡常数表达式为K=c(Cl ),将容器体积压缩为原
2 2
来一半,当体系再次达到平衡时,因温度不变,则K值不变,所以c(Cl )也不变,B错误;C项,反应的平衡
2
常数只与温度有关,减小产物浓度,平衡正向移动,但平衡常数不变,C正确;D项,Mg在氯气中燃烧为放
热反应,则MgCl (l)分解生成Cl(g)和Mg(l)为吸热反应,ΔH>0,温度升高平衡向正反应方向移动,反应的平
2 2
衡常数K变大,D正确;故选B。
2.在25 ℃时,密闭容器中X、Y、Z三种气体的起始浓度和平衡浓度如下表,下列说法错误的是( )物质 X Y Z
起始浓度/(mol·L-1) 0.1 0.2 0
平衡浓度/(mol·L-1) 0.05 0.05 0.1
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y 2Z,平衡常数为1 600
C.其他条件不变时,增大压强可使平衡常数增大
D.改变温度可以改变该反应的平衡常数
【答案】C
【解析】达到平衡消耗 X 的物质的量浓度为(0.1-0.05)mol·L-1=0.05 mol·L-1,因此转化率为
0.05/0.1×100%=50%,A项正确;根据化学反应速率之比等于化学计量数之比,因此三种组分的系数之比为:
(0.1-0.05)∶(0.2-0.05)∶0.1=1∶3∶2,因此反应方程式为:X+3Y 2Z,根据化学平衡常数的表达式,
K=0.12/(0.05×0.053)=1 600,B项正确;化学平衡常数只受温度的影响,与浓度、压强无关,C项错误、D项
正确。
3.某温度下2 L密闭容器中3种气体起始状态和平衡状态时的物质的量(n)如表所示,下列说法正确的是(
)
X Y W
n(起始状态)/mol 2 1 0
n(平衡状态)/mol 1 0.5 1.5
A.该温度下,此反应的平衡常数表达式是K=
B.其他条件不变,升高温度,若W的体积分数减小,则此反应ΔH<0
C.其他条件不变,使用催化剂,正、逆反应速率和平衡常数均增大,平衡不移动
D.其他条件不变,当密闭容器中混合气体密度不变时,表明反应已达到平衡
【答案】B
【解析】由表知,X、Y是反应物,W是生成物,且Δn(X)∶Δn(Y)∶Δn(W)=2∶1∶3,化学方程式为2X
+Y 3W,反应的平衡常数表达式是K=,A项错误;升高温度,若W的体积分数减小,说明平衡向逆
反应方向移动,则此反应的ΔH<0,B项正确;使用催化剂,平衡常数不变,C项错误;混合气体密度一直不
变,因此混合气体密度不变,不能说明反应已达到平衡,D项错误。
4.已知反应X(g)+Y(g) R(g)+Q(g)的平衡常数与温度的关系如表所示。830 ℃时,向一个2 L的
密闭容器中充入0.2 mol X和0.8 mol Y,反应初始4 s内v(X)=0.005 mol/(L·s)。下列说法正确的是( )
温度/℃ 700 800 830 1 000 1 200
平衡常数 1.7 1.1 1.0 0.6 0.4
A.4 s时容器内c(Y)=0.76 mol/LB.830 ℃达平衡时,X的转化率为80%
C.反应达平衡后,升高温度,平衡正向移动
D.1 200 ℃时反应R(g)+Q(g) X(g)+Y(g)的平衡常数K=0.4
【答案】B
【解析】反应初始4 s内X的平均反应速率v(X)=0.005 mol/(L·s),根据速率之比等于化学计量数之比,可
知v(Y)=v(X)=0.005 mol/(L·s),则4 s内Δc(Y)=0.005 mol·L-1·s-1×4 s=0.02 mol/L,Y的起始浓度为=0.4
mol/L,故4 s时c(Y)=0.4 mol/L-0.02 mol/L=0.38 mol/L,A项错误;设平衡时A的浓度变化量为x,则:
X(g) + Y(g) R(g)+Q(g)
开始(mol/L): 0.1 0.4 0 0
变化(mol/L): x x x x
平衡(mol/L): 0.1-x 0.4-x x x
故=1.0,解得x=0.08,所以平衡时X的转化率为×100%=80%,B项正确;由表格可知,温度升高,
化学平衡常数减小,平衡逆向移动,C项错误;1 200 ℃时反应X(g)+Y(g) R(g)+Q(g)的平衡常数值为
0.4,所以1 200 ℃时反应R(g)+Q(g) X(g)+Y(g)的平衡常数的值为=2.5,D项错误。
5.在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2molA和1molB,发生反应:2A(g)+B(g)
2C(g) ΔH=QkJ/mol。相关条件和数据见下表:
实验编号 实验Ⅰ 实验Ⅱ 实验Ⅲ
反应温度/℃ 700 700 750
达平衡时间/min 40 5 30
平衡时n(C)/mol 1.5 1.5 1
化学平衡常数 K K K
1 2 3
下列说法正确的是( )
A.K=K v ,平衡向正反应方向移动;
正 逆
v =v ,反应达到平衡状态,不发生平衡移动 ;
正 逆
v v ,平衡常数增大
正 逆
B.加入催化剂,平衡时CHCHOH(g)的浓度增大
3 2
C.恒容下,充入一定量的HO(g),平衡向正反应方向移动
2
D.恒容下,充入一定量的CH=CH (g),CH=CH (g)的平衡转化率增大
2 2 2 2
【答案】C
【解析】A项,该反应是一个气体分子数减少的反应,增大压强可以加快化学反应速率,正反应速率增大的幅度大于逆反应的,故v > v ,平衡向正反应方向移动,但是因为温度不变,故平衡常数不变,A不正确;
正 逆
B项,催化剂不影响化学平衡状态,因此,加入催化剂不影响平衡时CHCHOH(g)的浓度,B不正确;C项,
3 2
恒容下,充入一定量的HO(g),HO(g)的浓度增大,平衡向正反应方向移动,C正确;D项,恒容下,充入一
2 2
定量的CH=CH (g),平衡向正反应方向移动,但是CH=CH (g)的平衡转化率减小,D不正确;故选C。
2 2 2 2
【例2】(2021•辽宁选择性考试)某温度下,在恒容密闭容器中加入一定量X,发生反应2X(s) Y(s))
+Z(g),一段时间后达到平衡。下列说法错误的是( )
A.升高温度,若c(Z)增大,则ΔH>0
B.加入一定量Z,达新平衡后m(Y)减小
C.加入等物质的量的Y和Z,达新平衡后c(Z)增大
D.加入一定量氩气,平衡不移动
【答案】C
【解析】A项,根据勒夏特列原理可知,升高温度,化学平衡向着吸热反应方向移动,而c(Z)增大,说明
平衡正向移动,故则ΔH>0,A正确;B项,加入一定量Z,Z的浓度增大,平衡逆向移动,故达新平衡后
m(Y)减小,B正确;C项,加入等物质的量的Y和Z,Z的浓度增大,平衡逆向移动,由于X、Y均为固体,
故K=c(Z),达新平衡后c(Z)不变,C错误;D项,加入一定量氩气,加入瞬间,X、Z的浓度保持不变,故正、
逆反应速率不变,故平衡不移动,D正确;故选C。
【例3】(2022•全国甲卷)金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法
之一是将金红石(TiO)转化为TiCl ,再进一步还原得到钛。回答下列问题:
2 4
(1) TiO 转化为TiCl 有直接氯化法和碳氯化法。在 时反应的热化学方程式及其平衡常数如下:
2 4
(ⅰ)直接氯化:TiO(s)+2Cl(g)= TiCl (g)+O(g) ΔH =172kJ·mol−1 Kp =1.0×10-2
2 2 4 2 1 1
(ⅱ)碳氯化:TiO(s)+2Cl(g)+2C(s)=TiCl (g)+2CO(g) ΔH =-51kJ·mol−1 Kp =1.2×1012Pa
2 2 4 2 2
①反应2C(s)+O(g)=2CO(g)的ΔH为_______ kJ·mol−1,Kp=_______Pa。
2
②碳氯化的反应趋势远大于直接氯化,其原因是_______。
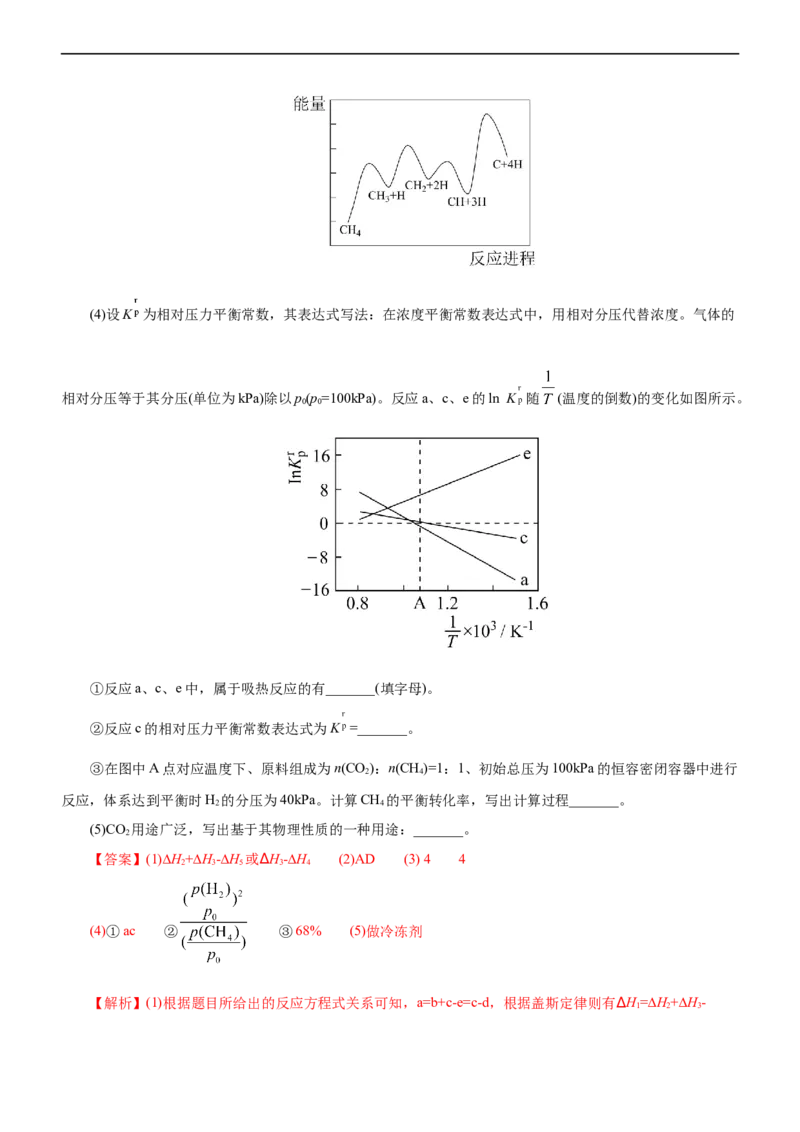
③对于碳氯化反应:增大压强,平衡_______移动(填“向左”“向右”或“不”);温度升高,平衡转化
率_______(填“变大”“变小”或“不变”)。
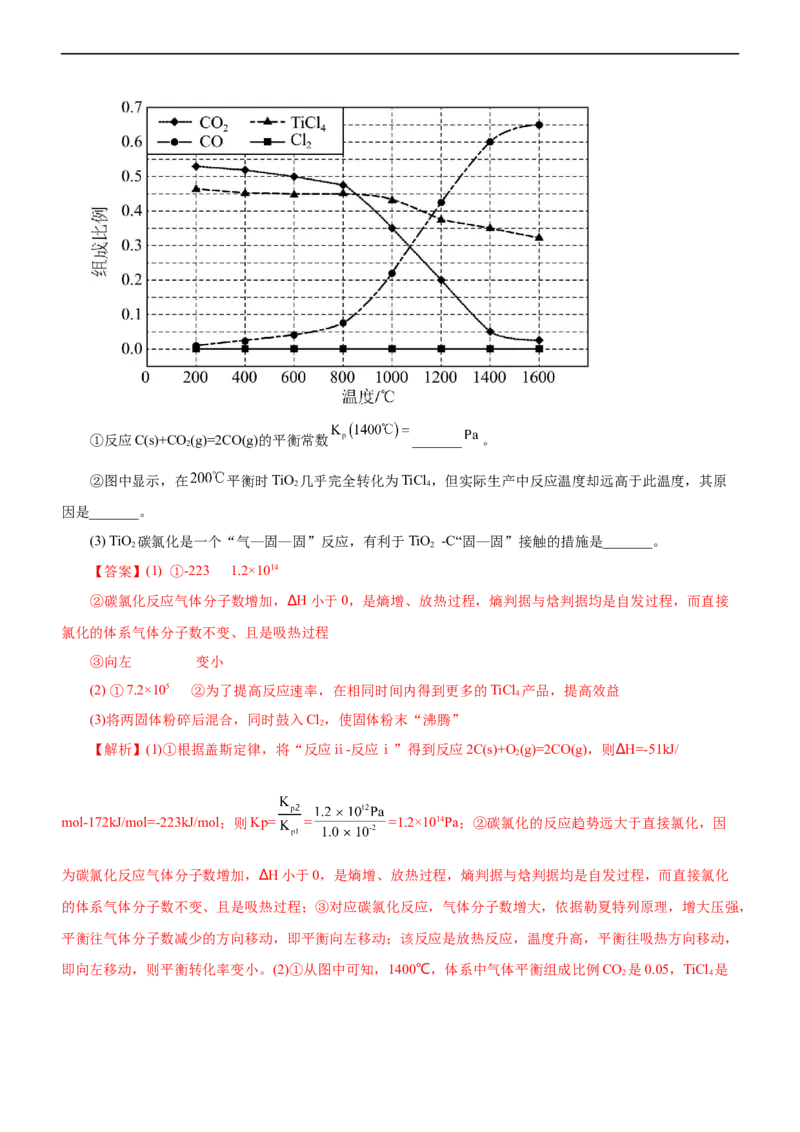
(2)在1.0×105Pa,将TiO、C、Cl 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量
2 2
分数)随温度变化的理论计算结果如图所示。①反应C(s)+CO(g)=2CO(g)的平衡常数 _______ 。
2
②图中显示,在 平衡时TiO 几乎完全转化为TiCl ,但实际生产中反应温度却远高于此温度,其原
2 4
因是_______。
(3) TiO 碳氯化是一个“气—固—固”反应,有利于TiO -C“固—固”接触的措施是_______。
2 2
【答案】(1) ①-223 1.2×1014
②碳氯化反应气体分子数增加,∆H小于0,是熵增、放热过程,熵判据与焓判据均是自发过程,而直接
氯化的体系气体分子数不变、且是吸热过程
③向左 变小
(2) ①7.2×105 ②为了提高反应速率,在相同时间内得到更多的TiCl 产品,提高效益
4
(3)将两固体粉碎后混合,同时鼓入Cl,使固体粉末“沸腾”
2
【解析】(1)①根据盖斯定律,将“反应ⅱ-反应ⅰ”得到反应2C(s)+O(g)=2CO(g),则∆H=-51kJ/
2
mol-172kJ/mol=-223kJ/mol;则Kp= = =1.2×1014Pa;②碳氯化的反应趋势远大于直接氯化,因
为碳氯化反应气体分子数增加,∆H小于0,是熵增、放热过程,熵判据与焓判据均是自发过程,而直接氯化
的体系气体分子数不变、且是吸热过程;③对应碳氯化反应,气体分子数增大,依据勒夏特列原理,增大压强,
平衡往气体分子数减少的方向移动,即平衡向左移动;该反应是放热反应,温度升高,平衡往吸热方向移动,
即向左移动,则平衡转化率变小。(2)①从图中可知,1400℃,体系中气体平衡组成比例CO 是0.05,TiCl 是
2 40.35,CO是0.6,反应C(s)+CO(g)=2CO(g)的平衡常数Kp(1400℃)= =
2
Pa=7.2×105Pa;②实际生产中需要综合考虑反应的速率、产率等,以达到最佳效益,实际反应温度远高于
200℃,就是为了提高反应速率,在相同时间内得到更多的TiCl 产品。(3)固体颗粒越小,比表面积越大,反应
4
接触面积越大。有利于TiO – C“固-固”接触,可将两者粉碎后混合,同时鼓入Cl,使固体粉末“沸腾”,
2 2
增大接触面积。
【变式探究】
1.将等物质的量的N 、H 气体充入某密闭容器中,在一定条件下,发生如下反应并达到平衡:N(g)+
2 2 2
3H(g) 2NH (g) ΔH<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡
2 3
的比较正确的是( )
选项 改变条件 新平衡与原平衡比较
A 增大压强 N 的浓度一定变小
2
B 升高温度 N 的转化率变小
2
C 充入一定量H H 的转化率不变,N 的转化率变大
2 2 2
D 使用适当催化剂 NH 的体积分数增大
3
【答案】B
【解析】A项,正反应是气体体积减小的反应,依据勒夏特列原理可知增大压强平衡向正反应方向移动,
但氮气的浓度仍然比原平衡大,不正确;B项,正反应是放热反应,则升高温度平衡向逆反应方向移动,氮气
的转化率降低,正确;C项,充入一定量的氢气,平衡向正反应方向移动,氮气的转化率增大,而氢气的转化
率降低,不正确;D项,催化剂只能改变反应速率而不能改变平衡状态,不正确,答案选B。
2.(2022·辽宁省丹东市五校高三联考)NO 和NO 存在平衡:2NO (g) NO(g) ΔH<0。下列分析
2 2 2 2 2 4
错误的是( )
A.断裂2molNO (g)中的共价键需能量小于断裂1molN O(g)中的共价键所需能量
2 2 4
B.1mol平衡混合气体中含N原子的物质的量大于1mol
C.恒容升温,由于平衡逆向移动导致气体颜色变深
D.恒温时,缩小容积,气体颜色变深是平衡正向移动导致的
【答案】D
【解析】项,该反应为放热反应,反应物的总能量大于生成物的总能量,则断裂2molNO (g)中的共价键
2
需能量小于断裂1molN O(g)中的共价键所需能量,故A正确;B项,平衡混合气体中含有二氧化氮和四氧化
2 4
二氮,1mol二氧化氮中含有1mol氮原子,1mol四氧化二氮中含有2mol氮原子,则1mol二氧化氮和四氧化二
氮混合气体中氮原子的物质的量一定大于1mol,故B正确;C项,该反应为放热反应,恒容条件下升高温度,平衡向逆反应方向移动,混合气体颜色变深,故C正确;D项,该反应为气体体积增大的反应,恒温时,缩小
容积,混合气体浓度增大,气体颜色变深,气体压强增大,增大压强,平衡向正反应方向移动,气体颜色变浅,
则恒温时,缩小容积,气体颜色变深是混合气体浓度增大导致的,故D错误;故选D。
3.(2022·上海市闵行区高三质量调研考试)一定温度下,在三个体积均为1L的恒容密闭容器中发生反应:
2CHOH(g) CHOCH (g)+HO(g)
3 3 3 2
起始物质的量(mol) 平衡物质的量(mol)
容器编
温度(℃)
号
CHOH(g) CHOCH (g) HO(g)
3 3 3 2
① 387 0.20 0.080 0.080
② 387 0.40
③ 207 0.20 0.090 0.090
下列说法正确的是( )
A.该反应的正反应为吸热反应
B.达到平衡时,容器①中的CHOH体积分数比容器②中的小
3
C.若容器①中反应达到平衡时增大压强,则各物质浓度保持不变
D.若起始向容器①中充入CHOH 0.10mol、CHOCH 0.10mol、HO 0.10mol,则反应将向正反应方向进
3 3 3 2
行
【答案】D
【解析】A项,对比①、③知,其它条件不变时,升高温度,平衡时生成物的量减少,说明升高温度平衡
逆向移动,则正反应为放热反应,故A错误;B项,①、②温度相同,但由于反应前后体积不变,增大反应物
浓度相当于是增大压强,平衡不移动。因此容器①中的CHOH体积分数和容器②中的相同,故B错误;C项,
3
若容器①中反应达到平衡时增大压强,平衡不移动,但容器容积减小,则各物质浓度均增大,故C错误;D项,
387℃时,根据三段式可知:
容器容积为1L,化学平衡常数K= =4,若起始时向容器①中充入CHOH 0.10mol、CHOCH
3 3 3
0.10mol、HO 0.10mol,浓度商Qc= =1 K ,p> 2p
1 2 2 1 1 3 2 3
C.v< v,α(SO ) >α (SO ) D.c> 2c,α(SO )+α(SO )<1
1 3 1 2 3 2 2 3 2 3 3 2
【答案】CD
【解析】对比容器的特点,将容器1和容器2对比,将容器1和容器3对比。容器2中加入4molSO 等效
3
于在相同条件下反应物投入量为4molSO 和2molO ,容器2中起始反应物物质的量为容器1的两倍,容器2相
2 2
当于在容器1达平衡后增大压强,将容器的体积缩小为原来的一半,增大压强化学反应速率加快,υ>υ ,增大
2 1
压强平衡向正反应方向移动,平衡时 c>2c ,p<2p ,α (SO )+α (SO )<1,容器1和容器2温度相同,K=K ;
2 1 2 1 1 2 2 3 1 2
容器3相当于在容器1达到平衡后升高温度,升高温度化学反应速率加快,υ>υ ,升高温度平衡向逆反应方向
3 1
移动,平衡时cp,α (SO )<α (SO ),Kυ ,c>2c,A项错误;B项,
3 1 3 1 3 2 1 2 3 1 2 1 2 1
Kp,则p<2p,B项错误;C项,υ>υ ,α (SO )<α (SO ),C项正确;D项,c>2c,c2c,α (SO )+α (SO )<1,α (SO )<α (SO ),则α (SO )+α (SO )<1,D项正确;故选CD。
2 3 1 2 2 3 3 2 1 2 2 3 3 2
5.(2022·浙江省6月选考)主要成分为HS的工业废气的回收利用有重要意义。
2
(1)回收单质硫。将三分之一的HS燃烧,产生的SO 与其余HS混合后反应:
2 2 2
。在某温度下达到平衡,测得密闭系统中各组分浓度分别为
c(H S)=2.0×10-5mol·L-1、c(SO )= 5.0×10-5mol·L-1、c(H O)=4.0×10-3mol·L-1,计算该温度下的平衡常数
2 2 2
_______。
(2)热解HS制H。根据文献,将HS和CH 的混合气体导入石英管反应器热解(一边进料,另一边出料),
2 2 2 4
发生如下反应:
Ⅰ 2HS(g) 2H(g)+ S (g) ΔH =170kJ·mol−1
2 2 2 1
Ⅱ CH(g)+ S (g) CS(g)+2H(g) ΔH =64kJ·mol−1
4 2 2 2 2
总反应:
Ⅲ 2HS(g)+CH(g) CS(g)+4H(g)
2 4 2 2投料按体积之比V(H S):V(CH )=2:1,并用N 稀释;常压,不同温度下反应相同时间后,测得H 和
2 4 2 2
CS 体积分数如下表:
2
温度/℃ 950 1000 1050 1100 1150
H/V(%) 0.5 1.5 3.6 5.5 8.5
2
CS/V(%) 0.0 0.0 0.1 0.4 1.8
2
请回答:
①反应Ⅲ能自发进行的条件是_______。
②下列说法正确的是_______。
A.其他条件不变时,用Ar替代N 作稀释气体,对实验结果几乎无影响
2
B.其他条件不变时,温度越高,HS的转化率越高
2
C.由实验数据推出HS中的S-H键强于CH 中的 键
2 4
D.恒温恒压下,增加N 的体积分数,H 的浓度升高
2 2
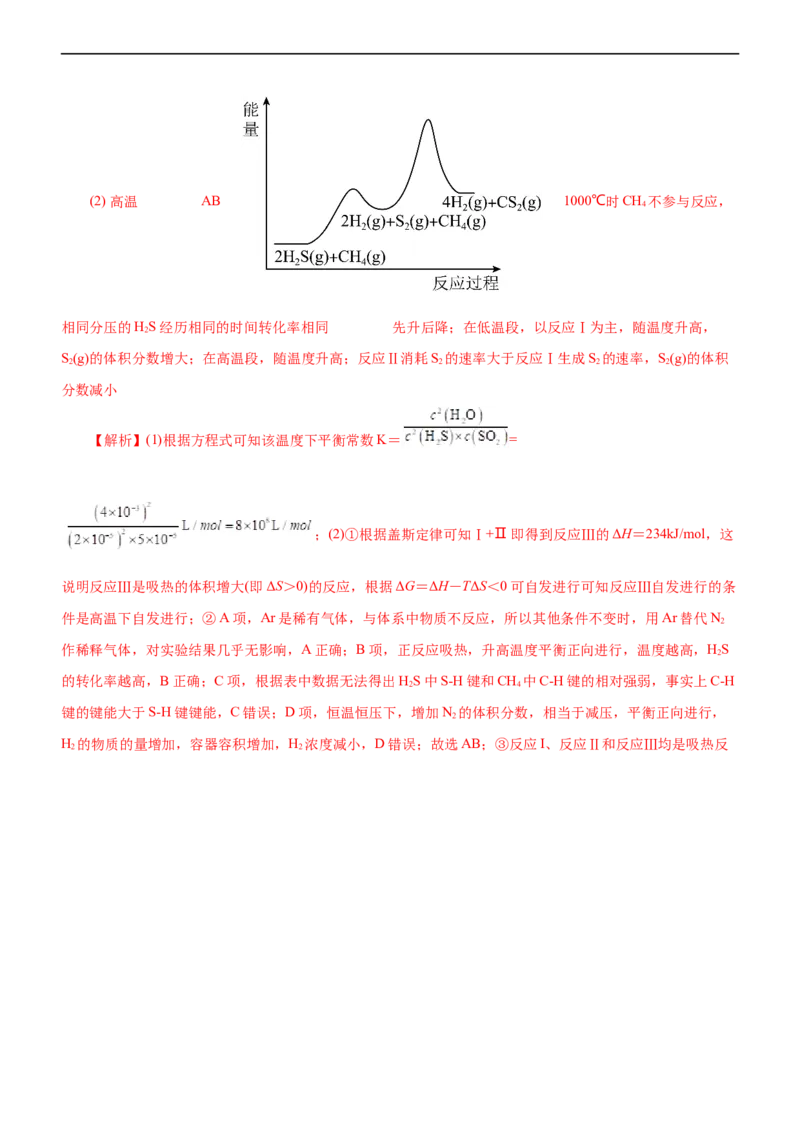
③若将反应Ⅲ看成由反应Ⅰ和反应Ⅱ两步进行,画出由反应原料经两步生成产物的反应过程能量示意图
_______。
④在1000℃,常压下,保持通入的HS体积分数不变,提高投料比[V(H S):V(CH )],HS的转化率不变,
2 2 4 2
原因是_______。
⑤在950℃~1150℃范围内(其他条件不变),S(g)的体积分数随温度升高发生变化,写出该变化规律并分析
2
原因_______。
【答案】(1)8×108 L·mol-1(2) 高温 AB 1000℃时CH 不参与反应,
4
相同分压的HS经历相同的时间转化率相同 先升后降;在低温段,以反应Ⅰ为主,随温度升高,
2
S(g)的体积分数增大;在高温段,随温度升高;反应Ⅱ消耗S 的速率大于反应Ⅰ生成S 的速率,S(g)的体积
2 2 2 2
分数减小
【解析】(1)根据方程式可知该温度下平衡常数K= =
;(2)①根据盖斯定律可知Ⅰ+Ⅱ即得到反应Ⅲ的ΔH=234kJ/mol,这
说明反应Ⅲ是吸热的体积增大(即ΔS>0)的反应,根据ΔG=ΔH-TΔS<0可自发进行可知反应Ⅲ自发进行的条
件是高温下自发进行;②A项,Ar是稀有气体,与体系中物质不反应,所以其他条件不变时,用Ar替代N
2
作稀释气体,对实验结果几乎无影响,A正确;B项,正反应吸热,升高温度平衡正向进行,温度越高,HS
2
的转化率越高,B正确;C项,根据表中数据无法得出HS中S-H键和CH 中C-H键的相对强弱,事实上C-H
2 4
键的键能大于S-H键键能,C错误;D项,恒温恒压下,增加N 的体积分数,相当于减压,平衡正向进行,
2
H 的物质的量增加,容器容积增加,H 浓度减小,D错误;故选AB;③反应I、反应Ⅱ和反应Ⅲ均是吸热反
2 2应,则反应过程能量示意图可表示为 ;④根据表中数据可知
1000℃时CH 不参与反应,相同分压的HS经历相同的时间转化率相同,所以在1000℃常压下,保持通入的
4 2
HS体积分数不变,提高投料比时HS的转化率不变;⑤由于在低温段,以反应Ⅰ为主,随温度升高,S(g)的
2 2 2
体积分数增大;在高温段,随温度升高;反应Ⅱ消耗S 的速率大于反应Ⅰ生成S 的速率,S(g)的体积分数减
2 2 2
小,因此变化规律是先升后降。
化学平衡图像题的解题流程