文档内容
题型 12 新型电化学装置
无论是全国卷还是各自主命题省份的试卷,对电化学考查的概率为100%,这主要源于电化学在中学
化学中的重要地位,在生活、生产中有着广泛而重要的应用,并且能很好地考查考生宏观辨识与微观探
折、变化观念与平衡思想以及证据推理与摸型认知等多重学科素养,根据对近年来考题的分析,电化学命
题往往以可充电电池的工作原理及电解原理的应用为背景,考查电极反应式的书写、离子移动方向、金属
的电化学腐蚀及防护等知识。或将原电池、电解原理与物质的制备、金属的提纯、金属的防护结合起来考
查,考查的角度主要有电极反应方程式的书写或正误判断、离子移动的方向、电极产物种类的判断与量的
计算等,根据近年来高考试题的分析来看,依据研究对象不同,可以将新型电化学装置分为五个题组,一
是依据原电池原理设计的新型电化学装置分析;二是依据二次电池原理设计的新型电化学装置分析;三是
依据电解池原理设计的新型电化学装置分析;四是依据电化学原理设计的组合式新型电化学装置分析;五
是依据电化学原理设计的金属腐蚀和防护电化学装置分析。
题组 01 依据原电池原理设计的新型电化学装置分析
【例1-1】(2024·新疆河南卷)一种可植入体内的微型电池工作原理如图所示,通过CuO催化消耗血糖
发电,
从而控制血糖浓度。当传感器检测到血糖浓度高于标准,电池启动。血糖浓度下降至标准,电池停止工
作。(血糖浓度以葡萄糖浓度计)电池工作时,下列叙述错误的是
A.电池总反应为
B.b电极上CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用
C.消耗18mg葡萄糖,理论上a电极有0.4mmol电子流入
D.两电极间血液中的 在电场驱动下的迁移方向为b→a
【答案】C
【分析】由题中信息可知,b电极为负极,发生反应 ,然后再发生
;a电极为正极,发生反应 ,在这个过程中发生
的总反应为 。
【解析】A.由题中信息可知,当电池开始工作时,a电极为电池正极,血液中的 在a电极上得电子生
成 ,电极反应式为 ;b电极为电池负极, 在b电极上失电子转化成
CuO,电极反应式为 ,然后葡萄糖被CuO氧化为葡萄糖酸,CuO被还原
为 ,则电池总反应为 ,A正确;B.b电极上CuO将葡萄糖被CuO氧化为
葡萄糖酸后被还原为 , 在b电极上失电子转化成CuO,在这个过程中CuO的质量和化学性质保
持不变,因此,CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用,B正确;C.根据反应
可知, 参加反应时转移2 mol电子, 的物质的量为
0.1 mmol,则消耗18 mg葡萄糖时,理论上a电极有0.2 mmol电子流入,C错误;D.原电池中阳离子从
负极移向正极迁移,故 迁移方向为b→a,D正确。综上所述,本题选C。
【例1-2】(2023·海南卷)利用金属Al、海水及其中的溶解氧可组成电池,如图所示。下列说法正确的
是
A.b电极为电池正极B.电池工作时,海水中的 向a电极移动
C.电池工作时,紧邻a电极区域的海水呈强碱性
D.每消耗1kgAl,电池最多向外提供37mol电子的电量
【答案】A
【分析】铝为活泼金属,发生氧化反应为负极,则石墨为正极;
【解析】A.由分析可知,b电极为电池正极,A正确;B.电池工作时,阳离子向正极移动,故海水中的
向b电极移动,B错误;C.电池工作时,a电极反应为铝失去电子生成铝离子 ,铝离子
水解显酸性,C错误;D.由C分析可知,每消耗1kgAl(为 ),电池最多向外提供
mol电子的电量,D错误;故选A。
【提分秘籍】
1.电极反应
(1)反应要求:自发进行放热的氧化还原反应。
(2)根据化合价升降判断反应类型和电极类型:正极发生价降低的还原反应,负极发生价升高的氧化反
应。
2.电子流向:负极 正极(电子不能在溶液中流动)。
3.电流流向:正极 负极 正极。
4.离子流向:离子只能在溶液中流动,不能在导线上流动。
(1)原电池:阳离子→正极;阴离子→负极;
(2)盐桥中:阳离子→正极;阴离子→负极。
5.电解质溶液的选择
(1)碱金属电极:不选择水溶液及醇类,一般选择有机电解质或固体电解质;
(2)盐桥式原电池:负极材料和与其反应的电解质在不同的容器中。
6.电化学中溶液pH的变化
(1)电极pH变化
看该电极反应是消耗还是产生H+ 或OH- ; 若H+ 或OH- 无变化,看该电极是消耗还是产生水。
(2)溶液pH变化
① ②
看总反应是消耗还是产生H+ 或OH- ; 若H+ 或OH- 无变化,看总反应是消耗还是产生水。
7.判断电极方程式是否正确
① ②
(1)看电极反应是氧化反应还是还原反应;
(2)看得反应是得电子还是失电子;
(3)看产物能否与溶液反应酸性溶液:方程式中不能出现OH- ; 碱性溶液:方程式中不能出现H+ 。
看电极产物能否和环境中的其他物质反应
① ②
③ 酸
CH4 碱性
CO
O2-
性
氧化产物 CO2
CO HCO CO
酸
O2 碱性 中性 CO2
性
还原产物 H2O OH- OH-
CO
(4)看物质拆分是否正确
强酸、强碱、可溶性盐溶液可拆
非溶液和熔融状态下进行的反应不能写成离子方程式形式
①
原子团不能拆分
②
(5)看有无隐含的酸碱性
③
酸性溶液:产物是NH4+ 、Fe3+ 、Cu2+ 等弱阳离子
碱性溶液:有金属氧化物、氢氧化物参与的反应
①
8.新型化学电源中电极反应式的书写三步骤
②
【变式演练】
【变式1-1】(2024·云南·模拟预测)微生物燃料电池是利用微生物作为催化剂降解污水中的有机物(以对
苯二甲酸为例),其原理如图装置所示。下列判断错误的是A.微生物电池在处理废水时的能量转化为化学能变为电能
B.该微生物电池工作时,电流由 极经负载流向 极
C.该微生物电池原理图中的离子交换膜为阴离子交换膜
D.该微生物电池的负极电极反应式为
【答案】C
【分析】根据原理图分析,氧气转化为水,发生还原反应, 电极为正极;对苯二甲酸转化为二氧化碳,
发生氧化反应,a为负极,据以上分析解答。
【解析】A.微生物电池属于原电池,所以在处理废水时的能量转化为化学能变为电能,A正确;B.由
分析可知, 电极为原电池的负极, 电极为正极,电流由 极经负载流到 极,B正确;C.由装置图可
知,负极上对苯二甲酸放电生成的氢离子经离子交换膜流向正极,离子交换膜为阳离子交换膜,C错误;
D.该微生物原电池的负极电极反应是 发生氧化反应生成CO2 。其电极反应式为
,D正确;故答案为:C。
【变式1-2】(2024·全国·模拟预测)我国科学家发明了一种新型短路膜电池,利用 分离 的装置如
图所示。下列说法中正确的是A.正极反应为
B.正极反应消耗22.4L ,理论上需要转移2mol电子
C.该装置用于空气中 的捕获, 最终由出口A流出
D.该电池中电子由负极经短路膜流向正极
【答案】D
【分析】通入氧气的一极为正极,电极反应式为 , 与 反应得到 ,
通入氢气的一极为负极,电极反应式为 , 与 反应生成 ,实现 的分离。
【解析】A.由分析可知,正极的电极反应式为 ,A错误;B.未指明是否处在标
准状况下,无法计算22.4L 的物质的量,则无法计算反应中需要转移的电子数,B错误;C.由题图可
知,负极生成 ,则 最终由出口B流出,C错误;D.由题图可知,电子可以在短路膜中移动,该
电池中负极上失去的电子经短路膜流向正极,D正确;故选D。
题组 02 依据二次电池原理设计的新型电化学装置分析
【例2-1】(2024·宁夏四川卷)科学家使用 研制了一种 可充电电池(如图所示)。电池工
作一段时间后, 电极上检测到 和少量 。下列叙述正确的是
A.充电时, 向阳极方向迁移
B.充电时,会发生反应
C.放电时,正极反应有
D.放电时, 电极质量减少 , 电极生成了
【答案】C
【分析】Zn具有比较强的还原性, 具有比较强的氧化性,自发的氧化还原反应发生在Zn与MnO2
之间,所以 电极为正极,Zn电极为负极,则充电时 电极为阳极、Zn电极为阴极。
【解析】A.充电时该装置为电解池,电解池中阳离子向阴极迁移,即 向阴极方向迁移,A不正确;
B.放电时,负极的电极反应为 ,则充电时阴极反应为Zn2++2e-=Zn,即充电时Zn元素化合
价应降低,而选项中Zn元素化合价升高,B不正确;C.放电时 电极为正极,正极上检测到
和少量 ,则正极上主要发生的电极反应是 ,C正确;
D.放电时,Zn电极质量减少0.65g(物质的量为0.010mol),电路中转移0.020mol电子,由正极的主要
反应 可知,若正极上只有 生成,则生成 的物质的量为0.020mol,但是正极上还有 生成,因此, 的物质的量小于0.020mol,D不正确;综上所
述,本题选C。
【例2-2】(2023·新疆内蒙古卷)室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种
室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化
纤维素纸作为另一电极。工作时,在硫电极发生反应: S8+e-→ S , S +e-→S ,2Na++ S
+2(1- )e-→Na2Sx
下列叙述错误的是
A.充电时Na+ 从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为:2Na++ S8+2e-→Na2Sx
D.炭化纤维素纸的作用是增强硫电极导电性能
【答案】A
【分析】由题意可知放电时硫电极得电子,硫电极为原电池正极,钠电极为原电池负极。
【解析】A.充电时为电解池装置,阳离子移向阴极,即钠电极,故充电时,Na+ 由硫电极迁移至钠电
极,A错误;B.放电时Na在a电极失去电子,失去的电子经外电路流向b电极,硫黄粉在b电极上得电
子与a
电极释放出的Na+ 结合得到Na2Sx ,电子在外电路的流向为a→b,B正确;C.由题给的一系列方程式相加
可以得到放电时正极的反应式为2Na++ S8+2e-→Na2Sx ,C正确;D.炭化纤维素纸中含有大量的炭,炭
具有良好的导电性,可以增强硫电极的导电性能,D正确;故答案选A。
【提分秘籍】
1.二次电电池的特点
(1)放电时为原电池,电极属性为正负极
(2)充电时为电解池,电极属性为阴阳极
(3)阳极连正极,电极反应式相反,充电时变成阳极
(4)阴极连负极,电极反应式相反,充电时变成阴极
(5)充电时,电池上“-”极应接电源的负极
2.图解二次电池的充放电3.二次电池的充放电规律
a.充电时电极的连接:充电的目的是使电池恢复其供电能力,因此负极应与电源的负极相连以获得电子,
可简记为负接负后作阴极,正接正后作阳极。
b.工作时的电极反应式:同一电极上的电极反应式,在充电与放电时,形式上恰好是相反的;同一电极周
围的溶液,充电与放电时pH的变化趋势也恰好相反。
4.二次电池电极反应式的书写方法
a.标:先标出原电池总反应式电子转移的方向和数目,找出参与负极和正极反应的物质。
b.写:写出一个比较容易书写的电极反应式(书写时一定要注意电极产物是否与电解质溶液共存)
c.减:在电子守恒的基础上,总反应式减去写出的电极反应式即得另一电极反应式。
充电时的电极反应与放电时的电极反应过程相反,即:
充电时的阳极反应与放电时的正极反应相反;充电时的阴极反应与放电时的负极反应相反。
【变式演练】
【变式2-1】(2024·湖北武汉·模拟预测)中国科学院物理研究所发明了一种以对苯二甲酸二钠复合材料
和硬碳(多孔形态,化学式为C)为电极材料的有机钠离子电池,其内部结构如下图所示,放电时,a电
极发生如下变化:
下列说法错误的是
A.放电时,a电极电势高于b电极
B.充电时, 向b电极移动
C.充电时,b电极的电极反应式为
D.用该电池为一个 的充电宝充满电,a电极质量增加 ( ,一个电子的电量
, 为 )
【答案】D【分析】放电时,a电极发生反应: ,说明
Na+ 移向a电极,a电极为正极,b电极为负极,以此解答。
【解析】A.由分析可知,放电时,a电极为正极,b电极为负极,a电极电势高于b电极,A正确;B.
由分析可知,放电时,a电极为正极,b电极为负极,则充电时,a电极为阳极,b电极为阴极,Na+ 向阴
极移动,B正确;C.由分析可知,充电时,b电极为阴极,电极反应式为: ,C正
确;D.a电极为正极,电极方程式为: +2e-+2Na+=
,若a电极质量增加82.8g时,参与反应的n(Na+)= ,转移
3.6mol电子,则充入电量为 mAh,D错误;故选D。
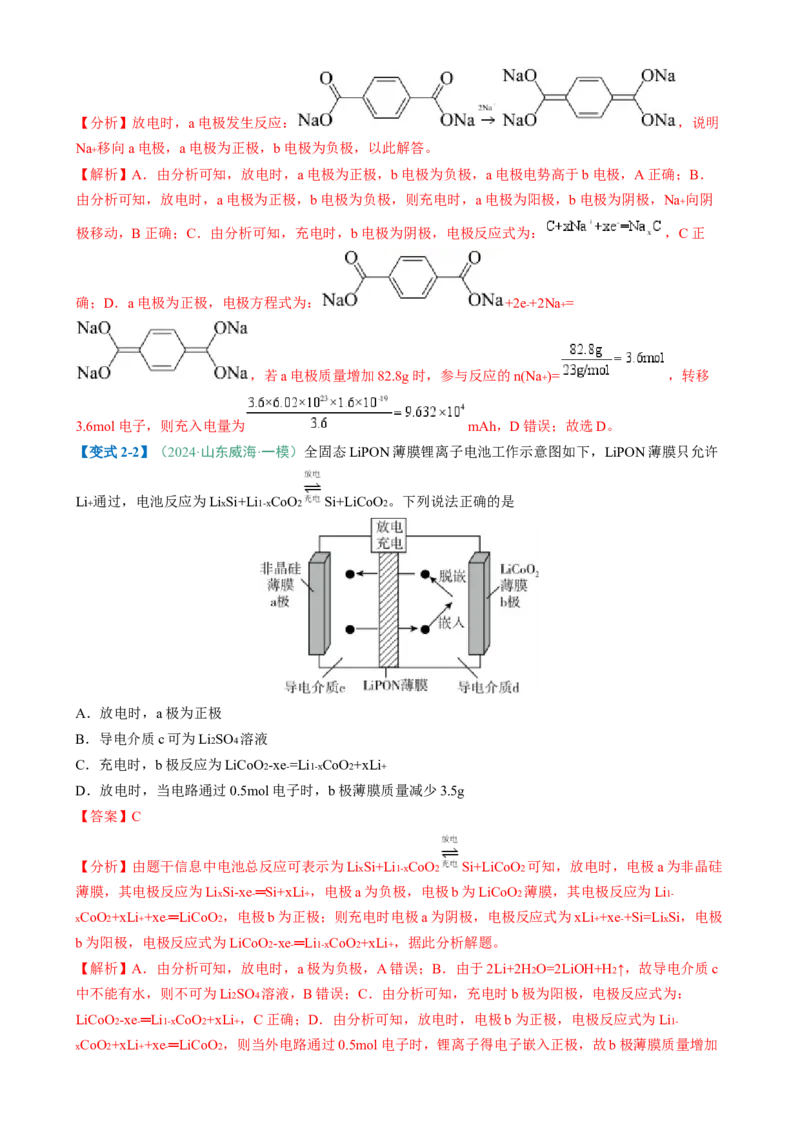
【变式2-2】(2024·山东威海·一模)全固态LiPON薄膜锂离子电池工作示意图如下,LiPON薄膜只允许
Li+ 通过,电池反应为LixSi+Li1-xCoO2 Si+LiCoO2 。下列说法正确的是
A.放电时,a极为正极
B.导电介质c可为Li2SO4 溶液
C.充电时,b极反应为LiCoO2-xe-=Li1-xCoO2+xLi+
D.放电时,当电路通过0.5mol电子时,b极薄膜质量减少3.5g
【答案】C
【分析】由题干信息中电池总反应可表示为LixSi+Li1-xCoO2 Si+LiCoO2 可知,放电时,电极a为非晶硅
薄膜,其电极反应为LixSi-xe-═Si+xLi+ ,电极a为负极,电极b为LiCoO2 薄膜,其电极反应为Li1-
xCoO2+xLi++xe-═LiCoO2 ,电极b为正极;则充电时电极a为阴极,电极反应式为xLi++xe-+Si=LixSi,电极
b为阳极,电极反应式为LiCoO2-xe-═Li1-xCoO2+xLi+ ,据此分析解题。
【解析】A.由分析可知,放电时,a极为负极,A错误;B.由于2Li+2H2O=2LiOH+H2↑,故导电介质c
中不能有水,则不可为Li2SO4 溶液,B错误;C.由分析可知,充电时b极为阳极,电极反应式为:
LiCoO2-xe-═Li1-xCoO2+xLi+ ,C正确;D.由分析可知,放电时,电极b为正极,电极反应式为Li1-
xCoO2+xLi++xe-═LiCoO2 ,则当外电路通过0.5mol电子时,锂离子得电子嵌入正极,故b极薄膜质量增加0.5mol×7g∙mol-1=3.5g,D错误;答案选C。
题组 03 依据电解池原理设计的新型电化学装置分析
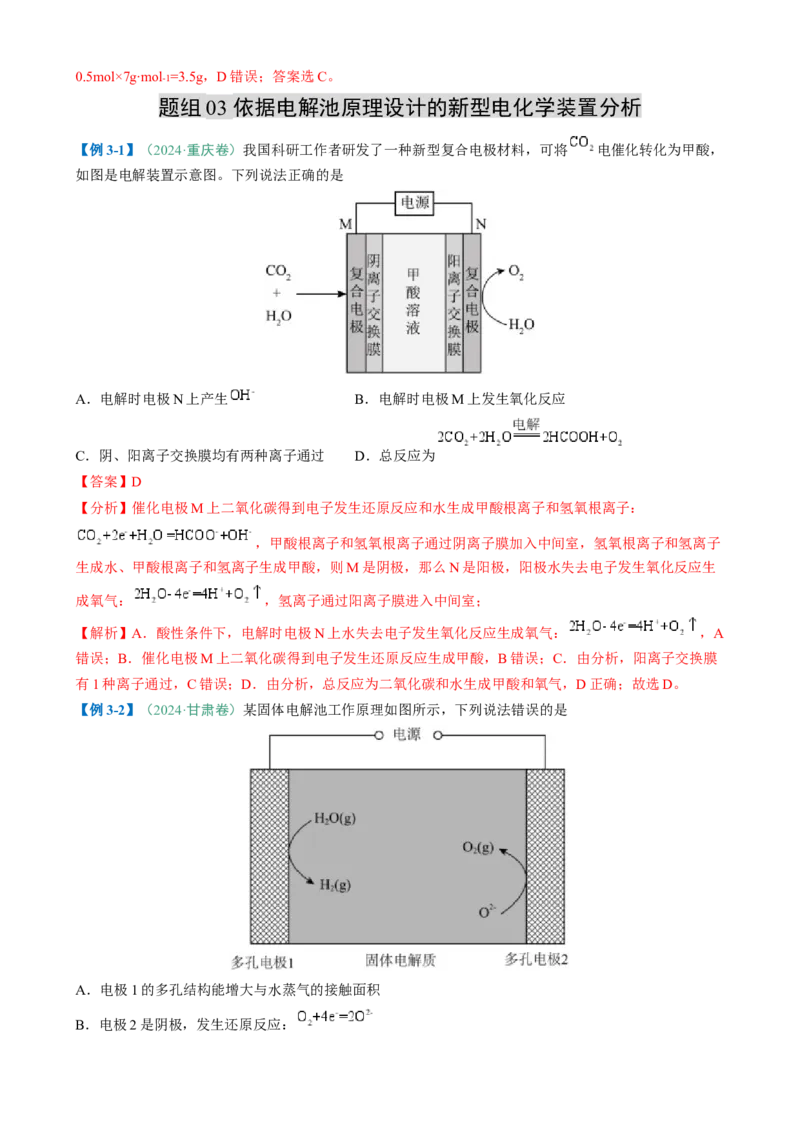
【例3-1】(2024·重庆卷)我国科研工作者研发了一种新型复合电极材料,可将 电催化转化为甲酸,
如图是电解装置示意图。下列说法正确的是
A.电解时电极N上产生 B.电解时电极M上发生氧化反应
C.阴、阳离子交换膜均有两种离子通过 D.总反应为
【答案】D
【分析】催化电极M上二氧化碳得到电子发生还原反应和水生成甲酸根离子和氢氧根离子:
,甲酸根离子和氢氧根离子通过阴离子膜加入中间室,氢氧根离子和氢离子
生成水、甲酸根离子和氢离子生成甲酸,则M是阴极,那么N是阳极,阳极水失去电子发生氧化反应生
成氧气: ,氢离子通过阳离子膜进入中间室;
【解析】A.酸性条件下,电解时电极N上水失去电子发生氧化反应生成氧气: ,A
错误;B.催化电极M上二氧化碳得到电子发生还原反应生成甲酸,B错误;C.由分析,阳离子交换膜
有1种离子通过,C错误;D.由分析,总反应为二氧化碳和水生成甲酸和氧气,D正确;故选D。
【例3-2】(2024·甘肃卷)某固体电解池工作原理如图所示,下列说法错误的是
A.电极1的多孔结构能增大与水蒸气的接触面积
B.电极2是阴极,发生还原反应:C.工作时 从多孔电极1迁移到多孔电极2
D.理论上电源提供 能分解
【答案】B
【分析】多孔电极1上H2O(g)发生得电子的还原反应转化成H2(g),多孔电极1为阴极,电极反应为
2H2O+4e-=2H2 +2O2- ;多孔电极2上O2- 发生失电子的氧化反应转化成O2(g),多孔电极2为阳极,电极
反应为2O2--4e-=O2 。
【解析】A.电极1的多孔结构能增大电极的表面积,增大与水蒸气的接触面积,A项正确;B.根据分
析,电极2为阳极,发生氧化反应:2O2--4e-=O2 ,B项错误;C.工作时,阴离子O2- 向阳极移动,即
O2- 从多孔电极1迁移到多孔电极2,C项正确;D.根据分析,电解总反应为2H2O(g) 2H2 +O2 ,
分解2molH2O转移4mol电子,则理论上电源提供2mol电子能分解1molH2O,D项正确;答案选B。
【提分秘籍】
1.电解池的工作原理
(1)电极名称及电极反应式(电解CuCl2 溶液为例)
总反应式:CuCl2 Cu+Cl2↑
(2)电解过程的三个流向
电子流向:电源负极→电解池阴极;电解池的阳极→电源的正极;
离子流向:阳离子→电解池的阴极,阴离子→电解池的阳极。
①
电流方向:电源正极→电解池阳极→电解质溶液→电解池阴极→电源极。
②
2.电极产物判断
③
(1)阳极产物的判断
活性电极(除Au、Pt以外的金属材料作电极),电极材料失电子,生成金属阳离子。
惰性电极(Pt、Au、石墨),要依据阴离子的放电顺序加以判断。
①
②
阴离子的放电顺序:活泼电极>S2- >I- >Br- >Cl- >OH- >含氧酸根离子。S2- 、I- 、Br- 、Cl- 放电,
产物分别是S、I2 、Br2 、Cl2 ;若OH- 放电,则得到H2O和O2 。(2)阴极产物的判断
直接根据阳离子放电顺序进行判断。
阳离子放电顺序:Ag+ >Fe3+ >Cu2+ >H+(酸)>Fe2+ >Zn2+ >H+(水)>Al3+ >Mg2+ 。
若金属阳离子(Fe3+ 除外)放电,则得到相应金属单质;若H+ 放电,则得到H2 。
放电顺序本质遵循氧化还原反应的优先规律,即得(失)电子能力强的离子先放电。
①
3.电极反应式、电解方程式的书写
②
(1)首先判断阴、阳极,分析阳极材料是惰性电极还是活泼电极。
(2)再分析电解质水溶液的组成,找全离子并分阴离子、阳离子两组(不要忘记水溶液中的H+ 和OH
-)。
(3)然后排出阴、阳两极的放电顺序:
阴极:阳离子放电顺序:Ag+ >Fe3+ >Cu2+ >H+(酸)>Fe2+ >Zn2+ >H+(水)>Al3+ >Mg2+ >Na+ >Ca2+
>K+ 。
阳极:活泼电极>S2- >I- >Br- >Cl- >OH- >含氧酸根离子。
(4)分析电极反应,判断电极产物,写出电极反应式,要注意遵循原子守恒和电荷守恒。
(5)最后写出电解反应的总化学方程式或离子方程式,并注明“电解”条件。
【特别提醒】 阴极不管是什么材料,电极本身都不反应,一定是溶液(或熔融电解质)中的阳离子放电,
注意离子导体(电解质)是水溶液还是非水状态。 阳极材料不同,电极产物、电极反应式可能不同,最常
①
用、最重要的放电顺序为阳极:Cl->OH- ;阴极
②
:Ag+>Cu2+>H+ 。 电解水溶液时,K+ ~Al3+ 不可能
在阴极放电,即不可能用电解水溶液的方法得到K、Ca、Na、Mg、Al等金属。 书写电解池中的电极反
③
应式时,要以实际放电的离子表示,但书写总电解反应方程式时,弱电解质要写成分子式。 电解质溶
④
液中未参与放电的离子是否与放电后生成的离子发生反应(离子共存)。 要确保两极电子转移数目相同,
⑤
且注明条件“电解”。
⑥
4.判断电解后溶液酸、碱生成的方法
(1)若电解产物只有H2 ,而无O2 ,则阴极生成碱。
(2)若电解产物只有O2 ,而无H2 ,则阳极生成酸。
(3)若电解产物既有O2 ,又有H2 ,且二者物质的量之比为1 2,则实质是电解水,阳极生成酸,阴极生
成碱,最终溶液中无酸和碱生成。但溶液浓度可能变大。
∶
5.惰性电极电解电解质溶液后要恢复原电解质溶液的浓度,需加适量的某物质时,遵循“少什么加什么,
少多少加多少”的原则,所加物质可以是阴极与阳极产物的化合物。
6.分析电解过程的思维流程7.电化学计算中常用的三种方法
(1)根据总反应计算
先写出电极反应,再写出总反应,最后根据总反应列出比例式计算。
(2)根据电子守恒计算
用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电子
数
①
相等;
用于混合溶液中电解的分阶段计算。
(3)根据关系式计算
②
根据得失电子守恒建立起已知量与未知量之间的桥梁,构建计算所需的关系式。
如以电路中通过4 mol e- 为桥梁可构建以下关系式:
(式中M为金属,n为其离子的化合价数值)该
关系式具有总览电化学计算的作用和价值,熟记电极反应,灵活运用关系式便能快速解答常见的电化学计
算问题。
【变式演练】
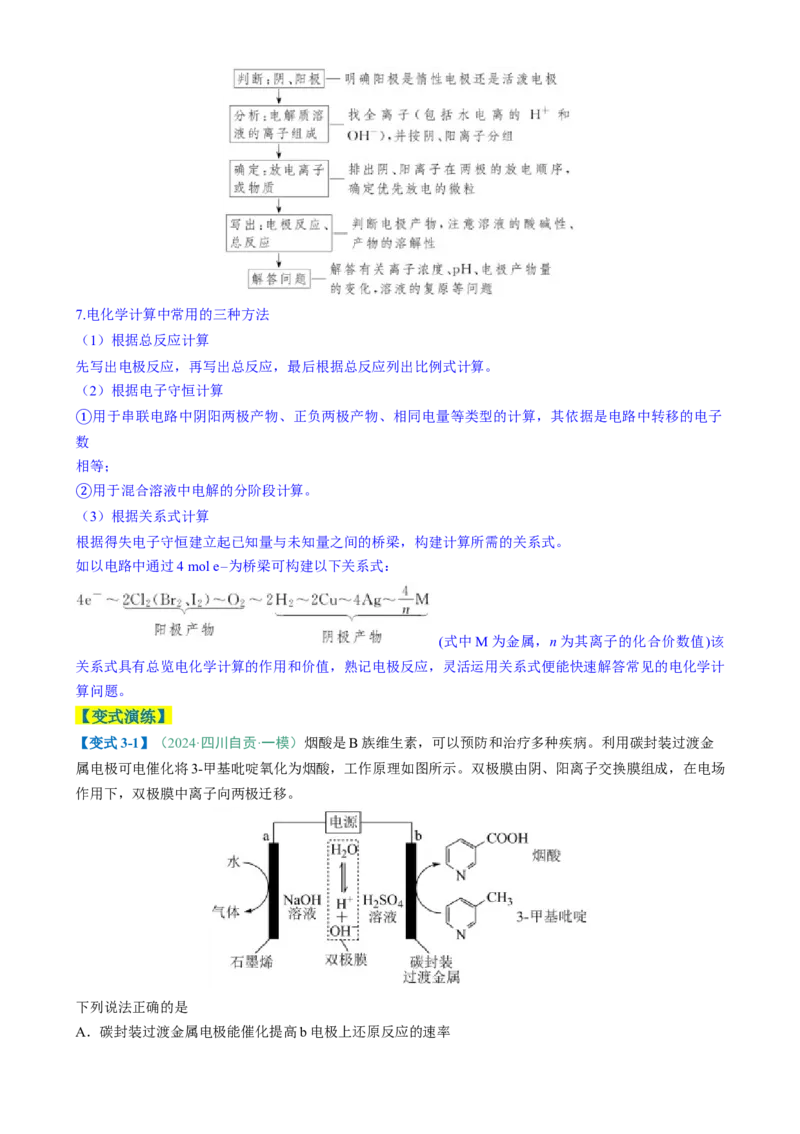
【变式3-1】(2024·四川自贡·一模)烟酸是B族维生素,可以预防和治疗多种疾病。利用碳封装过渡金
属电极可电催化将3-甲基吡啶氧化为烟酸,工作原理如图所示。双极膜由阴、阳离子交换膜组成,在电场
作用下,双极膜中离子向两极迁移。
下列说法正确的是
A.碳封装过渡金属电极能催化提高b电极上还原反应的速率B.该装置工作时,OH- 向a极移动
C.a极的电极反应式为2H2O+2e-=2OH-+H2↑
D.制备0.1mol烟酸时双极膜中质量减少3.6g
【答案】C
【分析】由题干图示信息可知,3-甲基吡啶转化为烟酸发生氧化反应,则b为电解池阳极,电极反应为:
-6e-+6OH-= +4H2O ,a为电解池阴极,电极反应为:2H2O+2e-=2OH-+H2↑,
据此分析解题。
【解析】A.由分析可知,b电极为阳极,阳极上发生氧化反应,即碳封装过渡金属电极能防止阳极电极
自身放电,提高b电极3-甲基吡啶转化为烟酸氧化反应的速率,A错误;B.由分析可知,a为电解池阴
极,b为电解池阳极,故该装置工作时,OH- 向b极移动,B错误;C.由分析可知,a极的电极反应式为
2H2O+2e-=2OH-+H2↑,C正确;D.由分析可知,制备烟酸的电极反应为: -6e-+6OH-=
+4H2O,制备0.1mol烟酸时转移电子为0.6mol,根据电子守恒可知,双极膜中有
0.6molOH- 移向阳极,0.6molH+ 移向阴极,即质量减少0.6mol×18g/mol=10.8g,D错误;故答案为:C。
【变式3-2】(2024·云南丽江·一模)通过电解废旧锂电池中的 可获得难溶性的 和 ,
电解示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略
不计)。下列说法正确的是
A.电极A为阳极,发生氧化反应
B.电极B的电极反应:4OH-+Mn2+-2e-=MnO2+2H2O
C.电解一段时间后溶液中 浓度减小
D.电解结束,可通过调节 除去 ,再加入 溶液以获得
【答案】D
【分析】由图可知,该装置为电解池,电极A为与直流电源负极相连的阴极,酸性条件下,LiMn2O4 在阴
极得到电子发生还原反应生成锰离子,电极反应式为 ,电极B为
阳极,水分子作用下,锰离子在阳极失去电子发生氧化反应生成二氧化锰和氢离子,电极反应式为2H2O+Mn2+-2e-=MnO2+4H+ ,则电解的总反应方程式为 。
【解析】A.由分析可知,电极B为阳极,发生氧化反应,A错误;B.由分析可知,电极B为阳极,电
极反应式为2H2O+Mn2+-2e-=MnO2+4H+ ,B错误;C.由分析可知,电解的总反应方程式为
,反应生成了 ,电解一段时间后,溶液中 浓度
增大,C错误;D.由分析可知,电解的总反应方程式为2LiMn2O4+4H+ 2Li++Mn2++3MnO2+2H2O,
电解结束后,可通过调节溶液pH将锰离子转化为沉淀除去,然后再加入碳酸钠溶液,从而获得碳酸锂,
D正确;故选D。
题组 04 依据电化学原理设计的组合式新型电化学装置分析
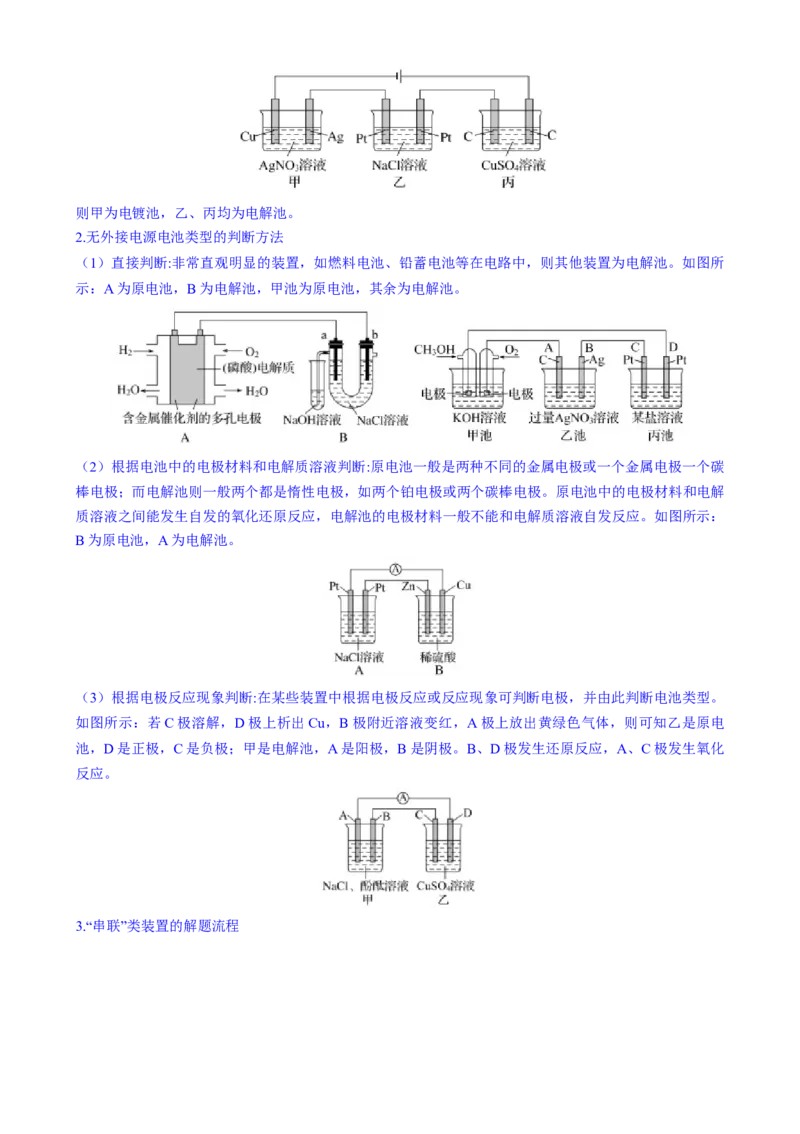
【例4-1】(2024·福建卷)一种兼具合成功能的新型锂电池工作原理如图。电解质为含 有机溶液。放
电过程中产生 ,充电过程中电解LiCl产生 。下列说法正确的是
A.交换膜为阴离子交换膜
B.电解质溶液可替换为LiCl水溶液
C.理论上每生成 ,需消耗2molLi
D.放电时总反应:
【答案】D
【分析】放电过程中产生 ,由图可知,放电过程中氮气得到电子发生还原反应生成Li3N,
Li3N又转化为 和LiCl,则左侧电极为正极,右侧电极为负极;
【解析】A.放电过程中负极锂失去电子形成锂离子,锂离子通过阳离子交换膜进入左侧生成
,A错误;B.锂为活泼金属,会和水反应,故电解质溶液不能为水溶液,B错误;C.充
电过程中电解LiCl失去电子发生氧化反应产生 : ,锂离子在阴极得到电子发生还原生
成锂单质: ,则每生成 ,同时生成2mol Li;放电过程中,消耗6mol Li,同时生成
4mol LiCl,则整个充放电过程来看,理论上每生成 ,需消耗1mol Li,C错误;D.由分析,放电过程中,正极氮气得到电子发生还原反应生成Li3N,Li3N又转化为 和LiCl,负极锂失去电
子发生氧化反应生成锂离子,总反应为 ,D正确;故选
D。
【例4-2】(2022·山东卷)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生
成 ,将废旧锂离子电池的正极材料 转化为 ,工作时保持厌氧环境,并定时将乙室溶液
转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为
D.若甲室 减少 ,乙室 增加 ,则此时已进行过溶液转移
【答案】BD
【分析】由于乙室中两个电极的电势差比甲室大,所以乙室是原电池,甲室是电解池,然后根据原电池、
电解池反应原理分析解答。
【解析】A.电池工作时,甲室中细菌上乙酸盐的阴离子失去电子被氧化为CO2 气体,同时生成H+ ,电
极反应式为CH3COO--8 e-+2 H2O =2CO2↑+7 H+ ,H+ 通过阳膜进入阴极室,甲室的电极反应式为Co2++2e-
=Co,因此,甲室溶液pH逐渐减小,A错误;B.对于乙室,正极上LiCoO2 得到电子,被还原为C
o2+ ,同时得到Li+ ,其中的O2- 与溶液中的H+ 结合H2O,电极反应式为2LiCoO2+2e-+8H+=2Li++2Co2+
+4H2O,负极发生的反应为CH3COO--8 e-+2 H2O =2CO2↑+7 H+ ,负极产生的H+ 通过阳膜进入正极室,但
是乙室的H+ 浓度仍然是减小的,因此电池工作一段时间后应该补充盐酸,B正确;C.电解质溶液为酸
性,不可能大量存在OH- ,乙室电极反应式为:LiCoO2+e-+4H+=Li++Co2++2H2O,C错误;D.若甲室
Co2+ 减少200 mg,则电子转移物质的量为n(e-)= ;若乙室Co2+ 增加300 mg,则转
移电子的物质的量为n(e-)= ,由于电子转移的物质的量不等,说明此时已进行过溶
液转移,即将乙室部分溶液转移至甲室,D正确;故合理选项是BD。
【提分秘籍】
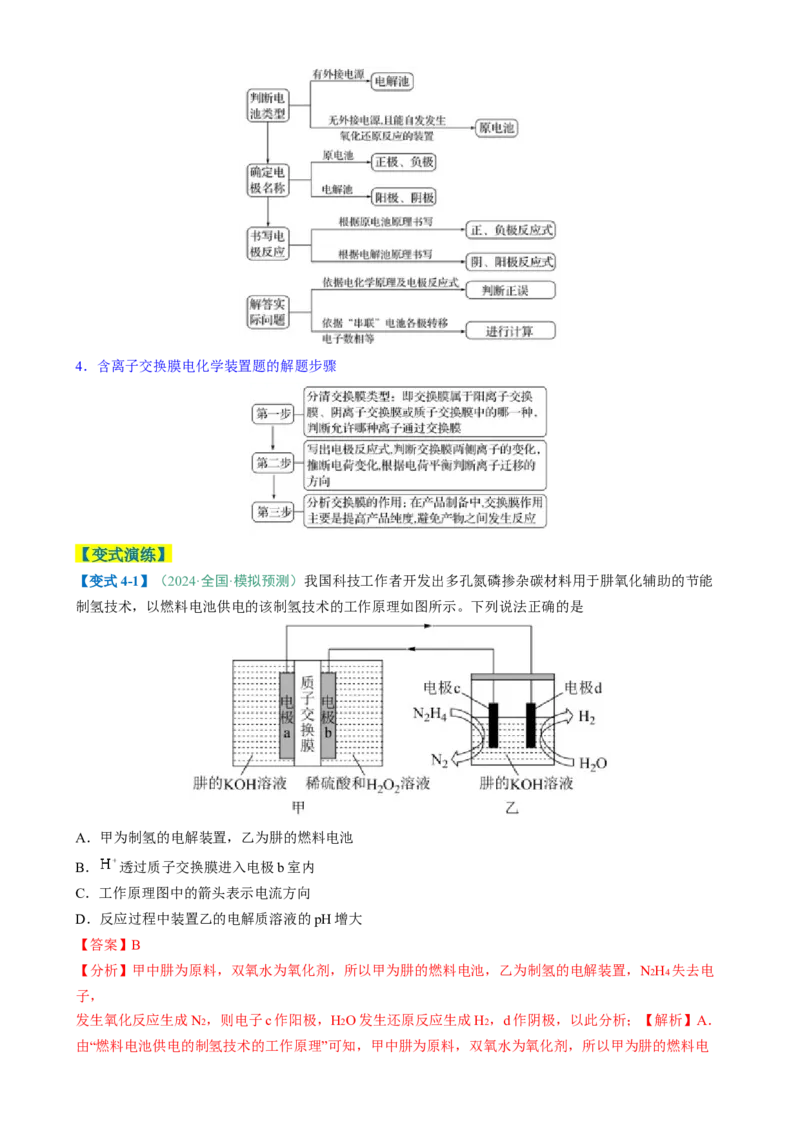
1.有外接电源电池类型的判断方法:有外接电源的各电池均为电解池,若电池阳极材料与电解质溶液中的
阳离子相同,则该电池为电镀池。如则甲为电镀池,乙、丙均为电解池。
2.无外接电源电池类型的判断方法
(1)直接判断:非常直观明显的装置,如燃料电池、铅蓄电池等在电路中,则其他装置为电解池。如图所
示:A为原电池,B为电解池,甲池为原电池,其余为电解池。
(2)根据电池中的电极材料和电解质溶液判断:原电池一般是两种不同的金属电极或一个金属电极一个碳
棒电极;而电解池则一般两个都是惰性电极,如两个铂电极或两个碳棒电极。原电池中的电极材料和电解
质溶液之间能发生自发的氧化还原反应,电解池的电极材料一般不能和电解质溶液自发反应。如图所示:
B为原电池,A为电解池。
(3)根据电极反应现象判断:在某些装置中根据电极反应或反应现象可判断电极,并由此判断电池类型。
如图所示:若C极溶解,D极上析出Cu,B极附近溶液变红,A极上放出黄绿色气体,则可知乙是原电
池,D是正极,C是负极;甲是电解池,A是阳极,B是阴极。B、D极发生还原反应,A、C极发生氧化
反应。
3.“串联”类装置的解题流程4.含离子交换膜电化学装置题的解题步骤
【变式演练】
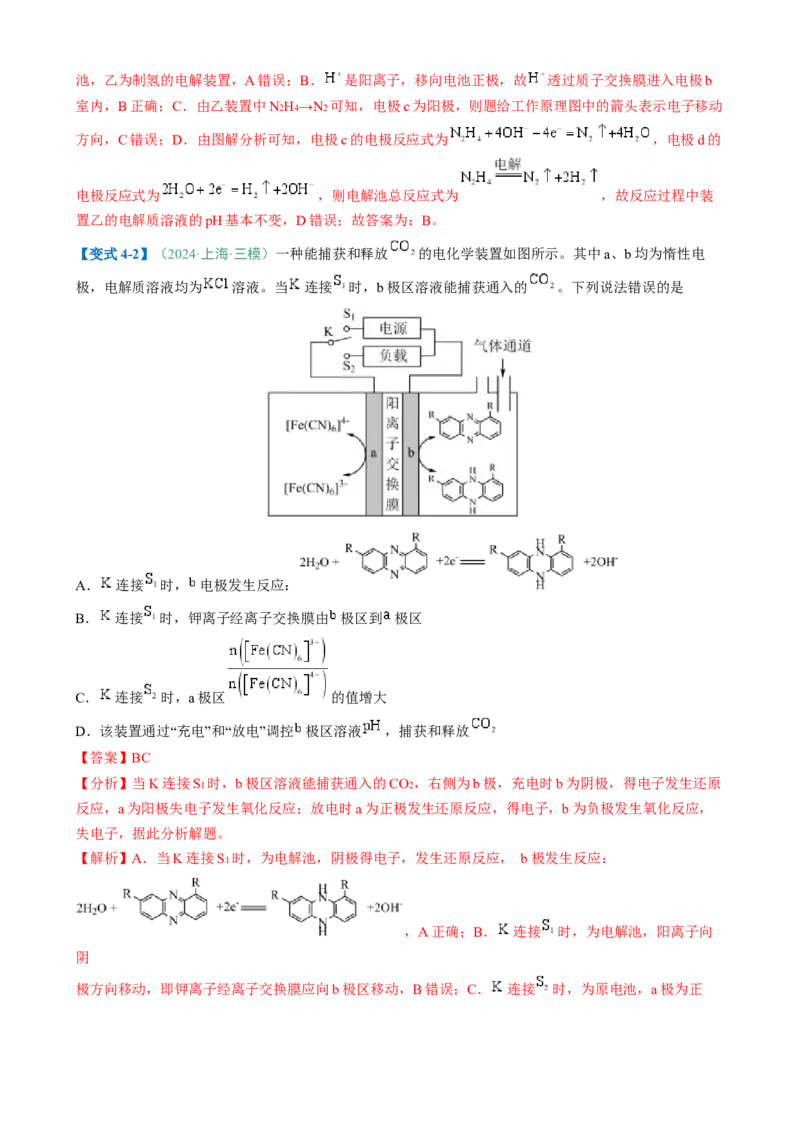
【变式4-1】(2024·全国·模拟预测)我国科技工作者开发出多孔氮磷掺杂碳材料用于肼氧化辅助的节能
制氢技术,以燃料电池供电的该制氢技术的工作原理如图所示。下列说法正确的是
A.甲为制氢的电解装置,乙为肼的燃料电池
B. 透过质子交换膜进入电极b室内
C.工作原理图中的箭头表示电流方向
D.反应过程中装置乙的电解质溶液的pH增大
【答案】B
【分析】甲中肼为原料,双氧水为氧化剂,所以甲为肼的燃料电池,乙为制氢的电解装置,N2H4 失去电
子,
发生氧化反应生成N2 ,则电子c作阳极,H2O发生还原反应生成H2 ,d作阴极,以此分析;【解析】A.
由“燃料电池供电的制氢技术的工作原理”可知,甲中肼为原料,双氧水为氧化剂,所以甲为肼的燃料电池,乙为制氢的电解装置,A错误;B. 是阳离子,移向电池正极,故 透过质子交换膜进入电极b
室内,B正确;C.由乙装置中N2H4→N2 可知,电极c为阳极,则题给工作原理图中的箭头表示电子移动
方向,C错误;D.由图解分析可知,电极c的电极反应式为 ,电极d的
电极反应式为 ,则电解池总反应式为 ,故反应过程中装
置乙的电解质溶液的pH基本不变,D错误;故答案为:B。
【变式4-2】(2024·上海·三模)一种能捕获和释放 的电化学装置如图所示。其中a、b均为惰性电
极,电解质溶液均为 溶液。当 连接 时,b极区溶液能捕获通入的 。下列说法错误的是
A. 连接 时, 电极发生反应:
B. 连接 时,钾离子经离子交换膜由 极区到 极区
C. 连接 时,a极区 的值增大
D.该装置通过“充电”和“放电”调控 极区溶液 ,捕获和释放
【答案】BC
【分析】当K连接S1 时,b极区溶液能捕获通入的CO2 ,右侧为b极,充电时b为阴极,得电子发生还原
反应,a为阳极失电子发生氧化反应;放电时a为正极发生还原反应,得电子,b为负极发生氧化反应,
失电子,据此分析解题。
【解析】A.当K连接S1 时,为电解池,阴极得电子,发生还原反应, b极发生反应:
,A正确;B. 连接 时,为电解池,阳离子向
阴
极方向移动,即钾离子经离子交换膜应向b极区移动,B错误;C. 连接 时,为原电池,a极为正极,发生还原反应,得电子, ,则a极区 减小,C错误;
D.该装置通过连接不同开关,实现“充电”和“放电”改变OH- 浓度以调控b极区溶液pH,捕获和释放
,D正确;答案选BC。
题组 05 依据电化学原理设计的金属腐蚀和防护电化学装置分析
【例5-1】(2024·浙江卷)金属腐蚀会对设备产生严重危害,腐蚀快慢与材料种类、所处环境有关。下图
为两种对海水中钢闸门的防腐措施示意图:
下列说法正确的是
A.图1、图2中,阳极材料本身均失去电子
B.图2中,外加电压偏高时,钢闸门表面可发生反应:
C.图2中,外加电压保持恒定不变,有利于提高对钢闸门的防护效果
D.图1、图2中,当钢闸门表面的腐蚀电流为零时,钢闸门、阳极均不发生化学反应
【答案】B
【解析】A.图1为牺牲阳极的阴极保护法,牺牲阳极一般为较活泼金属,其作为原电池的负极,其失去
电子被氧化;图2为外加电流保护法,阳极材料为辅助阳极,其通常是惰性电极,本身不失去电子,电解
质溶液中的阴离子在其表面失去电子,如海水中的 ,A不正确;B.图2中,外加电压偏高时,钢闸
门表面积累的电子很多,除了海水中的 放电外,海水中溶解的 也会竞争放电,故可发生
,B正确;C.图2为外加电流保护法,理论上只要能对抗钢闸门表面的腐蚀电流即
可,当钢闸门表面的腐蚀电流为零时保护效果最好;腐蚀电流会随着环境的变化而变化,若外加电压保持
恒定不变,则不能保证抵消腐蚀电流,不利于提高对钢闸门的防护效果,C不正确;D.图1当钢闸门表
面的腐蚀电流为零时,说明钢闸门被保护,钢闸门不发生化学反应,图2中当钢闸门表面的腐蚀电流为零
时,说明钢闸门被保护,辅助阳极上发生了氧化反应,D不正确;综上所述,本题选B。
【例5-2】(2020·江苏卷)将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题图所示
的情境中,下列有关说法正确的是A.阴极的电极反应式为
B.金属M的活动性比Fe的活动性弱
C.钢铁设施表面因积累大量电子而被保护
D.钢铁设施在河水中的腐蚀速率比在海水中的快
【答案】C
【分析】该装置为原电池原理的金属防护措施,为牺牲阳极的阴极保护法,金属M作负极,钢铁设备作
正极,据此分析解答。
【解析】A.阴极的钢铁设施实际作原电池的正极,正极金属被保护不失电子,故A错误;B.阳极金属M
实际为原电池装置的负极,电子流出,原电池中负极金属比正极活泼,因此M活动性比Fe的活动性强,
故B错误;C.金属M失电子,电子经导线流入钢铁设备,从而使钢铁设施表面积累大量电子,自身金属
不再失电子从而被保护,故C正确;D.海水中的离子浓度大于河水中的离子浓度,离子浓度越大,溶液
的导电性越强,因此钢铁设施在海水中的腐蚀速率比在河水中快,故D错误;故选:C。
【提分秘籍】
1、电化学腐蚀
(1)化学腐蚀和电化学腐蚀往往同时发生,只是电化学腐蚀比化学腐蚀更普遍,速率也大得多危害更
大。
(2)析氢腐蚀和吸氧腐蚀取决于金属表面电解质溶液的酸碱性,实际情况中以吸氧腐蚀为主。
(3)钢铁发生析氢腐蚀或吸氧腐蚀时,负极都是铁,失电子生成Fe2+ ,而非Fe3+ 。
2、电化学腐蚀的规律
(1)对同一种金属来说,其他条件相同时腐蚀的快慢:强电解质溶液>弱电解质溶液>非电解质溶液。
(2)活泼性不同的两金属:活泼性差别越大,活泼性强的金属腐蚀越快。
(3)对同一种电解质溶液来说,电解质溶液浓度越大,腐蚀越快,且氧化剂的浓度越高,氧化性越强,
腐蚀越快(钝化除外)。
(4)电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护措施的腐蚀。
3、金属的防护
1)改变金属材料的组成:在金属中添加其他金属或非金属制成性能优异的合金。如普通钢加入镍、铬制
成不锈钢,钛合金不仅具有优异的抗腐蚀性能且具有良好的生物相容性。
2)在金属表面覆盖保护层:在金属表面覆盖致密的保护层,将金属制品与周围物质隔开是一种普遍采用
的防护方法。在钢铁制品表面喷油漆、涂矿物性油脂、覆盖搪瓷等;电镀锌、锡、铬、镍等,利用化学方
法、
离子注入法、表面渗镀等方式在金属表面形成稳定的钝化膜。
3)电化学保护法:金属在发生电化学腐蚀时,总是作为原电池负极(阳极)的金属被腐蚀,作为正极(阴极)的金属不被腐蚀,如果能使被保护的金属成为阴极,就不易被腐蚀。
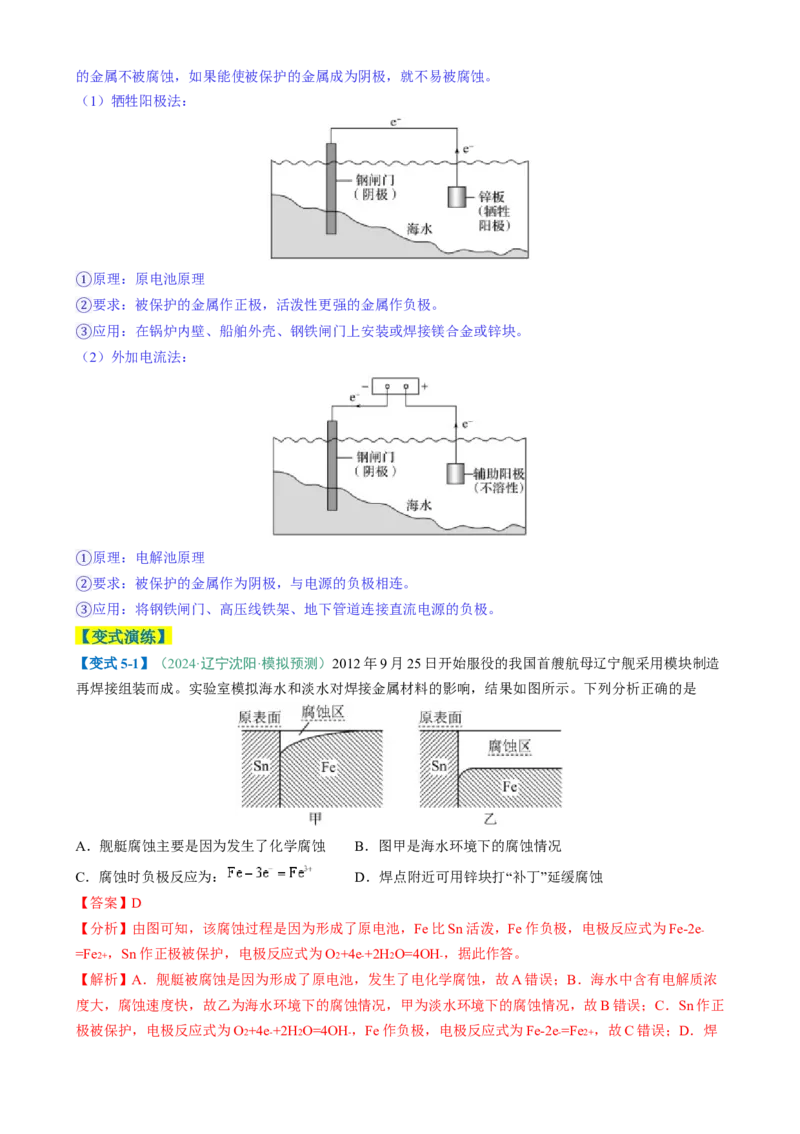
(1)牺牲阳极法:
原理:原电池原理
要求:被保护的金属作正极,活泼性更强的金属作负极。
①
应用:在锅炉内壁、船舶外壳、钢铁闸门上安装或焊接镁合金或锌块。
②
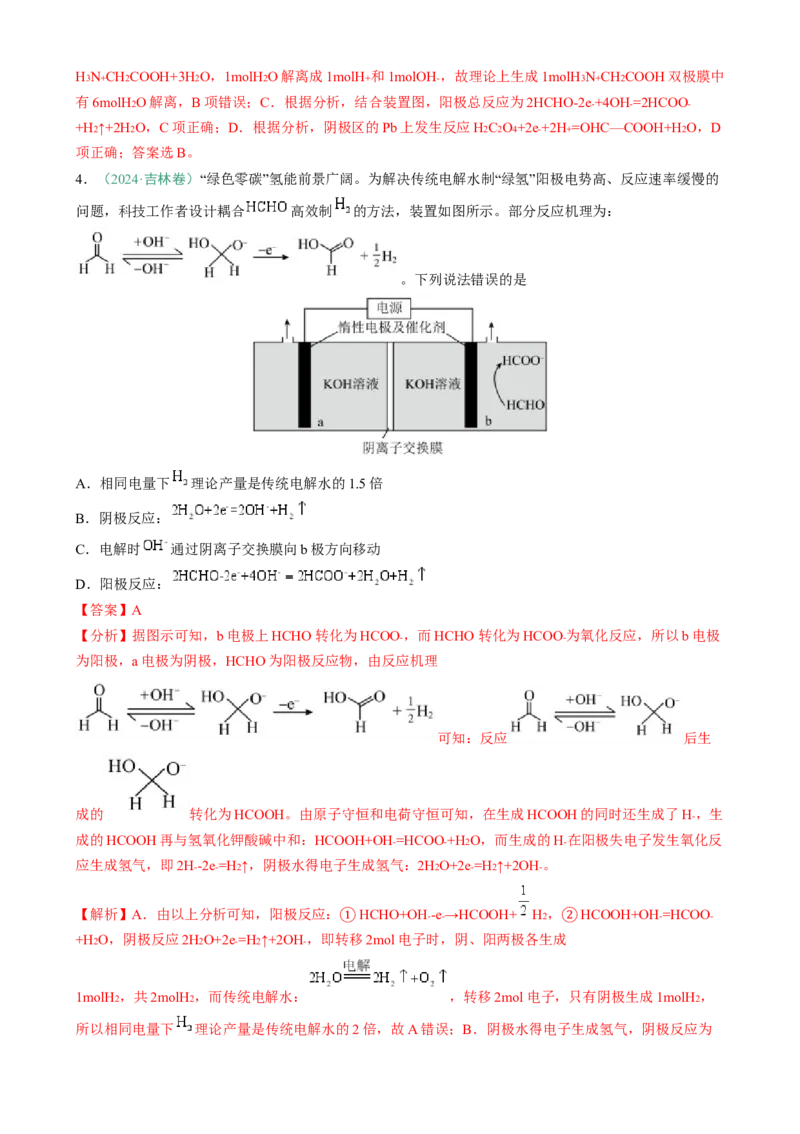
(2)外加电流法:
③
原理:电解池原理
要求:被保护的金属作为阴极,与电源的负极相连。
①
应用:将钢铁闸门、高压线铁架、地下管道连接直流电源的负极。
②
【变式演练】
③
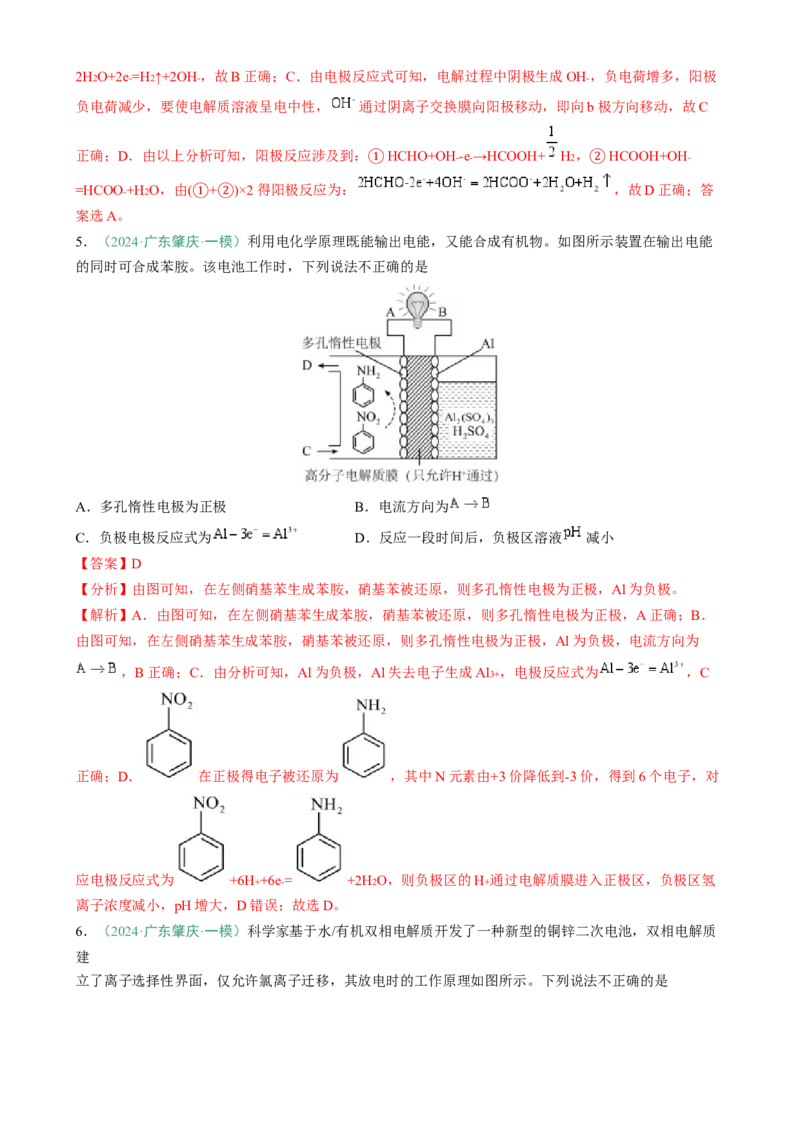
【变式5-1】(2024·辽宁沈阳·模拟预测)2012年9月25日开始服役的我国首艘航母辽宁舰采用模块制造
再焊接组装而成。实验室模拟海水和淡水对焊接金属材料的影响,结果如图所示。下列分析正确的是
A.舰艇腐蚀主要是因为发生了化学腐蚀 B.图甲是海水环境下的腐蚀情况
C.腐蚀时负极反应为: D.焊点附近可用锌块打“补丁”延缓腐蚀
【答案】D
【分析】由图可知,该腐蚀过程是因为形成了原电池,Fe比Sn活泼,Fe作负极,电极反应式为Fe-2e-
=Fe2+ ,Sn作正极被保护,电极反应式为O2+4e-+2H2O=4OH- ,据此作答。
【解析】A.舰艇被腐蚀是因为形成了原电池,发生了电化学腐蚀,故A错误;B.海水中含有电解质浓
度大,腐蚀速度快,故乙为海水环境下的腐蚀情况,甲为淡水环境下的腐蚀情况,故B错误;C.Sn作正
极被保护,电极反应式为O2+4e-+2H2O=4OH- ,Fe作负极,电极反应式为Fe-2e-=Fe2+ ,故C错误;D.焊点附近用锌块打“补丁”,Zn比Fe活泼,Zn作负极,Fe作正极被保护,可延缓腐蚀,故D正确;故选:
D。
【变式5-2】(2024·浙江·模拟预测)城镇地面下常埋有纵横交错的金属管道,当金属管道或铁轨在潮湿
土壤中形成电流回路时,就会引起这些金属制品的腐蚀。为了防止这类腐蚀的发生,某同学设计图所示的
装置。下列有关说法中正确的是
A.电流由 经过导线流向钢铁制品
B. 块表面随着时间的进行,会有 产生
C.钢铁管道与电源正极相连的保护法是外加电流保护法
D.应选用电阻率小的导体,比如 来避免能量损耗
【答案】B
【分析】钢铁输水管与镁块相连形成原电池,镁作负极,发生氧化反应被腐蚀,钢铁输水管作正极,受到
保护。
【解析】A.钢铁输水管与镁块相连形成原电池,镁作负极,发生氧化反应被腐蚀,钢铁输水管作正极,
电流由钢铁制品经过导线流向 ,A错误;B.由分可知,镁作负极,Mg失去电子生成Mg2+ ,Mg2+ 在
潮湿的环境中会水解转化为 ,B正确;C.Mg为活泼金属,可作为牺牲阳极,则将Mg与钢铁
输水管相连是用牺牲阳极法保护钢铁输水管,C错误;D.Fe比Ag活泼,若选用 作为导体,Ag与钢
铁制品形成原电池,钢铁制品作负极会被腐蚀,D错误;故选B。
1.(2024·四川自贡·一模)利用物质由高浓度向低浓度自发扩散的能量可制成浓差电池。在海水中的不
锈钢制品,缝隙处氧浓度比海水低,易形成浓差电池而发生缝隙腐蚀。缝隙处腐蚀的机理如图所示。下列
说法正确的是A.金属缝隙内表面为正极,外自由表面为负极
B.缝隙内溶液的pH增大,加快了缝隙内的腐蚀速率
C.为了维持电中性,海水中大量的 进入缝隙
D.正极的电极反应式为
【答案】C
【解析】A.根据氧气得电子发生还原反应生成氢氧根离子可知,金属缝隙外自由表面为正极,金属缝隙
内表面为负极,故A项错误;B.金属缝隙外自由表面为正极,生成氢氧根离子,缝隙外溶液的pH增
大,加快了缝隙内的腐蚀速率,故B项错误;C.阴离子由正极向负极移动·所以大量 进入缝隙来维持
电中性,故C项正确;D.正极为氧气得电子发生还原反应生成氢氧根离子,电极反应式
,故D项错误;故本题选C。
2.(2024·山东卷)以不同材料修饰的 为电极,一定浓度的 溶液为电解液,采用电解和催化相结
合的循环方式,可实现高效制 和 ,装置如图所示。下列说法错误的是
A.电极a连接电源负极
B.加入Y的目的是补充
C.电解总反应式为
D.催化阶段反应产物物质的量之比
【答案】B
【分析】电极b上Br- 发生失电子的氧化反应转化成 ,电极b为阳极,电极反应为Br- -6e-+3H2O=+6H+ ;则电极a为阴极,电极a的电极反应为2H2O+2e-=H2↑+2OH- ;电解总反应式为Br-+3H2O
+3H2↑;催化循环阶段 被还原成Br- 循环使用、同时生成O2 ,实现高效制H2 和O2 ,即Z为O2 。
【解析】A.根据分析,电极a为阴极,连接电源负极,A项正确;B.根据分析电解过程中消耗H2O和
Br- ,而催化阶段 被还原成Br- 循环使用,故加入Y的目的是补充H2O,维持NaBr溶液为一定浓度,
B项错误;C.根据分析电解总反应式为Br-+3H2O +3H2↑,C项正确;D.催化阶段,Br元素的
化合价由+5价降至-1价,生成1molBr- 得到6mol电子,O元素的化合价由-2价升至0价,生成1molO2 失
去4mol电子,根据得失电子守恒,反应产物物质的量之比n(O2) n(Br-)=6 4=3 2,D项正确;答案选B。
∶ ∶ ∶
3.(2024·湖北卷)我国科学家设计了一种双位点 电催化剂,用 和 电化学催化合成
甘氨酸,原理如图,双极膜中 解离的 和 在电场作用下向两极迁移。已知在 溶液中,甲
醛转化为 ,存在平衡 。 电极上发生的电子转移反应为
。下列说法错误的是
A.电解一段时间后阳极区 减小
B.理论上生成 双极膜中有 解离
C.阳极总反应式为
D.阴极区存在反应
【答案】B
【分析】在KOH溶液中HCHO转化为HOCH2O- :HCHO+OH-→HOCH2O- ,存在平衡HOCH2O-+OH-
[OCH2O]2-+H2O,Cu电极上发生的电子转移反应为[OCH2O]2--e-=HCOO-+H∙,H∙结合成H2 ,Cu电极为阳
极;PbCu电极为阴极,首先HOOC—COOH在Pb上发生得电子的还原反应转化为OHC—COOH:
H2C2O4+2e-+2H+=OHC—COOH+H2O,OHC—COOH与HO—N+H3 反应生成HOOC—CH=N—OH:OHC
—COOH+HO—N+H3→HOOC—CH=N—OH+H2O+H+ ,HOOC—CH=N—OH发生得电子的还原反应转化
成H3N+CH2COOH:HOOC—CH=N—OH+4e-+5H+=H3N+CH2COOH+H2O。
【解析】A.根据分析,电解过程中,阳极区消耗OH- 、同时生成H2O,故电解一段时间后阳极区c(OH-)
减小,A项正确;B.根据分析,阴极区的总反应为H2C2O4+HO—N+H3+6e-+6H+=H3N+CH2COOH+3H2O,1molH2O解离成1molH+ 和1molOH- ,故理论上生成1molH3N+CH2COOH双极膜中
有6molH2O解离,B项错误;C.根据分析,结合装置图,阳极总反应为2HCHO-2e-+4OH-=2HCOO-
+H2↑+2H2O,C项正确;D.根据分析,阴极区的Pb上发生反应H2C2O4+2e-+2H+=OHC—COOH+H2O,D
项正确;答案选B。
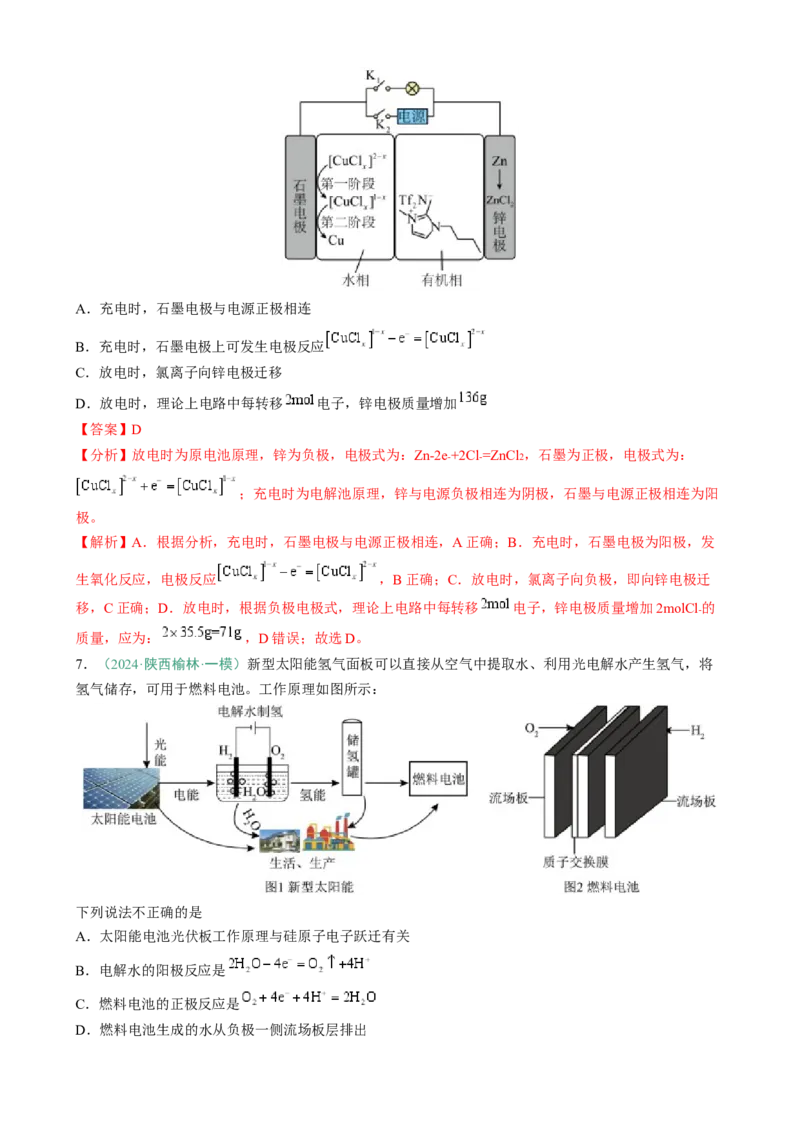
4.(2024·吉林卷)“绿色零碳”氢能前景广阔。为解决传统电解水制“绿氢”阳极电势高、反应速率缓慢的
问题,科技工作者设计耦合 高效制 的方法,装置如图所示。部分反应机理为:
。下列说法错误的是
A.相同电量下 理论产量是传统电解水的1.5倍
B.阴极反应:
C.电解时 通过阴离子交换膜向b极方向移动
D.阳极反应:
【答案】A
【分析】据图示可知,b电极上HCHO 转化为HCOO- ,而HCHO 转化为HCOO- 为氧化反应,所以b电极
为阳极,a电极为阴极,HCHO为阳极反应物,由反应机理
可知:反应 后生
成的 转化为HCOOH。由原子守恒和电荷守恒可知,在生成HCOOH的同时还生成了H- ,生
成的HCOOH再与氢氧化钾酸碱中和:HCOOH+OH-=HCOO-+H2O,而生成的H- 在阳极失电子发生氧化反
应生成氢气,即2H--2e-=H2↑,阴极水得电子生成氢气:2H2O+2e-=H2↑+2OH- 。
【解析】A.由以上分析可知,阳极反应: HCHO+OH--e-→HCOOH+ H2 , HCOOH+OH-=HCOO-
+H2O,阴极反应2H2O+2e-=H2↑+2OH- ,即转
①
移2mol电子时,阴、阳两极各生成
②
1molH2 ,共2molH2 ,而传统电解水: ,转移2mol电子,只有阴极生成1molH2 ,
所以相同电量下 理论产量是传统电解水的2倍,故A错误;B.阴极水得电子生成氢气,阴极反应为2H2O+2e-=H2↑+2OH- ,故B正确;C.由电极反应式可知,电解过程中阴极生成OH- ,负电荷增多,阳极
负电荷减少,要使电解质溶液呈电中性, 通过阴离子交换膜向阳极移动,即向b极方向移动,故C
正确;D.由以上分析可知,阳极反应涉及到: HCHO+OH--e-→HCOOH+ H2 , HCOOH+OH-
=HCOO-+H2O,由( + )×2得阳极反应为: ① ② ,故D正确;答
案选A。
① ②
5.(2024·广东肇庆·一模)利用电化学原理既能输出电能,又能合成有机物。如图所示装置在输出电能
的同时可合成苯胺。该电池工作时,下列说法不正确的是
A.多孔惰性电极为正极 B.电流方向为
C.负极电极反应式为 D.反应一段时间后,负极区溶液 减小
【答案】D
【分析】由图可知,在左侧硝基苯生成苯胺,硝基苯被还原,则多孔惰性电极为正极,Al为负极。
【解析】A.由图可知,在左侧硝基苯生成苯胺,硝基苯被还原,则多孔惰性电极为正极,A正确;B.
由图可知,在左侧硝基苯生成苯胺,硝基苯被还原,则多孔惰性电极为正极,Al为负极,电流方向为
,B正确;C.由分析可知,Al为负极,Al失去电子生成Al3+ ,电极反应式为 ,C
正确;D. 在正极得电子被还原为 ,其中N元素由+3价降低到-3价,得到6个电子,对
应电极反应式为 +6H++6e-= +2H2O,则负极区的H+ 通过电解质膜进入正极区,负极区氢
离子浓度减小,pH增大,D错误;故选D。
6.(2024·广东肇庆·一模)科学家基于水/有机双相电解质开发了一种新型的铜锌二次电池,双相电解质
建
立了离子选择性界面,仅允许氯离子迁移,其放电时的工作原理如图所示。下列说法不正确的是A.充电时,石墨电极与电源正极相连
B.充电时,石墨电极上可发生电极反应
C.放电时,氯离子向锌电极迁移
D.放电时,理论上电路中每转移 电子,锌电极质量增加
【答案】D
【分析】放电时为原电池原理,锌为负极,电极式为:Zn-2e-+2Cl-=ZnCl2 ,石墨为正极,电极式为:
;充电时为电解池原理,锌与电源负极相连为阴极,石墨与电源正极相连为阳
极。
【解析】A.根据分析,充电时,石墨电极与电源正极相连,A正确;B.充电时,石墨电极为阳极,发
生氧化反应,电极反应 ,B正确;C.放电时,氯离子向负极,即向锌电极迁
移,C正确;D.放电时,根据负极电极式,理论上电路中每转移 电子,锌电极质量增加2molCl- 的
质量,应为: ,D错误;故选D。
7.(2024·陕西榆林·一模)新型太阳能氢气面板可以直接从空气中提取水、利用光电解水产生氢气,将
氢气储存,可用于燃料电池。工作原理如图所示:
下列说法不正确的是
A.太阳能电池光伏板工作原理与硅原子电子跃迁有关
B.电解水的阳极反应是
C.燃料电池的正极反应是
D.燃料电池生成的水从负极一侧流场板层排出【答案】D
【分析】电解水时,阴极上水提供的氢离子得到电子发生还原反应,阳极上水通过的氢氧根离子失去电子
发生氧化反应;燃料电池中,通入氢气的一极为负极、发生氧化反应,通入氧气的一极为正极、发生还原
反应;
【解析】A.太阳能电池光伏板工作原理主要是光电效应,与硅原子电子跃迁有关,A正确;B.据分
析,电解水的阳极产生氧气,电极反应式是 ,B正确;C.燃料电池的正极上氧气
被还原,氢离子参与下,得电极反应式是 ,C正确;D.图2中负极方程式为H2-
2e-=2H+ ,,结合选项C,燃料电池生成的水从正极一侧流场板层排出,D不正确;选D。
8.(2023·广东卷)利用活性石墨电极电解饱和食盐水,进行如图所示实验。闭合 ,一段时间后
A.U型管两侧均有气泡冒出,分别是 和
B.a处布条褪色,说明 具有漂白性
C.b处出现蓝色,说明还原性:
D.断开 ,立刻闭合 ,电流表发生偏转
【答案】D
【分析】闭合 ,形成电解池,电解饱和食盐水,左侧为阳极,阳极氯离子失去电子生成氯气,电极反
应为2Cl-—2e-=Cl2↑,右侧为阴极,阴极电极反应为2H++2e-=H2↑,总反应为2NaCl+2H2O
2NaOH+H2↑+Cl2↑,据此解答。
【解析】A.根据分析,U型管两侧均有气泡冒出,分别是 和 ,A错误;B.左侧生成氯气,氯气
遇到水生成HClO,具有漂白性,则a处布条褪色,说明HClO具有漂白性,B错误;C.b处出现蓝色,
发生Cl2+2KI=I2+2KCl,说明还原性: ,C错误;D.断开 ,立刻闭合 ,此时构成氢氯燃料电
池,形成电流,电流表发生偏转,D正确;故选D。
9.(2024·湖南卷)在 水溶液中,电化学方法合成高能物质 时,伴随少量 生成,电解原
理如图所示,下列说法正确的是A.电解时, 向Ni电极移动
B.生成 的电极反应:
C.电解一段时间后,溶液pH升高
D.每生成 的同时,生成
【答案】B
【分析】由电解原理图可知,Ni电极产生氢气,作阴极,发生还原反应,电解质溶液为KOH水溶液,则
电极反应为: ;Pt电极 失去电子生成 ,作阳极,电极反应为:
,同时,Pt电极还伴随少量 生成,电极反应为:
。
【解析】A.由分析可知,Ni电极为阴极,Pt电极为阳极,电解过程中,阴离子向阳极移动,即 向
Pt电极移动,A错误;B.由分析可知,Pt电极 失去电子生成 ,电解质溶液为KOH水溶
液,电极反应为: ,B正确;C.由分析可知,阳极主要反应为:
,阴极反应为: ,则电解过程中发生的总反应主
要为: ,反应消耗 ,生成 ,电解一段时间后,溶液pH降
低,C错误;D.根据电解总反应: 可知,每生成1mol ,生成
0.5mol ,但Pt电极伴随少量 生成,发生电极反应: ,则生成1molH2 时
得到的部分电子由OH- 放电产生O2 提供,所以生成 小于0.5mol,D错误;故选B。
10.(2024·江西上饶·模拟预测)科学家成功研制出一种可在一分钟内完成充放电的超常性能铝离子电
池。该电池内部的 和有机阳离子构成电解质溶液,其放电工作原理如图所示。下列说法不正确的是A.放电时,铝为负极,石墨为正极
B.充电时, 向石墨电极移动
C.放电时,负极的电极反应式为
D.充电时,电子从石墨电极直接经导线流入铝电极,然后再经电解质溶液流回石墨电极
【答案】D
【分析】根据电池原理图可知,放电时铝电极为负极,石墨为正极;电解时铝电极为阴极,石墨为阳极。
【解析】A.放电时, 向负极移动,故铝为负极,石墨为正极,A项正确;B.充电时,铝为阴极,
石墨为阳极,阴离子向阳极移动,B项正确;C.放电时,负极上铝失电子结合 生成 ,发生
反应: ,C项正确;D.根据“电子不下水,离子不上岸”,电子不进入电解质溶
液,电解质溶液中是自由移动的离子导电,故充电时电子移动方向为:石墨电极→外加电源正极,外加电
源负极→铝电极,D项错误;答案选D。
11.(2024·浙江·模拟预测)一种清洁、低成本的氯碱工业双联装置工作原理如图所示,浓缩海水可以造
成溶液中离子浓度差异,使离子从高浓度区域向低浓度区域迁移,从而产生离子电流。下列说法不正确的
是
A.电极Y为负极,可以在X、Z电极上收集到H2
B.与传统氯碱工业相比,该双联装置的优点是可避免使用离子交换膜
C.装置Ⅱ中的电极质量每变化mg,装置I中可制得 LiCl
D.随着装置的运行,电极Z附近溶液的pH增大,电极W附近有白色沉淀出现
【答案】C
【分析】结合题干信息,装置Ⅰ为原电池,装置Ⅱ为电解池,装置Ⅰ中,Li+ 移向X电极,故X为正极,Y为负极;Z为阴极,W为阳极,X电极反应为2H++2e-=H2↑,W电极反应为Ag-e-=Ag+ ,生成的银离子
再发生Ag++Cl-=AgCl↓,Z电极反应为2H2O+2e-=H2↑+2OH- ,据此分析解答。
【解析】A.根据分析,电极Y为负极,可以在X、Z电极上收集到H2 ,故A正确;B.反应中,氯离子
生成氯化银,可以不使用离子交换膜,故与传统氯碱工业相比,该双联装置可避免使用离子交换膜,故B
正确;C.W电极反应为Ag-e-=Ag+ ,装置Ⅱ中的W电极质量每变化mg,该电极减少mg银,转移电子的
物质的量为 ,结合得失电子守恒,故装置I中X电极生成 LiCl,则装置I中可制得
LiCl,故C错误;D.Z电极反应为2H2O+2e-=H2↑+2OH- ,随着装置的运行,电极Z附近溶液的
pH增大,电极W反应为Ag-e-=Ag+ ,生成的银离子再发生Ag++Cl-=AgCl↓,故附近有白色沉淀出现,故D
正确;故选C。
12.(2024·湖北·一模)我国科研人员设计了一条从乳酸增值至丙氨酸的电化学转化路径,同时可以实现
废水的再利用,原理如图所示。已知:在外电场作用下,水分子会在双极膜的界面层解离为 和 。
下列说法错误的是
A.理论上将废水中 还原到羟胺 需转移 电子
B.阳极发生的反应为
C.阴极发生的反应为
D.双极膜在阳极区产生 ,阴极区产生
【答案】A
【分析】由图可知,在外电场作用下,左侧物质去氢发生氧化反应,则左侧电极为阳极,右侧电极为阴
极,据此分析解答。
【解析】A. 中N为+5价, 中N为-1价,理论上将 还原到羟胺 需转移6个电
子,题干中未说明 的物质的量,无法计算电子的转移数目,A错误;B.由分析可知,左侧为阳
极,发生的反应为 ,B正确;C.由分析可知,左侧
为阴极,发生的反应为 ,C正确;D.电解池
中,阳离子向阴极移动,阴离子向阳极移动,故双极膜在阳极区产生 ,阴极区产生 ,D正确;故选A。
13.(2024·全国·模拟预测)我国科技工作者开发出多孔氮磷掺杂碳材料用于肼氧化辅助的节能制氢技
术,以燃料电池供电的该制氢技术的工作原理如图所示。下列说法正确的是
A.甲为制氢的电解装置,乙为肼的燃料电池
B. 透过质子交换膜进入电极b室内
C.工作原理图中的箭头表示电流方向
D.反应过程中装置乙的电解质溶液的pH增大
【答案】B
【分析】甲中肼为原料,双氧水为氧化剂,所以甲为肼的燃料电池,乙为制氢的电解装置,N2H4 失去电
子,发生氧化反应生成N2 ,则电子c作阳极,H2O发生还原反应生成H2 ,d作阴极,以此分析;
【解析】A.由“燃料电池供电的制氢技术的工作原理”可知,甲中肼为原料,双氧水为氧化剂,所以甲为
肼的燃料电池,乙为制氢的电解装置,A错误;B. 是阳离子,移向电池正极,故 透过质子交换膜
进入电极b室内,B正确;C.由乙装置中N2H4→N2 可知,电极c为阳极,则题给工作原理图中的箭头表
示电子移动方向,C错误;D.由图解分析可知,电极c的电极反应式为
,电极d的电极反应式为 ,则电解池总反应式为 ,故反
应过程中装置乙的电解质溶液的pH基本不变,D错误;故答案为:B。
14.(2024·贵州卷)一种太阳能驱动环境处理的自循环光催化芬顿系统工作原理如图。光阳极发生反
应: , 。体系中 与Mn(Ⅱ)/Mn(Ⅳ)发生
反应产生的活性氧自由基可用于处理污水中的有机污染物。
下列说法错误的是
A.该芬顿系统能量转化形式为太阳能 电能 化学能
B.阴极反应式为C.光阳极每消耗 ,体系中生成
D. 在Mn(Ⅱ)/Mn(Ⅳ)的循环反应中表现出氧化性和还原性
【答案】C
【分析】该装置为电解池,光阳极上水失电子生成H2O2 和氢离子,电极反应式为
,阴极上氧气和氢离子得电子生成过氧化氢,电极反应式为
;
【解析】A.该装置为电解池,利用光能提供能量转化为电能,在电解池中将电能转化为化学能,A正
确;B.由图可知,阴极上氧气和氢离子得电子生成过氧化氢,电极反应式为 ,B
正确;C.光阳极上水失电子生成H2O2 和氢离子,电极反应式为 ,每转移2mol
电子生成 ,此时阴极也生成 : ,即光阳极每消耗1molH2O,体
系中生成 ,C错误;D.由Mn(Ⅳ)和过氧化氢转化为Mn(Ⅱ)过程中,锰元素化合价降低,
做还原剂,表现还原性,由Mn(Ⅱ)转化为Mn(Ⅳ)时, 中O元素化合价降低,做氧化剂,表现
氧化性,D正确;故选C。
15.(2024·广东卷)一种基于氯碱工艺的新型电解池(下图),可用于湿法冶铁的研究。电解过程中,下列
说法不正确的是
A.阳极反应:
B.阴极区溶液中 浓度逐渐升高
C.理论上每消耗 ,阳极室溶液减少
D.理论上每消耗 ,阴极室物质最多增加
【答案】C
【分析】左侧电极为阴极,发生还原反应, 在碱性条件下转化为Fe,从而实现冶铁,电极反应为:
;右侧电极为阳极,溶液为饱和食盐水, 放电产生氯气,电极反应
为: ;中间为阳离子交换膜, 由阳极向阴极移动。
【解析】A.由分析可知,阳极反应为: ,A正确;B.由分析可知,阴极反应为:
,消耗水产生 ,阴极区溶液中 浓度逐渐升高,B正确;C.由
分析可知,理论上每消耗 ,转移6mol电子,产生3mol ,同时有6mol 由阳极转移至阴极,则阳极室溶液减少 ,C错误;D.由分析可知,理论上每消耗 ,转移
6mol电子,有6mol 由阳极转移至阴极,阴极室物质最多增加 ,D正确;故选C。
16.(2024·全国·模拟预测)以KNO3 溶液为电解质溶液,利用双极膜电解器连续电合成NH3 的简化装置
如图所示。双极膜只允许 和 通过,且双极膜可促进H2O的电离。下列说法正确的是
A.阳极产生NH3 ,阴极产生O2
B.通电后 移向阴极
C.阳极需不断补充碱液
D.总反应:
【答案】B
【分析】本题以合成氨的双极膜电解器为载体考查电解池的工作原理,由N元素化合价的变化可知,阴
极电极反应式为 ,阳极电极反应式为 ,总反应
为 ,阳极产生O2 ,阴极产生NH3 。
【解析】A.由题干信息可知电解硝酸钾得到氨气,发生还原反应,所以阴极生成氨气,阳极水放电生成
氧气;A错误;B.在电解池中,通电后 (阳离子)移向阴极,B正确;C.阳极电极反应式为:
,因此阳极不需要补充碱液,C错误;D.选项中方程式未配平,总反应式应
为: ,D错误;故选B。
17.(2024·全国·模拟预测)某工业废水中主要含有 和 溶质,现采用电化学
方法对废水进行处理,同时达到回收 和氮肥的目的,其装置如图所示。已知双极膜在直流电场
的作用下会将复合层中的水解离成 和 。下列说法不正确的是A.阴极室产生的气体是
B.若电解过程中阳极室溶液体积不发生改变,则其pH始终保持不变
C.电解结束后,回收室中的物质可通过过滤操作进行分离
D.电解结束后,原料室中溶液为 和 的混合溶液
【答案】D
【分析】阴极室,氢离子放电产生氢气, ;硫酸根通过阴离子交换膜,铵根通过阳离子
交换膜,在回收室得到硫酸铵,原料室中氢离子通过双极膜,得到醋酸,阳极室,氢氧根放电
,生成氧气。
【解析】A.阴极室中发生得电子的还原反应,电极反应式为 ,产生的气体是 ,A正
确;B.阳极室中发生失电子的氧化反应,电极反应式为 ,每当有4mol 参
加反应,双极膜会解离出4mol 进行补充,所以若电解过程中阳极室溶液体积不发生改变,则其pH
始终保持不变,B正确;C.电解过程中,阴极室中的 通过阴离子交换膜迁移到回收室中,原料室中
的 和 通过阳离子交换膜迁移到回收室中,在回收室中得到难溶性 和易溶性 ,
所以回收室中的物质可以通过过滤操作进行分离,C正确;D.原料室中的 因阳离子交换膜和
双极膜的存在不能发生迁移,双极膜产生的 会与之结合生成 , 因阳离子交换膜的存在
不能迁移至原料室中,所以电解结束后,原料室溶液中一定有 ,可能含有剩余的
和 ,D错误;答案选D。
18.(2024·江西卷)我国学者发明了一种新型多功能甲醛﹣硝酸盐电池,可同时处理废水中的甲醛和硝
酸根离子(如图)。下列说法正确的是
A.CuAg电极反应为2HCHO+2H2O﹣4e
﹣
═2HCOO
﹣
+H2↑+2OH
﹣B.CuRu电极反应为 6H2O+8e
﹣
═NH3↑+9OH
﹣
C.放电过程中,OH 通过质子交换膜从左室传递到右室
﹣
D.处理废水过程中溶液pH不变,无需补加KOH
【答案】B
【分析】由原电池中电子移动方向可知,CuAg为负极,HCHO失去电子生成HCOO- 和H2 ,电极方程式
为:2HCHO+4OH-﹣2e
﹣
═2HCOO
﹣
+H2↑+2H2O,CuRu为正极, 得到电子生成NH3 ,电极方程式为:
6H2O+8e
﹣
═NH3↑+9OH
﹣
,以此解答。
【解析】A.由分析可知,CuAg为负极,HCHO失去电子生成HCOO- 和H2 ,根据得失电子守恒和电荷守
恒配平电极方程式为:2HCHO+4OH-﹣2e
﹣
═2HCOO
﹣
+H2↑+2H2O,A错误;B.由分析可知,CuRu为正
极, 得到电子生成NH3 ,根据得失电子守恒和电荷守恒配平电极方程式为: 6H2O+8e
﹣
═NH3↑+9OH
﹣
,B正确;C.质子交换膜只允许H+ 通过,C错误;D.由分析可知,负极电极方程式为:
2HCHO+4OH-﹣2e
﹣
═2HCOO
﹣
+H2↑+2H2O,正极电极方程式为: 6H2O+8e
﹣
═NH3↑+9OH
﹣
,总反应
为8HCHO+ 7OH-=NH3 +8HCOO-+4 H2↑+2H2O,处理废水过程中消耗OH- ,溶液pH减小,需补加
KOH,D错误;故选B。
19.(2023·广东卷)负载有 和 的活性炭,可选择性去除 实现废酸的纯化,其工作原理如图。下
列说法正确的是
A. 作原电池正极
B.电子由 经活性炭流向
C. 表面发生的电极反应:
D.每消耗标准状况下 的 ,最多去除
【答案】B
【分析】 在Pt得电子发生还原反应,Pt为正极,Ag失去电子与溶液中的Cl- 反应,Ag为负极。
【解析】A.由分析可知,Ag失去电子与溶液中的Cl- 反应生成AgCl,Ag为负极,A错误;B.电子由负
极 经活性炭流向正极 ,B正确;C.溶液为酸性,故 表面发生的电极反应为
,C错误;D.每消耗标准状况下 的 ,转移电子2mol,而 失去2mol电子,故最多去除
,D错误。故选B。
20.(2024·安徽卷)我国学者研发出一种新型水系锌电池,其示意图如下。该电池分别以 (局部
结构如标注框内所示)形成的稳定超分子材料和 为电极,以 和 混合液为电解质溶液。下列说法错误的是
A.标注框内所示结构中存在共价键和配位键
B.电池总反应为:
C.充电时,阴极被还原的 主要来自
D.放电时,消耗 ,理论上转移 电子
【答案】C
【分析】由图中信息可知,该新型水系锌电池的负极是锌、正极是超分子材料;负极的电极反应式为
,则充电时,该电极为阴极,电极反应式为 ;正极上发生 ,则充
电时,该电极为阳极,电极反应式为 。
【解析】A.标注框内所示结构属于配合物,配位体中存在碳碳单键、碳碳双键、碳氮单键、碳氮双键和
碳氢键等多种共价键,还有由 提供孤电子对、 提供空轨道形成的配位键,A正确;B.由以上分析
可知,该电池总反应为 ,B正确;C.充电时,阴极电极反应式为 ,
被还原的Zn2+ 主要来自电解质溶液,C错误;D.放电时,负极的电极反应式为 ,因此消耗
0.65 g Zn(物质的量为0.01mol),理论上转移0.02 mol电子,D正确;综上所述,本题选C。
21.(2024·广西卷)某新型钠离子二次电池(如图)用溶解了NaPF6 的二甲氧基乙烷作电解质溶液。放电时
嵌入PbSe中的Na变成Na+ 后脱嵌。下列说法错误的是
A.外电路通过1mol电子时,理论上两电极质量变化的差值为23g
B.充电时,阳极电极反应为:
C.放电一段时间后,电解质溶液中的Na+ 浓度基本保持不变
D.电解质溶液不能用NaPF6 的水溶液替换
【答案】A【分析】放电时嵌入PbSe中的Na变成Na+ 后脱嵌,则右侧电极为负极,Na失电子生成Na+ ;Na+ 透过允
许Na+ 通过的隔膜从右侧进入左侧,则左侧为正极。
【解析】A.外电路通过1mol电子时,负极有1molNa失电子生成Na+ 进入右侧溶液,溶液中有
1molNa+ 从右侧进入左侧,并与正极的Na3-xV2(PO4)3 结合,则理论上两电极质量变化的差值为2mol×23g/
mol=46g,A错误;B.充电时,左侧电极为阳极,Na3V2(PO4)3 失电子生成Na3-xV2(PO4)3 ,则阳极电极反
应为: ,B正确 ;C.放电一段时间后,负极产生的Na+ 的物
质的量与负极区通过隔膜进入左极区的Na+ 的物质的量相同,进入左极区的Na+ 与参加左侧正极反应的
Na+ 的物质的量相同,所以电解质溶液中的Na+ 浓度基本保持不变,C正确 ;D.Na能与水反应,所以电
解质溶液不能用NaPF6 的水溶液替换,D正确 ;故选 A。
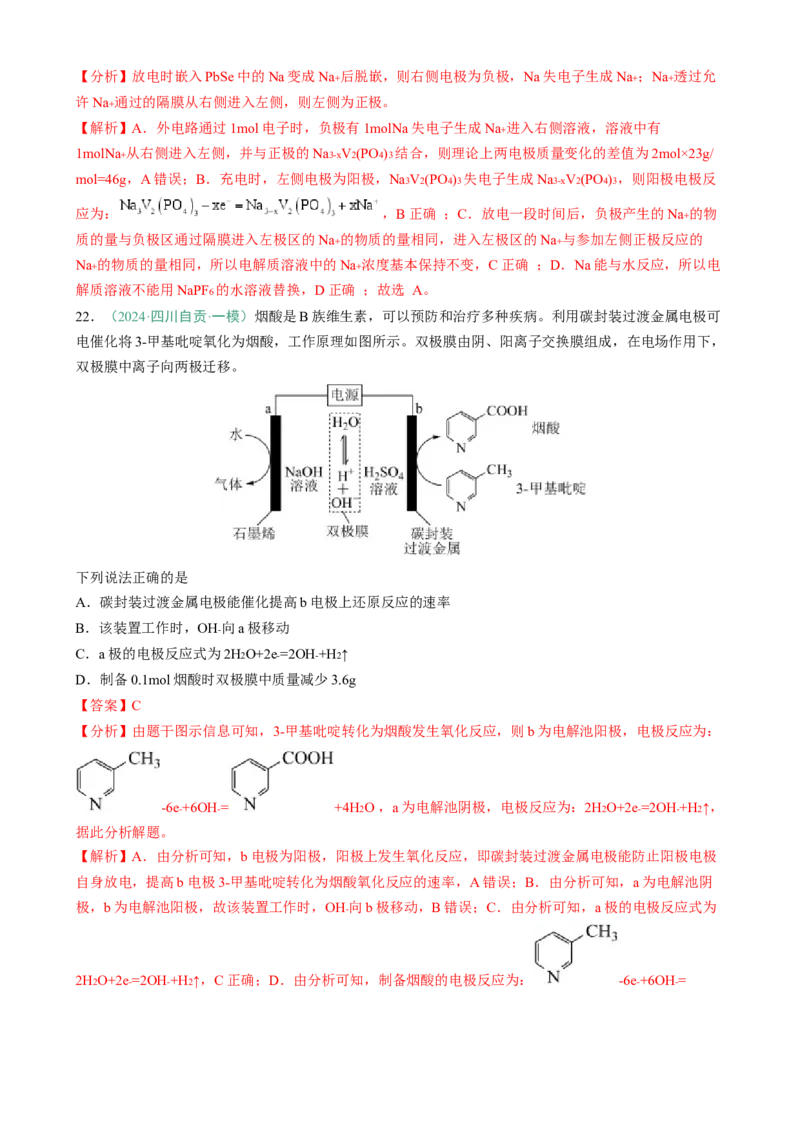
22.(2024·四川自贡·一模)烟酸是B族维生素,可以预防和治疗多种疾病。利用碳封装过渡金属电极可
电催化将3-甲基吡啶氧化为烟酸,工作原理如图所示。双极膜由阴、阳离子交换膜组成,在电场作用下,
双极膜中离子向两极迁移。
下列说法正确的是
A.碳封装过渡金属电极能催化提高b电极上还原反应的速率
B.该装置工作时,OH- 向a极移动
C.a极的电极反应式为2H2O+2e-=2OH-+H2↑
D.制备0.1mol烟酸时双极膜中质量减少3.6g
【答案】C
【分析】由题干图示信息可知,3-甲基吡啶转化为烟酸发生氧化反应,则b为电解池阳极,电极反应为:
-6e-+6OH-= +4H2O ,a为电解池阴极,电极反应为:2H2O+2e-=2OH-+H2↑,
据此分析解题。
【解析】A.由分析可知,b电极为阳极,阳极上发生氧化反应,即碳封装过渡金属电极能防止阳极电极
自身放电,提高b电极3-甲基吡啶转化为烟酸氧化反应的速率,A错误;B.由分析可知,a为电解池阴
极,b为电解池阳极,故该装置工作时,OH- 向b极移动,B错误;C.由分析可知,a极的电极反应式为
2H2O+2e-=2OH-+H2↑,C正确;D.由分析可知,制备烟酸的电极反应为: -6e-+6OH-=+4H2O,制备0.1mol烟酸时转移电子为0.6mol,根据电子守恒可知,双极膜中有
0.6molOH- 移向阳极,0.6molH+ 移向阴极,即质量减少0.6mol×18g/mol=10.8g,D错误;故答案为:C。