文档内容
题型 10 陌生反应机理图
依据陌生反应机理图命题的试题在近几年高考中频繁出现。题目主要以图示的形式来描述某一化学变
化所经历的全部反应,就是把一个复杂反应分解成若干个反应,然后按照一定规律组合起来,从而达到阐
述复杂反应的内在联系的目的。陌生反应机理图像一般取材于实际科研成果,充分体现了化学反应的本
质,高考常以此为载体考查反应原理、活化能、反应热、催化剂等知识,是近年高考的命题热点,由于陌
生度高,思维转化大,且命题视角在不断地创新和发展,成为大多数考生的失分点,这类试题难点是需要
学生能从陌生图像中提取有效信息进行解题,从机理类型不同,可将陌生反应机理图试题分为四个题组,
一是基元反应及反应历程机理分析的正误判断:二是能垒图、过渡态理论及其反应机理分析的正误判断;
三是催化剂、活化能及其反应机理分析的正误判断;四循环反应机理图像分析的正误判断。
题组 01 基元反应及反应历程机理分析的正误判断
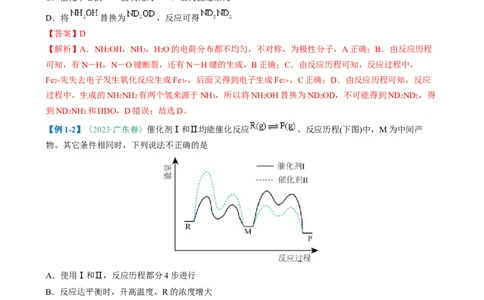
【例1-1】(2023·全国卷)“肼合成酶”以其中的 配合物为催化中心,可将 与 转化为肼(
),其反应历程如下所示。下列说法错误的是
A. 、 和 均为极性分子
B.反应涉及 、 键断裂和 键生成
C.催化中心的 被氧化为 ,后又被还原为
D.将 替换为 ,反应可得
【答案】D
【解析】A.NH2OH,NH3 ,H2O的电荷分布都不均匀,不对称,为极性分子,A正确;B.由反应历程
可知,有N-H,N-O键断裂,还有N-H键的生成,B正确;C.由反应历程可知,反应过程中,
Fe2+ 先失去电子发生氧化反应生成Fe3+ ,后面又得到电子生成Fe2+ ,C正确;D.由反应历程可知,反应
过程中,生成的NH2NH2 有两个氢来源于NH3 ,所以将NH2OH替换为ND2OD,不可能得到ND2ND2 ,得
到ND2NH2 和HDO,D错误;故选D。
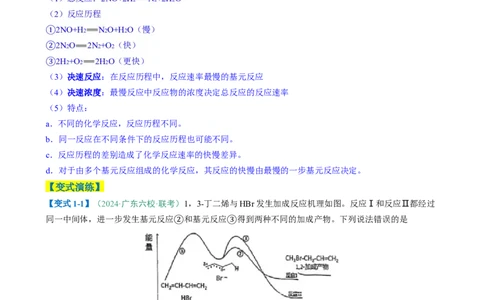
【例1-2】(2023·广东卷)催化剂Ⅰ和Ⅱ均能催化反应 。反应历程(下图)中,M为中间产
物。其它条件相同时,下列说法不正确的是
A.使用Ⅰ和Ⅱ,反应历程都分4步进行
B.反应达平衡时,升高温度,R的浓度增大
C.使用Ⅱ时,反应体系更快达到平衡
D.使用Ⅰ时,反应过程中M所能达到的最高浓度更大
【答案】C
【解析】A.由图可知两种催化剂均出现四个波峰,所以使用Ⅰ和Ⅱ,反应历程都分4步进行,A正确;
B.由图可知该反应是放热反应,所以达平衡时,升高温度平衡向左移动,R的浓度增大,B正确;C.
由图可知Ⅰ的最高活化能小于Ⅱ的最高活化能,所以使用Ⅰ时反应速率更快,反应体系更快达到平衡,C
错误;D.由图可知在前两个历程中使用Ⅰ活化能较低反应速率较快,后两个历程中使用Ⅰ活化能较高反
应速率较慢,所以
使用Ⅰ时,反应过程中M所能达到的最高浓度更大,D正确;故选C。【提分秘籍】
1.基元反应:
大多数的化学反应不能一步完成,在微观上是分几步完成的,这每一步反应都叫一个基元反应
如:反应H2O2 +2Br- +2H+===Br2 +2H2O,通过大量实验提出它们微观过程如下:
H+ +H2O2 H3O
①H3O +Br-===H2O+HOBr
②
HOBr+H+ +Br-===H2O+Br2
2.反应历程:
③
由基元反应构成的反应序列,又称反应机理。
(1)总反应:2NO+2H2 N2+2H2O
(2)反应历程
2NO+H2 N2O+H2O(慢)
①
2N2O 2N2+O2 (快)
②
2H2+O2 2H2O(更快)
(3)决速反应:在反应历程中,反应速率最慢的基元反应
③
(4)决速浓度:最慢反应中反应物的浓度决定总反应的反应速率
(5)特点:
a.不同的化学反应,反应历程不同。
b.同一反应在不同条件下的反应历程也可能不同。
c.反应历程的差别造成了化学反应速率的快慢差异。
d.对于由多个基元反应组成的化学反应,其反应的快慢由最慢的一步基元反应决定。
【变式演练】
【变式1-1】(2024·广东六校·联考)1,3-丁二烯与HBr发生加成反应机理如图。反应Ⅰ和反应Ⅱ都经过
同一中间体,进一步发生基元反应 和基元反应 得到两种不同的加成产物。下列说法错误的是
② ③
A.基元反应 H>0,基元反应 H<0
B.基元反应 相对于基元反应 为慢反应
①△ ②△
C.同一条件下,反应Ⅱ的倾向性比反应Ⅰ的倾向性大
③ ②
D.反应过程中,升高温度,1,2-加成产物的产率明显增加
【答案】D
【解析】A.根据反应机理图可知,基元反应 为吸热反应 H>0,基元反应 为放热反应 H<0,A正
① △ ② △确;
B.基元反应 活化能较大,反应速率较慢,所以基元反应 相对于基元反应 为慢反应,B正确;C.
根据
③
,反应可自发进行,两反应均为熵减
③
反应,反应Ⅰ为吸
②
热反应,反应Ⅱ为放热反
应,反应Ⅱ的倾向性比反应Ⅰ的倾向性大,C正确;D.根据反应机理图可知,1,2-加成反应活化能较
小,升高温度,对于1,2-加成反应产率影响较小,D错误;答案选D。
【变式1-2】(2024·云南大理·二模)某反应可有效降低汽车尾气污染物的排放,一定条件下该反应(均为
气体)经历三个基元反应阶段,反应历程如下图所示(TS表示过渡态)。下列说法错误的是
A.该过程包含一个吸热反应和两个放热反应
B.反应 逆反应的活化能为
C.该过②程的总反应为
D.反应 生成2mol 时,转移电子数为
【答案】D
③
【分析】从图中可得出三个热化学方程式:
反应 :2NO=N2O2 H1=+199.2kJ∙mol-1 ;
反应
①
:N2O2+CO=CO △2+N2O H2=-513.5kJ∙mol-1 ;
反应 ② :CO2+N2O+CO=2CO2+N △2 H3=-306.6kJ∙mol-1 据此分析解题。
【解析】A.由图可知,三个基元反应中,反应 和反应 的反应物总能量大于生成物的总能量,属于
③ △
放热反应, 属于吸热反应,A正确;B.正反应活化能减焓变值为逆应活化能,反应 逆反应的活化能
② ③
为130 kJ∙mo①l-1-(-513.5) kJ∙mol-1= ,B正确;C.利用盖斯定律,将反应 +② + 得,
H=+199.2kJ∙mol-1+(-513.5kJ∙mol-1)+ (-306.6
①
)kJ∙m
②
ol-1
③
]=
-620.9kJ∙mol-1 ,C正确;D.反应 :CO △2+N2O+CO=2CO2+N2 H3=--306.6kJ∙mol-1 ,根据反应式可知N
的化合价+1→0价,生成2mol ③时,转移电子数为 ,D错误△;故选D。
题组 02 能垒图、过渡态理论及其反应机理分析的正误判断
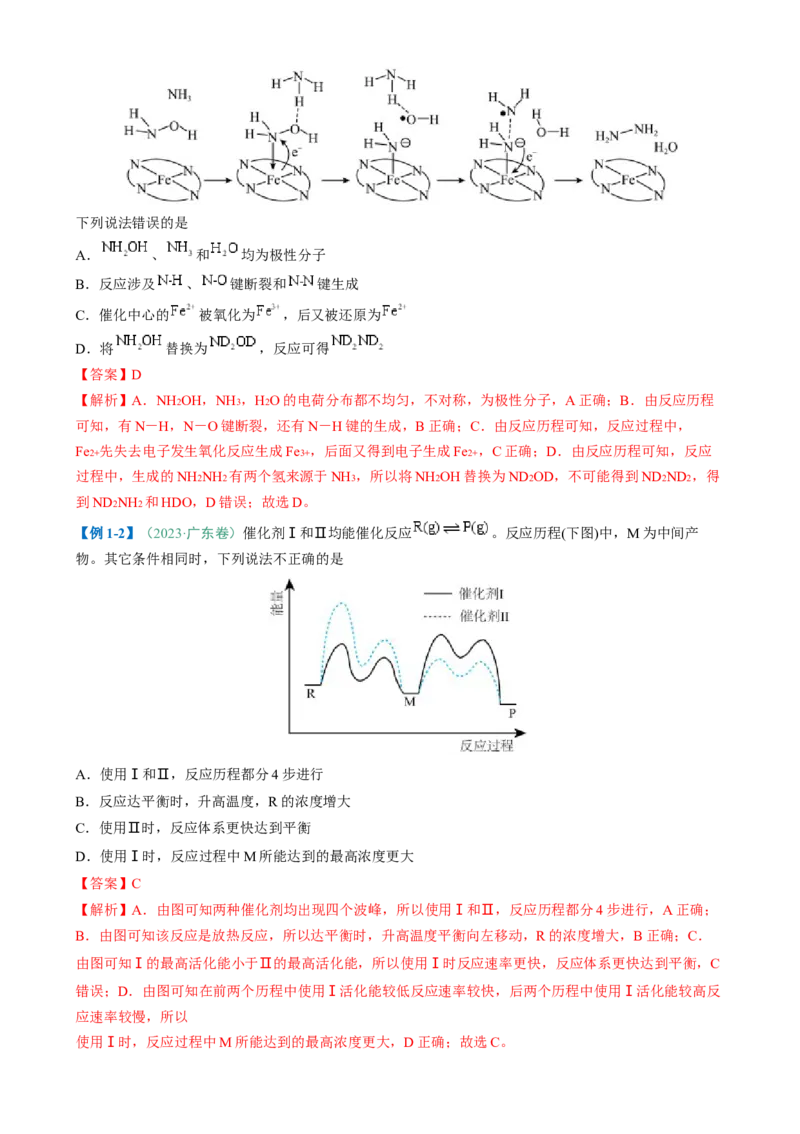
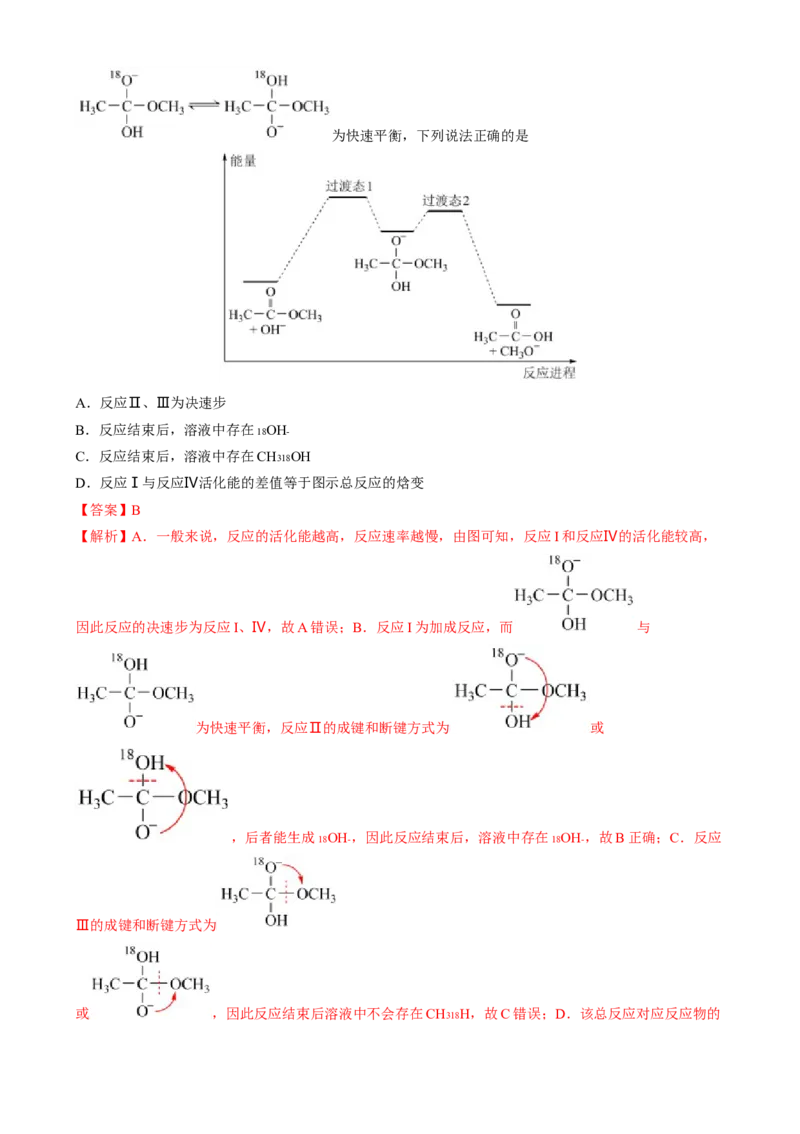
【例2-1】(2021·山东卷) 18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
能量变化如图所示。已知为快速平衡,下列说法正确的是
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在 18OH-
C.反应结束后,溶液中存在CH318OH
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
【答案】B
【解析】A.一般来说,反应的活化能越高,反应速率越慢,由图可知,反应I和反应Ⅳ的活化能较高,
因此反应的决速步为反应I、Ⅳ,故A错误;B.反应I为加成反应,而 与
为快速平衡,反应Ⅱ的成键和断键方式为 或
,后者能生成 18OH- ,因此反应结束后,溶液中存在 18OH- ,故B正确;C.反应
Ⅲ的成键和断键方式为
或 ,因此反应结束后溶液中不会存在CH318H,故C错误;D.该总反应对应反应物的总能量高于生成物总能量,总反应为放热反应,因此 和CH3O- 的总能量与
和OH- 的总能量之差等于图示总反应的焓变,故D错误;综上所述,正确的是B项,故
答案为B。
【例2-2】(2024·贵州卷)AgCN与 可发生取代反应,反应过程中 的C原子和N原子均可
进攻 ,分别生成腈 和异腈 两种产物。通过量子化学计算得到的反应
历程及能量变化如图(TS为过渡态,Ⅰ、Ⅱ为后续物)。
由图示信息,下列说法错误的是
A.从 生成 和 的反应都是放热反应
B.过渡态TS1是由 的C原子进攻 的 而形成的
C.Ⅰ中“ ”之间的作用力比Ⅱ中“ ”之间的作用力弱
D.生成 放热更多,低温时 是主要产物
【答案】D
【解析】A.由反应历程及能量变化图可知,两种路径生成的产物的总能量均低于反应物,故从
生成 和 的反应都是放热反应,A项正确;B.与Br原子相连的C原子为
,由反应历程及能量变化图可知,过渡态TS1是由CN- 的C原子进攻 的 ,形成碳碳键,
B项正确;C.由反应历程及能量变化图可知,后续物Ⅰ、Ⅱ转化为产物,分别断开的是 和
,且后者吸收更多的能量,故Ⅰ中“ ”之间的作用力比Ⅱ中“ ”之间的作用力弱,C项正确;
D.由于生成 所需要的活化能高,反应速率慢,故低温时更容易生成 ,为主要产
物,D项错误;故选D。
【提分秘籍】
1.过渡态理论
过渡态理论认为,反应物分子并不只是通过简单碰撞直接形成产物,而是必须经过一个形成活化络合物的
过渡状态,并且达到这个过渡状态需要一定的活化能,再转化成生成物。这与爬山类似,山的最高点便是
过渡态。2.基元反应过渡状态理论
(1)基元反应过渡状态理论认为,基元反应在从反应物到产物的变化过程中要经历一个中间状态,这个
状态称为过渡态
AB+C―→[A…B…C]―→A+BC
反应物 过渡态 产物
(2)过渡态是处在反应过程中具有最高能量的一种分子构型,过渡态能量与反应物的平均能量的差值相
当于活化能。如:一溴甲烷与NaOH溶液反应的历程可以表示为:
CH3Br+OH-―→[Br…CH3…OH]―→Br- +CH3OH
反应物 过渡态 产物
3.多步反应的活化能及与速率的关系
(1)多步反应的活化能:一个化学反应由几个基元反应完成,每一个基元反应都经历一个过渡态,及达
到该过渡态所需要的活化能(如图E1 、E2),而该复合反应的活化能只是由实验测算的表观值,没有实际物
理意义。
(2)活化能和速率的关系:基元反应的活化能越大,反应物到达过渡态就越不容易,该基元反应的速率
就越慢。一个化学反应的速率就取决于速率最慢的基元反应。
(3)能垒(活化能):即反应物状态达到活化状态所需能量。根据变换历程的相对能量可知,最大差值
为:其最大能垒(活化能)
(4)在钯基催化剂表面上,甲醇制氢( )的反应历程如下图所示,其中吸
附在钯催化剂表面上的物种用*标注.该历程中最大能垒(活化能) 179.6 ,该步骤的基元反应方程式为
(5)曲线上的峰
峰的个数表示中间反应的个数,不一定表示中间产物的种类
峰谷
①
a.峰前的峰谷:表示该中间反应反应物的能量
②
b.峰后的峰谷:表示该中间反应生成物的能量
4.突破能量变化的能垒图
(1)通览全图,理清坐标的含义。能量变化的能垒图的横坐标一般表示反应的历程,横坐标的不同阶段
表示一个完整反应的不同阶段。纵坐标表示能量的变化,不同阶段的最大能垒即该反应的活化能;
(2)细看变化,分析各段反应。仔细观察曲线(直线)的变化趋势,分析每一阶段发生的反应是什么,各
段反应是放热还是吸热,能量升高的为吸热,能量下降的为放热;
(3)综合分析,做出合理判断。综合整合各项信息,回扣题目要求,做出合理判断。如利用盖斯定律将
各步反应相加,即得到完整反应;催化剂只改变反应的活化能,但不改变反应的反应热,也不会改变反应
的转化律。
【变式演练】
【变式2-1】(2024·江西景德镇·二模)一定温度下,反应 的机理
第1步为 ,理论计算后续步骤可能的反应机理如图所示,TS1和TS2表示过渡态。下列说法错
误的是
A.该反应的 B.机理a、b均表示2步基元反应
C.机理a、b决速步的能垒: D.由机理a可知键能大小:Cl-SiH-Si,D错误;故选D。
【变式2-2】(2024·四川自贡·一模)碳酸二甲酯 是一种低毒、性能优良的有机合
成中间体,科学家提出了新的合成方案(吸附在固体催化剂表面上的物种用*标注),反应机理如图所
示。
下列说法正确的是
A.反应过程中除固体催化剂外,还使用了 做催化剂
B.反应进程中决速步骤的能垒为
C.第3步的基元反应方程式为:
D.升高温度,合成碳酸二甲酯反应速率增加,平衡向逆反应方向移动
【答案】A
【解析】A.HO·在反应前参与反应,反应后又生成,作催化剂,A正确;B.反应进程中经过渡态Ⅰ的
反应
能垒最大,是决速步骤,其能垒为[103.1-(-22.6)]×102eV=1.257×104eV,B错误;C.第3步的基元反应方
程式为: ,C错误;D.由图可以看出,
2CH3OH+CO2→CH3OCOOCH3+H2O H>0,升高温度,合成碳酸二甲酯反应速率增加,平衡向正反应方
向移动,D错误;故答案为:A。
△
题组 03 催化剂、活化能及其反应机理分析的正误判断
【例3-1】(2024·甘肃卷)甲烷在某含 催化剂作用下部分反应的能量变化如图所示,下列说法错误的
是A. B.步骤2逆向反应的
C.步骤1的反应比步骤2快 D.该过程实现了甲烷的氧化
【答案】C
【解析】A.由能量变化图可知, ,A项正确;B.由能量变化图可知,步骤
2逆向反应的 ,B项正确;C.由能量变化图可知,步骤1的活化能
,步骤2的活化能 ,步骤1的活化能大于步骤2的活化能,步骤
1的反应比步骤2慢,C项错误;D.该过程甲烷转化为甲醇,属于加氧氧化,该过程实现了甲烷的氧
化,D项正确;故选C。
【例3-2】(2024·安徽卷)某温度下,在密闭容器中充入一定量的 ,发生下列反应:
, ,测得各气体浓度与反应时间的关系如图所示。下列反应进
程示意图符合题意的是
A. B. C. D.
【答案】B
【分析】由图可知,反应初期随着时间的推移X的浓度逐渐减小、Y和Z的浓度逐渐增大,后来随着时
间的推移X和Y的浓度逐渐减小、Z的浓度继续逐渐增大,说明X(g) Y(g)的反应速率大于Y(g) Z(g)
的反应速率,则反应X(g) Y(g)的活化能小于反应Y(g) Z(g)的活化能。
【解析】A.X(g) Y(g)和Y(g) Z(g)的∆H都小于0,而图像显示Y的能量高于X,即图像显示X(g)
Y(g)为吸热反应,A项不符合题意;B.图像显示X(g) Y(g)和Y(g) Z(g)的∆H都小于0,且X(g)Y(g)的活化能小于Y(g) Z(g)的活化能,B项符合题意;C.图像显示X(g) Y(g)和Y(g) Z(g)的
∆H都小于0,但图像上X(g) Y(g)的活化能大于Y(g) Z(g)的活化能,C项不符合题意;D.图像显示
X(g) Y(g)和Y(g) Z(g)的∆H都大于0,且X(g) Y(g)的活化能大于Y(g) Z(g)的活化能,D项不符
合题意;选B。
【提分秘籍】
1.催化剂:存在少量就能显著改变反应速率,反应结束时,其自身的质量、组成和化学性质基本不变的物
质。
2.催化特点:
高效性,可以大大地加快反应速率。
选择性,反应不同,催化剂不同。
①
同等程度地加快正、逆反应的速率。
②
不能改变反应的可能性和平衡常数。
③
3.催化剂的催化机理:
④
催化剂的催化过程一般是催化剂跟其中的一种反应物首先发生反应,生成过渡物,然后再跟另外的反应物
反应,生成产物,同时催化剂重新生成。催化剂生成的过渡物比没有催化剂生成的过渡物的能量要低,因
而使反应更加容易发生和进行。这就是改变了其反应历程。即催化剂参与化学反应,生成能量更低的中间
产物,降低了达到过渡态所需要的活化能,使反应易于发生,速率加快。这就是我们经常说的催化剂改变
反应途径,降低反应的活化能。
4.催化剂与活化能、焓变
催化剂能降低反应所需活化能,化学反应速率加快,但不影响焓变∆H的大小,不影响平衡。
5.活化能
(1)正反应的活化能:反应物到最高点的能量差Ea正 =E1kJ·mol-1
(2)逆反应的活化能:生成物到最高点的能量差Ea逆 =E2kJ·mol-1
(3)活化能和反应热的关系
放热反应:Ea正 <Ea逆
①吸热反应:Ea正 >Ea逆
(4)活化能和反应速率的关系
②
关系:活化能越大,反应速率越慢
决速反应:活化能最大的反应或速率最慢的反应
①
决速浓度:最慢反应中反应物的浓度决定总反应的反应速率
②
【变式演练】
③
【变式3-1】(2024·广东广州·三模)基于非金属原子嵌入石墨烯三嗪基 中,用于催化一氧化碳加氢
生成甲醇的反应历程如图,其中吸附在催化剂表面上的物种用“ ”标注,下列说法中错误的是
A.整个反应历程中有极性键的断裂和生成
B.过渡态相对能量:TS55>TS44>TS77
C.物种吸附在催化剂表面的过程为吸热过程
D.反应决速步的活化能为
【答案】C
【解析】A.由图可知,一氧化碳催化加氢生成甲醇的反应中有极性键的断裂和生成,故A正确;B.由
图可知,过渡态相对能量的大小顺序为TS55>TS44>TS77,故B正确;C.由图可知,吸附在催化剂表面
的生
成物总能量低于反应物的总能量,为放热过程,故C错误;D.反应的活化能越大,反应速率越慢,反应
决速步为慢反应,由图可知,反应H2CO*+H =H3CO-H 的活化能最大,反应速率最慢,则反应决速步的
活化能为0.35eV—(—0.60eV)=0.95eV,故D正确;故选C。
【变式3-2】(24-25高三上·湖南·开学考试)近日,中国科学院化学研究所韩布兴院士/康欣晨研究员课题
组使用原子分散的Fe-N-C材料为催化剂,以草酸和硝酸盐或氮氧化物为原料(N2 和CO2 分别为氮源和碳
源),进行了电催化C-N偶联制备甘氨酸。原理如图所示(OA为HOOC-COOH,GX为HOOC-CHO,GC
为HOOC-CH2OH)。下列叙述正确的是A.活化能:反应ⅱ>反应ⅲ
B.在阳极区生成甘氨酸
C.OA→GX反应式为
D.反应ⅳ的原子利用率等于100%
【答案】C
【解析】A.活化能越小,反应越快,活化能:反应ⅱ<反应ⅲ,A项错误;B.以草酸和硝酸盐为原料合
成H2NCH2COOH中,C、N的化合价都降低,发生了还原反应,故甘氨酸在阴极区生成,B项错误;C.
根据题图可知,OA生成GX,同时有水生成,C项正确;D.反应ⅳ为
,原子利用率小于100%,D项错误;故答案选C。
题组 04 循环反应机理图像分析的正误判断
【例4-1】(2022·北京卷)CO2 捕获和转化可减少CO2 排放并实现资源利用,原理如图1所示。反应 完
成之后,以N2 为载气,以恒定组成的N2 、CH4 混合气,以恒定流速通入反应器,单位时间流出气体各
①
组
分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到CO2 ,在催化剂上有积碳。
下列说法不正确的是
A.反应 为CaO+CO2=CaCO3 ;反应 为CaCO3+CH4 CaO+2CO+2H2
① ②
B.t1~t3 ,n(H2)比n(CO)多,且生成H2 速率不变,可能有副反应CH4 C+2H2
C.t2 时刻,副反应生成H2 的速率大于反应 生成H2 速率
D.t3 之后,生成CO的速率为0,是因为反
②
应 不再发生
【答案】C
②
【解析】A.由题干图1所示信息可知,反应 为CaO+CO2=CaCO3 ,结合氧化还原反应配平可得反应
① ②为 ,A正确;B.由题干图2信息可知,t1~t3 ,n(H2)比n(CO)多,且生
成H2 速率不变,且反应过程中始终未检测到CO2 ,在催化剂上有积碳,故可能有副反应
,反应 和副反应中CH4 和H2 的系数比均为1:2,B正确;C.由题干反应 方程式
可知,H2 和CO的反应速率
②
相等,而t2 时刻信息可知,H2 的反应速率未变,仍然为2mmol/min
②
,而CO变
为1~2mmol/min之间,故能够说明副反应生成H2 的速率小于反应 生成H2 速率,C错误;D.由题干图
2信息可知,t3 之后,CO的速率为0,CH4 的速率逐渐增大,最终
②
恢复到1,说明生成CO的速率为0,是
因为反应 不再发生,而后副反应逐渐停止反应,D正确;答案选C。
【例4-2】②(2023·湖南卷) 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科
学家合成的某 (Ⅱ)催化剂(用 表示)能高效电催化氧化 合成 ,其反应机理如图
所示。
下列说法错误的是
A. (Ⅱ)被氧化至 (Ⅲ)后,配体 失去质子能力增强
B.M中 的化合价为
C.该过程有非极性键的形成
D.该过程的总反应式:
【答案】B
【解析】A. (Ⅱ)被氧化至 (Ⅲ)后, 中的 带有更多的正电荷,其与N原子成键
后, 吸引电子的能力比 (Ⅱ)强,这种作用使得配体 中的 键极性变强且更易断裂,因此
其失去质子( )的能力增强,A说法正确;B. (Ⅱ)中 的化合价为+2,当其变为 (Ⅲ)后,
的化合价变为+3, (Ⅲ)失去2个质子后,N原子产生了1个孤电子对, 的化合价不变;M为
,当 变为M时,N原子的孤电子对拆为2个电子并转移给 1个电子,
其中 的化合价变为 ,因此,B说法不正确;C.该过程M变为 时,
有 键形成, 是非极性键,C说法正确;D.从整个过程来看, 4个 失去了2个电子后生成了1个 和2个 , (Ⅱ)是催化剂,因此,该过程的总反应式为 ,
D说法正确;综上所述,本题选B。
【提分秘籍】
1.循环机理图中物质的判断
(1)有进有出的物质参与反应,常作催化剂;
(2)只进不出的为反应物、原料;
(3)不进只出的物质为生成物、产品。
2.循环转化机理图像的解读
对于“循环”反应过程图像,位于“环上”的物质一般是催化剂或中间体,如 、 、 和 ,“入环”的物
质为反应物,如 和 ,“出环”的物质为生成物,如 和 。在机理图中,先找到确定的反应物,反应
⑤ ⑥ ⑦ ⑧
物一般是通过一个箭头进入整个历程的物质,(产物一般多是通过一个箭头最终脱离这个历程的物质)与之
① ④ ② ③
同时反应的就是催化剂,并且经过一个完整循环之后又会生成;中间产物则是这个循环中的任何一个环
节。如下图中,MoO3 则是该反应的催化剂,图中剩余的三个物质均为中间产物。
3.循环机理图题的解题思路
(1)通览全图,找准一“剂”三“物”
催化剂:催化剂在机理图中多数是以完整的循环出现的,以催化剂粒子为主题的多个物种一定在机理
图中的主线上
①
反应物:通过一个箭头进入整个历程的物质一般是反应物;
生成物:通过一个箭头最终脱离整个历程的物质多是产物;
②
中间体:通过一个箭头脱离整个历程,但又生成的是中间体,通过两个箭头进入整个历程的中间物质
③
也是中间体,中间体有时在反应历程中用“[ ]”标出。
④
(2)逐项分析得答案:根据第一步由题给情境信息,找出催化剂、反应物、生成物、中间体,再结合每
一选项设计的问题逐项分析判断,选出正确答案
【变式演练】
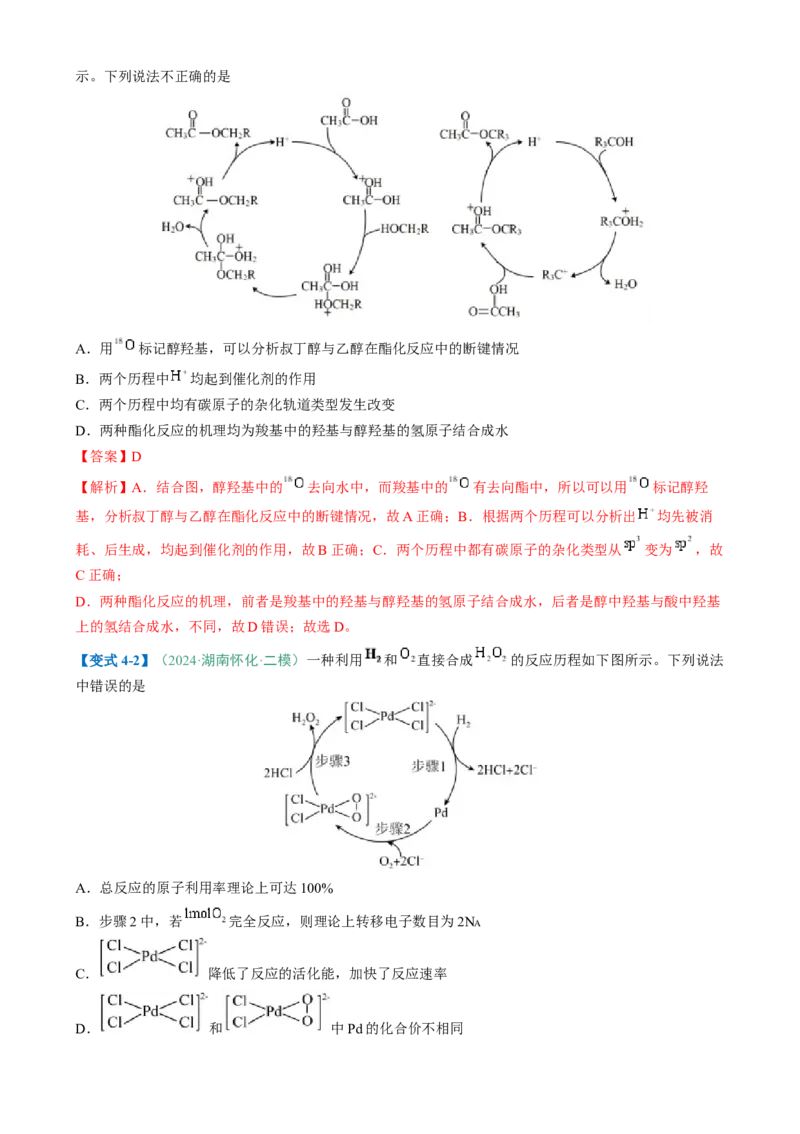
【变式4-1】(2025·浙江·联考)伯醇(记为 )和叔醇(记为 )发生酯化反应的机理如下图所示。下列说法不正确的是
A.用 标记醇羟基,可以分析叔丁醇与乙醇在酯化反应中的断键情况
B.两个历程中 均起到催化剂的作用
C.两个历程中均有碳原子的杂化轨道类型发生改变
D.两种酯化反应的机理均为羧基中的羟基与醇羟基的氢原子结合成水
【答案】D
【解析】A.结合图,醇羟基中的 去向水中,而羧基中的 有去向酯中,所以可以用 标记醇羟
基,分析叔丁醇与乙醇在酯化反应中的断键情况,故A正确;B.根据两个历程可以分析出 均先被消
耗、后生成,均起到催化剂的作用,故B正确;C.两个历程中都有碳原子的杂化类型从 变为 ,故
C正确;
D.两种酯化反应的机理,前者是羧基中的羟基与醇羟基的氢原子结合成水,后者是醇中羟基与酸中羟基
上的氢结合成水,不同,故D错误;故选D。
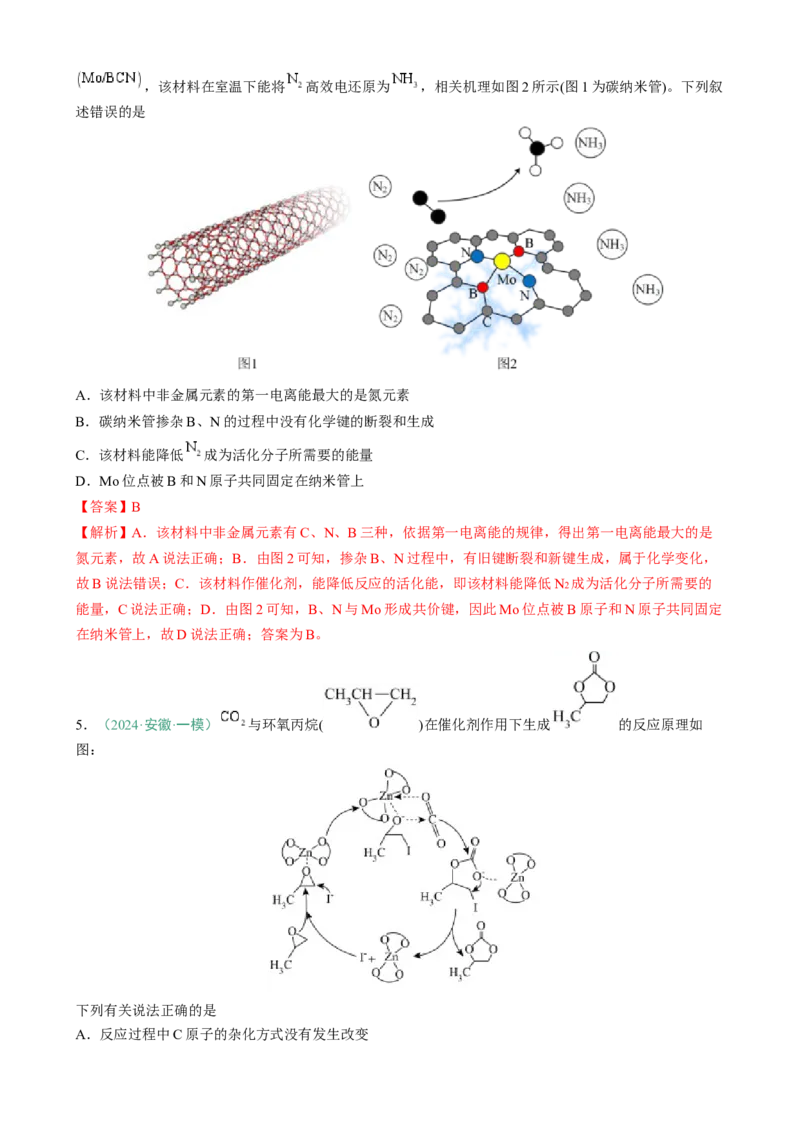
【变式4-2】(2024·湖南怀化·二模)一种利用 和 直接合成 的反应历程如下图所示。下列说法
中错误的是
A.总反应的原子利用率理论上可达100%
B.步骤2中,若 完全反应,则理论上转移电子数目为2NA
C. 降低了反应的活化能,加快了反应速率
D. 和 中Pd的化合价不相同【答案】D
【分析】由图示可知,步骤1为: +H2→Pd+2HCl+2Cl- 、步骤2为:Pd+O2+2Cl-→
、步骤3为: +2HCl→ +H2O2 ,所以总反应为:
;
【解析】A.总反应为 ,理论上反应物全部转化为H2O2 ,故原子利用率理论上为
100%,故A正确;B.步骤2为Pd+O2+2Cl-→ ,若 完全反应,则理论上转移电
子数目为2NA ,故B正确;C.由分步反应及总反应可知, 为催化剂,催化剂可降低反
应的活化能,加快反应速率,故C正确;D. 中Cl化合价为-1价,则Pd元素为+2价,
中Cl化合价为-1价、O化合价为-1价,则Pd元素为+2价,Pd的化合价相同,故D错
误;故选D。
1.(2024·广东卷)对反应 (I为中间产物),相同条件下: 加入催化剂,反应达到平衡所需
时间大幅缩短; 提高反应温度, 增大, 减小①。基于以上事实,可能的反应历
程示意图(——为无催化剂,------为有催化剂)为
②
A. B. C. D.
【答案】A
【解析】提高反应温度, 增大,说明反应 的平衡逆向移动,即该反应为放热反
应, 减小,说明S生成中间产物I的反应平衡正向移动,属于吸热反应,由此可排除C、D
选项,加入催化剂,反应达到平衡所需时间大幅缩短,即反应的决速步骤的活化能下降,使得反应速率大
幅加快,活化能大的步骤为决速步骤,符合条件的反应历程示意图为A,故A正确,故选A。
2.(2024·山东日照·二模)在 催化作用下, 与 反应转化为 和 的反应历程和相对能量
变化关系如图所示(逸出后物质状态不发生变化,在图中略去)。下列说法错误的是
A.该反应的
B.生成 的反应是决速步骤
C.反应历程中存在极性键、非极性键的断裂和形成
D.使用高活性催化剂可以降低反应的最大能垒(活化能)
【答案】C
【解析】A.由反应机理图可知,反应物能量高于产物,故为放热反应,该反应的 ,A正确;B.
能量越高的反应是决速步骤,故生成 的反应是决速步骤,B正确;C.反应历程中不存在非极性键的断
裂,
存在极性键(C-O)的断裂,存在极性键(C-O)、非极性键( )的形成,C错误;D.使用高活性催化剂可
以降低反应的最大能垒(活化能),提高反应速率,D正确;故选C。
3.(2021·重庆卷)“天朗气清,惠风和畅。”研究表明,利用Ir+ 可催化消除大气污染物N2O和CO,简化
中间反应进程后,相对能量变化如图所示。已知CO(g)的燃烧热∆H = -283 kJ·mol-1 ,则2N2O(g)=2N2(g) +
O2(g)的反应热∆H (kJ·mol-1)为
A.-152 B.-76 C.+76 D.+152
【答案】A
【解析】已知CO(g)的燃烧热∆H = -283 kJ·mol-1 ,可得 ,由图
可得N2O(g)+CO(g)=N2(g)+CO2(g)∆H=-330+123-229+77=-359kJ/mol ,由盖斯定律,(反应 -
①
)×2可得
反应2N2O(g)=2N2(g) + O2(g),反应热∆H =( -359+283)×2 =-152kJ·m
②
ol-1 ,故选:A。
② ①
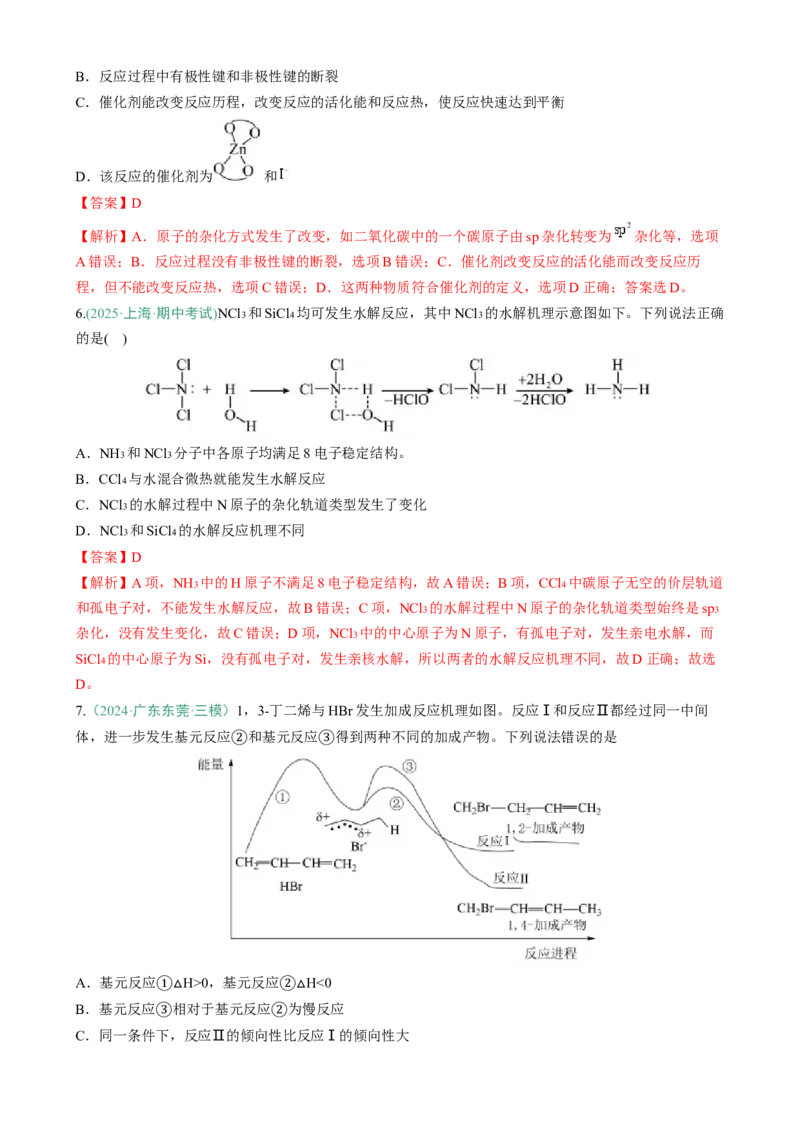
4.(2024·黑龙江·三模)某高校合成了一种 共掺杂多孔碳纳米管负载的钼 单原子位点,该材料在室温下能将 高效电还原为 ,相关机理如图2所示(图1为碳纳米管)。下列叙
述错误的是
A.该材料中非金属元素的第一电离能最大的是氮元素
B.碳纳米管掺杂B、N的过程中没有化学键的断裂和生成
C.该材料能降低 成为活化分子所需要的能量
D.Mo位点被B和N原子共同固定在纳米管上
【答案】B
【解析】A.该材料中非金属元素有C、N、B三种,依据第一电离能的规律,得出第一电离能最大的是
氮元素,故A说法正确;B.由图2可知,掺杂B、N过程中,有旧键断裂和新键生成,属于化学变化,
故B说法错误;C.该材料作催化剂,能降低反应的活化能,即该材料能降低N2 成为活化分子所需要的
能量,C说法正确;D.由图2可知,B、N与Mo形成共价键,因此Mo位点被B原子和N原子共同固定
在纳米管上,故D说法正确;答案为B。
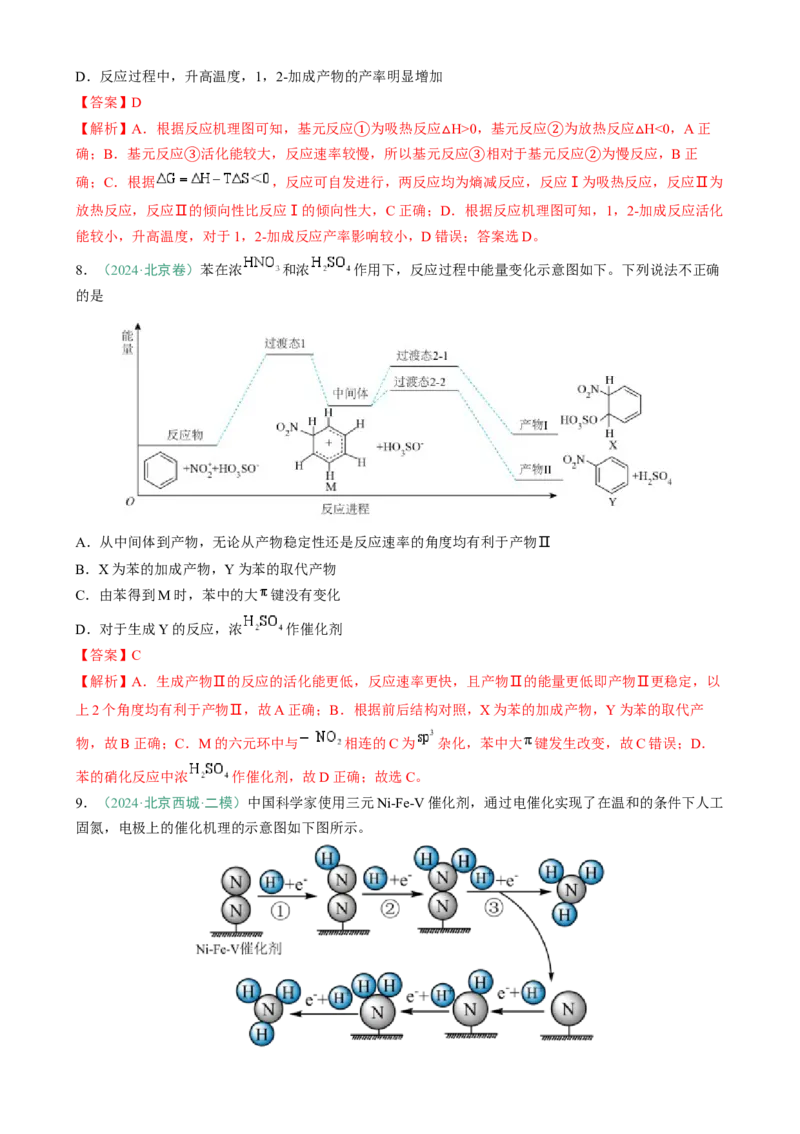
5.(2024·安徽·一模) 与环氧丙烷( )在催化剂作用下生成 的反应原理如
图:
下列有关说法正确的是
A.反应过程中C原子的杂化方式没有发生改变B.反应过程中有极性键和非极性键的断裂
C.催化剂能改变反应历程,改变反应的活化能和反应热,使反应快速达到平衡
D.该反应的催化剂为 和
【答案】D
【解析】A.原子的杂化方式发生了改变,如二氧化碳中的一个碳原子由sp杂化转变为 杂化等,选项
A错误;B.反应过程没有非极性键的断裂,选项B错误;C.催化剂改变反应的活化能而改变反应历
程,但不能改变反应热,选项C错误;D.这两种物质符合催化剂的定义,选项D正确;答案选D。
6.(2025·上海·期中考试)NCl3 和SiCl4 均可发生水解反应,其中NCl3 的水解机理示意图如下。下列说法正确
的是( )
A.NH3 和NCl3 分子中各原子均满足8电子稳定结构。
B.CCl4 与水混合微热就能发生水解反应
C.NCl3 的水解过程中N原子的杂化轨道类型发生了变化
D.NCl3 和SiCl4 的水解反应机理不同
【答案】D
【解析】A项,NH3 中的H原子不满足8电子稳定结构,故A错误;B项,CCl4 中碳原子无空的价层轨道
和孤电子对,不能发生水解反应,故B错误;C项,NCl3 的水解过程中N原子的杂化轨道类型始终是sp3
杂化,没有发生变化,故C错误;D项,NCl3 中的中心原子为N原子,有孤电子对,发生亲电水解,而
SiCl4 的中心原子为Si,没有孤电子对,发生亲核水解,所以两者的水解反应机理不同,故D正确;故选
D。
7.(2024·广东东莞·三模)1,3-丁二烯与HBr发生加成反应机理如图。反应Ⅰ和反应Ⅱ都经过同一中间
体,进一步发生基元反应 和基元反应 得到两种不同的加成产物。下列说法错误的是
② ③
A.基元反应 H>0,基元反应 H<0
B.基元反应 相对于基元反应 为慢反应
①△ ②△
C.同一条件下,反应Ⅱ的倾向性比反应Ⅰ的倾向性大
③ ②D.反应过程中,升高温度,1,2-加成产物的产率明显增加
【答案】D
【解析】A.根据反应机理图可知,基元反应 为吸热反应 H>0,基元反应 为放热反应 H<0,A正
确;B.基元反应 活化能较大,反应速率较慢,所以基元反应 相对于基元反应 为慢反应,B正
① △ ② △
确;C.根据
③
,反应可自发进行,两反应均为
③
熵减反应,反应Ⅰ为
②
吸热反应,反应Ⅱ为
放热反应,反应Ⅱ的倾向性比反应Ⅰ的倾向性大,C正确;D.根据反应机理图可知,1,2-加成反应活化
能较小,升高温度,对于1,2-加成反应产率影响较小,D错误;答案选D。
8.(2024·北京卷)苯在浓 和浓 作用下,反应过程中能量变化示意图如下。下列说法不正确
的是
A.从中间体到产物,无论从产物稳定性还是反应速率的角度均有利于产物Ⅱ
B.X为苯的加成产物,Y为苯的取代产物
C.由苯得到M时,苯中的大 键没有变化
D.对于生成Y的反应,浓 作催化剂
【答案】C
【解析】A.生成产物Ⅱ的反应的活化能更低,反应速率更快,且产物Ⅱ的能量更低即产物Ⅱ更稳定,以
上2个角度均有利于产物Ⅱ,故A正确;B.根据前后结构对照,X为苯的加成产物,Y为苯的取代产
物,故B正确;C.M的六元环中与 相连的C为 杂化,苯中大 键发生改变,故C错误;D.
苯的硝化反应中浓 作催化剂,故D正确;故选C。
9.(2024·北京西城·二模)中国科学家使用三元Ni-Fe-V催化剂,通过电催化实现了在温和的条件下人工
固氮,电极上的催化机理的示意图如下图所示。下列说法不正确的是
A. 中均断开N原子间的π键,形成N-Hσ键
B.电①催②化③过程的电极反应:
C.该电极上可能发生生成氢气的反应
D.三元Ni-Fe-V催化剂可降低固氮反应的活化能
【答案】A
【解析】A.由图可知, 中断开N原子间的π键但 没有断开N原子间的π键, 断开N原子间的
σ
①② ③ ③
键,A错误;B.由图可知,电催化过程的电极反应: ,B正确;C.由图可知,氢
离子得电子生成了氢原子,两个氢原子之间可以得到氢气,因此该电极上可能发生生成氢气的反应,C正
确;D.三元Ni-Fe-V催化剂可降低固氮反应的活化能,加快化学反应速率,D正确;故选A。
10.(2024·陕西榆林·一模)用钌基催化剂催化 和 的反应过程如图所示。
当反应生成 液态 时放出 的热量。下列说法正确的是
A.该反应的热化学方程式为
B.图示中物质Ⅱ为该反应的催化剂,物质Ⅲ为中间产物
C.使用催化剂可以降低反应的活化能,同时可以改变反应的焓变
D.反应历程中既有非极性键的断裂又有非极性键的形成
【答案】A
【解析】A.该图为钌(Ru)基催化剂催化CO2(g)和H2(g)的反应示意图,反应生成92g液态HCOOH时放出
62.4kJ的热量,2mol CO2(g)和2mol H2(g)时反应生成92g (2mol)液态HCOOH放出62.4kJ的热量,则热化
学方程式为CO2(g)+H2(g) =HCOOH(l) ΔH=-31.2kJ/mol-1 ,A正确;B.物质I为反应起点存在的物质,且
在整个过程中量未发生改变,物质I为催化剂,物质Ⅱ、Ⅲ为中间过程出现的物质,为中间产物,B错
误;C.催化剂可以降低反应的活化能,但不能改变反应的焓变,C错误;D.由反应示意图可知反应过
程中不存在非极性键的形成,D错误;故选A。
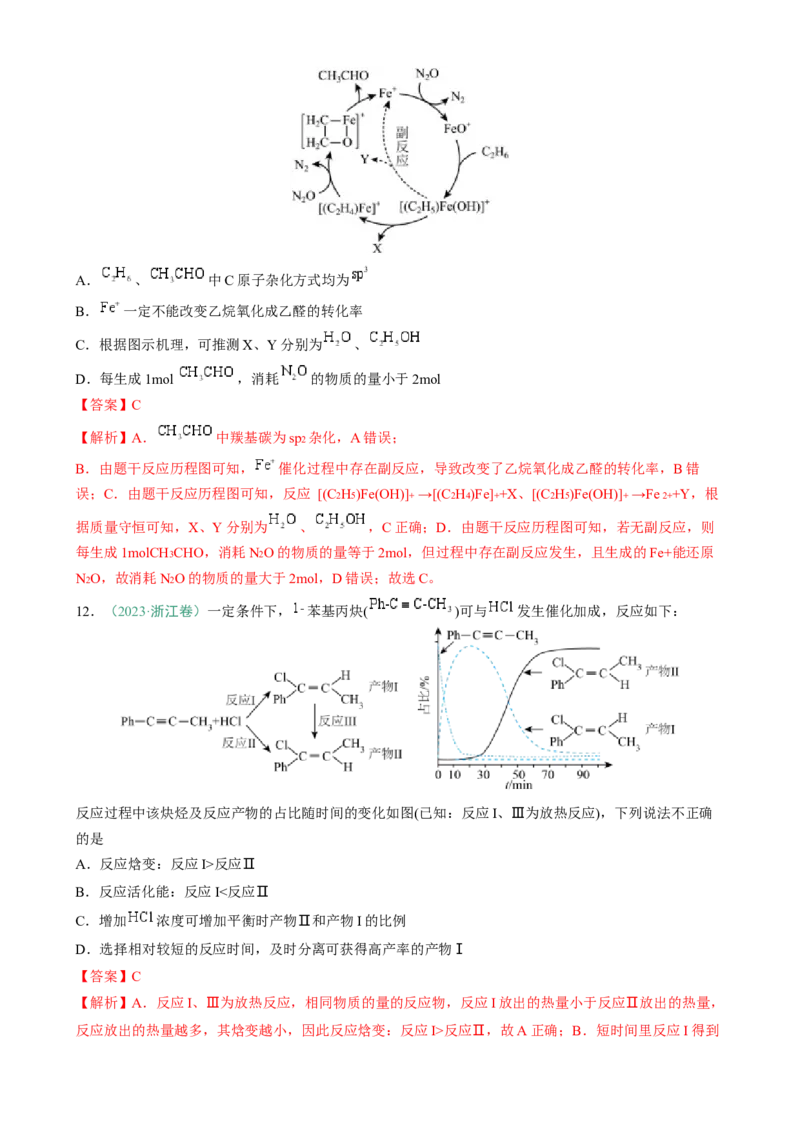
11.(2024·福建龙岩·二模)乙烷催化氧化为乙醛在合成化学和碳资源利用等方面均有重大意义。在
催化下乙烷氧化成乙醛的机理如图所示。下列说法正确的是A. 、 中C原子杂化方式均为
B. 一定不能改变乙烷氧化成乙醛的转化率
C.根据图示机理,可推测X、Y分别为 、
D.每生成1mol ,消耗 的物质的量小于2mol
【答案】C
【解析】A. 中羰基碳为sp2 杂化,A错误;
B.由题干反应历程图可知, 催化过程中存在副反应,导致改变了乙烷氧化成乙醛的转化率,B错
误;C.由题干反应历程图可知,反应 [(C2H5)Fe(OH)]+ →[(C2H4)Fe]++X、[(C2H5)Fe(OH)]+ →Fe 2++Y,根
据质量守恒可知,X、Y分别为 、 ,C正确;D.由题干反应历程图可知,若无副反应,则
每生成1molCH3CHO,消耗N2O的物质的量等于2mol,但过程中存在副反应发生,且生成的Fe+能还原
N2O,故消耗N2O的物质的量大于2mol,D错误;故选C。
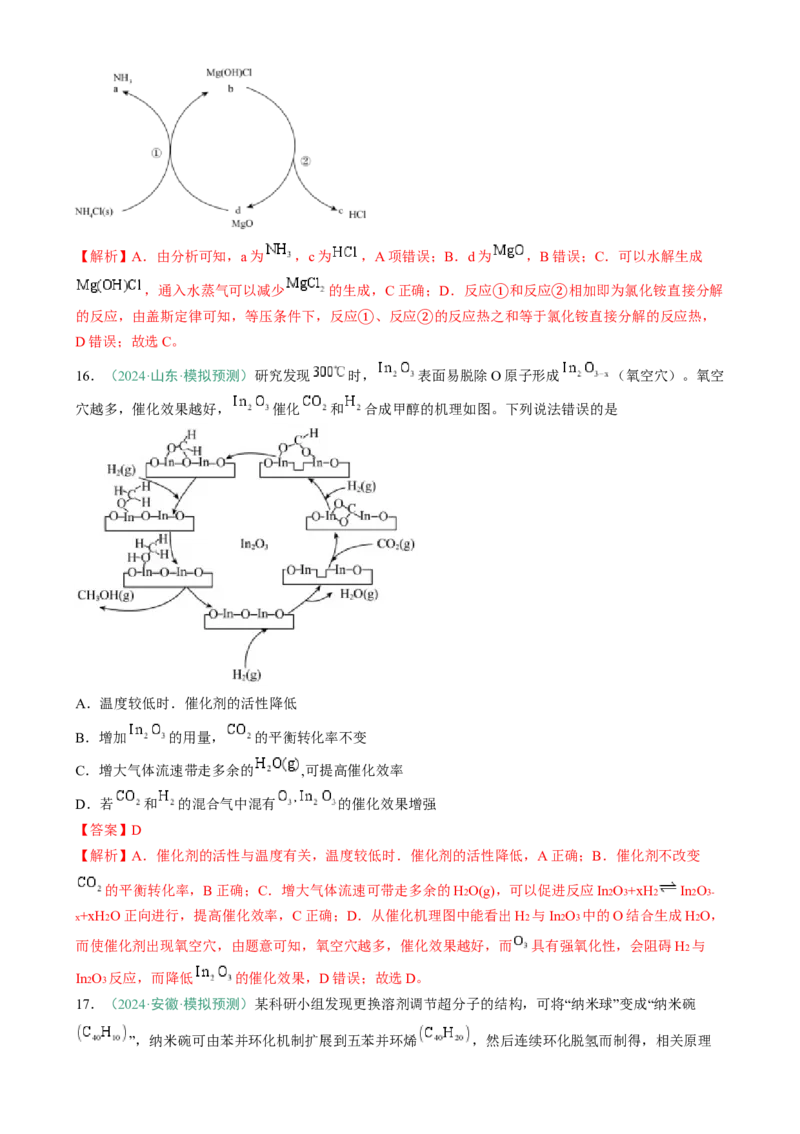
12.(2023·浙江卷)一定条件下, 苯基丙炔( )可与 发生催化加成,反应如下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法不正确
的是
A.反应焓变:反应I>反应Ⅱ
B.反应活化能:反应I<反应Ⅱ
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
【答案】C
【解析】A.反应I、Ⅲ为放热反应,相同物质的量的反应物,反应I放出的热量小于反应Ⅱ放出的热量,
反应放出的热量越多,其焓变越小,因此反应焓变:反应I>反应Ⅱ,故A正确;B.短时间里反应I得到的产物比反应Ⅱ得到的产物多,说明反应I的速率比反应Ⅱ的速率快,速率越快,其活化能越小,则反应
活化能:反应I<反应Ⅱ,故B正确;C.产物I和产物II存在可逆反应,则产物II和产物I的比值即该可
逆反应的平衡常数K,由于平衡常数只与温度有关,所以增加HCl浓度平衡时产物II和产物I的比例不
变,故C错误;D.根据图中信息,选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ,故D正
确。
综上所述,答案为C。
13.(2024·江西新余·二模)催化剂 催化 加氢制甲醇的机理如图所示。已知:图中 吸附过
程表示为 ; 吸附过程表示为 ;氢化过程表示为
(*为催化剂活性位点)。下列说法错误的是
A.氧空位浓度高,有利于增强 的吸附能力
B. 活化位点和 活化位点是不相同的
C.脱附过程表示为
D.降低氢化过程的活化能,一定能有效加快甲醇的生成速率
【答案】D
【解析】A.根据图示,氧空位与二氧化碳作用,氧空位浓度高,有利于增强CO2 的吸附能力,故A正
确;B.根据图示,CO2 活化位点是氧空位,与H2 活化位点不相同,故B正确;C.根据图示,脱附过程
表示为 ,故C正确;D.降低氢化过程的活化能,氢化过程的速率加快,总反
应速率由慢反应决定,所以不一定能有效加快甲醇的生成速率,故D错误;故选D。
14.(2024·北京顺义·二模)我国科研人员研究发现 原子活化乙烷的反应机理,一种机理如图所示。下列说法不正确的是
A.决定反应速率的步骤是中间体 过渡态2
B. 键的形成与断裂使得氢原子发生了迁移
C.该过程涉及非极性键的断裂与形成
D.总反应为
【答案】C
【解析】A.中间体 过渡态2的正反应活化能最大,反应速率最慢,是决定反应速率的步骤,故A正
确;B.Co可活化C2H6 放出CH4 ,Co-H键的形成使H原子发生了迁移,故B正确;C.根据反应历程可
知,涉及到C-C键的断裂和C-H键形成,没有涉及非极性键的形成,故C错误;D.由起点和终点物质可
知,反应物的总能量低于生成物的总能量,该反应是吸热反应,总反应为Co(s)+C2H6(g)→CoCH2(s)
+CH4(g)∆H>0,故D正确;答案为C。
15.(2023·北京卷)一种分解氯化铵实现产物分离的物质转化关系如下,其中 代表 或
中的一种。下列说法正确的是
A.a、c分别是
B. 既可以是 ,也可以是
C.已知 为副产物,则通入水蒸气可减少 的产生
D.等压条件下,反应 、 的反应热之和,小于氯化铵直接分解的反应热
【答案】C
① ②
【分析】 分解的产物是 和 ,分解得到的 与 反应生成 , 又
可以分解得到 和 ,则a为 ,b为 ,c为 ,d为 。【解析】A.由分析可知,a为 ,c为 ,A项错误;B.d为 ,B错误;C.可以水解生成
,通入水蒸气可以减少 的生成,C正确;D.反应 和反应 相加即为氯化铵直接分解
的反应,由盖斯定律可知,等压条件下,反应 、反应 的反应热之和等于氯化铵直接分解的反应热,
① ②
D错误;故选C。
① ②
16.(2024·山东·模拟预测)研究发现 时, 表面易脱除O原子形成 (氧空穴)。氧空
穴越多,催化效果越好, 催化 和 合成甲醇的机理如图。下列说法错误的是
A.温度较低时.催化剂的活性降低
B.增加 的用量, 的平衡转化率不变
C.增大气体流速带走多余的 ,可提高催化效率
D.若 和 的混合气中混有 的催化效果增强
【答案】D
【解析】A.催化剂的活性与温度有关,温度较低时.催化剂的活性降低,A正确;B.催化剂不改变
的平衡转化率,B正确;C.增大气体流速可带走多余的H2O(g),可以促进反应In2O3+xH2 In2O3-
x+xH2O正向进行,提高催化效率,C正确;D.从催化机理图中能看出H2 与In2O3 中的O结合生成H2O,
而使催化剂出现氧空穴,由题意可知,氧空穴越多,催化效果越好,而 具有强氧化性,会阻碍H2 与
In2O3 反应,而降低 的催化效果,D错误;故选D。
17.(2024·安徽·模拟预测)某科研小组发现更换溶剂调节超分子的结构,可将“纳米球”变成“纳米碗
”,纳米碗可由苯并环化机制扩展到五苯并环烯 ,然后连续环化脱氢而制得,相关原理图如图。有关说法正确的是
A.常温常压下,五苯并环烯为液体
B.纳米碗易溶于水
C.由图可知,反应 为吸热反应
D.该机理中反应最大的能垒为
【答案】C
【解析】A.五苯并环烯 为碳原子个数较多的烃,常温常压下为固体,A错误;B.纳米碗
属于烃类有机物,难溶于水,B错误;C.由图可知,反应 为吸热反应,C正确;
D.该机理中反应最大的能垒为 ,D错误;故答案为:C。
18.(2022·重庆卷)“千畦细浪舞晴空”,氮肥保障了现代农业的丰收。为探究(NH4)2SO4 的离子键强弱,
设计如图所示的循环过程,可得 H4/(kJ•mol-1)为
△
A.+533 B.+686 C.+838 D.+1143
【答案】C
【解析】 ; ;
① ② ③
; ;
④ ⑤
; ;则 + -
- + 得 ,得到 +838 kJ•mol-1, 所以A B ⑥D错误, C正确,故选C。 ⑤ ①
⑥
19.
②
(2
③
024·广
④
东·二模)纳米碗C40H10 是一种奇特的碗状共轭体系。高温条件下,C40H10 可以由C40H20 分
子经过连续5步氢抽提和闭环脱氢反应生成。其中 的反应机理和能量变化
如图。下列说法不正确的是A.选择相对较高的温度更有利于制备纳米碗
B.推测 C40H10 纳米碗中含5个五元环
C.
D.该反应历程包含了3步基元反应,且第3步是该反应的决速步骤
【答案】B
【解析】A.由题干反应历程图可知,该反应总反应为一个吸热反应,升高温度平衡正向移动,且反应速
率加快,给选择相对较高的温度更有利于制备纳米碗,A正确;B.由C40H20 的结构可知其中含有1个五
元环,10个六元环,每脱两个氢形成一个五元环,则C40H10 总共含有6个五元环,10个六元环,B错
误;C.由题干反应历程图可知,该反应总反应为:
,C正确;D.该反应包含3个基元反应,分别为C40H20+H• •C40H19+H2 ,•C40H19
•C40H19 、C40H19 •C40H18+H•,其中第三个反应的活化能最大,反应速率最慢,是该反应的决速步
骤,D正确;故答案为:B。
20.(2024·北京卷)可采用 催化氧化法将工业副产物 制成 ,实现氯资源的再利用。反应
的热化学方程式: 。下图所示为该法的一种催化
机理。
下列说法不正确的是
A.Y为反应物 ,W为生成物
B.反应制得 ,须投入
C.升高反应温度, 被 氧化制 的反应平衡常数减小
D.图中转化涉及的反应中有两个属于氧化还原反应【答案】B
【分析】由该反应的热化学方程式可知,该反应涉及的主要物质有HCl、O2 、CuO、Cl2 、H2O;CuO与Y
反应生成Cu(OH)Cl,则Y为HCl;Cu(OH)Cl分解生成W和Cu2OCl2 ,则W为H2O;CuCl2 分解为X和
CuCl,则X为Cl2 ;CuCl和Z反应生成Cu2OCl2 ,则Z为O2 ;综上所述,X、Y、Z、W依次是 、
、 、 。
【解析】A.由分析可知,Y为反应物 ,W为生成物 ,A正确;B. 在反应中作催化剂,会
不断循环,适量即可,B错误;C.总反应为放热反应,其他条件一定,升温平衡逆向移动,平衡常数减
小,C正确;D.图中涉及的两个氧化还原反应是 和 ,D正确;故选B。
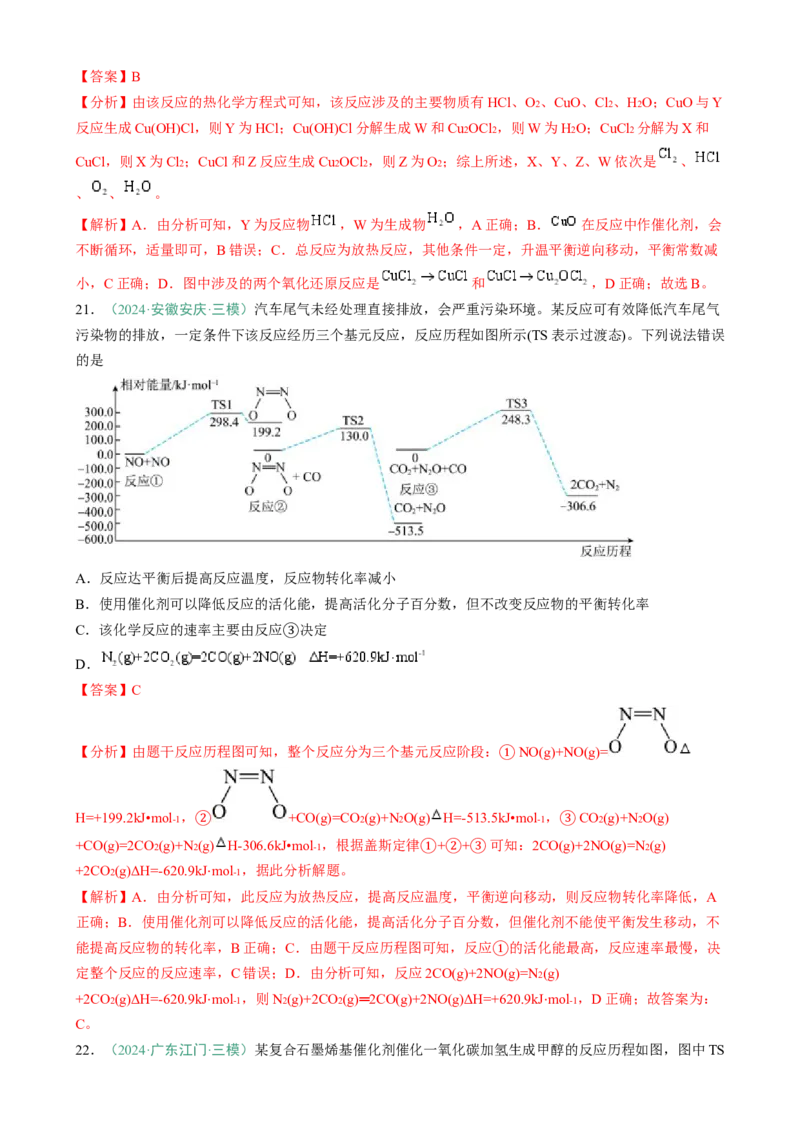
21.(2024·安徽安庆·三模)汽车尾气未经处理直接排放,会严重污染环境。某反应可有效降低汽车尾气
污染物的排放,一定条件下该反应经历三个基元反应,反应历程如图所示(TS表示过渡态)。下列说法错误
的是
A.反应达平衡后提高反应温度,反应物转化率减小
B.使用催化剂可以降低反应的活化能,提高活化分子百分数,但不改变反应物的平衡转化率
C.该化学反应的速率主要由反应 决定
D. ③
【答案】C
【分析】由题干反应历程图可知,整个反应分为三个基元反应阶段: NO(g)+NO(g)=
①
H=+199.2kJ•mol-1 , +CO(g)=CO2(g)+N2O(g) H=-513.5kJ•mol-1 , CO2(g)+N2O(g)
+CO(g)=2CO2(g)+N2② (g) H-306.6kJ•mol-1 ,根据盖斯定律 + + 可知:2CO(
③
g)+2NO(g)=N2(g)
+2CO2(g)ΔH=-620.9kJmol-1 ,据此分析解题。
① ② ③
【解析】A.由分析可知,此反应为放热反应,提高反应温度,平衡逆向移动,则反应物转化率降低,A
⋅
正确;B.使用催化剂可以降低反应的活化能,提高活化分子百分数,但催化剂不能使平衡发生移动,不
能提高反应物的转化率,B正确;C.由题干反应历程图可知,反应 的活化能最高,反应速率最慢,决
定整个反应的反应速率,C错误;D.由分析可知,反应2CO(g)+2N
①
O(g)=N2(g)
+2CO2(g)ΔH=-620.9kJmol-1 ,则N2(g)+2CO2(g)═2CO(g)+2NO(g)ΔH=+620.9kJ mol-1 ,D正确;故答案为:
C。
⋅ ⋅
22.(2024·广东江门·三模)某复合石墨烯基催化剂催化一氧化碳加氢生成甲醇的反应历程如图,图中TS表示过渡态,吸附在催化剂表面上的物种用“*”标注,下列说法中正确的是
A.整个反应历程包含五个基元反应
B.物种吸附在催化剂表面的过程为吸热过程
C.该反应的决速步骤为:
D.反应过程中,涉及非极性键的断裂和形成
【答案】C
【解析】A.从微观上看,反应物分子一般总是经过若干的简单反应步骤,才最后转化为产物分子的。每
一个简单的反应步骤,就是一个基元反应。基元反应步骤要求反应物一步变成生成物,没有任何中间产
物,由图可知,整个反应历程中有四个基元反应,A错误;B.由图可知,吸附在催化剂表面的生成物总
能量低于反应物的总能量,为放热过程,B错误;C.反应的活化能越大,反应速率越慢,反应决速步为
慢反应,由图可知,反应 活化能最大,反应速率最慢,C正确;D.根据反应历
程图可知,第一步基元反应中涉及H-H非极性键的断裂,但是整个过程中没有非极性键的生成,D错
误;故选C。