文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(山东专用)
黄金卷01
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Si 28
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.下列有关物质类别的说法正确的是
A.PO 属于酸性氧化物
2 5
B.油脂属于高分子化合物
C.棉花、麻和蚕丝均为碳水化合物
D.氮化硼纤维属于有机高分子材料
2.实验室中下列做法错误的是
A.用剩的白磷药品放回原试剂瓶
B.用石蜡油保存金属钠
C.高锰酸钾固体保存在带橡胶塞的棕色广口瓶中
D.临近滴定终点时,滴定管的尖嘴接触锥形瓶内壁
3.下列除杂试剂选用正确且除杂过程涉及氧化还原反应的是
选项 物质(括号内为杂质) 除杂试剂
A CO 2( SO 2) 饱和 NaHCO 3溶液
B Al 2 O 3( Fe 2 O 3) 盐酸、NaOH溶液、 CO 2
C NH 3( H 2 O ) 无水 CaCl 2
D 溴苯( Br 2) NaOH溶液
4.硅与碳同主族,是构成地壳的主要元素之一,下列说法正确的是
A.单质硅和金刚石中的键能:SiSiCC
B.CH 和SiH 中v 化合价均为-4价
4 4 0
C.SiO 中Si原子的杂化方式为sp
2
D.碳化硅硬度很大,属于分子晶体
5.能正确表示下列反应的离子方程式是
A.(NH ) Fe(SO ) 溶液与少量Ba(OH) 溶液反应:SO2- + Ba2+ = BaSO↓
4 2 4 2 2 4 4
电解
B.电解AlCl 水溶液:Al3++4C1-+2H O +2H ↑+2Cl↑
3 2 AlO- 2 2
2C.乙酸乙酯与NaOH溶液共热: CHCOOCH CH +OH- CHCOO -+ CHCHOH
3 2 3 3 3 2
D.CuSO 溶液中滴加稀氨水: Cu2++2OH-= Cu(OH) ↓
4 2
6.设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.1LpH=1的HC O 溶液中含有阳离子总数为0.2N
2 2 4 A
B.12.0g二氧化硅晶体中含Si-O键的数目为0.4N
A
C.常温下,1.6gO 与O 的混合气体中所含的原子数目为0.1N
2 3 A
D.含0.4molHCl的浓盐酸与足量MnO 反应,转移电子数目为0.2N
2 A
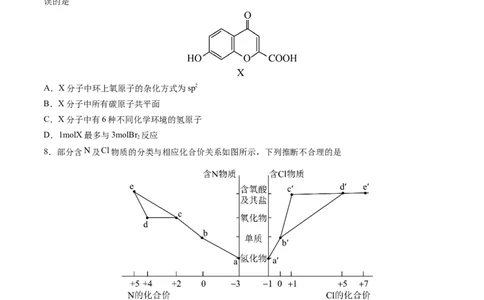
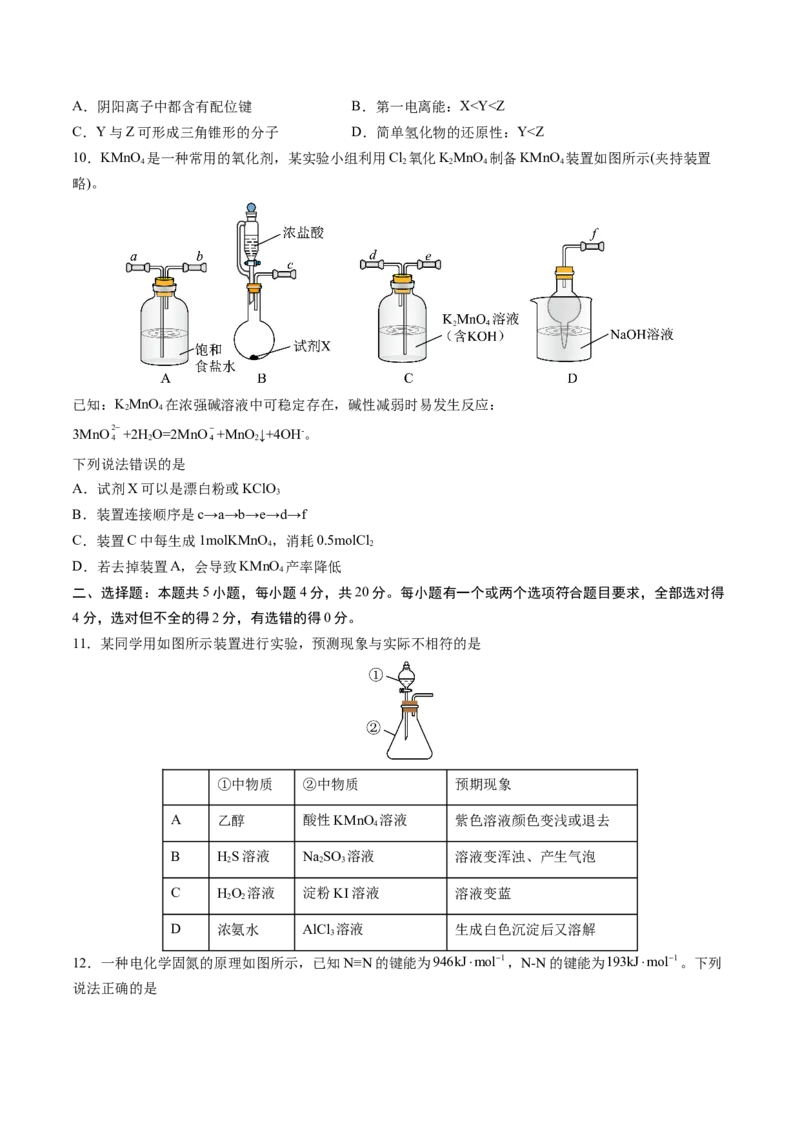
7.异黄酮类化合物是药用植物的有效成分之一,一种异黄酮类化合物X的结构如图所示。下列说法中错
误的是
A.X分子中环上氧原子的杂化方式为sp2
B.X分子中所有碳原子共平面
C.X分子中有6种不同化学环境的氢原子
D.1molX最多与3molBr 反应
2
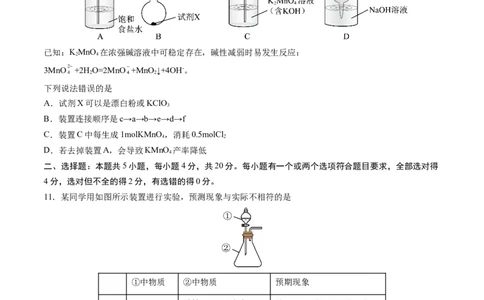
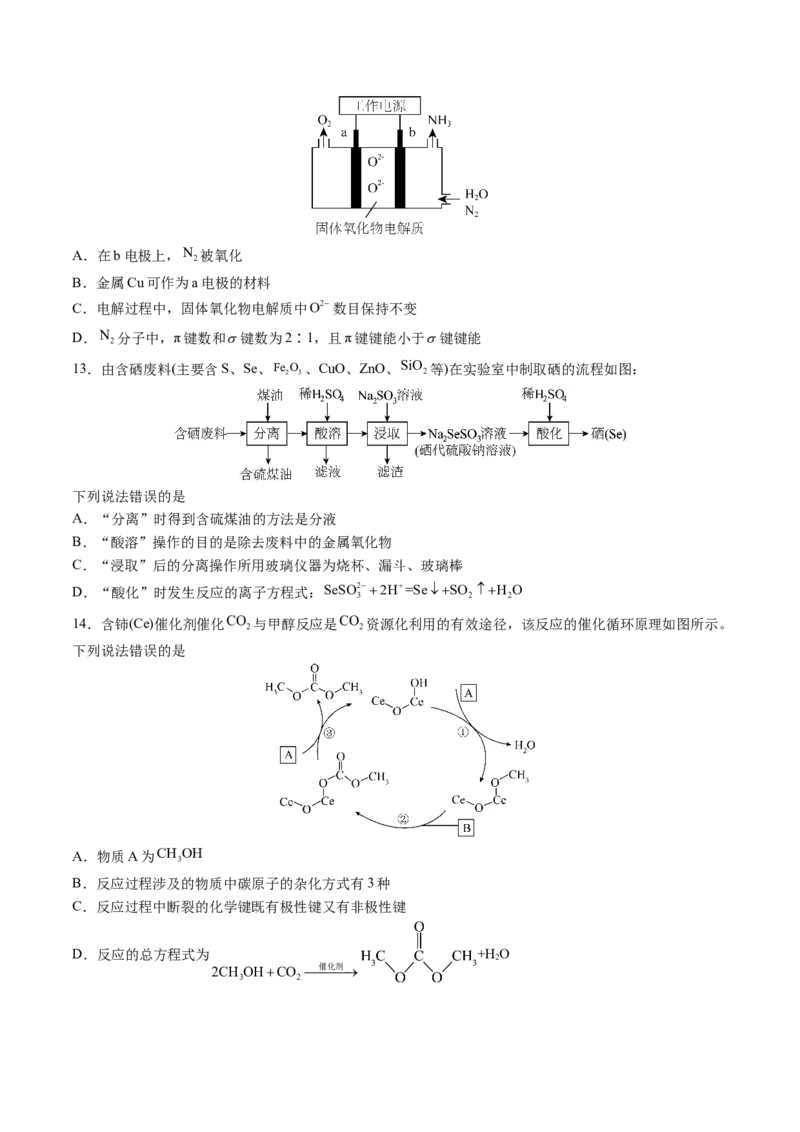
8.部分含N及Cl物质的分类与相应化合价关系如图所示,下列推断不合理的是
A.对应含氧酸的酸性强弱为:e'>e
B.工业上通过abcde 来制备HNO
3
C.久置的b'水溶液pH会变小
D.利用a还原c或者d可以消除氮氧化物的污染
9.W、X、Y、Z均为周期表中前两周期元素,其原子序数依次增大,X原子基态电子排布中无单电子。
四种元素可以组成A B型离子化合物,阴阳离子皆由两种元素组成,且均为正四面体形。下列说法错误的
2
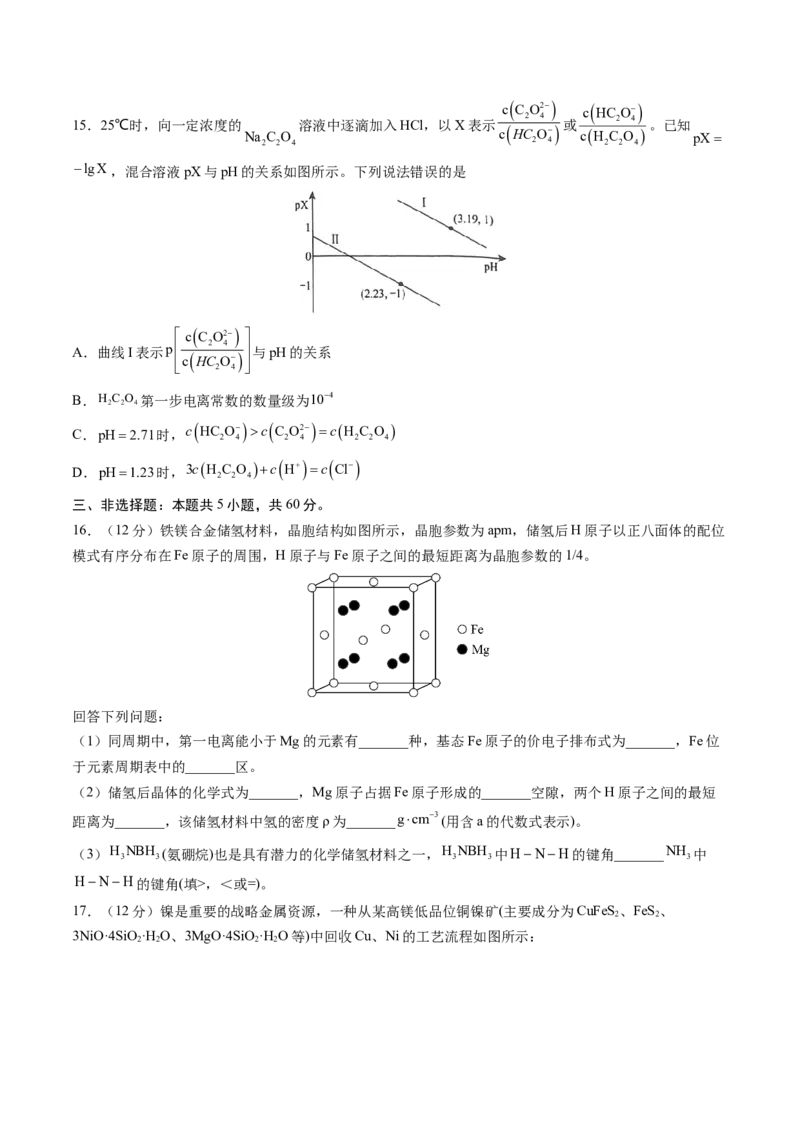
是A.阴阳离子中都含有配位键 B.第一电离能:X,<或=)。
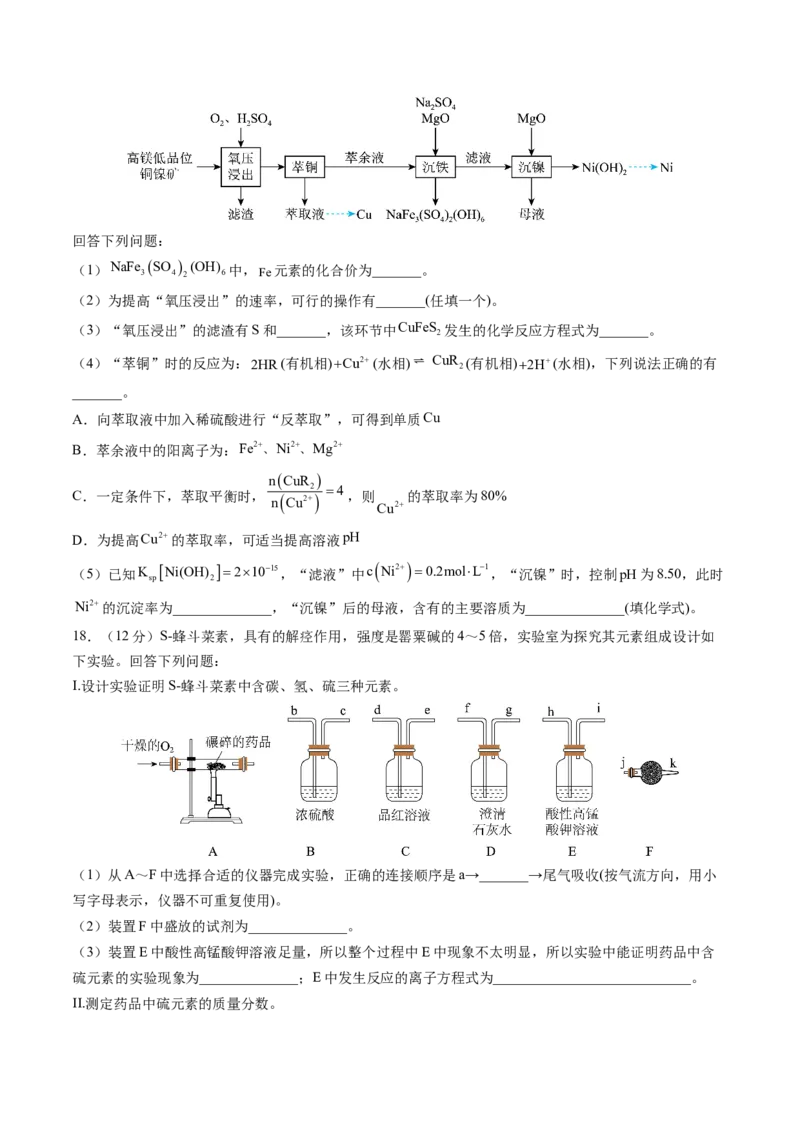
17.(12分)镍是重要的战略金属资源,一种从某高镁低品位铜镍矿(主要成分为CuFeS、FeS、
2 2
3NiO·4SiO·HO、3MgO·4SiO·HO等)中回收Cu、Ni的工艺流程如图所示:
2 2 2 2回答下列问题:
(1)NaFe
3
SO
4
2
(OH)
6
中,Fe元素的化合价为_______。
(2)为提高“氧压浸出”的速率,可行的操作有_______(任填一个)。
(3)“氧压浸出”的滤渣有S和_______,该环节中CuFeS 发生的化学反应方程式为_______。
2
(4)“萃铜”时的反应为:2HR(有机相)Cu2(水相) CuR
2
(有机相)2H(水相),下列说法正确的有
_______。
A.向萃取液中加入稀硫酸进行“反萃取”,可得到单质Cu
B.萃余液中的阳离子为:Fe2、Ni2、Mg2
nCuR
2 4
C.一定条件下,萃取平衡时,
n
Cu2+ ,则 的萃取率为80%
Cu2
D.为提高Cu2的萃取率,可适当提高溶液pH
(5)已知K Ni(OH) 21015,“滤液”中c Ni2 0.2molL1 ,“沉镍”时,控制pH为8.50,此时
sp 2
Ni2的沉淀率为______________,“沉镍”后的母液,含有的主要溶质为______________(填化学式)。
18.(12分)S-蜂斗菜素,具有的解痉作用,强度是罂粟碱的4~5倍,实验室为探究其元素组成设计如
下实验。回答下列问题:
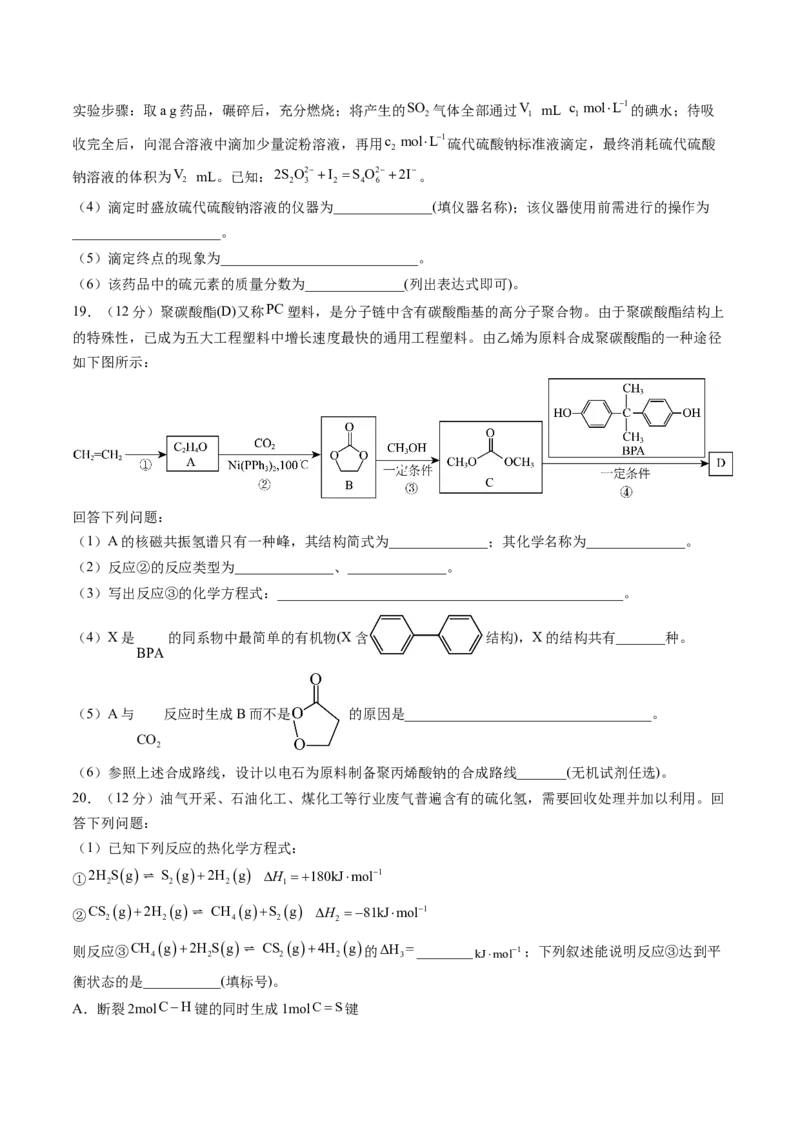
I.设计实验证明S-蜂斗菜素中含碳、氢、硫三种元素。
(1)从A~F中选择合适的仪器完成实验,正确的连接顺序是a→_______→尾气吸收(按气流方向,用小
写字母表示,仪器不可重复使用)。
(2)装置F中盛放的试剂为______________。
(3)装置E中酸性高锰酸钾溶液足量,所以整个过程中E中现象不太明显,所以实验中能证明药品中含
硫元素的实验现象为______________;E中发生反应的离子方程式为____________________________。
II.测定药品中硫元素的质量分数。实验步骤:取a g药品,碾碎后,充分燃烧;将产生的SO 气体全部通过V mL c molL1 的碘水;待吸
2 1 1
收完全后,向混合溶液中滴加少量淀粉溶液,再用c molL1硫代硫酸钠标准液滴定,最终消耗硫代硫酸
2
钠溶液的体积为V mL。已知:2S O2I S O22I 。
2 2 3 2 4 6
(4)滴定时盛放硫代硫酸钠溶液的仪器为______________(填仪器名称);该仪器使用前需进行的操作为
_____________________。
(5)滴定终点的现象为____________________________。
(6)该药品中的硫元素的质量分数为______________(列出表达式即可)。
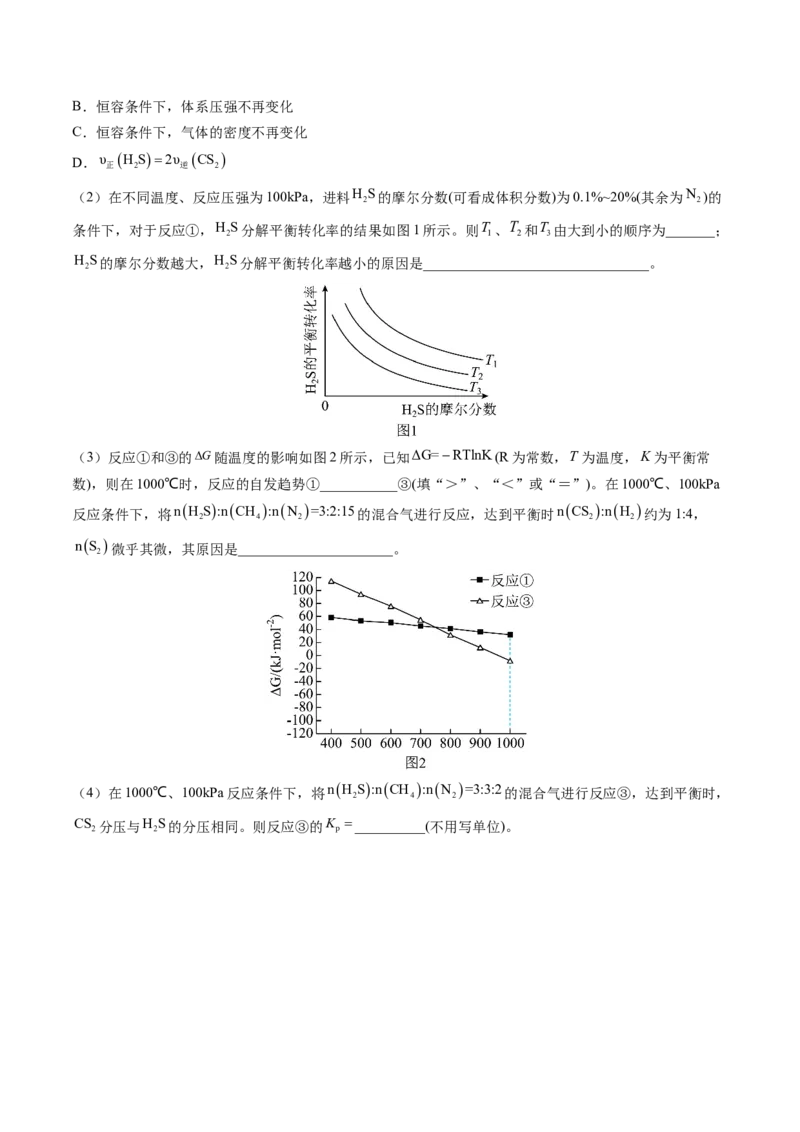
19.(12分)聚碳酸酯(D)又称PC塑料,是分子链中含有碳酸酯基的高分子聚合物。由于聚碳酸酯结构上
的特殊性,已成为五大工程塑料中增长速度最快的通用工程塑料。由乙烯为原料合成聚碳酸酯的一种途径
如下图所示:
回答下列问题:
(1)A的核磁共振氢谱只有一种峰,其结构简式为______________;其化学名称为______________。
(2)反应②的反应类型为______________、______________。
(3)写出反应③的化学方程式:_________________________________________________。
(4)X是 的同系物中最简单的有机物(X含 结构),X的结构共有_______种。
BPA
(5)A与 反应时生成B而不是 的原因是___________________________________。
CO
2
(6)参照上述合成路线,设计以电石为原料制备聚丙烯酸钠的合成路线_______(无机试剂任选)。
20.(12分)油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加以利用。回
答下列问题:
(1)已知下列反应的热化学方程式:
①2H Sg S g2H g H 180kJmol1
2 2 2 1
②CS g2H g CH gS g H 81kJmol1
2 2 4 2 2
则反应③CH
4
g2H
2
Sg CS
2
g4H
2
g 的ΔH
3
=________kJmol1;下列叙述能说明反应③达到平
衡状态的是___________(填标号)。
A.断裂2molCH键的同时生成1molCS键B.恒容条件下,体系压强不再变化
C.恒容条件下,气体的密度不再变化
D.υ H S2υ CS
正 2 逆 2
(2)在不同温度、反应压强为100kPa,进料H S的摩尔分数(可看成体积分数)为0.1%~20%(其余为N )的
2 2
条件下,对于反应①,H S分解平衡转化率的结果如图1所示。则T 、 T 和T 由大到小的顺序为_______;
2 1 2 3
H S的摩尔分数越大,H S分解平衡转化率越小的原因是________________________________。
2 2
(3)反应①和③的G随温度的影响如图2所示,已知ΔG=RTlnK(R为常数,T 为温度,K为平衡常
数),则在1000℃时,反应的自发趋势①___________③(填“>”、“<”或“=”)。在1000℃、100kPa
反应条件下,将nH S:nCH :nN =3:2:15的混合气进行反应,达到平衡时nCS :nH
约为1:4,
2 4 2 2 2
nS
微乎其微,其原因是______________________。
2
(4)在1000℃、100kPa反应条件下,将nH S:nCH :nN =3:3:2的混合气进行反应③,达到平衡时,
2 4 2
CS 分压与H S的分压相同。则反应③的K __________(不用写单位)。
2 2 p