文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(山东专用)
黄金卷01
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Si 28
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.下列有关物质类别的说法正确的是
A.PO 属于酸性氧化物 B.油脂属于高分子化合物
2 5
C.棉花、麻和蚕丝均为碳水化合物 D.氮化硼纤维属于有机高分子材料
【答案】A
【解析】A.能和碱反应生成盐和水的氧化物属于酸性氧化物;PO 属于酸性氧化物,A正确;
2 5
B.高分子化合物是相对分子质量几万、几十万的很大的化合物;油脂不属于高分子化合物,B错误;
C.棉花、麻均为植物纤维,属于碳水化合物;蚕丝为动物蛋白质,不是碳水化合物,C错误;
D.氮化硼纤维属于新型无机非金属材料,D错误;
故选A。
2.实验室中下列做法错误的是
A.用剩的白磷药品放回原试剂瓶
B.用石蜡油保存金属钠
C.高锰酸钾固体保存在带橡胶塞的棕色广口瓶中
D.临近滴定终点时,滴定管的尖嘴接触锥形瓶内壁
【答案】C
【解析】A.白磷在空气中易自燃,所以实验用剩的白磷药品放回原试剂瓶,不能随意丢弃,否则会引发
火灾,故A正确;
B.金属钠易与空气中的氧气和水蒸气反应,所以实验室中用石蜡油保存金属钠,隔绝金属钠与空气的接
触,故B正确;
C.高锰酸钾具有强氧化性,会腐蚀橡胶塞,所以高锰酸钾固体保存在带玻璃塞的棕色广口瓶中,故C错
误;
D.临近滴定终点时,应使滴定管的尖嘴接触锥形瓶内壁,使残余在滴定管的尖嘴的液体进入到锥形瓶中,
减小实验误差,故D正确;
故选C。
3.下列除杂试剂选用正确且除杂过程涉及氧化还原反应的是
选项 物质(括号内为杂质) 除杂试剂
A CO 2( SO 2) 饱和 NaHCO 3溶液
B Al 2 O 3( Fe 2 O 3) 盐酸、NaOH溶液、 CO 2C NH 3( H 2 O ) 无水 CaCl 2
D 溴苯( Br 2) NaOH溶液
【答案】D
【解析】A.用饱和NaHCO 溶液来除去CO 中的SO ,反应原理为:2NaHCO +SO=Na SO +2CO +H O该
3 2 2 3 2 2 3 2 2
反应未有化合价改变,不属于氧化还原反应,A不合题意;
B.用NaOH溶液、CO 即可除去Al O 中的Fe O,涉及的反应先后为:Al O+2NaOH=2NaAlO +H O、
2 2 3 2 3 2 3 2 2
Δ
NaAlO +2H O+CO=Al(OH) ↓+NaHCO、2Al(OH) Al O+3H O,试剂盐酸可以不用,且未有元素化合价
2 2 2 3 3 3 2 3 2
改变,均不属于氧化还原反应,B不合题意;
C.干燥氨气不能用无水CaCl ,试剂错误,C不合题意;
2
D.除去溴苯中的Br ,用NaOH溶液然后分液,反应原理为:2NaOH+Br =NaBr+NaBrO+H O,该反应有
2 2 2
元素化合价改变,属于氧化还原反应,D符合题意;
故答案为:D。
4.硅与碳同主族,是构成地壳的主要元素之一,下列说法正确的是
A.单质硅和金刚石中的键能:SiSiCC
B.CH 和SiH 中v 化合价均为-4价
4 4 0
C.SiO 中Si原子的杂化方式为sp
2
D.碳化硅硬度很大,属于分子晶体
【答案】A
【解析】A.原子半径:Si>C,键长:Si-Si>C-C,则键能:Si-Si<C-C,故A正确;
B.H的电负性大于Si,SiH 中Si的化合价为4价,故B错误;
4
C.SiO 中Si的价层电子对数为4,原子的杂化方式为sp3杂化,故C错误;
2
D.碳化硅的硬度很大,属于共价晶体,故D错误;
故选A。
5.能正确表示下列反应的离子方程式是
A.(NH ) Fe(SO ) 溶液与少量Ba(OH) 溶液反应:SO2- + Ba2+ = BaSO↓
4 2 4 2 2 4 4
电解
B.电解AlCl 水溶液:Al3++4C1-+2H O +2H ↑+2Cl↑
3 2 AlO- 2 2
2
C.乙酸乙酯与NaOH溶液共热: CHCOOCH CH +OH- CHCOO -+ CHCHOH
3 2 3 3 3 2
D.CuSO 溶液中滴加稀氨水: Cu2++2OH-= Cu(OH) ↓
4 2
【答案】C
【解析】A. (NH) Fe(SO ) 溶液与少量Ba(OH) 溶液反应,氢氧根先和Fe2+反应,再和铵根离子反应,
4 2 4 2 2
Ba(OH) 量少,铵根离子和氢氧根不反应,故:Fe2++2OH-+SO2- + Ba2+ = BaSO↓+Fe(OH) ↓,A错误;B.
2 4 4 2电解
电解AlCl 水溶液应生成氢氧化铝和氢气、氯气,离子方程式为:2Al3++6Cl-+6H O
3 2
2Al(OH) ↓+3H ↑+3Cl↑,B错误;C. 酯在碱性条件下水解,离子方程式为: CHCOOCH CH +OH-
3 2 2 3 2 3
CHCOO -+ CHCHOH,C正确;D. 一水合氨为弱碱,不可拆,离子方程式为:
3 3 2
Cu2++2NH H O= CuOH 2NH ,D错误;故选C。
3 2 2 4
6.设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.1LpH=1的HC O 溶液中含有阳离子总数为0.2N
2 2 4 A
B.12.0g二氧化硅晶体中含Si-O键的数目为0.4N
A
C.常温下,1.6gO 与O 的混合气体中所含的原子数目为0.1N
2 3 A
D.含0.4molHCl的浓盐酸与足量MnO 反应,转移电子数目为0.2N
2 A
【答案】C
【解析】A.1LpH=1的HC O 溶液中氢离子浓度为0.1mol/L,氢离子为0.1mol,含有阳离子总数为
2 2 4
0.1N ,A错误;B.12.0g二氧化硅晶体为0.2mol,1个硅原子形成4个硅氧键,则含Si-O键的数目为
A
0.8N ,B错误;C.常温下,1.6gO 与O 的混合气体中只含有氧原子,氧原子为1.6g÷16g/mol=0.1mol,则
A 2 3
所含的原子数目为0.1N ,C正确;D.随着反应的进行盐酸浓度减小,反应不再进行,故转移电子数目小
A
于0.2N ,D错误;故选C。
A
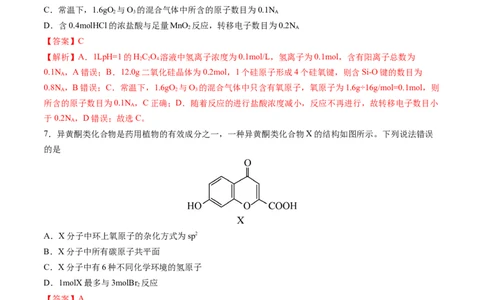
7.异黄酮类化合物是药用植物的有效成分之一,一种异黄酮类化合物X的结构如图所示。下列说法错误
的是
A.X分子中环上氧原子的杂化方式为sp2
B.X分子中所有碳原子共平面
C.X分子中有6种不同化学环境的氢原子
D.1molX最多与3molBr 反应
2
【答案】A
【解析】A.X分子中环上只有一个氧原子,杂化方式为sp3,A错误;
B.X分子中苯环和碳碳双键在一个平面,所以所有碳原子共平面,B正确;
C.X分子中有6种不同化学环境的氢原子 ,C正确;
D.1molX中苯环消耗2molBr ,碳碳双键消耗1molBr 最多与3molBr 反应,D正确;
2 2 2故选A。
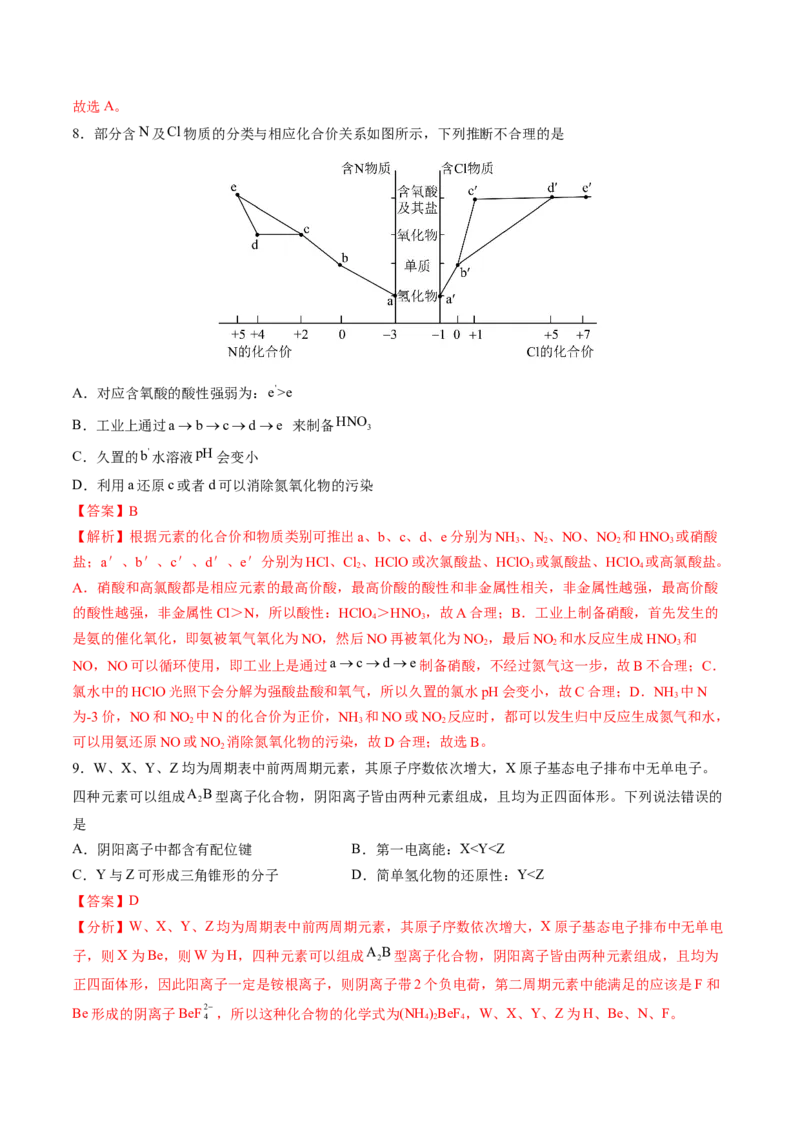
8.部分含N及Cl物质的分类与相应化合价关系如图所示,下列推断不合理的是
A.对应含氧酸的酸性强弱为:e'>e
B.工业上通过abcde 来制备HNO
3
C.久置的b'水溶液pH会变小
D.利用a还原c或者d可以消除氮氧化物的污染
【答案】B
【解析】根据元素的化合价和物质类别可推出a、b、c、d、e分别为NH 、N、NO、NO 和HNO 或硝酸
3 2 2 3
盐;a'、b'、c'、d'、e'分别为HCl、Cl、HClO或次氯酸盐、HClO 或氯酸盐、HClO 或高氯酸盐。
2 3 4
A.硝酸和高氯酸都是相应元素的最高价酸,最高价酸的酸性和非金属性相关,非金属性越强,最高价酸
的酸性越强,非金属性Cl>N,所以酸性:HClO>HNO,故A合理;B.工业上制备硝酸,首先发生的
4 3
是氨的催化氧化,即氨被氧气氧化为NO,然后NO再被氧化为NO ,最后NO 和水反应生成HNO 和
2 2 3
NO,NO可以循环使用,即工业上是通过acde制备硝酸,不经过氮气这一步,故B不合理;C.
氯水中的HClO光照下会分解为强酸盐酸和氧气,所以久置的氯水pH会变小,故C合理;D.NH 中N
3
为-3价,NO和NO 中N的化合价为正价,NH 和NO或NO 反应时,都可以发生归中反应生成氮气和水,
2 3 2
可以用氨还原NO或NO 消除氮氧化物的污染,故D合理;故选B。
2
9.W、X、Y、Z均为周期表中前两周期元素,其原子序数依次增大,X原子基态电子排布中无单电子。
四种元素可以组成A B型离子化合物,阴阳离子皆由两种元素组成,且均为正四面体形。下列说法错误的
2
是
A.阴阳离子中都含有配位键 B.第一电离能:XZ,D错误;
故选D。
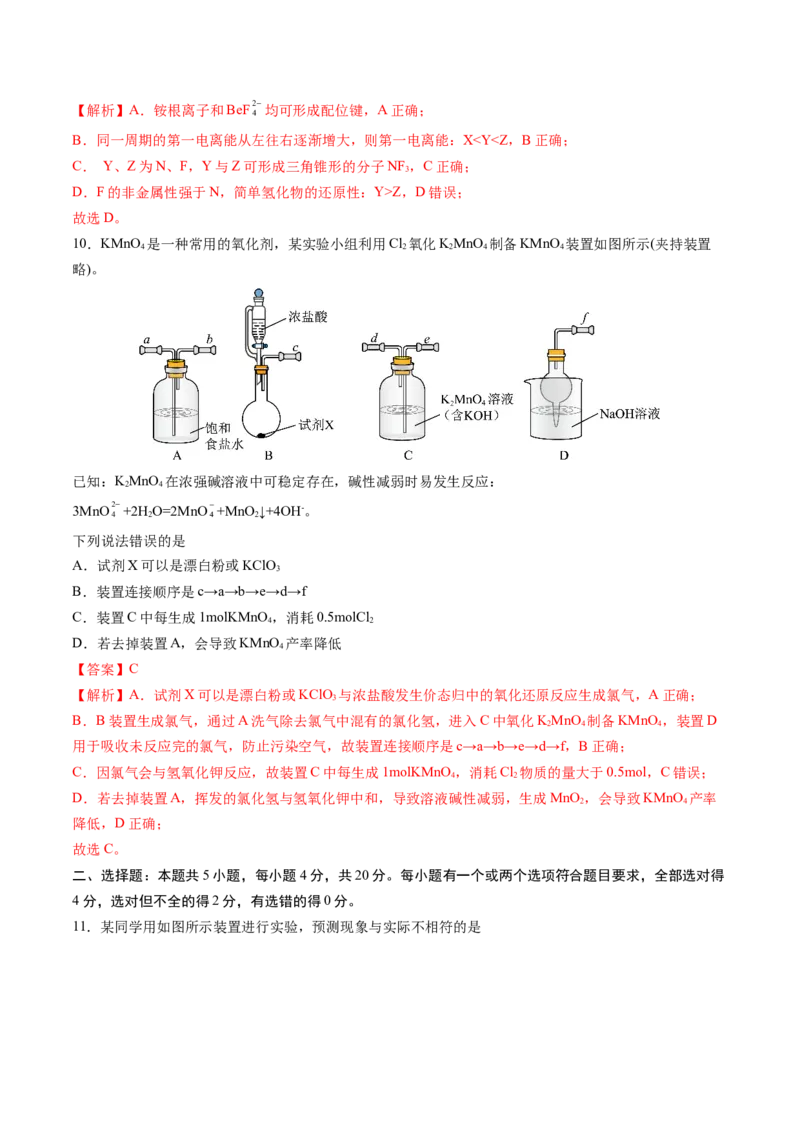
10.KMnO 是一种常用的氧化剂,某实验小组利用Cl 氧化KMnO 制备KMnO 装置如图所示(夹持装置
4 2 2 4 4
略)。
已知:KMnO 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4
3MnO 2 +2H O=2MnO+MnO↓+4OH-。
4 2 4 2
下列说法错误的是
A.试剂X可以是漂白粉或KClO
3
B.装置连接顺序是c→a→b→e→d→f
C.装置C中每生成1molKMnO,消耗0.5molCl
4 2
D.若去掉装置A,会导致KMnO 产率降低
4
【答案】C
【解析】A.试剂X可以是漂白粉或KClO 与浓盐酸发生价态归中的氧化还原反应生成氯气,A正确;
3
B.B装置生成氯气,通过A洗气除去氯气中混有的氯化氢,进入C中氧化KMnO 制备KMnO ,装置D
2 4 4
用于吸收未反应完的氯气,防止污染空气,故装置连接顺序是c→a→b→e→d→f,B正确;
C.因氯气会与氢氧化钾反应,故装置C中每生成1molKMnO,消耗Cl 物质的量大于0.5mol,C错误;
4 2
D.若去掉装置A,挥发的氯化氢与氢氧化钾中和,导致溶液碱性减弱,生成MnO ,会导致KMnO 产率
2 4
降低,D正确;
故选C。
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得
4分,选对但不全的得2分,有选错的得0分。
11.某同学用如图所示装置进行实验,预测现象与实际不相符的是①中物质 ②中物质 预期现象
A 乙醇 酸性KMnO 溶液 紫色溶液颜色变浅或退去
4
B HS溶液 NaSO 溶液 溶液变浑浊、产生气泡
2 2 3
C HO 溶液 淀粉KI溶液 溶液变蓝
2 2
D 浓氨水 AlCl 溶液 生成白色沉淀后又溶解
3
【答案】BD
【解析】A.乙醇能和酸性高锰酸钾发生氧化还原反应使得溶液褪色,预测现象与实际相符,故A不符合
题意;
B.硫化氢和亚硫酸钠发生氧化还原反应生成硫单质沉淀,预测现象与不实际相符,故B符合题意;
C.过氧化氢和碘化氢生成能使淀粉变蓝色的碘单质,预测现象与实际相符,故C不符合题意;
D.铝离子和弱碱氨水生成不溶于氨水的氢氧化铝沉淀,预测现象与实际不相符,故D符合题意;
故选BD。
12.一种电化学固氮的原理如图所示,已知N≡N的键能为946kJmol1,N-N的键能为193kJmol1。下列
说法正确的是
A.在b电极上,N 被氧化
2
B.金属Cu可作为a电极的材料
C.电解过程中,固体氧化物电解质中O2数目保持不变
D.N 分子中,π键数和键数为2∶1,且π键键能小于键键能
2
【答案】C
【解析】由装置可知,b电极的N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,因此b为
2 3
阴极,电极反应式为N+3H O+6e-=2NH+3O2-,a为阳极,电极反应式为2O2-+4e-=O 。A.由分析可得,b
2 2 3 2
电极上N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,即N 被还原,A错误;B.a为阳
2 3 2
极,若金属Cu作a的电极材料,则金属Cu优先失去电子,B错误;C.电解过程中,阴极电极反应式为2N+6H O+12e-=4NH+6O2-,阳极电极反应式为6O2-+12e-=3O ,固体氧化物电解质中O2数目保持不变,
2 2 3 2
故C正确;D.N 分子中存在氮氮三键,π键数和键数为2∶1,已知N≡N的键能为946kJmol1,N-N
2
946kJmol1193kJmol1
的键能为 ,则π键键能为 376.5kJmol1,π键键能大于 键键能,
193kJmol1 2
故D错误;故选C。
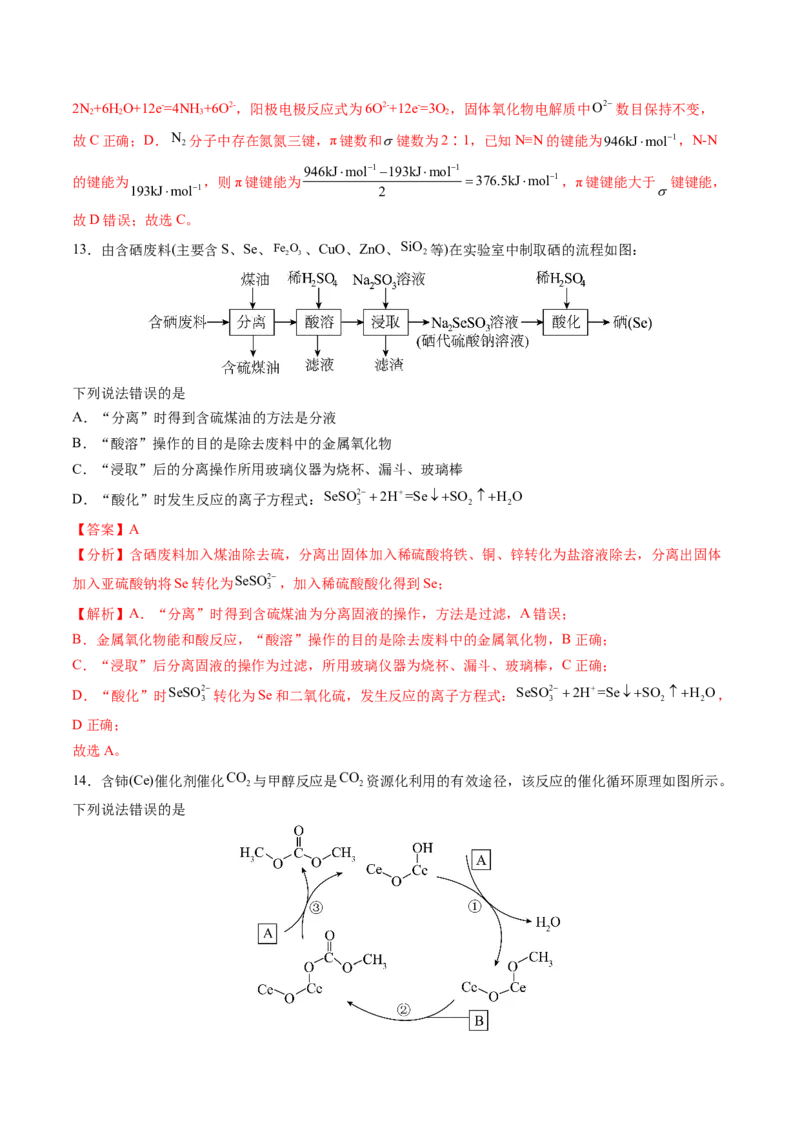
13.由含硒废料(主要含S、Se、Fe O 、CuO、ZnO、SiO 等)在实验室中制取硒的流程如图:
2 3 2
下列说法错误的是
A.“分离”时得到含硫煤油的方法是分液
B.“酸溶”操作的目的是除去废料中的金属氧化物
C.“浸取”后的分离操作所用玻璃仪器为烧杯、漏斗、玻璃棒
D.“酸化”时发生反应的离子方程式:SeSO22H=SeSO H O
3 2 2
【答案】A
【分析】含硒废料加入煤油除去硫,分离出固体加入稀硫酸将铁、铜、锌转化为盐溶液除去,分离出固体
加入亚硫酸钠将Se转化为SeSO2
,加入稀硫酸酸化得到Se;
3
【解析】A.“分离”时得到含硫煤油为分离固液的操作,方法是过滤,A错误;
B.金属氧化物能和酸反应,“酸溶”操作的目的是除去废料中的金属氧化物,B正确;
C.“浸取”后分离固液的操作为过滤,所用玻璃仪器为烧杯、漏斗、玻璃棒,C正确;
D.“酸化”时SeSO2 转化为Se和二氧化硫,发生反应的离子方程式:SeSO22H=SeSO H O,
3 3 2 2
D正确;
故选A。
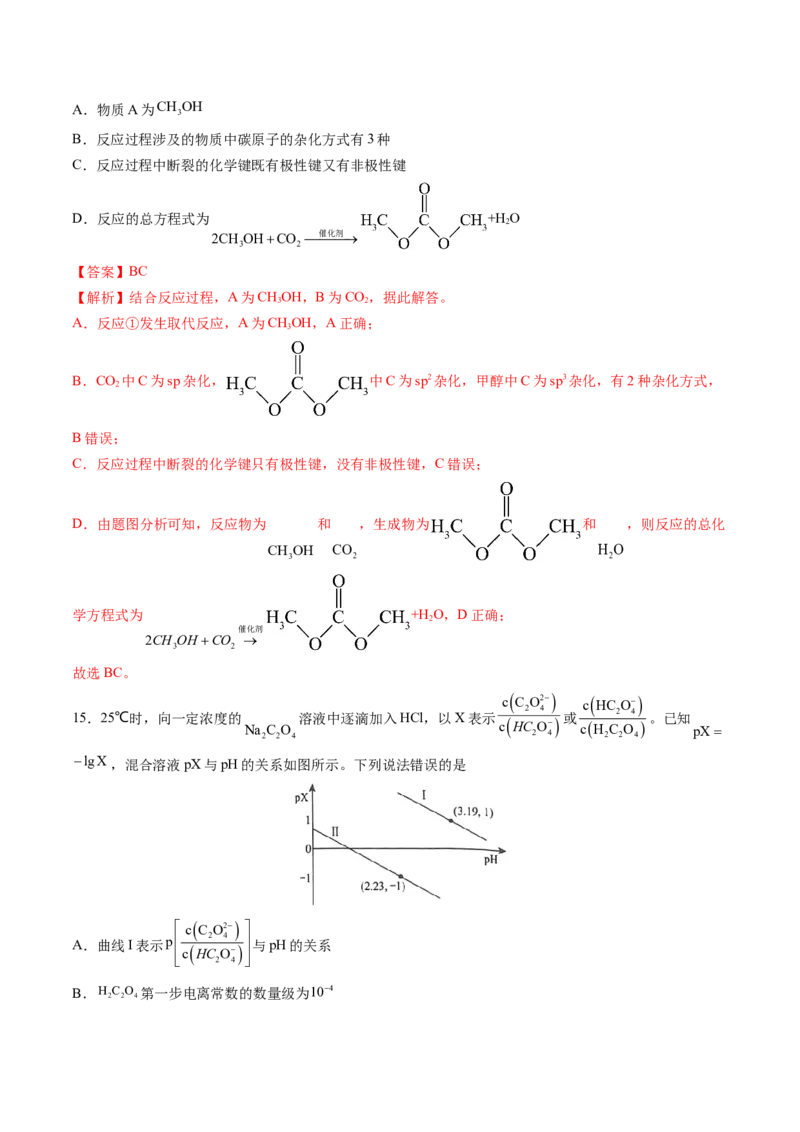
14.含铈(Ce)催化剂催化CO 与甲醇反应是CO 资源化利用的有效途径,该反应的催化循环原理如图所示。
2 2
下列说法错误的是A.物质A为CH OH
3
B.反应过程涉及的物质中碳原子的杂化方式有3种
C.反应过程中断裂的化学键既有极性键又有非极性键
D.反应的总方程式为 +H O
2
2CH OHCO 催化剂
3 2
【答案】BC
【解析】结合反应过程,A为CHOH,B为CO,据此解答。
3 2
A.反应①发生取代反应,A为CHOH,A正确;
3
B.CO 中C为sp杂化, 中C为sp2杂化,甲醇中C为sp3杂化,有2种杂化方式,
2
B错误;
C.反应过程中断裂的化学键只有极性键,没有非极性键,C错误;
D.由题图分析可知,反应物为 和 ,生成物为 和 ,则反应的总化
CH OH CO H O
3 2 2
学方程式为 +H O,D正确;
2
催化剂
2CH OH CO
3 2
故选BC。
c C O2 c HC O
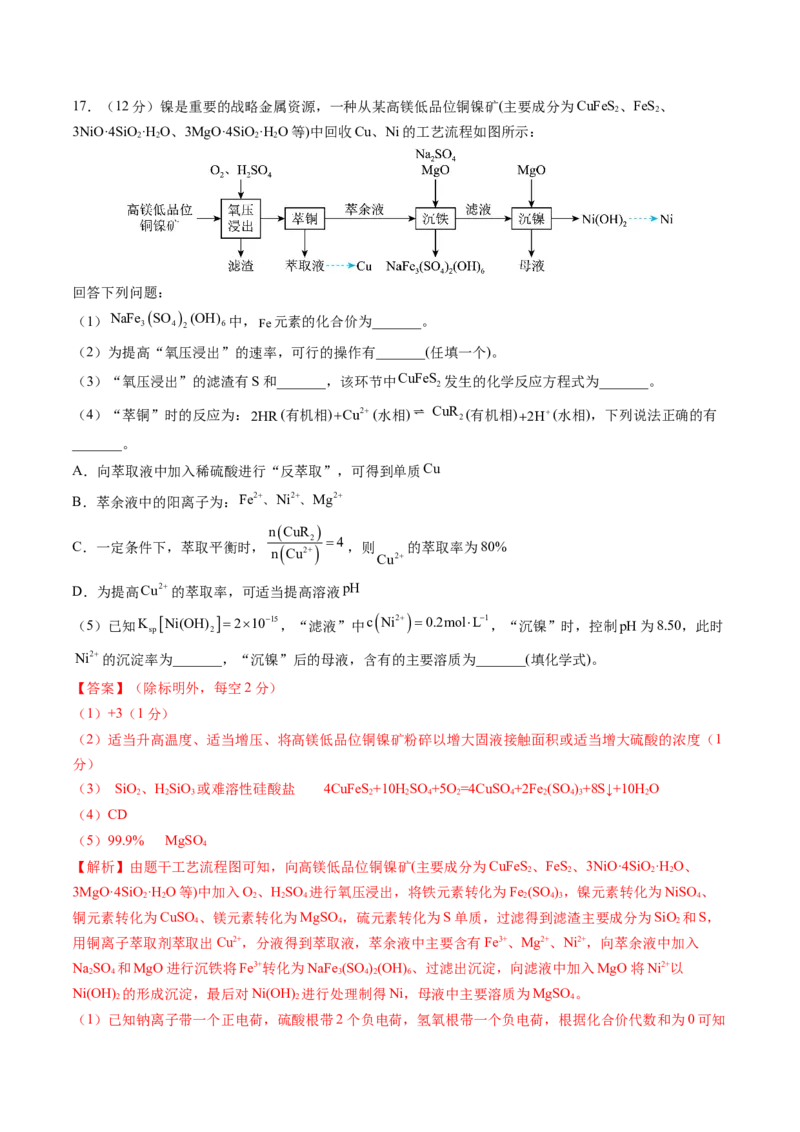
15.25℃时,向一定浓度的
Na 2 C 2 O 4
溶液中逐滴加入HCl,以X表示
c
HC
2
2 O
4
4
或
cH 2 C
2
2 O
4
4
。已知
pX
lgX,混合溶液pX与pH的关系如图所示。下列说法错误的是
c C O2
A.曲线I表示p 2 4 与pH的关系
c
HC
O
2 4
B.H C O 第一步电离常数的数量级为104
2 2 4C.pH2.71时,c HC O c C O2 cH C O
2 4 2 4 2 2 4
D.pH1.23时,3cH C O c H c Cl
2 2 4
【答案】BD
c
C
O2-
c
H+
【分析】当 , ,K = 2 4 =c H+ ;当 ,
pX0 c HC O- =c C O2- a2 c HC O- pX0
2 4 2 4 2 4
c
HC
O-
c
H+
cH C O =c HC O-,K a1 = cH 2 C 4 O =c H+ ;由于K a1 >K a2 ,结合图像可知,曲线Ⅱ表示
2 2 4 2 4 2 2 4
c HC O- c C O2-
p 2 4 与 的关系、曲线Ⅰ表示p 2 4 与 的关系;
cH C O pH c HC O- pH
2 2 4 2 4
c
C
O2-
【解析】A.由分析可知,Ⅰ表示p 2 4 与 的关系;,A正确。
c
HC
O-
pH
2 4
c
HC
O-
c
H+
B.由点(2.23,-1)可知, 第一步电离常数为K = 2 4 =10110-2.23=10-1.23,其数量级
H C O a1 cH C O
2 2 4 2 2 4
为10-2,B错误。
c
C
O2-
C.由图可知, 时,p 2 4 >0,则 ;
pH2.71 c
HC
O-
c
HC
O-
>c
C
O2-
2 4 2 4 2 4
c HC O- c H+ c C O2- c H+
K = 2 4 =10110-2.23=10-1.23,由点(3.19,1)可知, K = 2 4 =10-110-3.19=10-4.19 ;
a1 cH C O a2 c HC O-
2 2 4 2 4
c2 H+ c C O2- 10-2.712 c C O2-
K K = 2 4 =10-5.42,此时 ,则K K = 2 4 =10-5.42,得
a1 a2 cH C O pH2.71 a1 a2 cH C O
2 2 4 2 2 4
c C O2- =cH C O ,C正确。
2 4 2 2 4
D.由电荷守恒可知,c
H+
+c
Na+
=c
OH-
+c
Cl-
+c
HC
O-
+2c
C
O2-
;由物料守恒可知,
2 4 2 4
c Na+ =2c HC O- +2c C O2- +2cH C O ;两式联立可得:
2 4 2 4 2 2 4
c
HC
O-
c
H+
c H+ +c HC O- +2cH C O =c OH- +c Cl-;K a1 = cH 2 C 4 O =10-1.23, pH1.23 时,
2 4 2 2 4 2 2 4
c HC O- =cH C O ,则有c H+ +3cH C O =c OH- +c Cl- ,D错误。
2 4 2 2 4 2 2 4
故选BD。
三、非选择题:本题共5小题,共60分。
16.(12分)铁镁合金储氢材料,晶胞结构如图所示,晶胞参数为apm,储氢后H原子以正八面体的配位
模式有序分布在Fe原子的周围,H原子与Fe原子之间的最短距离为晶胞参数的1/4。回答下列问题:
(1)同周期中,第一电离能小于Mg的元素有_______种,基态Fe原子的价电子排布式为_______,Fe位
于元素周期表中的_______区。
(2)储氢后晶体的化学式为_______,Mg原子占据Fe原子形成的_______空隙,两个H原子之间的最短
距离为_______,该储氢材料中氢的密度ρ为_______gcm3(用含a的代数式表示)。
(3)H NBH (氨硼烷)也是具有潜力的化学储氢材料之一,H NBH 中HNH的键角_______NH 中
3 3 3 3 3
HNH的键角(填>,<或=)。
【答案】(除标明外,每空2分)
(1)2(1分) 3d64s2(1分) d(1分)
241
2 gcm-3
(2)MgFeH 正四面体(1分) apm
2 6 N (a1010)3
4
A
(3)>
【解析】(1)同周期元素第一电离能从左到右有增大的趋势,但Mg核外电子排布形成3s全满结构,能
量较低,则第一电离能大于相邻元素,则第一电离能小于Mg的元素有Na、Al,共2种,Fe元素是26号
元素,核外电子排布式为: 1s22s22p63s23p63d64s2,基态Fe原子的价电子排布式为3d64s2,Fe位于元素周期
表中的d区。
1 1
(2)如图所示,晶胞中有8个Mg原子,Fe原子位于顶点、面心,晶胞中Fe原子数目6 8 4 ,
2 8
储氢后H原子以正八面体的配位模式有序分布在Fe原子的周围,则H原子数目为4×6=24个,储氢后晶体
的化学式为MgFeH,据图,Mg原子占据Fe原子形成的正四面体空隙;已知H原子构成正八面体、铁原
2 6
1
子位于正八面体的体心,晶胞参数为apm,H原子与Fe原子之间的最短距离为晶胞参数的 ,即H原子与
4
1 2
Fe原子之间距离为 apm,则两个H原子之间的最短距离为 apm,该储氢材料每个晶胞中含24个H
4 4
241 241
g gcm-3
原子、氢质量 ,晶胞体积 ,则储氢材料中氢的密度ρ为 (用含a
N (a1010)3cm3 N (a1010)3
A A
的代数式表示)。
(3)H NBH (氨硼烷)中氮原子有3个共价键、1个配位键,氨分子中氮原子有3个共价键、1对孤电子对,
3 3
孤电子对和成键电子对之间的排斥力大于成键电子对之间的排斥力,则H NBH 中HNH的键角>NH
3 3 3
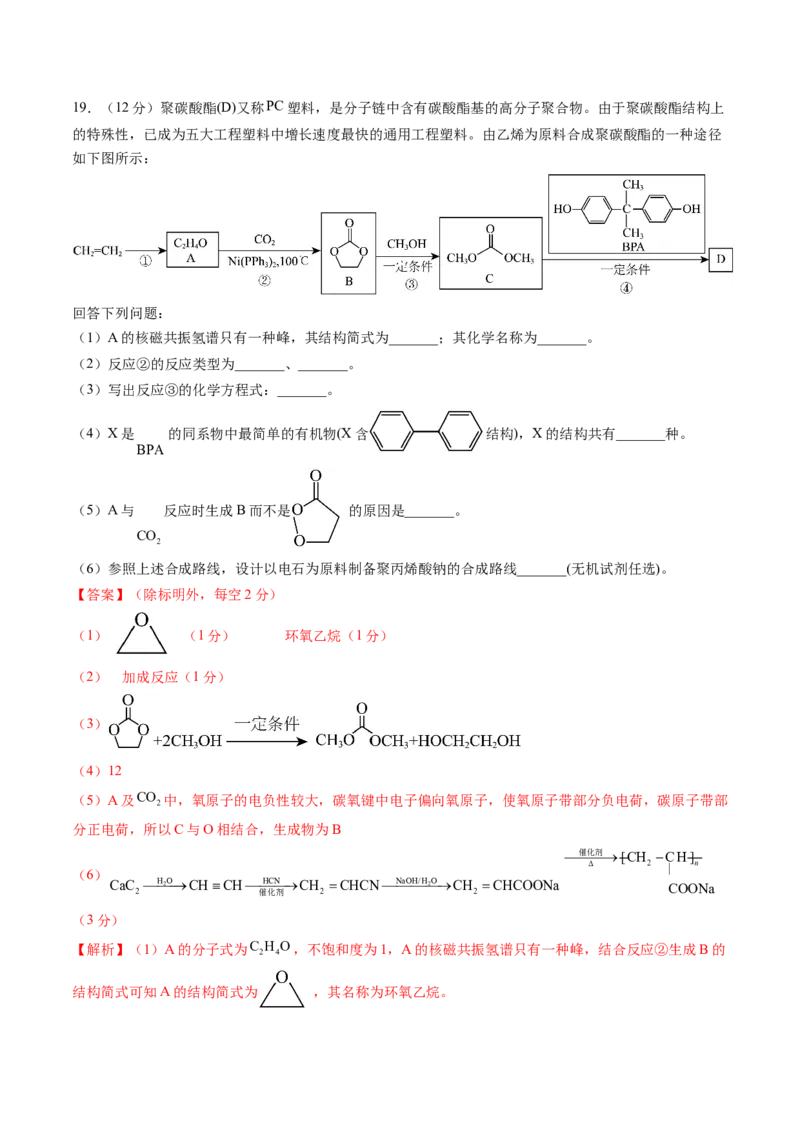
中HNH的键角。17.(12分)镍是重要的战略金属资源,一种从某高镁低品位铜镍矿(主要成分为CuFeS、FeS、
2 2
3NiO·4SiO·HO、3MgO·4SiO·HO等)中回收Cu、Ni的工艺流程如图所示:
2 2 2 2
回答下列问题:
(1)NaFe
3
SO
4
2
(OH)
6
中,Fe元素的化合价为_______。
(2)为提高“氧压浸出”的速率,可行的操作有_______(任填一个)。
(3)“氧压浸出”的滤渣有S和_______,该环节中CuFeS 发生的化学反应方程式为_______。
2
(4)“萃铜”时的反应为:2HR(有机相)Cu2(水相) CuR
2
(有机相)2H(水相),下列说法正确的有
_______。
A.向萃取液中加入稀硫酸进行“反萃取”,可得到单质Cu
B.萃余液中的阳离子为:Fe2、Ni2、Mg2
nCuR
2 4
C.一定条件下,萃取平衡时,
n
Cu2+ ,则 的萃取率为80%
Cu2
D.为提高Cu2的萃取率,可适当提高溶液pH
(5)已知K Ni(OH) 21015,“滤液”中c Ni2 0.2molL1 ,“沉镍”时,控制pH为8.50,此时
sp 2
Ni2的沉淀率为_______,“沉镍”后的母液,含有的主要溶质为_______(填化学式)。
【答案】(除标明外,每空2分)
(1)+3(1分)
(2)适当升高温度、适当增压、将高镁低品位铜镍矿粉碎以增大固液接触面积或适当增大硫酸的浓度(1
分)
(3) SiO、HSiO 或难溶性硅酸盐 4CuFeS+10H SO +5O =4CuSO+2Fe (SO )+8S↓+10H O
2 2 3 2 2 4 2 4 2 4 3 2
(4)CD
(5)99.9% MgSO
4
【解析】由题干工艺流程图可知,向高镁低品位铜镍矿(主要成分为CuFeS、FeS、3NiO·4SiO ·H O、
2 2 2 2
3MgO·4SiO ·H O等)中加入O、HSO 进行氧压浸出,将铁元素转化为Fe (SO ),镍元素转化为NiSO 、
2 2 2 2 4 2 4 3 4
铜元素转化为CuSO 、镁元素转化为MgSO ,硫元素转化为S单质,过滤得到滤渣主要成分为SiO 和S,
4 4 2
用铜离子萃取剂萃取出Cu2+,分液得到萃取液,萃余液中主要含有Fe3+、Mg2+、Ni2+,向萃余液中加入
NaSO 和MgO进行沉铁将Fe3+转化为NaFe (SO )(OH) 、过滤出沉淀,向滤液中加入MgO将Ni2+以
2 4 3 4 2 6
Ni(OH) 的形成沉淀,最后对Ni(OH) 进行处理制得Ni,母液中主要溶质为MgSO 。
2 2 4
(1)已知钠离子带一个正电荷,硫酸根带2个负电荷,氢氧根带一个负电荷,根据化合价代数和为0可知NaFe
3
SO
4
2
(OH)
6
中,Fe元素的化合价为+3价,故答案为:+3;
(2)将高镁低品位铜镍矿粉碎以增大固液接触面积、适当升高反应温度、充分搅拌和适当增大硫酸的浓
度等措施均能提高“氧压浸出”的速率,故答案为:将高镁低品位铜镍矿粉碎以增大固液接触面积或适当
升高反应温度或充分搅拌或适当增大硫酸的浓度;
(3)由分析可知,“氧压浸出”的滤渣有S和SiO,该环节中CuFeS 与HSO 、O 反应生成CuSO 、
2 2 2 4 2 4
Fe (SO )、S和HO,根据氧化还原反应配平可得该反应的化学反应方程式为:
2 4 3 2
4CuFeS+10H SO +5O =4CuSO+2Fe (SO )+8S↓+10H O,故答案为:SiO;
2 2 4 2 4 2 4 3 2 2
4CuFeS+10H SO +5O =4CuSO+2Fe (SO )+8S↓+10H O;
2 2 4 2 4 2 4 3 2
(4)A.向萃取液中加入稀硫酸进行“反萃取”,萃取平衡逆向移动,故可得到Cu2+,得不到单质Cu,A
错误;B.由题干分析结合小问1分析可知,萃余液中主要含有Fe3+、Mg2+、Ni2+,B错误;C.一定条件
nCuR
下,萃取平衡时, n Cu2+ 2 4 ,即被萃取的Cu2+也就是形成CuR 2 的Cu2+是残留在溶液中的Cu2+的4倍,
4
则 的萃取率为 ×100%=80%,C正确;D.适当提高溶液 则H+浓度减小,平衡正向移动,故可
Cu2 4+1 pH
提高Cu2的萃取率,D正确;故答案为:CD;
(5)已知K Ni(OH) 21015,“滤液”中c Ni2 0.2molL1 ,“沉镍”时,控制pH为8.50,此时
sp 2
Ksp[Ni(OH) ] 210-15
溶液中c(OH-)=10-5.5mol/L,溶液中残留的Ni2+浓度为:c(Ni2+)= 2 = =0.0002mol/L,则此
c2(OH-) (10-5.5)2
0.2mol/L-0.02mol/L
时 的沉淀率为 100%≈99.9%,由分析可知,“沉镍”后的母液,含有的主要溶质
Ni2 0.2mol/L
为MgSO ,故答案为:99.9%;MgSO 。
4 4
18.(12分)S-蜂斗菜素,具有的解痉作用,强度是罂粟碱的4~5倍,实验室为探究其元素组成设计如
下实验。回答下列问题:
I.设计实验证明S-蜂斗菜素中含碳、氢、硫三种元素。
(1)从A~F中选择合适的仪器完成实验,正确的连接顺序是a→_______→尾气吸收(按气流方向,用小
写字母表示,仪器不可重复使用)。
(2)装置F中盛放的试剂为_______。
(3)装置E中酸性高锰酸钾溶液足量,所以整个过程中E中现象不太明显,所以实验中能证明药品中含
硫元素的实验现象为_______;E中发生反应的离子方程式为_______。II.测定药品中硫元素的质量分数。
实验步骤:取a g药品,碾碎后,充分燃烧;将产生的SO 气体全部通过V mL c molL1 的碘水;待吸
2 1 1
收完全后,向混合溶液中滴加少量淀粉溶液,再用c molL1硫代硫酸钠标准液滴定,最终消耗硫代硫酸
2
钠溶液的体积为V mL。已知:2S O2I S O22I 。
2 2 3 2 4 6
(4)滴定时盛放硫代硫酸钠溶液的仪器为_______(填仪器名称);该仪器使用前需进行的操作为_______。
(5)滴定终点的现象为_______。
(6)该药品中的硫元素的质量分数为_______(列出表达式即可)。
【答案】(除标明外,每空2分)
(1)jk→de→hi→fg
(2)无水硫酸铜(1分)
(3) C中品红溶液褪色(1分) 2MnO5SO 2H O=5SO2+2Mn24H
4 2 2 4
(4)碱式滴定管 (1分) 检查是否漏液(1分)
(5)滴入最后半滴标准液后,溶液由蓝色褪为无色,且30s不恢复
cV-c V
1 1 2 2 3210-3
(6) 2
100%
a
【分析】由题意可知,整个实验过程中不需要干燥,B装置无需使用,A~F的仪器中,品红用来检验SO ,
2
澄清石灰水用来检验CO ,酸性高锰酸钾溶液用来除去SO ,干燥管中试剂需要检验的是水蒸气,所以应
2 2
该盛放无水硫酸铜,正确的连接顺序是a→jk→de→hi→fg→尾气吸收。
【解析】(1)由分析可知,正确的连接顺序是a→k→de→hi→fg,故答案为:k→de→hi→fg;
(2)由分析可知,装置F中盛放的试剂为无水硫酸铜,故答案为:无水硫酸铜;
(3)装置E中酸性高锰酸钾溶液足量,所以整个过程中E中现象不太明显,所以实验中能证明药品中含
硫元素的实验现象为C中品红溶液褪色;E中发生反应的离子方程式为
2MnO5SO 2H O=5SO2+2Mn24H ,故答案为:C中品红溶液褪色;
4 2 2 4
2MnO5SO 2H O=5SO2+2Mn24H;
4 2 2 4
(4)滴定时盛放硫代硫酸钠溶液的仪器为碱式滴定管;滴定管使用前需进行的操作为检查是否漏液,故
答案为:碱式滴定管;检查是否漏液;
(5)滴定终点的现象为滴入最后半滴标准液后,溶液由蓝色褪为无色,且30 s不恢复,故答案为:滴入
最后半滴标准液后,溶液由蓝色褪为无色,且30s不恢复;
(6)由题意分析可知,由硫代硫酸钠计算剩余的I
2
,用总量减去该数据,可得氧化SO
2
的I
2
,综合计算可
cV-c V /23210-3
得该药品中的硫元素的质量分数为 1 1 2 2 100%,故答案为:
a
cV-c V /23210-3
1 1 2 2 100%。
a19.(12分)聚碳酸酯(D)又称PC塑料,是分子链中含有碳酸酯基的高分子聚合物。由于聚碳酸酯结构上
的特殊性,已成为五大工程塑料中增长速度最快的通用工程塑料。由乙烯为原料合成聚碳酸酯的一种途径
如下图所示:
回答下列问题:
(1)A的核磁共振氢谱只有一种峰,其结构简式为_______;其化学名称为_______。
(2)反应②的反应类型为_______、_______。
(3)写出反应③的化学方程式:_______。
(4)X是 的同系物中最简单的有机物(X含 结构),X的结构共有_______种。
BPA
(5)A与 反应时生成B而不是 的原因是_______。
CO
2
(6)参照上述合成路线,设计以电石为原料制备聚丙烯酸钠的合成路线_______(无机试剂任选)。
【答案】(除标明外,每空2分)
(1) (1分) 环氧乙烷(1分)
(2) 加成反应(1分)
(3)
(4)12
(5)A及CO 中,氧原子的电负性较大,碳氧键中电子偏向氧原子,使氧原子带部分负电荷,碳原子带部
2
分正电荷,所以C与O相结合,生成物为B
催化剂[CH CH]
2 | n
(6)
CaC H2 OCHCHHCNCH CHCNNaOH/H2 OCH CHCOONa COONa
2 催化剂 2 2
(3分)
【解析】(1)A的分子式为C H O,不饱和度为1,A的核磁共振氢谱只有一种峰,结合反应②生成B的
2 4
结构简式可知A的结构简式为 ,其名称为环氧乙烷。(2)从物质的结构变化可知,反应②是CO 的一个CO打开发生的加成反应。
2
(3)反应③是酯交换反应,其方程式为: 。
(4)X是BPA的最简单同系物,说明X含两个苯环及两个羟基,其结构就是将两个羟基连在“
”上,要注意两个苯环可以旋转,X分子结构中有3种等效氢,其一取代物有3种同
分异构体,在此基础上确定二取代物,则有 (7种)、 (4种)、
(1种),共12种。
(5)A及CO 中,氧原子的电负性大于碳原子,碳氧键中电子偏向氧原子,使氧原子带部分负电荷,碳原
2
子带部分正电荷,所以C与O相结合,生成物为B而不是 。
(6)以电石为原料制备聚丙烯酸钠,要解决的主要问题是碳链的增长。电石与水反应制得乙炔,乙炔与
HCN的加成可增长碳链,且水解后可形成羧基。故该流程为:
催化剂[CH CH]
2 | n
。
CaC H2 OCHCHHCNCH CHCNNaOH/H2 OCH CHCOONa COONa
2 催化剂 2 2
20.(12分)油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加以利用。回
答下列问题:
(1)已知下列反应的热化学方程式:
①2H Sg S g2H g H 180kJmol1
2 2 2 1
②CS g2H g CH gS g H 81kJmol1
2 2 4 2 2
则反应③CH
4
g2H
2
Sg CS
2
g4H
2
g 的ΔH
3
=________kJmol1;下列叙述能说明反应③达到平
衡状态的是___________(填标号)。
A.断裂2molCH键的同时生成1molCS键
B.恒容条件下,体系压强不再变化
C.恒容条件下,气体的密度不再变化
D.υ H S2υ CS
正 2 逆 2
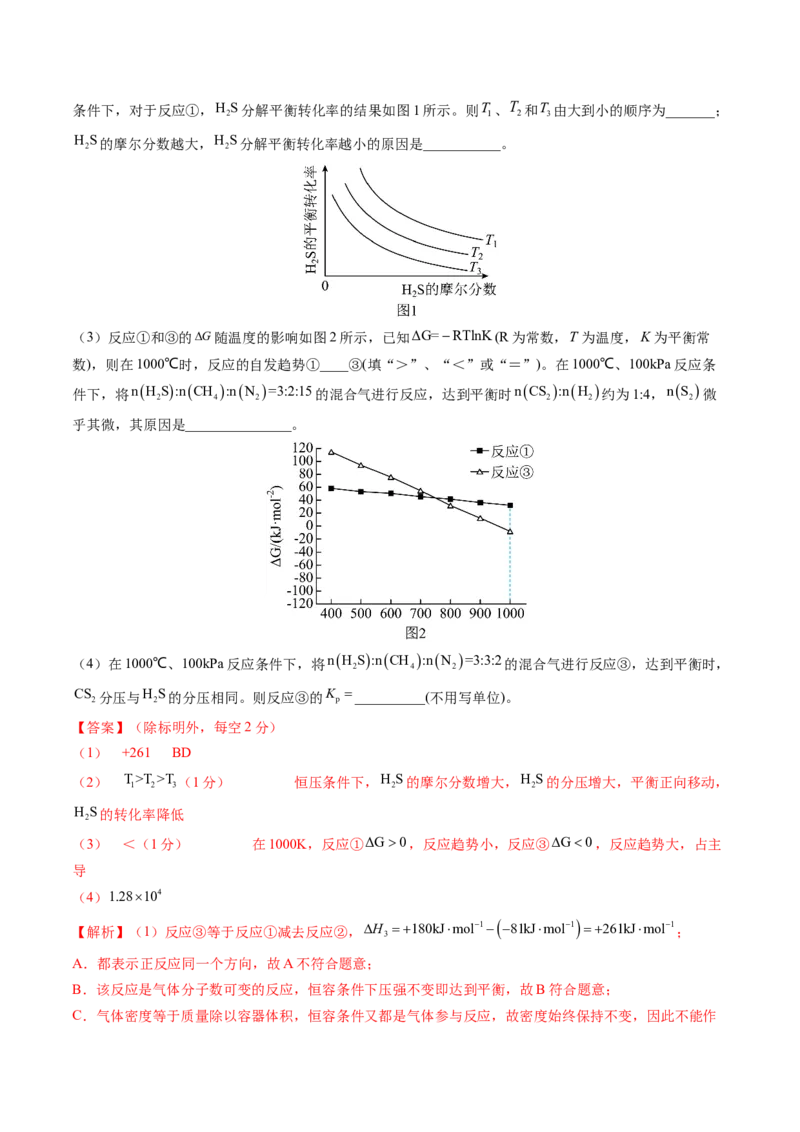
(2)在不同温度、反应压强为100kPa,进料H S的摩尔分数(可看成体积分数)为0.1%~20%(其余为N )的
2 2条件下,对于反应①,H S分解平衡转化率的结果如图1所示。则T 、 T 和T 由大到小的顺序为_______;
2 1 2 3
H S的摩尔分数越大,H S分解平衡转化率越小的原因是___________。
2 2
(3)反应①和③的G随温度的影响如图2所示,已知ΔG=RTlnK(R为常数,T 为温度,K为平衡常
数),则在1000℃时,反应的自发趋势①____③(填“>”、“<”或“=”)。在1000℃、100kPa反应条
件下,将nH S:nCH :nN =3:2:15的混合气进行反应,达到平衡时nCS :nH 约为1:4,nS
微
2 4 2 2 2 2
乎其微,其原因是_______________。
(4)在1000℃、100kPa反应条件下,将nH S:nCH :nN =3:3:2的混合气进行反应③,达到平衡时,
2 4 2
CS 分压与H S的分压相同。则反应③的K __________(不用写单位)。
2 2 p
【答案】(除标明外,每空2分)
(1) +261 BD
(2) T>T >T (1分) 恒压条件下,H S的摩尔分数增大,H S的分压增大,平衡正向移动,
1 2 3 2 2
H S的转化率降低
2
(3) <(1分) 在1000K,反应①ΔG0,反应趋势小,反应③G0,反应趋势大,占主
导
(4)1.28104
【解析】(1)反应③等于反应①减去反应②,H 180kJmol1 81kJmol1 261kJmol1 ;
3
A.都表示正反应同一个方向,故A不符合题意;
B.该反应是气体分子数可变的反应,恒容条件下压强不变即达到平衡,故B符合题意;
C.气体密度等于质量除以容器体积,恒容条件又都是气体参与反应,故密度始终保持不变,因此不能作为平衡的标志,故C不符合题意;
D.有υ H S2υ CS ,一个正反应,一个逆反应,速率之比等于计量系数之比,则达到平衡,故D
正 2 逆 2
符合题意;
故答案为:+261;BD。
(2)反应①是吸热反应,温度越高,平衡正向移动,则H S的转化率越大,故T>T >T ;恒压条件下,
2 1 2 3
H S的摩尔分数增大,H S的分压增大,平衡正向移动,H S的转化率降低;故答案为:T>T >T ;恒压
2 2 2 1 2 3
条件下,H S的摩尔分数增大,H S的分压增大,平衡正向移动,H S的转化率降低。
2 2 2
(3)在1000K,反应①ΔG0,不易自发,反应③G0,容易自发,故反应自发趋势①<③;根据图
中曲线和ΔG=RTlnK可知ΔG越大,反应平衡常数K越小,反应趋势越小,在1000K,反应①ΔG0,
反应趋势小,反应③G0,反应趋势大,占主导;故答案为:<;在1000K,反应①ΔG0,反应趋势
小,反应③G0,反应趋势大,占主导。
CH
4
(g) +2H
2
S(g)
CS
2
(g) +4H
2
(g)
初始 3mol 3mol 0 0
(4)设 ,列三段式 ,达到平衡时,
转化 xmol 2xmol xmol 4xmol
nH S=3mol 平衡 (3x)mol (32x)mol xmol 4xmol
2
CS
2
分压与H
2
S的分压相同即有32xx,求解x1,平衡后气体的总物质的量为
1 4
100 (100 )4
,则K 10 10 1.28104 ;故答案为: 。
p 2 1
100 (100 )2
2mol1mol1mol4mol2mol10mol 10 10 1.28104