文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(山东专用)
黄金卷04
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 V 51
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.化学与食品密切相关.下列说法正确的是
A.健康食品不含任何添加剂 B.烘焙面包用小苏打作膨松剂
C.氮气防腐是利用了氮气的物理性质 D.食品袋中放置生石灰可防止氧化变质
2.下列各项实验的基本操作,其中正确的是
A.用湿润的pH试纸测定硫酸溶液的pH
B.用浓硫酸干燥二氧化硫
C.金属钠着火时,用泡沫灭火器灭火
D.蒸发操作中,将蒸发皿放在铁架台的铁圈上,并垫上石棉网加热
3.下列说法错误的是
A.顺-2-丁烯和反-2-丁烯加氢产物相同
B.苯酚和甲醛通过加聚反应可制得高分子材料
C.可用酸性KMnO 溶液鉴别甲苯和环已烷
4
D.淀粉和纤维素在酸作用下水解的最终产物都是葡萄糖
4.向含 的废水中加入铁粉和 可制备 ,反应如下
,下列说法正确的是
A. 的电子式为
B.加入 的作用是提供 和调节
C. 电离方程式:
D.反应中每生成 转移 电子
5.物质的结构决定物质的性质。设N 为阿伏加德罗常数的值。下列说法错误的是
A
A.DNA通过氢键结合成稳定的双螺旋结构
B.46g由二甲醚(CHOCH )和乙醇组成的混合物中,杂化方式为sp2杂化的原子数为2N
3 3 A
C.键角:CO >NF >P
3 4
D.基态Mn原子中,两种自旋状态的电子数之比为2∶3
6.近日北京大学肿瘤医院发现,天然小分子白皮杉醇在胃癌治疗中有重要应用价值。其结构如图所示,
下列有关白皮杉醇的说法正确的是
A.不能使酸性 溶液褪色B.苯环上氢原子的一氯代物有4种
C. 白皮杉醇最多能与 发生反应
D. 白皮杉醇最多能与 发生加成反应
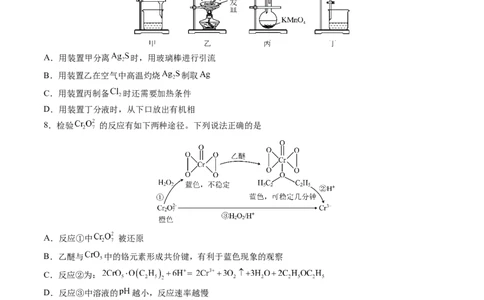
7.实验室从废定影液[含 和 等]中回收 和 的主要步骤为:向废定影液中加入 溶液
沉银,过滤、洗涤及干燥,灼烧 制 ;制取 并通入滤液氧化 ,用苯萃取分液。其中部分操作
的装置如图,下列叙述正确的是
A.用装置甲分离 时,用玻璃棒进行引流
B.用装置乙在空气中高温灼烧 制取
C.用装置丙制备 时还需要加热条件
D.用装置丁分液时,从下口放出有机相
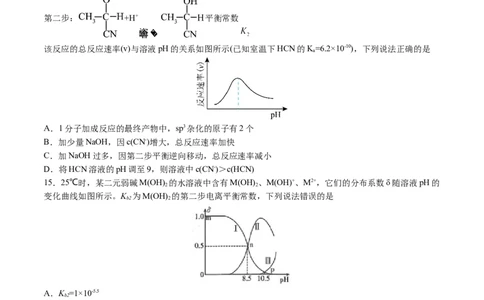
8.检验 的反应有如下两种途径。下列说法正确的是
A.反应①中 被还原
B.乙醚与 中的铬元素形成共价键,有利于蓝色现象的观察
C.反应②为:
D.反应③中溶液的 越小,反应速率越慢
9.室温下,下列实验探究方案能达到探究目的的是
选项 探究方案 探究目的
将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加KSCN溶液,观察 食品脱氧剂样品中有无+3价
A
溶液颜色变化 铁
B 用pH计测量等浓度的醋酸、盐酸的pH,比较溶液pH大小 是弱电解质
炭可与浓HNO 反应生成
3
C 向浓HNO 中插入红热的炭,观察生成气体的颜色
3
NO
2向淀粉溶液中加适量20%H SO 溶液,加热,冷却后加NaOH溶液 淀粉溶液在稀硫酸和加热条
2 4
D
至碱性,再加少量碘水,观察溶液颜色变化 件下是否水解
10.X、Y、Z、W、Q是原子序数依次增大且不超过20的主族元素。X是地壳中含量最多的元素,Y基态
原子核外s能级和p能级电子数相等,Z与X同主族,Q的焰色试验呈紫色。列说法正确的是
A.简单离子半径;
B.X的第一电离能比同周期的相邻元素的大
C.Z的简单气态氢化物的热稳定性比W的强
D.Q最高价氧化物对应水化物的碱性比Y的弱
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得
4分,选对但不全的得2分,有选错的得0分。
11.以铁硼矿(主要成分为 和 ,还有少量 、FeO、CaO、 和 等)为原料
制备硼酸 的工艺流程如图所示:
下列说法错误的是
A.浸渣中的物质是 、 和
B.“净化除杂”需先加 溶液再调节溶液的pH
C.操作a为蒸发浓缩、冷却结晶
D.“粗硼酸”中的主要杂质是氢氧化铝
12.实验室分别进行如下实验:①向 溶液中滴加酸性 溶液,溶液由蓝色变为淡黄色;②向
溶液中滴加浓盐酸,产生黄绿色气体,溶液变蓝。已知 ;蓝色; :淡黄色、强氧化
性。下列说法错误的是
A.①中氧化剂与还原剂物质的量之比为
B.②的离子反应为
C.由①②可知,氧化性:
D. 溶液中滴加 可发生反应
13.我国科学家利用 电池,以 水溶液作为锌离子电池的介质,可实现快速可逆的协同转化
反应。如图所示,放电时该电池总反应为: 。下列说法正确的是A.放电时,Zn为负极,发生氧化反应
B.放电时, 参与反应,转移
C.充电时, 通过阳离子交换膜从 极移向 极
D.充电时,阳极发生反应:
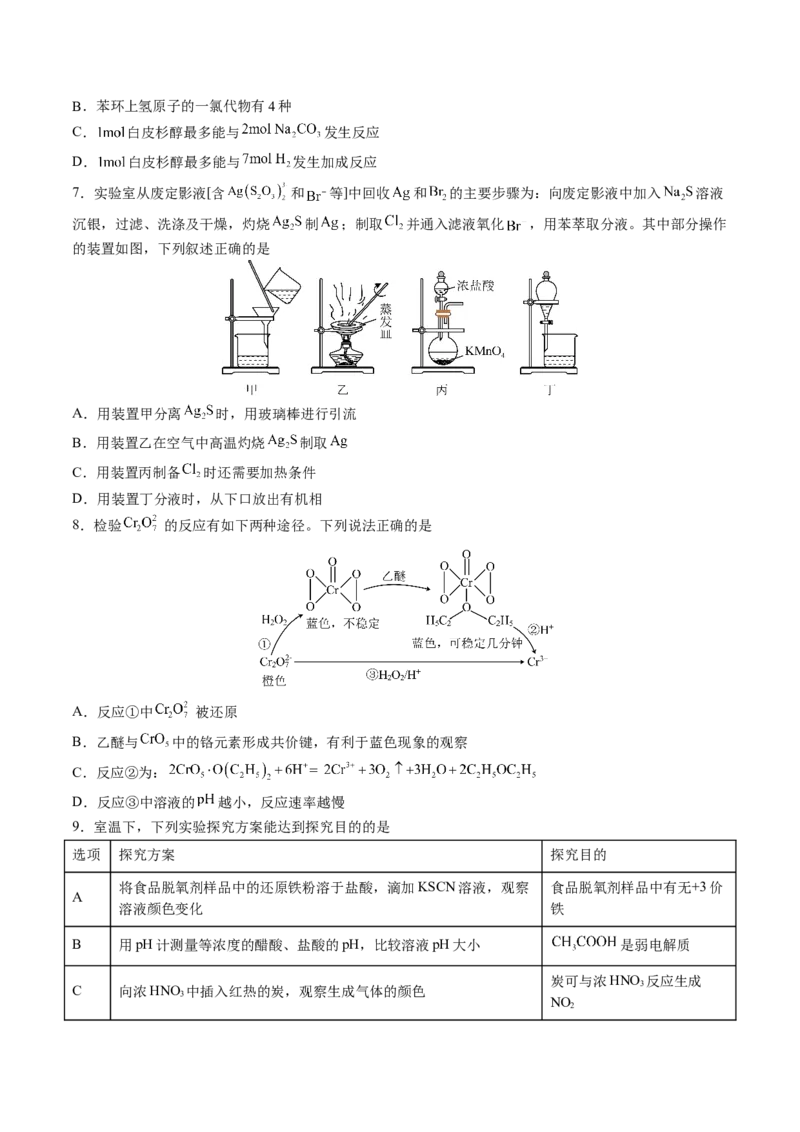
14.乙醛与HCN的加成反应分两步进行:
第一步: +CN- 平衡常数
第二步: +H+ 平衡常数
该反应的总反应速率(v)与溶液pH的关系如图所示(已知室温下HCN的K=6.2×10-10),下列说法正确的是
a
A.1分子加成反应的最终产物中,sp3杂化的原子有2个
B.加少量NaOH,因c(CN-)增大,总反应速率加快
C.加NaOH过多,因第二步平衡逆向移动,总反应速率减小
D.将HCN溶液的pH调至9,则溶液中c(CN-)>c(HCN)
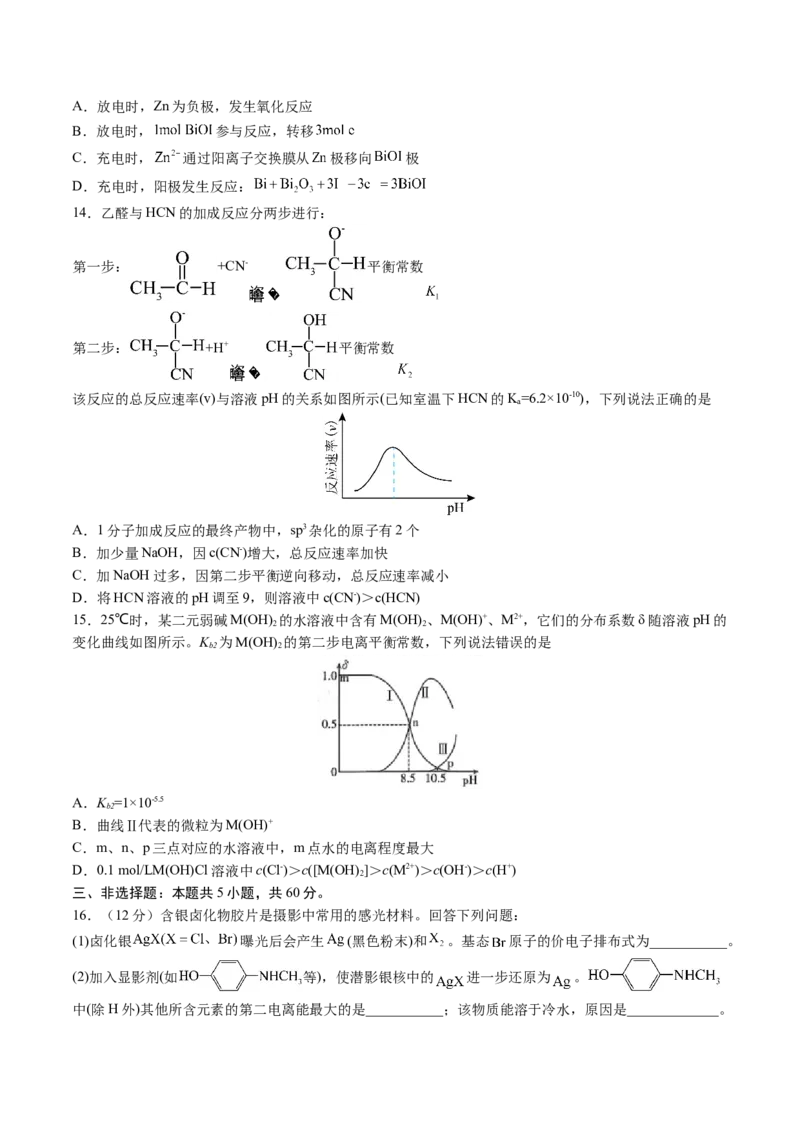
15.25℃时,某二元弱碱M(OH) 的水溶液中含有M(OH) 、M(OH)+、M2+,它们的分布系数δ随溶液pH的
2 2
变化曲线如图所示。K 为M(OH) 的第二步电离平衡常数,下列说法错误的是
b2 2
A.K =1×10-5.5
b2
B.曲线Ⅱ代表的微粒为M(OH)+
C.m、n、p三点对应的水溶液中,m点水的电离程度最大
D.0.1 mol/LM(OH)Cl溶液中c(Cl-)>c([M(OH) ]>c(M2+)>c(OH-)>c(H+)
2
三、非选择题:本题共5小题,共60分。
16.(12分)含银卤化物胶片是摄影中常用的感光材料。回答下列问题:
(1)卤化银 曝光后会产生 (黑色粉末)和 。基态 原子的价电子排布式为___________。
(2)加入显影剂(如 等),使潜影银核中的 进一步还原为 。
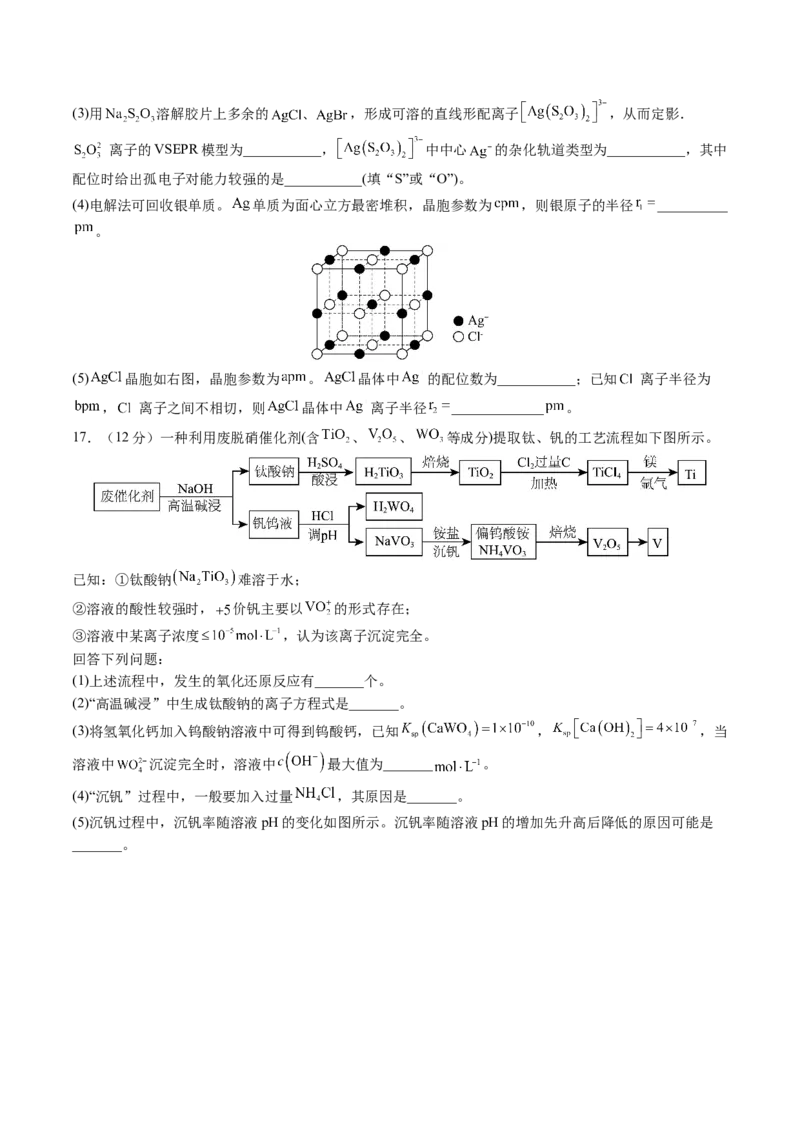
中(除H外)其他所含元素的第二电离能最大的是___________;该物质能溶于冷水,原因是_____________。(3)用 溶解胶片上多余的 ,形成可溶的直线形配离子 ,从而定影.
离子的VSEPR模型为___________, 中中心 的杂化轨道类型为___________,其中
配位时给出孤电子对能力较强的是___________(填“S”或“O”)。
(4)电解法可回收银单质。 单质为面心立方最密堆积,晶胞参数为 ,则银原子的半径 __________
。
(5) 晶胞如右图,晶胞参数为 。 晶体中 的配位数为___________;已知 离子半径为
, 离子之间不相切,则 晶体中 离子半径 _____________ 。
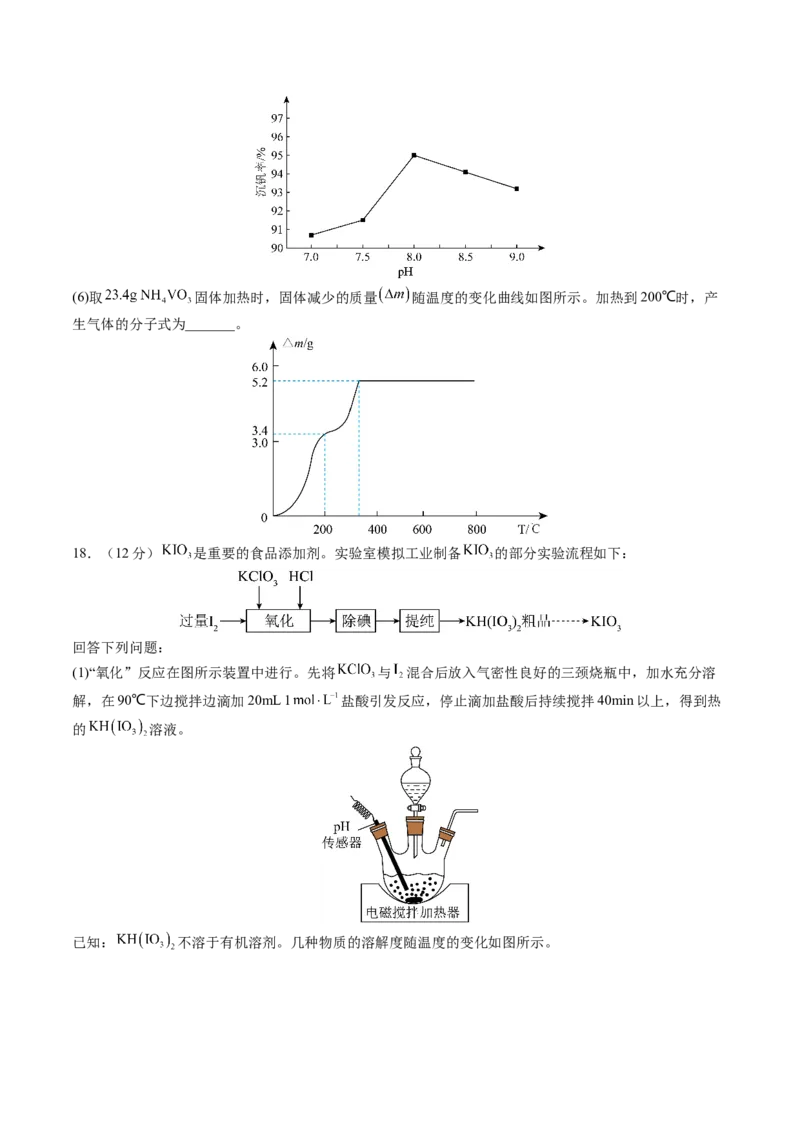
17.(12分)一种利用废脱硝催化剂(含 、 、 等成分)提取钛、钒的工艺流程如下图所示。
已知:①钛酸钠 难溶于水;
②溶液的酸性较强时, 价钒主要以 的形式存在;
③溶液中某离子浓度 ,认为该离子沉淀完全。
回答下列问题:
(1)上述流程中,发生的氧化还原反应有_______个。
(2)“高温碱浸”中生成钛酸钠的离子方程式是_______。
(3)将氢氧化钙加入钨酸钠溶液中可得到钨酸钙,已知 , ,当
溶液中 沉淀完全时,溶液中 最大值为_______ 。
(4)“沉钒”过程中,一般要加入过量 ,其原因是_______。
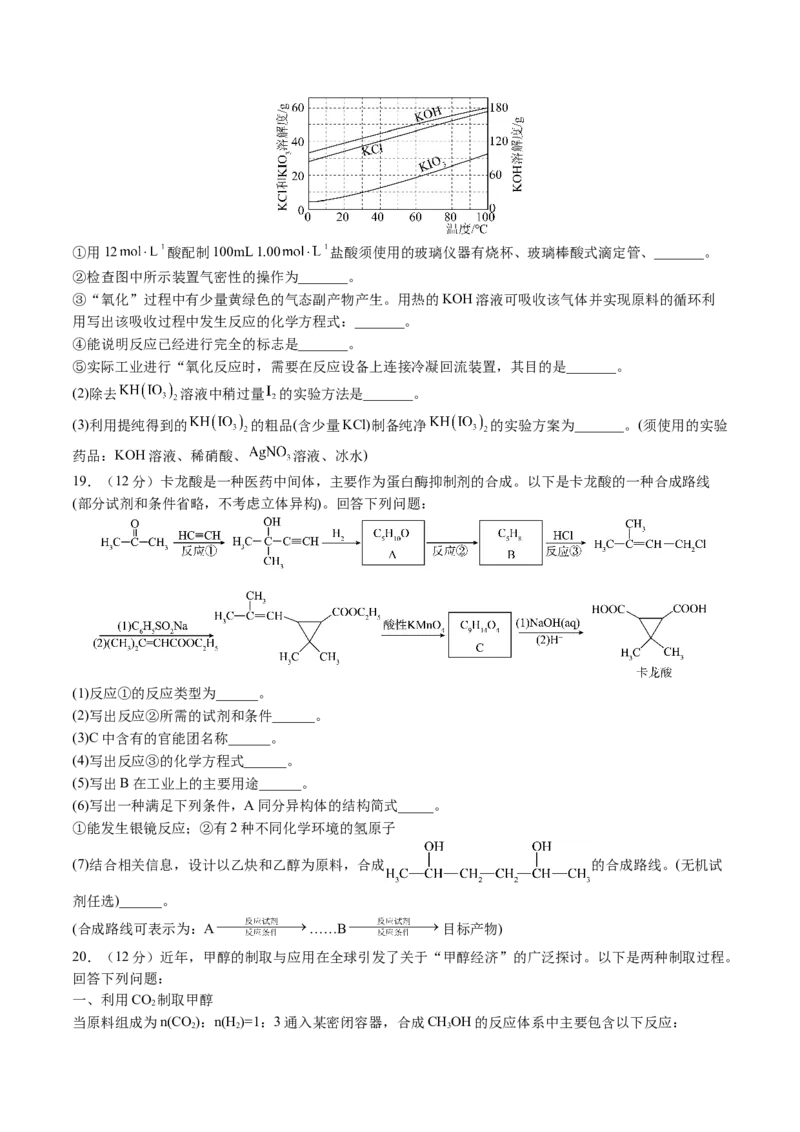
(5)沉钒过程中,沉钒率随溶液pH的变化如图所示。沉钒率随溶液pH的增加先升高后降低的原因可能是
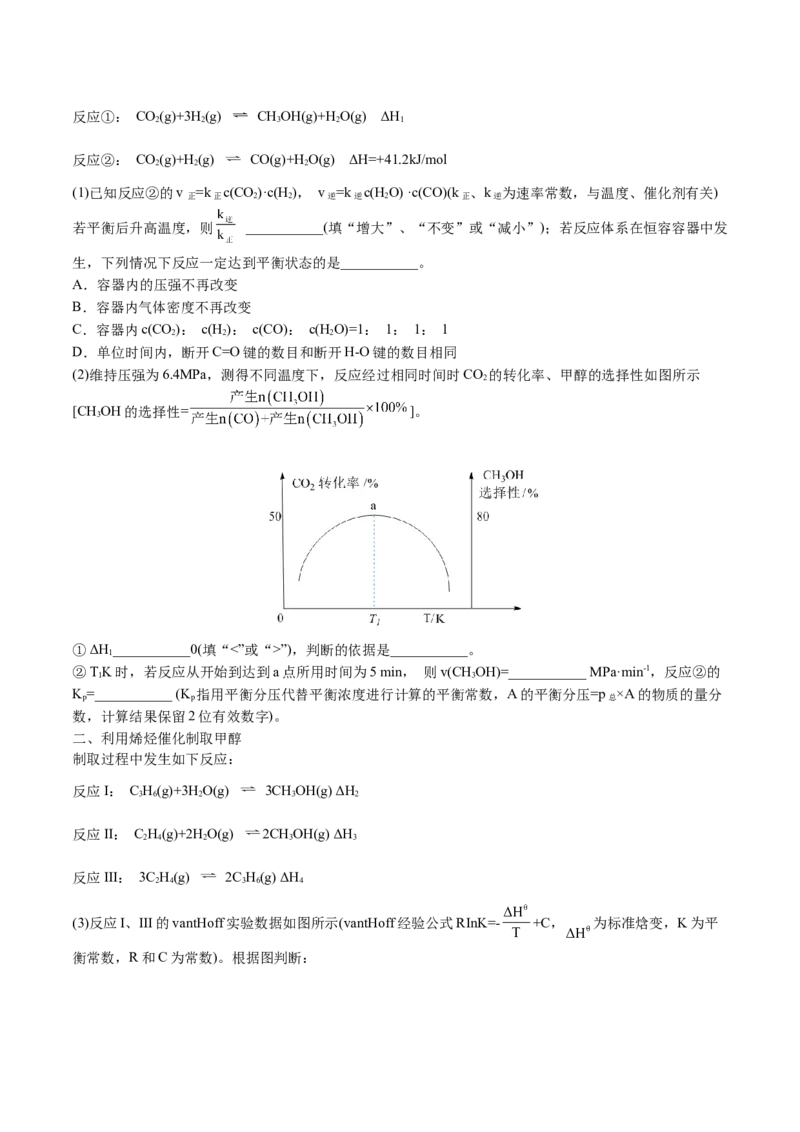
_______。(6)取 固体加热时,固体减少的质量 随温度的变化曲线如图所示。加热到200℃时,产
生气体的分子式为_______。
18.(12分) 是重要的食品添加剂。实验室模拟工业制备 的部分实验流程如下:
回答下列问题:
(1)“氧化”反应在图所示装置中进行。先将 与 混合后放入气密性良好的三颈烧瓶中,加水充分溶
解,在90℃下边搅拌边滴加20mL 1 盐酸引发反应,停止滴加盐酸后持续搅拌40min以上,得到热
的 溶液。
已知: 不溶于有机溶剂。几种物质的溶解度随温度的变化如图所示。①用12 酸配制100mL 1.00 盐酸须使用的玻璃仪器有烧杯、玻璃棒酸式滴定管、_______。
②检查图中所示装置气密性的操作为_______。
③“氧化”过程中有少量黄绿色的气态副产物产生。用热的KOH溶液可吸收该气体并实现原料的循环利
用写出该吸收过程中发生反应的化学方程式:_______。
④能说明反应已经进行完全的标志是_______。
⑤实际工业进行“氧化反应时,需要在反应设备上连接冷凝回流装置,其目的是_______。
(2)除去 溶液中稍过量 的实验方法是_______。
(3)利用提纯得到的 的粗品(含少量KCl)制备纯净 的实验方案为_______。(须使用的实验
药品:KOH溶液、稀硝酸、 溶液、冰水)
19.(12分)卡龙酸是一种医药中间体,主要作为蛋白酶抑制剂的合成。以下是卡龙酸的一种合成路线
(部分试剂和条件省略,不考虑立体异构)。回答下列问题:
(1)反应①的反应类型为______。
(2)写出反应②所需的试剂和条件______。
(3)C中含有的官能团名称______。
(4)写出反应③的化学方程式______。
(5)写出B在工业上的主要用途______。
(6)写出一种满足下列条件,A同分异构体的结构简式_____。
①能发生银镜反应;②有2种不同化学环境的氢原子
(7)结合相关信息,设计以乙炔和乙醇为原料,合成 的合成路线。(无机试
剂任选)______。
(合成路线可表示为:A ……B 目标产物)
20.(12分)近年,甲醇的制取与应用在全球引发了关于“甲醇经济”的广泛探讨。以下是两种制取过程。
回答下列问题:
一、利用CO 制取甲醇
2
当原料组成为n(CO):n(H )=1:3通入某密闭容器,合成CHOH的反应体系中主要包含以下反应:
2 2 3反应①: CO(g)+3H(g) CHOH(g)+H O(g) ΔH
2 2 3 2 1
反应②: CO(g)+H(g) CO(g)+H O(g) ΔH=+41.2kJ/mol
2 2 2
(1)已知反应②的v =k c(CO)·c(H), v =k c(HO) ·c(CO)(k 、k 为速率常数,与温度、催化剂有关)
正 正 2 2 逆 逆 2 正 逆
若平衡后升高温度,则 ___________(填“增大”、“不变”或“减小”);若反应体系在恒容容器中发
生,下列情况下反应一定达到平衡状态的是___________。
A.容器内的压强不再改变
B.容器内气体密度不再改变
C.容器内c(CO): c(H): c(CO): c(HO)=1: 1: 1: 1
2 2 2
D.单位时间内,断开C=O键的数目和断开H-O键的数目相同
(2)维持压强为6.4MPa,测得不同温度下,反应经过相同时间时CO 的转化率、甲醇的选择性如图所示
2
[CHOH的选择性= ]。
3
①ΔH___________0(填“<”或“>”),判断的依据是___________。
1
②TK时,若反应从开始到达到a点所用时间为5 min, 则v(CHOH)=___________ MPa·min-1,反应②的
1 3
K=___________ (K 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=p ×A的物质的量分
p p 总
数,计算结果保留2位有效数字)。
二、利用烯烃催化制取甲醇
制取过程中发生如下反应:
反应I: C H(g)+3HO(g) 3CHOH(g) ΔH
3 6 2 3 2
反应II: C H(g)+2HO(g) 2CHOH(g) ΔH
2 4 2 3 3
反应III: 3C H(g) 2C H(g) ΔH
2 4 3 6 4
(3)反应I、III的vantHoff实验数据如图所示(vantHoff经验公式RInK=- +C, 为标准焓变,K为平
衡常数,R和C为常数)。根据图判断:ΔH=___________(用含ΔH 和ΔH 的计算式表示),反应III的 ___________ kJ ·mol-1。
3 2 4