文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(湖北专用)
黄金卷05
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Fe 56 Co 59 Cu 64 Ga 70
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.中华优秀传统文化源远流长,化学与文化传承密不可分。下列说法正确的是
A.海昏侯墓出土了大量保存完好的精美金器,这与金的惰性有关
B.“丹砂(HgS)烧之成水银,积变又还成丹砂”中涉及的反应为可逆反应
C.“九秋风露越窑开,夺得千峰翠色来”,“翠色”是因为成分中含有氧化亚铜
D.“世间丝、麻、裘、褐皆具素质”,“丝、麻、裘”的主要成分都是蛋白质
【答案】A
【解析】A.金的化学性质稳定,使得其能保存完好,故A正确;B.“丹砂(HgS)烧之成水银,积变又还
成丹砂”中涉及的两个反应条件不同,不为可逆反应,故B错误;C.“翠色”为青色或者绿色,而氧化
亚铜为砖红色,可能来自亚铁离子,诗句中的“翠色”不可能来自氧化亚铜,故C错误;D.“麻”的主
要成分是纤维素,故D错误;故答案选A。
2.自然科学的尽头是哲学,中学化学教材中蕴含着许多哲学思想和观点。下列说法错误的是
A.氧化还原反应相关概念及联系体现了对立统一规律
B.同主族元素所表现的性质体现了矛盾只有普遍性无特殊性
C.两物质反应因某一物质浓度不同而产物不同体现了量变质变规律
D.化学反应中的各种守恒关系体现了事物变化发展及普遍联系的一般规律。
【答案】B
【解析】A.氧化还原反应相关概念例如氧化剂、还原剂;被氧化、被还原等体现了对立统一规律,故A
正确;B.同主族元素所表现的性质体现了矛盾既有普遍性也有特殊性,例如同主族元素的最高正化合价
相同,但是氧和氟没有正价,故B错误;C.两物质反应因某一物质浓度不同而产物不同体现了量变质变
规律,例如稀硫酸与Fe反应生成氢气,浓硫酸使Fe钝化,故C正确;D.化学反应中的各种守恒关系体
现了事物变化发展及普遍联系的一般规律,例如质量守恒、电荷守恒等,故D正确。答案选B。3.我国古代的青铜器工艺精湛,有很高的艺术价值和历史价值。下列说法不正确的是
A.商代后期制作的司母戊鼎,其主要成分是铜合金
B.青铜文物在潮湿的土壤环境中比在干燥的环境中易被腐蚀
C.与火法冶铜(以Cu S为原料)相比,采用湿法冶铜(以CuSO 为原料)的优点是减少了环境污染和能源消
2 4
耗
D.《本草纲目》中载有一药物,名“铜青”,铜青是铜器上的绿色物质,则铜青就是青铜
【答案】D
【解析】A.司母戊鼎是已知中国古代最重的青铜器,司母戊鼎是铜与锌等金属熔合而成的合金,A正确;
B.青铜文物为合金,在潮湿环境中易形成原电池,发生电化学腐蚀,腐蚀速率更快,B正确;C.火法治
铜(以Cu S为原料)会产生SO ,对环境造成污染,同时高温条件下耗能较高,而湿法治铜(以CuSO 为原
2 2 4
料)采用置换反应原理,相比火法治铜减少了环境污染和能源的消耗,C正确;D.铜青是铜器上的绿色物
质,则铜青是铜绿,而青铜是合金,D错误。答案选D。
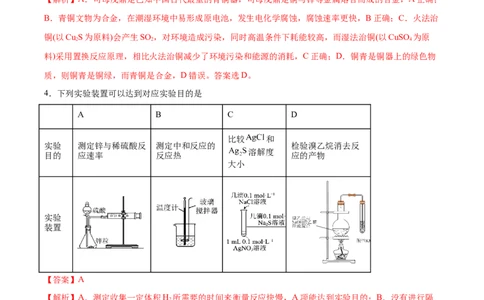
4.下列实验装置可以达到对应实验目的是
A B C D
比较 和
实验 测定锌与稀硫酸反 测定中和反应的 检验溴乙烷消去反
溶解度
目的 应速率 反应热 应的产物
大小
实验
装置
【答案】A
【解析】A.测定收集一定体积H 所需要的时间来衡量反应快慢,A项能达到实验目的;B.没有进行隔
2
热和保温,B项不能达到实验目的;C.加入NaCl溶液后溶液中有AgCl、AgNO,再加入NaS产生黑色
3 2
沉淀,可能来自于AgNO 的转化也可能是AgCl,无法确定AgCl转化为Ag S,无法比较溶解度大小,C项
3 2
不能达到实验目的;D.挥发的乙醇也能使酸性高锰酸钾褪色从而干扰烯烃的检验,D项不能达到实验目
的;故选A。
5.N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.12g金刚石含碳碳单键的数目为4N
A
B.高温下铁粉与水蒸气反应,固体质量增加6.4g,反应转移的电子数为0.8N
AC.1molCO 与足量NaOH溶液反应,溶液中 的数目为N
2 A
D.2.8g 中含有的质子数为1.4N
A
【答案】B
【解析】A.在金刚石晶体中,每个碳原子与相邻的4个碳原子共形成4个共价键,平均每个碳原子形成2
个共价键,则12g金刚石(含C的物质的量为1mol)含碳碳单键的数目为2N ,A不正确;B.高温下铁粉与
A
水蒸气反应,生成Fe O 和H,固体质量增加6.4g,增加的质量为参加反应HO中O元素的质量,则水的
3 4 2 2
物质的量为 =0.4mol,HO中的H元素全部转化为H,所以反应转移的电子数为
2 2
0.4mol×2N =0.8N ,B正确;C.1molCO 与足量NaOH溶液反应,生成1mol ,但 在水溶液中会
A A 2
发生水解,所以溶液中 的数目小于为N ,C不正确;D.1个 的质子数为14,2.8g 的物质的
A
量为 ,则含有的质子数为 <1.4N ,D不正确;故选B。
A
6.下列化学用语表示错误的是
A.MgCl 的电子式:
2
B.NH 分子的VSEPR模型:
3
C.用化学方程式表示FeO在空气中受热:6FeO+O 2Fe O
2 3 4
D.用离子方程式表示氨水中滴入少量硝酸银溶液:Ag++ 2 NH·H O =[AgNH )]++2H O
3 2 3 2 2
【答案】B
【解析】A.MgCl 是离子化合物,电子式为 ,A项正确;B. NH 分子中心原子的价
2 3层电子对数 ,VSEPR模型为正四面体形,B项错误;C.FeO在空气中受热生成四氧化三铁,
化学方程式为:6FeO+O 2Fe O,C项正确;D.由于氨水是过量的,则生成了稳定的[Ag(NH)]+,正确
2 3 4 3 2
的离子方程式为:Ag++ 2NH ·H O =[AgNH )]++2H O,D项正确;故选B。
3 2 3 2 2
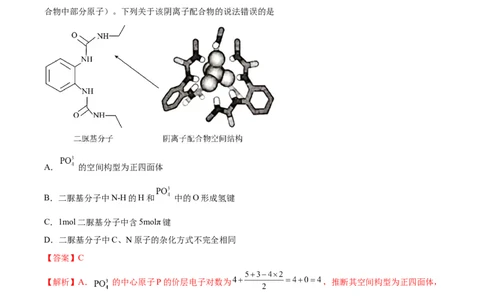
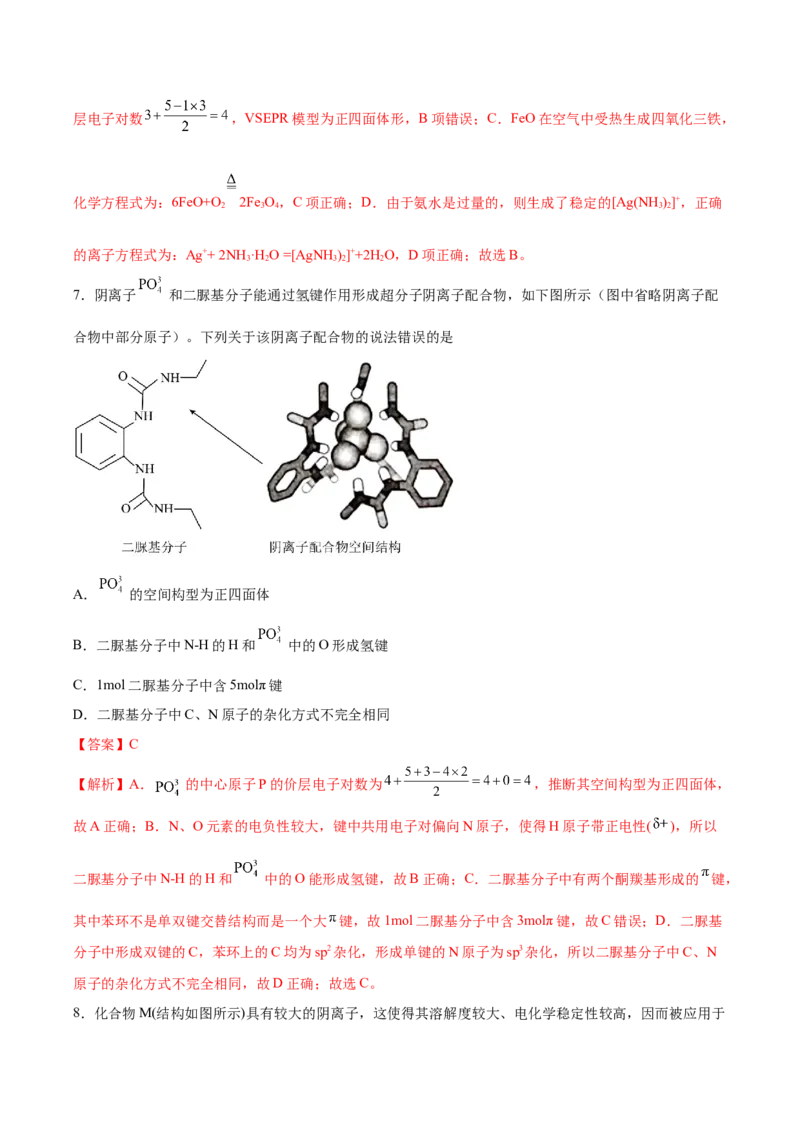
7.阴离子 和二脲基分子能通过氢键作用形成超分子阴离子配合物,如下图所示(图中省略阴离子配
合物中部分原子)。下列关于该阴离子配合物的说法错误的是
A. 的空间构型为正四面体
B.二脲基分子中N-H的H和 中的O形成氢键
C.1mol二脲基分子中含5molπ键
D.二脲基分子中C、N原子的杂化方式不完全相同
【答案】C
【解析】A. 的中心原子P的价层电子对数为 ,推断其空间构型为正四面体,
故A正确;B.N、O元素的电负性较大,键中共用电子对偏向N原子,使得H原子带正电性( ),所以
二脲基分子中N-H的H和 中的O能形成氢键,故B正确;C.二脲基分子中有两个酮羰基形成的 键,
其中苯环不是单双键交替结构而是一个大 键,故1mol二脲基分子中含3molπ键,故C错误;D.二脲基
分子中形成双键的C,苯环上的C均为sp2杂化,形成单键的N原子为sp3杂化,所以二脲基分子中C、N
原子的杂化方式不完全相同,故D正确;故选C。
8.化合物M(结构如图所示)具有较大的阴离子,这使得其溶解度较大、电化学稳定性较高,因而被应用于电池电解液中。M的组成元素W、X、Y、Z、L均为短周期主族元素且原子半径依次增大,基态L原子仅
s能级上填充电子,基态Y原子s能级上的电子数是p能级上的2倍,W的简单氢化物的沸点高于同主族
相邻元素。下列说法正确的是
A.元素的第一电离能:Y>X>W
B.M中属于p区的元素有4种
C.L形成的单质在X形成的单质中燃烧主要生成
D.M中L和Z元素最外层均不满足 结构
【答案】B
【分析】由题干信息可知,M的组成元素W、X、Y、Z、L均为短周期主族元素且原子半径依次增大,基
态L原子仅s能级上填充电子结合L为+1价离子,故L为Li,基态Y原子s能级上的电子数是p能级上的
2倍,且Y能形成4个共价键,半径比Li小,故Y为C,原子半径大小在C和Li之间的元素为Be、B,且
Z周围形成4个共价键,则Z为B,W的简单氢化物的沸点高于同主族相邻元素且W的半径最小,则W
为F,X可以形成2个共价键,且半径在F和C之间,故X为O,综上分析可知,W、X、Y、Z、L分别
为F、O、C、B、Li。
【解析】A.由分析可知,W为F、X为O、Y为C,根据同一周期元素第一电离能呈增大趋势,ⅡA与Ⅲ
A、ⅤA与ⅥA反常,故元素的第一电离能为F>O>C即W >X>Y,A错误;B.由分析可知,W、X、
Y、Z、L分别为F、O、C、B、Li,故M中除Li属于s区,其余4种元素属于p区,B正确;C.由分析
可知,X为O、L为Li,L形成的单质即Li在X形成的单质O 中燃烧只能生成LiO即LX,得不到LiO
2 2 2 2 2
即 ,C错误;D.由分析可知,L为Li,Z为B,由题干图示信息可知,Z周围形成4个共价键,即M
中L元素即Li+最外层不满足 结构,而Z元素即B最外层满足 结构,D错误;故答案为:B。
9.湖南大学段阿冰副教授领导的课题组提出了手性磷酸(CPA)催化的环酮和1,4-苯醌的 氧化反应合理
的反应路径模型(如图1所示)和相应的吉布斯自由能曲线图(如图2所示,Ts表示过渡态,RC表示反应过
程中的中间产物)。下列说法正确的是A.从能量的角度看,化合物Ⅰ比Ⅳ更稳定
B.总历程的决速步骤为INT1生成INT2的反应
C.化合物Ⅰ变为Ⅱ过程中存在极性键的断裂与形成
D.催化剂能改变反应机理,加快反应速率,改变反应热,从而提高转化率
【答案】C
【解析】A.能量越低越稳定,从图2中可以看出,化合物Ⅰ比Ⅳ能量更高,因此化合物Ⅳ更稳定,A错
误;B.决速步骤为反应过程中活化能最高的步骤,从图2中可以看出INT1生成INT2的反应活化能并非
最高,B错误;C.化合物Ⅰ变为Ⅱ过程中,存在C-O断裂和O-H形成,因此存在极性键的断裂与形成,
C正确;D.催化剂不能改变改变反应热,无法提高转化率,D错误;故选C。
10.实验室合成并提纯山梨酸乙酯(密度0.926g/cm3,沸点195.5℃)的过程如下图所示。下列说法错误的是
A.操作①控温110℃,不能选用水浴加热的方法
B.操作③中试剂a为碳酸氢钠,可以通过观察气泡现象控制试剂用量
C.操作③④均为分液操作,均应收集下层液体
D.操作②⑤为过滤,操作⑥为蒸馏
【答案】C
【分析】山梨酸、乙醇在浓硫酸作用下发生酯化反应生成山梨酸乙酯,产物混合物过滤除去沸石,滤液中
加碳酸钠溶液把混合物中的山梨酸转化为可溶于水的山梨酸钠,分液,水洗,分液,加干燥剂MgSO 除水,
4
过滤,滤液蒸馏得产品山梨酸乙酯。
【解析】A.水浴加热温度不能高于100℃,操作①控温110℃,不能选用水浴加热的方法,故A正确;B.操作③中试剂a为碳酸氢钠,碳酸钠和山梨酸反应放出二氧化碳气体,可以根据观察气泡现象控制试
剂用量,故B正确;C.操作③④均为分液操作,山梨酸乙酯的密度小于水的密度,均应收集上层液体,
故C错误;D.操作②是分离出沸石,操作⑤是分离出MgSO 固体,②⑤均为过滤,操作⑥是分离山梨酸
4
乙酯和乙醇,用蒸馏法分离,故D正确;选C。
11.一种抗血小板聚集药物X的结构如下图所示。下列说法正确的是
A.1个X分子中含有2个手性碳原子 B.X中存在4种含氧官能团
C.1molX最多能与2molNaOH发生反应 D.X遇 溶液显紫色
【答案】A
【解析】A.根据手性碳原子的定义,该有机物中含有手性碳原子位置如图所示
,该有机物有2个手性碳原子,A正确;B.根据结构简式,含氧官
能团为酯基、醚键和羟基,有三种含氧官能团,B错误;C.该有机物中能与NaOH反应的官能团是酯基,
但 ,1mol该酯基消耗2molNaOH,因此1mol该有机物最多消耗
3molNaOH,C错误;D.不含酚-OH,遇FeCl 溶液不能显紫色,D错误;故选A。
3
12. 和 互为同素异形体,臭氧分子极性较小;离子液体在室温或者稍高于室温会呈现液态,如盐
的熔点只有12℃;分子间氢键广泛存在,如形成平面型多聚硼酸晶体等。下列说法正确的是
A. 在水中的溶解度小于在四氯化碳中的溶解度
B. 和 的中心原子杂化方式不相同C.大多数离子液体由体积大的阴、阳离子构成
D.硼酸晶体在水中的溶解度随温度升高而增大与分子间氢键无关
【答案】C
【解析】A. 和水都是极性分子,四氯化碳为非极性分子,根据相似相溶原理, 在水中的溶解度大于
在四氯化碳中的溶解度,A错误;B. 中心原子S原子的价层电子对数为 , 中
心原子S原子的价层电子对数为 ,故中心原子都采用 杂化,B错误;C.阴阳离子体
积较大,使得阴阳离子间距离较大,离子键较弱,离子液体在室温或者稍高于室温会呈现液态,故大多数
离子液体由体积大的阴、阳离子构成,C正确;D.硼酸分子之间存在氢键,影响硼酸分子与水分子之间
形成氢键,升高温度硼酸溶解度增大是因为硼酸分子间的氢键断裂,重新与水分子形成氢键,D错误;故
选C。
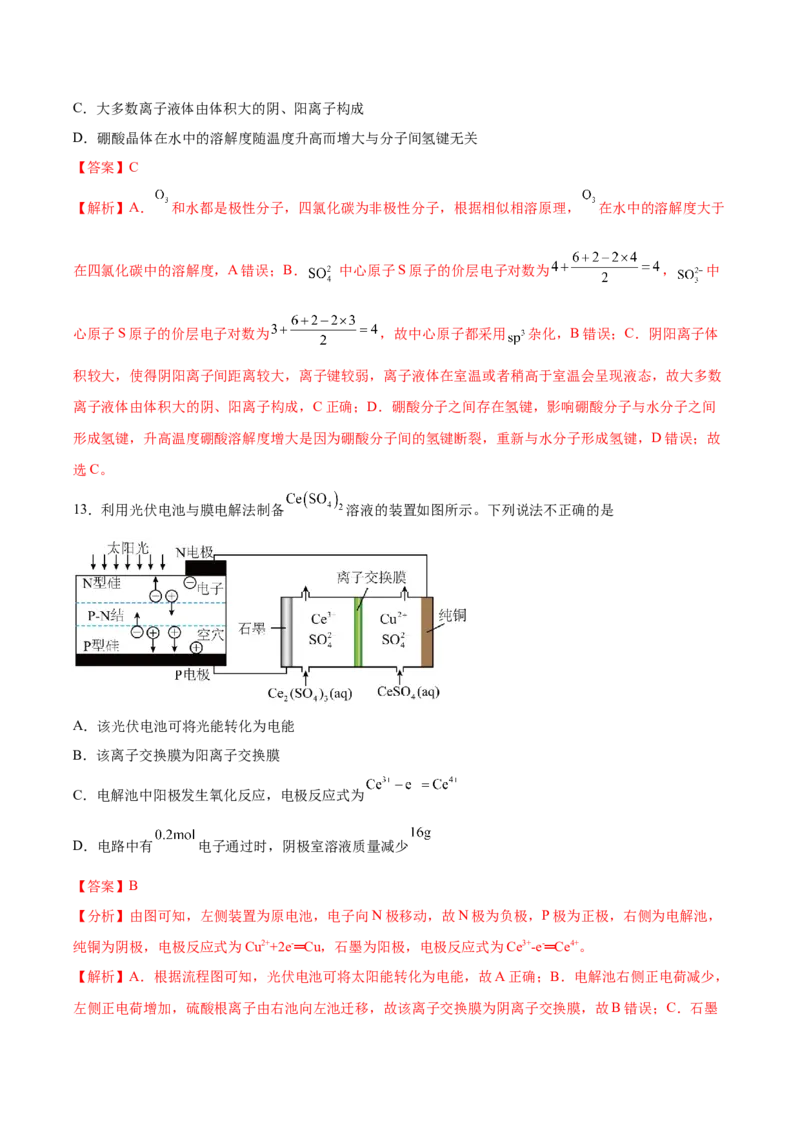
13.利用光伏电池与膜电解法制备 溶液的装置如图所示。下列说法不正确的是
A.该光伏电池可将光能转化为电能
B.该离子交换膜为阳离子交换膜
C.电解池中阳极发生氧化反应,电极反应式为
D.电路中有 电子通过时,阴极室溶液质量减少
【答案】B
【分析】由图可知,左侧装置为原电池,电子向N极移动,故N极为负极,P极为正极,右侧为电解池,
纯铜为阴极,电极反应式为Cu2++2e-═Cu,石墨为阳极,电极反应式为Ce3+-e-═Ce4+。
【解析】A.根据流程图可知,光伏电池可将太阳能转化为电能,故A正确;B.电解池右侧正电荷减少,
左侧正电荷增加,硫酸根离子由右池向左池迁移,故该离子交换膜为阴离子交换膜,故B错误;C.石墨为阳极发生氧化反应,电极反应式为Ce3+-e-═Ce4+,故C正确;D.纯铜为阴极,电极反应式为Cu2++2e-
═Cu,电路中有0.2mol电子通过时,析出Cu质量为0.1mol×64g/mol=6.4g,同时有0.1mol硫酸根离子由右
池向左池迁移,质量减少0.1mol×96g/mol=9.6g,阴极室溶液质量共减少6.4g+9.6g=16g,故D正确;故选:
B。
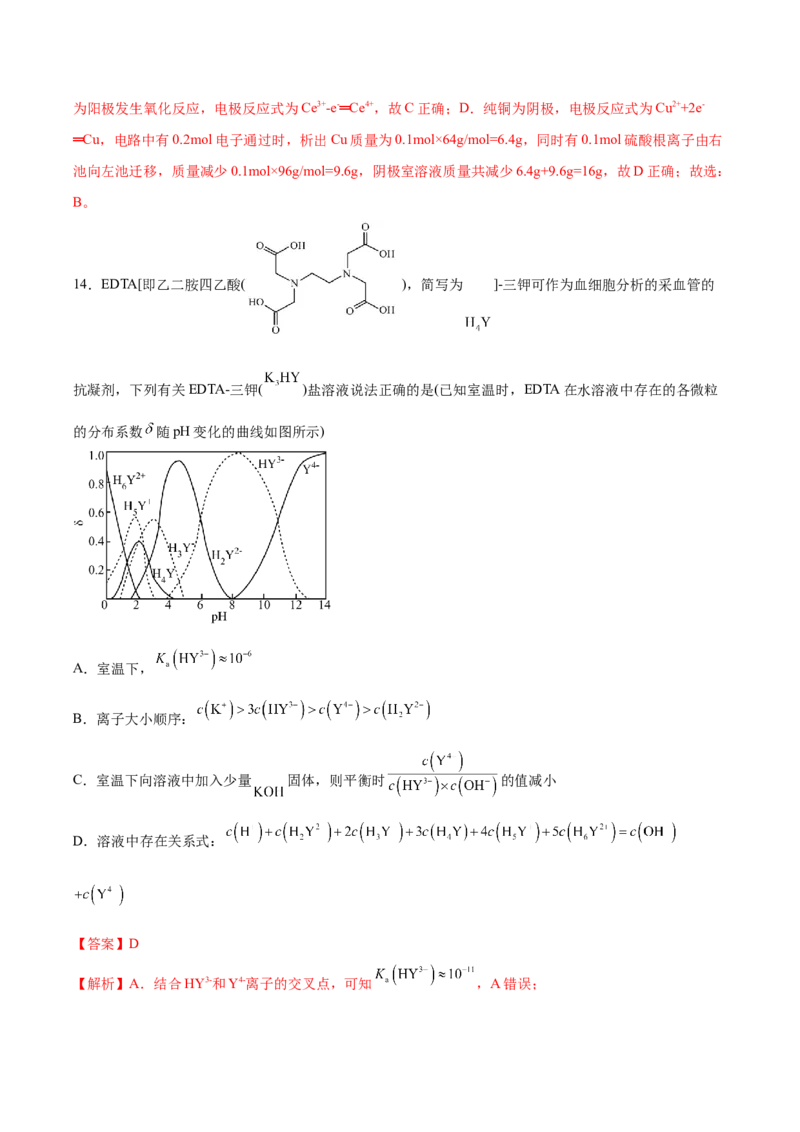
14.EDTA[即乙二胺四乙酸( ),简写为 ]-三钾可作为血细胞分析的采血管的
抗凝剂,下列有关EDTA-三钾( )盐溶液说法正确的是(已知室温时,EDTA在水溶液中存在的各微粒
的分布系数 随pH变化的曲线如图所示)
A.室温下,
B.离子大小顺序:
C.室温下向溶液中加入少量 固体,则平衡时 的值减小
D.溶液中存在关系式:
【答案】D
【解析】A.结合HY3-和Y4-离子的交叉点,可知 ,A错误;B. 溶液中,HY3-和既存在电离,也存在水解反应,由溶液PH≈8,可知其水解大于电离,所以正确
的顺序为: ,B错误;C.由水解反应 ,可知
= ,则温度不变K 不变, 不变,C错误;D.溶液中存在电荷
h
守恒物料守恒关系:
,物料守恒关系
,由电荷守恒减去物料守恒
关系式,可得D项关系式,D正确;故选D。
15.采用了氮化镓元件的充电器体积小、质量轻,在发热量、效率转换上相比普通充电器也有更大的优势,
被称为“快充黑科技”,下图是氮化镓的三种晶体结构(N 表示阿伏加德罗常数的值)。下列有关说法错误
A
的是
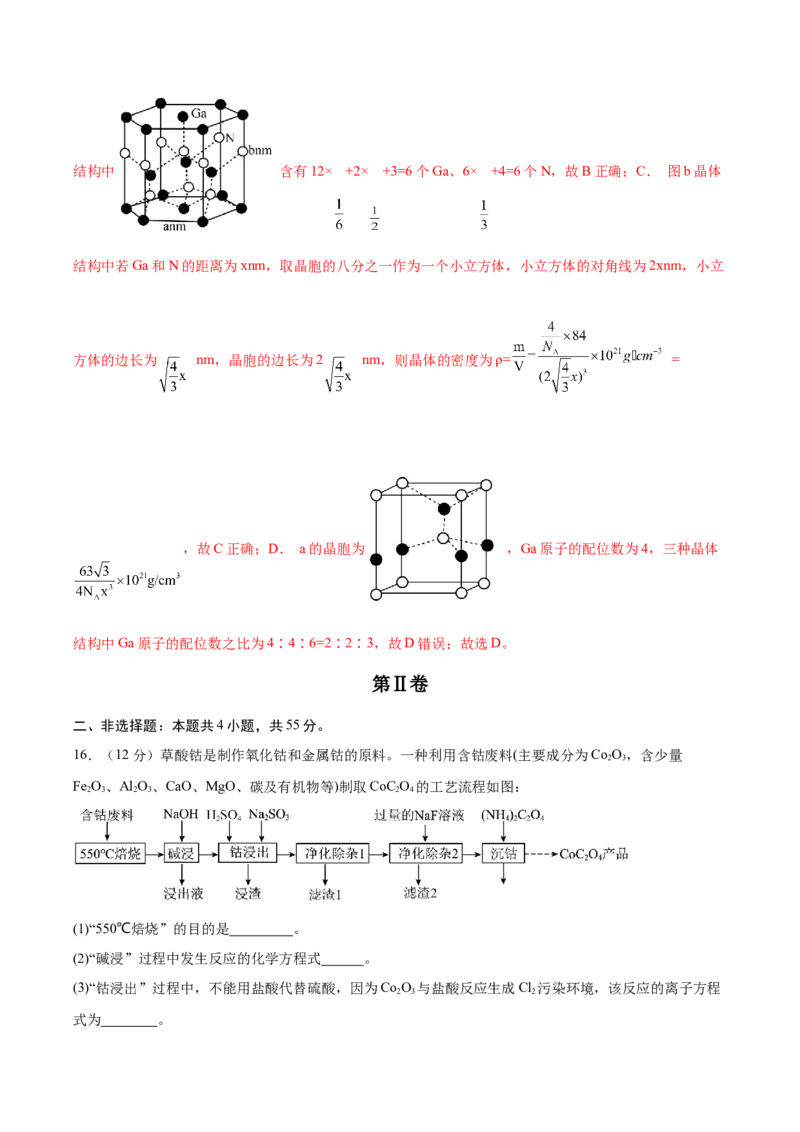
A.Ga、N均属于p区元素
B.图a晶体结构中含有6个Ga、6个N
C.图b晶体结构中若Ga和N的距离为xnm,则晶体的密度为
D.三种晶体结构中Ga原子的配位数之比为3∶2∶3
【答案】D
【解析】A. Ga、N的价电子分别是4s24p1、2s22p3、Ga、N均属于p区元素,故A正确;B. 图a晶体结构中 含有12× +2× +3=6个Ga、6× +4=6个N,故B正确;C. 图b晶体
结构中若Ga和N的距离为xnm,取晶胞的八分之一作为一个小立方体,小立方体的对角线为2xnm,小立
方体的边长为 nm,晶胞的边长为2 nm,则晶体的密度为ρ= =
,故C正确;D. a的晶胞为 ,Ga原子的配位数为4,三种晶体
结构中Ga原子的配位数之比为4∶4∶6=2∶2∶3,故D错误;故选D。
第Ⅱ卷
二、非选择题:本题共4小题,共55分。
16.(12分)草酸钴是制作氧化钴和金属钴的原料。一种利用含钴废料(主要成分为Co O,含少量
2 3
Fe O、Al O、CaO、MgO、碳及有机物等)制取CoC O 的工艺流程如图:
2 3 2 3 2 4
(1)“550℃焙烧”的目的是 。
(2)“碱浸”过程中发生反应的化学方程式 。
(3)“钴浸出”过程中,不能用盐酸代替硫酸,因为Co O 与盐酸反应生成Cl 污染环境,该反应的离子方程
2 3 2
式为 。(4)“净化除杂1”过程中,先在40~50℃加入HO,再升温至80~85℃,加入NaCO 溶液,调pH至4.5.滤
2 2 2 3
渣1的主要成分是 。金属离子与HO 反应的离子方程式为 。
2 2
(5)“净化除杂2”过程中,加入NaF以除去原溶液中Ca2+(浓度为1.0×10﹣3molL﹣1)和Mg2+,若控制溶液中c(F
﹣)=2.0×10﹣3molL﹣1,则Ca2+的去除率准确值为 。[已知某温度下,⋅K (CaF )=4.0×10﹣11]
sp 2
(6)如图为二水合⋅草酸钴(CoC
2
O
4
2H
2
O摩尔质量为183g/mol)在空气中受热的质量变化曲线,曲线中300℃及
以上所得固体均为钴氧化物。写⋅出B点物质与O 在一定温度下发生反应生成C点物质的化学方程式
2
。
【答案】(1)除去碳和有机物(1分)
(2)AlO+2NaOH+3HO=2NaAl(OH) (2分)
2 3 2 4
(3)Co O+2Cl−+6H+=2Co2++Cl↑+3H O(2分)
2 3 2 2
(4)Fe(OH) (1分) HO+2Fe2++2H+=2Fe3++2H O(2分)
3 2 2 2
(5)99%(2分)
(6)3CoC O+2O Co O+6CO (2分)
2 4 2 3 4 2
【分析】含钴废料焙烧可除去碳及有机物,NaOH碱浸除去Al O,钴浸出用NaSO 在酸性条件下将Co O
2 3 2 3 2 3
还原为Co2+,同时Fe3+也被还原为Fe2+,净化除杂1中先用HO 将Fe2+氧化为Fe3+,再调pH转化为
2 2
Fe(OH) 沉淀,“净化除杂2”过程中,加入NaF将原溶液中Ca2+和Mg2+转化为CaF和MgF沉淀,最后用草
3
酸铵将Co2+沉淀为CoC O。
2 4
【解析】(1)根据分析可知,“550℃焙烧”的目的是除去碳和有机物;(2)“碱浸”过程中发生反应
为Al O 溶于NaOH溶液,化学方程式为:Al O+2NaOH+3HO=2NaAl(OH) ;(3)“钴浸出”过程中,
2 3 2 3 2 4
不能用盐酸代替硫酸,因为Co O 具有氧化性,可以把盐酸氧化为Cl,该反应的离子方程式为:
2 3 2
Co O+2Cl−+6H+=2Co2++Cl↑+3H O;(4)“净化除杂1”过程中,先在40~50℃加入HO,再升温至80~
2 3 2 2 2 2
85℃,加入NaCO 溶液,调pH至4.5,滤渣1的主要成分是Fe(OH) ,金属离子与HO 反应的离子方程式
2 3 3 2 2
为HO+2Fe2++2H+=2Fe3++2H O;(5)若控制溶液中c(F-)=2.0×10-3mol•L-1,该温度下,
2 2 2
K (CaF )=c(Ca2+)c2(F-)=c(Ca2+)(2.0×10-3)2=4.0×10-11,解得:c(Ca2+)=10-5mol•L-1,则除钙率为=
sp 2=99%;(6)起始时,n(CoC O•2H O)= =0.1mol,B点时,失重
2 4 2
为(18.3-14.7)g=3.6g,即失去0.2mol水,所以B点为CoC O,设C点的成分为Co O,根据原子守恒,则
2 4 x y
= ≈3:4,即C点剩余固体的化学式为Co O,则B点物质与O 在一定温度下发生
3 4 2
反应生成C点物质的化学方程式为:3CoC O+2O Co O+6CO 。
2 4 2 3 4 2
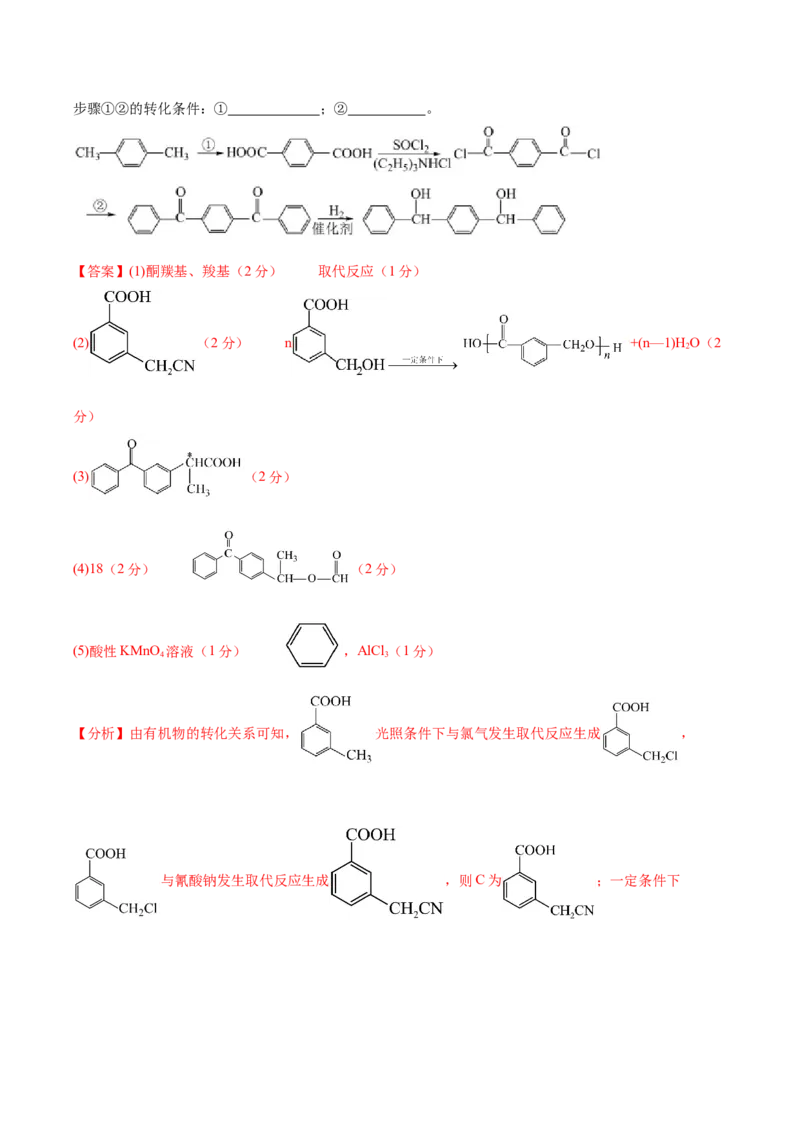
17.(15分)酮基布洛芬片是用于治疗各种关节肿痛以及牙痛、术后痛等的非处方药。其合成路线如图所
示:
(1)酮基布洛芬中官能团的名称为 ,D→E的反应类型为 。
(2)写出C的结构简式: ;G中含有手性碳原子,请你用*标出G的结构简式中手性碳
。
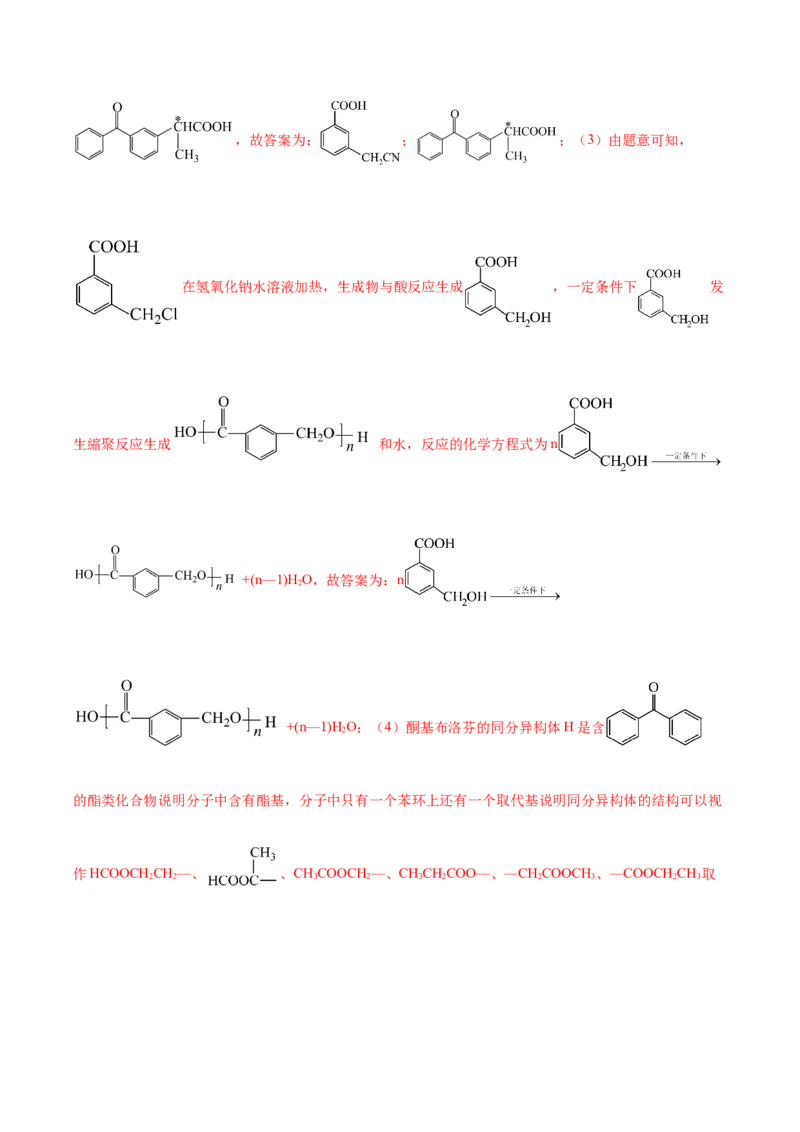
(3)B在 NaOH 水溶液加热,生成物与酸反应生成有机物 M,写出在一定条件下 M生成高聚物的化学反
应方程式 。
(4)H为酮基布洛芬的同分异构体,则符合下列条件的H有 种。
①含 的酯类化合物②其中只有一个苯环上还有一个取代基
其中核磁共振氢谱有8组峰,且峰面积之比为 3:2:2:2:2:1:1:1的结构简式为 。
(5)下面是以 为原料,设计制备的 一种合成路线,请你写出步骤①②的转化条件:① ;② 。
【答案】(1)酮羰基、羧基(2分) 取代反应(1分)
(2) (2分) n +(n—1)HO(2
2
分)
(3) (2分)
(4)18(2分) (2分)
(5)酸性KMnO 溶液(1分) ,AlCl (1分)
4 3
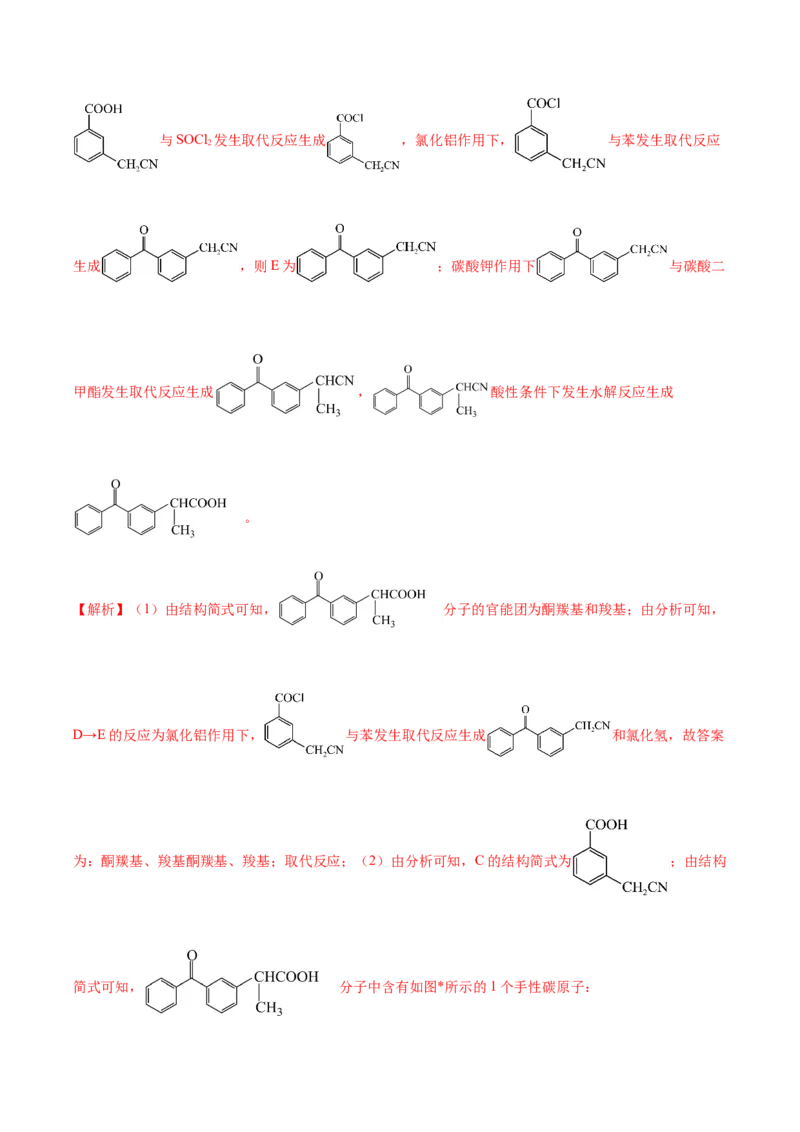
【分析】由有机物的转化关系可知, 光照条件下与氯气发生取代反应生成 ,
与氰酸钠发生取代反应生成 ,则C为 ;一定条件下与SOCl 发生取代反应生成 ,氯化铝作用下, 与苯发生取代反应
2
生成 ,则E为 ;碳酸钾作用下 与碳酸二
甲酯发生取代反应生成 , 酸性条件下发生水解反应生成
。
【解析】(1)由结构简式可知, 分子的官能团为酮羰基和羧基;由分析可知,
D→E的反应为氯化铝作用下, 与苯发生取代反应生成 和氯化氢,故答案
为:酮羰基、羧基酮羰基、羧基;取代反应;(2)由分析可知,C的结构简式为 ;由结构
简式可知, 分子中含有如图*所示的1个手性碳原子:,故答案为: ; ;(3)由题意可知,
在氢氧化钠水溶液加热,生成物与酸反应生成 ,一定条件下 发
生縮聚反应生成 和水,反应的化学方程式为n
+(n—1)HO,故答案为:n
2
+(n—1)HO;(4)酮基布洛芬的同分异构体H是含
2
的酯类化合物说明分子中含有酯基,分子中只有一个苯环上还有一个取代基说明同分异构体的结构可以视
作HCOOCH CH—、 、CHCOOCH —、CHCHCOO—、—CHCOOCH 、—COOCH CH 取
2 2 3 2 3 2 2 3 2 3代了 分子中1个苯环上的氢原子,共有3×6=18种;其中核磁共振氢谱有8组峰,且峰
面积之比为3:2:2:2:2:1:1:1的结构简式为 ,故答案为:18;
;(5)由有机物的转化关系可知,步骤①发生的反应为
与酸性高锰酸钾溶液发生氧化反应生成 ,步骤②发生的
反应为氯化铝作用下 与 发生取代反应生成 和
氯化氢故答案为:酸性KMnO 溶液; ,AlCl 。
4 3
18.(14分)实验室可利用正丁醇为原料,与乙炔、CO发生反应合成有机原料丙烯酸丁酯,其合成原理
为:
相关实验装置如图所示:物质 密度 沸点/℃ 部分性质
正丁醇 0.80 117.7 易溶于丙酮,易燃
易溶于丙酮,易燃;温度过高时容易
丙烯酸丁酯 0.89 145.7
自聚生成聚丙烯酸丁酯
丙酮 0.79 56 易燃易爆
实验过程:
Ⅰ.将50mL正丁醇、30mL丙酮以及3g纳米NiO加入装置甲中;Ⅱ.使用加热磁力搅拌器加热控制温度
在110℃左右;Ⅲ.将乙和丙中制备的乙炔与CO气体同时缓缓通入装置甲中,加热回流3小时;Ⅳ.将三
颈烧瓶中的液体过滤、减压蒸馏,将得到的粗品再纯化,得到丙烯酸丁酯纯品。
试回答下列问题:
(1)纳米NiO的作用是 ,将其处理成纳米级的目的是 。
(2)装置甲中三颈烧瓶的规格为 (填字母)。
A.100mL B.200mL C.500mL
(3)使用装置乙可制备 ,同时电石中的CaS、 能发生水解反应产生 和 。在试管N中
和 反应产生Cu和两种常见的最高价含氧酸,该反应的化学方程式为 ;酸性高锰酸钾也能与
和 反应,但不能用其代替硫酸铜溶液,主要原因是 。
(4)装置丙中草酸晶体( )分解的化学方程式为 。步骤Ⅳ获得粗品和粗品纯化均采用减
压蒸馏,其优点为:降低沸点,节约能源; 。
(5)若最后获得的丙烯酸丁酯纯品的质量为54.0g,则该实验的产率为 (结果保留两位有效数字)。【答案】(1)作催化剂(1分) 增大接触面积,加快反应速率,使催化效率更高(2分)
(2)B(2分)
(3) (2分) 乙炔也能与酸性高锰酸钾溶液反应(1分)
(4) (2分) 加快蒸馏速率,避免因温度过高而自聚生成聚丙烯
酸丁酯(2分)
(5)78%(2分)
【分析】利用正丁醇为原料,与乙炔、CO发生反应合成有机原料丙烯酸丁酯,装置乙中可制备 ,同
时电石中的CaS、 能发生水解反应产生 和 ,通入 溶液除杂,装置丙中生成CO,将乙
和丙中制备的乙炔与CO气体同时缓缓通入装置甲中,加热回流3小时;将三颈烧瓶中的液体过滤、减压
蒸馏,将得到的粗品再纯化,得到丙烯酸丁酯纯品。
【解析】(1)正丁醇和丙酮反应,纳米NiO作催化剂,将其处理成纳米级可增大接触面积,加快反应速
率,使催化效率更高,故答案为催化剂;增大接触面积,加快反应速率,使催化效率更高。
(2)由实验步骤Ⅰ可知,实验中用到将50mL正丁醇和30mL丙酮,共80mL液体,应选用200mL三颈烧
瓶,故答案为B。
(3)在试管N中 和 反应产生Cu和两种常见的最高价含氧酸为HPO 和HSO ,化学方程式为
3 4 2 4
;虽然酸性高锰酸钾也能与 和 反应,但不能用其
代替硫酸铜溶液,主要原因是乙炔也能与酸性高锰酸钾溶液反应,故答案为
;乙炔也能与酸性高锰酸钾溶液反应。
(4) 分解生成二氧化碳和一氧化碳,化学方程式为
。步骤Ⅳ获得粗品和粗品纯化均采用减压蒸馏,其优点为:降低沸点,节约能源;加快蒸馏速率,避免因温度过高而自聚生成聚丙烯酸丁酯;故答案为
;加快蒸馏速率,避免因温度过高而自聚生成聚丙烯酸丁酯。
(5)正丁醇的密度为 ,50mL正丁醇的质量为40g,物质的量为 ,则理论上生成的丙烯
酸丁酯的质量为 ,则该实验的产率为 ,故答案为78%。
19.(14分) 的转化和利用是实现碳中和的有效途径。其中 转换为 被认为是最可能利用
的路径,该路径涉及反应如下:
反应I:
反应Ⅱ:
请回答下列问题:
(1)反应I在 (填“高温”“低温”或“任意温度”)下可以自发进行。
(2)在特定温度下,由稳定态单质生成 化合物的焓变叫该物质在此温度下的标准生成焓( )。下
表为几种物质在 的标准生成焓,则反应Ⅱ的
物质
0 -394 -111 -242
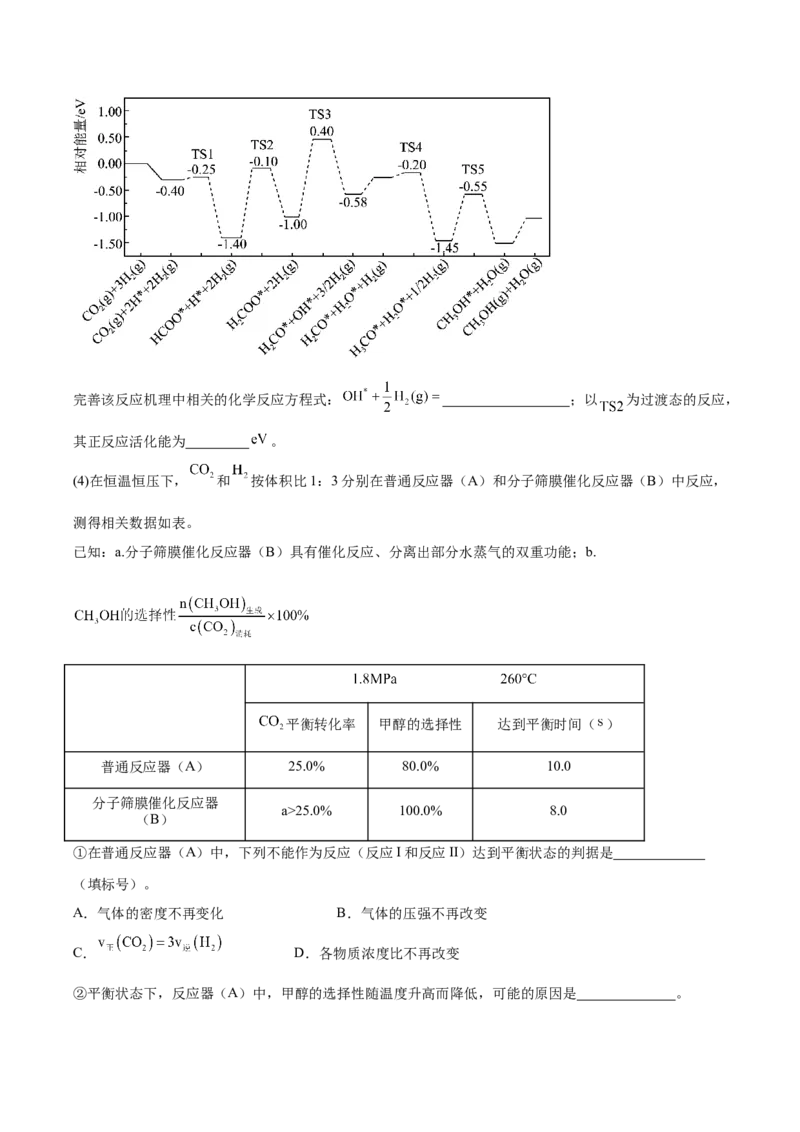
(3)在催化剂条件下,反应I的反应机理和相对能量变化如图(吸附在催化剂表面上的粒子用*标注, 为
过渡态):完善该反应机理中相关的化学反应方程式: ;以 为过渡态的反应,
其正反应活化能为 。
(4)在恒温恒压下, 和 按体积比1:3分别在普通反应器(A)和分子筛膜催化反应器(B)中反应,
测得相关数据如表。
已知:a.分子筛膜催化反应器(B)具有催化反应、分离出部分水蒸气的双重功能;b.
平衡转化率 甲醇的选择性 达到平衡时间( )
普通反应器(A) 25.0% 80.0% 10.0
分子筛膜催化反应器
a>25.0% 100.0% 8.0
(B)
①在普通反应器(A)中,下列不能作为反应(反应I和反应II)达到平衡状态的判据是
(填标号)。
A.气体的密度不再变化 B.气体的压强不再改变
C. D.各物质浓度比不再改变
②平衡状态下,反应器(A)中,甲醇的选择性随温度升高而降低,可能的原因是 。③在反应器(B)中, 的平衡转化率明显高于反应器(A),可能的原因是 。
④岩反应器(A)中初始时 ,反应Ⅱ的化学平衡常数 (Ⅱ)= (用最简的
分数表示)。
【答案】(1)低温(1分)
(2)+41(1分)
(3) (1分) 1.3(1分)
(4)①BC(2分)
②反应I为放热反应,反应Ⅱ为吸热反应,温度升高,反应I的化学平衡逆向移动,反应Ⅱ的化学平衡正
向移动(2分)
③反应器B中分子筛能催化反应I而不能催化反应Ⅱ且能分离出部分水蒸气,促使反应I化学平衡正向移
动(2分)
④ (2分)
【解析】(1)反应Ⅰ是放热反应,ΔH<0,根据方程式可知ΔS<0,根据ΔG=ΔH-TΔS<0反应能自发进行,
则该反应在低温下能自发进行,故答案为:低温;(2)根据标准生成焓的定义,反应Ⅱ的ΔH等于水和
CO的标准生成焓之和减去CO 的标准生成焓,即ΔH=-242kJ/mol-111kJ/mol-(-394kJ/mol)=+41kJ/mol;
2
(3) 从图中第五步反应可知,OH*+ H(g)=HO*,以TS2为过渡态的反应,其正反应活化能为-0.10eV-
2 2
(-1.40eV)=1.30eV;(4)①A.恒温恒压条件下,随着反应Ⅰ进行,气体体积减小,容器体积随之减小,
因容器体积改变,气体的密度不断变化,当气体密度不变时,反应达到平衡,故A不选;B.反应在恒温
恒压条件下进行,无论是否达到平衡,气体的压强始终不变,故B选;C.容器中进行的是两个反应,反
应物都是CO 和H,且参加反应的CO 和H 的物质的量之比不相等,所以v (CO)=3v (H )不能说明正逆
2 2 2 2 正 2 逆 2
反应速率相等,反应未达到平衡,故C选;D.随着反应进行,各物质的浓度不断变化,各物质浓度比不
再改变,说明反应达到平衡,故D不选;故选BC; ②反应Ⅰ为放热反应,反应Ⅱ为吸热反应,温度升高,
反应Ⅰ的化学平衡逆向移动,反应Ⅱ的化学平衡正向移动,故平衡状态下反应器A中,甲醇的选择性随温
度升高而降低。故答案为:反应I为放热反应,反应Ⅱ为吸热反应,温度升高,反应I的化学平衡逆向移
动,反应Ⅱ的化学平衡正向移动;③反应器B中二氧化碳平衡转化率大于A且甲醇选择性为100%,说明
只发生反应Ⅰ,即反应器B中分子筛能催化反应Ⅰ而不能催化反应Ⅱ且能分离出部分水蒸气,促使反应Ⅰ
化学平衡正向移动;故答案为:在反应器(B)中,分子筛能催化反应I而不能催化反应Ⅱ且能分离出部分水蒸气,导致反应Ⅰ化学平衡正向移动;④根据已知和表格中数据可知,反应器A中初始n(CO)=1mol,初
2
始投入氢气3mol,CO 平衡转化率为25%,说明反应掉二氧化碳共0.25mol,甲醇选择性为80%,说明反
2
应Ⅰ生成甲醇0.2mol,则同时生成水0.2mol,则消耗氢气0.6mol,消耗二氧化碳0.2mol,则反应Ⅱ消耗
CO 0.05mol,消耗氢气0.05mol,生成CO 0.05mol,生成水0.05mol,则平衡时CO 物质的量为0.75mol,
2 2
H 物质的量为2.35mol,CO物质的量为0.05mol,HO物质的量为0.25mol,反应Ⅱ为等体积反应,各物质
2 2
的分压之比等于物质的量之比,所以K = 。
P