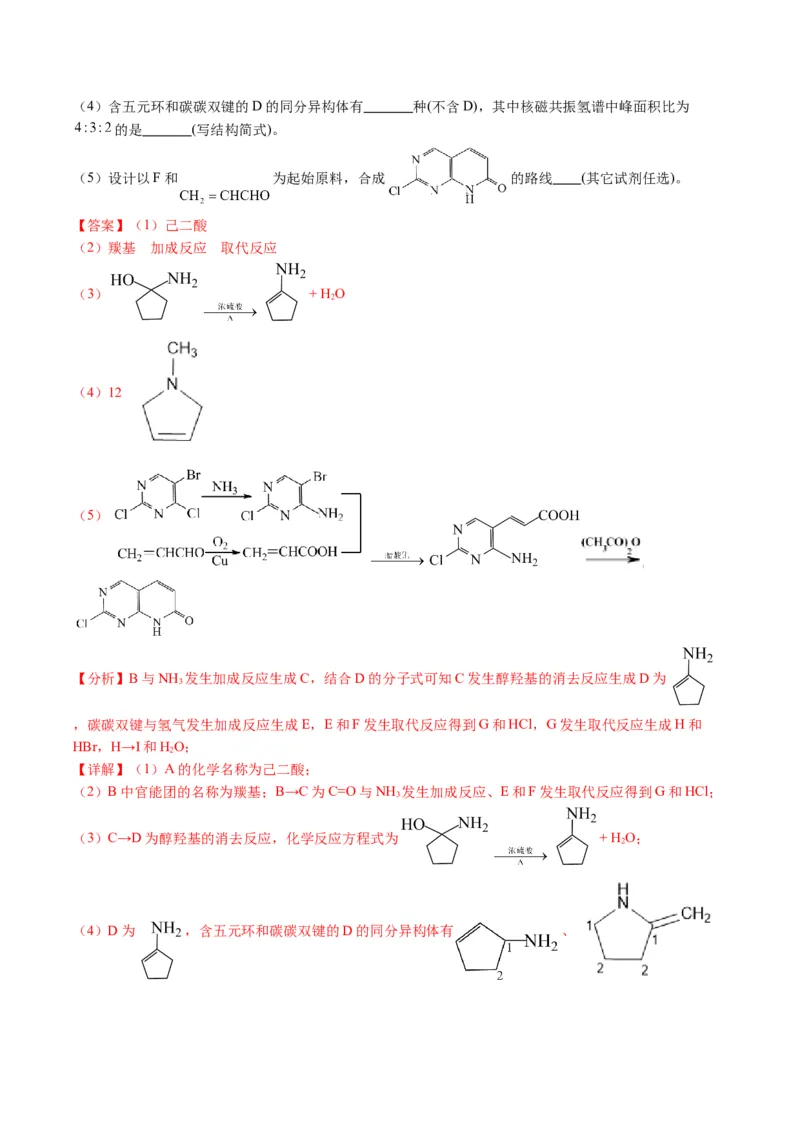
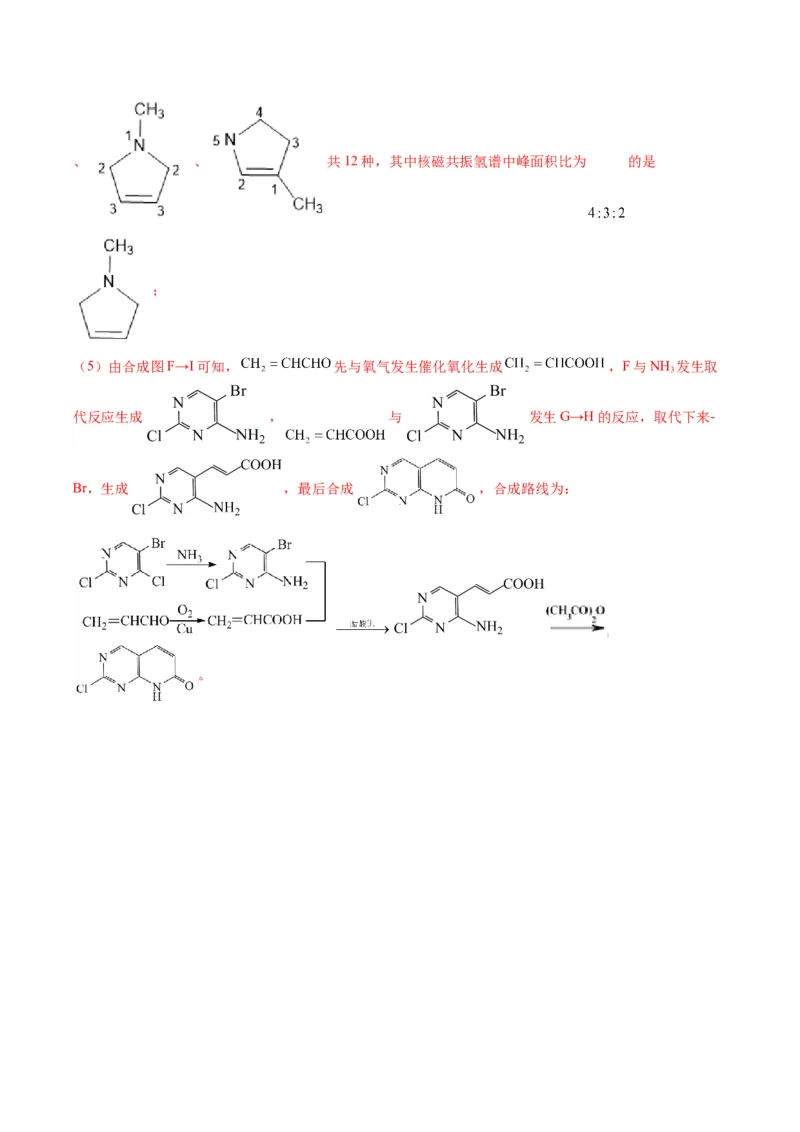
文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(全国卷老教材)
黄金卷05
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 O 16 N 14 Cl 35.5 Ca 40 Fe 56 Ce 140 V 51
第Ⅰ卷
一、单项选择题:共14题,每题3分,共42分。每题只有一个选项最符合题意。
1.化学与人类生产、生活、社会可持续发展等密切相关。下列说法正确的是
A.中国空间站的食物可谓太空一绝,航天员喜欢吃的“宫保鸡丁”的主要成分是有机物
B.“可燃冰”是一种有待大量开发的新能源,开采过程中发生大量泄漏不会对环境产生影响
C.清华大学打造的世界首款异构融合类脑芯片——天机芯的主要材料与光导纤维的相同
D.用于制造“山东舰”上舰载机降落拦阻索的特种钢属于新型无机非金属材料
【答案】A
【详解】A.“宫保鸡丁”主要成分鸡肉属于蛋白质,蛋白质属于有机物,A正确;
B.“可燃冰”开采过程中发生泄漏的气体是甲烷,甲烷是引起温室效应的气体之一,B错误;
C.天机芯的主要材料是半导体材料晶体硅,光导纤维的主要成分是具有良好光学特性的二氧化硅,二者
不同,C错误;
D.特种钢属于金属材料,不属于新型无机非金属材料,D错误。
故选A。
2.有关化学用语正确的是
A.氯化氢的比例模型: B.37Cl—的结构示意图:
C.乙烯分子的球棍模型: D.甲基的电子式:
【答案】C
【详解】A.氯化氢分子是直线形分子,氯原子比氢原子大,氯化氢的比例模型为 ,故A错误;
B.氯离子核电荷数为17,核外电子数为18,有3个电子层,最外层电子数为8,离子的结构示意图为
,故B错误;
C.乙烯分子的结构简式为CH=CH ,分子的球棍模型为 ,故C正确;
2 2
D.甲基的结构简式为—CH,电子式为 ,故D正确;
3
故选C。
3.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.加入Al粉产生 的溶液中: 、 、 、B.澄清透明溶液中: 、 、 、
C. 的溶液中: 、 、 、
D.由水电离的 的溶液中: 、 、 、
【答案】B
【详解】A.加入Al粉产生 的溶液为酸性或者碱性溶液,若为碱性溶液, 能够与氢氧根离子发
生反应;若为酸性溶液, 与氢离子反应,在溶液中一定不能大量共存,故A不选;
B.澄清透明溶液中, 、 、 、 四种离子之间不发生反应,一定能大量共存,故B选;
C. 的溶液中c(H+)Y>Z B.离子半径:W>Z>Y
C.A与C可以反应生成B D.X和Y组成的二元化合物中不含有非极性键
【答案】C【分析】X、Y、Z、W为原子序数依次增大的四种短周期主族元素,A、B、C、D、E为上述四种元素中
的一种或几种所组成的物质,已知Y元素最外层电子数是内层的3倍,则Y为O元素;Z与Y同主族,则
Z为S元素、W为Cl元素;E、B分别为Y、Z元素对应的单质,A中含有18个电子,D有漂白性,结合
图中转化可知,A为HS、D为HClO、B为S、E为O、C为SO ,则X为H元素。
2 2 2
【详解】A.元素的非金属性越强,简单气态氢化物的稳定性越强,元素的非金属性强弱顺序为O>Cl>S,
则简单气态氢化物的稳定性强弱顺序为O>Cl>S,故A错误;
B.电子层结构相同的离子,核电荷数越大,离子的离子半径越小,则硫离子的离子半径大于氯离子,故
B错误;
C.硫化氢与二氧化硫发生氧化还原反应生成硫和水,故C正确;
D.过氧化氢分子是含有极性键和非极性键的共价化合物,故D错误;
故选C。
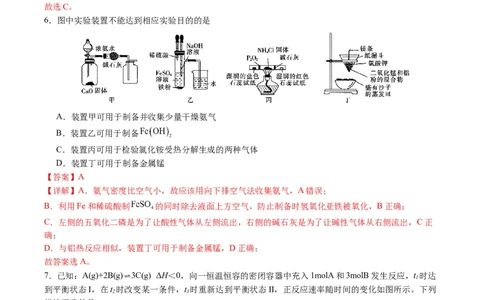
6.图中实验装置不能达到相应实验目的的是
A.装置甲可用于制备并收集少量干燥氨气
B.装置乙可用于制备
C.装置丙可用于检验氯化铵受热分解生成的两种气体
D.装置丁可用于制备金属锰
【答案】A
【详解】A.氨气密度比空气小,故应该用向下排空气法收集氨气,A错误;
B.利用Fe和稀硫酸制 的同时除去液面上方空气,防止制备时氢氧化亚铁被氧化,B正确;
C.左侧的五氧化二磷是为了让酸性气体从左侧流出,右侧的碱石灰是为了让碱性气体从右侧流出,C正
确;
D.与铝热反应相似,装置丁可用于制备金属锰,D正确;
故答案选A。
7.已知:A(g)+2B(g)⇌3C(g) ΔH<0,向一恒温恒容的密闭容器中充入1molA和3molB发生反应,t
1
时达
到平衡状态I,在t 时改变某一条件,t 时重新达到平衡状态II,正反应速率随时间的变化如图所示。下列
2 3
说法正确的是
A.容器内压强不变,表明反应达到平衡 B.t 时改变的条件:向容器中加入C
2
C.平衡时A的体积分数φ:φ(II)<φ(I) D.平衡常数K:
【答案】B【分析】根据图象可知,向恒温恒容密闭容器中充入1molA和3molB发生反应,反应时间从开始到t 阶
1
段,正反应速率不断减小,t-t 时间段,正反应速率不变,反应达到平衡状态,t-t 时间段,改变条件使正
1 2 2 3
反应速率逐渐增大,平衡向逆反应方向移动,t 以后反应达到新的平衡状态,据此结合图象分析解答。
3
【详解】A.容器内发生的反应为A(g)+2B(g)⇌3C(g),该反应是气体分子数不变的可逆反应,所以在恒温
恒容条件下,气体的压强始终保持不变,则容器内压强不变,不能说明反应达到平衡状态,故A错误;
B.根据图象变化曲线可知,t-t 过程中,t 时v 瞬间不变,平衡过程中不断增大,则说明反应向逆反应方
2 3 2 正
向移动,且不是“突变”图象,属于“渐变”过程,所以排除温度与催化剂等影响因素,改变的条件为:
向容器中加入C,故B正确;
C.最初加入体系中的A和B的物质的量的比值为1:3,当向体系中加入C时,平衡逆向移动,最终A和
B各自物质的量增加的比例为1:2,因此平衡时A的体积分数φ(II)>φ(I),故C错误;
D.平衡常数K只与温度有关,因该反应在恒温条件下进行,所以K保持不变,故D错误;
故选B。
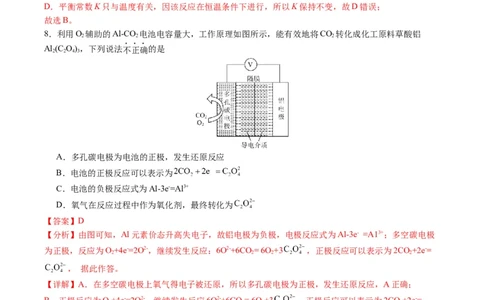
8.利用O 辅助的Al-CO 电池电容量大,工作原理如图所示,能有效地将CO 转化成化工原料草酸铝
2 2 2
Al (C O),下列说法不正确的是
2 2 4 3
A.多孔碳电极为电池的正极,发生还原反应
B.电池的正极反应可以表示为
C.电池的负极反应式为Al-3e-=Al3+
D.氧气在反应过程中作为氧化剂,最终转化为
【答案】D
【分析】由图可知,Al元素价态升高失电子,故铝电极为负极,电极反应式为Al-3e- =A13+;多空碳电极
为正极,反应为O+4e-=2O2-,继续发生反应:6O2-+6CO = 6O +3 ,正极反应可以表示为2CO+2e-=
2 2 2 2
, 据此作答。
【详解】A.在多空碳电极上氧气得电子被还原,所以多孔碳电极为正极,发生还原反应,A正确;
B.正极反应为O+4e-=2O2-,继续发生反应6O2-+6CO = 6O +3 ,正极反应可以表示为2CO+2e-=
2 2 2 2
,B正确;
C.A1元素价态升高失电子,故铝电极为负极,电极反应式为Al-3e-=Al3+,C正确;
D.O+4e-=2O2-,继续发生反应6O2-+6CO = 6O +3 ,可见氧气为反应的催化剂,D错误;
2 2 2
故合理选项是D。
9.碲被誉为“现代工业的维生素”,它在地壳中的丰度值很低。某科研小组从粗铜精炼的阳极泥(主要含
有 )中提取粗碲的工艺流程如图所示。下列有关说法不正确的是已知:①“焙烧”后,碲主要以 形式存在;② 微溶于水,易溶于强酸和强碱。
A.“焙烧”用到的主要仪器有:坩埚、泥三角、酒精灯、玻璃棒
B.“碱浸”时反应的离子方程式为
C.“碱浸”后所得的滤渣中含有Au、Ag,可用稀盐酸将其分离
D.“还原”时 作还原剂
【答案】C
【分析】阳极泥焙烧,得到 、CuO、Ag、Au的混合物,加入氢氧化钠,发生反应
,过滤得 溶液,加入硫酸生成 ,酸性条件下用 还原
得到Te单质。
【详解】A.焙烧固体,应用坩埚,且放在泥三角上,另外加热时需要用酒精灯,并用玻璃棒搅拌,故A
正确;
B. 是两性氧化物,“碱浸”时与氢氧化钠溶液反应,反应的离子方程式为
,故B正确;
C.“碱浸”后所得的滤渣中含有的Au、Ag,均为不活泼金属,与稀盐酸都不反应,可以用稀硝酸将其分
离,故C错误;
D.“还原”反应的离子方程式是 ,反应中S元素化合价升高,
作还原剂,故D正确;
选C。
10.合成布洛芬的方法如图所示(其他物质省略)。下列说法错误的是
A.X分子中所有原子可能共平面 B.Y的分子式为
C.X、Y都能发生加成反应 D.布洛芬能与碳酸钠溶液反应
【答案】A
【详解】A.X分子中存在饱和碳原子,饱和碳原子与其所连4个原子之间为四面体结构,所有原子不可
能都共面,A错误;
B.Y分子中含有13个C,16个H,2个O,故分子式为:C H O,B正确;
13 16 2
C.X、Y中苯环能与氢气发生加成反应,X中碳碳三键、Y中碳碳双键均能发生加成反应,C正确;
D.布洛芬中含有羧基,能与碳酸钠反应,D正确;
故答案选A。
11.下列反应的离子方程式书写正确的是A.金属Na与 溶液反应:
B. 溶于过量HI溶液:
C.澄清石灰水与过量小苏打溶液混合:
D.草酸( )与酸性 溶液反应:
【答案】C
【详解】A.Na会与溶液中的水反应生成氢氧化钠,氢氧化钠与镁离子生成氢氧化镁沉淀,离子方程式为
,A错误;
B. 会氧化 生成亚铁离子和碘单质, ,B错误;
C.澄清石灰水与过量小苏打溶液混合,钙离子完全转化为碳酸钙沉淀、氢氧根离子完全转化为水,碳酸
氢根离子过量转化为碳酸根离子,反应为: ,C正确;
D.草酸是弱酸,写离子方程式时不能拆开, ,D错误;
故选C。
12.25℃,用浓度为 的NaOH溶液滴定20.00mL浓度为 的三种酸HX、HY、
HZ,滴定曲线如图所示。下列说法不正确的是
A.在相同温度下,同浓度的三种酸溶液的导电能力:HZ>HY>HX
B.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时,溶液中存在:
C.滴定至终点时,消耗的NaOH溶液体积相同
D.根据滴定曲线,可知
【答案】B
【详解】A.V(NaOH)=0时,0.1000mol•L-1的三种酸HX、HY、HZ的pH依次减小,c(H+)由小到大顺序
为:HX<HY<HZ,相同浓度的这三种溶液,导电能力大小顺序是HZ>HY>HX,故A正确;
B.酸性:HY>HX,将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时,HY
已经完全反应,溶液中溶质为等物质的量浓度的NaX、NaY,水解程度:X->Y-,则溶液中c(X-)<c(Y-),
故B错误;
C.三种酸都是一元酸且物质的量浓度、溶液体积都相等,滴定终点时消耗的n(NaOH)相等,c(NaOH)相
等,则V(NaOH)相等,故C正确;
D.当NaOH溶液滴到10mL时,溶质等物质的量浓度的NaY、HY,溶液中c(HY)≈c(Y-),HA的电离平衡
常数K(HY)= ×c(H+)≈c(H+)=10-pH=10-5mol/L,故D正确;
a故选:B。
13.实验探究是化学学习的方法之一、根据下列实验设计的现象所得实验结论正确的是
选项 实验设计 现象 实验结论
在坩埚中加入16.4g ,加热一段时 加热后坩埚内固体为
A 质量为12.8g
和 混合物
间,在干燥器中冷却,称量剩余固体质量
产生白色沉淀,加
B 向鸡蛋清溶液中滴入几滴硫酸铜溶液 蛋白质发生了变性
水后沉淀不溶解
分别用蒸馏水、 溶液喷洒甲、乙 喷洒 溶液的纸
C 能促进纸张的老化
两张白纸,静置、干燥 张老化明显
烧瓶中有红棕色气 木炭具有还原性,能还
D 在烧瓶中加入木炭颗粒与浓硝酸,然后加热
体产生 原
A.A B.B C.C D.D
【答案】B
【详解】A.116.4g 中含结晶水为 ,则坩埚中剩余物质质量为
12.8g时,坩埚内固体为CaC O,A项错误;
2 4
B.Cu是重金属元素,向鸡蛋清溶液中滴入几滴硫酸铜溶液,蛋白质会发生变性,产生白色沉淀,且变性
不可逆,故B正确;
C.氯化铝溶液中含铝离子和氯离子,由实验操作和现象不能证明Cl-能促进纸张的老化,铝离子也可能使
纸张老化,C项错误;
D.红棕色气体也可能是由浓硝酸受热分解生成,故由实验操作和现象不能证明木炭具有还原性,D项错
误;
答案选B。
14.T℃下,三种硫酸盐 (M表示 或 或 )的沉淀溶解平衡曲线如图所示。已知
, 。下列说法正确的是
A. 在任何条件下都不可能转化为
B.X点和Z点分别是 和 的饱和溶液,对应的溶液中
C.T℃下,反应 的平衡常数为
D.T℃时,用 溶液滴定 浓度均为 和 的混合溶液, 先沉淀
【答案】D
【分析】已知 , ,结合C、B、A点数据,则K (BaSO)=
sp 4
c(Ba2+)c(SO )=10-10,K (PbSO )= c(Pb2+)·c(SO )=10-7.6,K (SrSO )= c(Sr2+)·c(SO )=10-6.4。
sp 4 sp 4
【详解】A.因SrSO 、PbSO 、BaSO 为同类型沉淀,再结合题图可知,
4 4 4
K (BaSO)