文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(全国卷老教材)
黄金卷05
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 O 16 N 14 Cl 35.5 Ca 40 Fe 56 Ce 140 V 51
第Ⅰ卷
一、单项选择题:共14题,每题3分,共42分。每题只有一个选项最符合题意。
1.化学与人类生产、生活、社会可持续发展等密切相关。下列说法正确的是
A.中国空间站的食物可谓太空一绝,航天员喜欢吃的“宫保鸡丁”的主要成分是有机物
B.“可燃冰”是一种有待大量开发的新能源,开采过程中发生大量泄漏不会对环境产生影响
C.清华大学打造的世界首款异构融合类脑芯片——天机芯的主要材料与光导纤维的相同
D.用于制造“山东舰”上舰载机降落拦阻索的特种钢属于新型无机非金属材料
2.有关化学用语正确的是
A.氯化氢的比例模型:
B.37Cl—的结构示意图:
C.乙烯分子的球棍模型:
D.甲基的电子式:
3.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.加入Al粉产生 的溶液中: 、 、 、
B.澄清透明溶液中: 、 、 、
C. 的溶液中: 、 、 、
D.由水电离的 的溶液中: 、 、 、
4.设N 表示阿伏加德罗常数的数值,下列说法正确的是
A
A.常温下,60g乙酸与甲酸甲酯的混合物中,含有的碳原子数为2N
A
B.25℃时,pH=7的纯水中含有的OH⁻数为10﹣7N
A
C.1molI (g)和1molH 在密闭容器中充分反应,所得混合气体的分子数小于2N
2 2 A
D.标准状况下,22.4LCH Cl 中C﹣Cl键的数目为2N
2 2 A
5.X、Y、Z、W为原子序数依次增大的四种短周期主族元素,A、B、C、D、E为上述四种元素中的一种
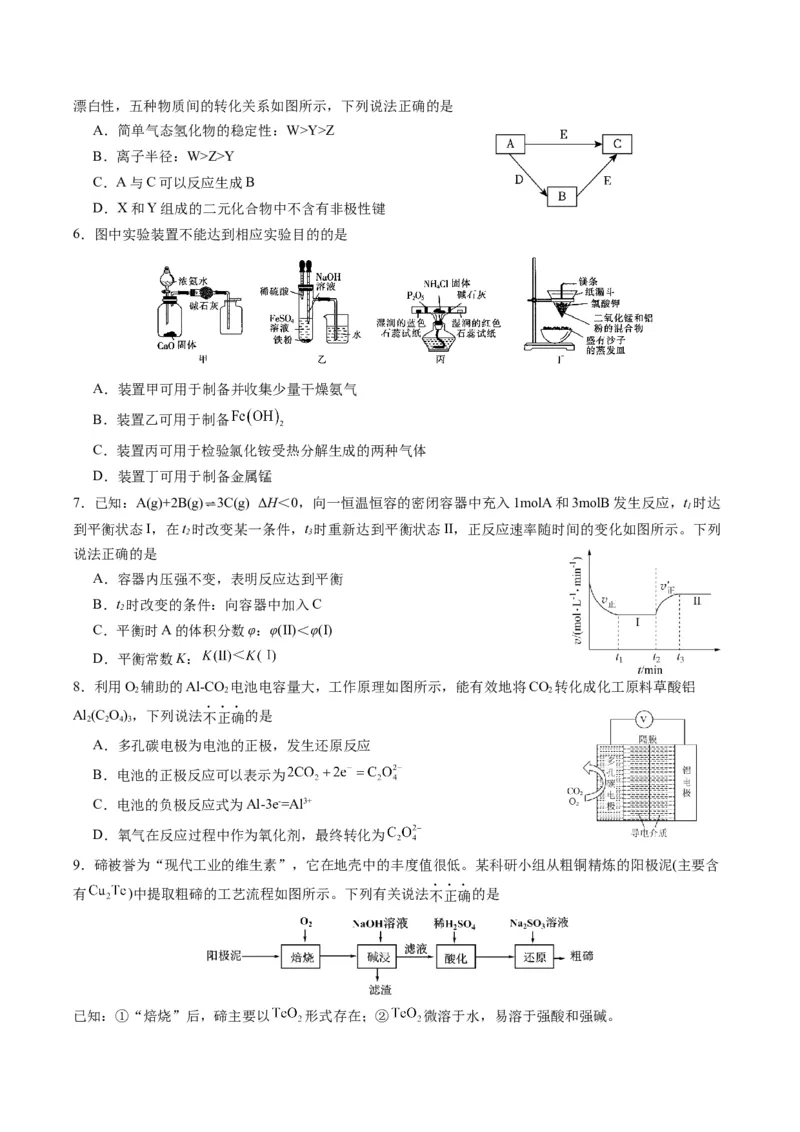
或几种所组成的物质。已知Y元素最外层电子数是内层的3倍,Z与Y同主族,A中含有18个电子,D有漂白性,五种物质间的转化关系如图所示,下列说法正确的是
A.简单气态氢化物的稳定性:W>Y>Z
B.离子半径:W>Z>Y
C.A与C可以反应生成B
D.X和Y组成的二元化合物中不含有非极性键
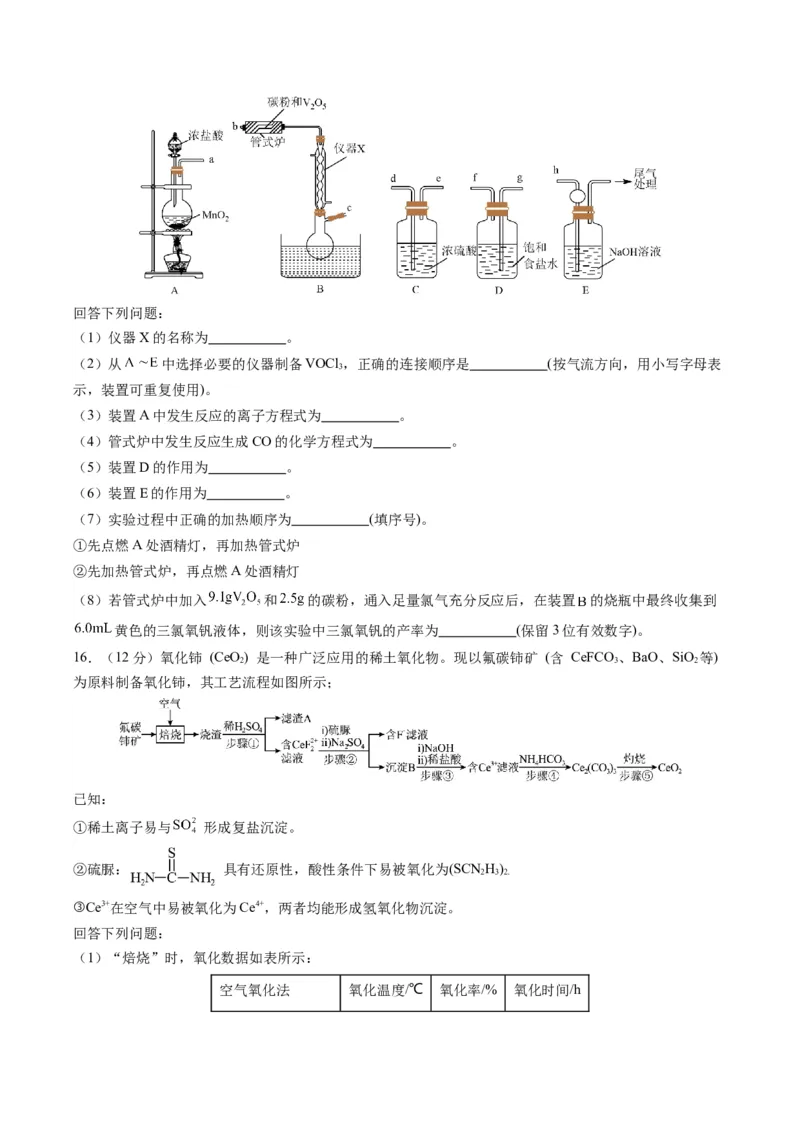
6.图中实验装置不能达到相应实验目的的是
A.装置甲可用于制备并收集少量干燥氨气
B.装置乙可用于制备
C.装置丙可用于检验氯化铵受热分解生成的两种气体
D.装置丁可用于制备金属锰
7.已知:A(g)+2B(g)⇌3C(g) ΔH<0,向一恒温恒容的密闭容器中充入1molA和3molB发生反应,t
1
时达
到平衡状态I,在t 时改变某一条件,t 时重新达到平衡状态II,正反应速率随时间的变化如图所示。下列
2 3
说法正确的是
A.容器内压强不变,表明反应达到平衡
B.t 时改变的条件:向容器中加入C
2
C.平衡时A的体积分数φ:φ(II)<φ(I)
D.平衡常数K:
8.利用O 辅助的Al-CO 电池电容量大,工作原理如图所示,能有效地将CO 转化成化工原料草酸铝
2 2 2
Al (C O),下列说法不正确的是
2 2 4 3
A.多孔碳电极为电池的正极,发生还原反应
B.电池的正极反应可以表示为
C.电池的负极反应式为Al-3e-=Al3+
D.氧气在反应过程中作为氧化剂,最终转化为
9.碲被誉为“现代工业的维生素”,它在地壳中的丰度值很低。某科研小组从粗铜精炼的阳极泥(主要含
有 )中提取粗碲的工艺流程如图所示。下列有关说法不正确的是
已知:①“焙烧”后,碲主要以 形式存在;② 微溶于水,易溶于强酸和强碱。A.“焙烧”用到的主要仪器有:坩埚、泥三角、酒精灯、玻璃棒
B.“碱浸”时反应的离子方程式为
C.“碱浸”后所得的滤渣中含有Au、Ag,可用稀盐酸将其分离
D.“还原”时 作还原剂
10.合成布洛芬的方法如图所示(其他物质省略)。下列说法错误的是
A.X分子中所有原子可能共平面
B.Y的分子式为
C.X、Y都能发生加成反应
D.布洛芬能与碳酸钠溶液反应
11.下列反应的离子方程式书写正确的是
A.金属Na与 溶液反应:
B. 溶于过量HI溶液:
C.澄清石灰水与过量小苏打溶液混合:
D.草酸( )与酸性 溶液反应:
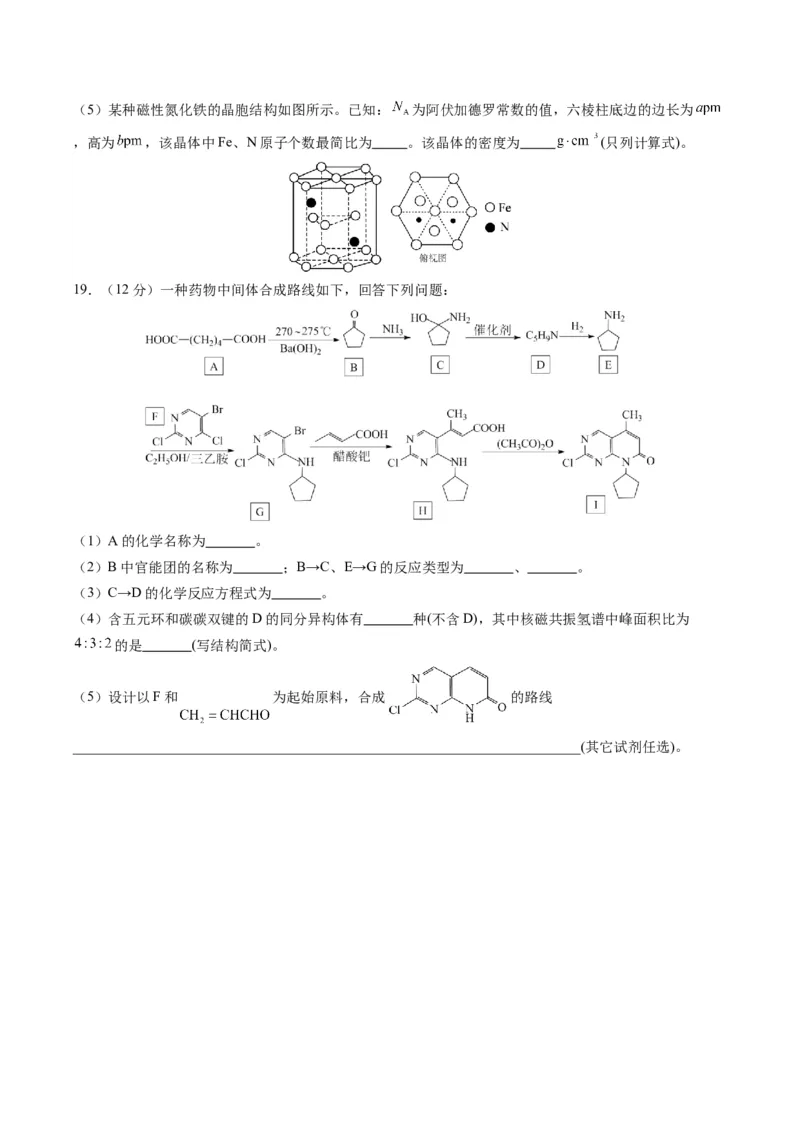
12.25℃,用浓度为 的NaOH溶液滴定20.00mL浓度为 的三种酸HX、HY、
HZ,滴定曲线如图所示。下列说法不正确的是
A.在相同温度下,同浓度的三种酸溶液的导电能力:HZ>HY>HX
B.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时,溶液中存在:
C.滴定至终点时,消耗的NaOH溶液体积相同
D.根据滴定曲线,可知
13.实验探究是化学学习的方法之一、根据下列实验设计的现象所得实验结论正确的是选项 实验设计 现象 实验结论
在坩埚中加入16.4g ,加热一段时 加热后坩埚内固体为
A 质量为12.8g
和 混合物
间,在干燥器中冷却,称量剩余固体质量
产生白色沉淀,加
B 向鸡蛋清溶液中滴入几滴硫酸铜溶液 蛋白质发生了变性
水后沉淀不溶解
分别用蒸馏水、 溶液喷洒甲、乙 喷洒 溶液的纸
C 能促进纸张的老化
两张白纸,静置、干燥 张老化明显
烧瓶中有红棕色气 木炭具有还原性,能还
D 在烧瓶中加入木炭颗粒与浓硝酸,然后加热
体产生 原
14.T℃下,三种硫酸盐 (M表示 或 或 )的沉淀溶解平衡曲线如图所示。已知
, 。下列说法正确的是
A. 在任何条件下都不可能转化为
B.X点和Z点分别是 和 的饱和溶液,对应的溶液中
C.T℃下,反应 的平衡常数为
D.T℃时,用 溶液滴定 浓度均为 和 的混合溶
液, 先沉淀
第Ⅱ卷
二、非选择题:共5题,共58分。
15.(11分)三氯氧钒(VOCl ,M=173.5g/mol)是一种重要的无机试剂,主要用作溶剂、烯烃聚合的催化
3
剂,还可用于钒有机化合物的合成。已知三氯氧钒为黄色液体,密度为1.84g/cm3,熔点为-77℃,沸点为
126℃,遇水会迅速水解生成HCl和一种氧化物。某小组同学利用如图装置以氯气、VO 和碳粉为原料制
2 5
备三氯氧钒。回答下列问题:
(1)仪器X的名称为 。
(2)从 中选择必要的仪器制备VOCl ,正确的连接顺序是 (按气流方向,用小写字母表
3
示,装置可重复使用)。
(3)装置A中发生反应的离子方程式为 。
(4)管式炉中发生反应生成CO的化学方程式为 。
(5)装置D的作用为 。
(6)装置E的作用为 。
(7)实验过程中正确的加热顺序为 (填序号)。
①先点燃A处酒精灯,再加热管式炉
②先加热管式炉,再点燃A处酒精灯
(8)若管式炉中加入 和 的碳粉,通入足量氯气充分反应后,在装置 的烧瓶中最终收集到
黄色的三氯氧钒液体,则该实验中三氯氧钒的产率为 (保留3位有效数字)。
16.(12分)氧化铈 (CeO) 是一种广泛应用的稀土氧化物。现以氟碳铈矿 (含 CeFCO、BaO、SiO 等)
2 3 2
为原料制备氧化铈,其工艺流程如图所示;
已知:
①稀土离子易与 形成复盐沉淀。
②硫脲: 具有还原性,酸性条件下易被氧化为(SCN H)
2 3 2.
③Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀。
回答下列问题:
(1)“焙烧”时,氧化数据如表所示:
空气氧化法 氧化温度/℃ 氧化率/% 氧化时间/h暴露空气中 450~500 80 14
对流空气氧化炉
450~500 98 6
中
在对流空气氧化炉中可大大缩短氧化时间的原因是 。
(2)焙烧后加入稀硫酸浸出,Ce的浸出率和稀硫酸浓度、温度有关,其关系如图所示,则使Ce的浸出率
最高应该选择的条件是 。
(3)加入硫脲的目的是将 还原为Ce3+,反应的离子方程式为 。步骤③加入盐酸后,通
常还需加另一种化学试剂X,根据题中信息推测 。
(4)步骤④的离子方程式为 。若“沉铈”中,Ce3+恰好沉淀完全[c(Ce3+)为1.0×10﹣5mol/L,
此时溶液的pH为5,则溶液中c( )= mol/L(保留2位有效数字)。{已知常温下
K (H CO)=4.3×10﹣7,K (H CO)=5.6×10﹣11,K [Ce (CO)]=1.0×10﹣28}。
a1 2 3 a2 2 3 sp 2 3 3
(5)若Ce (CO) 经步骤⑤充分灼烧后质量减少5.8t,则获得CeO 的质量为 t。
2 3 3 2
(6)Ce4+溶液可以吸收大气中的污染物NO 减少空气污染,其转化过程如图所示(以NO 为例)该转化过程
x 2
中的催化剂为 。
17.(11分)研究碳、氮、硫元素化合物的性质及其相互转化对建设生态文明、美丽中国具有重要意义,
请回答下列问题
Ⅰ.已知热化学方程式:
Fe O(s)+3CO(g)=2Fe(s)+3CO (g) △H=﹣25kJ•mol﹣1
2 3 2 1
3Fe O(s)+CO(g)=2Fe O(s)+CO(g) △H=﹣47kJ•mol﹣1
2 3 3 4 2 2
Fe O(s)+CO(g)=3FeO(s)+CO (g) △H=+19kJ•mol﹣1
3 4 2 3
(1)已知FeO(s)被CO(g)还原成Fe(s) (g)的正反应活化能为234kJ/mol,则其逆反应活化能为
2
kJ/mol。
Ⅱ.一种以CO 为碳源,在催化剂作用下催化加氢制备可再生能源甲醇的反应如下:
2反应i:CO(g)+3H(g) CHOH(g)+H O(g) △H=﹣49.1kJ•mol﹣1
2 2 3 2 4
反应ii:CO(g)+H(g) CO(g)+HO(g) △H=+41.1kJ•mol﹣1
2 2 2 5
(2)往恒容密闭容器中按n(CO)∶n(H )=1∶3(总量为amol)充入反应物,在合适催化剂作用下,CO 的平衡转
2 2 2
化率和甲醇的选择率(转化为甲醇的CO 物质的量与参加反应的CO 总物质的量之比)如图所示。在513K达
2 2
平衡时,甲醇的物质的量为 mol(列出计算式即可)。随着温度的升高,ABC所在曲线逐减升
高的原因是 。
(3)现向恒温恒容(0.1MPa)的密闭容器中充入1molCO 、3molH 和6molHe,选择合适的催化剂使其仅按
2 2
反应i进行,反应10min后达平衡 的转化率为20%,则氢气的分压变化率为 MPa•min﹣1(请计算出
2
结果),该反应的K = MPa﹣2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,列出
p
计算式即可)。
Ⅲ.研究人员开发了一种新型的硼、氮共掺杂的多孔石墨烯材料作为正极催化剂的锂—二氧化碳二次电池
(如图),实现了碳酸锂在电池中的高度可逆分解,减少二氧化碳的排放。
(4)给电池充电时,阳极反应式为 。
18.(12分)近日,科学家利用铁配合物催化氮气选择性转化成肼。铁配合物结构如图所示(Et为乙基)。
回答下列问题:
(1)基态 最外层有 个电子, 转化为 时失去的是 轨道上的电子。
(2) 所含元素中,电负性最大的元素是 。P原子的杂化类型是 。
(3) 和 的相对分子质量相同,但是常温常压下, 呈液态,而 呈气态,其主要原因是
。
(4) 的VSEPR模型为 。 最多能与 反应。(5)某种磁性氮化铁的晶胞结构如图所示。已知: 为阿伏加德罗常数的值,六棱柱底边的边长为
,高为 ,该晶体中Fe、N原子个数最简比为 。该晶体的密度为 (只列计算式)。
19.(12分)一种药物中间体合成路线如下,回答下列问题:
(1)A的化学名称为 。
(2)B中官能团的名称为 ;B→C、E→G的反应类型为 、 。
(3)C→D的化学反应方程式为 。
(4)含五元环和碳碳双键的D的同分异构体有 种(不含D),其中核磁共振氢谱中峰面积比为
的是 (写结构简式)。
(5)设计以F和 为起始原料,合成 的路线
________________________________________________________________________(其它试剂任选)。