文档内容
解密五大平衡常数(1)
重难点 题型 分值
1. 熟练掌握几种常数的表达式,含义,影
响因素及其应用
重点 2. 重点掌握有关化学平衡常数的计算,与
溶度积有关的几种计算
选择题、填空题 4-6分
3. 通过对几种常数的比较,掌握其意义
1. 几种平衡常数的应用
难点
2. 有关化学平衡常数的计算
1. 化学平衡常数(K)、电离平衡常数(K 或K )、水的离子积常数(K )、水解平衡
a b w
第1页常数(K )、沉淀溶解平衡常数(K )本质上都是平衡常数,都只是温度的函数,体现了
h sp
平衡时溶液中离子浓度的特定关系,其大小只受温度影响。
2. 五大平衡常数是《化学反应原理》的重要内容,属于新课标新增的重点内容,使化学
由定性描述走向定量研究,“用数据来说话”让化学变得富有活力,所以从一定意义上讲
掌握了五大平衡常数,就掌握了一把解决有关平衡问题的金钥匙。因此,可以预测这“五
大平衡常数”在今后的高考中,将继续成为考查的重点及热点。
一、化学平衡常数
1. 概念
在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂
之积的比值是一个常数,用符号K表示。
2. 表达式
(1)对于反应 mA(g)+nB(g) pC(g)+qD(g),化学平衡常数
,式子均为平衡浓度(气体或溶液)。
c(CO)⋅c(H )
2
c(H O)
如:C(s)+HO(g) CO(g)+H (g)的平衡常数表达式K= 2
2 2
。
【注意】①固体和纯液体物质的浓度视为常数,通常不写入平衡常数表达式中,但水
蒸气需写入。
②计算时,代入平衡常数表达式的浓度是平衡浓度。
(2)化学平衡常数是指某一个具体反应的平衡常数,当化学反应方向改变或化学计量
数改变时,化学平衡常数也发生改变,例如:
化学方程式 平衡常数表达式 相互关系
c(N )⋅c3 (H )
2NH (g) N (g)+3H 2 2
3 2 2
(g) K = c2 (NH 3 ) 1
1
c2 (NH ) K
N 2 (g)+3H 2 (g) 2NH 3 3 K 1 = 2(用 K 2 表示)
(g) c(N )⋅c3 (H ) 1
K = 2 2 √K
2 2
K = 2( 或 K )
1 3 c(NH ) 3 2
3 (用K 表示)
2 2 1 3 2
N (g)+ H (g)
2 2 c2 (N )⋅c2 (H )
NH (g) K = 2 2
3 3
【实例】已知下列反应在某温度下的平衡常数:
H(g)+S(s) HS(g) K
2 2 1
S(s)+O(g) SO (g) K
2 2 2
则在该温度下反应H (g)+SO (g) O (g)+HS(g)的平衡常数为K / K 。
2 2 2 2 1 2
(用K 、K 表示)
1 2
第2页【点拨】化学平衡常数与化学方程式书写形式的关系
①正、逆反应的平衡常数互为倒数。
1
n
②若化学方程式中各物质的化学计量数都变成n倍或 倍,则化学平衡常数变为原来
1
n
的n次幂或 次幂。
③两方程式相加得到新的化学方程式,其化学平衡常数是两反应平衡常数的乘积。
3. 影响因素
只与温度有关,与物质的浓度、压强等无关。
①对于正向吸热的可逆反应:升高温度,平衡正向移动,导致生成物浓度增大,反应
物浓度减小,K值增大,反之,降温则K值减小。
②对于正向放热的可逆反应:升高温度,平衡逆向移动,导致生成物浓度减小,反应
物浓度增大,K值减小,反之,降温则K值增大。
4. 应用
(1)判断可逆反应进行的程度
平衡常数越大,说明生成物的平衡浓度越大,反应物的平衡浓度越小,反应物的转化
率越大。即该反应进行得越完全。
K <10-5 10-5~105 >105
反应程度 很难进行 反应可逆 反应可接近完全
(2)判断化学反应进行的方向
对于可逆反应aA(g)+bB(g) cC(g)+dD(g)的任意状态时的浓度商Q
cc (C)⋅cd (D)
ca (A)⋅cb (B)
(即K表达式中带入任意时刻的浓度),浓度商Q= 。
Q K,反应向逆反应方向进行,v(正)<v(逆)
(3)判断可逆反应的热效应
5. 有关化学平衡常数的计算
(1)明确三个量——起始量、转化量、平衡量
第3页N + 3H 2NH
2 2 3
起始量 1 3 0
转化量 a b c
平衡量 1-a 3-b c
【注意】没有标明单位,可以是物质的量,也可以是浓度
①反应物的平衡量=起始量-转化量。
②生成物的平衡量=起始量+转化量。
③各物质转化浓度(物质的量)之比等于它们在化学方程式中化学计量数之比。转化
浓度是联系化学方程式、平衡浓度、起始浓度、转化率、化学反应速率的桥梁。因此抓住
转化浓度是解题的关键。
(2)掌握四个公式
n(转化) c(转化)
n(起始) c(起始)
①反应物的转化率= ×100%= ×100%。
②生成物的产率:实际产量(指生成物)占理论产量的百分数。一般地,转化率越大,
原料利用率越高,产率越大。
实际产量
理论产量
产率= ×100%。
平衡量
平衡时各物质的总量
③平衡时混合物组分的百分含量= ×100%。
某组分的物质的量
混合气体总的物质的量
④某组分的体积分数= ×100%。
(3)谨记一个答题模板
对于反应:mA(g)+nB(g) pC(g)+qD(g),令A、B起始物质的量分别
为a mol、b mol,达到平衡后,A的转化量为mx mol,容器容积为V L,则有以下关系:
mA(g)+nB(g) pC(g)+qD(g)
起始/mol a b 0 0
转化/mol mx nx px qx
平衡/mol a-mx b-nx px qx
px qx
p q
( )⋅( )
V V
a−mx b−nx
m n
( ) ⋅( )
V V
则有:①K=
a−mx
V
②c (A)= mol·L-1
平
mx
a
③α(A) = ×100%
平
第4页a−mx
×100%
a+b+(p+q−m−n)x
④φ(A)=
p
平 a+b+(p+q−m−n)x
p
⑤ 始=
a+b
⑥平衡时体系的平均摩尔质量:
a⋅M(A)+b⋅M(B)
M
=
a+b+(p+q−m−n)x
g·mol-1
【注意】计算平衡常数时代入的必须是各物质的平衡浓度(对于反应前后气体总体积
不变的反应,也可以用各物质平衡时的物质的量)。平衡常数的单位是一个复合单位,可
写,也可以不写。
【即时练】1
研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO (g)+ NaCl(s) NaNO (s)+ ClNO(g)K ΔH < 0(I)
2 3 1 1
2NO(g)+ Cl (g) 2ClNO(g)K ΔH<0(Ⅱ)
2 2
(1)4NO (g)+ 2NaCl(s) 2NaNO (s)+2NO(g)+ Cl (g)的平衡常数K =
2 3 2
(用K 、K 表示)。
1 2
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2L恒容密闭容器中加
入0. 2mol NO和0. 1mol Cl ,10min时反应(Ⅱ)达到平衡。测得10min内v(ClNO)=7.
2
5×10-3mol·L-l·min-1,则平衡后n(Cl)= mol,NO的转化率α = 。
2 1
【答案】(1)K= (2)2. 5×10-2 75%
【解析】(1)将题干中已知的两个化学方程式做如下处理:(I)×2-(Ⅱ)可得
4NO (g)+2NaCl(s)=2NaNO (s)+2NO(g)+ Cl (g),则其平衡常数K= 。
2 3 2
(2)根据“三段式”:
2NO(g)+ Cl (g) 2ClNO(g)
2
起始(mol•L-1) 0. 1 0. 05 0
转化(mol•L-1) 0. 1α 0. 05α 0. 1α
1 1 1
平衡(mol•L-1) 0. 1-0. 1α 0. 05-0. 5α 0. 1α
1 1 1
v (ClNO)= 7. 5×10-3mol·L-1·min-1,得α =75%,平衡时n(C1 )=
1 2
(0. 05-0. 05α )mol·L-1×2L=0. 025mol。
1
二、电离平衡常数
第5页1. 概念:在一定条件下,弱电解质的电离达到平衡时,溶液中电离出的各种离子浓度的
乘积与溶液中未电离的分子的浓度之比是一个常数,这个常数称为电离平衡常数,简称电
离常数。弱酸用K 表示,弱碱用K 表示。
a b
2. 表达式:
c(A−)⋅c(H+)
c(HA)
(1)对于一元弱酸HA:HA H+ + A+,电离常数K= 。
a
c(B+)⋅c(OH−)
c(BOH)
(2)对于一元弱碱BOH:BOH B+ + OH-,电离常数K = 。
b
(3)多元弱酸分步电离,各级电离常数的大小关系是K K K ……故其酸性主要决
1 2 3
定于第一步电离。
≫ ≫
3. 影响因素:
内因(决定性因素),弱电解质本身的性质。
外因,只与温度有关,升温,K值增大(因为弱电解质的电离是吸热的)。电离常数
同化学平衡常数一样,只与温度有关,而不受溶液中粒子浓度的影响,由于电离过程是吸
热的,因此电离常数随着温度的升高而增大。
4. 应用:
①衡量弱电解质电离的难易程度。在相同条件下,K 值越大,表示该弱电解质越易电
离,所对应的酸性或碱性相对越强。
②判断盐溶液的酸性或碱性强弱,碱或酸的电离常数越大,对应的盐水解程度越小,
酸性或碱性越弱。
③判断弱酸性酸性的相对强弱,进而判断某些酸参加的复分解反应能否发生。一般符
合“强酸制弱酸”规律。
④判断微粒浓度比值的变化。加水稀释弱电解质溶液时,能促进其电离,溶液中离子
和分子的浓度会发生相应的变化,但电离常数不变,题目中经常利用电离常数不变这一特
点来判断溶液中某些微粒浓度比值的变化情况。
如 将 0.1mol/LCH COOH 溶 液 加 水 稀 释 , 溶 液 中
3
,稀释过程中,c(H+)减小,K 值不变,则
a
的值变大。
⑤判断电离平衡的移动方向。向稀醋酸中加入冰醋酸,此时c(CHCOOH)增大,溶
3
液中有关微粒的浓度商 ,电离平衡正向移动;反之,向
第6页溶液中通入HCl气体,则因c(H+)增大,使Q>Ka,电离平衡逆向移动。
【即时练】
已知HCO 的第二级电离常数K =5. 6×10-11,HClO的电离常数K=3. 0×10-8,写出下列
2 3 2
条件下所发生反应的离子方程式:
(1)少量Cl 通人到过量的NaCO 溶液中:
2 2 3
(2)Cl 与NaCO 按物质的量之比1:1恰好反应:
2 2 3
(3)少量CO 通入到过量的NaClO溶液中:
2
【答案】(1)Cl+H O+2CO2-=2HCO-+Cl-+ClO-
2 2 3 3
(2)Cl+H O+CO2-=HCO-+Cl-+HclO
2 2 3 3
(3)ClO-+CO +H O═HClO+HCO -
2 2 3
三、水的离子积常数(K )
w
1. 概念:一定温度下,水或稀的水溶液中c(H+)与c(OH-)的乘积是一个常数,称
为水的离子积常数,简称水的离子积,用K 表示,即K = c(H+)·c(OH-)。
w W
2. 表达式:K = c(H+)·c(OH-)。在稀溶液中,c(H+)·c(OH-)= K ,其中c
W W
(H+)、c(OH-)是溶液中的H+、OH-浓度:水电离出的H+ 数目与OH-数目相等。
25℃时, K = 1. 0×10-14。
w
3. 影响因素:只与温度有关,温度升高,K 增大。常温下(25℃),K = 1. 0×10-14;
w w
100℃,K = 1. 0×10-12。
w
【注意】K 不仅适用于纯水中,还适用于稀的电解质水溶液。
w
4. 应用
①通过K 的大小比较相应温度的高低。
w
②溶液中c(H+)与c(OH-)相互换算。
③酸、碱、能水解的盐溶液中水电离出的c(H+)或c(OH-)的计算等。
【即时练】
下图表示水中c(H+)和c(OH-)的关系,下列判断错误的是( )
A. 两条曲线间任意点均有c(H+)·c(OH-)=K
W
B. M区域内任意点均有c(H+)<c(OH-)
C. 图中T<T
1 2
第7页D. XZ线上任意点均有pH=7
【答案】D
【解析】根据水的离子积定义可知A项正确;XZ线上任意点都存在c(H+)=c(OH
-),所以M区域内任意点均有c(H+)<c(OH-),B项正确;因为图像显示T 时水的
1
离子积小于T 时水的离子积,而水的电离程度随温度升高而增大,则 T <T ,C项正确;
2 1 2
XZ线上只有X点的pH=7,D项错误。
四、盐的水解常数(K )
h
一元弱酸强碱盐的水解常数:K =K /K,在常温下,水的离子积常数K 为一常数,故
h w a w
弱酸强碱盐的水解常数值K 取决于弱酸的电离常数K 的大小。K 越小,即酸越弱,则K
b a a b
越大,说明该盐的水解程度越大;反之,K 越大,K 越小,水解程度越小。
a b
强酸弱碱盐的水解常数:K=K /K ,组成该盐的碱越弱,水解常数K 越大,水解程度
h w b b
也就越大。
多元弱酸盐的水解常数:多元弱酸盐的水解比较复杂,它们的水解过程与多元弱酸的
电离相似,也是分步进行的,每一步都有相应的水解常数。但通常由于第一步的水解程度
远远大于第二步的水解程度,主要考虑第一步的水解。
如:CO2- + H O HCO -+ OH-的
3 2 3
K =
h
如:HCO - + H O HCO + OH-的
3 2 2 3
【即时练】
NaHCO 的水溶液呈碱性,通过简要的计算说明原因。(已知:HCO 的电离常数
3 2 3
K =4. 4×10-7,K =4. 7×10-11)
1 2
【解析】NaHCO 电离出的HCO -既能水解也能电离,只需比较其水解和电离程度的
3 3
大小即可。电离:HCO - CO2-+H+(呈酸性),K =4. 7×10-11。水解:HCO -+ H O
3 3 2 3 2
HCO + OH-(呈碱性),K =K /K =2. 3×10-8。K>K ,说明水解程度大于其电离程度,
2 3 h w 1 h 2
故NaHCO 的水溶液呈碱性。
3
五、难溶电解质的溶度积常数(K )
sp
1. 概念:一定温度下,在难溶电解质的饱和溶液中,各离子浓度幂之积为一常数,称为
溶度积常数,简称溶度积,符号为K 。
sp
2. 表达式:对于M A 的饱和溶液,M A (s) mMn++(aq)+nAm+(aq),Ksp=cm
m n m n
(Mn+)·cn(Am+),固体纯物质不列入平衡常数。
第8页3. 影响因素:
(1)内因
难溶电解质本身的性质,这是主要决定因素。
(2)外因
K 只受温度的影响(通常随温度的升高而增大),在一定温度下,K 是一个常数。
sp sp
【注意】①溶度积的大小只与难溶电解质本身的性质和温度有关,与浓度无关。
②升高温度,少数平衡向生成沉淀的方向移动,如Ca(OH) 的溶解平衡。
2
4. 应用:
(1)判断沉淀生成的顺序
对于同类型(同种类型是指从化学式组成来看阴、阳离子个数之比相等。)且含有相
同离子的沉淀,溶度积越小,沉淀越先生成。例如向物质的量浓度相等的 NaCl和NaI的混
合溶液中逐滴加入AgNO 溶液,先生成AgI沉淀,后生成AgCl沉淀。这是因为沉淀I-所
3
需的c(Ag+)比沉淀C1-所需的c(Ag+)小。
(2)判断沉淀生成的条件
生成沉淀的条件是满足Q>K ,由此可以计算出使离子沉淀完全的条件。通常认为当
sp
溶液中的离子浓度小于等于10-5mol·L-1时,该离子已沉淀完全。以Fe(OH) 为例,可
3
计算Fe3+完全沉淀所需控制的pH:K [Fe(OH)]=2.8×10-39,当c(Fe3+)=10-5mol·L-1时,
sp 3
c(OH-)= 6. 54×10-12mol·L-1,c(H+)=1. 53×10-3mol·L-1,pH≈2.
8,故Fe在pH=2. 8时沉淀完全。同理可计算Cu²+、Mg²+、Fe2+等金属离子沉淀完全时溶液
的pH。
5. 与溶度积有关的几种计算
(1)已知溶度积,求饱和溶液中某种离子的浓度。如K (AgCl)= a,则饱和AgC1
sp
溶液中,c(Ag+)= 。
(2)已知溶度积和溶液中某种参与沉淀溶解平衡的离子浓度,求达到沉淀溶解平衡后
另一种参与沉淀溶解平衡的离子浓度。如某温度下K (AgCl)=a,在0. 1mol·L-1的NaCl
sp
溶液中加入过量的AgCl固体,达到平衡后c(Ag+)=10a mol·L-1。
(3)计算沉淀转化反应的平衡常数,如对于反应Cu2+(aq)+ZnS(s) CuS(s)+
Zn2+(aq),Ksp(ZnS)=c(Zn2+)·c(S2-),K (CuS)=c(Cu2+)·c(S2-),该反应的
sp
平衡常数 。
如:AgCl+I- AgI+Cl-[已知:K (AgCl)=1. 8×10-10、K (AgI)=8. 5×10-
sp sp
c(Cl−) c(Ag+)⋅c(Cl−) K
sp
(AgCl) 1.8×10−10
17] 反 应 的 平 衡 常 数 K =
c(I−)
=
c(Ag+)⋅c(I−)
=
K
sp
(AgI)
=
8.5×10−17
第9页≈2.12×106。
【注意】①误认为只要K 越大,其溶解度就会越大。其实溶解度不只与K 有关,还
sp sp
与难溶物化学式中的各离子配比有关。只有同类型的难溶物的K 大小才可用于比较其溶解
sp
度大小。
②一定温度下,误认为溶解度受溶液中相同离子浓度的影响而导致K 改变。实际上
sp
K 只受温度影响,温度不变则K 不变,如Mg(OH) 在MgCl 溶液中的溶解度要小于在
sp sp 2 2
纯水中的溶解度,而K [Mg(OH)]不变。
sp 2
③误认为K 小的不能转化为K 大的,只能实现K 大的向K 小的转化。实际上,当
sp sp sp sp
两种难溶电解质的K 相差不是很大时,通过调节某种离子的浓度,可实现难溶电解质由
sp
K 小的向K 大的转化。
sp sp
【小试牛刀】已知:某温度时,K (FeC O )=2. 0×10-7,K (CaC O )=2. 5×10-
sp 2 4 sp 2 4
9。下列说法不正确的是( )
A. 向NaC O 溶液中加入FeCl 与CaCl ,当两种沉淀共存时,溶液中c(Fe2+)∶c
2 2 4 2 2
(Ca2+)=80∶1
B. 向FeC O 悬浊液中加入适量CaCl ,可以生成CaC O 沉淀
2 4 2 2 4
C. CaC O 饱和溶液的物质的量浓度为5×10-5 mol·L-1
2 4
D. FeC O 的溶解度小于CaC O 的溶解度
2 4 2 4
【答案】D
c(Fe2+) K
sp
(FeC
2
O
4
) 2.0×10−7
【解析】A 项,当两种沉淀共存时,
c(Ca2+)
=
K
sp
(CaC
2
O
4
)
=
2.5×10−9
=
2−
80∶1,正确;B项,向FeC O 悬浊液中加入适量CaCl ,当c(Ca2+)·c(C O4 )>K
2 4 2 2 sp
(CaC O )时,则有CaC O 沉淀,正确;C项,CaC O 饱和溶液中,c(Ca2+)=c(C O
2 4 2 4 2 4 2
2− 2−
4 )且c(Ca2+)·c(C O4 )=2. 5×10-9,故CaC O 浓度为5×10-5 mol·L-1,正确;D项
2 2 4
K (FeC O)>K (CaC O),故FeC O 溶解度大。
sp 2 4 sp 2 4 2 4
(答题时间:40分钟)
一、选择题
1. 在一定温度下的密闭容器中,加入1 mol CO和1 mol H O(g)发生反应:CO(g)
2
+H O(g) CO(g)+H (g),达到平衡时测得n(H)为0. 5 mol,下列说法不正确
2 2 2 2
的是( )
A. 在该温度下平衡常数K=1
第10页B. 平衡常数与反应温度无关
C. CO的转化率为50%
D. 其他条件不变,改变压强平衡不移动
2. 25 ℃,两种酸的电离常数如下表。
K K
a1 a2
HA 1. 3×10-2 6. 3×10-6
2
HB 4. 2×10-7 5. 6×10-11
2
下列叙述中正确的是( )
A. H A的电离方程式:HA===2H++A2-
2 2
K
W
B. 常温下,在水中NaB的水解平衡常数为:K
=4.2×10−7
2 b1
C. 等浓度的NaA和NaB溶液,由水电离产生的H+浓度大小关系为前者大于后者
2 2
D. 向NaHB溶液中加入少量HA溶液,可发生反应:2HB-+H A===A2-+2H B
2 2 2
3. 常温下,取一定量的PbI 固体配成饱和溶液,t时刻改变某一条件,离子的浓度变化
2
如图所示[注:第一次平衡时c(I-)=2×10-3 mol·L-1,c(Pb2+)=1×10-3 mol·L-1]。下列有关
说法正确的是( )
A. 常温下PbI 的K =2×10-6
2 sp
B. 温度不变,向PbI 饱和溶液中加入少量硝酸铅浓溶液,PbI 的溶解度不变,c
2 2
(Pb2+)增大
C. t时刻改变的条件可能是升高温度,PbI 的K 增大
2 sp
D. 常温下K (PbS)=8×10-28,向PbI 的悬浊液中加入NaS溶液,PbI (s)+S2-(aq)
sp 2 2 2
PbS(s)+2I-(aq)反应的化学平衡常数为5×1018
4. 下列关于化学平衡常数(K)、电离平衡常数(K 或K )、水解平衡常数(K )、沉
a b h
淀溶解平衡常数(K )、水的离子积常数(K )的叙述中错误的是( )
sp W
A. K值越大,正反应进行的程度越大,一般地说,K>105时,该反应进行得就基本完
全了
B. 比较K 与离子积Q 的相对大小,可判断难溶电解质在给定条件下沉淀能否生成或
sp c
溶解
C. K、K 或K 、K 、K 、K 都与温度有关,温度越高,常数值越大
a b h sp W
第11页D. 弱酸HA的K 与NaA的K 、水的离子积常数K 三者间的关系可表示为K =K·K
a h W W a h
5. 将固体NH I置于密闭容器中,在一定温度下发生下列反应:①NH I(s) NH
4 4 3
(g)+HI(g)
②2HI(g) H(g)+I (g)。达到平衡时,c(H)=0. 5 mol·L-1,c(HI)=4
2 2 2
mol·L-1,则此温度下反应①的平衡常数为( )
A. 9 B. 16 C. 20 D. 25
6. 下列溶液或浊液中,关于离子浓度的说法正确的是 ( )
A. 一定浓度的氨水加水稀释的过程中,c(NH +)/c(NH ·H O)的比值减小
4 3 2
B. 浓度均为0. 1 mol·L-1的NaCO、NaHCO 混合溶液中:c(CO2-)>c(HCO -),且
2 3 3 3 3
2c(Na+)=3c(HCO)+3c(HCO -)+3c(CO2-)
2 3 3 3
C. 常温下0. 4 mol·L-1 HB溶液和0. 2 mol·L-1 NaOH溶液等体积混合后溶液的pH=3,
则溶液中微粒浓度存在下面关系:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
D. 假设HClO的电离平衡常数为K,碳酸的电离平衡常数分别记为:K 和K ,已知:
a a1 a2
K >K>K ,则发生反应:2NaClO+CO (少量)+H O=Na CO+2HClO
a1 a a2 2 2 2 3
二、非选择题
7. 研究氮氧化物的反应机理,对于消除环境污染有重要意义。升高温度绝大多数的化学
反应速率增大,但是2NO(g)+O (g) 2NO (g)的速率却随温度的升高而减小。
2 2
某化学小组为研究特殊现象的实质原因,查阅资料知:
2NO(g)+O(g) 2NO (g)的反应历程分两步:
2 2
①2NO(g) NO(g)(快)
2 2
v =k c2(NO) v =k c(NO) ΔH<0
1正 1正 1逆 1逆 2 2 1
②NO(g)+O(g) 2NO (g)(慢)
2 2 2 2
v =k c(NO)·c(O) v =k c2(NO ) ΔH<0
2正 2正 2 2 2 2逆 2逆 2 2
请回答下列问题:
(1)一定温度下,反应2NO(g)+O (g)2NO (g)达到平衡状态,请写出用
2 2
k 、k 、k 、k 表示的平衡常数表达式K=________,根据速率方程分析,升高温度该
1正 1逆 2正 2逆
反应速率减小的原因是________(填字母)。
a. k 增大,c(NO)增大
2正 2 2
b. k 减小,c(NO)减小
2正 2 2
c. k 增大,c(NO)减小
2正 2 2
d. k 减小,c(NO)增大
2正 2 2
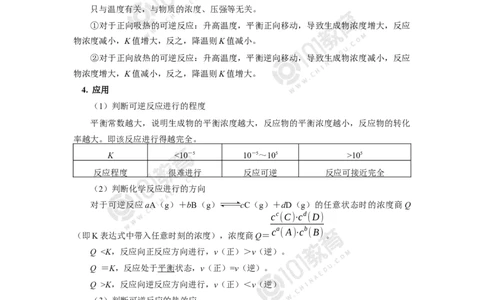
(2)由实验数据得到v ~c(O)的关系可用如图表示。当x点升高到某一温度时,
2正 2
反应重新达到平衡,则变为相应的点为______(填字母)。
第12页8. HS 与 CO 在高温下发生反应:HS(g)+CO (g) COS(g)+HO
2 2 2 2 2
(g)。在610 K时,将0. 10 mol CO 与0. 40 mol H S充入2. 5 L的空钢瓶中,反应平衡后
2 2
水的物质的量分数为0. 02。
①HS的平衡转化率α=__________%,反应平衡常数K=________。
2 1
②在620 K重复实验,平衡后水的物质的量分数为0. 03,HS的转化率α______α ,
2 2 1
该反应的ΔH______0。(填“>”“<”或“=”)
③向反应器中再分别充入下列气体,能使HS转化率增大的是________(填标号)。
2
A. H S B. CO
2 2
C. COS D. N
2
第13页1.【答案】B
【解析】 CO(g)+ H O(g) CO(g)+H (g)
2 2 2
起始(mol) 1 1 0 0
反应(mol) 0. 5 0. 5 0. 5 0. 5
平衡(mol) 0. 5 0. 5 0. 5 0. 5
0.5×0.5
由反应方程式及以上数据判断可得K=
0.5×0.5
=1,A正确;平衡常数与反应温度有关,
0.5
1
B错误;CO的转化率为 ×100%=50%,C正确;该反应为一个气体化学计量数不变的反
应,改变压强,平衡不移动,D正确。
2.【答案】D
【解析】根据电离平衡常数,HA为二元弱酸,分步电离,电离方程式应分步书写,A
2
c(HB−)⋅c(OH−)
c(B2−)
项错误;水中NaB的水解平衡为B2-+H O HB-+OH-,K = ,分子分
2 2 b1
K
W
母同乘以氢离子浓度,则K =
5.6×10−11
,B项错误;越弱越水解,由于HB的K 小于
b1 2 a2
HA的K ,所以等浓度的NaA和NaB溶液,B2-的水解程度大,由水电离产生的H+浓度
2 a2 2 2
大,C项错误。
3.【答案】D
【解析】K =c(Pb2+)·c2(I-)=4×10-9,A错误;加入硝酸铅,c(Pb2+)增大,PbI 的
sp 2
溶解度减小,B错误;t时刻时c(I-)增加、c(Pb2+)不变,所以改变的条件不可能是升
c2 (I−) c2 (I−)⋅c(Pb2+)
c(S2−) c(S2−)⋅c(Pb2−)
高温度,C错误;K= = = ,D正确。
4.【答案】C
【解析】相同条件下不同反应的K值越大,表示反应进行的程度越大;相同的化学反
应在不同条件下,K值越大,表示反应进行的程度越大,A正确;比较K 与离子积Q 的
sp c
相对大小,可判断难溶电解质在给定条件下沉淀能否生成或溶解,Q>K 时,溶液过饱和
c sp
有沉淀析出;Q=K 时,溶液饱和,沉淀与溶解处于平衡状态;Qc(Na+)=0. 1 mol·L-1,因此c
−
(B-)>c(Na+)>c(HB)>c(H+)>c(OH-),C项正确;HClO的酸性比HCO3 强,所
以NaClO+CO (少量)+H O NaHCO +HClO,D项错误。
2 2 3
k ⋅k
1 2
正 正
k ⋅k
7.【答案】(1) 1 逆 2 逆 c (2)a
【解析】(1)由反应达到平衡状态可知,v =v 、v =v ,所以v ×v =v ×v
1正 1逆 2正 2逆 1正 2正 1逆 2
,即 k c2(NO)×k c(NO )·c(O )=k c(NO )×k c2(NO ),则 K=
逆 1正 2正 2 2 2 1逆 2 2 2逆 2
c2 (NO 2 ) k 1 正 ⋅k 2 正
c2 (NO)⋅c(O 2 ) = k 1 逆 ⋅k 2 逆。
(2)因为决定2NO(g)+O (g) 2NO (g)速率的是反应②,升高温度,v
2 2 2正
减小,平衡向逆反应方向移动,c(O )增大,因此当x点升高到某一温度时,c(O )增
2 2
大,v 减小,符合条件的点为a。
2正
8.【答案】①2. 5 2. 8×10-3 ②> > ③B
【解析】①用三段式法计算:该反应前后是等气体分子数反应,平衡时n(HO)=0.
2
02×0. 50 mol=0. 01 mol。
HS(g)+CO(g) COS(g)+HO(g)
2 2 2
起始/mol 0. 40 0. 10 0 0
转化/mol 0. 01 0. 01 0. 01 0. 01
平衡/mol 0. 39 0. 09 0. 01 0. 01
0.01
0.40
α(HS)= ×100%=2. 5%。对于等气体分子数反应,可直接用物质的量替代浓
2
c(COS)⋅c(H
2
O) 0.01×0.01
度计算平衡常数:K=
c(H
2
S)⋅c(CO
2
)
=
0.39×0.09
≈2. 8×10-3。②总物质的量不变,
第15页HO的物质的量分数增大,说明平衡向右移动,HS的转化率增大。即升高温度,平衡向
2 2
正反应方向移动,正反应是吸热反应。③平衡之后,再充入HS,则CO 的转化率增大,
2 2
HS的转化率减小,A项错误;充入CO ,平衡向右移动,HS的转化率增大,B项正确;
2 2 2
充入COS,平衡向左移动,HS的转化率减小,C项错误;充入N ,无论体积是否变化,
2 2
对于气体分子数相等的反应,平衡不移动,HS的转化率不变,D项错误。
2
第16页解密五大平衡常数(2)
重难点 题型 分值
1. 通过对几种常数的比较,掌握其意义
重点
2. 不同反应或过程平衡常数之间的换算
选择题、填空题 2-4分
难点 不同反应或过程平衡常数之间的换算
四个常数的比较及其计算
1. 四个常数之间的比较
水的离子 难溶电解质溶度积常
化学平衡常数 电离平衡常数
积 数
符号 K K K 或K K
w a b sp
mA(g)+nB(g) HO M A (s) mMn+
2 m n
反应举例 HA H+ + A-
pC(g)+qD H++OH- + ( aq ) +nAm+
第17页(g) (aq),
K =c ( H c(A−)⋅c(H+)
W
Ka=
c(HA) Ksp=cm ( Mn+ ) ·cn
表达式 + ) ·c
(Am+)
(OH-)
水,酸。
弱电解质的电离 难溶电解质的溶解平
适用范围 可逆反应平衡体系 碱、盐的
平衡体系 衡体系
稀溶液
只与温度
只与温度有关,
只与温度有关,与浓 有关,升 只与难溶电解质和温
影响因素 升高温度,K 或
a
度、压强的变化无关 高温度, 度有关
K 增大
b
K 增大
w
规律 遵循平衡移动原理;温度不变,平衡常数不变
注意 固体或纯液体的浓度视为常数,不列入平衡常数的表达式
K ( 或 K ) 越
a b
K 越大, 相同类型的难溶电解
w
K越大,正反应进行 大,弱电解质的
意义 水的电离 质,K 越大,溶解度
sp
的程度越大 酸性(或碱性)
程度越大 越大
越强
2. 四个平衡常数间的计算关系
(1)K、K 、K 间的关系
a h w
强碱弱酸盐,如CHCOONa,在水溶液中CHCOO-+H O CHCOOH + OH-。
3 3 2 3
(2)K 、K 、K 间的关系
b h w
强酸弱碱盐:如NH Cl在水溶液中存在NH + + H O NH •H O + H+。
4 4 2 3 2
(3)K 、 K 、K 之间的关系
h w sp
多元弱碱一元强酸,如氯化铁:
Fe3+(aq)+3H O(1) Fe(OH)(s)+3H+(aq)
2 3
K=c3(H+)/c(Fe3+)。
h
第18页将(K )3=c3(H+)×c3(OH-)与 K =c(Fe3+)×c3(OH-)两式相除,消去 c3
w sp
(OH-)可得K=(K )3/K
h w sp
【即时练】化学平衡常数K、弱电解质的电离平衡常数K 或K 及溶度积常数K 是高
a b sp
中化学中常见的几种常数。它们都能反映相应的可逆变化进行的程度,下列关于以上常数
的说法正确的是( )
A. 对于可逆反应,若改变条件使平衡右移,则达到新的平衡时的平衡常数K一定增大
B. 一定温度下,在 a mol·L-1的饱和石灰水中加入适量的 b mol·L-1 CaCl 溶液
2
(b>a),则一定有Ca(OH) 析出
2
C. 相同温度时,CHCOOH的电离平衡常数K 与NH ·H O的电离平衡常数K 相等,
3 a 3 2 b
所以CHCOONH 的水溶液显中性
3 4
D. 升高温度,以上常数均增大
【答案】C
【解析】平衡常数只与温度有关,A错误;加入CaCl 溶液时溶液体积增大,c(OH
2
-)减小,不一定析出Ca(OH),B错误;化学平衡常数升温时不一定增大,与反应的热
2
效应有关,D错误。
例题1 某温度下,将2 mol A和3 mol B充入一密闭容器中,发生反应:aA(g)+B
(g) C(g)+D(g),5 min后达到平衡,已知该温度下其平衡常数K=1,若温度
不变时将容器的体积扩大为原来的10倍,A的转化率不发生变化,则( )
A. a=3 B. a=2
C. B的转化率为40% D. B的转化率为60%
【答案】C
【解析】温度不变,扩大容器体积(相当于减小压强)时,A的转化率不变,说明反
应前后气体的体积不变,即a=1,A、B错误;设达到平衡时,B的转化量为x mol,则
A、B、C、D的平衡量分别为(2-x)mol、(3-x)mol、x mol、x mol,设容器体积为
x2
(2−x)(3−x)
1 L,则平衡常数K=1= ,解得x=1. 2,B的转化率=1. 2÷3×100%=40%,
C正确,D错误。
例题2 Ⅰ. 在一个容积为2 L的密闭容器中加入2 mol N 和6 mol H ,发生如下反应:
2 2
第19页N
2
(g)+3H
2
(g) ⇌2NH
3
(g) ΔH<0,5 min 后达到平衡,测得 c(NH
3
)=0. 5
mol/L。
(1)该条件下此反应的化学平衡常数的表达式 K=______。温度升高,则 K 值
________(填“变大”“变小”或“不变”)。
(2)从反应开始到平衡,用H 的浓度变化表示的反应速率为________。
2
(3)若平衡时,移走1 mol N 和3 mol H ,在相同温度下再达平衡时c(NH )______
2 2 3
(填“>”“<”或“=”)0. 25 mol/L。
Ⅱ. 25 ℃,将0. 4 mol/L CH COOH溶液和0. 2 mol/L NaOH溶液各100 mL混合后,pH
3
=5。(设混合后溶液总体积为两溶液体积之和)
(1)混合溶液中离子浓度由大到小的顺序是_________________。
(2)①c(CHCOO-)+c(CHCOOH)=________ mol/L,②c(CHCOO-)-c
3 3 3
(CHCOOH)=________ mol/L。
3
Ⅲ. 已知25 ℃时,K [Fe(OH) ]=8×10-39,该温度下反应Fe(OH) +3H+ Fe3+
sp 3 3
+3HO的平衡常数为________________(列式并计算)。向0.001 mol/L FeCl 溶液中通入
2 3
氨气(体积变化忽略不计),开始沉淀时溶液的pH为________。(lg 5=0. 7)
c2 (NH )
3
c(N )⋅c3 (H )
【答案】Ⅰ.(1) 2 2 变小
(2)0. 15 mol/(L·min)
(3)<
Ⅱ. (1)c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3
(2)①0. 2 ②2×10-5[或2×(10-5-10-9]
c(Fe3+) K
sp
8×10−39
c3 (H+) (K ) 3 (1×10−14 ) 3
Ⅲ. K= = w = =8×103 2. 3
【解析】Ⅰ. (1)由化学方程式可知,平衡常数表达式为 K=c2(NH )/[c(N )·c3
3 2
(H)],因为正反应为放热反应,所以升高温度,平衡向逆反应方向移动,K变小。
2
(2)用氨气表示速率为0. 5 mol/L÷5 min=0. 1 mol/(L·min),再根据速率比等于计
量数比,则用氢气表示速率为0. 15 mol/(L·min)。
(3)移走氮气和氢气,平衡向逆反应方向移动,氨的浓度减小,达平衡后其浓度小于
0. 25 mol/L。
Ⅱ. (1)二者混合后,溶质是等物质的量的醋酸和醋酸钠,所以离子浓度大小为 c
(CHCOO-)>c(Na+)>c(H+)>c(OH-)。
3
(2)①因为CHCOO-与CHCOOH总的物质的量不变,只是溶液体积扩大了一倍,
3 3
所以二者浓度和为0. 2 mol/L;②由溶液中的物料守恒得2c(Na+)=c(CHCOO-)+c
3
(CHCOOH),电荷守恒得c(Na+)+c(H+)=c(CHCOO-)+c(OH-),则c
3 3
第20页(CHCOO-)-c(CHCOOH)=2×(10-5-10-9) mol/L。
3 3
Ⅲ. 由 K=c(Fe3+)/c3(H+),K [Fe(OH) ]=c(Fe3+)×c3(OH-),K=
sp 3
K /(K )3=8×103;8×10-39=0. 001×c3(OH-),c(OH-)=2×10-12 mol/L,c(H+)=
sp w
5×10-3 mol/L,pH=2. 3。
例题3 已知K、K、K 、K 、K 分别表示化学平衡常数、弱酸的电离平衡常数、水
a w h sp
的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。
(1)有关上述常数的说法正确的是________(双选;填选项字母)。
a. 它们都能反映一定条件下对应变化进行的程度
b. 它们的大小都随温度的升高而增大
c. 常温下,CHCOOH在水中的K 大于在饱和CHCOONa溶液中的K
3 a 3 a
d. 一定温度下,在CHCOONa溶液中,K =K·K
3 w a h
(2)25℃时,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合所得溶液中c(NH
+
4)=c(Cl-),则溶液显________(填“酸”“碱”或“中”)性;用含a的代数式表
示NH ·H O的电离常数K =________。
3 2 b
−
(3)25 ℃时,HSO HSO3 +H+的电离常数K=1×10-2mol·L-1,则该温度下pH
2 3 a
−
=3、c(HSO3 )=0. 1 mol·L-1的NaHSO 溶液中c(HSO )=________。
3 2 3
(4)高炉炼铁中发生的反应有
FeO(s)+CO(g) Fe(s)+CO(g) ΔH<0
2
该反应的平衡常数表达式K=________;
已知1 100 ℃时,K=0. 25,则平衡时CO的转化率为________;在该温度下,若测得
高炉中 c(CO )=0. 020 mol·L-1,c(CO)=0. 1 mol·L-1,则此时反应速率是 v
2 正
________v (填“>”“<”或“=”)。
逆
(5)已知常温下Fe(OH) 和Mg(OH) 的K 分别为8. 0×10-38、1. 0×10-11,向浓
3 2 sp
度均为0. 1 mol·L-1的FeCl 、MgCl 的混合溶液中加入碱液,要使Fe3+完全沉淀而Mg2+不
3 2
沉淀,应该调节溶液pH的范围是________。(已知lg 2=0. 3,离子浓度低于10-5mol·L-1
时认为沉淀完全)
10−9
【答案】(1)ad (2)中
a−0.01
(3)0. 01 mol·L-1
c(CO )
2
(4)
c(CO)
20% > (5)[3. 3,9)
【解析】(1)对于正反应为放热反应的化学平衡,升高温度,平衡逆向移动,平衡常
数减小,b选项错误;温度不变,CHCOOH的电离常数不变,c选项错误。(2)根据电荷
3
+ +
守恒得c(H+)+c(NH4)=c(Cl-)+c(OH-),因为c(NH4)=c(Cl-),所以
第21页c(NH+
4
)⋅c(OH−) 5×10−3 ×10−7
c(H+)=c(OH-),故溶液显中性。K =
c(NH
3
⋅H
2
O)
=
0.5a−5×10−3
=
b
10−9 c(H+)⋅c(HSO−)
3
a−0.01
。(3)由K =
c(H
2
SO
3
)
,代入数据得 c(HSO )=0. 01 mol·L-1。
a 2 3
c(CO )
2
(4)根据方程式可得K=
c(CO)
;设开始时c(CO)=a mol·L-1,平衡时c(CO )=b
2
b b b
mol·L-1,则
a−b
=0. 25,得a=5b,则平衡时CO的转化率为
a
=
5b
×100%=20%;Q
c
c(CO )
2
=
c(CO)
=0. 20<0. 25,故v >v 。(5)K [Fe(OH) ]=c(Fe3+)·c3(OH-),Fe3+
正 逆 sp 3
8.0×10−38
10−5
完全沉淀时 c3(OH-)= ,得c(OH-)=2×10-11mol·L-1,pH=3. 3,Mg
1.0×10−11
0.1
(OH) 开始沉淀时c2(OH-)= =1. 0×10-10,得c(OH-)=1×10-5mol·L-
2
1,pH=9,调节pH范围为[3. 3,9)。
(答题时间:40分钟)
一、选择题
1. 1L Ag C O 饱和溶液中质量为0. 06257g,若不考虑离子强度,水解等因素,Ag C O
2 2 4 2 2 4
的K 是( )
sp
A. 4. 24×10-8 B. 3. 50×10-11
C. 2. 36×10-10 D. 8. 74×10-12
2. 下表是五种银盐的溶度积常数K (25℃),下列说法不正确的是( )
sp
化学式 AgCl Ag SO Ag S AgBr AgI
2 4 2
溶度积 1. 4×10-10 1. 4×10-5 6. 3×10-50 7. 7×10-13 8. 51×10-16
A. 25℃时五种银盐的饱和溶液中,c(Ag+)最大的是Ag SO 溶液
2 4
B. 在氯化银的悬浊液中加入NaS溶液可以生成黑色的Ag S
2 2
C. 25℃时,在等物质的量浓度的NaCl、CaCl 两溶液中加入足量的AgCl固体形成饱和
2
溶液,则两溶液中AgCl的溶度积相同,且两溶液中c(Ag+)也相同
D. AgBr沉淀可以转化成AgI沉淀,而 AgI沉淀在一定条件下也可以转化成AgBr沉淀
3. 根据表中提供的数据,判断下列说法正确的是( )
化学式 电离常数(25℃)
HCN 4.9×10-10
第22页HCO K=4.3×10-7
2 3 1
K=5.6×10-11
2
A. 等浓度的NaCN、NaHCO 、NaCO 溶液中,pH(NaCO)>pH(NaCN)>pH
3 2 3 2 3
(NaHCO )
3
B. a mol·L-1 HCN溶液与b mol·L-1 NaOH溶液等体积混合后,所得溶液中c(Na+)=c
(CN-),则a一定等于b
C. 等浓度的NaCN、NaHCO 混合溶液中,c(Na+)+c(H+)=c(CN-)+c
3
(HCO -)+c(OH-)
3
D. NaCN溶液中通入少量CO,发生的反应可表示为2NaCN+HO+CO===2HCN+
2 2 2
NaCO
2 3
4. 已知25℃时,弱电解质的电离平衡常数:Ka(CHCOOH)=1.8×10-5,Ka(HSCN)
3
=0. 13。在物质的量浓度均为0. 1 mol·L-1的CHCOONa和NaSCN混合溶液中,下列排序正
3
确的是( )
A. c(OH-)>c(CHCOOH)>c(HSCN)>c(H+)
3
B. c(OH-)>c(HSCN)>c(CHCOOH)>c(H+)
3
C. c(OH-)>c(SCN-)>c(CHCOO-)>c(H+)
3
D. c(OH-)>c(CHCOO-)>c(SCN-)>c(H+)
3
5. 0. 10 mol·L-1 HA溶液中有1%的HA电离,则HA的电离平衡常数K 为( )
a
A. 1. 0×10-5
B. 1. 0×10-7
C. 1. 0×10-8
D. 1. 0×10-9
二、非选择题
6. 室温下,HSO 的电离平衡常数K =1. 0×10-2、K =1. 0×10-7。
2 3 a1 a2
(1)该温度下NaHSO 的水解平衡常数K =________,NaHSO 溶液的pH________
3 h 3
c(H SO )
2 3
c(HSO−)
(填“>”、“<”或“=”)7;若向NaHSO 溶液中加入少量I ,则溶液中 3
3 2
将________(填“增大”、“减小”或“不变”)。
2−
(2)0. 1 mol/L Na SO 溶液的pH=________,从平衡移动的角度解释SO3 的K >
2 3 h1
K 。
h2
第23页第24页1.【答案】B
【解析】0. 06257gAg C O 的物质的量是2. 06×10-4mol,则饱和溶液中阴阳离子的浓
2 2 4
度分别是2. 06×10-4mol/L、4. 12×10-4mol/L,所以其溶度积常数是(4. 12×10-4)2×2.
06×10-4=3. 50×10-11,答案选B。
2.【答案】C
【解析】根据溶度积常数的表达式可计算出饱和溶液中离子的浓度,A正确;根据沉
淀转化的方向,即向生成更难溶的方向转化可知,B正确;溶度积常数只与温度有关系,
而与离子的浓度大小是无关系的。选项C中两种溶液中氯离子的浓度是不同的,虽然溶度
积常数相同,但两溶液中c(Ag+)是不相同的,选项C不正确;只有溶液中离子积大于溶
度积常数,就可以生成相应的沉淀,所以选项D正确,答案选D。
3.【答案】A
【解析】从K的相对大小可以反映酸的电离能力,从而可以判断出反应的方向,如果
不结合题中数据,只是通过物质的化学式考虑,很可能会错选D项。由于电离常数:K
(HCO)>K(HCN)>K(HCO),所以电离能力:HCO>HCN>HCO -,等浓度
2 3 1 2 3 2 2 3 3
的NaCN、NaHCO 、NaCO 溶液中,pH(NaCO)>pH(NaCN)>pH(NaHCO ),A
3 2 3 2 3 3
项正确;根据电荷守恒知,当c(Na+)=c(CN-)时有c(H+)=c(OH-),显然a>b,
B项错误;由电荷守恒知C项表达式中缺少c(CO2-),C项错误;由于K(HCN)>K
3
(HCO),所以电离能力:HCN>HCO -,则NaCN溶液中通入少量CO,不可能生成
2 3 2 3 2
NaCO,而只能生成NaHCO ,D项错误。
2 3 3
4.【答案】A
【解析】电离平衡常数越大,酸性越强。说明醋酸的酸性弱于HSCN的。但酸越弱,
相应的钠盐越容易水解,碱性就越强。所以选项A正确,答案选A。
5.【答案】A
【解析】发生电离的HA的物质的量浓度:c(HA) =0. 10 mol·L-1×1% =1. 0×10-3
mol·L-1,根据:HA H++A-,则平衡时:c(H+)=c(A-)=1. 0×10-3 mol·L-1,c(HA)
=0. 10 mol·L-1-1. 0×10-3 mol·L-1≈0. 10 mol·L-1,将有关数据代入平衡常数表达式得:
平
c(H+)⋅c(A−)
=1.0×10−5
c(HA)
K= 。
a
6.【答案】(1)1. 0×10-12 < 增大
(2)10 一级水解产生的OH-对二级水解有抑制作用
c(HSO−)⋅c(H+)
3
c(H SO ) −
【解析】(1)K = 2 3 ,由 HSO3 +HO HSO +OH-,K =
a1 2 2 3 h
第25页c(H SO )⋅c(OH−) c(H SO )⋅c(OH−)⋅c(H+) K
2 3 2 3 w
c(HSO− 3 ) = c(HSO− 3 )⋅c(H+) = K a 1 =1.0×10-12<K a2 ,这说明
−
HSO3 的电离能力强于水解能力,故溶液显酸性,pH<7;当加入少量I 时,+4价的硫元
2
素被氧化,溶液中有硫酸(强酸)生成,导致溶液的酸性增强,
c(H SO )
2 3
c(HSO−)
c(H+)增大,c(OH-)减小,但因温度不变,故 K 不变,则 3 增大。
h
K
w
K 2−
(2)同理可求出K h1 = a 2 =1. 0×10-7,Na 2 SO 3 溶液的碱性主要由SO3 的一级水解决定,
− 2−
设溶液中 c(OH-)=x mol/L,则c(HSO3 )≈x mol/L、c(SO3 )=0. 1 mol/L-x
mol/L≈0. 1 mol/L,利用水解平衡常数易求出x=1. 0×10-4 mol/L,pH=10。一级水解产生
的OH-对二级水解有抑制作用,导致二级水解程度降低。
第26页