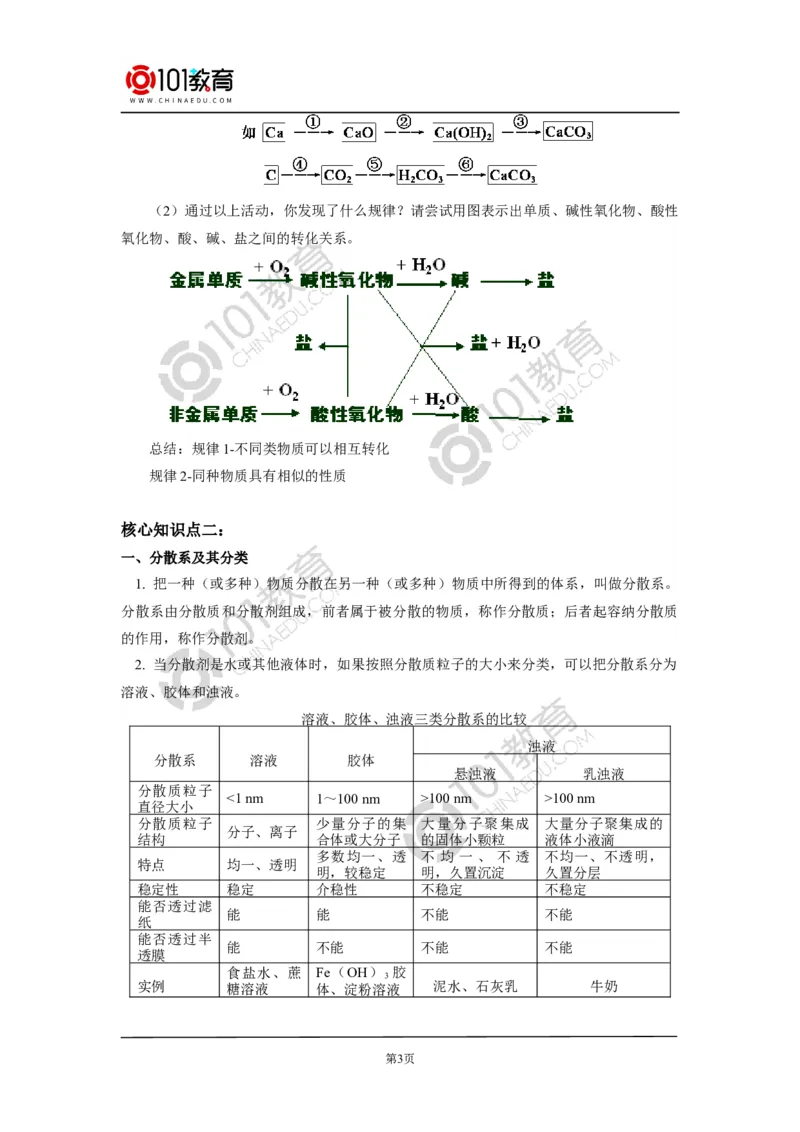
文档内容
高中化学 物质的分类及转化
编稿老师 辛华 一校 黄楠 二校 林卉 审核 徐晓红
重难点 题型 分值
学会分类,能运用熟悉的化学物质和已掌握的相
重点
关知识用交叉分类法和树状分类法进行分类。
选择 3-5分
难点 胶体的性质及应用、分散系的本质
核心知识点一:
一、常见的分类方法
(一)交叉分类法
第1页1. 含义:根据不同的分类标准,对同一事物进行多种分类的方法,即对同一物质以不同
的标准进行分类。
2. 举例
(二)树状分类法
1. 含义:对同类事物按照某种属性进行再分类的分类法。
2. 举例
【特别提醒】物质的分类标准不同,同一种物质可能有不同的归类。
二、物质的转化
1. 酸、碱、盐的性质
(1)酸的化学性质
酸的主要化学性质 反应实例(写出化学方程式)
酸与活泼金属反应 Fe + HSO =FeSO +H ↑
2 4 4 2
酸与碱性氧化物反应 Fe O+6HCl=2FeCl +3H O
2 3 3 2
酸与碱反应 HSO +Ba(OH) =BaSO↓+2H O
2 4 2 4 2
酸与某些盐反应 HSO + BaCl =BaSO↓+ 2HCl
2 4 2 4
(2)讨论:酸、碱、盐的主要化学反应中,涉及的化学反应类型
反应类型 举例 表达式
化合反应 CaO+H O=Ca(OH) A+B=AB
2 2
分解反应 2HO 2HO+O↑ AB =A+B
2 2 2 2
置换反应 Fe+CuSO=FeSO +Cu A+BC=B+AC
4 4
复分解反应 NaOH+HCl=NaCl+H O AB+CD=AD+CB
2
2. 物质的转化
(1)用化学方程式表示下列转化关系。
第2页(2)通过以上活动,你发现了什么规律?请尝试用图表示出单质、碱性氧化物、酸性
氧化物、酸、碱、盐之间的转化关系。
总结:规律1-不同类物质可以相互转化
规律2-同种物质具有相似的性质
核心知识点二:
一、分散系及其分类
1. 把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系,叫做分散系。
分散系由分散质和分散剂组成,前者属于被分散的物质,称作分散质;后者起容纳分散质
的作用,称作分散剂。
2. 当分散剂是水或其他液体时,如果按照分散质粒子的大小来分类,可以把分散系分为
溶液、胶体和浊液。
溶液、胶体、浊液三类分散系的比较
浊液
分散系 溶液 胶体
悬浊液 乳浊液
分散质粒子
<1 nm 1~100 nm >100 nm >100 nm
直径大小
分散质粒子 少量分子的集 大量分子聚集成 大量分子聚集成的
分子、离子
结构 合体或大分子 的固体小颗粒 液体小液滴
多数均一、透 不 均 一 、 不 透 不均一、不透明,
特点 均一、透明
明,较稳定 明,久置沉淀 久置分层
稳定性 稳定 介稳性 不稳定 不稳定
能否透过滤
能 能 不能 不能
纸
能否透过半
能 不能 不能 不能
透膜
食盐水、蔗 Fe(OH) 胶
3
实例 糖溶液 体、淀粉溶液 泥水、石灰乳 牛奶
第3页二、胶体
1. Fe(OH) 胶体的制备
3
(1)反应原理:FeCl + 3H O Fe ( OH ) (胶体)+ 3HC l
3 2 3
(2)操作步骤
向25 mL沸水中逐滴加入5~6滴FeCl 饱和溶液,继续煮沸至溶液呈现红褐色。
3
(3)注意事项
①加热至溶液呈红褐色后停止加热;
②不能用自来水,用蒸馏水,不能搅拌。
2. 胶体的性质
(1)丁达尔效应:可见光束通过胶体时,在入射光的侧面可看见胶体中有一条光亮的
通路,这种现象称为丁达尔效应。这是由胶体粒子对光线散射而形成的,在实验室里可利
用该性质鉴别胶体和溶液。
(2)胶体的聚沉:
①聚沉方法:加热、加入电解质溶液、加入与胶粒带相反电荷的胶体。
②应用:如制作豆腐、明矾净水、江河入海口形成的沙洲等。
说明:胶体性质区别其他分散系的本质特征是分散质粒子直径为1~100 nm。
3. 胶体知识注意事项
(1)胶体微粒一般是离子、分子或难溶物的聚集体,但有些高分子化合物,如淀粉、
蛋白质,因其分子非常大,其相对分子质量通常为几万、几十万甚至上百万、千万,因此
一个分子就是一个胶体微粒,它们的溶液是胶体。
(2)区分胶体和其他分散系的最简便方法是丁达尔效应。
(3)胶体具有介稳性的主要原因是胶体粒子带有相同电荷。
(4)在Fe(OH) 胶体中,Fe(OH) 胶体粒子的数目要远远小于原FeCl 溶液中Fe3
3 3 3
+的数目。
(5)把握净水剂及其作用原理。
核心知识点一:
分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )
A. HO、HCOOH、Cu (OH)CO 均含有氧元素,都是氧化物
2 2 2 3
B. HClO、HSO (浓)、HNO 均具有氧化性,都是氧化性酸
2 4 3
第4页C. HF、CHCOOH、CHCHOH都易溶于水,都是电解质
3 3 2
D. HCOOH、HCO、HSO 分子中均含有两个氢原子,都是二元酸
2 3 2 4
【考点】本题考查物质的分类,根据物质的性质找出物质的共同点。
【解析】氧化物是指组成物质的元素只有两种,其中一种是氧元素,如 HO、CO、
2
NaO ,A中HCOOH是羧酸,Cu (OH) CO 是碱式盐,A项错;CHCHOH是非电解质,
2 2 2 2 3 3 2
C项错;HCOOH分子中只有羟基氢可以电离,属于一元酸,D项错。
【答案】B
对于化学反应:A+B=C+D,下列说法正确的是( )
A. 若A、B为酸和碱,则C、D中不一定有水
B. 若A、B为两种化合物,则C、D也一定为化合物
C. 若生成物C和D分别为两种沉淀,则A、B可能为盐和碱
D. 若生成物C、D中有一种为单质,则该反应一定是置换反应
【考点】本题考查不同物质之间的转化关系,让学生学会通过反应推测物质,和通过
物质反推可能是什么反应。
【解析】A项,酸与碱反应生成盐与HO;B项,CO与CuO反应生成Cu与CO ;D
2 2
项,CO与CuO反应生成单质Cu和CO,但不是置换反应。
2
【答案】C
在给定条件下,下列选项所示的物质间转化均能实现的是( )
A. Fe FeCl Fe(OH)
2 2
B. S SO HSO
3 2 4
C. CaCO CaO CaSiO
3 3
D. NH NO HNO
3 3
【考点】本题考查常见物质以及其所发生的反应,并判断反应是否可以发生。
【解析】A项,Fe和Cl 反应只生成FeCl 得不到FeCl ,错误;B项,S在O 中燃烧只
2 3 2 2
生成SO 得不到SO ,错误;D项,NO不和水反应,错误。
2 3
【答案】C
第5页核心知识点二:
正确的打“√”,错误的打“×”
(1)胶体的性质
①溶液是电中性的,胶体是带电的( )
②胶体与溶液都可以通过滤纸、半透膜和分子筛( )
③用激光笔照射鸡蛋清溶液,侧面可观察到明显的光路( )
(2)胶体的制备、应用及纳米材料
①浓氨水中滴加FeCl 饱和溶液可制得Fe(OH) 胶体( )
3 3
②明矾与水反应生成的Al(OH) 胶体能吸附水中悬浮物,可用于水的净化( )
3
③碳纳米管属于胶体分散系,该材料具有超强的吸附能力( )
【考点】本题通过判断考查胶体的本质特点和基本性质
【解析】(1)①胶体不带电,胶粒带电荷
②胶体不能通过半透膜
③鸡蛋清是胶体,可以发生丁达尔效应
(2)①浓氨水中滴加FeCl 饱和溶液可制得Fe(OH) 沉淀
3 3
②Al(OH) 胶体能吸附水中悬浮物
3
③碳纳米管不属于胶体
【答案】(1)①× ②× ③√(2)①× ②√ ③×
磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性。制备时将等
物质的量的FeSO 和Fe (SO ) 的溶液混合,滴入稍过量的氢氧化钠溶液,随后加入油酸
4 2 4 3
钠溶液,即可生成黑色的分散质粒子直径为5.5~36 nm 的磁流体。下列说法中正确的是(
)
A. 所得的分散系属于溶液
B. 所得的分散系中分散质为Fe O
2 3
C. 当一束强可见光通过该分散系时会出现光亮的“通路”
D. 该分散系很不稳定
【考点】本题考查胶体的性质
【解析】解题的关键是抓住胶体区别于其他分散系的本质特征:分散质粒子直径在1
~100 nm,丁达尔效应是胶体特有的现象。由题可知该磁流体分散质粒子直径是5.5~36
nm,则该磁流体属于胶体,A不正确;胶体具 有一定的稳定性,D不正确;具有磁性的铁
的化合物是Fe O。
3 4
【答案】C
第6页下列现象或新技术应用中,不涉及胶体性质的是( )
A. 在饱和氯化铁溶液中逐滴加NaOH溶液,产生红褐色沉淀
B. 使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
C. 清晨,在茂密的树林中,常常可以看到从枝叶间透过的一道道光柱
D. 肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
【考点】本题考查胶体的性质及胶体在日常生活中的应用。
【解析】制取氢氧化铁胶体的方法是在沸水中滴入饱和的氯化铁溶液,得到红褐色氢
氧化铁胶体,在饱和氯化铁溶液中逐滴加NaOH溶液,产生的氢氧化铁粒子的聚集体已大
于100nm,形成的是悬浊液;血液是胶体,通过微波可以使胶体凝聚;树林中的水雾是气
溶胶,也具有丁达尔效应;血液透析是利用渗析原理,让血液中的毒素通过半透膜而除去。
【答案】A
1. 交叉分类法与树状分类法的区别
交叉分类法是对同一物质以不同的分类标准或角度进行分类;树状分类法是对同类物
质按不同的属性进行逐级分类,各级之间为从属关系,同级之间为并列关系。
2. 酸、碱、盐的理解
(1)溶于水能电离出H+的化合物不一定是酸,如NaHSO;溶于水能电离出OH-的
4
化合物不一定是碱;如Mg(OH)Cl;盐的构成中不一定仅有金属阳离子和酸根阴离子,
如NH Cl,非金属元素可形成阳离子NH;酸根离子中不一定只有非金属元素,如MnO。
4
(2)酸分子中有几个H原子,不一定就是几元酸,如CHCOOH是一元酸。
3
3. 单质、纯净物和混合物
由同种元素组成的物质不一定是单质,也可能属于混合物,如O 和O 的混合气体是
2 3
混合物;只有由同一种元素组成的纯净物才属于单质。
4. 胶体
(1)胶体区别其他分散系的本质特征是分散质颗粒直径大小(1~100 nm)。
(2)胶体的物理性质:①丁达尔效应;②电泳现象;③介稳性;④布朗运动;⑤胶体
粒子不能透过半透膜,但能透过滤纸。
胶体粒子的直径一般在1~100 nm之间,它决定了胶体粒子具有较大的表面积,吸附
力很强,能在水中吸附悬浮固体或色素形成沉淀,从而达到净化水的目的,这就是胶体净
水的原理。能在水中自然形成胶体,并且对水质无明显副作用的物质有 KAl(SO )
4
第7页·12H O、FeCl ·6H O等,这样的物质被称为净水剂,其形成胶体的化学原理是Al3+、Fe3+
2 2 3 2
发生水解反应生成Al(OH) 胶体、Fe(OH) 胶体。
3 3
5. 溶液、胶体、浊液三类分散系的比较
浊液
分散系 溶液 胶体
悬浊液 乳浊液
分散质粒子
<1 nm 1~100 nm >100 nm >100 nm
直径大小
分散质粒子 少量分子的集 大量分子聚集成 大量分子聚集成的
分子、离子
结构 合体或大分子 的固体小颗粒 液体小液滴
多数均一、透 不 均 一 、 不 透 不均一、不透明,
特点 均一、透明
明,较稳定 明,久置沉淀 久置分层
稳定性 稳定 介稳性 不稳定 不稳定
能否透过滤
能 能 不能 不能
纸
能否透过半
能 不能 不能 不能
透膜
食盐水、蔗 Fe(OH) 胶
3
实例 糖溶液 体、淀粉溶液 泥水、石灰乳 牛奶
(答题时间:25分钟)
1. 符合如图中阴影部分的物质是( )
A. NaHCO B. Cu (OH)CO C. NaCl D. Na CO
3 2 2 3 2 3
2. 《神农本草经》说:“水银……熔化(加热)还复为丹。”《黄帝九鼎神丹经》中的
“柔丹”、“伏丹”都是在土釜中加热Hg制得的。这里的“丹”是指( )
A. 氯化物 B. 合金 C. 硫化物 D. 氧化物
3. 下列物质间的转化能一步实现的是( )
A. Na CO NaOH
2 3
B. CaCO Ca(OH)
3 2
C. NaNO NaCl
3
D. FeSO CuSO
4 4
4. 汽车尾气是造成大气污染的主要原因之一,在汽车排气管上安装“催化转换器”使汽
车的尾气转换成无毒气体是目前最有效的手段之一。如果用 表示碳原子,用○表示氧原
子,用 表示氮原子,如图为气体转化的微观过程。请你根据图示回答下列问题:
第8页(1)A、B、C三种物质可以归为一类的依据是____________________________。
(2)将C归为化合物,将D归为单质的理由是_____________________________。
(3)用化学反应方程式表示为________________________________________。化学变
化过程中消耗的A物质和生成的C物质的质量比为________。
(4)从微观的角度去描述你获得的关于化学变化的有关信息(答出一条即可)
________________________________________________________________。
5. 下列说法中正确的是( )
A. 胶体区别于其他分散系的本质特征是具有丁达尔效应
B. 利用半透膜可除去淀粉溶液中的少量NaCl
C. 溶液是电中性的,胶体是带电的
D. 纳米材料粒子直径一般在10-9~10-7m之间,因此纳米材料属于胶体
6. 下列关于胶体的叙述中不正确的是( )
A. 用肉眼就可以把胶体和溶液、浊液区别开来
B. 向Fe(OH) 胶体中加入少量HSO 溶液,会生成红褐色沉淀
3 2 4
C. 可利用丁达尔效应区分胶体与溶液
D. 胶体微粒具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳
现象
7. 下列事实与胶体性质无关的是( )
A. 在豆浆里加入盐卤做豆腐
B. 在河流入海处易形成沙洲
C. 一束平行光线照射蛋白质溶液时,从侧面可以看到一束光亮的通路
D. 三氯化铁溶液中滴入氢氧化钠溶液时,出现红褐色沉淀
8. 在如图所示的有关物质转化关系中,各物质均是我们中学化学所学的物质。C为一种
黑色粉末,D为一种气体。
请根据框图中物质的转化关系及相关信息,用化学式填写下列空白:
(1)若 F 为可溶性碱,G 为蓝色沉淀,则 A 为______________,D 可能为
______________。
第9页(2)若G为蓝色沉淀,H为难溶性盐,则I为______________。
(3)若G、H都属于盐,且G为蓝色溶液,则I可能为___________________,F可能
为____________。
第10页1. D
2.【答案】D
【解析】在土釜中加热Hg,金属汞可以和氧气发生反应得到氧化汞,氧化汞属于物质
分类中的氧化物。
3. 【解析】 NaCO 与Ba(OH)、Ca(OH) 等反应可一步生成NaOH。
2 3 2 2
【答案】A
4. 【解析】(1)根据图示可知A、B、C、D分别是NO、CO、CO 和N ,NO、CO、
2 2
CO 都属于氧化物,都含有氧元素。(2)二氧化碳是由不同种元素组成的分子,属于化合
2
物,而氮气是由同种元素组成的分子,属于单质。(3)根据图示直接写出化学方程式即可。
(4)根据质量守恒定律,在化学变化过程中原子的种类、数目、质量没有发生改变,元素
的种类和质量也没有发生改变,只有物质的种类和分子的种类发生了改变。
【答案】(1)都由两种元素组成且都含有氧元素
(2)二氧化碳是由不同种元素组成的分子,而氮气是由同种元素组成的分子
(3)2CO+2NO N+2CO 15∶22
2 2
(4)化学变化中原子的种类、数目、质量没有发生改变(其他合理答案也可)
5. 【解析】胶体与其他分散系的本质区别是分散质粒子的直径大小,丁达尔效应是胶体
的一种性质,A项错误;半透膜能允许直径在1 nm以下的小分子或离子透过,1 nm以上的
胶体粒子不透过,因此可以用半透膜除去淀粉溶液中的NaCl,B项正确;胶体中的胶粒带
正电荷,但整个胶体不带电,呈电中性,C项错误;胶体是分散系,属于混合物,直径在1
~100 nm之间的纳米材料不一定是分散系,若是纯净物,则不属于胶体,D项错误。
【答案】B
6. 【解析】肉眼不能区分胶体和溶液,A错误;HSO 是电解质,向Fe(OH) 胶体中
2 4 3
加少量HSO 溶液,胶体发生了聚沉,生成红褐色沉淀,B正确;胶体会产生明显的丁达
2 4
尔效应,据此可区分胶体与溶液,C正确;胶粒能吸附阳离子或阴离子而带有电荷,能在
电场作用下产生电泳现象,D正确。
【答案】A
7. 【解析】豆浆里的蛋白质是胶体,遇电解质(盐卤)发生聚沉;河流中土壤胶粒遇海
水中的电解质发生聚沉;蛋白质胶体能发生丁达尔效应;氯化铁溶液与氢氧化钠溶液的反
应为FeCl +3NaOH=Fe(OH)↓+3NaCl。
3 3
【答案】D
8. 【解析】由题中框图关系可知,黑色粉末与一种气体在加热条件下反应生成A、B两
种物质,应为氧化铜被还原。因为D点燃可生成B,若D为氢气,B为水,若D为CO,B
第11页为CO ,C为CuO,A为Cu。因CuO可与酸反应,所以I为酸,E为铜盐,当G为蓝色沉
2
淀Cu(OH) 时,F应为可溶性碱,H为盐。因H为难溶性盐,则F为Ba(OH) ,H为
2 2
BaSO ,I为HSO 。若G、H都属于盐,且G为蓝色溶液,则根据复分解反应的规律H为
4 2 4
难溶性盐,若I为HCl,则E为CuCl ,F为AgNO ,G为Cu(NO ) ,H为AgCl;若I为
2 3 3 2
HSO ,则E为CuSO ,F为BaCl ,G为CuCl ,H为BaSO。
2 4 4 2 2 4
【答案】(1)Cu H 或CO (2)HSO (3)HCl或HSO AgNO 或BaCl
2 2 4 2 4 3 2
第12页