文档内容
化学反应速率的计算与比较同步练习
(答题时间:40分钟)
一、选择题
1. 下列关于化学反应速率的说法中,正确的是( )
A. 化学反应速率是指某一时刻、某种反应物的瞬时反应速率
B. 化学反应速率为0. 8 mol·L-1·s-1是指反应1 s时某物质的浓度为0. 8 mol·L-1
C. 根据化学反应速率的大小可以推知化学反应的快慢
D. 对于一个化学反应来说,其反应速率越大,反应现象就越明显
2. 将4 mol A气体和2 mol B气体在2 L密闭的容器中混合,并在一定条件下发生反应:
2A(g)+B(g)=xC(g),若经2 s后测得A物质的量为2. 8 mol,C的浓度为0. 6
mol·L-1,下列几种说法,正确的是( )
①2 s内用物质A表示的平均反应速率为0. 3 mol·L-1·s-1 ②2 s内用物质B表示的平
均反应速率为0. 6 mol·L-1·s-1 ③2 s时物质B的转化率为70%
④x=2
A. ①③ B. ①④
C. ②③ D. ③④
3. 在某恒容密闭容器中投入X、Y、W、Q四种物质,经一段时间后测得各物质的物质
的量如下表所示:
X Y W Q
10 min 1. 0 mol 3. 0 mol 1. 0 mol 2. 0 mol
20 min 0. 5 mol 1. 5 mol 2. 0 mol 1. 0 mol
上述容器中发生的化学反应方程式可能是( )
A. X+2Y=2W+2Q B. 3X+Y+2W=2Q
C. X+3Y+2Q=2W D. X+2Y+3Q=2W
4. 在N+3H 2NH 的反应中,经过一段时间后,NH 的浓度增加0. 6mol/L,在此时
2 2 3 3
间内用H 表示的平均反应速率为0. 45mol/(L·s),则所经历的时间是( )
2
A. 0. 44秒 B. 1秒 C. 1. 33秒 D. 2秒
5. 将6 mol CO 和8 mol H 充入一容积为2 L的密闭容器中(温度保持不变)发生反应
2 2
CO (g)+3H (g) CHOH(g)+HO(g) ΔH<0。测得H 的物质的量随时间
2 2 3 2 2
变化如图所示(图中字母后的数字表示对应的坐标)。该反应在8~10 min内CO 的平均
2
反应速率是( )
第1页A. 0. 5 mol·L-1·min-1 B. 0. 1 mol·L-1·min-1
C. 0 mol·L-1·min-1 D. 0. 125 mol·L-1·min-1
6. 将等物质的量的A、B混合放于2 L的密闭容器中,发生反应3A(g)+B(g)
xC(g)+2D(g)。经5 min后测得D的浓度为0. 5 mol·L-1,c(A)∶c(B)
=3∶5,v(C)=0. 1 mol·L-1·min-1。
则:(1)x=________。
(2)前5 min内B的反应速率v(B)=________。
(3)5 min时A的转化率为________。
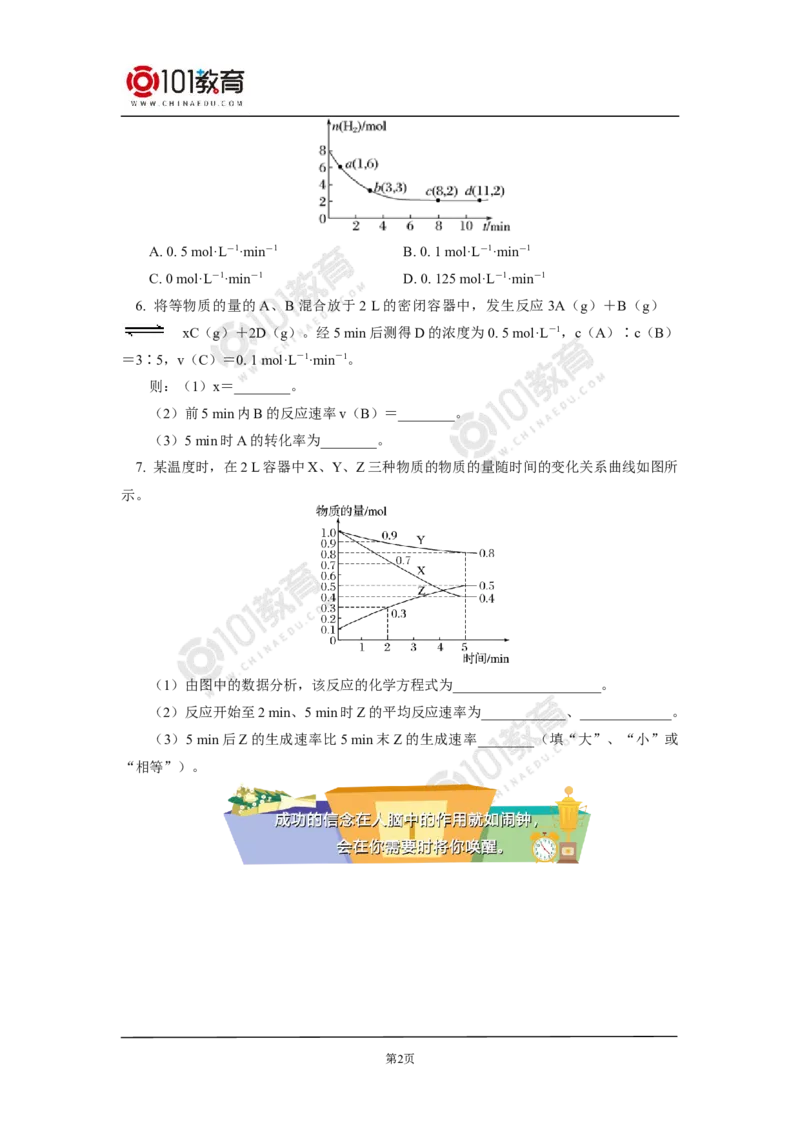
7. 某温度时,在2 L容器中X、Y、Z三种物质的物质的量随时间的变化关系曲线如图所
示。
(1)由图中的数据分析,该反应的化学方程式为_____________________。
(2)反应开始至2 min、5 min时Z的平均反应速率为____________、_____________。
(3)5 min后Z的生成速率比5 min末Z的生成速率________(填“大”、“小”或
“相等”)。
第2页化学反应速率的计算与比较同步练习参考答案
1. 【答案】C
【解析】A项中,化学反应速率是指一段时间内某种反应物或生成物的平均反应速率;
B项中0. 8 mol·L-1·s-1不是指反应1 s时某物质的浓度为0. 8 mol·L-1,而是指1 s内该物质
的浓度变化量为0. 8 mol·L-1;D项中反应速率与反应现象无必然联系。
2. 【答案】B
4mol−2.8mol
【解析】由题干信息计算出v(A)=
2L×2s
=0. 3 mol·L-1·s-1,则v(B)
=0. 15 mol·L-1·s-1;2 s时A消耗1. 2 mol,则B消耗0. 6 mol,所以B的转化率为30%;2
0.6mol⋅L−1
2s
s时生成物C的浓度为0. 6 mol·L-1,所以v(C)= =0. 3 mol·L-1·s-1,v
(A)∶v(C)=2∶x=1∶1,得x=2,故①④正确。
3. 【答案】C
【解析】从表格数据可看出X、Y、Q的物质的量减少,而W的物质的量增加,说明
X、Y、Q是反应物,W是产物。在同一容器中,相同时间内,各物质的速率之比等于物质
的量变化量之比,等于化学计量数之比。n(X)∶n(Y)∶n(Q)∶n(W)=(1. 0 mol
-0. 5 mol)∶(3. 0 mol-1. 5 mol)∶(2. 0 mol-1. 0 mol)∶(2. 0 mol-1. 0 mol)=
1∶3∶2∶2,所以X、Y、Q、W的计量数之比为1∶3∶2∶2,选C。
4. 【答案】D
【解析】经过一段时间后,c(H)=3/2c(NH )= 0. 9mol/L,由v=Δc/Δt可得,
2 3
Δt=Δc/v=0. 9mol/L÷0. 45mol/(L·s)=2s,选D。
5. 【答案】C
【解析】由图可知,在 8~10 min内,H 的物质的量都是 2 mol,因此v(H )=
2 2
2mol−2mol
2L×2min
=0 mol·L-1·min-1,根据化学反应速率之比等于化学计量数之比,v(CO )
2
1
3
= v(H)=0 mol·L-1·min-1,故C项正确。
2
6. 【答案】(1)2 (2)0. 05 mol·L-1·min-1 (3)50%
0.5mol⋅L−1
5min
【解析】(1)v(D)= =0. 1 mol·L-1·min-1=v(C),由此推知x=
2。
v(C) 0.1mol⋅L−1 ⋅min−1
(2)v(B)= 2 = 2 =0. 05 mol·L-1·min-1。
(3)设起始A、B的浓度均为a mol·L-1
3A(g) + B(g) 2C(g)+2D(g)
第3页起始浓度/mol·L-1 a a 0 0
转化浓度/mol·L-1 0. 75 0. 25 0. 5 0. 5
5min浓度/mol·L-1 a-0. 75 a-0. 25 0. 5 0. 5
(a-0. 75)∶(a-0. 25)=3∶5 解得:a=1. 5
0.75mol⋅L−1
所以A的转化率为αA=
1.5mol⋅L−1
×100%=50%。
7.【答案】(1)3X+Y 2Z
(2)0. 05 mol·L-1·min-1 0. 04 mol·L-1·min-1
(3)相等
【解析】(1)根据图示,X减少了0. 6 mol,Y减少了0. 2 mol,Z生成了0. 4 mol,
故X、Y、Z的物质的量变化之比为3∶1∶2,因5 min后三者共存,故反应的方程式为3X
+Y 2Z。
(2)根据图中数据,依据反应速率计算公式可计算出反应速率,需注意Z的初始物质
的量是0. 1 mol。
(3)5 min后Z的物质的量不再变化,反应速率相等。
第4页有效碰撞理论与活化能同步练习
(答题时间:40分钟)
一、选择题
1. 能增加反应物分子中活化分子的百分数的是( )
A. 降低温度 B. 使用催化剂
C. 增大压强 D. 增加浓度
2. 下列说法不正确的是( )
A. 只有当碰撞的分子具有足够的能量和适当的取向时,才能发生化学变化
B. 能发生有效碰撞的分子必须具有足够高的能量
C. 无论是吸热反应还是放热反应,升高温度都能增大活化分子百分数
D. 活化分子间的碰撞一定是有效碰撞
3. 下列说法不正确的是( )
A. 反应物分子(或离子)间的每次碰撞是反应的先决条件
B. 反应物的分子的每次碰撞都能发生化学反应
C. 活化分子具有比普通分子更高的能量
D. 活化能是活化分子的平均能量与普通反应物分子平均能量之差,如图所示正反应的
活化能为E-E
1
4. 一定条件下的可逆反应:2SO
2
(g)+O
2
(g) ⇌2SO
3
(g),若改变下列条件,可提高
反应物中的活化分子百分数的是( )
A. 升高温度 B. 降低温度
C. 增大压强 D. 增大反应物浓度
5. 下列关于碰撞理论的基本观点,描述不正确的选项是( )
A. 反应物分子之间发生相互碰撞是发生化学反应的必要条件
B. 活化分子是指具有较高能量,能够发生有效碰撞的分子
C. 活化分子之间的碰撞一定是有效碰撞
D. 发生有效碰撞的条件是分子具有较高能量并且有合适的碰撞取向
6. 在密闭容器中发生反应mA(g)+nB(g)=wC(g),同一时间段内测得:A的浓
度每分钟减少0. 15 mol·L-1,B的浓度每分钟减少0. 05 mol·L-1,C的浓度每分钟增加0. 1
mol·L-1。则下列叙述正确的是( )
第5页A. 在容器容积和温度不变的条件下,随着反应的进行,体系的压强逐渐增大
B. 化学计量数之比是m∶n∶w=3∶1∶2
C. 单位时间内反应物浓度的减少等于生成物浓度的增加
D. 若在前10 s内A减少了x mol,则在前20 s内A减少了2x mol
7. 下列说法正确的是( )
A. 升高温度和加入催化剂都可以改变反应所需的活化能,增大化学反应速率
B. 有效碰撞是指反应物活化分子间的碰撞
C. 增大压强,可以使单位体积内气体的活化分子数增多,有效碰撞几率增大
D. 焓就是指反应热
8. 一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线
如图所示。下列描述正确的是( )
A. 反应开始到10 s,用Z表示的反应速率为0. 158 mol·L-1·s-1
B. 反应开始到10 s,X的物质的量浓度减少了0. 79 mol·L-1
C. 反应开始到10 s时,Y的转化率为79. 0%
D. 反应的化学方程式为X(g)+Y(g) Z(g)
9. 下列说法中正确的说法有几个
①活化分子间的碰撞一定能发生化学反应
②普通分子间的碰撞有时也能发生化学反应
③增大反应物浓度,可增大活化分子百分数,从而使有效碰撞次数增多
④有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子
的百分数,从而使反应速率增大
⑤化学反应的实质是旧化学键断裂和新化学键形成的过程
⑥催化剂能增大活化分子百分数,从而成千成万倍地增大化学反应速率
A. 1个 B. 2个 C. 3个 D. 4个
二、非选择题
10. CH -CO 催化重整不仅可以得到合成气(CO和H ),还对温室气体的减排具有重要
4 2 2
意义。回答下列问题:
(1)CH-CO 催化重整反应为:CH (g)+CO (g)=2CO(g)+2H (g)。
4 2 4 2 2
第6页已知:C(s)+2H (g)=CH(g) ΔH=-75 kJ·mol-1
2 4
C(s)+O (g)=CO(g) ΔH=-394 kJ·mol-1
2 2
C(s)+ O(g)=CO(g) ΔH=-111 kJ·mol-1
2
该催化重整反应的ΔH = kJ·mol-1。有利于提高CH 平衡转化率的条件是
4
_______(填标号)。
A. 高温低压 B. 低温高压 C. 高温高压 D. 低温低压
第7页有效碰撞理论与活化能同步练习参考答案
1.【答案】B
【解析】A. 降低温度减小反应物分子中活化分子的百分数,故A错误;B. 使用催化
剂可增大反应物中的活化分子百分数,故B正确;C. 增大压强可使活化分子的浓度增大,
但百分数不变,故C错误;D. 增加浓度可使活化分子的浓度增大,但百分数不变,故D
错误;故答案为B。
2.【答案】D
【解析】A. 当碰撞的分子具有足够的能量时才能成为活化分子,且适当的取向时发生
有效碰撞,可发生化学反应,故A正确;B. 能发生有效碰撞的分子必须为活化分子,需要
具有足够高的能量,故B正确;C. 升高温度,分子的能量增大,增大活化分子百分数,故
C正确;D. 活化分子发生碰撞时,只有适当的取向时,才能发生有效碰撞,故D错误
3.【答案】B
【解析】只有活化分子发生有效碰撞才能发生化学反应,因此B项错误;A、C、D三
项均正确。
4.【答案】A
【解析】升高温度可提高反应物中的活化分子百分数,降低温度降低反应物中的活化
分子百分数,增大压强、增大反应物浓度只增大活化分子的浓度,不改变活化分子百分数
故答案为A。
5.【答案】C
【解析】A. 反应物分子之间发生有效碰撞才会发生化学反应,反应物分子之间发生相
互碰撞是发生化学反应的必要条件,故A正确;B. 活化分子是指具有较高能量,能够发生
有效碰撞的分子,是普通分子吸收能量后的结果,故B正确;C. 活化分子之间的碰撞不一
定是有效碰撞,只有当活化分子有合适取向时的碰撞才是有效碰撞,故C错误;D. 分子具
有较高能量并且有合适的碰撞取向时才能发生有效碰撞,即分子具有较高能量并且有合适
的碰撞取向是分子发生有效碰撞的条件,故D正确。
6.【答案】B
【解析】由题意知,v(A)∶v(B)∶v(C)=3∶1∶2。根据化学反应中各物质的
反应速率之比等于化学方程式中相应物质的化学计量数之比可知,m∶n∶w=3∶1∶2,
A、C项均错误,B项正确。反应过程中,反应都不是等速率进行的,前10 s与前20 s内反
应速率不同,D项错误。
7.【答案】C
【解析】A. 升高温度不能改变反应所需的活化能,但可以提高活化分子的百分数,加
快反应速率,故A错误;B. 反应物活化分子之间有合适取向的碰撞才可能发生化学反应,
第8页而能发生化学反应的碰撞就是有效碰撞,故B错误;C. 增大压强,气体的体积减小,增大
活化分子的浓度,有效碰撞几率增大,反应速率增大,故C正确;D. 焓不是反应热,体系
的等压反应热就等于焓变,故D错误
8.【答案】C
【解析】由图像中数据计算用不同物质的浓度变化表示的化学反应速率之比,也就是
化学计量数之比,然后即可推出化学方程式。由图像可知:X、Y的物质的量逐渐减少,
为反应物,Z的物质的量逐渐增多,为生成物。10 s内它们的物质的量变化分别为X:(1.
20-0. 41)mol=0. 79 mol;Y:(1. 00-0. 21)mol=0. 79 mol;Z:(1. 58-0)mol=1.
58 mol。故反应化学方程式为X+Y 2Z,D项错;
Δc(Z) Δn(Z) 1.58mol
= =
A项:v(Z)= Δt V⋅Δt 2L×10s =0. 079 mol·L-1·s-1;B项:Δc(X)=
Δn(X) 0.79mol 0.79mol
V = 2L =0. 395 mol·L-1;C项,Y的转化率= 1.00mol ×100%=79. 0%。
9.【答案】B
【解析】①活化分子的碰撞有一定的合适取向,故错误;②普通分子间的碰撞没有发
生化学反应,因为发生有效碰撞是活化分子,具有一定的能量,故错误;③增大反应物浓
度,增大单位体积内活化分子的个数,从而使有效碰撞次数增多,故错误;④有气体参加
的化学反应,增大压强,增大单位体积内活化分子的个数,从而使反应速率增大,故错误;
⑤化学反应的实质是旧键的断裂和新键的生成,故正确;⑥催化剂降低活化能,增大活化
分子百分数,从而增大化学反应速率,故正确。
10.【答案】(1)247 A
【解析】(1)C(s)+2H (g)=CH(g) ΔH=-75 kJ·mol-1 ①
2 4
C(s)+O (g)=CO(g) ΔH=-394 kJ·mol-1 ②
2 2
C(s)+ O(g)=CO(g) ΔH=-111 kJ·mol-1 ③
2
运用盖斯定律,③×2-①-②可得CH (g)+CO (g)=2CO(g)+2H (g) ΔH=
4 2 2
[(-111×2)-(-75)-(-394)] kJ·mol-1=247 kJ·mol-1。正反应为气体体积增大的吸热反应,
故升温、减压有利于平衡正向移动,提高CH 的平衡转化率,A正确。
4
第9页