文档内容
第二章 分子结构与性质
第二节 分子的空间结构
第二课时 杂化轨道理论简介
【学习目标】1. 理解杂化轨道理论的主要内容。
2. 能用杂化轨道理论解释或预测某些分子或离子空间结构。
【学习重点】应用杂化轨道理论解释分子的空间结构。
【学习难点】用杂化轨道理论解释含有孤电子对的分子的空间结构。
【课前预习】
旧知回顾:
1、书写C和H的 电子排布式和轨道表示式?
H:1s1 C:1s22s22p2
2、CH 的电子式、结构式和空间构型?
4
正四面体形
3、价层电子对的计算公式?
1
(a−xb)
2
价层电子对数=σ键电子对数+
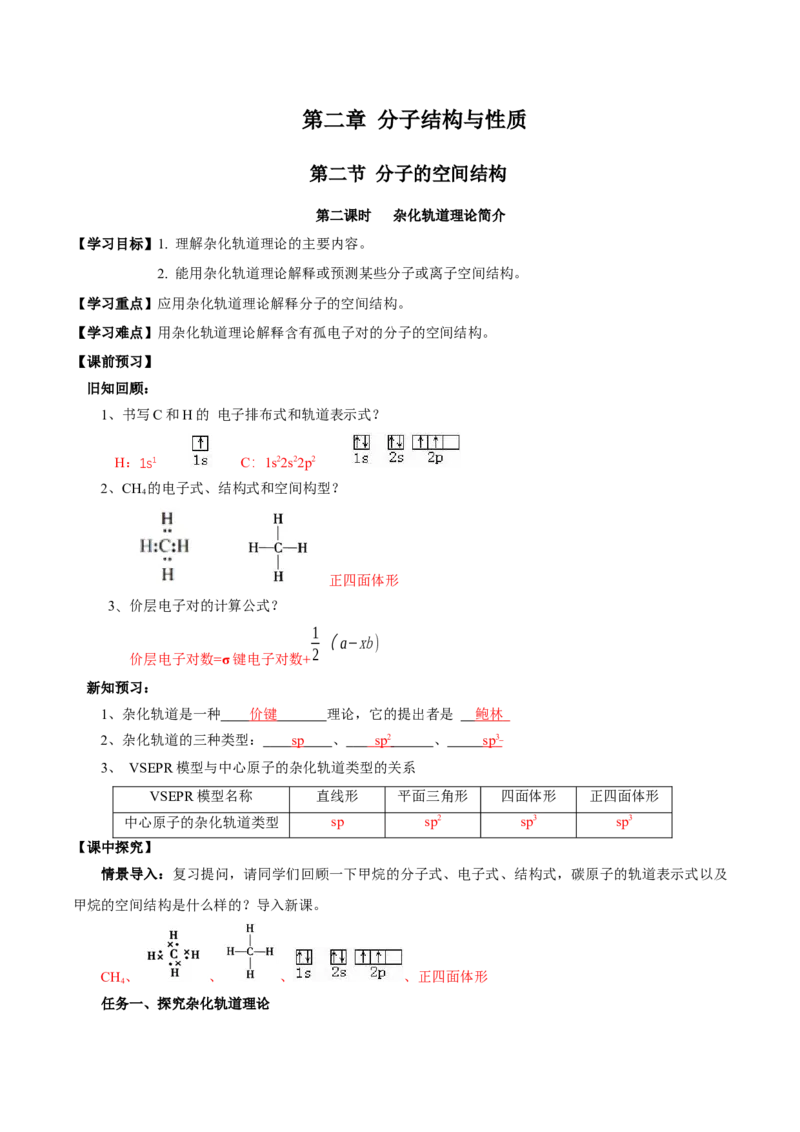
新知预习:
1、杂化轨道是一种 价键 理论,它的提出者是 鲍林
2、杂化轨道的三种类型: s p 、 s p 2 、 s p 3
3、 VSEPR模型与中心原子的杂化轨道类型的关系
VSEPR模型名称 直线形 平面三角形 四面体形 正四面体形
中心原子的杂化轨道类型 sp sp2 sp3 sp3
【课中探究】
情景导入:复习提问,请同学们回顾一下甲烷的分子式、电子式、结构式,碳原子的轨道表示式以及
甲烷的空间结构是什么样的?导入新课。
CH、 、 、 、正四面体形
4
任务一、探究杂化轨道理论【学生活动】阅读教材P 第2、3、4、5自然段和P 图2-15和图2-16,小组合作,回答下列问题:
47 48
1、杂化轨道类型
类型 形成过程 夹角 空间结构
sp3 sp3杂化轨道是由1个s轨道和3个p轨道杂化形成的 109°28′ 正四面体形
sp2 sp2杂化轨道是由1个s轨道和2个p轨道杂化而成的 120° 平面三角形
sp sp杂化轨道是由1个s轨道和1个p轨道杂化而成的 180° 直线形
2、原子轨道发生sp、sp2杂化时,还有未参与杂化的p轨道,可用于形成 π 键,而杂化轨道用于
形成 σ 键或用来容纳 未参与成键的孤电子对 。
任务二、探究杂化轨道类型与分子的空间结构的关系
【学生活动】阅读教材P 自然段和P 表2-5,补充下列表格:
48 49
VSEPR模型 直线形 平面三角形 四面体形
中心原子的杂 sp sp2 sp3
化轨道类型
任务三、探究杂化轨道类型的判断方法
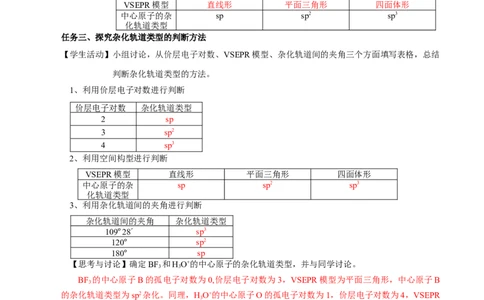
【学生活动】小组讨论,从价层电子对数、VSEPR模型、杂化轨道间的夹角三个方面填写表格,总结
判断杂化轨道类型的方法。
1、利用价层电子对数进行判断
价层电子对数 杂化轨道类型
2 sp
3 sp2
4 sp3
2、利用空间构型进行判断
VSEPR模型 直线形 平面三角形 四面体形
中心原子的杂 sp sp2 sp3
化轨道类型
3、利用杂化轨道间的夹角进行判断
杂化轨道间的夹角 杂化轨道类型
109º28´ sp3
120º sp2
180º sp
【思考与讨论】确定BF 和HO+的中心原子的杂化轨道类型,并与同学讨论。
3 3
BF 的中心原子B的孤电子对数为0,价层电子对数为3,VSEPR模型为平面三角形,中心原子B
3
的杂化轨道类型为sp2杂化。同理,HO+的中心原子O的孤电子对数为1,价层电子对数为4,VSEPR
3
模型为四面体形,中心原子O的杂化轨道类型为sp3杂化。
【对应训练1】下列关于杂化轨道的说法错误的是( )
A.并不是所有的原子轨道都参与杂化
B.同一原子中能量相近的原子轨道参与杂化
C.杂化轨道能量集中,有利于牢固成键
D.杂化轨道数与杂化前后轨道数不相同
【答案】D【解析】杂化轨道数与杂化前后轨道数相同,D错误。
【对应训练2】杂化轨道理论是鲍林为了解释分子的空间结构提出的。下列关于 sp、sp2、sp3杂化轨
道的夹角的比较正确的是( )
A.sp杂化轨道的夹角最大 B.sp2杂化轨道的夹角最大
C.sp3杂化轨道的夹角最大 D.sp、sp2、sp3杂化轨道的夹角相等
【答案】A
【解析】sp3、sp2、sp杂化轨道的夹角分别为109°28´、120°、180°,故A项正确。
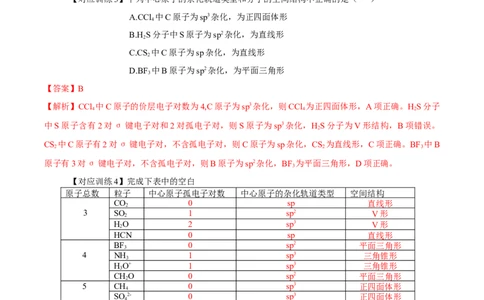
【对应训练3】下列中心原子的杂化轨道类型和分子的空间结构不正确的是( )
A.CCl 中C原子为sp3杂化,为正四面体形
4
B.H S分子中S原子为sp2杂化,为直线形
2
C.CS 中C原子为sp杂化,为直线形
2
D.BF 中B原子为sp2杂化,为平面三角形
3
【答案】B
【解析】CCl 中C原子的价层电子对数为4,C原子为sp3杂化,则CCl 为正四面体形,A项正确。HS分子
4 4 2
中S原子含有2对σ键电子对和2对孤电子对,则S原子为sp3杂化,HS分子为V形结构,B项错误。
2
CS 中C原子有2对σ键电子对,不含孤电子对,则C原子为sp杂化,CS 为直线形,C项正确。BF 中B
2 2 3
原子有3对σ键电子对,不含孤电子对,则B原子为sp2杂化,BF 为平面三角形,D项正确。
3
【对应训练4】完成下表中的空白
原子总数 粒子 中心原子孤电子对数 中心原子的杂化轨道类型 空间结构
CO 0 sp 直线形
2
3 SO 1 sp2 V形
2
HO 2 sp3 V形
2
HCN 0 sp 直线形
BF 0 sp2 平面三角形
3
4 NH 1 sp3 三角锥形
3
HO+ 1 sp3 三角锥形
3
CHO 0 sp2 平面三角形
2
5 CH 0 sp3 正四面体形
4
SO 2- 0 sp3 正四面体形
4
【解析】CO 的价层电子对数=2+1/2(4-2×2)=0,孤电子对数为0,所以杂化轨道类型是sp杂化。空间结构
2
为直线形;SO 的价层电子对数=2+1/2(6-2×2)=3,孤电子对数为1,所以杂化轨道类型是sp2杂化,空间结
2
构为V形;HO的价层电子对数=2+1/2(6-2×1)=4,孤电子对数为2,所以杂化轨道类型是sp3杂化,空间结
2
构为V形;HCN的结构式为H-C≡N,碳的孤电子对数为0,有2对σ键电子对,所以杂化轨道类型是sp
杂化,空间结构为直线形;BF 的价层电子对数=3+1/2(3-3×1)=3,孤电子对数为0,所以杂化轨道类型是
3
sp2杂化,空间结构为平面三角形;NH 的价层电子对数=3+1/2(5-3×1)=4,孤电子对数为1,所以杂化轨道
3
类型是sp3杂化,空间结构为三角锥形;HO+的价层电子对数=3+1/2(6-1-3×1)=4,孤电子对数为1,所以杂
3化轨道类型是sp3杂化,空间结构为三角锥形;CHO的结构式为
2
,碳的孤电子对数为0,有3对σ键电子对,所以杂化轨道类型是sp2杂化,空间结构为平面三
角形;CH 的价层电子对数=4+1/2(4-1×4)=0,孤电子对数为0,所以杂化轨道类型是sp3杂化,空间结构为
4
正四面体形;SO 2-的价层电子对数=4+1/2(6+2-2×4)=0,孤电子对数为0,所以杂化轨道类型是sp3杂化,空
4
间结构为正四面体形。
【课后巩固】1.(易)下列说法中,正确的是( )
A.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对
B.凡是中心原子采取sp3杂化的分子,其空间结构都是正四面体形
C.凡是AB 型的共价化合物,其中心原子A均采用sp3杂化轨道成键
3
D.SCl 属于AB 型共价化合物,中心原子S采取sp3杂化轨道成键
2 2
【答案】A
【解析】中心原子采取sp3杂化的分子,若中心价层电子不含孤电子对,空间结构是正四面体形,若含1对
孤电子对,则为三角锥形,若含2对孤电子对,则为V形,B错误;AB 型的共价化合物,若A原子最外
3
层含有1对孤电子对,则A原子采取sp3杂化,若A原子最外层不含孤电子对,则A原子采取sp2杂化,C
错误;SCl 中S原子形成2个σ健,且含2对孤电子对,则S原子采取sp3杂化,D错误。
2
2.(易)下列分子中的中心原子是sp2杂化的是( )
A.NH B.CH C.BF D.HO
3 4 3 2
【答案】C
【解析】根据杂化轨道的数目判断中心原子杂化方式:杂化轨道数目=σ键数+弧电子对数。NH 中N原子
3
形成3个σ键且含1对孤电子对,则N原子采取sp3杂化,A错误;CH 中C原子形成4个σ键,不含孤电
4
子对,则C原子采取sp3杂化,B错误;BF 中B原子形成3个σ键,不含孤电子对,则B原子采取sp2杂
3
化,C正确;HO分子中O原子形成2个σ键且含2对孤电子对,则O原子采取sp3杂化,D错误。
2
3.(易)关于CO 和SO 的说法中,正确的是( )
2 2
A.C和S上都没有孤电子对
B.C和S都是sp3杂化
C.都是AB 型,所以空间结构都是直线形
2
D.CO 的空间结构是直线形,SO 的空间结构是V形
2 2
【答案】D
【解析】CO 中C原子的孤电子对数为1/2(4-2×2)=0, SO 中S原子的孤电子对数为1/2(6-2×2)=1,A错误:
2 2C原子采取sp2杂化,S原子采取sp3杂化,B错误; CO 是直线形,SO 是V形,C错误,D正确。
2 2
4.(易)下列有关sp2杂化轨道的说法错误的是( )
A.由同一能层上的s轨道与p轨道杂化而成
B.所形成的3个sp2杂化轨道的能量相同
C.每个sp2杂化轨道中s能级成分占三分之一
D.sp2杂化轨道最多可形成2个σ键
【答案】D
【解折】同一能层上的s轨道与p轨道的能量差异不大,sp2杂化轨道是由同一能层上的s轨道与p轨道杂
化而成的,A项正确;同种类型的杂化轨道能量相同,B项正确;sp2杂化轨道是由1个s轨道与2个p轨
道杂化而成的,C项正确;sp2杂化轨道最多可形成3个σ键,D项错误。
5.(中)在SO 分子中,分子的空间结构为V形,S原子采用sp2杂化,那么SO 的键角( )
2 2
A.等于120° B.大于120° C.小于120° D.等于180°
【答案】C
【解折】SO 分子的 VSEPR模型为平面三角形,从理论上看其键角应为 120°,但由于SO 分子中的S原子
2 2
有一对孤电子对,对其他的两个化学键存在排斥作用,因此SO 分子中的键角应小于120°。
2
6.(中)CH+、CH—、-CH 都是重要的有机反应中间体,下列说法不正确的是( )
3 3 3
A.碳原子均采取sp2杂化
B.CH +中所有原子共面
3
C.CH —的空间结构为三角锥形
3
D. CH+和CH—结合可得到CHCH
3 3 3 3
【答案】A
【解折】CH—和-CH 中碳原子采取sp3杂化,A项错误;CH+中碳原子采取sp2杂化,为平面三角形,所有
3 3 3
原子共面,B 项正确;CH—中 C 采取 sp3杂化,为三角锥形,C 项正确;CH+和 CH—结合可得到
3 3 3
CHCH,D项正确。
3 3
7.(易)下列分子的中心原子采取sp2杂化的是( )
A.HO B.NH C. C H D.CH
2 3 2 4 4
【答案】C
【解析】根据价层电子对互斥模型判断中心原子杂化类型,σ键个数、孤电子对数和中心原子杂化类型如
下表:
σ键个数 孤电子对数 中心原子杂化类型
HO 2 2 sp3
2
NH 3 1 sp3
3
C H 3 0 sp2
2 4
CH 4 0 sp3
4
8.(易)正误判断,正确的打“√”,错误的打“×”。(1)杂化轨道只用于形成共价键( )
(2)中心原子若通过sp3杂化轨道成键,则该分子一定为正四面体形结构( )
(3)NH 为三角锥形,N发生sp2杂化( )
3
(4)只要分子的空间结构为平面三角形,中心原子均为sp2杂化( )
(5)中心原子是sp杂化的,其分子的空间结构不一定为直线形( )
(6)价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数( )
【答案】(1)×(2)×(3)×(4)√(5)×(6)√
【解析】(1)杂化轨道用于形成σ键或者用来容纳未参与成键的孤电子对
(2)也可以是三角锥形,例如氨气,或者V形,例如水
(3)N发生了sp3杂化
(4)利用空间构型可以判断杂化方式
(5)利用空间构型可以判断杂化方式,一定为直线形
(6)σ键计入,π键不计入
9.乙炔分子的碳原子采取什么杂化方式?它的杂化轨道用于形成什么化学键?怎样理解它存在碳碳三键?
答案:乙炔分子中的碳原子采取sp杂化方式。在乙炔分子中,2个碳原子各以1个sp杂化轨道与1个氢原
子的1s轨道重叠形成1个C-Hσ键,同时又各以另1个sp杂化轨道形成1个C-Cσ键。除此之外,两个碳
原子又通过各自的2个未参加杂化的轨道(相互垂直)重叠形成了2个π键。因此,乙炔的三键中有1个σ
键和2个π键。
10. (易)计算下列各微粒中心原子的杂化轨道数,判断中心原子的杂化轨道类型,写出VSEPR模型名称。
(1)CS : 、 、
2
(2)NH +: 、 、
4
(3)H O: 、 、
2
(4)PCl : 、 、
3
(5)BCl : 、 、
3
【答案】(1)2 sp 直线形 (2)4 sp3 正四面体形 (3)4 sp3 四面体形
(4)4 sp3 四面体形(5)3 sp2 平面三角形